Цитомегалия вирус или бактерия
Обновлено: 24.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
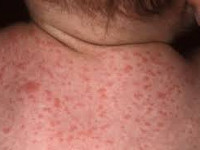
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Цитомегаловирусная инфекция у беременных — это клинически манифестное или латентно протекающее инфекционное заболевание, вызванное цитомегаловирусом, возникшее до зачатия или во время гестации. Проявляется гипертермией, катаральными симптомами, шейным и подчелюстным лимфаденитом, сиалоаденитом, общей интоксикацией, беловато-голубыми белями, реже — гепатомегалией, спленомегалией, генерализованной лимфаденопатией. Диагностируется с помощью серологических и молекулярных лабораторных методов. Лечение проводится специфическим человеческим иммуноглобулином, рекомбинантным альфа-2-интерфероном, при тяжелом течении — синтетическими аналогами нуклеозидов.
МКБ-10
Общие сведения
Цитомегаловирусная инфекция (цитомегалия, ЦМВИ) — одно из наиболее распространенных инфекционных заболеваний, внутриутробно поражающих плод и вызывающих различные врожденные аномалии. В зависимости от региона антитела к цитомегаловирусу определяются у 40-98% пациенток репродуктивного возраста. Цитомегалия чаще встречается в группах населения с низким уровнем социального и экономического развития. В России серопозитивными к ЦМВИ являются до 90% женщин, инфицированность среди беременных старше 30 лет достигает 97-98%. В европейских странах врожденная цитомегалия выявляется с частотой 3-5 случаев на 1000 родов, в других государствах этот показатель составляет от 0,2 до 2,2%.

Причины
Заболевание вызывается крупным ДНК-содержащим цитомегаловирусом (ЦМВ), принадлежащим к семейству герпес-вирусов. Специалисты выделяют три штамма возбудителя, каждый из которых может самостоятельно инфицировать организм одного и того же человека. Заражение происходит до зачатия либо во время беременности. Вирусы пожизненно персистируют в организме женщины, поражая практически все виды тканей. Часть инфекционистов считает ЦМВ условно-патогенным микроорганизмом, клинически значимая реактивация которого наблюдается только при значительном угнетении иммунитета.
Усиление патогенности цитомегаловируса в гестационном периоде связано с физиологической иммуносупрессией, защищающей генетически чужеродный плод от отторжения. Под влиянием эстрогенов, прогестерона, кортизола у беременной уменьшается абсолютное и относительное количество Т-лимфоцитов, непосредственно участвующих в элиминации вирусов и поврежденных клеток, снижается их цитотоксичность. В результате ускоряется репликация цитомегаловирусов, они быстрее распространяются по организму и при недостаточном уровне защитных антител преодолевают плацентарный барьер.
Патогенез
Особенностью цитомегаловирусной инфекции является множественность путей заражения. Вирус распространяется аэрогенным, контактным, фекально-оральным, гемотрансфузионным, половым, вертикальным способами, в том числе трансплацентарно от беременной к плоду. Из-за сравнительно низкой вирулентности для инфицирования важен тесный контакт с зараженным. Возбудитель ЦМВИ определяется практически во всех биологических средах: слюне, крови, моче, слезной жидкости, ликворе, грудном молоке, цервикальном, вагинальном, уретральном секрете, сперме, слизи из прямой кишки, околоплодных водах.
После попадания в организм цитомегаловирусы адсорбируются на поверхности клеток, проникают в них, проходят полный цикл репликации ДНК, после чего сформированные вирионы распространяются на соседние клетки, с кровью разносятся по организму. Наиболее чувствителен к вирионам протоковый эпителий слюнных желез, в первую очередь околоушных, других экзокринных желез.
После лимфогенной и гематогенной генерализации обычно наступает фаза непродуктивной инфекции (скрытого носительства) с длительным сохранением вирусной частицы внутри зараженной клетки и передачей при делении дочерним клеткам. У женщин с нормальным иммунитетом клиническая манифестация не происходит, заболевание сразу приобретает характер носительства. Цитомегаловирус может длительное время персистировать в неактивной форме в чувствительных клетках. Проникновение ЦМВ в лимфоциты и мононуклеары обеспечивает его защиту от противовирусных антител.
При падении иммунитета у беременных возможна реактивация цитомегаловирусной инфекции с разрушением ядер клеток, в которых персистировал вирус, гематогенной диссеминацией, поражением железистых органов, развитием васкулитов, индукцией специфического цитомегалического метаморфоза клеток разных тканей. При гестации вирусы из межворсинчатого пространства проникают через плаценту и гематогенно инфицируют плод. Установлено, что ЦМВ способен повреждать мембрану трофобласта.
Классификация
Систематизация основных форм цитомегаловирусной инфекции у беременных проводится с учетом выраженности клинической картины и времени манифестации патологического процесса. Такой подход наиболее оправдан с точки зрения прогнозирования возможных осложнений заболевания и выбора оптимальной тактики ведения беременности. Специалисты в сфере акушерства и гинекологии, инфекционных болезней различают следующие варианты инфекции:
- Первично-манифестнаяЦМВИ. Самый неблагоприятный вариант течения патологии. Возникает в результате первичного инфицирования беременной, у которой отсутствуют специфические IgG. Отличается высокой вероятностью трансплацентарного переноса вируса (до 30-75%) и внутриутробного поражения плода. В период гестации выявляется не более чем у 4% пациенток. При заражении с острой симптоматикой в I триместре рекомендован аборт.
- Носительство. Наиболее частая форма цитомегаловирусной болезни у беременных. Носительницами являются женщины, у которых до зачатия была активная форма заболевания или инфекция на фоне сильного иммунитета сразу перешла в непродуктивную фазу. Иммуноглобулины G, циркулирующие в крови пациентки, защищают плод от заражения ЦМВ. При исключении иммуносупрессорных воздействий риск патологического течения гестации минимален.
- Реактивация латентной инфекции. При значительном снижении иммунитета у носительниц цитомегаловируса развивается характерная клиническая картина. Заболевание в той или иной степени обостряется у 40-50% серопозитивных беременных. В 0,15-0,36% случаев вирус передается трансплацентарно ребенку. Наибольший риск врожденных аномалий наблюдается при обострении цитомегаловирусной болезни на 7-12 неделях гестационного срока.
Симптомы ЦМВИ у беременных
Возможны беловато-голубые влагалищные выделения. При существенном снижении иммунитета определяется увеличение печени, селезенки с появлением тяжести, дискомфорта, распирания в правом и левом подреберьях, генерализованное увеличение лимфоузлов. Длительность острой фазы, как правило, составляет до 2-3 недель.
Осложнения
Осложненное течение гестации наблюдается преимущественно при острой или реактивированной инфекции. У таких пациенток чаще возникают спонтанные выкидыши, связанные с тяжелыми эмбрио- и фетопатиями, преждевременные роды, вызванные гипертонусом матки, замершие беременности, мертворождение. Из-за повреждения мембраны трофобласта ЦМВИ может осложниться приращением плаценты, гипертрофией и ранним старением плацентарной ткани, фетоплацентарной недостаточностью, внутриутробной гипоксией и задержкой развития плода.
Во время родов возможна преждевременная отслойка плаценты, массивная кровопотеря из-за атонического кровотечения. В послеродовом периоде отмечаются латентные эндометриты. В последующем повышается вероятность развития дисменореи.
При острой первичной цитомегаловирусной болезни существенно возрастает риск трансплацентарного инфицирования плода и развития многоводия. Дети зачастую рождаются недоношенными, с низкой малой тела. Особенно опасно заражение ЦМВ в 1-м триместре, часто вызывающее микроцефалию, хориоретинит, нейросенсорную тугоухость, другие аномалии развития.
Врожденная цитомегалия после внутриутробного инфицирования может протекать бессимптомно, проявляться тяжело протекающими манифестными формами или в виде последствий поражения отдельных органов (гепатомегалии, затяжной желтухи, нарушений сосания и глотания, стойкого снижения мышечного тонуса, тремора, анемии, тромбоцитопении, отставания в умственном и моторном развитии, пневмонии, миокардита, панкреатита, колита, нефрита). Отдаленными последствиями ЦМВИ у детей являются слепота, глухота, речевые нарушения, проявляющиеся на 2-5-м году жизни.
У беременных со значительной иммуносупрессией ЦМВИ протекает тяжелее, экстрагенитальные осложнения выявляются чаще. Неблагоприятными формами заболевания считаются цитомегаловирусные поражения легких (интерстициальная пневмония), мозга (менингит, энцефалит), периферической нервной системы (миелит, полирадикулоневрит), сердца (миокардит, перикардит), кроветворения (тромбоцитопения, гемолитическая анемия). Прямая угроза для жизни беременной возникает при быстрой генерализации инфекции с развитием сепсиса, инфекционно-токсического шока, ДВС-синдрома.
Диагностика
Сложность своевременного выявления ЦМВИ связана с отсутствием симптоматики у большинства беременных и полиморфностью клинической картины при манифестации. Учитывая повышенный риск перинатального заражения ребенка цитомегаловирусной инфекцией, в качестве скрининга рекомендовано проведение анализа на TORCH-комплекс. Ведущими методами диагностики являются лабораторные анализы, позволяющие верифицировать инфекционного агента, обнаружить серологические маркеры и определить остроту процесса. План обследования пациенток с подозрением на цитомегалию включает такие исследования, как:
- Иммуноферментный анализ. ИФА считается наиболее достоверным и информативным методом диагностики цитомегаловирусной болезни. Наличие активной инфекции подтверждает выявление IgM и более чем 4-кратное нарастание титра IgG. О давности инфицирования свидетельствуют данные об авидности иммуноглобулинов G (при показателе
- ПЦР-диагностика. Цитомегаловирусные нуклеиновые кислоты определяют в биологических секретах, которые могут содержать возбудителя. Обычно для анализа берут кровь, мочу, цервикальный секрет, буккальные мазки. Обнаружение вирусной ДНК подтверждает инфицированность, а количественные методы исследования позволяют контролировать течение инфекции.
Для оценки состояния плода, выявления фетоплацентарной недостаточности, возможных аномалий по показаниям проводятся:
- УЗИ плода и плаценты;
- допплерография маточно-плацентарного кровотока;
- фетометрия;
- КТГ;
- фонокардиография плода;
- биопсия хориона.
Цитомегалию дифференцируют с ВИЧ-инфекцией, инфекционным мононуклеозом, токсоплазмозом, листериозом, герпесом, вирусными гепатитами, бактериальным сепсисом, лимфогранулематозом, острым лейкозом. При необходимости пациентку консультирует инфекционист, вирусолог, иммунолог, онколог, онкогематолог.
Лечение ЦМВИ у беременных
Выбирая тактику ведения гестации, учитывают клиническую форму ЦМВИ и срок инфицирования. Женщинам с цитомегалией, первично-манифестировавшей в период 1 триместра, рекомендовано проведение аборта. Прерывание беременности по медицинским показаниям также показано пациенткам с клинически и лабораторно подтвержденной первичной инфекцией при обнаружении до 22 недели УЗ-признаков пороков развития плода. В остальных случаях возможна пролонгация гестации.
Беременным с носительством медикаментозное лечение не назначается. При отсутствии клинических и лабораторных признаков реактивации цитомегаловирусной болезни требуется коррекция образа жизни, направленная на предотвращение значительной иммуносупрессии. Больным необходимы достаточные отдых и сон, исключение чрезмерных физических и психологических нагрузок, полноценное питание, прием витаминно-минеральных комплексов, профилактика ОРВИ, осторожность при назначении препаратов, снижающих иммунитет.
Беременным с активной формой инфекции проводится лечение, направленное на купирование обострения и прекращение экскреции цитомегаловируса. Сложность выбора адекватной медикаментозной терапии связана с фетотоксичностью большинства противовирусных средств. С учетом возможных показаний и противопоказаний для лечения ЦМВИ при гестации применяются:
- Антицитомегаловирусный человеческий иммуноглобулин. Гипериммунные препараты позволяют восстановить титр специфических IgG, блокировать репликацию возбудителя и ограничить его диссеминацию. Использование иммуноглобулина человека существенно снижает риск внутриутробного инфицирования вирусом цитомегалии.
- Рекомбинантный α-2-интерферон. Препарат стимулирует Т-хелперы и Т-киллеры, повышая уровень Т-клеточного иммунитета. Усиливает активность фагоцитов и скорость дифференцировки В-лимфоцитов. Угнетает репликацию цитомегаловирусов и способствует их инактивации различными иммунными агентами. Рекомендован в виде ректальных свечей.
- Синтетические аналоги нуклеозидов. Назначаются только при тяжелых генерализованных формах цитомегаловирусной инфекции, когда риск токсических эффектов препаратов оправдан спасением жизни беременной. Противовирусные препараты ингибируют ДНК-полимеразу вирусных частиц и за счет этого тормозят синтез цитомегаловирусной ДНК.
Индукторы интерфероногенеза, иммуномодуляторы применяют крайне редко из-за возможного преждевременного прерывания гестации. В качестве немедикаментозных методов допустимо проведение эндоваскулярного лазерного облучения крови и плазмафереза.
Роды при ЦМВИ
Предпочтительным методом родоразрешения являются естественные роды. Кесарево сечение выполняется при наличии абсолютных акушерских или экстрагенитальных показаний или при сочетании относительных (внутриутробном инфицировании цитомегаловирусом, хронической гипоксии плода, II-III степенях задержки его развития, первичном и вторичном бесплодии в анамнезе).
Прогноз и профилактика
Своевременное выявление латентной ЦМВИ и профилактика ее активации существенно улучшают исход беременности как для женщины, так и для плода. Прогноз неблагоприятен при генерализации первичной цитомегаловирусной инфекции. При установленном диагнозе цитомегалии показано планирование зачатия с учетом рекомендаций акушера-гинеколога, купирование активного процесса, прегравидарная иммунокоррекция с использованием пептидных иммуностимуляторов и рекомбинантных интерферонов.
Противовирусная терапия женщин с манифестной ЦМВИ на 75% снижает риск реактивации инфекции в наиболее опасном по возникновению осложнений 1 триместре. Общая профилактика заражения предполагает соблюдение правил личной гигиены с частым мытьем рук, отказ от близких прямых контактов с другими людьми.
1. Цитомегаловирусная инфекция и беременность/ Мельникова С.Е., Троик Е.Б.// Детская медицина Северо-Запада – 2012 - Т. 3, №3.
2. Цитомегаловирусная инфекция и беременность (прегравидарная подготовка и терапия)/ Короткова Н.А., Прилепская В.Н.// Эффективная фармакотерапия. – 2016 - №22.
3. Цитомегаловирусная инфекция. Этиология, эпидемиология, патогенез, клиника, лабораторная диагностика, лечение, профилактика/ Марданлы С.Г., Кирпичникова Г.И., Неверов В.А. — 2011.
4. Цитомегаловирусная инфекция в практике врача: современный алгоритм диагностики и лечения/ Извекова И.Я., Михайленко М.А., Краснова Е.И.// Лечащий врач. – 2018.
Врожденная цитомегалия – инфекционное заболевание, которое развивается при внутриутробном или интранатальном заражении ребенка цитомегаловирусом и характеризуется множественными пороками и поражениями внутренних органов. Заболевание часто протекает бессимптомно, при выраженной клинике основными симптомами являются поражения мозга (энцефалопатии, микроцефалия, гидроцефалия и др.), гепатит, пневмония, нефрит, сиалоаденит, патология органов зрения и слуха. Врожденная цитомегалия диагностируется методами ИФА и ПЦР, вирус обнаруживается в крови, моче, мазке из горла. Основа специфического лечения – антицитомегаловирусный иммуноглобулин.
Общие сведения
Врожденная цитомегалия – наиболее часто встречающаяся врожденная инфекция. Частота заболевания среди новорожденных – 0,2-2,5%. Если беременная женщина переносит первичную цитомегаловирусную инфекцию, вероятность заболевания ребенка колеблется от 30 до 50%. В случае вторичной инфекции у матери заражение плода встречается крайне редко и составляет 1% случаев. Врожденная цитомегалия является актуальной проблемой для педиатрии. В настоящее время заболеваемость значительно возросла. Очень часто имеет место запоздалая диагностика в связи с отсутствием клинических проявлений сразу после рождения ребенка. Огромное внимание уделяется вопросу ранней профилактики заболевания. Проводится обучение медицинского персонала, меняются стандарты обследования беременных и новорожденных. Своевременно начатая терапия позволяет значительно снизить уровень инвалидности среди детей, перенесших врожденную цитомегалию. Активно ведется разработка вакцины против цитомегаловируса.

Причины врожденной цитомегалии
Причина инфекции – ДНК-содержащий вирус цитомегалии, относящийся к семейству герпес-вирусов. Во внешней среде вирус устойчив при комнатной температуре, однако не выдерживает воздействия 20% раствора этилового спирта и других дезинфектантов. Возбудитель цитомегалии способен выживать внутри клетки в течение многих лет. Риск инфицирования женщины повышается, если во время беременности она контактирует с больными цитомегалией, работает в местах большого скопления людей (детские сады, школы, медицинские учреждения). Особую роль играет иммунитет самой матери. Например, если женщина уже перенесла цитомегаловирусную инфекцию прежде, то при повторной активации вируса во время беременности ребенок с большой долей вероятности родится неинфицированным.
Инфицирование ребенка возможно пренатально (трансплацентарным путем) и интранатально, то есть при прохождении через родовые пути. Второй вариант встречается значительно чаще. С кровотоком возбудитель разносится ко всем тканям и органам. Вирус высокотропен к клеткам слюнных желез, именно в эти клетки он внедряется в первую очередь. Чаще всего его обнаруживают в околоушных слюнных железах, реже – в подчелюстных и других. В выводных протоках слюнных желез вирус может долгое время размножаться, не выходя за их пределы. Вирус специфическим образом изменяет клетки, и эти изменения легко обнаружить при микроскопии. Пораженные клетки значительно увеличиваются в размерах и содержат скопления вируса (видимые под микроскопом включения). Такие клетки называют цитомегалами. Кроме слюнных желез, поражаются многие другие органы, в основном, паренхиматозные: печень, почки, поджелудочная железа. Для врожденной цитомегалии характерно поражение головного мозга.
Классификация врожденной цитомегалии
Различают локализованную и генерализованную форму врожденной цитомегалии, однако такое разделение условно, поскольку при малейшем снижении иммунитета у плода инфекция приобретает генерализованное течение. Врожденная цитомегалия может быть острой, затяжной и хронической. При острой и затяжной формах наблюдаются характерные симптомы; если процесс хронический, он может диагностироваться только по вирусемии. Некоторые авторы отдельно выделяют гепатолиенальную, легочную, мозговую и кишечную форму инфекции, однако поскольку врожденная цитомегалия часто сопровождается симптомами со стороны нескольких органов, данная классификация также условна.
Симптомы врожденной цитомегалии
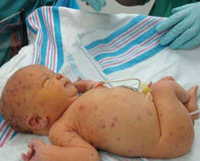
Если заражение женщины происходит на ранних сроках гестации, то беременность может закончиться выкидышем или внутриутробной гибелью плода. При рождении инфицированного ребенка в 90% случаев врожденная цитомегалия протекает бессимптомно (субклинически). На манифестную форму приходится около 10% наблюдений, однако уровень смертности при клинически выраженной форме заболевания достигает 10-30%. Манифестная форма инфекции сопровождается триадой симптомов: желтуха, геморрагический синдром и гепатоспленомегалия. С рождения выявляется петехиальная сыпь по всему телу, кровоизлияния в кожу и слизистые оболочки, кровь в стуле. Геморрагический синдром самостоятельно проходит через 1-2 недели после рождения.
Отличие врожденной цитомегалии от приобретенной – обязательное поражение головного мозга. У новорожденного может диагностироваться энцефалопатия, микроцефалия, гидроцефалия, часто отмечаются судороги и тремор. Иногда при манифестной форме заболевания развивается энцефалит с последующим образованием кальцификатов в головном мозге. Со стороны других органов нередко диагностируется пневмония, поражение почек, гепатит, сиалоаденит, ретинопатия, поражение органа слуха. Частота сенсоневральной тугоухости составляет, по разным данным, от 10 до 25% случаев. Реже выявляются врожденные пороки сердца: дефекты межпредсердной и межжелудочковой перегородки, пороки развития клапанов (аортального, митрального, легочной артерии).
Характерным признаком заболевания является низкая масса тела ребенка. В 30% случаев дети рождаются недоношенными. В дальнейшем нарастает гипотрофия, что также требует специального лечения. Поражение мозга впоследствии приводит к задержке психомоторного развития и олигофрении. Минимальная мозговая дисфункция имеет место, даже если мозговые нарушения не выявлялись в период новорожденности и первых лет жизни. Тяжелое течение цитомегаловирусного гепатита, как правило, приводит к билиарному циррозу печени в возрасте от 6 до 12 месяцев.
Диагностика врожденной цитомегалии
Пренатальная диагностика проводится в том случае, если будущая мать переносит цитомегаловирусную инфекцию в период беременности. Однако это лишь позволяет выявить у плода патологии, сопутствующие инфекции, но не само заболевание. Если врожденная цитомегалия была заподозрена еще во время беременности, то у новорожденного обязательно производится забор крови для исключения или подтверждения диагноза. Это важный момент, поскольку после рождения симптомы инфекции в большинстве случаев отсутствуют. Поэтому лабораторные исследования играют огромную роль в диагностике врожденной цитомегалии.
Диагноз ставится при обнаружении в крови и моче непосредственно частиц вируса (ПЦР), а также признаков иммунного ответа на вирусемию, то есть антител IgM и IgG (метод ИФА). Основные сложности диагностики связаны с тем, что антитела обнаруживаются в крови новорожденного, даже если заболевание было у его матери во время беременности, а сам малыш при этом не был инфицирован. Обнаруженные антитела в этом случае могут быть материнскими. Поэтому ИФА-исследование проводится в динамике. Для подтверждения диагноза необходимо повышение титра IgG-антител не менее чем в 4 раза в повторном анализе, который выполняется через неделю после первого.
Врожденная цитомегалия также диагностируется с помощью метода ПЦР. Обнаружение ДНК вируса в крови подтверждает заражение на 100%. Минус данного метода – его длительность. Кроме того, вирусемия не является достоверным признаком активности инфекции. ПЦР-диагностика позволяет подтвердить заключение ИФА, поэтому используется в совокупности с другими методами.
В связи с частым бессимптомным течением врожденной цитомегалии важную роль играют стандарты диагностики. Заболевание новорожденного обязательно исключается педиатром, если мать переносила во время беременности цитомегалию или мононуклеозоподобные заболевания, либо имеет в анамнезе случаи выкидышей или мертворождения. Основная цель диагностики – раннее выявление заболевания. Чем раньше начато лечение, тем лучше дальнейший прогноз для ребенка.
Лечение и профилактика врожденной цитомегалии
Назначение терапии возможно только после точной диагностики заболевания. Это очень важный момент, потому что проведение лечения без подтвержденного диагноза может навредить ребенку. Лечение проводится строго в условиях стационара. Применяется специфический антицитомегаловирусный иммуноглобулин. Препарат содержит антитела против цитомегаловируса. Попадая в кровь, они связываются с частицами вируса и инактивируют их. Помимо специфической терапии, используются препараты интерферона и индукторы интерферона. Проводится симптоматическая терапия гепатита, нефрита, мозговых нарушений и других сопутствующих патологий. Лечение считается успешным, если вирус не обнаруживается в крови.
Профилактика врожденной цитомегалии у ребенка начинается с первых дней беременности. Будущей маме важно полностью исключить контакты с больными цитомегаловирусной инфекцией, а также избегать мест большого скопления людей. Если заражение вирусом уже случилось, очень важно, как можно раньше это обнаружить. С целью снижения риска передачи вируса от матери к ребенку используется антицитомегаловирусный иммуноглобулин, который вводится внутривенно беременной женщине. Для повышения противовирусного иммунитета также используются индукторы интерферона. Специфическая профилактика (вакцина) в настоящее время находится в стадии разработки и клинических исследований.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Бактериальный вагиноз: причины появления, симптомы, диагностика и способы лечения.
Определение
Бактериальный вагиноз — это инфекционное полимикробное заболевание, связанное с изменением микрофлоры влагалища, при котором происходит значимое уменьшение количества или полное исчезновение палочек Додерлейна (лактобактерий) и их замещение факультативными анаэробными микроорганизмами и/или возбудителем гарднереллеза. Увеличение уровня лейкоцитов в вагинальном отделяемом и признаки воспаления стенок влагалища могут отсутствовать.
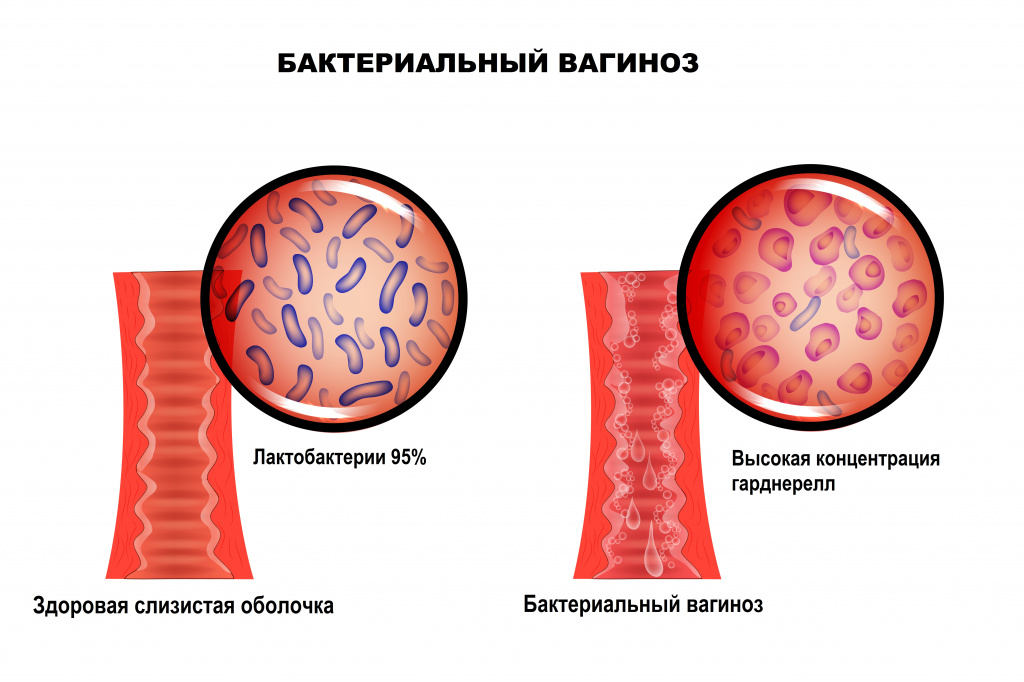
Отличительной особенностью заболевания является отсутствие какого-либо одного конкретного возбудителя. Микрофлора, приходящая на смену лактобактериям, может быть различной и чаще всего представлена условно-патогенными бактериями. Кислотность среды влагалища смещается в сторону ощелачивания. При нарушении экосистемы влагалища формируется хорошо структурированная полимикробная пленка (биопленка - форма микробных сообществ), покрывающая вагинальный эпителий и состоящая из анаэробных бактерий, что приводит к рецидивирующему течению бактериального вагиноза. В биопленках бактерии защищены от компонентов врожденного и приобретенного иммунитета.
В норме ведущее место (95%) в вагинальном микробиоценозе занимают палочки Додерлейна, продуцирующие перекись водорода и молочную кислоту.
Они поддерживают постоянство богатой кислородом кислой рН-среды и играют роль местных факторов защиты. В случае нарушения защитных механизмов патогенные или условно-патогенные микроорганизмы транзиторной или факультативной флоры прикрепляются к клеткам влагалищного эпителия с последующим размножением и повреждением тканей.
Бактериальный вагиноз является наиболее частой причиной патологических вагинальных выделений у женщин репродуктивного возраста, однако иногда он может наблюдаться и у девочек до менархе, и у женщин в период менопаузы.
Причины появления бактериального вагиноза
Предрасполагающие факторы, ведущие к развитию бактериального вагиноза:
- использование антибактериальных препаратов;
- длительное применение внутриматочных контрацептивов;
- ношение синтетического нижнего белья, злоупотребление прокладками на каждый день и тампонами, которые препятствуют проникновению кислорода;
- длительный прием антибиотиков;
- хронические заболевания кишечника и другие состояния, вызывающие дисбактериоз;
- использование пероральных контрацептивов;
- перенесенные ранее воспалительные заболевания урогенитального тракта;
- нарушение гормонального статуса, сопровождающееся нарушением менструального цикла, преимущественно по типу олигоменореи или аменореи;
- атрофия слизистой оболочки влагалища;
- снижение иммунитета;
- воздействие малых доз ионизирующего излучения;
- стрессовые воздействия на организм.
Классификация бактериального вагиноза на основании микроскопического исследования:
- Компенсированный бактериальный вагиноз — количество лактобактерий снижено, что является фактором риска заселения влагалища патогенными микроорганизмами.
- Субкомпенсированный — низкий уровень лактобактерий и растущее число условно-патогенных микроорганизмов.
- Декомпенсированный — в мазке выявляются условно-патогенные микроорганизмы, лактобактерии отсутствуют, выражены клинические симптомы бактериального вагиноза.
У большинства женщин бактериальный вагиноз протекает бессимптомно и может быть обнаружен случайно во время рутинного осмотра и взятия мазка.
Интенсивный рост факультативной флоры, образование патологических биопленок сопровождается появлением влагалищных выделений с характерным неприятным запахом.
Хронический бактериальный вагиноз — это непрерывное течение заболевания более 2-х месяцев, несмотря на проводимое лечение. Как правило, он сочетается с нарушением гормонального фона и атрофией слизистой оболочки влагалища.
Диагностика бактериального вагиноза
При постановке диагноза у врача есть четыре критерия, которыми он пользуется. Наличие у пациентки трех из них говорит в пользу бактериального вагиноза.
Микроскопическое (бактериоскопическое) исследование мазка, окрашенного по Граму. Материалом для оценки состояния флоры влагалища служат гинекологические мазки (отделяемое наружных половых органов, уретры, влагалища, шейки матки, полости матки).
Читайте также:

