Цитомегаловирус и вирус папилломы человека это одно и тоже
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Цитомегаловирус: причины появления, симптомы, диагностика и способы лечения.
Определение
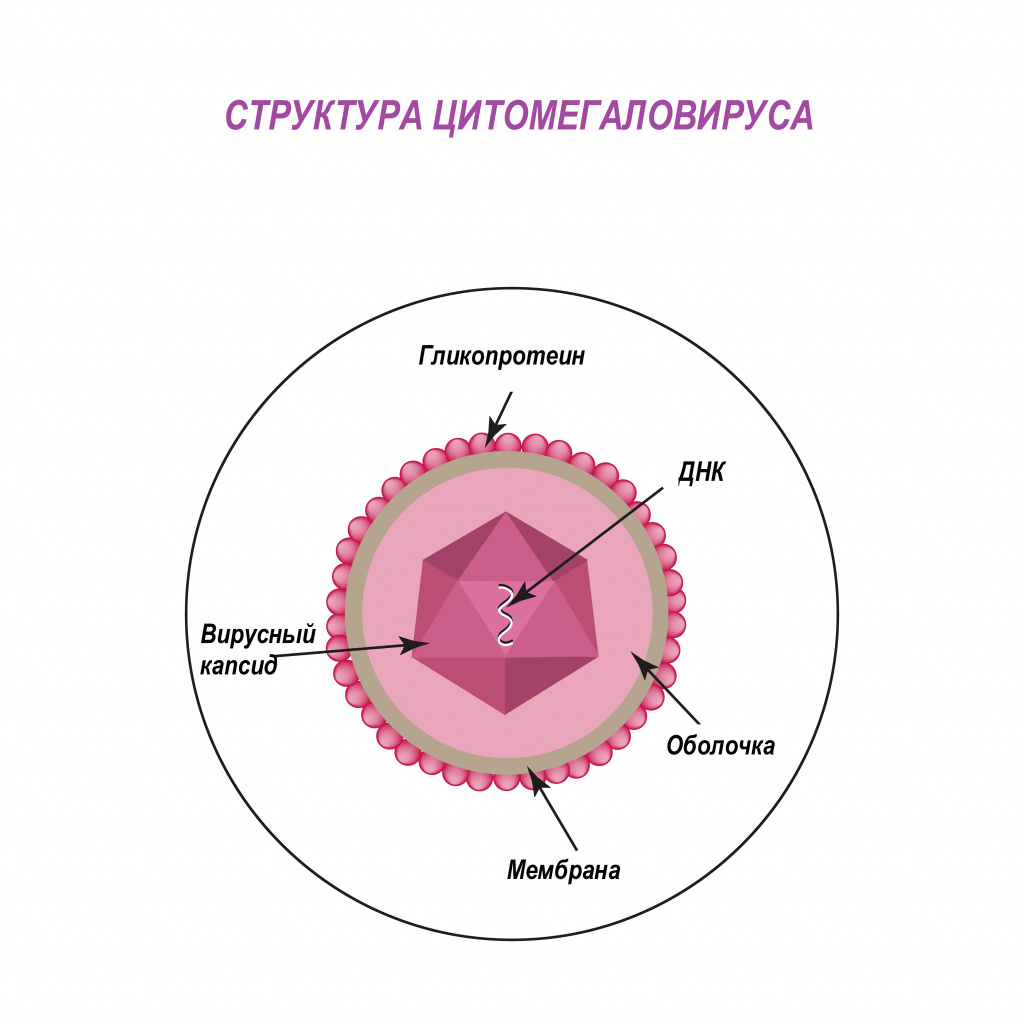
Цитомегаловирус (ЦМВ, или цитомегаловирусная болезнь) – хроническое инфекционное заболевание вирусной этиологии, характеризующееся многообразием клинических форм и проявлений - от бессимптомного течения до тяжелого поражения внутренних органов и центральной нервной системы. Возбудитель ЦМВ – представитель семейства герпесвирусов (вирус герпеса человека 5-го типа).
Попадая в клетки организма, цитомегаловирус способен оставаться в них пожизненно. У лиц с нормально функционирующей иммунной системой в подавляющем большинстве случаев инфекция протекает по типу вирусоносительства. При угнетении иммунитета вирус активизируется, вызывая клинические симптомы болезни.
По различным данным доля носителей цитомегаловируса в России составляет порядка 73-90% - то есть именно у такого количества людей выявляются антитела к ЦМВ.
Причины появления цитомегаловирусной болезни
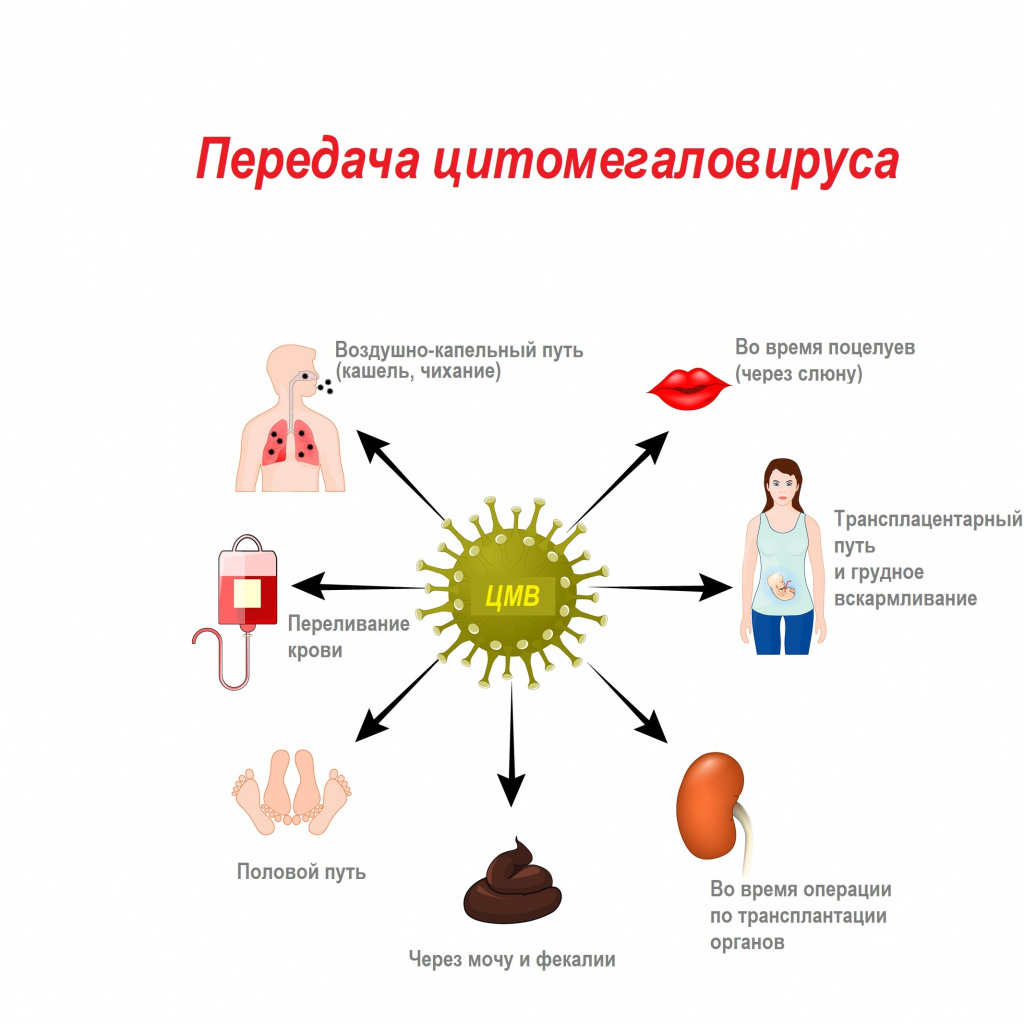
Цитомегаловирус передается через биологические жидкости: слюну, мочу, кровь, вагинальный секрет, слезы, сперму, фекалии, грудное молоко.
Из-за лабильности возбудителя и низкой концентрации вируса в выделениях для передачи инфекции необходим длительный, частый и тесный контакт с носителем.
Механизмы передачи вируса — воздушно-капельный (аэрозольный путь), контактный (контактно-бытовой и половой), гемоконтактный (парентеральный, а также при пересадке органов), вертикальный (от матери к плоду), фекально-оральный (алиментарный — через грудное молоко).
Заражение плода реализуется за счет трансплацентарной передачи от матери к плоду, которая возможна в течение всей беременности. Наибольшую опасность для плода представляет первичная инфекция на ранних сроках беременности, поскольку часто вызывает формирование врожденных пороков развития.
Особое свойство ЦМВ — способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов, в первую очередь ИНФ-α. При острой инфекции вирус поражает преимущественно эпителиальные клетки легких, печени, кишечника, почек, мочевого пузыря, молочных и слюнных желез, генитального тракта. Цитомегаловирус может инфицировать нервные клетки, клетки гладкой мускулатуры, костного мозга.
Классификация заболевания
По характеру инфицирования:
- врожденное (внутриутробное),
- постнатальное (приобретенное).
- латентная инфекция,
- персистирующая инфекция,
- активная (низкой, средней, высокой степени тяжести) инфекция.
- острая инфекция,
- реактивация вируса,
- реинфекция.
Инкубационный период цитомегаловирусной болезни составляет от 15 дней до трех месяцев (при манифестной, выраженной форме заболевания). Однако чаще первичное инфицирование протекает или бессимптомно, или по типу легкой формы ОРЗ – у пациента наблюдаются незначительная слабость, лихорадка (температура 37,1-38,0°С), дискомфорт в мышцах, першение в горле, иногда насморк, увеличение шейных лимфатических узлов, болезненность слюнных желез, головная боль, отсутствие аппетита.
У беременных острая первичная инфекция протекает, как правило, бессимптомно (25–50%) или с неспецифическими проявлениями (с лихорадкой, астенией и головной болью).
В редких случаях развиваются гепато- и спленомегалия, гепатит с минимальной степенью активности цитолитического синдрома, дерматиты, васкулиты, интерстициальный пневмонический процесс, тромбоцитоз или тромбоцитопения, лимфоцитоз.
У больных с иммунодефицитом цитомегаловирусная инфекция протекает тяжело - вирус быстро распространяется по организму и вызывает серьезные осложнения.
Диагностика цитомегаловируса
Диагностические мероприятия начинаются со сбора жалоб и анамнеза, в том числе акушерско-гинекологического анамнеза матери.
Затем врач проводит объективное обследование (физикальное, неврологическое и антропометрическое).
Лабораторные исследования - общие и специфические:
-
общий анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgМ; цитомегаловирусная инфекция; ЦМВ-инфекция; специфические иммуноглобулины класса М к цитомегаловирусу. Cytomegalovirus; CMV Antibody; IgM; CMV infection; CMV-specific IgM. Краткое описание исследования Anti-CMV.
Синонимы: Анализ крови на антитела к цитомегаловирусу; АТ-ЦМВ-IgG; Цитомегаловирусная инфекция; ЦМВ-инфекция; Специфические иммуноглобулины класса G к цитомегаловирусу. Cytomegalovirus; CMV Antibody, IgG; CMV infection; CMV-specific IgG. Краткое описание исследования Anti-CMV-IgG .
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирус – широко распространённый вирус семейства герпесвирусов. После окончания острого периода инфекция цитомегаловирусом обычно переходит в латентную форму, из которой может реактивироваться. Цитомегаловирус относят к так называемым оппортунистическим инфекциям: выраженные клинич.
Цитомегаловирусная инфекция входит в группу репродуктивно значимых инфекций, обозначаемых как TORCH-комплекс (название образовано начальными буквами в латинских наименованиях - Toxoplasma, Rubella, Cytomegalovirus, Herpes); первичное инфицирование данными возбудителями, либо обострение .
К каким врачам обращаться
С первичными жалобами пациенты обращаются к врачу-терапевту или врачу общей практики (семейному врачу), детей ведет врач-педиатр . Могут потребоваться консультации инфекциониста - для верификации диагноза, стоматолога - при поражениях слизистой оболочки рта, кардиолога - при наличии врожденного порока сердца, нейрохирурга - при пороках центральной нервной системы, невропатолога - для оценки неврологической патологии, гематолога - при выраженных гематологических изменениях и геморрагическом синдроме, окулиста - для исследования глазного дна, отоларинголога - для исследования слухового аппарата.
Лечение цитомегаловирусной болезни
Субклинические формы ЦМВ-инфекции и латентное носительство крайне распространены, поэтому в большинстве случаев не требуют специфической терапии даже при выявлении антител. Их лечение направлено на усиление защитных сил организма при помощи иммуномодуляторов и профилактику факторов риска, которые приводят к обострению заболевания.
Для терапии клинически активных форм инфекции применяют:
- комплекс патогенетической (противовирусной) терапии, который разрабатывается профильными специалистами и включает препараты прямого противовирусного действия для минимизации риска осложнений, сокращения времени течения заболевания, а также профилактики рецидивов;
- иммунотерапию – антицитомегаловирусный иммуноглобулин назначают преимущественно детям при манифестных формах заболевания и беременным;
- дезинтоксикационную терапию, которая направлена на купирование синдрома интоксикации;
- метаболическую терапию - для восстановления обмена веществ в организме;
- симптоматическую терапию - для купирования воспалительных и токсических проявлений заболевания.
Проблема клинически выраженной инфекции актуальна для лиц, имеющих иммуносупрессию иной природы, в частности, онкогематологических пациентов, больных лучевой болезнью, лиц, длительно принимающих кортикостероидную, туберкулостатическую терапию, а также перенесших ожоговую травму.
Острое течение ЦМВ может привести к развитию гепатита с повышением уровня аминотрансфераз и атипичным лимфоцитозом.
Ученые предполагают роль цитомегаловируса как одного из кофакторов в развитии системных васкулитов, хронических диссеминированных заболеваний легких (в частности, фиброзирующего альвеолита), криоглобулинемии, опухолевых процессов (аденокарциномы предстательной железы, аденокарциномы толстой кишки, рака шейки матки), атеросклероза, кардиомиопатии, детского церебрального паралича, эпилепсии, синдрома Гийена-Барре, синдрома хронической усталости, аутизма.
Первичное инфицирование цитомагаловирусом у беременных женщин существенно повышает риск преждевременных родов, самопроизвольного выкидыша, многоводия, замершей беременности, внутриутробного инфицирования и даже гибели плода. Врожденная ЦМВ-инфекция может стать триггерным фактором развития тяжелых генерализованных форм и инвалидизирующих исходов заболевания, таких как потеря слуха, зрения, умственная отсталость, микроцефалия, судорожный синдром и пр. Такие пожизненные проблемы со здоровьем развиваются примерно у каждого пятого ребенка с врожденной цитомегаловирусной инфекцией.
Профилактика цитомегаловирусной болезни
Женщинам, планирующим беременность, необходимо пройти обследование на наличие ЦМВ. При обнаружении вируса важно получить консультацию врача-иммунолога.
Профилактика или превентивное лечение (активный мониторинг пациентов по уровню вирусной нагрузки и назначение противовирусных препаратов пациентам с признаками инфекции) являются эффективными способами предотвращения развития цитомегаловирусной инфекции после трансплантации органов.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Особенности течения цитомегаловирусной инфекции урогенитального тракта у сексуально активных женщин
Журнал: Клиническая дерматология и венерология. 2013;11(3): 69‑75
Чернова Н.И. Особенности течения цитомегаловирусной инфекции урогенитального тракта у сексуально активных женщин. Клиническая дерматология и венерология. 2013;11(3):69‑75.
Chernova NI. Specific features of cytomegalovirus infection of the urogenital tract in sexually active women. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):69‑75. (In Russ.).
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Цитомегаловирусная инфекция (ЦМВИ) — широко распространенное инфекционное заболевание человека, с вертикальным, половым, парентеральным, оральным путями передачи, реализующимися через кровь, цервикальный и вагинальный секреты, сперму и женское молоко. В большинстве случаев инфекция протекает без клинических проявлений. При иммуносупрессии, вызванной разными причинами, цитомегаловирус (ЦМВ) способен привести к развитию заболевания с многообразными симптомами, что обусловлено его способностью инфицировать практически все системы органов (ретинит, увеит, серонегативный мононуклеоз, пневмония, гепатит, болезни желудочно-кишечного тракта, центральной нервной системы, посттрансфузионный синдром) [1—5].
В среднем у 90—95% взрослого населения обнаруживаются антитела к ЦМВ. В литературе приводятся многочисленные данные об особенностях течения ЦМВИ у новорожденных, беременных и иммунонекомпетентных пациентов. В настоящий момент обследованию на ЦМВИ подлежат следующие категории граждан: женщины при подготовке к беременности, беременные и пациенты с выявленными иммунодефицитными состояниями. Изучению значимости ЦМВ в патологии взрослого населения уделяется особое внимание [6—9]. Однако не учитывается, что ЦМВ нередко способствует хроническому воспалительному поражению органов малого таза и гениталий, что обусловливает низкую эффективность терапии инфекций, передаваемых половым путем (ИППП), и снижение репродуктивной способности пациентов.
Цель настоящего исследования — определение форм течения ЦМВИ урогенитального тракта у сексуально активных женщин репродуктивного возраста.
Материал и методы
Под наблюдением находились 356 пациенток с ЦМВИ, которая характеризовалась наличием в крови анти-CMV IgG.
Для выявления достоверных триггерных клинических и лабораторных факторов, ассоциирующихся с ЦМВИ урогенитального тракта, данные опроса и обследования больных сравнивали с результатами аналогичных исследований, проведенных в контрольной группе, которая состояла из 120 женщин. Критериями отбора являлись: репродуктивный возраст, отсутствие беременности, лактации, системной и местной антибактериальной терапии в течение 1 месяца до начала данного обследования, нормальное состояние микрофлоры урогенитального тракта и исключенная ЦМВИ.
Результаты
Важное значение для выяснения характера ЦМВИ имеют сведения о перенесенных соматических и инфекционных заболеваниях. Частота экстрагенитальной патологии косвенно отражает состояние противоинфекционной защиты организма и иммунной системы в целом.

При анализе соматической патологии (табл. 2) наиболее часто в основной группе по сравнению с контрольной отмечались инфекционные вирусные заболевания (82,58% случаев), патология желудочно-кишечного тракта (55,9%) и заболевания органов дыхания (20,51%). У пациенток с ЦМВИ в 4,2 раза чаще отмечалась патология эндокринной системы (в 31,46% случаев; p<0,05).
Подробному анализу были подвергнуты данные о гинекологических заболеваниях, которые относятся к факторам, влияющим на состояние системного и локального иммунитета.

Среди перенесенных гинекологических заболеваний наиболее часто встречались патология шейки матки (44,10% случаев; p<0,05) и воспалительные заболевания органов малого таза (75%; p<0,05) по сравнению с контролем (табл. 3). Кроме того, у женщин с ЦМВИ чаще наблюдались ИППП (в 55,34% случаев; p<0,05) и бесплодие (28,65%; p<0,05).

При изучении особенностей сексуального анамнеза (табл. 4) выявлено, что у пациенток с ЦМВИ в 3 раза чаще (p<0,05) отмечалось раннее начало половой жизни. Соотношение женщин по количеству половых партнеров в обеих группах было сопоставимым. В ходе анализа особенностей сексуальных предпочтений установлено, что пациентки основной группы чаще практиковали аногенитальные контакты (p<0,05).
Незащищенные половые контакты (включая без использования презерватива с последующей обработкой раствором мирамистина) в анамнезе имели более 84% пациенток с ЦМВ и 70% женщин из группы контроля (p<0,05).
Таким образом, вероятным предрасполагающим фактором для ЦМВИ урогенитального тракта являлось раннее начало половой жизни и большое количество незащищенных аногенитальных контактов.
При клиническом обследовании анализировали особенности субъективных ощущений, проводили тщательный общий и гинекологический осмотр.
Таким образом, у пациенток с ЦМВИ при гинекологическом осмотре чаще выявлялся острый или хронический воспалительный процесс в малом тазу.

Результаты микроскопического исследования мазков отделяемого генитального тракта, окрашенных по Граму, представлены в табл. 6.

Анализ результатов культурального исследования отделяемого мочеполового тракта женщин выявил доминирование грибов Candida spp. (48,60%), G. vaginalis (30,62%), T. vaginalis (21,35%). У большинства женщин в биотопах влагалища имела место ассоциация ЦМВИ с условно-патогенными бактериями (Streptococcus, St. aureus, Ureaplasma spp., M. hominis) в высоком титре (более 10 5 КОЕ/мл; табл. 7).

Результаты комплексного обследования этих женщин представлены в табл. 8.
У 71 (19,9%) женщины состояние вагинальной микроэкологии было оценено как нормоценоз. Проанализировав полученные данные, можно было выделить его некоторые особенности, которые в ряде случаев позволили назвать указанное состояние нормоценозом только условно. Так, только у 22 (6,18%) женщин из 356 состояние микроэкологии полностью соответствовало всем критериям нормы репродуктивного возраста: при микроскопии вагинального отделяемого отсутствовала выраженная лейкоцитарная реакция (количество лейкоцитов не превышало 10 в поле зрения), эпителий был представлен клетками поверхностного и промежуточного слоев, количество микрофлоры было умеренным при абсолютном преобладании морфотипа лактобактерий. Морфотипы условно-патогенных микроорганизмов (УПМ) не определялись. При культуральном исследовании титр лактобацилл составлял 10 6-8 КОЕ/мл вагинального отделяемого, а концентрации УПМ были низкими (менее 10 3 КОЕ/мл).
Наиболее частой патологией среди 356 обследованных пациенток с ЦМВИ оказался кандидоз (57,30%), в большинстве случаев сопровождавшийся умеренным повышением титра УПМ (Streptococcus группы В в 10 6 КОЕ/мл и St. aureus более 10 6 КОЕ/мл).
Аэробный вагинит (1,12%) как вариант дисбиоза влагалища был обусловлен колонизацией вагинального биотопа высокими титрами E. coli (более 10 7 КОЕ/мл) и стрептококков группы В (10 6 КОЕ/мл). По данным микроскопии в этих случаях также отмечалась выраженная лейкоцитарная реакция (более 40 лейкоцитов в поле зрения).
У 21,06% женщин микроскопически был установлен бактериальный вагиноз, что сопровождалось высокой колонизацией факультативно-анаэробной и анаэробной флоры (более 10 6 КОЕ/мл).
В 0,56% случаев состояние вагинальной микроэкологии было оценено как другой вариант дисбиоза влагалища, когда при минимальном содержании микрофлоры (данные микроскопии) доминировали факультативно-анаэробные и аэробные УПМ (грамположительные кокки), а лактоморфотипы были единичными в поле зрения.
Таким образом, только у 19,9% пациенток с ЦМВИ имелся классический вариант микроценоза, в остальных случаях микрофлора влагалища претерпевала изменения, связанные с нарастанием титра факультативно-анаэробных УПМ. У 80,1% женщин выявлены нарушения микроценоза влагалища, в большинстве случаев связанные с увеличением количества Candida spp. При исследовании отделяемого из уретры с помощью ПЦР идентифицированы возбудители ИППП и УПМ. Наиболее часто выявлялись ДНК HPV (11,52%), T. vaginalis, M. hominis, HSV 1-го и 2-го типов (2,81 и 3,08% соответственно), С. trachomatis были идентифицированы в уретре у 5,34% больных.
В цервикальном канале в 5 раз чаще определялись УПМ и патогены. Так, наиболее часто у женщин с ЦМВИ были выделены вирус папилломы человека (42,13%), T. vaginalis (11,52%), M. hominis (21,63%), С. trachomatis (18,82%) и Ureaplasma spp. (24,44%).
В соскобах из влагалища также наиболее часто определялась ДНК вируса папилломы человека (43,25%), T. vaginalis (21,35%), M. hominis (14,89%), Ureaplasma spp. (19,38%), а также G. vaginalis (25%).
При исследовании проб из прямой кишки были идентифицированы ДНК ВПЧ (28,93%) и M. hominis (11,24%).

Для верификации диагноза ЦМВИ проводили расширенный анализ результатов, полученных разными методами исследования (табл. 9).
При анализе данных с целью выявления маркеров ЦМВИ установлена наибольшая частота обнаружения анти-CMV IgG — 356 (100%) случаев. Анти-CMV IgM были выявлены у 89 (25%) женщин. Обнаружение антител класса G к CMV свидетельствовало как об инфицированности, так и о наличии в большинстве случаев сформированного специфического противовирусного иммунитета. Выявление антител класса М совместно с IgG было одним из признаков реактивации данной вирусной инфекции.
При исследовании материала, полученного из урогенитального тракта с помощью ПЦР, ДНК CMV была обнаружена у 208 (58,43%) женщин.
ЦМВ на культуре фибробластов легких человека при исследовании крови выявлен у 93 (26,12%) женщин, мочи — у 199 (55,90%), слюны — у 204 (57,30%) больных, влагалищного отделяемого — у 225 (63,20%), из цервикального канала — в 268 (75,28%) случаях. В целом ЦМВ был обнаружен у 268 (75,28%) пациенток.
Учитывая этиологию, патогенез и клинические проявления ЦМВИ урогенитального тракта, пациенткам с реактивированной и латентной формой ЦМВИ проводилась комплексная терапия инфекционного процесса в соответствии с клиническими рекомендациями по ведению больных с ИППП. Противовирусное лечение включало использование препарата Панавир. Основное действующее вещество данного препарата — гексозный гликозид, полученный методом ферментативного гидролиза с последующей газожидкостной хроматографией, состоящий из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы, уроновых кислот. В ряде экспериментальных и клинических исследований установлена противовирусная и иммуномодулирующая активность Панавира. Данный препарат повышает неспецифическую резистентность организма к разным инфекциям и способствует индукции интерферона, Панавир (5 мл 0,004% раствора) применялся парентерально (внутривенно струйно) 1 раз в сутки через 48 ч (3 инъекции в 1-ю неделю лечения), затем — через 72 ч (2 инъекции во 2-ю неделю терапии). Всего на курс пришлось 5 инъекций в течение 2 недель.
При контрольном исследовании, проведенном через 14 дней после лечения, лишь у 2 (8,0%) пациенток с латентной формой ЦМВИ выявлен CMV в культуре клеток отделяемого цервикального канала, ДНК CMV не определялась у 24 (96%) больных. В результате лечения при реактивированной форме ЦМВИ была констатирована негативация IgM анти-CMV в крови у 100% женщин. При исследовании CMV на культуре фибробластов эмбрионов человека вирурия установлена у 1 (5,56%) пациентки, выделение из цервикального канала отмечено у 3 (16,67%). Результаты вирусологического обследования крови, слюны, влагалищных выделений были отрицательными у всех женщин. При проведении ПЦР наличие ДНК CMV выявлено у 2 (11,11%) пациенток, получавших парентерально Панавир.
Таким образом, в ходе исследования определены основные диагностические клинико-лабораторные критерии разных форм ЦМВИ урогенитального тракта сексуально активных женщин репродуктивного возраста, на основании которых возможности определения данной инфекции существенно увеличились. Наличие клинических проявлений при реактивированной ЦМВИ и определение вирусов при подостром или хроническом течении воспалительных заболеваний органов малого таза способствовали определению значимости данной инфекции в развитии патологии гениталий. Применение препарата Панавир в комплексной терапии повышало эффективность лечения в 89,5% случаев, что позволяет рекомендовать препарат Панавир для комплексной терапии ЦМВИ.
Вирусный энцефалит смешанного генеза (цитомегаловирус и вирус простого герпеса 1-го типа)
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(12): 100‑104
Шавловская О.А. Вирусный энцефалит смешанного генеза (цитомегаловирус и вирус простого герпеса 1-го типа). Журнал неврологии и психиатрии им. С.С. Корсакова. 2013;113(12):100‑104.
Virus encephalitis of mixed genesis (cytomegalovirus and simple herpes virus type 1). Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2013;113(12):100‑104. (In Russ.).
Вирусные энцефалиты - одно из наиболее тяжелых поражений нервной системы. Доказана ведущая роль вируса в патогенезе воспалительного процесса в ЦНС при таких заболеваниях, как герпетический и клещевой энцефалит, полиомиелит и др. В то же время существует ряд острых вирусных поражений ЦНС, так называемых постинфекционных острых диссеминированных энцефаломиелитов, имеющих сходную клиническую картину, но вызываемых разными вирусами: простого герпеса 1-го и 2-го типа (ВПГ-1, ВПГ-2) [3, 5, 7, 12, 14], цитомегаловируса (ЦМВ) [4], Эпштейна-Барр [17], гриппа [6], гепатита С [21] и др.
Неврологические симптомы острых диссеминированных энцефаломиелитов обычно проявляются на 4-13-й день после перенесенной инфекции или вакцинации, к 4-7-му дню заболевания нарастают симптомы неврологического дефицита и когнитивные нарушения. Эти заболевания нередко характеризуются острым началом с мультифокальным поражением ЦНС, включая энцефалопатию и множественные очаги на МРТ, заболевание нередко встречается у детей младшего возраста с симптомами оптикомиелита и рассеянного склероза [19].
Доля герпетических энцефалитов (ГЭ) является наибольшей среди тяжелых заболеваний, поражающих нервную систему, в структуре вирусных энцефалитов составляет около 20%, частота - 2-4 случая на 1 млн населения в год [4, 9, 13]. Это наиболее частая причина спорадических фатальных случаев энцефалита у детей старше 6 мес и взрослых в России [7], странах Европы и Америки [15]. Наиболее частые формы герпетических поражений ЦНС протекают в виде нейроинфекций - энцефалиты, миелиты, менингиты и др. [9]. Очаговая неврологическая симптоматика проявляется в виде моно- и гемипарезов [1]. Нередко эпилептические приступы являются первыми признаками поражения ЦНС при ГЭ [16].
Один из широко распространенных герпесвирусов - вирус Varicella zoster (варицелла зостер, ВВЗ). Ежегодно частота заболевания опоясывающим герпесом колеблется в зависимости от возраста и иммунного статуса заболевших в пределах 0,4-1,6 на 1000 человек в возрасте до 20 лет и от 4,5 до 11 случаев - в возрасте до 80 лет и старше [2]. Клиническая картина ГЭ характеризуется острым началом с высокой температурой в течение 3-4 дней с последующим развитием неврологической симптоматики. Частым признаком ГЭ является нарушение сознания вплоть до развития комы вследствие быстро нарастающего отека мозга. В 90% случаев отмечается поражение височных отделов [3]. Е.П. Деконенко и соавт. [5] описывают 44 пациента с ГЭ, получавших ацикловир, в 47,6% случаев на КТ-исследовании было выявлено поражение двух полушарий головного мозга, в 52,4% - одного. Одной из главных черт всех герпесвирусов является их способность переходить в латентное состояние с периодической реактивацией. Первичная инфекция кожи и слизистых может быть манифестной или асимптомной.
Е.П. Деконенко [2] было также установлено, что энцефалит обычно развивается на 7-10-й день после герпетических высыпаний и может проявляться в течение 6 нед после острого периода.
В случае хронической герпетической инфекции ЦНС речь не идет о переходе острого ГЭ в хронический процесс [9]. В этом случае может иметь место и энцефаломиелитическая форма инфекции, которая протекает с оптикомиелитическим или менингомиелитическим синдромами.
В этой статье описывается редкий клинический случай с проявлениями вирусного энцефалита, ассоциированного с цитомегаловирусом и висусом простого герпеса 1-го типа.
Больная К., 45 лет, казашка по национальности, врач-фармаколог, кандидат медицинских наук, обратилась за амбулаторной консультативной помощью 23.01.12.
Пациентка жаловалась на слабость в левых конечностях (больше в руке), подволакивание (шарканье) левой ноги и иногда подворачивание левой стопы при ходьбе, ухудшение зрения во время чтения книг, нарушение кратковременной памяти и эпизодические подергивания в левой руке (за последние полгода они участились до 2-3 раз в неделю).
Из анамнеза жизни: родилась в большой семье (четвертой по счету), имеет 6 братьев и сестер. С детства страдает аллергическими реакциями, аллергические проявления имеет и племянник (сын младшей сестры). Простудными заболеваниями болеет крайне редко. Детей нет (последствие перенесенного в молодости аборта).
В октябре 2011 г. больная самостоятельно отменила мидокалм, так как посчитала, что эта терапия увеличивает интенсивность боли в правой паховой области и вызывает иррадиацию боли в направлении колена; тогда же отметила слабость в левых руке и ноге.
Дополнительно к сказанному можно отметить, что 16.01.12 больной была проведена магнитно-резонансная томография (МРТ) головного мозга: в белом веществе обоих полушарий, преимущественно субкортикально, определяются множественные очаги повышенного МР-сигнала с четкими контурами, размером 2-8 мм, без перифокального отека; единичный очаг 3 мм - в лучистости мозолистого тела слева. Заключение: МР-картина многоочагового поражения белого вещества, вероятно, сосудистого генеза, следует дифференцировать с демиелинизирующим заболеванием (см. рисунок). Рисунок 1. МРТ головного мозга больной К. от 16.01.12. Множественные очаги повышенного МР-сигнала с четкими контурами.
При осмотре больной отмечено, что она носит на шее медицинскую повязку из-за болезненности при глотании в левой половине глотки. Врач-отоларинголог поставил диагноз герпетической ангины.
Неврологический статус в день обращения за помощью 23.01.12: недостаточность конвергенции за счет левого глаза (с детства); нистагма нет; снижена чувствительность на левой половине лица; легкая асимметрия лица за счет левой половины; зрение снижено на оба глаза (–5 OS, –6 OD); сухожильные рефлексы с рук и ног симметричны, с расширением рефлексогенных зон; патологические знаки с верхних конечностей - непостоянный симптом Россолимо; снижен тонус в верхних и нижних конечностях, больше слева; снижена сила в верхних конечностях, больше слева; координаторные пробы выполняет уверенно; ходьба с открытыми и закрытыми глазами - без особенностей; при наклоне головы симптом Лермитта не выявляется; чувствительных изменений на теле и в конечностях не выявлено.
Для уточнения характера нарушений и исключения демиелинизирующего процесса в тот же день была проведена консультация окулиста и исследование вызванных потенциалов (ВП) ствола мозга. Заключение окулиста: диски зрительных нервов розовые, границы четкие; OU=6D, миопия высокой степени. Слуховые ВП ствола мозга и зрительные ВП при использовании шахматного паттерна - в норме. Было рекомендовано также исследование ЦСЖ, но от проведения люмбальной пункции больная отказалась в категорической форме.
В последующие дни обследование пациентки было продолжено.
Гемостазиологическое исследование (18.01.12): волчаночный коагулянт, Д-димеры - в норме. Параметры системы гемостаза: АЧТВ, антитромбин-3, фибриноген, протромбин, МНО, тромбиновое время - в норме. Ревмопробы: ревматоидный фактор, антистрептолизин-О, С-реактивный белок - отрицательные.
Исследование иммунологического статуса (15.01.12): показатели CD45/CD3 + (60% все Т-лимф., норма 55-75), CD45/CD3 + /CD4 + (41% Т-хелпер, норма 35-65), CD45/CD3 + /CD4 + (0,97·10 9 /л все Т-лимф., норма 0,6-1,9), CD45/CD3 + /CD8 + (18% цитотокс., норма 12-30), CD45/CD3 + /CD8 + (0,426·10 9 /л Л цитол., норма 0,3-0,8) и CD4/CD8 (2,278, норма 1,2-2,5) - в норме; параметр CD45/CD3 + снижен до 0,22·10 9 /л все Т-лимф. (норма 0,9-2,2) [1] .
Уровень глюкозы крови (27.01.12) - 5,04 ммоль/л, т.е. в пределах нормы.
Биохимический анализ крови (26.01.12): липопротеины низкой плотности - холестерин, триглицериды - в пределах нормы; повышены показатели: холестерин общ. - до 5,8 ммоль/л, липопротеины высокой плотности -холестерин - до 2,24 ммоль/л.
Исследование иммунологического статуса 05.02.12: CD95 54% (норма 23-60%), CD45/CD8 + CD38 + снижен до 9,0 (норма 10,0-20,0), CD8 + CD38 + повышен до 52,0 (норма 20,0-50,0).
Серологическая диагностика 26.01.12: Syphilis RPR, антитела к ВИЧ (анти-HIV ½), анти-HCV IgG (антитела класса G к вирусу гепатита С), HBsAg (антиген вируса гепатита В) - не обнаружены. ПЦР (полимеразная цепная реакция) и другие инфекции: ДНК ЦМВ, ДНК вируса Эпштейна-Барр, ДНК вируса герпеса VI типа) - не обнаружены.
Показатели исследования иммунологического статуса 05.02.12 были следующими: НСТ-тест 7 у.е. (норма 12-30 у.е.), НСТ-стим 15 у.е. (норма 40-95 у.е.), IgG 19,2 г/л (норма 7-20 г/л), IgA 1,84 г/л (норма 0,7-5 г/л), IgM 1,36 г/л (норма 0,2-2 г/л) - в рамках нормы. Маркеры инфекций ИФА: анти-HSV IgG (I и II), анти-HSV IgМ, анти-ЕВV-VСА IgG (антитела к вирусу Эпштейна-Барр), анти-ЕВV-VСА IgМ, анти-CMV IgM - не обнаружены, повышен показатель анти-СМV IgG (антитела класса G к ЦМВ) до 39,66 Е/мл [2] .
При повторном исследовании (14.03.12): анти-CMV IgG повышен до 200,4 АЕ/мл [3] ; анти-EBV-VCA IgG и анти-EBV-EBNA IgG не обнаружены, повышен показатель анти-HSV IgG I (антитела к ВПГ-1) до 7,51 Е/мл и снижен показатель анти-HSV IgG II (антитела к ВПГ-2) до 0,33 Е/мл [4] .
Таким образом, повышение титров антител к ЦМВ подтверждает его участие в этиологии заболевания. Антитела к ВПГ-1, которые определялись к 14.03.12, указывают на его подключение в качестве возбудителя заболевания.
Повторный осмотр 06.02.12: за период с 23.01.12 по 06.02.12 больная лечилась противовирусным препаратом валтрекс по рекомендации оториноларинголога, после чего отметила снижение чувствительности на слизистой полости рта слева. Предъявляет жалобы на снижение чувствительности на левой щеке, прикусывание слизистой оболочки левой щеки также из-за снижения чувствительности в этой зоне. Назначено симптоматическое лечение: нейромультивит, рибоксин, мильгамма, омега-3. В неврологическом статусе: без отрицательной динамики. В течение 1 мес ежедневно делала гимнастику для восстановления силы в руках.
Было рекомендовано продолжение симптоматической терапии до консультации в Институте полиомиелита и вирусных энцефалитов им. М.П. Чумакова. Заключение вирусолога 07.06.12: острый диссеминированный энцефаломиелит под вопросом. Специфическая терапия в данный момент не показана.
15.09.12 была проведена МРТ, по результатам которой было выявлено многоочаговое поражение белого вещества, без отрицательной динамики в сравнении с МРТ от 16.01.12.
Повторное обследование 17.09.12: больная жалоб не предъявляет. В неврологическом статусе отрицательной динамики нет. Пациентка успешно работает в коммерческой клинике.
Окончательный диагноз: вирусный энцефалит, ассоциированный с цитомегаловирусом и вирусом простого герпеса 1-го типа.
Описанный случай достаточно сложен для однозначной трактовки клинических симптомов и результатов инструментальных и лабораторных исследований. Тем не менее нами предпринята попытка соответствующего анализа представленного наблюдения.
Известно, что вирусный энцефалит простого герпеса верифицируют на основании данных исследования ЦСЖ с применением ПЦР [11, 18].
Y. Guo и соавт. [17] наблюдали пациентку 19 лет, страдавшую ГЭ в течение 8 лет. В анамнезе нет указаний на то, что больная переносила какое-либо тяжелое инфекционное (вирусное) заболевание. В сыворотке крови были выявлены высокие титры антител к вирусам ВПГ-1, ВПГ-2, опоясывающего лишая, ветряной оспы, Эпштейна-Барр, гриппа A. У больной была обнаружена гетерозиготная мутация гена TLR3. На основании данного исследования авторы заключили, что дефицит гена TLR3 обусловливает предрасположенность к восприимчивости вируса простого герпеса у здоровых лиц. Аналогичные результаты получили V. Sancho-Shimizu и соавт. [20]: дефицит гена TLR3 - новая генетическая этиология энцефалита, вызванного вирусом Herpes simplex.
М.Е. Хмара [9] описал 52 больных с особым типом развития патологического процесса, не сопровождающегося общеинфекционными проявлениями, характерными для типичного острого ГЭ, и это позволило при дальнейшем анализе рассматривать таких больных как переносящих первичную хроническую герпетическую инфекцию ЦНС. Известны случаи развития хронического герпетического энцефалита через 12 лет после перенесенного острого ГЭ. Ж.Р. Идрисовой и соавт. [6] проведено исследование 60 больных с острыми вирусными энцефалитами, у 14 из которых был диагностирован ГЭ. По данным исследования, отличительная особенность ГЭ - возрастание уровня общего IgE, в 7 раз превышающее возрастную норму на 3-4-й неделе болезни.
Ранее Е.П. Деконенко и соавт. [4] был описан случай менингоэнцефалита, ассоциированного с цитомегаловирусом, вирусом простого герпеса и ВВЗ у подростка 16 лет. Развитие острого инфекционного заболевания сопровождалось нарушением высших мозговых функций (спутанность сознания, бред, галлюцинации, генерализованные тонико-клонические судороги) с последующей верификацией обширного очага на МРТ. Характер неврологических изменений с преобладанием психических нарушений, повышение белка и незначительное увеличение цитоза в ЦСЖ были расценены как проявления энцефалопатии на фоне реактивации латентной инфекции ВВЗ, происшедшей у пациентки, - реконвалесцента тяжелой формы менингоэнцефалита, вызванного сочетанной инфекцией цитомегаловирусом и вирусом простого герпеса.
Таким образом, в описанном нами редком случае вялотекущего течения вирусного энцефалита, ассоциированного с цитомегаловирусом и вирусом простого герпеса, диагностика заболевания была основана на определении специфических антител к вирусу герпеса 1-го типа и цитомегаловируса в крови.
В последнее время появляются публикации, указывающие на недостаточную чувствительность исследования ЦСЖ за исключением определения в ней антител. Хотя в настоящее время большинство нейроинфекций диагностируется с применением метода ПЦР, имеющего большие преимущества, он не лишен недостатков, поскольку может быть псевдонегативным в первые 3-4 дня болезни и его чувствительность существенно снижается после 10-20-го дня.
Не исключена возможность вирусных осложнений в восстановительный период после перенесенного энцефалита в стадии реконвалесценции [4], как наблюдалось в описанном случае (высыпания на лице, герпетическая ангина). Хотя течение энцефалита у наблюдаемой больной было относительно легким, несмотря на двустороннее поражение головного мозга, его исход можно считать достаточно благополучным. Больная полностью социально адаптирована и продолжает успешно работать. Вероятно, сказался положительный эффект от постоянно проводившегося лечения противовирусными препаратами (валтрекс, фамвир).
[1] CD - сокр. от англ. cluster of differentiation, cluster designation - кластер дифференцировки, используемый для дифференцировочных антигенов лейкоцитов человека, применяется в иммунофенотипировании для отнесения клеток к тому или иному типу по представленным на клеточных мембранах молекулам-маркерам: T-лимфоциты CD45 + , CD3 + ; Т-хелперы CD45 + , CD3 + , CD4 + ; цитотоксические Т-лимфоциты CD45 + , CD3 + , CD8 + . Количество CD4 и CD8 T-лимфоцитов в крови используется для мониторинга развития ВИЧ-инфекции [8, 10].
Цитомегаловирусная и папилломавирусная инфекции: возможности лечения и прегравидарной подготовки с применением противовирусного препарата на растительной основе
Журнал: Российский вестник акушера-гинеколога. 2015;15(4): 12‑17
Ежедневно человек вступает в контакт с огромным количеством микроорганизмов и вирусов, которые могут вызывать изменения функций систем организма, приводя к различным по тяжести и длительности заболеваниям, а также к неблагоприятным последствиям этих болезней.
Основными этапами взаимодействия вирусов с клеткой хозяина являются адсорбция (взаимодействие специфических рецепторов вируса и клетки хозяина), слияние суперкапсида с мембраной клетки, выделение нуклеиновых кислот нуклеокапсида и активация вирусной нуклеиновой кислоты, синтез нуклеиновых кислот и вирусных белков, сборка вирионов и выход новых вирусных частиц из клеток в межклеточное пространство, кровь или лимфу [1, 2].
К наиболее распространенным инфекциям относится инфекция, вызванная вирусами простого герпеса (ВПГ), основными особенностями которой по современным представлениям являются глобальный нозоареал распространенности, множество путей и способов передачи вирусов, чрезвычайно высокая инфицированность во всем мире, корреляция серопозитивности с социально-экономическими условиями, существование вирусов в ассоциациях с коинфекциями, высокая естественная восприимчивость людей и ряд других факторов. В Российской Федерации и странах СНГ ежегодно регистрируется около 22 млн случаев рецидивов герпесвирусной инфекции [3].
К группе вирусов, являющихся возбудителями герпетической инфекции, относятся цитомегаловирусы (ЦМВ). Актуальность изучения заболеваний, вызванных этими вирусами, обусловлена неблагоприятными последствиями, которые могут возникать в случае инфицирования в периоде новорожденности или на первом году жизни ребенка, или при первичном заболевании матери во время беременности [4]. По данным статистики, на первом году жизни антитела к цитомегаловирусной инфекции (ЦМВИ) обнаруживаются у 20% детей. У посещающих детские сады детей распространенность инфекции составляет 25—80%, во взрослой популяции антитела к ЦМВ встречаются у 85—90% населения [5].
Источником инфицирования может быть вирусоноситель, больной острой формой (в случае первичного инфицирования) или больной в период обострения инфекции. Пути передачи инфекции: воздушно-капельный, половой, контактный, пероральный, парентеральный, энтеральный и вертикальный, при этом передача вирусов может осуществляться через все биологические жидкости и выделения организма (слюна, моча и др.). При проникновении в организм иммунокомпетентных лиц, после первичного инфицирования, вирус может оставаться в организме пожизненно, в этом случае инфекция протекает бессимптомно (вирусоносительство), так как вирус защищен лимфоцитами от действия специфических антител и интерферона [6].
В современной медицинской литературе латентное течение инфекции, вызванной ЦМВ, обозначается как ЦМВ-инфекция, а клинически выраженное течение с поражением органов — как ЦМВ-болезнь. Развитие ЦМВ-болезни характеризуется лейкоцитарной инфильтрацией различных органов, что косвенно свидетельствует об участии в этом патологическом процессе интерлейкина-8, макрофагального воспалительного протеина-1α (MIP-1α) и других хемокинов и адгезивных молекул [7].
Клинически выраженное заболевание может развиваться при первичном инфицировании, при активации латентной инфекции на фоне снижения резистентности организма, что может наблюдаться у детей, беременных, взрослых со сниженным иммунитетом.
Клиническая картина ЦМВИ неспецифична и во многом зависит от пути инфицирования, состояния иммунной системы. Наиболее типичными симптомами ЦМВ-болезни являются лихорадка выше 38 °C, лейкопения, тромбоцитопения, повышение активности печеночных ферментов [8]. При ЦМВ-болезни могут развиваться поражение желудочно-кишечного тракта, гриппоподобные симптомы, воспалительные процессы носо- и ротоглотки. Наиболее тяжелая форма заболевания — ЦМВ-пневмония, характеризуется развитием тяжелой дыхательной недостаточности нередко с резистентностью к антибиотикам.
Вирусоносительство, проявляющееся стойким обнаружением антител класса G к ЦМВ, наблюдается у 90—95% взрослого населения (ЦМВ-позитивность), при этом вирусоноситель не опасен для окружающих, однако при снижении иммунитета носительство может перейти в активную форму, что вызывает появление антител класса М или многократное повышение уровня антител класса G. Генерализованная форма может возникать у лиц с выраженным иммунодефицитом и проявляться воспалением околоушных и подчелюстных слюнных желез, печеночной ткани, надпочечников, селезенки, суставов и других органов. Проявлениями локализованной формы у женщин может быть цервицит, эндометрит, сальпингоофорит, воспаление слюнных желез, шейных лимфатических узлов, у мужчин может быть бессимптомное носительство или вялотекущий уретрит.
У беременных женщин в 50—85% случаев обнаруживаются антитела к цитомегаловирусам, а у 1—12% беременных может наблюдаться первичное инфицирование, представляющее опасность для плода [5].
Первичная ЦМВИ и реактивация хронического процесса могут вызывать такие осложнения как неразвивающаяся беременность или невынашивание беременности, фетоплацентарная недостаточность, синдром задержки роста плода, многоводие, преждевременная отслойка плаценты и другие. Следует отметить, что при первичном инфицировании риск передачи вируса плоду выше, чем при обострении хронической инфекции, а последствия для плода зависят от срока гестации, при котором произошло первичное заражение или реактивация инфекции [9]. В случае, если первичное инфицирование женщины произошло в первой половине беременности, то у 8—10% детей, рожденных этими матерями, могут возникать клинические проявления в виде гепатоспленомегалии, гепатита, тромбоцитопении, петехиальной сыпи, микроцефалии, ретинита, гипербилирубинемии, гипотрофии, синдрома задержки роста плода, пневмонии и других проявлений [10, 11].
Инфицирование во второй половине беременности может приводить к хронической врожденной ЦМВИ, в тяжелых случаях — к нарушению функции центральной нервной системы, печени, нарушению зрения и слуха. Интранатальное и раннее постнатальное инфицирование, возникающее при вскармливании новорожденных серопозитивными матерями, протекает, как правило, без клинических проявлений и встречается чаще, чем трансплацентарное.
Трудности диагностики ЦМВИ связаны с отсутствием сезонной цикличности заболеваемости, характерных клинических проявлений заболевания, частой распространенностью латентных форм течения инфекционного процесса.
Другая широко распространенная вирусная инфекция — папилломавирусная (ПВИ) является ведущей причиной рака шейки матки, возникновения кондилом, плоскоклеточных неоплазий различной локализации. Распространенность инфекции вируса папилломы человека (ВПЧ) в мире среди женщин в возрасте 15—74 лет с отрицательными результатами цитологических мазков варьирует в зависимости от региона и составляет от 5 до 40%. Наиболее широко инфекция распространена среди сексуально активных подростков и женщин молодого возраста; 85% женщин в течение своей жизни инфицируются вирусом [12].
В литературе описано более 200 типов папилломавируса, которые являются строгими эпителиотропами, поражающими эпителий кожи и слизистых оболочек гениталий и других органов (гортань, ротовая полость, глаза и др.) [13].
ВПЧ подразделяют на две группы: ВПЧ низкого и высокого онкогенного риска. Высокоонкогенные типы ВПЧ ассоциированы в первую очередь с плоскоклеточными интраэпителиальными поражениями аногенитальной области (шейки матки — CIN, вульвы — VIN, влагалища — VaIN, ануса — AIN). ВПЧ является причиной рака шейки матки в 91—99,7%, рака вульвы (69%), влагалища (75%), полового члена (63%), предстательной железы, яичника — в 10—30%, рака гортани и ротовой полости — в 10—30% случаев [10].
Способность к неограниченно долгому персистированию ВПЧ в организме больного обусловлена особенностями жизненной стратегии этих вирусов, основанной на блокировании механизмов врожденного и адаптивного антивирусного иммунитета [11]. Механизм развития рака связывают с интеграцией вирусного генома в хромосомы клеток хозяина и длительной его персистенцией [13].
Противовирусная защита организма хозяина — очень сложный и многокомпонентный механизм. Отличительным свойством вирусов в целом, ЦМВ и ВПЧ в частности, является то, что они не могут самостоятельно размножаться, но способны эффективно репродуцироваться в чувствительных клетках макроорганизма, где реализуют свою генетическую программу по созданию потомства [14—16]. При первичном взаимодействии с вирусами инфекционным агентам противостоят неспецифические защитные механизмы организма, к которым относятся эпителий кожи, слизистые оболочки. После проникновения вируса внутрь клетки основную роль в обеспечении местного иммунитета играют интерфероны, другие цитокины, вырабатываемые зараженными клетками, а также лимфоциты, макрофаги, обеспечивающие фагоцитоз и разрушение вирусов. Образующиеся при вирусных инфекциях антитела действуют непосредственно на вирусы или на клетки, инфицированные ими [17].
Практически все вирусы индуцируют выработку интерферонов, их образование является одной из наиболее ранних защитных реакций организма на внедрение вирусов; интерфероны способны подавлять внутриклеточные этапы репродукции вирусов в зараженных клетках, обеспечивать невосприимчивость к вирусам окружающих здоровых клеток и предотвращать диссеминацию вирусов в организме. Поэтому применение иммунотропных препаратов, интерферона и его индукторов становится необходимой частью общепринятого патогенетического лечения различных инфекционных заболеваний [18].
Основным методом диагностики ЦМВ является серологический с выявлением специфических антител к антигенам вируса. Для выявления особенностей течения инфекции рекомендуется определение авидности иммуноглобулинов классов M и G и антител к вирусному белку. Молекулярно-биологические методы (ДНК-гибридизация, лигандная цепная реакция, полимеразная цепная реакция) при диагностике ЦМВИ, ПВИ и других инфекций позволяют выявлять ранние стадии, латентную и персистентную инфекцию, количественные параметры возбудителей. Цитологический метод применяется для проведения экспресс-диагностики ЦМВИ на поверхности хориона, плодных оболочек.
Лечение. Этиотропные препараты для лечения пациентов с вирусными (цитомегаловирусной, герпесвирусной, папилломавирусной и др.) инфекциями отсутствуют. При лечении больных с тяжелыми, генерализованными формами ЦМВИ возможно применение препаратов, обладающих противовирусным действием (ацикловир, ганцикловир, валацикловир, фамцикловир, фоскарнет и др.), которые прямо или опосредованно ингибируют вирусную ДНК-полимеразу, снижают вирусную продукцию у пациенток с клиническими симптомами, характерными для герпесвирусных инфекций. Однако эти агенты весьма токсичны, и требуется строгий контроль, особенно при длительном применении, за содержанием препарата в крови. Как правило, эти препараты назначают пациенткам после трансплантации или при выраженном снижении иммунитета [19, 20].
Токсичность препаратов в значительной степени ограничивает их применение. Препараты противопоказаны беременным, кормящим матерям и новорожденным, а также не рекомендуются женщинам, планирующим беременность.
Пациенткам с активной инфекцией в прегравидарный период с целью профилактики и лечения внутриутробной инфекции, а также лечения генерализованных форм возможно проведение профилактического лечения, позволяющего обеспечить в подавляющем большинстве случаев наступление беременности и благоприятное ее течение. С этой целью в прегравидарный период показано применение растительных противовирусных препаратов, рекомбинантного интерферона α-2, иммуноглобулина нормального человеческого и др. [21, 22].
В настоящее время весьма перспективным является препарат растительного происхождения, основным действующим компонентом которого служит очищенный экстракт побегов растения Solanum tuberosum, оказывающий противовирусное действие. На основе этого экстракта создан препарат Панавир, представляющий собой полисахарид, относящийся к классу гексозных гликозидов. Панавир способен повышать неспецифическую резистентность организма к инфекциям и индукцию интерферона, приводить к стабилизации показатели тканевого и гуморального иммунитета, что чрезвычайно важно для женщин, планирующих беременность.
Формы выпуска Панавира: раствор для внутривенных инъекций, ректальные и вагинальные суппозитории, гель для наружного применения и гель-спрей Панавир-Интим и Панавир-Инлайт. Панавир показал свою эффективность в лечении больных с папилломавирусной [23], цитомегаловирусной и герпетической инфекциями [24—26], вирусным гапатитом С [27], клещевым энцефалитом [28] и рядом других заболеваний.
Лечение пациенток с экзофитными кондиломами, хирургическое лечение при кондиломатозных высыпаниях (криодеструкция, радиоволновая хирургия, медикаментозная коагуляция, лазерная вапоризация), особенно проводимое в целях подготовки к беременности, можно комбинировать с местным лечением Панавиром. При этом обработка кондилом гелем Панавир, вагинальное орошение спреем или применение вагинальных (ректальных) суппозиториев способствуют более быстрому заживлению кожных рубцов, уменьшению частоты рецидивов, что важно для женщин, планирующих беременность. Экзофитные формы папилломавирусной инфекции могут возникать на фоне герпетических высыпаний или у женщин-носительниц ВПГ при хламидийной или других инфекциях. Перед назначением лечения рекомендуется проведение предварительного обследования женщин, а в случае выявления инфекций — проведение этиотропной терапии с последующим восстановлением микробиоценоза влагалища, что улучшает результаты лечения. По данным Г.Г. Анташян [23], при комплексном лечении больных с экзофитными формами ПВИ отмечается достоверное снижение частоты проведения деструктивных процедур, а также увеличение межрецидивных интервалов.
Обоснованным является применение Панавира при лечении пациенток с герпетическими поражениями кожи и слизистых оболочек, а также вирусоносительства. При лечении пациентов с рецидивирующим генитальным герпесом выявлено достоверное иммунокорригирующее и противовоспалительное действие препарата, увеличение длительности периодов ремиссии, что свидетельствует об эффективности Панавира [29—31]. Проведение лечения в период планирования беременности позволит снизить риск обострения инфекции в гестационный период.
Проведенные исследования показали хорошую переносимость препарата. Клинические испытания показали отсутствие мутагенного, тератогенного, канцерогенного, аллергизирующего и эмбриотоксического действия препарата при наличии слабого цитотоксического и антипролиферативного эффектов [32]. Назначение Панавира возможно в период прегравидарной подготовки, во II и III триместрах беременности в случае первичной инфекции или реактивации инфекционного процесса.
Для лечения пациенток с заболеваниями, вызванными вирусами, могут быть рекомендованы парентеральные формы Панавира, при этом терапевтическая доза препарата составляет 200 мкг действующего вещества. Кратность внутривенного введения и длительность лечения зависят от возбудителя заболевания. В случае подготовки к беременности, лечения цитомегаловирусной и папилломавирусной инфекций раствор Панавира применяют трехкратно в течение 1-й недели с интервалом 48 ч и двукратно в течение 2-й недели с интервалом 72 ч внутривенно медленно струйно. Возможно также применение Панавира в форме ректальных суппозиториев ежедневно на ночь в течение 10 дней с возможным повтором курса лечения через 1 мес.
Возможно интравагинальное введение суппозиториев при лечении больных с ПВИ-ассоциированной патологией шейки матки или ВПГ-инфицированием, при этом рекомендуемая длительность лечения также составляет 10 дней. Для лечения больных с экзофитными кондилломами рекомендуется нанесение геля Панавир тонким слоем на пораженные участки кожи и/или слизистых оболочек 5 раз в сутки. Продолжительность лечения составляет 4—5 дней, при необходимости курс лечения может быть продлен до 10 дней.
М.М. Дамиров и соавт. [33] показали высокую эффективность комплексного лечения пациенток с плоскоклеточными интраэпителиальными поражениями шейки матки низкой степени выраженности на фоне персистирующей ВПЧ-инфекции 0,004% раствором Панавира по схеме: 5 мл раствора внутривенно медленно курсом в 5 инъекций с и нтервалом 48 ч между первым и вторым введениями с последующим интервалом в 72 ч при одновременном местном применении препарата Панавир-Интим в форме геля интравагинально 2 раза в день в течение 10 дней с экспозицией 10—15 мин после введения препарата.
В 2012 г. проведено открытое рандомизированное сравнительное многоцентровое контролируемое клиническое исследование по изучению безопасности, переносимости и терапевтической эффективности раствора панавира для внутривенного введения 0,04 мг/мл в комплексной терапии беременных с хронической цитомегаловирусной инфекцией в стадии обострения во II и III триместрах беременности [34].
Цель исследования — провести оценку безопасности, переносимости и эффективности Панавира для внутривенного введения в составе комплексной терапии цитомегаловирусной инфекции у беременных во II и III триместре. Было выявлено, что терапия ЦМВ-инфекции Панавиром способствовала эрадикации вирусов, при этом ЦМВ серологическим методом не был обнаружен у женщин, получавших лечение, а также вирусная инфекция не оказала неблагоприятного влияния на течение беременности, развитие плодов и здоровье новорожденных.
Обобщение результатов проведенных исследований позволяет сделать заключение о перспективности дальнейшего изучения терапевтических свойств препарата Панавир в отношении вирусных инфекций, они убедительно доказали, что противовирусный препарат Панавир является эффективным средством при лечении больных с ЦМВИ, ВПЧ, ВПГ, клещевым энцефалитом, может применяться в период прегравидарной подготовки женщин группы высокого риска активизации этих инфекций во время беременности. Препарат показан в случае подготовки к беременности женщин с отягощенным анамнезом, при персистенции папилломавирусной инфекции, хронической, недавно перенесенной острой или с обострением других вирусных инфекций, а также женщинам, у которых диагностировано нарушение интерферонового статуса.
Поиск натуральных природных фармакологических агентов и анализ механизмов их действия является весьма актуальным аспектом в вопросе создания нового поколения противовирусных лекарственных препаратов с целью лечения инфекций человека.
Читайте также:

