Цвет желчи при гепатите
Обновлено: 24.04.2024
К наиболее распространенным хроническим заболеваниям желчного пузыря и желчевыводящих путей относятся хронические холециститы [1]. Хронический холецистит — воспалительное заболевание, вызывающее поражение стенки желчного пузыря, образование в нем камней
К наиболее распространенным хроническим заболеваниям желчного пузыря и желчевыводящих путей относятся хронические холециститы [1].
Хронический холецистит — воспалительное заболевание, вызывающее поражение стенки желчного пузыря, образование в нем камней и моторно-тонические нарушения билиарной системы. Развивается постепенно, редко после острого холецистита. При наличии камней говорят о хроническом калькулезном холецистите, при их отсутствии — хроническом бескаменном холецистите. Часто протекает на фоне других хронических заболеваний желудочно-кишечного тракта: гастрита, панкреатита, гепатита. Чаще страдают женщины [2].
Развитие хронического холецистита обусловлено бактериальной флорой (кишечная палочка, стрептококки, стафилококки и др.), в редких случаях анаэробами, глистной инвазией (описторхии, лямблии) и грибковым поражением (актиномикоз), вирусами гепатита. Встречаются холециститы токсической и аллергической природы.
Проникновение микробной флоры в желчный пузырь происходит энтерогенным, гематогенным или лимфогенным путем. Предрасполагающим фактором возникновения холецистита является застой желчи в желчном пузыре, к которому могут приводить желчные камни, сдавления и перегибы желчевыводящих протоков, дискинезии желчного пузыря и желчевыводящих путей, нарушения тонуса и двигательной функции желчных путей под влиянием различных эмоциональных стрессов, эндокринных и вегетативных расстройств, патологических рефлексов измененных органов пищеварительной системы. Застою желчи в желчном пузыре также способствуют опущение внутренностей, беременность, малоподвижный образ жизни, редкие приемы пищи и др.; имеет также значение заброс панкреатического сока в желчные пути при их дискинезии с его протеолитическим действием на слизистую оболочку желчных протоков и желчного пузыря [1].
Непосредственным толчком к вспышке воспалительного процесса в желчном пузыре часто являются переедание, особенно прием очень жирной и острой пищи, прием алкогольных напитков, острый воспалительный процесс в другом органе (ангина, пневмония, аднексит и т. д.).
Хронический холецистит может возникнуть после острого, но чаще развивается самостоятельно и постепенно, на фоне желчнокаменной болезни, гастрита с секреторной недостаточностью, хронического панкреатита и других заболеваний органов пищеварения, ожирения [3]. Факторы риска развития хронического холецистита представлены в таблице 1.
При хроническом холецистите характерна тупая, ноющая боль в области правого подреберья постоянного характера или возникающая через 1–3 ч после приема обильной и особенно жирной и жареной пищи. Боль иррадиирует вверх, в область правого плеча и шеи, правой лопатки. Периодически может возникать резкая боль, напоминающая желчную колику. Нередки диспепсические явления: ощущение горечи и металлического вкуса во рту, отрыжка воздухом, тошнота, метеоризм, нарушение дефекации (нередко чередование запора и поноса), а также раздражительность, бессонница.
Желтуха не характерна. При пальпации живота, как правило, определяется чувствительность, а иногда и выраженная болезненность в проекции желчного пузыря на переднюю брюшную стенку и легкое мышечное сопротивление брюшной стенки (резистентность). Часто положительны симптомы Мюсси-Георгиевского, Ортнера, Образцова-Мерфи. Печень несколько увеличена, с плотноватым и болезненным при пальпации краем при осложнениях (хронический гепатит, холангит). Желчный пузырь в большинстве случаев не пальпируется, так как обычно он сморщен вследствие хронического рубцово-склерозирующего процесса. При обострениях наблюдаются нейтрофильный лейкоцитоз, повышение СОЭ и температурная реакция. При дуоденальном зондировании часто не удается получить пузырной порции В желчи (вследствие нарушения концентрационной способности желчного пузыря и нарушения пузырного рефлекса) или же эта порция желчи имеет несколько более темную окраску, чем А и С, часто мутна. При микроскопическом исследовании в дуоденальном содержимом обнаруживается большое количество слизи, клеток десквамированного эпителия, лейкоцитов, особенно в порции В желчи (обнаружению лейкоцитов в желчи не придают такого значения, как раньше; как правило, они оказываются ядрами распадающихся клеток дуоденального эпителия). Бактериологическое исследование желчи (особенно повторное) позволяет определить возбудителя холецистита.
При холецистографии отмечается изменение формы желчного пузыря, часто его изображение получается нечетким вследствие нарушения концентрационной способности слизистой, иногда в нем обнаруживаются камни. После приема раздражителя — холецистокинетика — отмечается недостаточное сокращение желчного пузыря. Признаки хронического холецистита определяются и при ультразвуковом исследовании (в виде утолщения стенок пузыря, деформации его и т. д.).
Течение в большинстве случаев длительное, характеризуется чередованием периодов ремиссии и обострения; последние часто возникают в результате нарушений питания, приема алкогольных напитков, тяжелой физической работы, присоединения острых кишечных инфекций, переохлаждения.
Прогноз в большинстве случаев благоприятный. Ухудшение общего состояния больных и временная потеря их трудоспособности характерны лишь в периоды обострения болезни. В зависимости от особенностей течения выделяют латентную (вялотекущую), наиболее распространенную — рецидивирующую, гнойно-язвенную формы хронического холецистита.
Диагностика хронических холециститов
Диагностика хронических холециститов основывается на анализе:
- анамнеза (характерные жалобы, очень часто в семье имеются другие больные с патологией желчевыводящих путей) и клинической картины заболевания;
- данных ультразвукового исследования;
- результатов компьютерной томографии гепатопанкреатобилиарной зоны, гепатосцинтиграфии;
- клинических и биохимических показателей крови и желчи;
- показателей копрологического исследования.
Отличительной особенностью диагностики хронических холециститов является проведение дуоденального зондирования с последующим микроскопическим и биохимическим исследованиями состава желчи.
Дуоденальное зондирование проводят утром натощак. Наилучшим желчегонным средством, применяющимся для получения порций В и С при дуоденальном зондировании, является холецистокинин, при применении которого дуоденальная желчь содержит гораздо меньше примесей желудочного и кишечного соков. Доказано, что наиболее рационально производить фракционное (многомоментное) дуоденальное зондирование с точным учетом количества выделяющейся желчи во времени. Фракционное дуоденальное зондирование позволяет более точно определить тип секреции желчи.
Процесс непрерывного дуоденального зондирования состоит из 5 этапов. Количество желчи, выделившееся за каждые 5 мин зондирования, регистрируют на графике.
Первый этап — это время холедоха, когда истекает светло-желтая желчь из общего желчного протока в ответ на раздражение стенки двенадцатиперстной кишки оливой зонда. Собирают 3 порции по 5 мин каждая. В норме скорость выделения желчи порции А — 1-1,5 мл/мин. При большей скорости истечения желчи имеется основание думать о гипотонии, при меньшей скорости — о гипертонии общего желчного протока. Затем через зонд медленно (в течение 3 мин) вводят 33% раствор сульфата магния (в соответствии с возвратом больного — 2 мл на год жизни) и закрывают зонд на 3 мин. В ответ на это наступает рефлекторное закрытие сфинктера Одди, и истечение желчи прекращается.
Третий этап — время выделения желчи порции А. Начинается с момента открытия сфинктера Одди и появления светлой желчи. В норме за 2-3 мин вытекает 4–6 мл желчи (1-2 мл/мин). Большая скорость отмечается при гипотонии, меньшая — при гипертонии общего желчного протока и сфинктера Одди.
Четвертый этап — время выделения желчи порции В. Начинается с момента выделения темной пузырной желчи вследствие расслабления сфинктера Люткенса и сокращения желчного пузыря. В норме за 20–30 мин выделяется в зависимости от возраста около 22–44 мл желчи. Если опорожнение желчного пузыря происходит быстрее и количество желчи меньше указанного, то есть основание думать о гипертонически-гиперкинетической дисфункции пузыря, а если опорожнение идет медленнее и количество желчи больше указанного, то это свидетельствует о гипотонически-гипокинетической дисфункции пузыря, одной из причин которой может быть гипертония сфинктера Люткенса (исключение составляют случаи атонического холестаза, окончательная диагностика которого возможна при УЗИ, холецистографии, радиоизотопном исследовании).
Если желчь получить не удалось, то зондирование проводят через 2-3 дня на фоне подготовки больного препаратами атропина и папаверина. Непосредственно перед зондированием целесообразно применить диатермию, фарадизацию диафрагмального нерва. Микроскопию желчи проводят сразу же после зондирования. Материал для цитологического исследования можно сохранять в течение 1-2 ч, прибавляя к нему 10% раствор нейтрального формалина (2 мл 10% раствора на 10–20 мл желчи).
На посев необходимо посылать все 3 порции желчи (А, В, С).
Микроскопия желчи. Лейкоциты в желчи могут быть ротового, желудочного и кишечного происхождения, поэтому при дуоденальном зондировании лучше использовать двухканальный зонд, который позволяет постоянно отсасывать желудочное содержимое. Кроме того, при безусловно доказанном холецистите (при операции у взрослых) в 50–60% случаев в желчи порции В содержание лейкоцитов не увеличено. Лейкоцитам в желчи сейчас придается относительное значение при диагностике холецистита.
В современной гастроэнтерологии диагностическое значение не придается обнаружению в желчи порции В лейкоцитов и клеточного эпителия желчевыводящих путей. Важнейшим критерием является наличие в порции В микролитов (скопление слизи, лейкоцитов и клеточного эпителия), кристаллов холестерина, комочков желчных кислот и билирубината кальция, коричневых пленок — отложение слизи в желчи на стенке желчного пузыря.
Присутствие лямблий, описторхий может поддерживать различные патологические (в основном воспалительные и дискинетические) процессы в желудочно-кишечном тракте. В желчном пузыре здоровых людей лямблии не обитают, так как желчь вызывает их гибель. Желчь больных холециститом не обладает этими свойствами: лямблии поселяются на слизистой оболочке желчного пузыря и способствуют (в комплексе с микробами) поддержанию воспалительного процесса, дискинезии.
Таким образом, лямблии не могут вызвать холецистита, но могут быть причиной развития дуоденита, дискинезий желчных путей, т. е. отягощать холецистит, способствуя его хроническому течению. Если у больного обнаружены в желчи вегетативные формы лямблий, то в зависимости от клинической картины заболевания и результатов дуоденального зондирования как основной диагноз ставят либо хронический холецистит, либо дискинезию желчевыводящих путей, а как сопутствующий — кишечный лямблиоз.
Из биохимических отклонений желчи признаками холецистита являются повышение концентрации белка, диспротеинохолия, увеличение концентрации иммуноглобулинов G и A, С-реактивного протеина, щелочной фосфатазы, билирубина.
Результаты зондирования должны трактоваться с учетом анамнеза и клинической картины заболевания. Диагностической ценностью для выявления шеечного холецистита обладает компьютерная томография.
Эхографические (ультразвуковые) признаки хронического холецистита:
Во многих современных руководствах УЗИ-диагностику считают решающей в выявлении характера патологии желчного пузыря.
Как уже говорилось, дискинезия желчевыводящих путей не может быть основным или единственным диагнозом. Длительно текущая дискинезия желчевыводящих путей неизбежно приводит к избыточной контаминации кишечника, а та, в свою очередь, к инфицированию желчного пузыря, особенно при дискинезии гипотонического типа.
При хроническом заболевании желчевыводящих путей для исключения пороков их развития приводят холецистографию. При рентгенологическом исследовании у больных с гипотонической дискинезией виден увеличенный, расширяющийся книзу и нередко опущенный желчный пузырь; опорожнение его замедленное. Имеется гипотония желудка.
При гипертонической дискинезии тень желчного пузыря уменьшена, интенсивная, овальной или сферической формы, опорожнение ускоренное.
Инструментально-лабораторные данные
Течение хронического холецистита может быть рецидивирующим, скрытым латентным или в виде приступов печеночной колики.
При часто рецидивирующем холецистите возможно развитие холангита. Это воспаление крупных внутрипеченочных протоков. Этиология в основном та же, что и при холецистите. Часто сопровождается повышением температуры тела, иногда ознобом, лихорадкой. Температура хорошо переносится, что вообще характерно для коли-бациллярной инфекции. Характерно увеличение печени, край ее становится болезненным. Часто появляется желтизна, связанная с ухудшением оттока желчи вследствие закупорки желчных протоков слизью, присоединяется кожный зуд. При исследовании крови — лейкоцитоз, ускоренная СОЭ.
Лечение
При обострениях хронического холецистита больных госпитализируют в хирургические или терапевтические стационары и лечение проводят, как при остром холецистите. В легких случаях возможно амбулаторное лечение. Назначают постельный режим, диетическое питание (диета №5а) с приемом пищи 4–6 раз в день [1].
Этиотропное лечение назначается, как правило, в фазы обострения процесса. Из антибиотиков рекомендуется назначать препараты широкого спектра действия, которые поступают в желчь в достаточно высокой концентрации — макролиды, последнего поколения кларитромицин (синонимы: клацид, фромилид) 250 мг, 500 мг 2 раза в день и более известные эритромицин 250 мг 4 раза в день, пролонгированные тетрациклины доксициклин 100 мг, юнидокс солютаб 100 мг по схеме в первый день 200 мг за 2 приема, в дальнейшем по 100 мг во время еды в течение 6 дней. Все препараты назначаются в обычных терапевтических дозах курсами 7–10 дней. При лямблиозе желчных путей эффективны метронидазол 200 или 400 мг, суточная доза 1200 мг (синонимы: метрогил, трихопол, клион) или тинидазол 500 мг суточная доза 2 г в течение 2-3 дней. При описторхозе желчевыводящих путей эффективен противопаразитарный препарат празиквантел 600 мг по 25 мг/кг 1–3 раза/сут.
Для устранения дискинезии желчных путей, спастических болей, улучшения желчеоттока назначают симптоматическую терапию одним из следующих лекарственных препаратов.
Селективные миотропные спазмолитики: мебеверин (дюспаталин) по 200 мг 2 раза в день (утром и вечером, курс лечения 14 дней).
Прокинетики: цизаприд (координакс) 10 мг 3-4 раза в день; домперидон (мотилиум) 10 мг 3-4 раза в день; метоклопромид (церукал, реглан) 10 мг 3 раза в день.
Системные миотропные спазмолитики: но-шпа (дротаверин) 40 мг 3 раза в день; никошпан (но-шпа + витамин РР) 100 мг 3 раза в день.
М- холинолитики: бускопан (гиоцинабутил бромид) 10 мг 2 раза в день.
Сравнительная характеристика системных и селективных спазмолитиков отражена в таблице 2.
Преимущества селективного спазмолитика мебеверина (дюспаталина)
- Дюспаталин обладает двойным механизмом действия: устраняет спазм и не вызывает атонии кишечника.
- Действует непосредственно на гладкомышечную клетку, что ввиду сложности нервной регуляции кишечника является предпочтительным и позволяет получить предсказуемый клинический результат.
- Не действует на холинергическую систему и поэтому не вызывает таких побочных эффектов, как сухость во рту, нарушение зрения, тахикардию, задержку мочи, запор и слабость.
- Можно назначать пациентам, страдающим гипертрофией предстательной железы.
- Избирательно действует на кишечник и билиарный тракт.
- Отсутствуют системные эффекты: вся вводимая доза полностью метаболизируется при прохождении через стенку кишечника и печень до неактивных метаболитов и мебеверин не обнаруживается в плазме в крови.
- Большой клинический опыт применения.
- При наличии рефлюкса желчи в желудок рекомендуются антацидные препараты по 1 дозе спустя 1,5-2 ч после еды: маалокс (альгельдрат+магнезиум гидрохлорид), фосфалюгель (алюминиум фосфат).
Нарушения оттока желчи у больных хроническим холециститом корригируется желчегонными препаратами. Различают желчегонные средства холеретического действия, которые стимулируют образование и выделение желчи печенью, и холекинетические препараты, усиливающие мышечное сокращение желчного пузыря и поступление желчи в двенадцатиперстную кишку.
- оксафенамид, циквалон, никодин — синтетические средства;
- хофитол, аллохол, танацехол, тыквеол, холензим, лиобил, фламин, бессмертник, холагон, одестон, гепатофальк планта, гепабене, гербион капли желчегонные, кукурузные рыльца — растительного происхождения;
- фестал, дигестал, котазим — ферментные препараты, содержащие желчные кислоты.
Холекинетические препараты: холецистокинин, сульфат магния, сорбит, ксилит, карловарская соль, облепиховое и оливковое масло.
Холеретические препараты могут применяться при основных формах холецистита, в фазах затихающего обострения или ремиссии, назначаются обычно на 3 нед., затем препарат целесообразно сменить.
Больным некалькулезным холециститом с нарушениями физико-химических свойств желчи (дискринией) показано назначение в течение длительного периода времени (3–6 мес) пшеничных отрубей, энтеросорбентов (энтеросгель по 15 г 3 раза в день).
Диета: ограничение жирной пищи, ограничение калорийной пищи, исключение плохо переносимых продуктов. Регулярное 4-5-разовое питание.
При безуспешности консервативного лечения и частых обострениях необходимо хирургическое вмешательство.
Профилактика хронического холецистита заключается в соблюдении режима питания, занятиях спортом, физкультурой, профилактике ожирения, лечении очаговой инфекции.
По вопросам литературы обращайтесь в редакцию.
В статье представлены данные о нарушении билиарного статуса у пациентов с хроническими гепатитами В и С. При хронических гепатитах В и С имеют место выраженные изменения функционального состояния билиарного тракта, как в работе сфинктерного аппарата, так
The article presents data on disorders in biliary status in patients with chronic hepatitis B and C. In chronic hepatitis B and C, there are pronounced changes in the functional state of the biliary tract, both in the sphincter apparatus and in the gallbladder, as well as duodenal hypertension and increased hepatic choleresis. The revealed changes in the microscopic composition of bile also indirectly indicate the presence of inflammatory process in the biliary tract in patients with chronic hepatitis B and C.
В глобальном масштабе вирусный гепатит перешел на седьмое место причин смертей в 2013 г., по сравнению с 10-й ведущей причиной в 1990 г. [1]. Во всем мире вирусный гепатит А, по оценкам, поражает 1,4 млн человек в год [2]. Около 2 млрд человек в мире имеют доказательства прошлой или текущей инфекции гепатита В (HBV), из них 240 млн хронических носителей HBsAg [3]. Гепатит В, наряду с ассоциированной инфекцией вирусом гепатита D, является одним из наиболее распространенных патогенов, поражающих людей [4]. HBV ежегодно приводит к 650 000 смертей в результате гепатита, вызванного этим вирусным поражением печени [3].
Невозможно оценить ежегодную распространенность острой инфекции гепатита С (HCV) в мире, поскольку она протекает чаще бессимптомно. По оценкам экспертов, около 71 млн человек хронически инфицированы HCV во всем мире [2]. 55–85% этих людей имеют хроническую прогрессирующую HCV-инфекцию с 15–30-процентнным риском развития цирроза печени в течение двух десятилетий [5]. Китай, США и Россия имеют самую большую популяцию потребителей инъекционных наркотиков, которые инфицированы HCV.
HCV-инфекция характеризуется высокой частотой и разнообразием внепеченочных поражений. По результатам исследования 230 больных с хроническим гепатитом С (ХГС) в клинике им. Е. М. Тареева 47% пациентов имели внепеченочные поражения, что превышало частоту таковых при HBV-инфекции — 22–35% [6]. Как известно, печень и желчевыводящие пути анатомически функционально тесно взаимосвязаны. Поэтому патология печени может сопровождаться заболеваниями желчевыводящих путей. Поражения билиарного тракта, в том числе и функциональные расстройства, в какой-то степени обусловливают клинические проявления хронических гепатитов В и С.
В зарубежных исследованиях существуют единичные работы, в которых определена взаимосвязь ХГС и поражений желчевыводящих путей. Гепатит С стал прототипическим вирусным гепатитом с холангитовыми поражениями, которые представляют собой преимущественно интраэпителиальные лимфоцитарные инфильтрации [7] и лимфоидные агрегаты или образования фолликулов, обычно без повреждения канала. Эти ассоциированные с вирусом холангитовые поражения являются обратимыми и не приводят к прогрессированию процесса или кровотечению. Прогноз и ответ на терапию не связаны с наличием желчных поражений [8].
Среди гепатотропных вирусов вирус гепатита С чаще ассоциируется с холангитом. Развившийся холангит при вирусных гепатитах В и С является обратимым и не оказывает вредного влияния на течение заболевания или на эффективность терапии. При гепатите С в основе холангита лежит интраэпителиальная лимфоцитарная инфильтрация, как правило, без повреждения протоков. Несмотря на то, что вирус-индуцированный холангит является обратимым, все же происходят структурные повреждения, в том числе формирование дивертикулов, ассоциированных с воспалением. У этих пациентов обычно не регистрируется повышение уровня щелочной фосфатазы. Развитие холангита не ухудшает ответ на противовирусную терапию. Некоторые исследователи обнаружили частицы вируса гепатита в холангиоцитах [9, 10].
При HBV-инфекции описываемые гистологические изменения в желчных протоках существенно не отличаются от таковых при вирусном гепатите С, но встречаются в меньшем проценте случаев. Примерно в 25% случаев при HBV-инфекции биопсия показала наличие лимфоидных скоплений и в менее 10% случаев выявила повреждение желчных протоков. Поверхностный и ядерный антигены вируса гепатита В также были обнаружены в холангиоцитах [8].
K. S. Kumar с соавт. (2001) подтвердили влияние хронического холангита на течение гепатита С. В исследовании участвовали 620 пациентов с ХГС с повышенным уровнем щелочной фосфатазы сыворотки крови. У больных были исключены первичный билиарный цирроз печени и первичный склерозирующий холангит. Но у части пациентов морфологически было выявлено поражение внутрипеченочных желчных протоков. Авторы считают, что наличие холангита у данной группы пациентов связано с HCV-инфекцией [11].
В ряде других исследований также можно предположить роль НСV-инфекции в развитии поражения желчевыводящей системы (ЖВС). S. S. Sharma и соавт. выявили наличие функциональных расстройств сфинктера Одди у наркоманов с продолжительным стажем внутривенного введения наркотических веществ. Моторно-кинетические нарушения сфинктера Одди были подтверждены манометрией. Маркеры вирусных гепатитов у этих пациентов исследованы не были. Однако известно, что наркоманы составляют основную группу риска инфицирования HCV- и/или HBV-инфекцией. И именно этим вирусам, по-видимому, принадлежит роль в развитии дисфункциональных нарушений сфинктера Одди у данной категории пациентов [12].
Существуют работы, посвященные изучению возможной репликации вируса в желчном эпителии. M. A. Loriot с соавт. удалось in vitro инфицировать вирусом гепатита С клетки желчного эпителия у пациентов без НСV-инфекции. Это исследование, бесспорно, расширяет представление о клеточном тропизме вируса гепатита С и доказывает чувствительность желчного эпителия к данному вирусу [13].
К выводу о том, что билиарная система тесно связана с HCV-инфекцией и что желчь также инфицирована, как и сыворотка крови, пришли японские ученые. У 12 больных хроническим гепатитом С (у 8 была выявлена HCV PHK методом полимеразной цепной реакции) во время операции была аспирирована желчь тонкой пункционной иглой из желчного пузыря. У 5 больных с высоким содержанием РНК в сыворотке крови была обнаружена HCV PHK и в желчи. При сравнении уровней содержания вируса в сыворотке и желчи выявлено, что уровни РНК были одинаковыми. С помощью иммунопатологических исследований обнаружен вирус гепатита С в эпителиальных клетках у этих больных. В то же время у больных с отрицательной реакцией на HCV PHK вирус не был обнаружен ни в желчи, ни в желчных протоках [14].
Некоторые отечественные авторы также придерживаются точки зрения, что основной причиной расстройств ритмической деятельности билиарной системы являются воспалительные процессы в печени, приводящие к нарушению синтеза желчи, заметному уменьшению давления в протоковой системе и желчном пузыре, а в связи с этим и к постоянному спастическому сокращению сфинктера Одди [15–17].
По данным Н. Б. Волошиной (2004) у 89,6% пациентов с хроническим гепатитом В (ХВГ) диагностируются функциональные нарушения билиарного тракта. Среди них у 46,3% выявлено сочетание дисфункции сфинктера Одди по билиарному типу и гиперкинезии желчного пузыря, у 18,7% — изолированный гипертонус сфинктера Одди, 12,6% — имели гиперкинез желчного пузыря, 2,7% — гипокинез желчного пузыря и 1,6% — гипотонус сфинктера Одди. Было установлено, что функциональные нарушения билиарного тракта не зависят от типа вируса и ассоциированы с уровнем биохимической активности процесса [18].
Согласно исследованию В. А. Неронова (2010), у больных с хроническим HBV-поражением печени выявлен синдром хронической билиарной недостаточности, клинически проявляющийся жалобами на дискомфортные и (или) болевые ощущения в правом подреберье, непереносимость жирной пищи, метеоризм и обстипацию. Со стороны моторики билиарного тракта нарушен процесс работы сфинктерного аппарата желчевыводящих путей (гипертонус сфинктера Одди в 65,2% случаев — в стадии репликации, в 46,9% — в фазу интеграции вируса; гипертонус сфинктера Люткенса у 58,1% в фазу репликации и 47,2% в фазу интеграции вируса), также изменены физико-коллоидные свойства желчи с повышением плотности пузырной и печеночной порций, нарушен биохимический состав желчи, в виде снижения суммарного дебита холевой кислоты и фосфолипидов, а также холатохолестеринового и фосфолипидно-холестеринового коэффициентов. Что касается больных с хроническим HCV-поражением печени, билиарная недостаточность также имеет клинические проявления в виде непереносимости жирной пищи, метеоризма и обстипации. Со стороны моторики билиарного тракта выявлены следующие изменения: гипертонус сфинктера Одди в 79,6% у пациентов с высоким уровнем репликации и в 73,7% у пациентов с минимальной активностью. Гипертонус сфинктера Люткенса у 67,6% и у 69,3% соответственно. При изучении физико-коллоидных и биохимических свойств порций желчи установлены изменения в виде снижения дебита холевой кислоты и холатохолестеринового коэффициента. Выявлено, что хроническая билиарная недостаточность у больных с вирусными поражениями печени не специфична по отношению к возбудителю, а степень ее тяжести носит прямо пропорциональный характер степени активности вирусного процесса [19].
В работе В. Л. Останко (2010) проведено исследование состояния желчевыводящей системы (ЖВС) у пациентов с ХГС. Выявлено, что у 99% пациентов с ХГС наблюдаются изменения функционального состояния ЖВС в виде дисфункции желчного пузыря (гипотонически-гипокинетический тип у 82% и у 18% — гипертонически-гиперкинетический тип) и сфинктерного аппарата (гипертонус сфинктера Одди выявлен у 55,5% пациентов с гипертоническим типом дисфункции и у 1/3 пациентов при гипотонической дисфункции; также выявлены единичные больные с дисфункцией сфинктера Одди по гипокинетическому типу — 4%), сочетающиеся с нарушением коллоидного состава желчи в виде повышения степени литогенности (у 100% пациентов с ХГС). Причем обнаружена прямая корреляционная связь между стадией фиброза и риском развития желчекаменной болезни [20].
В своей работе К. В. Жданов и соавт. обследовали лиц молодого возраста с ХГС. У всех пациентов с помощью ультразвукового исследования, дуоденального зондирования, томографии было подтверждено наличие хронического холецистита. У 80% больных в желчи обнаружена патогенная микрофлора. В результате выполнения данной работы авторы сделали вывод, что успешная противовирусная терапия хронического гепатита С возможна только после проведения санации билиарного тракта [21].
Материалы и методы исследования
В нашей работе получены данные обследования 119 человек с хроническими гепатитами В и С в возрасте от 18 до 61 года (средний возраст составил 36,94 ± 11,2 года). Среди них — 45 женщин (37,8%) и 74 мужчины (62,2%). Согласно задачам исследования все пациенты разделены по этиологии заболевания на две группы: 1-я группа — 63 пациента с ХГС, 2-я группа — 56 пациентов с ХГВ. Контрольную группу составили 30 практически здоровых добровольцев аналогичного пола и возраста.
Всем больным проведено клиническое обследование, включающее сбор жалоб, анамнеза, объективный осмотр пациента. Клиническое обследование включало: общий анализ крови, общий анализ мочи, биохимический анализ крови, исследование уровней тканевых магния и цинка (в ногтях) методом масс-спектрометрии, иммунологическую диагностику маркеров вирусных гепатитов методами иммуноферментного анализа, полимеразной цепной реакции, эзофагогастродуоденоскопию, ультразвуковое исследование органов брюшной полости, электрокардиографию. Моторная функция ЖВС исследовалась путем проведения фракционного хроматического минутированного дуоденального зондирования с исследованием полученной желчи по методике В. А. Максимова [22].
Исследование проведено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации (в редакции 2000 г. с разъяснениями, данными на генеральной ассамблее ВМА, Токио, 2004), с правилами Качественной клинической практики Международной конференции по гармонизации (ICH GCP), этическими принципами, изложенными в Директиве Европейского Союза 2001/20/ЕС и требованиями национального российского законодательства. Протокол исследования был одобрен Комитетом по этике ФГБОУ ВО КемГМУ МЗ РФ; процедуры рассмотрения и одобрения исследования соответствовали требованиям национального законодательства. Каждый больной подписал информированное согласие на участие в исследованиях.
При характеристике качественных показателей строились таблицы сопряженности и вычислялись частоты, для количественных показателей рассчитывались средние величины и стандартное отклонение (M ± SD). При оценке различий качественных показателей использовался хи-квадрат Пирсона, критерий Z Стьюдента. При оценке связи между двумя количественными показателями использовался ранговый корреляционный анализ Спирмена. Для изучения влияния нескольких факторов на зависимую переменную (степень фиброза печени, индекс гистологической активности) применялся линейный регрессионный анализ. Достоверность различий абсолютных и относительных показателей оценивалась с использованием критериев Манна–Уитни, Крускалла–Уоллеса. Различия между параметрами сравнения считались статистически значимыми при р ≤ 0,05.
Моторно-эвакуаторная функция билиарного тракта у пациентов с хроническими гепатитами В и С оценивалась путем анализа данных, полученных при проведении фракционного хроматического минутированного дуоденального зондирования. Результаты хроматического минутированного дуоденального зондирования пациентов с хроническими гепатитами В и С представлены в табл. 1.
Учитывая выявленные нарушения моторно-эвакуаторной функции билиарного тракта, были выделены следующие группы больных (табл. 2).
Клинические проявления функциональных нарушений ЖВС у пациентов с ХВГ соответствовали хорошо известным признакам. Так, гипомоторная дисфункция ЖП сопровождалась болью тупого характера, чувством давления, распирания в правом подреберье, эпигастральной области, усиливающихся при смене положения тела, возникающих после погрешности в питании (жирная, жареная пища). При гипермоторной дисфункции ЖП больные жаловались на коликообразные боли в правом подреберье с иррадиацией в спину, под правую лопатку, правое плечо, эпигастральную область. Боли провоцировались приемом жирной, жареной пищи, физической нагрузкой, а также стрессовой ситуацией. Часть больных отмечала чувство горечи, особенно в утренние часы, тошноту, метеоризм.
Всем пациентам с ХВГ проведено исследование микроскопического состава желчи, результаты отражены в табл. 3.
Анализируя данные, представленные в табл. 3, видно, что у пациентов с ХВГ регистрировались изменения микроскопического состава желчи во всех порциях, что косвенно указывало на наличие воспалительного процесса в ЖВС. Так, в группе ХГС выявлены следующие изменения микроскопического состава желчи: слизь в порции А обнаружена у 57 человек (90,5%), в порции В — у 46 (73%) и в порции С — у 55 человек (87,3%). Эпителий цилиндрический в большом количестве в порции А встречался у чуть более половины группы (55,5%), в порции В — у 1/3 группы (20 человек), в порции С — у 28 человек (44,4%). Присутствие лейкоцитоидов более 10 в поле зрения в порции А выявлено у 10 человек (15,8%), в пузырной порции — у 6 человек (9,5%) и в печеночной порции — у 12 человек (19%). Обнаружение цилиндрического эпителия и слизи в значительном количестве, а также избыточного количества лейкоцитоидов свидетельствовало о наличии воспалительного процесса ЖВС. У небольшой части пациентов выявлены желчные соли в большом количестве: в порции А — у 3 человек (4,8%), в порциях В и С — у 6 человек в каждой (9,5%), что указывало на высокую литогенность желчи. Паразиты и простейшие не выявлены ни в одном случае.
В группе ХГВ регистрировались следующие изменения в микроскопическом составе желчи: в порции А слизь обнаружена у 38 человек (67,8%), в порции В — у 29 (51,8%), в порции С — у 39 (69,6%). Эпителий в значительном количестве выявлен в порции А — у 24 человек (42,8%), в порции В — у 12 (21,4%) и в порции С — у 5 человек (8,9%). Лейкоцитоиды более 10 в поле зрения присутствовали в порции А у 7 человек (12,5%), в порции В — у 6 человек (10,7%) и в порции С — у 5 человек (8,9%). Желчные соли в избыточном количестве выявлены в порции А у 8 человек (14,3%), в пузырной порции — у 4 (7,1%), в порции С желчные соли встречались единичные у пятой части группы (21,4%). Паразитов и простейших также, как и в группе ХГС, выявлено не было.
Выводы
Итак, анализируя данные, полученные в результате хроматического минутированного дуоденального зондирования, можно сделать вывод, что при хронических гепатитах В и С имеют место выраженные изменения функционального состояния билиарного тракта как в работе сфинктерного аппарата, так и в работе ЖП, а также дуоденальная гипертензия и повышение печеночного холереза. Выявленные изменения микроскопического состава желчи также косвенно указывают на наличие воспалительного процесса в ЖВС у пациентов с хроническими гепатитами В и С. Данные изменения билиарного статуса часто требуют уточнения и коррекции, но игнорируются лечащими врачами, снижая качество жизни пациентов.
Литература
Е. Ю. Плотникова* , 1 , доктор медицинских наук, профессор
М. С. Карягина**
М. А. Шамрай**
Е. Н. Баранова*, кандидат медицинских наук
* ФГБОУ ВО КемГМУ МЗ РФ, Кемерово
** ГАУЗ КО ОКБСМП им. Подгорбунского, Кемерово
Холестатический гепатит – это заболевание, в развитии которого ключевое значение имеет затруднение тока желчи, а также накопление составляющих ее компонентов в печени. Клинически болезнь проявляется зудом, дискомфортом в зоне правого подреберья, интенсивной желтухой, диспепсией, увеличением печени и появлением ксантелазм на коже. В диагностике основное значение имеют общеклиническое и биохимическое исследования крови с определением печеночных проб, УЗИ печени и желчного пузыря, сонография поджелудочной железы, МРТ органов брюшной полости. Терапия направлена на улучшение оттока желчи и нормализацию функции органа.
МКБ-10
Общие сведения
Холестатический гепатит представляет собой достаточно редкую патологию, в основе патогенеза которой лежит внутрипеченочный холестаз с ухудшением экскреторной функции клеток и повреждением протоков. Частота выявления заболевания не превышает 10% среди всех гепатитов с хроническим течением. Холестатический гепатит преимущественно встречается у людей пожилого возраста.
Несмотря на свою относительно низкую распространенность, заболевание плохо поддается лечению в связи с тем, что не всегда возможно четко установить его причину. Изучением этиологии и патогенеза, а также разработкой новых методов терапии холестатического гепатита занимается клиническая гастроэнтерология.

Причины
Данная патология может быть обусловлена внутрипеченочным или внепеченочным застоем желчи. В первом случае нарушение оттока желчи возможно как на уровне клеток печени, так и на уровне внутрипеченочных протоков. Причинами внутрипеченочного холестаза с последующим развитием гепатита может выступать:
- переход острого вирусного гепатита В, С или других типов в хроническую форму;
- поражение печени вирусами Эбштейна-Барра, герпеса, цитомегаловирусом, микоплазменная инфекция;
- прием различных препаратов, таких как аминазин, некоторые диуретики, антибиотики, анаболические стероиды, контрацептивы;
- воздействие токсинов, алкоголя, ядов;
- эндокринные заболевания.
Внепеченочный холестаз является следствием обструкции крупных протоков. В этом случае его возможными причинами служат:
- закупорка камнем общего желчного протока;
- хронический калькулезный холецистит;
- хронический панкреатит;
- рак головки поджелудочной железы и опухоли других органов гепатобилиарной системы.
На фоне холестаза в печени происходит деструкция гепатоцитов с последующим нарушением функции органа. В некоторых случаях установить причину развития заболевания не удается, что трактуется как идиопатический холестатический гепатит.
Симптомы холестатического гепатита
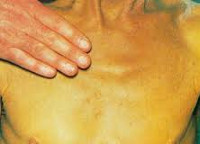
Симптоматика холестатического гепатита похожа на проявления других хронических заболеваний печени. Отличительными особенностями являются более выраженная желтуха и кожный зуд, который часто выступает первым проявлением болезни. Зуд в данном случае обусловлен попаданием в кровь желчных кислот вследствие застоя желчи в печени. Также у больных холестатической формой гепатита часто возникают ксантомы, которые имеют вид желтых пятен.
Цвет кала, как правило, становится более светлым, а моча темнеет. Пальпаторно определяется увеличение размеров и повышение плотности печени без спленомегалии. В период обострения возможно повышение температуры и неяркие симптомы интоксикации. Тяжесть клинической картины зависит от выраженности холестаза.
Диагностика
В диагностике заболевания важную роль играют лабораторные и инструментальные методы исследования. Из лабораторных методик основным для постановки диагноза холестаза считают биохимический анализ крови.
- Печеночные пробы. При биохимическом исследовании отмечается увеличение уровня билирубина за счет прямой фракции, повышение уровня трансаминаз, щелочной фосфатазы (более чем в 5 раз), гамма-глутаминтрансферазы и холестерина. Также можно определить повышенное количество в крови фосфолипидов, В-липопротеидов и желчных кислот.
- Серологическая и ПЦР-диагностика. Для подтверждения вирусной этиологии заболевания проводится исследование специфических маркеров методами ИФА и ПЦР. Характерным серологическим маркером внутрипеченочного холестаза является определение антимитохондриальных антител.
Из инструментальных методов используется эхографическая, рентгеновская, магнитно-резонансная, инвазивная диагностика:
- УЗИ печени и желчного пузыря. При ультразвуковом исследовании выявляются признаки хронического гепатита. УЗИ желчных путей, желчного пузыря и поджелудочной железы позволяет подтвердить или исключить внепеченочный холестаз.
- Рентгенография. При наличии сложностей в диагностике холестаза проводится ретроградная холангиопанкреатография, чрескожная чреспеченочная холангиография или холецистография, которые позволяют обнаружить камни в желчных путях в тех случаях, когда они не видны на УЗИ.
- МРТ. Современными неинвазивными методами выявления причин холестатического гепатита являются МР-панкреатохолангиография и МРТ гепатобилиарной зоны.
- Биопсия с гистологией. Для изучения морфологических изменений может проводиться пункционная биопсия печени, хотя она и не играет решающей роли в диагностике холестаза.
Лечение холестатического гепатита
Лечение хронического гепатита с холестатическим синдромом должно быть основано на устранении причины, которая привела к холестазу. Если причиной заболевания является воздействие токсических факторов или медикаментозных препаратов, то необходимо прекратить их поступление в организм. Всем больным рекомендуется придерживаться диеты №5, которая предусматривает исключение острой, жирной и жареной пищи. Обязательно минимизировать употребление алкоголя, который негативно влияет на клетки печени. Также рекомендовано полноценное питание с достаточным содержанием белка.
Медикаментозная терапия
На любой стадии заболевания желателен прием жирорастворимых витаминов А, Е, а также В12. Для улучшения функции гепатоцитов могут назначаться гепатопротекторы, эссенциальные фосфолипиды и липоевая кислота. При наличии внутрипеченочного холестаза с высокой активностью воспалительного процесса показано назначение небольших доз преднизолона для уменьшения выраженности патологических изменений.
Если больного беспокоит сильный зуд, необходимо применение препаратов для нейтрализации желчных кислот, таких как холестирамин или лигнин. Самым эффективным средством для лечения внутрипеченочного холестаза считается урсодезоксихолевая кислота, которая улучшает отток желчи. Препарат рекомендован всем больным с холестатическим гепатитом.
Хирургическое лечение
Если гепатит вызван внепеченочным холестазом, необходимо устранить его причину. Для этого используются различные оперативные методы:
- лапароскопическая или открытая холецистэктомия;
- резекция головки поджелудочной железы;
- экстракция конкрементов желчных протоков при РПХГ;
- эндоскопическая баллонная дилатация сфинктера Одди и др.
Прогноз и профилактика
При правильном лечении и устранении причины холестаза прогноз при холестатическом гепатите в целом благоприятный. Профилактика заболевания сводится к прекращению поступления в организм алкоголя и других гепатотоксических веществ, а также своевременному лечению патологии печени.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
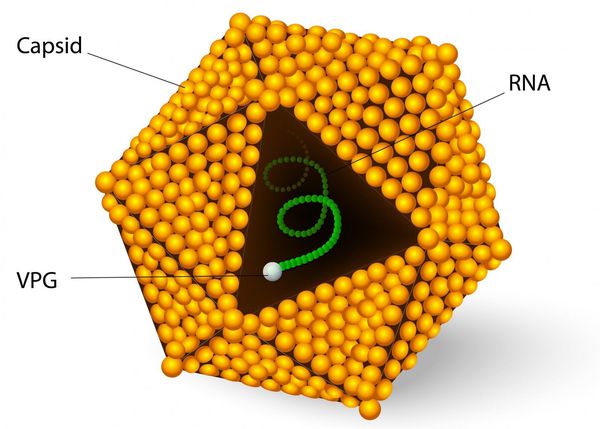
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
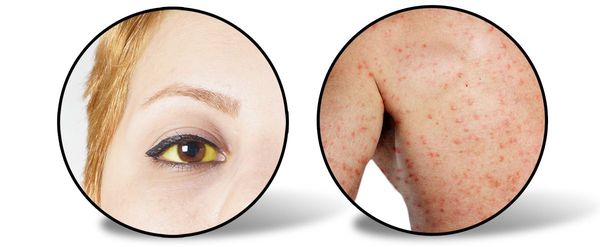
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
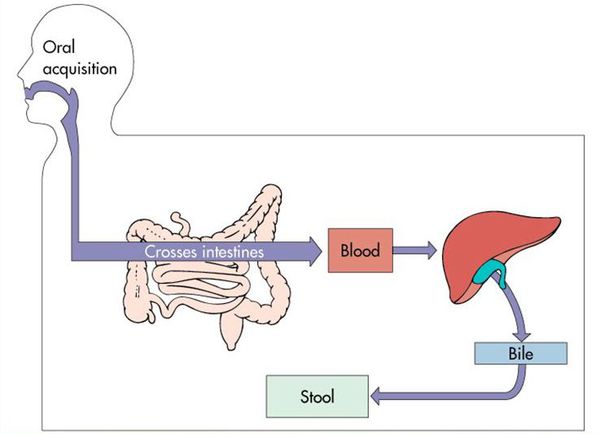
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
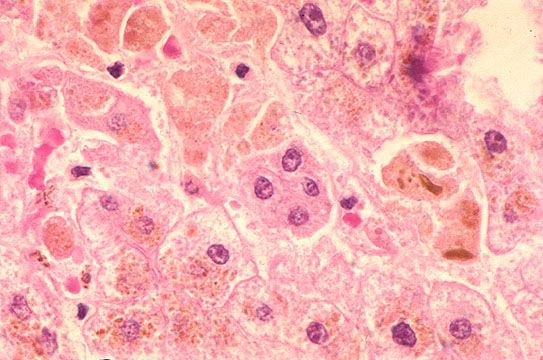
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
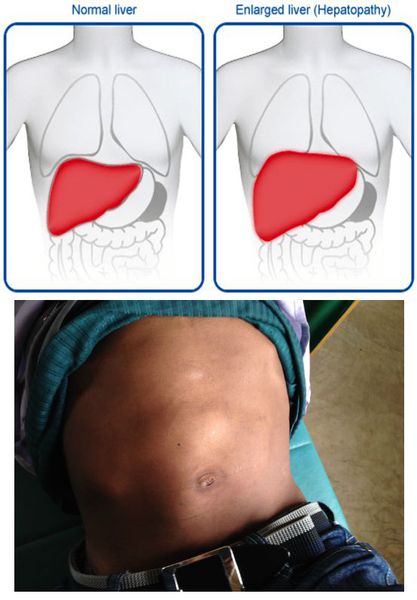
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
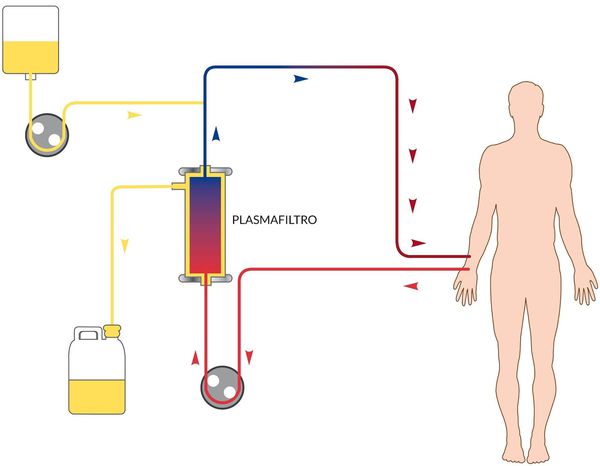
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
Читайте также:

