Для периферической крови больного чумой характерны
Обновлено: 25.04.2024
Геморрагическая лихорадка Крым-Конго (лат. febris haemorrhagica crimiana, син.: крымская геморрагическая лихорадка, Конго-Крымская геморрагическая лихорадка, среднеазиатская геморрагическая лихорадка) - острое инфекционное заболевание человека, передающееся через укусы клещей, характеризующееся лихорадкой, выраженной интоксикацией и кровоизлияниями на коже и внутренних органах. Впервые выявлено в 1944 году в Крыму. Возбудитель выявлен в 1945-м. В 1956 году в Конго было выявлено схожее заболевание. Исследования вируса установили его полную идентичность с вирусом, обнаруженным в Крыму.
Что провоцирует / Причины Крымской геморрагической лихорадки:
Возбудителем крымской геморрагической лихорадки является вирус из семейства Bunyaviridae, рода Nairovirus. Относится к арбовирусам (Arboviridae). Открыт в 1945 г. М. П. Чумаковым в Крыму, при исследовании крови больных солдат и переселенцев, заболевших при проведении работ по уборке сена. В 1956 г. в Конго из крови заболевшего мальчика был выделен аналогичный по антигенному составу вирус. Возбудитель получил название вирус Конго. Вирионы сферические, диаметр 92-96 нм, окружены липидосодержащей оболочкой. Наиболее чувствительны к вирусу культуры клеток почек эмбриона свиней, сирийских хомячков и обезьян. Плохо устойчив в окружающей среде. При кипячении вирус погибает мгновенно, при 37 `С - через 20 ч, при 45 `С - через 2 ч. В высушенном состоянии вирус остается жизнеспособным свыше 2 лет. В пораженных клетках локализуется преимущественно в цитоплазме.
Природный резервуар возбудителя - грызуны, крупный и мелкий рогатый скот, птицы, дикие виды млекопитающих, также сами клещи, способные передавать вирус потомству через яйца, и являющиеся вирусоносителями пожизненно. Источник возбудителя - больной человек или инфицированное животное. Вирус передается при укусе клеща, либо проведении медицинских процедур, связанных с инъекциями или забором крови. Основные переносчики - клещи Hyalomma marginatus, Dermacentor marginatus, Ixodes ricinus. Вспышки заболевания на территории России ежегодно бывают в Краснодарском и Ставропольском крае, Астраханской, Волгоградской и Ростовской областях, в республиках Дагестан, Калмыкия и Карачаево-Черкесии. Заболевание также встречается на юге Украины и в Крыму, Средней Азии, Китае, Болгарии, Югославии, Пакистане, Центральной, Восточной и Южной Африке (Конго, Кения, Уганда, Нигерия и др.). В 80 % случаев заболевают лица в возрасте от 20 до 60 лет.
Патогенез (что происходит?) во время Крымской геморрагической лихорадки:
В основе патогенеза геморрагической крымской лихорадки лежит повышение проницаемости сосудистой стенки. Нарастающая вирусемия обусловливает развитие тяжелого токсикоза, вплоть до инфекционно-токсического шока с диссеминированным внутрисосудистым свертыванием крови, угнетение кроветворения, что усугубляет проявления геморрагического синдрома.
Воротами инфекции является кожа в месте укуса клеща или мелкие травмы при контакте с кровью больных людей (при внутрибольничном заражении). На месте ворот инфекции выраженных изменений не наблюдается. Вирус проникает в кровь и накапливается в клетках ретикулоэндотелиальной системы. При вторичной более массивной вирусемии появляются признаки общей интоксикации, поражение эндотелия сосудов и развивается разной выраженности тромбогеморрагический синдром. Патологоанатомические изменения характеризуются множественными геморрагиями в слизистые оболочки желудка и кишечника, наличием крови в просвете, однако воспалительные изменения отсутствуют. Головной мозг и его оболочки гиперемированы, в них обнаруживаются кровоизлияния диаметром 1-1,5 см с разрушением мозгового вещества. По всему веществу мозга выявляют мелкие кровоизлияния. Кровоизлияния также наблюдаются в легких, почках и др. Многие вопросы патогенеза лихорадки Крым-Конго остаются неизученными.
При вскрытии обнаруживают множественные кровоизлияния в слизистых оболочках желудочно-кишечного тракта, кровь в его просвете, но воспалительные изменения отсутствуют. Головной мозг и его оболочки гиперемированы, в них обнаруживаются кровоизлияния диаметром 1-1,5 см с разрушением мозгового вещества. По всему веществу мозга выявляют мелкие кровоизлияния. Кровоизлияния также наблюдают в легких, почках, печени и др.
Симптомы Крымской геморрагической лихорадки:
Инкубационный период от одного до 14 дней. Чаще 3-5 дней. Продромальный период отсутствует. Болезнь развивается остро.
В начальном (предгеморрагическом) периоде отмечаются лишь признаки общей интоксикации, характерные для многих инфекционных болезней. Начальный период длится чаще 3-4 дня (от 1 до 7 дней). В этот период на фоне высокой лихорадки отмечают слабость, разбитость, головная боль, ломота во всем теле, сильная головная боль, боли в мышцах и суставах.
К более редким проявлениям начального периода относится головокружение, нарушение сознания, сильные боли в икроножных мышцах, признаки воспаления верхних дыхательных путей. Лишь у некоторых больных еще до развития геморрагического периода появляются характерные для этой болезни
симптомы - повторная рвота, не связанная с приемом пищи, боли в пояснице, боли в животе, преимущественно в эпигастральной области.
Постоянным симптомом является лихорадка, которая длится в среднем 7-8 дней, особенно типична для крымской геморрагической лихорадки температурная кривая. В частности, при появлении геморрагического синдрома отмечается снижение температуры тела до субфебрильной, через 1-2 дня температура тела вновь повышается, что обусловливает характерную для этой болезни "двугорбую" температурную кривую.
Геморрагический период соответствует периоду разгара заболевания. Выраженность тромбогеморрагического синдрома определяет тяжесть и исход болезни. У большинства больных на 2-4-й день болезни (реже на 5-7-й день) появляется геморрагическая сыпь на коже и слизистых оболочках, гематомы в местах инъекций, могут быть кровотечения (желудочные, кишечные и др.). Состояние больного резко ухудшается. Гиперемия лица сменяется бледностью, лицо становится одутловатым, появляются цианоз губ, акроцианоз. Сыпь на коже вначале петехиальная, в это время появляется энантема на слизистых оболочках ротоглотки, могут быть более крупные кровоизлияния в кожу. Возможны носовые, маточные кровотечения, кровохарканье, кровоточивость десен, языка, конъюнктив. Прогностически неблагоприятно появление массивных желудочных и кишечных кровотечений. Состояние больных становится еще более тяжелым, отмечаются нарушения сознания. Характерны боли в животе, рвота, понос; печень увеличена, болезненна при пальпации, симптом Пастернацкого положительный. Брадикардия сменяется тахикардией, АД снижено. У некоторых больных отмечается олигурия, нарастает остаточный азот. В периферической крови - лейкопения, гипохромная анемия, тромбоцитопения, СОЭ без существенных изменений. Лихорадка длится 10-12 дней. Нормализация температуры тела и прекращение кровотечений характеризует переход к периоду выздоровления. Длительно сохраняется астенизация (до 1-2 мес). У отдельных больных могут быть легкие формы болезни, протекающие без выраженного тромбогеморрагического синдрома, но они, как правило, остаются не выявленными.
Как осложнения могут наблюдаться сепсис, отек легкого, очаговая пневмония, острая почечная недостаточность, отит, тромбофлебиты. Летальность составляет от 2 до 50 %.
Диагностика Крымской геморрагической лихорадки:
Диагностика крымской геморрагической лихорадки основана на клинической картине, данных эпидемиологического анамнеза (пребывание в зоне природных очагов, нападение клещей, контакт с больными крымской геморрагической лихорадкой), результатах лабораторных исследований. В крови отмечается сниженное количество эритроцитов, лейкопения (до 1х109-2х109/л), нейтропения, тромбоцитопения. Для подтверждения диагноза используют выделение вируса из крови больного, с 6-10-го дня болезни определяется повышение титра антител в повторных пробах сыворотки крови больного в РСК, реакции диффузной преципитации а агаре, реакции пассивной гемагглютинации.
Дифференциальную диагностику проводят с другими вирусными болезнями, проявляющимися геморрагическим синдромом, особенно если больной в последние дни до развития клинических проявлений болезни находился в странах с тропическим и субтропическим климатом, с лептоспирозом, геморрагической лихорадкой с почечным синдромом, геморрагическим васкулитом, сепсисом и т.п.
Лечение Крымской геморрагической лихорадки:
Больных обязательно изолируют в инфекционном отделении стационара. Лечение симптоматическое и этиотропное. Назначают противовоспалительные препараты, мочегонные. Исключают применение препаратов, усиливающих поражение почек, например, сульфаниламиды. Также назначают противовирусные препараты (рибавирин, реаферон). В первые 3 дня вводят гетерогенный специфический лошадиный иммуноглобулин, иммунную сыворотку, плазму или специфический иммуноглобулин, полученные из сыворотки крови переболевших или привитых лиц. Специфический иммуноглобулин используется для экстренной профилактики у лиц, соприкасающихся с кровью больного.
Профилактика Крымской геморрагической лихорадки:
Для предотвращения заражения основные усилия направляют на борьбу с переносчиком заболевания. Проводят дезинсекцию помещений для содержания скота, предотвращают выпас на пастбищах, находящихся на территории природного очага. Людям в индивидуальном порядке следует использовать защитную одежду. Обрабатывать одежду, спальные мешки и палатки репеллентами. При укусах клеща в зоне обитания немедленно обратиться в медицинское учреждение за помощью. Для лиц, которые собираются въехать на территорию Юга России рекомендуется профилактическая вакцинация. В лечебных учреждениях следует учитывать высокую контагиозность вируса, а также его высокую концентрацию в крови больных. Поэтому больных необходимо помещать в отдельный бокс, а обслуживание доверять только специально обученному персоналу.
К каким докторам следует обращаться если у Вас Крымская геморрагическая лихорадка :
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Крымской геморрагической лихорадки, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Клиника и признаки чумы. Варианты и формы течения чумы
Инкубационный период 3-6 дней, может быть короче. Болезнь начинается остро, иногда внезапно, с сильного озноба, сменяющегося жаром, быстрым подъемом температуры до 40°С. Больные жалуются на сильную головную боль, головокружение, резкую слабость, тошноту, иногда появляется рвота, боль в мышцах. Состояние многих возбужденное, больные говорливы, излишне подвижны, суетливы, возможны бред и галлюцинации. Иногда, напротив, апатичны. Кожные покровы лица гиперемированы, оно одутловатое, глаза инъецированы, походка шатающаяся, речь невнятная, что бывало причиной диагностических ошибок, когда больных чумой в начальной стадии принимали за опьяневшего.
Клиническое течение чумы отличается разнообразием форм. Помимо общетоксического синдрома, вскоре на первый план выходят те или иные ее проявления. Общепринятой классификацией чумы является предложенная Г.П. Рудневым, большим знатоком этой инфекции. Он рассматривает клинику чумы с патогенетических и эпидемиологических позиций, что важно для практики ведения больных чумой и проведения противоэпидемических мероприятий.

Чумной бубон
Различают локальные формы-кожную, кожно-бубонную, бубонную и генерализованные: внутренне диссеминированные (первично-септическая) и внешне диссеминированные (первично-легочная, вторично-легочная, кишечная).
При кожной форме чумы местные изменения проходят стадии пятна, папулы, везикулы, пустулы, язвы. Язва отличается болезненностью, медленным заживлением с образованием рубца.
Характерным признаком бубонной формы является резко болезненный, увеличенный лимфоузел. Наиболее часто при чуме увеличиваются паховые, подмышечные и шейные лимфоузлы; они болезненны, локальная боль появляется в месте будущего бубона гораздо раньше, чем сам бубон. Над бубоном появляется отечность, увеличенные лимфоузлы сливаются в единый конгломерат, резко болезненный. Изменения окраски кожи, приобретающей красный лоснящийся цвет, появляются позднее самого бубона. Бубоны раньше, как правило, самостоятельно вскрывались с образованием втянутого рубца или склерозировались.
При современном лечении они могут рассасываться. В прошлом летальность даже при бубонной форме чумы достигала 40-90%. В настоящее время при антибиотикотерапии все больные выздоравливают.
Первично-септическая форма чумы встречается редко (1-3% случаев). Изменений на коже при этой форме болезни не наблюдается. Болезнь сразу приобретает картину остроразвивающегося сепсиса с быстрым нарастанием токсикоза, возможным появлением менингоэн-цефалита, развитием ТГС и скоротечным течением (1-3 дня). Заканчивается летальным исходом при явлениях ИТШ и комы.
Вторично-септическая форма чумы - следствие бубонной формы, которая быстро переходит в сепсис с прогрессирующей бактериемией и интоксикацией. Для нее характерны вторичные очаги инфекции с выраженными проявлениями геморрагической септицемии. Эта форма отличается большой тяжестью течения и частыми летальными исходами.
Клиника вторичной легочной чумы напоминает описанную картину поражения легких при первичной легочной чуме с той разницей, что ей предшествует развитие прогрессирующей бубонной формы, когда возникает гематогенная генерализация инфекции.
Патогенез чумы. Патогенез поражений возбудителем чумы. Признаки чумы. Клиника чумы. Клинические проявления чумы.
Чумная палочка внедряется в организм в месте укуса блохи. В свою очередь, инфинирование блохи происходит при её питании кровью грызунов в период бактериемии, предшествующей гибели животных. Патогенез заболевания до конца не изучен. Ни один Аг или токсин, синтезируемый Y. pestis, в отдельности не в состоянии вызвать заболевание.
Механизм развития чумы включает три стадии.
1. Лимфогенный перенос возбудителя чумы от места проникновения до лимфатических барьеров.
2. Распространение возбудителя чумы из лимфатических узлов в кровоток (бактериемия).
3. Распространение чумы до забарьерных клеточных систем (генерализованная септицемия). Проникшие бактерии чумы активно поглощаются фагоцитами, однако фагоцитарные реакции носят незавершённый характер и способствуют дальнейшему распространению возбудителя. Одновременно чумная палочка распространяется лимфогенно, вызывая множественный лимфаденит. Затем возбудитель чумы проникает в кровоток и диссеминирует в различные органы и ткани.
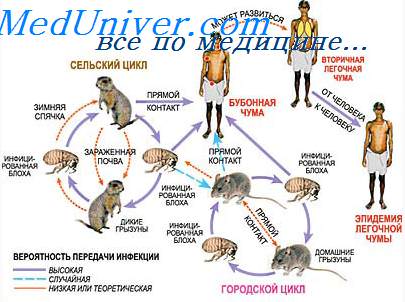
Признаки чумы. Клиника чумы. Клинические проявления чумы
Продолжительность инкубационного периода чумы составляет 3-6 сут (при эпидемиях или септических формах сокращается до 1-2 дней).
Чумная палочка не вызывает воспалительных изменений кожи и мигрирует в ближайший лимфатический узел, где развивается серозно-геморрагическое воспаление, и формируется резко болезненный бубон.
Патогенетически различают первичные (всегда связаны с местом входных ворот инфекции) и вторичные бубоны чумы (возникают лимфогенно). По клиническим проявлениям выделяют преимущественно локальные (кожную, кожно-бубонную и бубонную), генерализованные или внутренне-септические формы (первично- и вторично-септические), внешне диссеминированные формы чумы (первичную и вторичную лёгочную, кишечную).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Лейкоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Лейкозы – большая группа заболеваний кроветворной системы. Кроветворение (гемопоэз) – это многоэтапный процесс образования форменных элементов крови в специализированных органах кроветворения. К форменным элементам крови относятся лейкоциты (белые кровяные тельца), которые участвуют во врожденном и приобретенном иммунитете, эритроциты (красные кровяные тельца), которые осуществляют транспорт кислорода и углекислого газа, и тромбоциты, обеспечивающие свертываемость крови.
Главный орган, где располагаются полипотентные стволовые клетки, - костный мозг, который как раз и поражается при лейкозах.
В результате повреждения (мутации) в генетическом материале полипотентной стволовой клетки-предшественницы нарушается процесс созревания клеток. При остром лейкозе возникает большое количество незрелых (бластных) клеток, из которых образуется опухоль, разрастается в костном мозге, замещает нормальные ростки кроветворения и имеет тенденцию к метастазированию – распространению с током крови или лимфы в здоровые органы. При хронических лейкозах заболевание течет годами, происходит частичная задержка созревания клеток и опухоль образуется из созревающих и зрелых клеток.
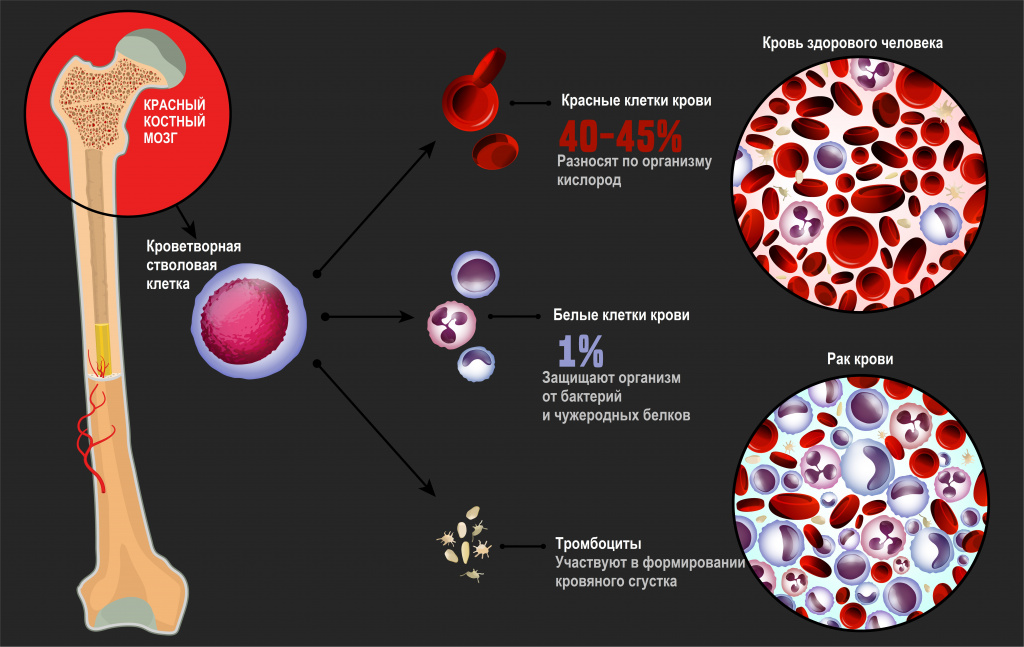
Причины возникновения лейкозов
К факторам риска развития лейкоза относятся:
- ионизирующая радиация: лучевая терапия по поводу других опухолей, облучение на рабочем месте, ультрафиолетовое излучение;
- воздействие на организм химических канцерогенных веществ;
- некоторые вирусы: HTLV (Т-лимфотропный вирус человека);
- бытовые факторы: добавки в пищевые продукты, курение, плохая экологическая обстановка;
- наследственная предрасположенность к раковым заболеваниям.
Лейкозы подразделяют на острые и хронические, а по типу поражения ростка кроветворения - на лимфоидные и миелоидные. Острый лейкоз никогда не переходит в хронический, а хронический не может стать острым (но его развитие может перейти в стадию бластного криза).
В зависимости от преобладания тех или иных опухолевых клеток выделяют бластные, цитарные и недифференцированные лейкозы.
Острый лимфобластный лейкоз (ОЛЛ) диагностируется у лиц любого возраста, начиная с младенческого и заканчивая пожилым, однако пик заболеваемости приходятся на детский возраст (60% пациентов с ОЛЛ моложе 20 лет). Острый лимфобластный лейкоз – самая распространенная опухоль кроветворной ткани у детей, которая составляет 30% всех злокачественных опухолей детского возраста. Заболеваемость ОЛЛ у пациентов пожилого возраста неуклонно возрастает: так, ежегодная частота ОЛЛ увеличивается с 0,39 случая на 100 тыс. населения в возрасте 35–39 лет, до 2,1 случая на 100 тыс. населения в возрасте ≥85 лет. Кроме того, приблизительно 30% ОЛЛ диагностируются в возрасте ≥60 лет.
Острым миелоидным лейкозом (ОМЛ) страдает в среднем 3-5 человек на 100 тыс. населения в год. Заболеваемость резко возрастает в возрасте старше 60 лет и составляет 12–13 случаев на 100 тыс. населения у лиц в возрасте старше 80 лет.
Хронический лимфобластный лейкоз (ХЛЛ) – самый частый вид лейкозов у взрослых, в то время как у детей этот вид опухоли не регистрируется. В европейских странах его частота составляет 4 случая на 100 тыс. населения в год и непосредственно связана с возрастом. У лиц старше 80 лет она составляет более 30 случаев на 100 тыс. в год.
Хронический миелолейкоз (ХМЛ) – редкое заболевание: 0,7 на 100 тыс. взрослого населения, пик заболеваемости приходится на 50-59 лет, однако до 33% больных ОМЛ - люди моложе 40 лет.
Симптомы лейкозов
Острый лейкоз в большинстве случаев дебютирует резко - внезапно повышается температура, появляются озноб, боль в горле, в суставах, отмечается резко выраженная слабость. Реже острый лейкоз может проявиться кровотечением. Иногда острый лейкоз начинается с постепенного ухудшения состояния больного, появления невыраженной боли в суставах и костях, кровоточивости. В единичных случаях возможно бессимптомное начало заболевания. У многих больных увеличиваются лимфоузлы и селезенка.
При хроническом лейкозе на начальной стадии, которая длится от года до трех лет, пациенты могут ни на что не жаловаться. Иногда беспокоят слабость, потливость, частые простудные заболевания, могут отмечаться тупые, ноющие боли в костях.
При подавлении эритроидного ростка, дающего красные кровяные тельца, возникает анемия и гемическая гипоксия (снижение количества кислорода в крови). При этом пациенты отмечают слабость, утомляемость, бледность кожных покровов.
При поражении мегакариоцитарного ростка падает количество тромбоцитов, поэтому возникает кровоточивость десен, слизистой оболочки носа, пищеварительного тракта, образуются синяки, кровоизлияния в различные органы. При прогрессировании лейкоза могут развиваться массивные кровотечения в результате ДВС синдрома (синдрома диссеминированного внутрисосудистого свертывания).
В результате недостатка лейкоцитов и снижения иммунитета развиваются инфекционные осложнения различной степени тяжести, что чаще всего проявляется лихорадкой.
Могут возникать язвенно-некротическая ангина, перитонзиллярные абсцессы, некротический гингивит, стоматит, пиодермия, параректальные абсцессы, пневмония, пиелонефрит. Существует значимый риск тяжелого течения инфекционных осложнений вплоть до развития сепсиса.
С током крови и лимфы опухолевые клетки попадают в здоровые органы, нарушают их структуру и функцию - наиболее подвержены метастатическим процессам печень, селезенка, лимфатические узлы, но метастазы могут поражать и кожу, и мозговые оболочки, и почки, и легкие.
Основные причины летальности у пациентов с лейкозом связаны с тем, что осложнения могут спровоцировать развитие сепсиса, полиорганную недостаточность, кровоизлияния в различные органы. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев.
Диагностика лейкозов
Диагностика лейкозов основывается на оценке морфологических особенностей клеток костного мозга и периферической крови. Поэтому всем пациентам с подозрением на лейкоз назначают общий анализ крови с подсчетом лейкоцитарной формулы и определением числа тромбоцитов.
Синонимы: Общий анализ крови (ОАК); Гемограмма; КАК; Развернутый анализ крови. Full blood count; FBC; Complete Blood Count (CBC); Hemogram; CBC with White Blood Cell Differential Count; Peripheral Blood Smear; Blood Film Examination; Complete blood count (CBC) with differential white blood cell coun.
Для определения объема опухолевого поражения, вероятности развития синдрома лизиса опухоли рекомендовано выполнение общетерапевтического биохимического анализа крови: АСТ, АЛТ, общий билирубин, глюкоза, мочевина, креатинин, общий белок, ЛДГ, магний, натрий, калий, кальций.
Аланинаминотрансфераза − внутриклеточный фермент, участвующий в метаболизме аминокислот. Тест используют в диагностике поражений печени, сердечной и скелетных мышц. Синонимы: Глутамат-пируват-трансаминаза; Глутамат-пируват-трансаминаза в сыворотке; СГПТ. Alanine aminotransferase; S.
Синонимы: Глутамино-щавелевоуксусная трансаминаза; Глутамат-оксалоацетат-трансаминаза сыворотки крови (СГОТ); L-аспартат 2-оксоглутарат аминотрансфераза; ГЩТ. Aspartateaminotransferase; Serum Glutamicoxaloacetic Transaminase; SGOT; GOT. Краткая характеристика определяемого вещества АсАТ .
Синонимы: Общий билирубин крови; Общий билирубин сыворотки. Totalbilirubin; TBIL. Краткая характеристика определяемого вещества Билирубин общий Билирубин – пигмент коричневато-желтого цвета, основное количество которого образуется в результате метаболизма гемовой части гемоглобина при дест.
Материал для исследования Сыворотка или плазма крови. Если нет возможности центрифугировать пробу через 30 минут после взятия для отделения сыворотки/плазмы от клеток, пробу берут в специальную пробирку, содержащую ингибитор гликолиза (флюорид натрия). Синони.
Синонимы: Диамид угольной кислоты; Карбамид; Мочевина в крови; Азот мочевины. Urea nitrogen; Urea; Blood Urea Nitrogen (BUN); Urea; Plasma Urea. Краткая характеристика аналита Мочевина Мочевина является основным азотсодержащим продуктом катаболизма белков и аминокислот в организме человека. .
Синонимы: Анализ крови на креатинин; Сывороточный креатинин; Креатинин сыворотки, оценка СКФ. Сreat; Сre; Blood Creatinine; Serum Creatinine; Serum Creat. Краткая характеристика определяемого вещества Креатинин Креатинин – низкомолекулярное азотсодержащее вещество, продукт метаболизма креа.
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок. Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР. Краткая характеристика определяемого вещества Общий белок Сыворотка крови (плазма крови, лишенная фибриногена) содержит множество белков, выполняющих разнообразны.
Синонимы: Анализ крови на ЛДГ; Лактатдегидрогеназа; L-лактат; НАД+Оксидоредуктаза; Дегидрогеназа молочной кислоты. Lactate dehydrogenase, Total; Lactic dehydrogenase; LDH; LD. Краткая характеристика определяемого вещества Лактатдегидрогеназа ЛДГ – цитоплазматический.
Синонимы: Анализ крови на магний; Общий магний; Ионы магния. Serum Magnesium Test; Magnesium test; Magnesium, blood; Serum magnesium. Краткая характеристика определяемого аналита Магний Магний, как и калий, содержится преимущественно внутри клеток. 1/3-1/2 всего магния организма .
Синонимы: Анализ крови на электролиты; Электролиты в сыворотке крови. Electrolyte Panel; Serum electrolyte test; Sodium, Potassium, Chloride; Na/K/Cl. Краткая характеристика определяемых веществ (Калий, Натрий, Хлор) Калий (К+) Основной внутриклеточный катион. Кал.
Общий кальций – основной компонент костной ткани и важнейший биогенный элемент, обладающий важными структурными, метаболическими и регуляторными функциями в организме. Синонимы: Анализ крови на общий кальций; Общий кальций в сыворотке. Total blood calcium; Total calcium; Bl.
Для определения вероятности развития тяжелых коагуляционных нарушений (как геморрагических, так и тромботических) рекомендовано исследование свертывающей системы крови.
С целью исключения поражения почек выполняют общий анализ мочи.
Диагностику хронического лейкоза проводят с помощью иммунофенотипического исследования лимфоцитов крови (ИФТ) методом проточной цитометрии.
Рекомендовано проведение стернальной пункции (пункции грудины) для получения цитологического препарата костного мозга и цитологическое и цитохимическое исследование мазка с целью уточнения диагноза и определения прогноза.
В ряде случаев показана биопсия опухолевого образования или лимфатического узла (или другого метастатического очага) и патологоанатомическое исследование полученного биопсийного материала.
Кроме того, врач может рекомендовать проведение иммунофенотипирования гемопоэтических клеток-предшественниц в костном мозге, цитогенетическое исследование аспирата костного мозга, молекулярно-генетические исследования мутаций в генах и др.
Из инструментальных методов диагностики проводятся:
-
эхокардиография для оценки функционального состояния сердечной мышцы;
Исследование, позволяющее оценить функциональные и органические изменения сердца, его сократимость, а также состояние клапанного аппарата.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Лечение лейкозов
Лечение лейкозов проводится в стационаре. Медикаментозное воздействие на опухоль специальными препаратами, губительно действующими на быстро делящиеся клетки, называется химиотерапией. При лечении острых лейкозов химиотерапию проводят в несколько этапов: индукция ремиссии, консолидация (закрепление) ремиссии, поддерживающая терапия и профилактика нейролейкемии (метастазирования опухолевых лейкозных клеток в головной и спинной мозг).
Период индукции ремиссии - это начальный этап, цель которого максимально уменьшить опухолевую массу и достичь ремиссии. Обычно для этого требуется 1-2 курса химиотерапии. Далее идет консолидация достигнутого эффекта - наиболее агрессивный и высокодозный этап лечения, задачей которого является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток. Этот этап также занимает 1-2 курса. За ним следует противорецидивное или поддерживающее лечение. При некоторых вариантах острых лейкозов требуется профилактика или, при необходимости, лечение нейролейкемии.
Для разных видов лейкозов у разных возрастных групп профессиональными сообществами разработаны схемы химиотерапии.
При лечении ХМЛ основными препаратами выбора являются ингибиторы тирозинкиназы, применяемые в непрерывном режиме – ежедневно, длительно, постоянно. Перерывы в приеме могут способствовать снижению эффективности терапии и прогрессированию заболевания. В случае неэффективности терапии может быть проведена трансплантацию гемопоэтических стволовых клеток или костного мозга.
В терапии ХЛЛ цели и схемы терапии химиотерапии определены возрастом пациента, числом и тяжестью сопутствующих заболеваний. Разработаны протоколы лечения для разных пациентов, в том числе схемы моно- и полихимиотерапии. Для профилактики инфекционных осложнений применяют внутривенное введение иммуноглобулина, рекомендована вакцинация от гриппа и пневмококковой инфекции.
Помимо химиотерапии пациенту может потребоваться трансфузионная терапия: переливание эритроцитарной массы, тромбоцитарной массы, изотонических растворов.
При присоединении инфекций показана антибиотикотерапия. На фоне лечения могут возникать тромботические осложнения, что требует антикоагулянтной терапии. Пациентам высокого риска в связи с вероятностью рецидива лейкоза применяют трансплантацию гемопоэтических стволовых клеток.
Профилактика лейкозов
Так как причины возникновения лейкозов не установлены, методов специфической профилактики до сих пор не существует.
Однако доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет.
Ряд исследователей предполагают, что около 20% случаев ОМЛ являются следствием курения.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Читайте также:

