Эбола это искусственный вирус
Обновлено: 19.04.2024
Для цитирования: Щелканов М.Ю., Zoumanigui N., Boiro M.Ye., Малеев В.В. Пять мифов о лихорадке Эбола: где кончается вымысел? РМЖ. Медицинское обозрение. 2015;23(2):58.
Эпидемия лихорадки Эбола, начавшаяся вконце 2013г., развивавшаяся без должной идентификации первые месяцы 2014г. ипревратившаяся всерьезную региональную проблему, прочно приковывает ксебе внимание специалистов, атакже политиков исредств массовой информации. Эта эпидемия еще раз показала, что встремительно глобализирующемся мире любое инфекционное заболевание, даже самое экзотическое, является .
Эпидемия лихорадки Эбола, начавшаяся в конце 2013 г., развивавшаяся без должной идентификации первые месяцы 2014 г. и превратившаяся в серьезную региональную проблему, прочно приковывает к себе внимание специалистов, а также политиков и средств массовой информации. Эта эпидемия еще раз показала, что в стремительно глобализирующемся мире любое инфекционное заболевание, даже самое экзотическое, является социально-значимым.
В данной работе в процессе разбора пяти наиболее часто встречающихся мифов о лихорадке Эбола излагаются научные данные о таксономическом статусе возбудителя, истории его открытия, этимологии терминов, причинах возникновения и ранних событиях современной эпидемии в Западной Африке, научно-практической помощи Гвинейской Республике со стороны Российской Федерации.
Миф 2. Современная эпидемия лихорадки Эбола в Западной Африке началась весной 2014 г.
Действительно, 23.03.2014 г. Африканское региональное бюро ВОЗ объявило об эпидемии лихорадки Эбола в Гвинейской Республике (в пределах лесистой части Северо-Гвинейской возвышенности); 29.03.2014 г. последовало подтверждение первого случая лихорадки Эбола в Республике Либерия, 25.05.2014 г. – в Республике Сьерра-Леоне. Однако это – официальные датировки. Результаты ретроспективного эпидемиологического расследования показывают, что современная эпидемия лихорадки Эбола в Западной Африке началась еще в декабре 2013 г. [1, 2].
Первым пациентом (П1) стал 2-летний Эмиль Уамунó (Emile Ouamouno), который остро заболел 24.12.2013 г. с симптомами лихорадки, рвоты, кровавого стула и умер 28.12.2013 г. Он жил со своей семьей на окраине небольшой (31 хижина) деревни Мельяндỳ (Meliando) (8° 37′ 21.36″ с.ш., 10° 3′ 51.12″ з.д.) в префектуре Гекедỳ (Gueckedou) провинции Нзерекорé (Nzerekore) (рис. 3).
В научной литературе приводятся различные даты смерти Эмиля Уамунó (06.12.2013 г. [1] vs. 28.12.2013 г. [2]) и первых 4-х пациентов (П1-4). Несмотря на то, что публикация S. Baize и соавт. [1] появилась раньше и именно ее данные широко цитируются средствами массовой информации, сведения A. Marí Saéz и соавт. [2] вызывают большее доверие, т. к. его авторы работали непосредственно в Мельянду, беседовали с очевидцами и проводили сверку с медицинскими записями в местном медицинском пункте. Кроме того, данные A. Marí Saéz и соавт. [2] по П1-4 лучше согласуются по срокам с последующими эпидемическими событиями.
На первом этапе (до начала марта 2014 г.) эпидемия развивалась по классическому сельскому типу (см. подробности у М.Ю. Щелканова и соавт. [3]): источником инфекции стали, по-видимому, выделения крыланов (Chiroptera, Megachiroptera), которые являются природным резервуаром эболавирусов [26–28], будучи способны переносить инфекцию бессимптомно. В лесном массиве, окружающем Мельяндỳ, были обнаружены несколько видов крыланов и летучих мышей. Возможно, источником инфекции стали заразившиеся от крыланов больные и ослабленные летучие мыши (Chiroptera, Microchiroptera), жившие в дуплистом дереве близ деревни, вокруг которого любили играть дети (см. Приложения в [2]).
Таким образом, к концу февраля 2014 г. вирус проник в крупные населенные пункты, и следующая стадия эпидемии начала развиваться по городскому типу [3], когда высокая плотность населения способствует быстрому распространению вируса контактным путем. В Западной Африке контактный путь распространения инфекционных заболеваний во многом связан с наличием специфических погребальных обрядов и невероятной скученностью в транспортных средствах. К 26.03.2014 г., когда ВОЗ объявила об идентификации этиологического агента эпидемии (EBOVZ), эпидемия городского типа уже вырвалась на вольный простор. В тот момент ее еще можно было остановить с помощью масштабных и слаженных противоэпидемических мероприятий, но осуществить их в сложнейших социально-экономических условиях современной Западной Африки оказалось невозможно. 27.03.2014 г. эпидемия достигла столицы Гвинейской Республики г. Конакри, и число заболевших стало нарастать лавинообразно.
Миф 3. Современная эпидемия лихорадки Эбола в Западной Африке – это результат применения биологического оружия: целенаправленно спланированного либо непреднамеренного (вышедших из-под контроля полевых испытаний)
Таким образом, эпидемия лихорадки Эбола в Западной Африке вспыхнула в декабре 2013 г. отнюдь не в результате преднамеренного или непреднамеренного использования биологического оружия, а в результате повышения активности циркуляции EBOVZ в его природных очагах на территории Северо-Гвинейской возвышенности. С учетом данных 2014 г. (табл. 1, рис. 1), необходимо внести изменения в классификацию природных очагов филовирусов: Африканская природно-очаговая область теперь подразделяется на две природно-очаговые провинции – Центральноафриканскую (ядро очага – Североконголезский природно-очаговый округ) и Западно-африканскую (ядро очага – Северогвинейский3 природно-очаговый округ) (рис. 1). Природным резервуаром являются крыланы (Chiroptera, Megachiroptera). Сравнительная характеристика циркуляции филовирусов в выделенных природно-очаговых провинциях должна стать предметом детальных исследований уже в ближайшем будущем. Молекулярно-генетический анализ полноразмерных генетических последовательностей штаммов EBOVZ, изолированных в 2014 г. в Западной Африке, не выявил у них принципиальных отличий от ранее известных вариантов этого вируса. Генетическая дистанция от штаммов, изолированных в 2008 г. в ДРК, составляет около 3% [1], что достаточно для выделения нового генотипа EBOVZ и полностью согласуется с концепцией наличия в Африке двух природно-очаговых провинций.
Миф 4. Население Западной Африки охвачено паникой, в т. ч. будучи напуганным искусственно завышенными показателями летальности
Население Западной Африки, к огромному сожалению, давно привыкло жить (и при этом – не паниковать) в условиях хронического эпидемического неблагополучия. Достаточно сказать, что детская смертность в странах Западной Африки превышает 60, в иные годы поднимаясь выше 100 (например, в 2008 г. в Республике Сьерра-Леоне и Республике Либерия). Средняя продолжительность жизни – 56 лет в Гвинейской Республике, 54 – в Республике Либерия, 45 – в Республике Сьерра-Леоне. В регионе отсутствуют или недостаточно масштабированы системы мониторинга социально-значимых инфекций: гриппа, вирусных гепатитов, заболеваний, передающихся половым путем. Территория Западной Африки включает сложнейшие в структурно-функциональном отношении сочетанные природные очаги инфекционных заболеваний, среди которых – помимо EBOVZ и TAFV (Filoviridae, Ebolavirus) (табл. 1, рис. 1) – следует отметить особо опасные вирусы Ласса (Arenaviridae, Arenavirus); Дугбе и Крымской-Конго геморрагической лихорадки (Bunyaviridae, Nairovirus); Бвамба, Буньямвера, Мпоко, Симбу, Татагине, Тягиня, Шамонда и Шуни (Bunyaviridae, Orthobunyavirus); Бханджа и лихорадки долины Рифт (Bunyaviridae, Phlebovirus); Вессельсброн, денге, желтой лихорадки, Западного Нила и Сабойя (Flaviviridae, Flavivirus); Кваранфил и озера Чад (Orthomyxoviridae, Quaranjavirus); Тогото (Orthomyxoviridae, Thogotovirus); Абадина, Киндия и синего языка овец (Reoviridae, Orbivirus); Синдбис и Чикунгунья (Togaviridae, Alphavirus); бактерии: Yersinia pestis, Salmonella enterica, S. bongori, S. subterranea (Enterobacteriaceae); Rickettsia spр., Coxiella spр., Rochalimaea spр. (Rickettsiae); Borrelia duttonii (Spirochaetaceae); Vibrio cholerae (Vibrionaceae); протозои: Entamoeba histolytica (Entamoebidae); Listeria monocytogenes (Listeriaceae); Plasmodium falciparum, P. malariae, P. ovale и P. vivax (Plasmodiidae); Leishmania donovani (Trypanosomatidae).
Однако перечень природно-очаговых патогенных микроорганизмов, распространенных в Западной Африке, далеко не исчерпывается приведенным перечнем. Ситуация серьезно осложняется отсутствием современных научных данных о таксономическом статусе, экологии и патогенности подавляющего большинства микроорганизмов, уже известных для данного региона, и которые могут быть открыты при развертывании соответствующих мониторинговых программ.
Основной причиной недостаточной развитости системы здравоохранения в Западной Африке является комплекс социально-экономических проблем, уходящих своими корнями в колониальное прошлое этого региона [22, 40]. Непродолжительный по историческим меркам период строительства социализма в Гвинейской Республике позволил при помощи СССР4 заложить основы современного здравоохранения и сформировать местные медицинские кадры. Распад СССР в начале 1990-х гг. существенно сократил масштабы этого сотрудничества.
В августе 2014 г. активные рабочие контакты между российскими и гвинейскими медицинскими специалистами были возобновлены: в Гвинейскую Республику прибыла экспертно-рекогносцировочная группа Роспотребнадзора и Минздрава России (рис. 4) [3]. В задачи группы входили обеспечение биологической безопасности посольства и российских граждан; научно-методическая поддержка местных специалистов; сбор аналитической информации непосредственно в очаге эпидемии; ознакомление с опытом гвинейских коллег по диагностике и лечению лихорадки Эбола, установление контактов с представителями ВОЗ и других международных организаций, осуществляющих деятельность по предотвращению распространения эпидемии, возобновление контактов со специалистами Гвинейского института им. Л. Пастера (г. Киндия), проведение переговоров с Министерством здравоохранения Гвинейской Республики с целью определения масштабов помощи со стороны Российской Федерации, а также получения приглашения на работу российских специализированных противоэпидемических бригад (СПЭБов).
Внедрение методов молекулярной диагностики лихорадки Эбола привело к закономерному снижению статистики летальности. И причина кроется совсем не в том, что прежде летальность сознательно завышалась. Благодаря молекулярной диагностике статистика стала учитывать все, а не только наиболее тяжелые случаи заболевания, что и привело к снижению летальности: 30.06.2014 г. – 73,4% (303/413); 30.07.2014 г. – 57,4% (826/1440); 26.08.2014 г. – 50,6% (1552/3069); 29.10.2014 г. – 35,9% (4910/13676); 26.11.2014 г. – 35,7% (5674/15901); 13.01.2015 г. – 39,5% (8386/21206). Снижение летальности после внедрения методов молекулярной диагностики было описано и при других вирусных инфекциях [11–14].
По поручению Президента Российской Федерации от 14.12.2014 г. российские военно-медицинские специалисты доставили в Гвинейскую Республику мобильный госпиталь, способный одновременно разместить на лечение 200 пациентов, в составе которого уже к 18.12.2014 г. были развернуты в г. Киндия (рис. 3), протестированы и штатно функционировали приемно-диагностическое отделение, диагностические лаборатории, три инфекционных отделения, отделение интенсивной терапии, стерилизационная, а также системы контроля за соблюдением санитарного режима. Российские медики организовали для гвинейских коллег курсы повышения квалификации по инфекционным болезням, организовали лечебный процесс, медицинскую логистику, разработали схемы действий при чрезвычайных ситуациях, санитарно-эпидемиологический мониторинг. 17.01.2014 г. на территории Гвинейского института им. Л. Пастера (г. Киндия) был открыт Российско-гвинейский центр микробиологических исследований, имеющий собственное клиническое отделение: инфекционный госпиталь, провизорный госпиталь, отделение переливания крови. В г. Киндия была перебазирована часть группировки мобильных лабораторий Роспотребнадзора. На открытии Центра присутствовал Президент Гвинейской Республики Альфа Конде (рис. 6). Предпринятые меры позволят не только улучшить ситуацию с диагностикой и лечением лихорадки Эбола, но и проводить плановый комплексный мониторинг природных очагов инфекционных заболеваний на территории Западной Африки.
Миф 5. Мир стоит перед лицом ужасной пандемии лихорадки Эбола, представляющей угрозу существованию человечества
Беспрецедентные масштабы современной эпидемии лихорадки Эбола в Западной Африке, впервые вышедшей на региональный уровень, могут быть объяснены 4 основными причинами: 1. наличие природных очагов EBOVZ на территории Западной Африки; 2. отсутствие научной информации о функционировании природных очагов EBOVZ в данном регионе (затруднило своевременную идентификацию возбудителя заболевания); 3. наличие своеобразных местных обрядов (в частности – обряда погребения, включающего многолюдные похороны и массовые омовения покойного), которые существенно способствуют распространению инфекционных агентов – включая EBOVZ – контактным путем; 4. сложнейшая социально-экономическая обстановка.
В Европе, Северной Евразии (включая Российскую Федерацию), Южной и Северной Америке отсутствуют природные очаги эболавируса Заир, поскольку ареал природного резервуара – крыланов (Chiroptera, Megachiroptera) – ограничивается субтропическими зонами Восточного полушария (рис. 1; [3]).
С высокой вероятностью, эпидемия лихорадки Эбола не выйдет за границы Западной Африки и закончится, хотя бы уже вследствие формирования достаточной иммунной прослойки среди местного населения этого региона. В остальных странах возможны завозные спорадические случаи заболевания, вероятность разрастания которых до эпидемических вспышек и эпидемий городского типа [3] определяется уровнем развития системы биологической безопасности конкретной страны.
Следует подчеркнуть, что проблема интродукции патогенных микроорганизмов появилась отнюдь не в связи с лихорадкой Эбола – острота этой проблемы неуклонно возрастает, начиная примерно с середины прошлого века, в связи с интенсификацией пассажирских потоков во всем мире. При этом, медицинский контроль в транспортных пунктах пропуска является необходимой, но недостаточной мерой, поскольку инфекционный больной в инкубационном периоде способен преодолеть самый строгий контроль и заболевает уже на новой территории. В частности, в Российской Федерации ежегодно регистрируют несколько сотен случаев завозных экзотических инфекционных заболеваний [41–43]. Все эти случаи быстро выявляются, грамотно идентифицируются, в результате проводимых оперативных мероприятий купируются возможные пути передачи возбудителя, и эпидемических вспышек удается избежать. Эффективность этих мероприятий и высокая степень настороженности системы биологической безопасности развитых стран мира (в т. ч. Российской Федерации) являются надежным барьером на пути распространения лихорадки Эбола.
Несколько дней назад, житель Ганы по имени Нана Кваме сделал заявление, которое потрясло интернет-сообщество. Приведенная ниже информация должна быть распространена. Нам нужно понять, что такое Эбола. Мир должен увидеть настоящие цели стоящие за истерией, раздуваемой вокруг Эболы. Вот как Нана Кваме описал происходящее в его родной стране:
Причины
Причина 1:
Причина 2:
Причина 3:
Помимо нигерийской нефти и алмазного экспорта из Сьерра Леоне, войска необходимы для принуждения к вакцинации (прививании вируса Эбола) той части населения Африки, которая достаточно осведомлена, чтобы стараться избегать вакцинации.
Причина 4:
Доктор Сирил Бродерик (Cyril Broderick) написал, что «определенные районы в Африке, в том числе и в западной Африке, уже много лет являются полигонами для испытаний, связанных с новыми болезнями, особенно с Эболой.
Я не являюсь экспертом по Эболе, но история имеет привычку повторяться. Вот мое предсказание. В США произойдет либо террористический акт, либо некая техногенная катастрофа, которая приведет к человеческим жертвам и дальнейшему усилению режима контроля над населением. Результатом катастрофы станет либо эпидемия (не обязательно Эболы), либо утечка био-химического оружия, которая также вызовет эпидемию. Возможно, вся ситуация будет просто инсценирована с помощью СМИ. В любом случае, все это позволит властям начать вакцинацию напуганного населения. Возможно в принудительном порядке. не проходите вакцинацию. Именно так будет распространяться Эбола и, в дальнейшем, распространение этого вируса по всему миру станет поводом для введения войск и создания баз в различных странах. Все это часть западной глобалистской политики.
На видео видно, как человек без спецкостюма и без маски спокойно подходит к носилкам, на которых лежит больной Эболой человек.
Заявители патента включают правительство США (в лице министерства здравоохранения и социальных служб США) и центр по контролю и профилактике заболеваний.

От лихорадки Эбола теперь существует четыре прививки: две американские и две российские

Сергей Нетёсов, доктор биологических наук, профессор, заведующий лабораторией биотехнологии и вирусологии факультета естественных наук Новосибирского государственного университета, член-корреспондент РАН
Африканский вирус оказался более актуальным, чем российские
Почему он Эбола
Возбудитель лихорадки — вирус Эбола — впервые был обнаружен в 1976 году во время вспышки болезни в районе реки Эбола, протекающей между тогдашним Заиром (ныне Демократическая Республика Конго) и Суданом.
Если рассмотреть хронику создания вакцины против вируса Эбола и современное состояние дел в этой области в мире и в России, то становится понятным, как это поможет всем нам.
Начало
Вирус Эбола был впервые идентифицирован в 1976 году во время крупной вспышки вызванного им заболевания в Судане и тогдашнем Заире (теперь Демократическая Республика Конго; ДРК). Поскольку такие вспышки позднее случались не каждый год и их охват в несколько последующих лет был намного меньше, то ученые ограничились в те времена лишь разработкой иммуноферментных диагностикумов на ее маркеры.
Правда, основные фундаментальные исследования были проведены, в том числе секвенирование генома этого возбудителя, причем российские ученые здесь были одними из первых, включая вашего покорного слугу.
В 1990-е, а особенно в 2000-е годы масштаб и число вспышек заметно увеличились, и некоторые лаборатории в США и Канаде начали разработки и вакцинных препаратов, и средств лечения, а также диагностикумов нового типа на основе полимеразной цепной реакции. Однако для проведения полного цикла доклинических испытаний вакцинных препаратов необходимы весьма значительные средства, а с учетом особой опасности этой инфекции значительную часть таких работ необходимо проводить в лабораториях высшего, четвертого уровня биобезопасности. Ввиду этих причин полного цикла доклинических исследований перспективных, кандидатных, как говорят специалисты, вакцин против Эбола-вирусной инфекции до 2014 года так и не было завершено ни в одной из лабораторий мира.
Природный резервуар вируса
По самым последним данным, природным резервуаром вируса Эбола вернее всего являются фруктоядные летучие мыши. Три вида таких мышей (Hypsignathus monstrosus, Epomops franqueti и Myonycteris torquata) могут быть носителями вируса без признаков заболевания. Из 24 видов растений и 19 видов позвоночных, экспериментально зараженных вирусом Эбола, удалось заразить только летучих мышей. Причем они не заболели, а просто несли в себе вирус в течение долгого времени. В обследовании в 2002–2003 годах 1030 животных, включая 679 летучих мышей из Габона и Республики Конго, только 13 фруктоядных мышей несли этот вирус. Кроме того, фрагменты вируса Эбола выделяли из тканей некоторых умерших западноафриканских равнинных горилл и центральноафриканских шимпанзе, которые иногда питаются фруктоядными летучими мышами. Что еще более важно, фрагменты РНК вируса Эбола были выявлены у клинически здоровых летучих мышей разных видов. Это означало, что летучие мыши могут быть носителями вируса без признаков заболевания, то есть хроническими носителями. А это и есть главное условие поддержания циркуляции вируса Эбола в природе.
Ускорение
Неожиданная по размаху, месту возникновения и продолжительности вспышка этого заболевания 2014 года в Гвинее, Сьерра-Леоне и Либерии сдвинула ситуацию с места. И уже в конце 2015 года несколько лабораторий и научно-исследовательских институтов в США, Канаде и некоторых других странах объявили о завершении доклинических испытаний нескольких кандидатных, вакцинных препаратов.
О создании прототипной вакцины объявили и у нас в России. Первыми были публикации группы ученых из НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи Министерства здравоохранения России о разработке живой вакцины на основе рекомбинантного аденовируса. Однако к этому времени и сама вспышка закончилась, так что испытывать эти вакцины в полевых условиях реальной эпидемии стало негде.
В том же 2018 году, и опять неожиданно, началась вспышка Эбола-вирусной инфекции в ДРК. Как оказалось, один из вакцинных препаратов, разработанный на основе рекомбинантного живого вируса везикулярного стоматита, прошел к этому времени ограниченные клинические испытания в США.
Как передается вирус Эбола
От человека к человеку вирус передается при попадании вируссодержащих жидкостей от больных людей или инфицированных животных на слизистые оболочки или на микротравмы на коже. У больных и умерших концентрация этого вируса в крови и на слизистых оболочках необычайно велика и достигает 10 млн вирусных частиц на 1 мл. Поэтому близкое общение с больным с большой вероятностью приводит к заражению. Наконец, уже выздоровевший человек может нести в себе вирус (в семени мужчин, в грудном молоке женщин) до одного года после выздоровления.

Обзор
Фотография жизнерадостного молотоголового крылана, потенциального переносчика вируса Эбола.
Автор
Редакторы

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Рисунок 1. Информационный плакат о вирусе Эбола.
Геморрагическая лихорадка Эбола — острая вирусная болезнь с высокой заразностью, которая характеризуется развитием тромбогеморрагического синдрома. Он выражается в снижении числа лейкоцитов (белых кровяных тел, частично отвечающих за иммунитет) у больного и, как следствие, — в уменьшении сопротивляемости организма инфекции; а затем и в снижении количества тромбоцитов, что приводит к нарушению свертываемости крови и, нередко, нарушению целостности сосудистой стенки и кровоизлияниям.
Вирус Эболы (рис. 1, 2) вызывает тяжелое заболевание с острым течением, которое обладает близкой к абсолютной летальностью в отсутствие лечения и средней — порядка 60% от всех заболевших — для пациентов, получающих симптоматическое лечение [1]. Распространяясь через физиологические жидкости больных или умерших людей и животных, а также через загрязненные биологическим материалом предметы, болезнь быстро поражает членов одной семьи или деревни после проявления симптомов инфекции. Низкая плотность населения в Африке — один из немногих естественных барьеров для передачи болезни, но представьте только потенциальную активность этого потрясающего патогена в городских условиях развитых стран! Вирус также разносится естественными носителями, обитателями влажных тропических лесов — крыланами (рис. 3), очаровательными летучими мышами, употребляемыми местными жителями в пищу.
Рисунок 2. Схема структуры вируса Эбола с изображением вирусной РНК и относительным расположением участков, кодирующих его элементы.
Рисунок 3. Крылан молотоголовый, естественный носитель вируса Эболы.
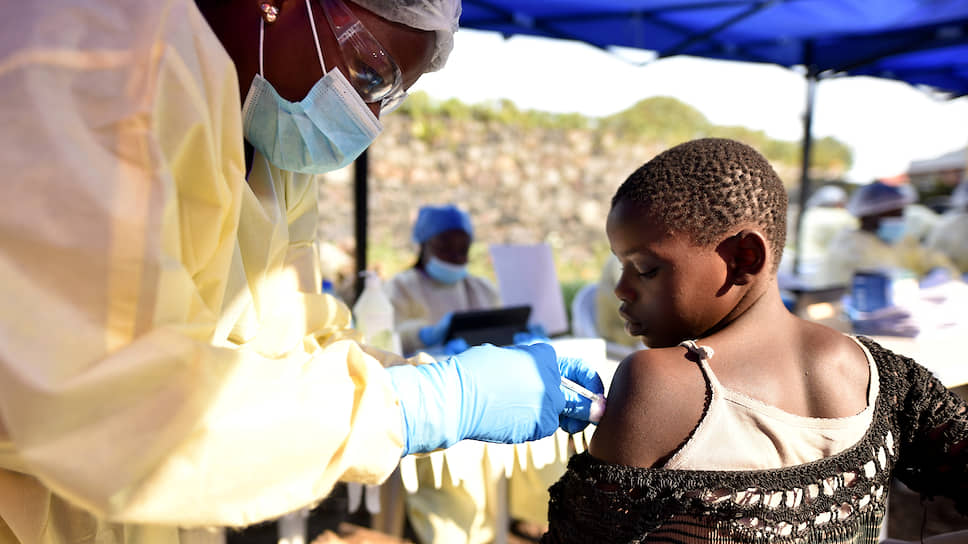
На первом этапе, наступающем через 6–10 дней после контакта с зараженным материалом [2], заболевшие (рис. 4) испытывают симптомы, схожие с другими распространенными в тропических странах заболеваниями, такими как малярия, тифоидная лихорадка (брюшной тиф) и менингит. А именно, у больного наблюдаются повышенная утомляемость, слабость, лихорадка с повышением температуры свыше 38 о С и боли в теле. Спустя еще некоторое время проявляются симптомы обыкновенных кишечных инфекций — тошнота, боли в животе, рвота и диарея.
Рисунок 4. Две медсестры около кровати с больным лихорадкой Эбола. Позднее пациент скончался.
Настоящий ад для заболевших начинается примерно через неделю после проявления первых характерных симптомов. До этого момента, без возможности сделать ПЦР-тест, геморрагическую лихорадку Эбола невозможно обнаружить.
Q-ПЦР (или количественная полимеразная цепная реакция ) — метод молекулярной биологии, позволяющий создать копии определенного фрагмента ДНК из исходного образца, повысив его содержание в пробе на несколько порядков. Он применяется с целью увеличения количества РНК вирусных частиц в пробе и их последующего детектирования посредством взаимодействия с флуоресцентным красителем и регистрации излучения оптическими системами.
Через неделю после проявления первых симптомов лихорадки у больных начинается стадия обильных кровотечений. Вирус Эбола вызывает некоторое снижение свертываемости крови, что в условиях жизни африканских народов в естественном ареале распространения инфекции может провоцировать сильные кровотечения в желудочно-кишечном тракте из-за особенностей слизистых оболочек тонкого и толстого кишечника в десяти процентах случаев, а обильное кровотечение из прочих слизистых — практически в каждом втором. Это приводит к наличию крови в рвоте, кашле и стуле, что многократно повышает заразность заболевания [4].
Как же трактовать частоту появления кровоизлияний? С точки зрения чистой статистики, одна десятая численности — небольшое количество, однако это потенциальные три сотни человек при многотысячной вспышке, подобной той, что была последней в ДРК на текущий момент, которые могут истекать кровью на улице, загрязнять предметы зараженной кровью и разносить инфекцию по округе. Слоняясь в умирающих деревнях, они могут неумышленно распространить вирус на людей, остановившихся с целью помочь и облегчить страдания кажущегося раненным измученного африканца. Инкубационный период болезни вполне может позволить таким туристам покинуть очаг эпидемии.
Именно этот обзор привлек внимание и вызвал оправданное беспокойство нескольких групп эпидемиологов, в том числе американских, к опасности заболевания, возбудитель которого был быстро отнесен к первой группе патогенности.
Рисунок 5. Карта распространения вируса Эбола во время вспышки в 2013–2016 годах.
Текущая обстановка в регионах распространения заболевания остается напряженной: вспышка 2018–2019 годов окончилась при поддержке экспериментальных вакцин как на основе модифицированной ДНК, содержащей гены нуклеопротеинов и гликопротеинов вируса Эболы, так и посредством наиболее свежих на тот момент разработок — векторных вакцин на основе рекомбинантных вирусов .
Параллельно с этим больным оказывалась симптоматическая медицинская помощь в полевых госпиталях и предоставление гуманитарной помощи для находящихся на карантине пострадавших стран. К несчастью, испытания и лечение больных сопровождались вооруженными нападениями на госпитали из-за продолжающейся гражданской войны в ДРК, что неоднократно подрывало миссию медиков и поиск эффективного лечения заболевания и тестирования противовирусных препаратов [8].
Что же такое Инмазеб?
Данный трехкомпонентный препарат состоит из натуральных человеческих специфических антител, которые взаимодействует с гликопротеинами вируса Эбола и блокируют его внедрение в клетки человека, что способствует снижению скорости репликации вирусных частиц и уменьшает тяжесть течения заболевания [10]. В сочетании с имеющимися протоколами лечения болезни, вызываемой вирусом Эбола, это значительно увеличивает эффективность терапии.
Антитела — это крупные глобулярные белки плазмы крови, выделяемые плазматическими клетками иммунной системы и предназначенные для нейтрализации клеток патогенов (бактерий, грибов, многоклеточных паразитов) и вирусов, а также белковых ядов и некоторых других чужеродных веществ. Каждое антитело распознает уникальный элемент патогена, отсутствующий в самом организме, — антиген, а в пределах данного антигена — определенный его участок. Связываясь с антигенами на поверхности патогенов, антитела могут либо непосредственно нейтрализовать их, либо привлекать другие компоненты иммунной системы, чтобы уничтожить чужеродные клетки или вирусные частицы.
Для нейтрализации перечисленных выше патогенов организмом вырабатывается смесь антител, направленных на специфическое связывание с инородными веществами, однако в ряде случаев, а именно — при создании медицинских препаратов узкого спектра действия требуется выделить один компонент из настоящего сонма различных белков, продуцируемых клетками иммунной системы с весьма ограниченным сроком жизни.
Рисунок 6. Строение и типы антител с указанием структурно значимых участков.
О потенциально успешном применении моноклональных антител сообщалось во время ранних клинических препарата ZMapp для лечения лихорадки Эбола [16], и хотя его эффективность не была полностью подтверждена, именно усилия создателей данного лекарственного средства и несколько спасенных жизней показали один из возможных путей борьбы с данной инфекцией. Так начались поиски эффективного типа антител для подавления или ослабления вируса с целью облегчения течения болезни и ее лечения.
Впервые препарат REGN-EB3 был применен в качестве экспериментального лечения во время вспышки заирского эболавируса в 2018 году как на взрослых пациентах, так и на детях параллельно с проведением третьей части клинических испытаний препарата [17]. Согласно данным предварительных исследований, рекомендуемая дозировка для каждого компонента препарата составила 50 мг/кг, однако по завершении вспышки и сбора данных рекомендуемая дозировка была поднята до 100 мг/кг. Препарат разводят перед применением и однократно вводят пациенту внутривенно [18].
Научная сторона исследований
Препарат REGN-EB3, состоящий из антител атолтивимаб (REGN3470), мафтивимаб (REGN3479) и одесивимаб (REGN3471), показал высокое сродство к гликопротеинам вируса Эболы как in silico — при моделировании его активности путем молекулярного докинга, — так и in vivo — при испытании на животных и на людях. Данные электронной микроскопии показали, что при одновременном применении трех типов антител, их связывание с гликопротеином происходит на различных участках, что полностью изменяет свойства белка [18].
Антитела группы атолтивимабов и мафтивимабов успешно нейтрализовали псевдовирусные частицы (клетки, снабженные гликопротеинами вируса Эболы) при сравнительно небольших концентрациях в крови, однако применение одного одесивимаба имело несколько меньший эффект, несмотря на его наибольшее сродство к белковой структуре антигена. Одновременное применение препарата, содержащего все три группы антител, показало полную защиту подопытных животных от летального исхода на пятый, восьмой и одиннадцатый день течения болезни в сравнении с контрольной группой, которой препарат не вводили [18], [19]. Последовательное изучение влияния дозировок препарата на эффективность лечения показало, что минимальная эффективная доза в 100 мг/кг является наименьшей для лучшего контроля за симптомами инфекции [19].
В ходе клинических испытаний препарата, проведенных во время вспышки 2018–2019 годов в ДРК, было обнаружено снижение средней летальности с 50 до 27% и уменьшение общей вирулентности патогена в ходе мутаций в естественной среде обитания, что, несомненно, показывает эффективность препарата в лечении заболевания, однако все еще предполагает комбинированную терапию для достижения наилучшего результата с минимальным количеством летальных исходов.
Обнаруженные во время клинических испытаний побочные эффекты от применения препарата REGN-EB3 включали в себя лихорадку, озноб, тахикардию, учащенное дыхание и другие симптомы (рис. 6), характерные для геморрагической лихорадки Эбола средней тяжести. Полное описание свойств и особенностей представлено на странице 177 опубликованного отчета [9].
Дальнейшие планы
Согласно данным Национальной библиотеки медицины США, протокол клинических испытаний NCT03576690 был одобрен к проведению 14 октября 2020 года, и по настоящее время проводится проверка препарата для лечения болезни, вызываемой заирским эболавирусом, в рамках расширенных клинических испытаний. К исследованиям допускаются люди всех возрастов и полов, которые имеют положительный результат ПЦР-теста и не обладают противопоказаниями к применению представленного протокола лечения геморрагической лихорадки Эбола. Также стоит отметить разрешение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США на включение в перечень допущенных до тестирования субъектов беременных женщин, инфицированных вирусом Эбола.
Несмотря на наличие вакцины от болезни, вызываемой вирусом Эбола у многих стран мира, считается, что ей необходимы дополнительные клинические испытания на людях. Параллельно с этим проводятся расширенные клинические исследования препарата моноклональных антител для терапии больных людей. Всё вместе это отражает стремление ученых к созданию не только средств для предотвращения поражения людей этим смертельно опасным вирусом, но и способов лечения для лиц в зоне риска, а именно — жителей Западной Африки, находящихся далеко от пунктов медицинской помощи. Создание единого комплекса мер по противодействию лихорадке Эбола может стать одним из ключей, необходимых жителям африканских республик для дальнейшего развития в неблагоприятных условиях жизни.
Читайте также:


