Эозинофилы повышенные при вирусе эпштейн-барр
Обновлено: 17.04.2024
Эпштейна-Барр вирусная инфекция (ЭБВИ) относится к наиболее распространенным инфекционным заболеваниям человека. Антитела (Ат) к вирусу Эпштейна-Барр (ВЭБ) обнаруживают у 60% детей первых двух лет жизни и у 80–100% взрослых [3, 13]. Заболеваемость острой формой ЭБВИ (ОЭБВИ) в различных регионах мира колеблется от 40 до 80 случаев на 100 тыс. населения [2]. Хроническая форма ЭБВИ (ХЭБВИ) развивается у 15–25% лиц после ОЭБВИ [1, 5, 15]. Установлена роль ВЭБ в развитии злокачественных новообразований, аутоиммунных заболеваний и синдрома хронической усталости [3, 5, 14, 15]. Все это свидетельствует об актуальности проблемы ЭБВИ.
ВЭБ, открытый в 1964 г. M. Epstein и Y. Barr, относится к γ-герпес-вирусам [3]. ВЭБ имеет в своем составе 3 антигена: капсидный (VCA), ранний (EA) и ядерный (EBNA). Своеобразие патологического процесса при ЭБВИ определяется способностью ВЭБ к трансформации В-лимфоцитов, пожизненной персистенции в организме человека, индукции вторичного иммунодефицитного состояния (ИДС), аутоиммунных реакций, злокачественных опухолей [1, 3, 5, 12].
Источник заражения ВЭБ — больные манифестными и бессимптомными формами. 70–90% лиц, перенесших ОЭБВИ, выделяют вирус в последующие 1–18 мес. Пути передачи ВЭБ: воздушно-капельный, контактно-бытовой, парентеральный, половой, вертикальный. ОЭБВИ характеризуется эпидемическими подъемами 1 раз в 6–7 лет, чаще регистрируется в возрасте от 1 до 5 лет, в организованных коллективах [4, 7, 9].
Иммунный статус 109 больных ОЭБВИ в возрасте от 5 до 14 лет в нашей работе выявил признаки активации Т-клеточного звена иммунной системы — повышение количества Т-лимфоцитов (CD3), цитотоксических Т-лимфоцитов (CD8), клеток с маркерами поздней активации (HLA-DR); поликлональную активацию В-лимфоцитов — увеличение количества CD20-клеток, иммуноглобулинов (Ig) IgA, IgM, IgG, циркулирующих иммунных комплексов (ЦИК). Обнаружены признаки угнетения иммунной системы: нормальное содержание Т-хелперов (CD4), снижение иммунорегуляторного индекса CD4/CD8, количества естественных киллерных клеток NK (CD16), повышение готовности иммунокомпетентных клеток к апоптозу (CD95). Наблюдалась активация кислородзависимого метаболизма нейтрофилов и редукция его адаптационных возможностей.
У трети обследованных детей (33,9%) ОЭБВИ протекала в форме микст-инфекции с цитомегаловирусами (ЦМВ), вирусами простого герпеса 1 и 2 типов (ВПГ-1, ВПГ-2). При бактериологическом исследовании мазков из ротоглотки у 41,3% пациентов выделены Streptococcus (S.) viridans, у 11,9% — Candida albicans, у 8,2% — Staphilococcus (Staph.) epidermidis, у 6,4% — S. pyogenes, у 2,7% — Klebsiella (Kl.) pneumoniae, у 41,3% — ассоциация бактерий. У 43,1% пациентов — серологические маркеры активной формы хламидийной инфекции, у 30,3% — микоплазмоза.
Возможны следующие исходы ОЭБВИ: латентная инфекция, ХЭБВИ, ИДС, онкологические, аутоиммунные заболевания, синдром хронической усталости [5, 8, 10, 11]. Переход в ХЭБВИ связан с комплексом неблагоприятных факторов в анте-, интра- и постнатальном периодах, нарушением нейроиммунноэндокринной регуляции, генетической предрасположенностью.
Проведенное нами обследование 60 детей в возрасте от 5 до 14 лет с ХЭБВИ показало, что в этой группе у 86,7% матерей имел место отягощенный акушерский анамнез; у 83,3% детей обнаружены перинатальная и постнатальная патология ЦНС, ЛОР-органов и др.
Нарушения иммунного статуса приводили к активации условно-патогенной микрофлоры, вирусных и грибковых инфекций. В микробном спектре слизистой ротоглотки пациентов с ХЭБВИ выделены S. Viridans (30%), Candida albicans (28,3%), Staph. Epidermidis (25%), S. Pyogenes (20%), Kl. Pneumoniae (8,4%), ассоциация бактерий (41,7%); у 28,3% — серологические маркеры активной формы хламидиоза, у 26,7% — микоплазмоза. У 90% пациентов заболевание протекало в форме микст-инфекции с участием герпес-вирусов: ВЭБ + ЦМВ, ВЭБ + ВПГ-1, ВПГ-2.
Классификация. Общепринятая классификация заболевания отсутствует; рекомендуем использовать разработанную нами рабочую классификацию ЭБВИ.
- По периоду возникновения: врожденная, приобретенная.
- По форме: типичная (инфекционный мононуклеоз), атипичная: стертая, бессимптомная, висцеральная.
- По тяжести: легкая, среднетяжелая, тяжелая.
- По течению: острая, затяжная, хроническая.
- По фазе: активная, неактивная.
- Осложнения: гепатит, разрыв селезенки, менингоэнцефалит, полирадикулонейропатия, миокардит, синусит, отит, гемолитическая анемия, тромбоцитопения, нейтропения, панкреатит и др.
- Микст-инфекция.
Примеры оформления диагноза:
- Осн.: Приобретенная ЭБВИ, типичная тяжелая форма (инфекционный мононуклеоз), острое течение, активная фаза. Осл.: Острый гепатит.
- Осн.: Приобретенная ЭБВИ, висцеральная форма (менингоэнцефалит, гепатит, нефрит), тяжелое хроническое течение, активная фаза. Осл.: острая печеночно-почечная недостаточность. Сопp.: Респираторный хламидиоз (ринофарингит, бронхит, пневмония).
Клиническая картина острой ЭБВИ впервые была описана Н. Ф. Филатовым (1885) и Е. Пфейфером (1889). Инкубационный период длится от 4-х дней до 7 нед. Полный симптомокомплекс формируется к 4–10-му дням болезни [4, 7].
Нами обследованы 109 детей с ОЭБВИ. У большинства пациентов заболевание начинается остро, с повышения температуры тела и появления симптомов интоксикации; реже отмечается постепенное начало: несколько дней наблюдается недомогание, слабость, вялость, снижение аппетита. Температура тела субфебрильная или нормальная. Ко 2–4-му дням болезни температура достигает 39–40 °С; лихорадка и симптомы интоксикации могут сохраняться в течение 2–3 и более недель.
Тонзиллит — наиболее частый и ранний симптом ОЭБВИ, сопровождается увеличением миндалин до II-III степени. Лакунарный рисунок подчеркнут за счет инфильтрации ткани миндалин или сглажен из-за лимфостаза. На миндалинах — налеты желтовато-белого или грязно-серого цвета в виде островков, полосок. Они исходят из лакун, имеют шероховатую поверхность (напоминают кружево), легко снимаются без кровоточивости, растираются, не тонут в воде. Характерно несоответствие размера налета и степени увеличения регионарных ЛУ. При фибринозно-некротическом характере налетов в случае их распространения за пределы миндалин необходим дифференциальный диагноз с дифтерией. Налеты на миндалинах исчезают, как правило, через 5–10 дней.
Гепатомегалия может быть обнаружена с первых дней болезни, однако чаще выявляется на второй неделе. Нормализация размеров печени происходит в течение полугода. У 15–20% больных в качестве осложнения развивается гепатит.
Спленомегалия относится к поздним симптомам, встречается у большинства больных. Нормализация размеров селезенки происходит в течение 1–3 нед.
Экзантема при ОЭБВИ появляется на 3–14-й дни болезни, имеет полиморфный характер — пятнистая, папулезная, пятнисто-папулезная, розеолезная, мелкоточечная, геморрагическая. Определенной локализации нет. Сыпь наблюдается в течение 4–10 дней, иногда оставляет пигментацию. У детей, получавших ампициллин или амоксициллин, сыпь появляется чаще (90–100%).
Гематологические изменения включают лейкоцитоз (10–30 х 10 9 /л), нейтропению с палочкоядерным сдвигом влево, увеличение количества лимфоцитов, моноцитов, атипичных мононуклеаров до 50–80%, повышение СОЭ до 20–30 мм/час. Характерный гематологический признак — атипичные мононуклеары в количестве 10–50%: они появляются к концу первой недели заболевания, сохраняются в течение 1–3 нед.
Хроническая ЭБВИ является исходом ОЭБВИ или развивается как первично-хроническая форма [2, 5, 8, 10, 11, 15]. Нами обследовано 60 детей с ХЭБВИ, клиника которой включала хронический мононуклеозоподобный синдром и полиорганную патологию. У всех пациентов обнаружены лимфопролиферативный синдром (генерализованная лимфаденопатия, гипертрофия небных и глоточной миндалин, увеличение печени и селезенки) и признаки хронической интоксикации (длительный субфебрилитет, слабость, снижение аппетита и др.). Вследствие развития ИДС наблюдались острые инфекции респираторного тракта и ЛОР-органов с обострениями до 6–11 раз в год: ринофарингиты (28,3%), фаринготонзиллиты (91,7%), аденоидиты (56,7%), отиты (11,7%), синуситы (20%), ларинготрахеиты (18,3%), бронхиты (38,3%), пневмонии (25%). Обращала внимание высокая частота полиорганной патологии, обусловленная длительной репликацией ВЭБ, вторичным ИДС, аутоиммунными реакциями (патология ЦНС; хронический гастрит, дискинезия желчевыводящих путей; кардиальный синдром, артралгии).
В последние годы описана врожденная ЭБВИ. Установлено, что риск ее при первичной ЭБВИ во время беременности составляет 67%, при реактивации — 22%. Клиника врожденной ЭБВИ сходна с ЦМВИ.
Установлена роль ВЭБ в развитии онкологических заболеваний и паранеопластических процессов — лимфомы Беркетта, назофарингеальной карциномы, лимфогранулематоза, опухолей желудка, кишечника, слюнных желез, матки, лейкоплакии языка и слизистой ротовой полости, а также ряда аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена, лимфоидного интерстициального пневмонита, хронического гепатита, увеита и др. [3, 5, 14, 15]. ВЭБ, наряду с вирусами герпеса человека 6 и 7 типов, является этиологическим фактором синдрома хронической усталости и наиболее частой причиной (15%) развития длительной лихорадки неясного генеза.
Диагностика ЭБВИ основана на учете групп риска, ведущих клинических синдромов и данных лабораторного исследования [8–11]. К группам риска у матери относят отягощенный анамнез, маркеры герпес-вирусных инфекций и др., у ребенка — перинатальное поражение ЦНС, аллергический фенотип, ИДС, маркеры герпес-вирусных инфекций и др. Ведущими клиническими синдромами ЭБВИ являются мононуклеозоподобный, общеинфекционный синдромы, экзантема, синдром полиорганной патологии.
В обязательный стандарт диагностики ЭБВИ входят клинический анализ крови, общий анализ мочи, биохимическое исследование крови, бактериологическое исследование слизи ротоглотки и носа, серологические маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм, УЗИ органов брюшной полости, консультация ЛОР-врача, по показаниям — рентгенография придаточных пазух носа, органов грудной клетки, ЭКГ. Дополнительный стандарт диагностики (в специализированном лечебно-профилактическом учреждении): маркеры ВЭБ, других герпес-вирусов, хламидий, микоплазм методом полимеразной цепной реакции (ПЦР), иммунограмма второго уровня, консультация иммунолога, по показаниям — коагулограмма, морфологическая картина стернальной пункции, консультация гематолога, онколога.
Методом иммуноферментного анализа (ИФА) определяют Ат к антигенам ВЭБ, что позволяет осуществить лабораторную диагностику ЭБВИ и определить период инфекционного процесса.
Ат класса IgM к VCA появляются одновременно с клиникой ОЭБВИ, сохраняются в течение 2–3 мес, повторно синтезируются при реактивации ВЭБ. Длительная персистенция высоких титров этих Ат характерна для ХЭБВИ, ВЭБ-индуцированных опухолей, аутоиммунных заболеваний, ИДС.
Ат класса IgG к EA достигают высокого титра на 3–4-й нед ОЭБВИ, исчезают через 2–6 мес. Они появляются при реактивации, отсутствуют при атипичной форме ЭБВИ. Высокие титры Ат данного класса выявляют при ХЭБВИ, ВЭБ-индуцированных онкологических и аутоиммунных заболеваниях, ИДС.
Ат класса IgG к EBNA появляются через 1–6 мес после первичной инфекции. Затем их титр уменьшается и сохраняется в течение всей жизни. При реактивации ЭБВИ происходит повторное увеличение их титра.
Большое значение имеет исследование авидности Ат класса IgG (прочности связывания антигена с Ат). При первичной инфекции сначала синтезируются Ат с низкой авидностью (индекс авидности (ИА) менее 30%). Для поздней стадии первичной инфекции характерны Ат со средней авидностью (ИА — 30–49%). Высокоавидные Ат (ИА — более 50%) образуются через 1–7 мес после инфицирования ВЭБ.
Серологическими маркерами активной фазы ЭБВИ являются Ат IgM к VCA и Ат IgG к EA, низкая и средняя авидность Ат IgG к маркерам неактивной фазы, Ат IgG к EBNA.
Материалом для ПЦР служат кровь, ликвор, слюна, мазки со слизистой ротоглотки, биоптаты органов и др. Чувствительность ПЦР при ЭБВИ (70–75%) ниже, чем при других герпесвирусных инфекциях (95–100%). Это связано с появлением ВЭБ в биологических жидкостях лишь при иммуноопосредованном лизисе инфицированных В-лимфоцитов.
На основании опыта лечения 169 детей с ЭБВИ нами разработан стандарт лечения этого заболевания.
Базисная терапия: охранительный режим; лечебное питание; противовирусные препараты: вироцидные препараты — инозин пранобекс (Изопринозин), аномальные нуклеозиды (Валтрекс, Ацикловир), Арбидол; препараты ИФН — рекомбинантный ИФН α-2β (Виферон), Кипферон, Реаферон-ЕС-Липинт, интерфероны для в/м введения (Реаферон-EC, Реальдирон, Интрон А, Роферон А и др.); индукторы ИФН — Амиксин, сверхмалые дозы антител к γ-ИФН (Анаферон), Циклоферон, Неовир. По показаниям: локальные антибактериальные препараты (Биопарокс, Лизобакт, Стопангин и др.); системные антибактериальные препараты (цефалоспорины, макролиды, карбапенемы); иммуноглобулины для внутривенного введения (Иммуновенин, Габриглобин, Интраглобин, Пентаглобин и др.); витаминно-минеральные комплексы — Мульти-табс, Вибовит, Санасол, Киндер Биовиталь гель и др.
Интенсификация базисной терапии по показаниям:
Симптоматическая терапия.
При лихорадке — жаропонижающие препараты (парацетамол, ибупрофен и др.); при затруднении носового дыхания — назальные препараты (Изофра, Полидекса, Називин, Виброцил, Адрианол и др.); при сухом кашле — противокашлевые препараты (Глаувент, Либексин), при влажном кашле — отхаркивающие и муколитические препараты (АмброГЕКСАЛ, бромгексин, ацетилцистеин и др.).
Эффективность этиотропной терапии ОЭБВИ оценена в двух группах больных. Пациенты 1-й группы (52 человека) получали инозин пранобекс (Изопринозин) в сочетании с рекомбинантным ИФН α-2β (Вифероном), больные 2-й группы (57 детей) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Клинико-серологические показатели до начала лечения и через 3 мес терапии представлены в табл. 1. У пациентов обеих групп в динамике отмечалось достоверное уменьшение таких симптомов, как генерализованная лимфаденопатия, тонзиллит, аденоидит, гепатомегалия и спленомегалия. Вместе с тем на фоне комбинированной терапии, положительная динамика клинических показателей была более значительной; острые респираторные инфекции (ОРИ) лишь у 19,2% больных 1-й группы и у 40,3% больных 2-й группы (p < 0,05). На фоне комбинированной терапии наблюдалось более быстрое исчезновение серологических маркеров репликации.
Эффективность этиотропной терапии исследована у 60 больных ХЭБВИ. Пациенты 1-й группы (30 детей) получали инозина пранобекс (Изопринозин) и рекомбинантный ИФН α-2β (Виферон), 2-я группа (30 человек) — монотерапию рекомбинантным ИФН α-2β (Вифероном). Независимо от схемы лечения через 3 мес после начала терапии отмечалось достоверное уменьшение частоты генерализованной лимфаденопатии, гипертрофии небных и глоточной миндалин, спленомегалии, интоксикационного, инфекционного и вегето-висцерального синдромов (табл. 2). Комбинация инозина пранобекса (Изопринозина) с рекомбинантным ИФН α-2β (Вифероном) способствовало более существенной динамике клинических показателей. Количество эпизодов ОРИ снизилось с 6–11 (7,9 ± 1,1) до 4–6 (5,2 ± 1,2) в год на фоне монотерапии рекомбинантным ИФН α-2β (Вифероном), и до 2–4 (2,5 ± 1,4) в год на фоне комбинированной терапии (p < 0,05). В обеих группах уменьшалась частота репликации ВЭБ, однако при сочетанном применении противовирусных препаратов этот эффект был более выраженным.
Побочных эффектов при использовании инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона) не было.
Результаты проведенного исследования свидетельствуют о потенцировании эффектов при комбинации инозина пранобекса (Изопринозина) с рекомбинантным ИФН a-2b (Вифероном) у больных ЭБВИ.
Потенцирование противовирусных, иммуномодулирующих и цитопротекторных эффектов этих препаратов приводит к более существенной, чем при монотерапии, положительной динамике проявлений клинических симптомов ЭБВИ, к исчезновению серологических маркеров активности инфекционного процесса. Следует отметить высокую эффективность и безопасность комбинированной терапии с использованием инозина пранобекса (Изопринозина) и рекомбинантного ИФН α-2β (Виферона).
Реабилитация. Ребенок наблюдается участковым врачом и инфекционистом, снимается с учета через 6–12 мес после исчезновения клинико-лабораторных показателей активности инфекционного процесса. Кратность осмотров — 1 раз в месяц. По показаниям рекомендуют консультацию ЛОР-врача, иммунолога, гематолога, онколога и др. Лабораторные и инструментальные исследования пациентов включают: клинический анализ крови 1 раз в месяц в течение 3 мес, затем 1 раз в 3 месяца, по показаниям — чаще; серологические маркеры ВЭБ методом ИФА один раз в три месяца, по показаниям — чаще; ПЦР крови, мазков из ротоглотки 1 раз в 3 месяца, по показаниям — чаще; иммунограмма — 1 раз в 3–6 мес; биохимическое и инструментальное исследования — по показаниям.
Реабилитационная терапия включает: охранительный режим, лечебное питание, противовирусные препараты по пролонгированным схемам. Под контролем иммунограммы осуществляют иммунокоррекцию. По показаниям назначают локальные антибактериальные препараты, курсы витаминно-минеральных комплексов, про- и пребиотиков, препаратов метаболической реабилитации, энтеросорбентов, антигистаминные препараты, гепато-, нейро- и ангиопротекторы, кардиотропные препараты, ферменты, гомеопатические средства, немедикаментозные методы лечения.
Таким образом, ЭБВИ характеризуется широким распространением, длительным течением с периодической реактивацией инфекционного процесса у части пациентов, возможностью развития осложнений и неблагоприятных исходов (онкозаболеваний, аутоиммунной патологии). Важную роль при ЭБВИ играет формирование вторичного ИДС. Ведущими клиническими синдромами ЭБВИ являются острый и хронический мононуклеозоподобный синдромы, интоксикационный, инфекционный, церебральный, гастроинтестинальный, кардиальный и артралгический синдромы. Диагностика ЭБВИ основана на анализе групп риска, выделении ведущих клинических синдромов и лабораторном исследовании. Лечение ЭБВИ является комплексным и включает этиотропные средства (виростатические препараты, интерферон и его индукторы), препараты патогенетической, иммуномодулирующей, симптоматической терапии. Сочетанное пролонгированное использование инозина пранобекс (Изопринозина) и рекомбинантного ИФН α-2β (Виферона), потенцирующих свои иммунокорригирующие и цитопротекторные эффекты, существенно повышает эффективность лечения. Больные ЭБВИ нуждаются в длительной реабилитации с обязательным контролем клинико-лабораторных показателей активности инфекционного процесса.
По вопросам литературы обращайтесь в редакцию.
Э. Н. Симованьян, доктор медицинских наук, профессор
В. Б. Денисенко, кандидат медицинских наук
Л. Ф. Бовтало, кандидат медицинских наук
А. В. Григорян
Ростовский ГМУ, Ростов-на-Дону
На сервисе СпросиВрача доступна консультация инфекциониста по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!


У вас сильно повышены эозинофилы, аллергопанель сдавали? Кал на гельминтозы методом 3х кратного обогащения?


Здравствуйте. На ЦМВ И ВПГ проверялись? Какие жалобы помимо температуры? Нужно сдать кал на яйца гельминтов и цисты простейших 3х кратно в лаборатории СЭС (чтобы смотрел празитолог) т.к за аллергию данных нет
Татьяна, кроме постоянной температуры повышены лейкоциты, эозинофилы, базофилы. Прикрепила ещё анализы

Здравствуйте! По результатам приведённых обследований у Вас персистирующая ВЭБ инфекция.Учитывая отсутствие четких клиничес их проявлений в настоящее время вне активации.Вам надо обследоваться на лямблиоз и другие паразитизмы.Сдайте кал на паразитов и яйца глистов методом обогащения,кровь на антитела к паразитам и ВИЧ

Возможно вся симптоматика определяется фоновым заболеванием. Рассеянный склероз в зависимости от этиологии может протекать с лимфоцитозом и эозинофилией
Нина, неврологи, у которых я состою на учёте, говорят, что рассеянный склероз не может быть причиной температуры и плохих анализов. К тому же болею более 10 лет, а такие проблемы максимум год


То есть причиной не являются различные наследственные факторы, вирусные агенты, токсические вещества?

На фоне неуточненного рассеянного склероза возможно и атипичное течение персистирующие вирусных инфекций.По поводу эозинофилии надо показаться гематологу.
Нина, и у гематолога была. тоже не знает как мне помочь и в чем причина моих жалоб. Это замкнутый круг, врачей посетила много, анализов сдала ещё больше, а найти никто ничего не может. По этой причине и обратилась на этот сайт, но, к сожалению, и здесь тупик

Получается,что все опять сходится на рассеянном склерозе.А иммунитет Вы проверяли?Надо проверить на аутоагрессия,то на наличие аутоиммунные нарушений.

Здравствуйте, Елена !
Наличие igG на ВЭБ и ЦМВ говорит лишь о том, что Ваш организм сталкивался с этими вирусами и выработал антитела (иммунитет) против них ! Отсутствие же igМ на эти же вирусы, означает, что в настоящее время активного инфекционного процесса нет !
Лечение от ВЭБ не требуется ! Этот вирус невозможно полностью уничтожить, удалить из организма ! Он в неактивной форме остаётся в организме пожизненно !
Этим вирусом инфицировано примерно половина населения земли !
Высокое содержание эозинофилов в крови указывает на возможное наличие паразитарных заболеваний , лямблиоза в том числе ! Для их исключения необходимо обследование у инфекциониста !
Удачи Вам !
Возникнут вопросы, - напишите !

Елена, здравствуйте !
Вы правы, анализ отрицателен и причина субфебрильной температур неясна !
Имеется такое понятие, - АНАЛИЗ КРОВИ НА СТЕРИЛЬНОСТЬ !
Я Вам рекомендую сдать такой анализ ! Бывает, что из хронических различных очагов воспаления в организме в кровь могут попасть бактерии и стать причиной такой температуры !

Здравствуйте, Елена! Положительный IgG к ВЭБ означает то, что Вы переболели вирусом и то, что на него выработаны иммунитет.
Он сейчас в неактивной форме и не требует лечения.

Здравствуйте! ВЭБ неактивен и не является причиной состояния. Сдайте ИФА крови на 4 гельминтов панель.

Здравствуйте. Никакой хронической ВЭБ-инфекции или цитомегаловирусной инфекции у вас по анализам нет. Высокие титры иммуноглобулина G в ваших анализах объясняются вашим основным аутоиммунным заболеванием.
В статье содержатся результаты собственных наблюдений за 140 детьми в возрасте от 1 до 15 лет с инфекционным мононуклеозом, сопровождавшимся лихорадкой, ангиной, увеличением лимфатических узлов, печени и селезенки. Проведена комплексная оценка изменений периферической крови при острой Эпштейн-Барр вирусной инфекции, цитомегаловирусной инфекции, инфекционном мононуклеозе неуточненной этиологии, микст-инфекции. Выполнен подсчет количества эритроцитов, лейкоцитов, тромбоцитов, лейкоцитарный индекс интоксикации, определение концентрации гемоглобина и гематокрита (Ht), скорости оседания эритроцитов. Верификацию возбудителя осуществляли с помощью молекулярно-генетического (ПЦР) метода исследования. На основании лабораторных данных были сформулированы дифференциально-диагностические особенности инфекционного мононуклеоза различной этиологии у детей. Доказано, что длительность и тяжесть течения инфекционного мононуклеоза напрямую зависят от типа возбудителя, возраста и состояния иммунитета больного.

1. Белан Ю.Б., Михайлова Т.А. Значение клинических и лабораторных данных в дифференциальной диагностике инфекционного мононуклеоза // Детские инфекции. - 2008. - № 1 (7). - С. 32-35.
2. Крамарь Л.В., Арова А.А., Карпухина О.А. Клинико-иммунологические характеристики мононуклеозоподобного синдрома у детей // Вестник Волгоградского государственного медицинского университета. - 2012. - № 1 (41). - С. 72-74.
3. Крамарь Л.В., Карпухина О.А., Арова А.А. Этиологическая структура и клинико-лабораторная характеристика мононуклеозоподобного синдрома у детей // Фундаментальные исследования. - 2012. - № 7 (1). - С. 92-95.
4. Рослый И.М., Абрамов С.В. Биохимические показатели в оценке цитолитических механизмов и метаболических процессов на примере инфекционного мононуклеоза // Эпидемиология и инфекционные болезни. - 2005. - № 5. - С. 33-41.
5. Симованьян Э.Н. Эпштейна-Барр вирусная инфекция у детей // Лечащий врач. - 2007. - № 7. - С. 36-41.
6. Уразова О.И., Новицкий В.В., Помогаева А.П. Клинико-гематологические и цитогенетические проявления инфекционного мононуклеоза у детей // Эпидемиология и инфекционные болезни. - 2004. - № 3. - С. 34-39.
7. Mossman K.L., Ashkar A.A. Herpesviruses and the innate immune response // Viral Immunol. - 2005. - Vol. 18. - № 2. - P. 267-281.
8. Randall R.E., Goodbourn S. Interferons and viruses: an interplay between induction, signalling, antiviral responses and virus countermeasures // J. Gen. Virol. - 2008. - Vol. 89. - P. 41-47.
Общий анализ крови (ОАК) - один из важнейших диагностических методов, тонко отражающих реакцию кроветворных органов на воздействие различных физиологических и патологических факторов. Данные, полученные при его выполнении, представляют собой интегральные показатели состояния гемопоэтической системы, зрелые элементы которой осуществляют основные защитные функции организма и принимают активное участие во всех видах обмена [7].
Количественные и качественные изменения форменных элементов крови характерны для многих инфекционных заболеваний как бактериальной, так и вирусной этиологии. Наиболее выраженные изменения в периферической крови наблюдаются при герпетических инфекциях, кори, краснухе, ВИЧ-инфекции, вирусных гепатитах и др. [1].
Инфекционный мононуклеоз - острое инфекционное заболевание, вызываемое герпетическими вирусами 4, 5, 6-го типов, характеризующееся лихорадочным состоянием, ангиной, увеличением лимфатических узлов, печени и селезенки [5].
В настоящее время инфекционный мононуклеоз следует считать полиэтиологическим заболеванием. Согласно МКБ -10 выделяют: инфекционный мононуклеоз, вызванный гамма-герпетическим вирусом Эпштейн-Барр (В27.01); цитомегаловирусный мононуклеоз (В27.1);
другой инфекционный мононуклеоз (В27.8); инфекционный мононуклеоз неуточненный (В27.9).
Основными проявлениями инфекционного мононуклеоза, определяющими его сущность и название, служат изменения в периферической крови, которые возникают в первые дни болезни и достигают максимума в ее разгар. Это умеренный лейкоцитоз, увеличение количества одноядерных элементов крови (лимфомоноцитоз), умеренное повышение СОЭ [8]. В начале болезни у большинства больных значительно снижается содержание сегментоядерных нейтрофилов и увеличивается количество палочкоядерных. Самым характерным признаком инфекционного мононуклеоза является наличие атипичных мононуклеаров, которые появляются в разгар болезни и сохраняются 2-3 недели. На ранних стадиях - это В-лимфоциты, содержащие специфические иммуноглобулины в цитоплазме. В последующие стадии большую часть атипичных мононуклеаров составляют Т-клетки [2].
Диагностическое значение имеет увеличение количества атипичных мононуклеаров с широкой цитоплазмой не менее чем до 10-12%, хотя число этих клеток может достигать 80-90%. Следует заметить, что отсутствие атипичных мононуклеаров при характерных клинических проявлениях заболевания не противоречит предполагаемому диагнозу, поскольку их появление в периферической крови может задерживаться до конца 2-3-й недели болезни [4].
При обследовании детей с инфекционным мононуклеозом анализ крови обычно включает определение количества эритроцитов, лейкоцитов, тромбоцитов, ретикулоцитов, подсчёт лейкоцитарной формулы, определение концентрации гемоглобина, СОЭ, вычисление цветового показателя и гематокрита (Ht).
Данные общего анализа крови позволяют получить комплексное представление о тяжести течения инфекционного мононуклеоза, наслоении бактериальной инфекции, эффективности проводимой терапии.
Цель исследования - выявление закономерностей изменения показателей периферической крови у детей при инфекционном мононуклеозе различной этиологии.
Материалы и методы исследования
Под нашим наблюдением находилось 140 детей с инфекционным мононуклеозом в возрасте от 1 до 15 лет, проходивших стационарное лечение в Волгоградской областной детской клинической инфекционной больнице. Верификацию возбудителя осуществляли с помощью молекулярно-генетического (ПЦР) метода исследования. Также всем больным проводилось комплексное обследование, которое включало в себя общеклинические (сбор анамнеза, осмотр, пальпацию, перкуссию, аускультацию) и лабораторно-инструментальные методы: общие анализы крови и мочи, биохимические тесты (АЛТ, АСТ, коэффициент де Ритиса, тимоловые пробы), УЗИ органов брюшной полости.
С целью определения степени интоксикации и выраженности гнойно-воспалительного процесса в ротоглотке при инфекционном мононуклеозе у детей производили расчёт лейкоцитарного индекса интоксикации (ЛИИ). Определение ЛИИ имело важное значение как для контроля за лечением, так и для прогноза заболевания.
Существует несколько способов расчета лейкоцитарного индекса интоксикации. Нами была выбрана формула В.К. Островского (1983), в которой в числителе находится сумма процентного содержания клеток миелоидного ряда, а в знаменателе - сумма остальных клеток белой крови [6].
Формула расчёта ЛИИ,
где: ПК - плазматические клетки, миел. - миелоциты, ю. - юные, п. - палочкоядерные, с. - сегментоядерные, Лимф. - лимфоциты, мон. - моноциты, э. - эозинофилы, б. - базофилы.
Результаты и их обсуждение
Данные, полученные при исследовании носоглоточной слизи и сыворотки крови у 140 детей методом ПЦР, показали, что на долю классического ИМ, вызванного Эпштейн-Барр вирусом (ЭБВ), приходилось 74,3% всех случаев. У 1/3 детей мононуклеоз был обусловлен другими возбудителями: в 9,2% - цитомегаловирусом (ЦМВ), в 8,6% - микст-инфицированием ЦМВ и ЭБВ, у 7,9% детей этиологию заболевания установить не удалось.
Далее нами был проведен анализ гемограмм наблюдаемых детей с учетом этиологии заболевания. Полученные данные представлены в табл. 1 и 2.
Таблица 1 - Частота встречаемости патологических изменений показателей ОАК при инфекционном мононуклеозе различной этиологии
Таблица 2 - Средние значения патологических показателей ОАК при инфекционном мононуклеозе различной этиологии
Сниж. гемоглобина (г/л)
Повыш. гемоглобина (г/л)
Сниж. гематокр. (г/л)
Ускорение СОЭ (мм/час)
Оценка данных таблиц показала, что при Эпштейн-Барр вирусном мононуклеозе лейкоцитоз отмечался у 43,3% больных, лейкопения - у 2,9%. Количество лейкоцитов колебалось в широких пределах - от 4,0х109 г/л до 32,7х109 г/ л и в среднем составляло 16,3±5,3х109 г/л. Характерным для ИМ-ЭБВ этиологии изменением в периферической крови было снижение сегментоядерных нейтрофилов (в среднем до 18,1±8,2%), что отмечалось у 39,4% детей. Нейтрофилез встречался редко и был зафиксирован только у 7,7% больных. В 16,3% случаев у детей с ИМ-ЭБВ этиологии в ОАК отмечался палочкоядерный сдвиг влево. Количество палочкоядерных нейтрофилов колебалось от 0 до 42%, составляя в среднем - 11,4±8,9%.
Процентное содержание лимфоцитов в периферической крови у детей было разнообразным и варьировало от 2,0 до 85,0%. Лимфоцитоз, при сравнении с нормальными возрастными показателями, был выявлен у 21,2% обследованных, лимфопения - у 15,4%. Нарастание моноцитов отмечалось у 23,0% детей, их среднее значение составило - 15,6±3,3%.
Наличие в периферической крови атипичных мононуклеаров при инфекционном мононуклеозе Эпштейн-Барр вирусной этиологии являлось кардинальным симптомом и встречалось в 74,0% случаев. Количество плазматических клеток было разнообразным и в большинстве случаев зависело от сроков заболевания. Так, у 39,4% больных их значение не превышало 10% и в среднем равнялось 5,5±2,8%. У 34,6% - количество атипичных мононуклеаров в крови было более 10% и имело среднее значение - 21,9±1,7%.
Тромбоцитопения была частым симптомом ЭБВ-инфекции и выявлялась у 52,9% больных. Значение показателей тромбоцитов колебалось в пределах от 81х109 до 173х109 г/л и в среднем составляло 131±14,5х109 г/л.
Ускорение СОЭ отмечалось у 34,6% детей при ЭБВ-инфекции. Значения данного показателя были разнообразными и колебались от 13 до 50 мм/час, в среднем составляя 24±10,9 мм/час.
Цитомегаловирусная инфекция была подтверждена у 13 детей, поступавших в стационар с диагнозом инфекционный мононуклеоз. Характерными особенностями ОАК крови при ЦМВ-инфекции были: значительный лейкоцитоз со сдвигом влево и повышением общего количества лейкоцитов до 17,5±6,6х109 г/л, который наблюдался у 1/3 больных, нейтропения (у 23,0%), лимфоцитоз (23,0%), эритроцитоз (30,8%), гипохромная анемия (30,8%), тромбоцитопения (53,8%), выраженное снижение гематокрита, в среднем до 25,7 ±1,2 г/л, что наблюдалось у 61,5% детей. Обращала на себя внимание высокая частота встречаемости атипичных мононуклеаров в периферической крови у больных цитомегаловирусной инфекцией (84,6%), причем их количество в подавляющем большинстве случаев превышало 10% и в среднем составляло 17,5±2,1%.
СОЭ при ЦМВ-инфекции чаще соответствовало возрастной норме, ее ускорение отмечалось лишь у 23,0% детей.
Инфекционный мононуклеоз, обусловленный одновременным инфицированием Эпштейн-Барр и цитомегаловирусом, был диагностирован у 12 детей. Изменение показателей ОАК при микст-инфекции также имело характерные особенности: лейкопения за счет снижения сегментоядерных нейтрофилов, что выявлялось в 33,3% случаев, выраженный лимфоцитоз (у 33,3%) с повышением количества лимфоцитов в среднем до 74,3±13,2%, нормальное содержание моноцитов. Атипичные мононуклеары при микст-инфекции обнаруживались в крови у 33,3% больных, что было вдвое реже, чем при изолированных Эпштейн-Барр и ЦМВ-инфекциях. Их количество в подавляющем большинстве случаев не превышало 10% и в среднем соответствовало 8,2±2,4%.
Характерной особенностью инфекционного мононуклеоза смешанной этиологии была высокая частота встречаемости ускоренной СОЭ, что было выявлено у 58,3% больных. Данный показатель колебался в пределах от 13 до 40 мм/час, в среднем составляя 21±9,9 мм/час.
СОЭ была ускоренной у 54,5% детей, колебалась в пределах от 15 до 36 мм/час, в среднем не превышала 21±7,9 мм/час.
Для оценки степени интоксикации и выраженности гнойно-воспалительного процесса в ротоглотке при инфекционном мононуклеозе у детей мы производили расчёт лейкоцитарного индекса интоксикации (табл. 3).
Таблица 3 - Значение лейкоцитарного индекса интоксикации при инфекционном мононуклеозе различной этиологии
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Эозинофилия: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Эозинофилия – это состояние, при котором отмечается повышение уровня эозинофилов в крови. Эозинофилы представляют собой один из видов белых клеток крови – лейкоцитов, образуются в костном мозге, откуда попадают в кровоток. Повышение их количества отмечается при паразитарных и аллергических заболеваниях, туберкулезе, инфекционных процессах и некоторых других состояниях и заболеваниях, требующих полноценного обследования и специфической терапии.
Разновидности эозинофилии
По количеству клеток в единице крови различают следующие эозинофилии:
- легкая, когда содержание эозинофилов составляет от 500 до 1500 в микролитре крови;
- умеренная, когда содержание эозинофилов составляет от 1500 до 5000 в микролитре крови;
- выраженная, когда содержание эозинофилов составляет более 5000 в микролитре крови.
- первичную, или клональную эозинофилию, которая наблюдается при патологиях крови;
- вторичную, или реактивную эозинофилию, которая развивается как ответная реакция на аллергены, паразитарные инвазии и т.д.
- идиопатическую, или транзиторную эозинофилию, причины которой выяснить не удается.
В наибольшей степени эозинофилы задействованы в иммунном ответе с выраженным аллергическим компонентом.
Аллергическая реакция является одной из форм ответа организма на проникновение извне чужеродных агентов (аллергенов).
Аллергеном может стать практически любое вещество, однако чаще в роли аллергена выступают белки. При первом попадании аллергена в организм клетки лимфоциты начинают вырабатывать особый вид антител IgE, играющих ключевую роль в развитии аллергической реакции при повторном контакте организма с данным аллергеном. Антитела активируют эозинофилы, приводя к их повышенному содержанию в крови.
Заболевания, при которых повышаются эозинофилы крови
Эозинофилия является характерным проявлением аллергических заболеваний и состояний, таких как:
- аллергический ринит и конъюнктивит;
- атопический дерматит;
- бронхиальная астма;
- пищевая аллергия и др.
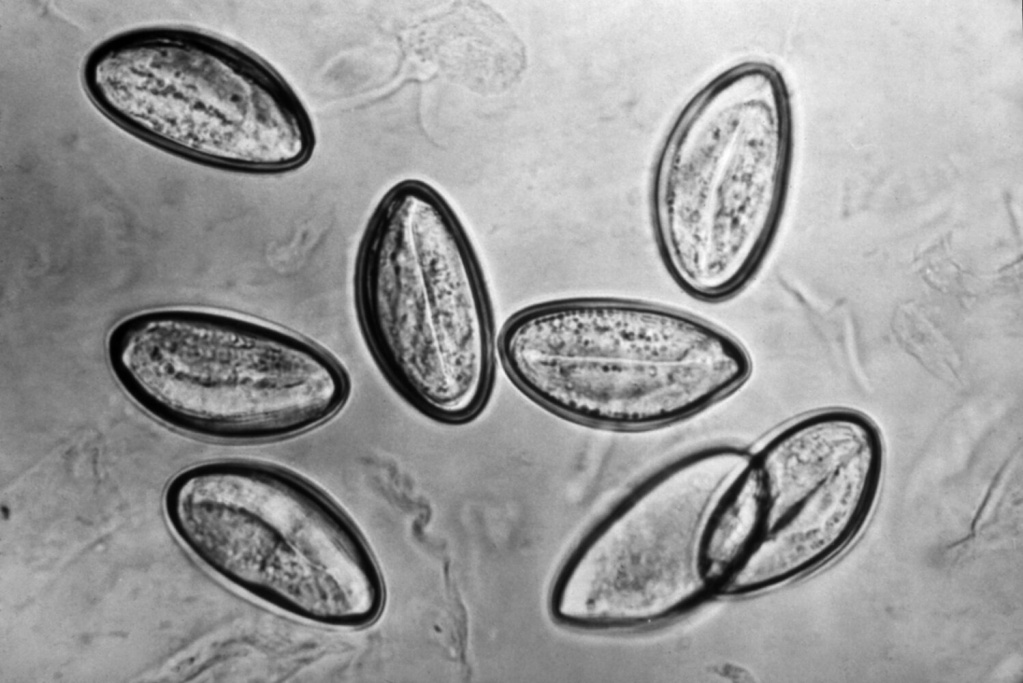
С одной стороны, эозинофилы обладают противопаразитарной активностью, за счет способности выделять эозинофильный катионный белок и активные формы кислорода, которые губительны для гельминтов. С другой стороны, продукты метаболизма гельминтов вызывают реакцию гиперчувствительности, для которой свойственны симптомы аллергии.
Следующая группа заболеваний, протекающих с повышением количества эозинофилов, - ревматологические патологии, или системные воспалительные заболевания соединительной ткани. Данные заболевания в абсолютном большинстве случаев являются аутоиммунными.
В основе аутоиммунных процессов лежит нарушение распознавания клетками иммунной системы собственных тканей, в результате чего они воспринимаются как чужеродные. Против них начинают вырабатываться антитела, и запускается воспалительный процесс.
Одним из аутоиммунных заболеваний, для которого характерна эозинофилия, является разновидность васкулита (воспаления сосудов) – эозинофильный гранулематоз с полиангиитом, или синдром Черджа–Стросса (воспаление мелких и средних кровеносных сосудов).
Эозинофилия может свидетельствовать о наличии в организме злокачественного процесса. Это связано с тем, что клетки злокачественных опухолей вырабатывают, среди прочего, вещества, стимулирующие образование эозинофилов. Так, эозинофилия является частым симптомом хронического миелолейкоза.
К каким врачам обращаться при эозинофилии
Эозинофилия не является самостоятельным заболеванием, но может быть признаком аллергических, аутоиммунных, инфекционных патологий.
Поэтому сначала можно обратиться к терапевту (врачу общей практики) или педиатру , если пациентом является ребенок. Зачастую данных, собранных в процессе опроса и клинического осмотра пациента, может оказаться достаточно для направления на прием к узкопрофильному специалисту. Так, при впервые выявленном аллергическом заболевании требуется консультация аллерголога-иммунолога, при гельминтозе - врача-инфекциониста, а при подозрении на аутоиммунный процесс – ревматолога.
Диагностика и обследование при эозинофилии
После тщательного сбора анамнеза и выявления ключевых фактов развития заболевания назначают лабораторные обследования.
Клинический анализ крови с определением лейкоцитарной формулы необходим для определения количества эозинофилов. В данном исследовании важно провести микроскопию мазка, которая позволяет не только достоверно подсчитать количество эозинофилов, но и выявить наличие в крови специфических клеток, характерных, например, для лейкоза и некоторых аутоиммунных заболеваний.
Синонимы: Общий анализ крови (ОАК); Гемограмма; КАК; Развернутый анализ крови. Full blood count; FBC; Complete Blood Count (CBC); Hemogram; CBC with White Blood Cell Differential Count; Peripheral Blood Smear; Blood Film Examination; Complete blood count (CBC) with differential white blood cell coun.
Читайте также:

