Есть ли антиген при гепатите с
Обновлено: 05.05.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Антитела к вирусу гепатита C класса IgM и IgG (anti-HCV total): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Гепатит С – вирусное заболевание, которое может протекать в бессимптомной и легкой форме в течение нескольких недель, но иногда может перейти в хроническую форму.
По статистике ВОЗ, самой частой причиной развития рака печени является предшествующее поражение органа вирусом гепатита С. У некоторых пациентов после контакта с вирусом развивается острая форма гепатита, а у ряда зараженных происходит спонтанная элиминация вируса (самостоятельное излечение) без проведения специфического лечения в течение нескольких лет после инфицирования.
Заражение вирусом гепатита С происходит при контакте с кровью, вагинальным секретом или спермой больного, при использовании загрязненных медицинских инструментов, в том числе в маникюрных и тату-салонах, при стоматологических и эстетических процедурах (инъекции ботокса, перманентный макияж), при введении наркотических веществ общими иглами и шприцами, при незащищенном половом контакте. Возможна передача вируса гепатита С от зараженной матери ребенку в процессе родов. Однако в настоящее время при выявлении этого заболевания у женщины практикуют отказ от естественных родов для снижения риска инфицирования ребенка. С учетом того, что вирус гепатита С не передается с грудным молоком, слюной, пищевыми продуктами, при поцелуях и объятьях, риск заражения бытовым путем минимален.
Диагностика гепатита С определяется особенностями строения вируса.

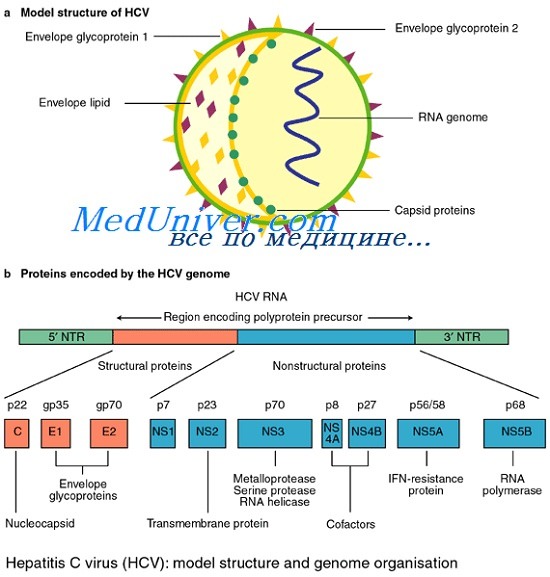
Вирус состоит из нуклеокапсида, содержащего РНК и окруженного липидной (жировой) мембраной, на поверхности которой расположены гликопротеины Е1 и Е2.
Синонимы: Суммарные антитела к вирусу гепатита С; анти-HCV. Anti-HCV IgG/IgM; Antibodies to Hepatitis C Virus, IgM + IgG; HCVAb, Total. Характеристика показателя Anti-HCV-total (антитела к антигенам вируса гепатита C суммарные) Внимание! При положительных и сомнительных реакциях срок выдачи ре.
Вирус гепатита С и его геном
Вирус гепатита С (HCV) идентифицирован в 1989 году американскими исследователями под руководством М. Houghton, когда была выделена нуклеиновая кислота при экспериментальном заражении шимпанзе и в дальнейшем получена ДНК-копия, которую использовали для создания библиотеки клонов. Скрининг образцов из этой библиотеки позволил выявить клон, экспрессирующий антиген, который реагировал с антителами из сывороток людей, больных посттрансфузионным гепатитом ни А ни В.
Далее был получен рекомбинантный белок, который содержал последовательность из 363 аминокислотных остатков вирусного белка. Эту последовательность обозначили как С-100-3 и использовали в качестве антигена при создании иммуноферментной тест-системы.
Геном вируса гепатита С представлен однонитевой позитивной линейной молекулой РНК, состоящей из 9379 оснований и кодирующей полипротеин из ЗОН аминокислот, который под действием вирусных и клеточных протеаз нарезается на отдельные вирусные белки. Таксономический анализ выявил принадлежность вируса гепатита С к семейству Flaviviridae самостоятельному роду Hepacivirus.
Проведенный анализ нуклеотидных последовательностей изолятов вируса гепатита С различных частей его генома сделал возможным классификацию этого вируса. Наиболее удобной в настоящее время является номенклатура P. Simmonds et al, 1993, основанная на анализе последовательностей области NS5. Эта классификация, а также разработанная примерно в это же время система Н. Okamoto et al., 1992 стала общепринятой. К наиболее распространенным в мире генотипам вируса гепатита С относят: la, lb, 2а, 2b и 3а. Эти генотипы распространены в странах Западной Европы и в Америке, причем преобладающим является генотип lb.
Совсем другое распределение генотипов HCV в странах центрального Востока и Северной и Центральной Африки. Генотип 4, главным образом 4а, доминирует в Египте, Йемене, Кувейте, Ираке, Саудовской Аравии, Заире, Бурунди, Габоне. На юге Африке наиболее часто встречается генотип 5а, который в других частях мира находили исключительно редко. Генотип 3 выявлен в странах Западной Европы, в Сингапуре, Таиланде, Мьянме и Восточной Индии. Всего выделено 9 подтипов третьего генотипа HCV.
В России также проведены исследования по определению структуры генотипов ВГС, циркулирующих в различных ее регионах. Наиболее часто — 60-70 % случаев определен генотип HCV lb. Далее следуют генотипы За, 1а, и 2а. Так, в 1998 году Е. В. Лисицина во Владимирской области выявила следующую структуру генотипов HCV: lb — 72,9 %, 2а — 2,9 %, 2Ь — 2,9 % и За — 15,7 %. В 5,7 % случаев с имеющимся набором праймеров генотип определить не удалось.
При этом было отмечено, что у лиц различного возраста структура генотипов различается. У лиц в возрасте 7-14 лет генотип It и За выявлен с одинаковой частотой —42,9%. Среди лиц старше 50 лет генотип lb выявлен в 90% случаев, тогда как За не определен вовсе.
Белки и антигены вируса гепатита С. Диагностика ВГС
Сегодня известно минимум 10 структурных и неструктурных белков, кодируемых геномом HCV. К структурным белкам относят core, envelop 1 и envelop 2. Белок core является белком нуклеокапсида, тогда как envelop 1 и envelop 2 — гликопротеины внешней оболочки вируса. В структурной зоне кодируется также белок р7, функция которого не ясна, однако аналогия с другими представителями семейства Flaviviridae позволяет предположить, что его функция связана с высвобождением вириона из инфицированной клетки.
Этот белок отщепляется клеточной пептидазой от envelop 2, но не во всех случаях, что обусловливает существование envelop 2 в виде двух форм более и менее протяженной.
Неструктурная область генома HCV кодирует 6 белков — NS2, NS3, NS4A, NS4B, NS5A и NS5B. Белок NS2 является вирусной металлозависимой протеиназой. Белок NS4A действует как эффектор или кофактор для NSЗ-протеолитической активности в NS4A/NS4B, NS4B/NS5A, NS5A/NS5B сайтах нарезания полипротеина вируса.
В настоящее время фрагменты структурных и неструктурных белков, полученных генноинженерным путем (рекомбинантные белки) или с помощью химического синтеза, используют в качестве антигенов при конструировании иммуноферментных тест-систем. Первое поколение иммуноферментных тест-систем появилось на рынке в 1989 году и было основано на прямом ИФА. В качестве иммуносорбента были использованы фрагменты двух белков, NS3 и NS4, обозначаемых как 5-1-1 и С100-3.
Одновременно были разработаны и подтверждающие тесты на основе иммуноблота с рекомбинантными белками (RIBA). Чувствительность этих тест-систем первого поколения составляла только 64% для ИФА и 55% для иммуноблота. Тест-системы второго поколения появились на рынке в 1991 году. В качестве антигенов, сорбированных на твердой фазе, в этих тест-системах использовали капсидные белки (фрагмент с22-3) и антигены неструктурных регионов NS3 (фрагменты с200 и сЗЗс) и NS4, что позволило повысить чувствительность и специфичность исследований. Поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) нагинается быстрее, гем на неструктурные белки, период от инфицирования до выявляемой сероконверсии удалось уменьшить до двух месяцев.
Подтверждающие тест-системы на основе иммуноблота позволяли идентифицировать участвующие в реакции антигены. Результаты, полученные при помощи этих тест-систем, интерпретировали как положительные лишь при реакции антител, находящихся в исследуемом субстрате, по крайней мере, с двумя антигенами, тогда как при наличии реакции лишь с одним из антигенов результат считали неопределенным. Было установлено, что специфичность второго поколения тест-систем зависела от источника антигенов. В 1993 году на рынке появилось третье поколение тест-систем. В дополнение к вышеупомянутым антигенам в этих тест-системах используются также антигены, аминокислотная последовательность которых соответствует иммунодоминантным участкам NS5 белков.
В тест-системах первого, второго и третьего поколений в качестве антигенов использовались или рекомбинантные, или синтетические пептиды. В настоящее время можно выделить также тест-системы четвертого поколения, в которых в качестве иммуносорбента используют сочетания рекомбинантных и синтетических пептидов.
Опыт применения тест-систем различных поколений в мире очень большой. Было установлено, что если с помощью тест-систем первого или второго поколения у больных с острым вирусным гепатитом С антитела выявляли на 10-16, а в ряде случаев и 25-30 неделе от начала заболевания, то диагностикумы третьего поколения позволяли сократить этот срок до 2-3 недель. Согласно обобщенным данным чувствительность тест-систем первого, второго и третьего поколений составляет соответственно 70-80%, 92-95% и 97%.
В то же время, по данным С. Colin, 2001, чувствительность тест-систем третьего поколения составила 98,9% у пациентов с хроническими заболеваниями печени и 97,2% на специальных контрольных панелях сывороток. Достижение высокой чувствительности иммуноферментных тест-систем 3 и 4 поколения сопряжено с некоторыми проблемами в обеспечении специфичности исследований, что в ряде случаев может приводить к появлению ложноположительных результатов. В литературе имеются данные о возможных погрешностях в специфичности ELISA 3 тест-систем. Они являются общими для всех ELISA тест-систем, включая тест-системы для диагностики СПИДа.
Ложнопозитивные результаты могут быть следствием повышенного содержания в образцах гамма-глобулинов (сыворотки пациентов африканской расы, миеломная болезнь, ревматоидные факторы), заболеваний печени (цирроз, рак), аутоиммунных заболеваний (коллагенозы, аутоиммунные гепатиты), других вирусных инфекций (ВИЧ, гепатит В) и длительного хранения сывороток в меняющихся температурных условиях. Проведение какой-либо иммунизации также может сопровождаться повышением частоты ложнопозитивных реакций. Рекомендуемые в настоящее время меры по устранению этой проблемы следующие: а) повторная постановка образца в этой же ИФТС; б) повторная детекция anti-HCV в другой ИФТС; в) использование подтверждающих тестов на основе ИФА и иммуноблота.
Однако использование предлагаемых способов подтверждения результатов зачастую приводят к расхождениям в их итоговой трактовке, что показано исследованиями российских и зарубежных исследователей.
В настоящее время производители ИФТС для детекции anti-HCV достигают высокой чувствительности или за счет более полного выявления антител к NS3 или антител к антигенам core. Сравнительные исследования, выполненные на различных группах риска и специальных контрольных панелях показали, что тест-системы, лучше выявлявшие антитела к NS3, оказались несколько более чувствительными, чем тест-системы, лучше выявлявшие антитела к антигенам core. Их чувствительность составляла, соответственно 99,9% и 98,6%.
Диагностика гепатитов В и С у гематологических больных - анализы, особенности
Современная этиологическая диагностика вирусных гепатитов основана на обнаружении специфических маркеров соответствующих вирусов. Один из методов их выявления — тестирование различных антигенов вируса и антител к ним в ИФА. Наиболее прогрессивна и информативна так называемая генная диагностика: обнаружение вирусной РНК или ДНК с помощью ПЦР.
Для диагностики гепатита В в ИФА исследуют:
1) HBsAg-поверхностный антиген гепатита В, ранее называвшийся австралийским. Он указывает на факт инфицированности гепатитом В;
2) HbeAg — антиген инфекционности, свидетельствующий об активной вирусной репликации;
3) анти-НВс —антитела к ядерному антигену вируса гепатита В: класса IgM—ранние антитела острого периода, класса IgG—поздние антитела к ядерному антигену;
4) анти-НВе — антитела к HBeAg, чаще всего характеризующие прекращение активной репликации вируса (так называемая сероконверсия);
5) анти-HBs—антитела к HBsAg, обеспечивающие протективный иммунитет.
С помощью ПЦР для диагностики гепатита В тестируют ДНК вируса гепатита В — основного маркера репликации вируса.
Для диагностики гепатита С исследуют:
1) с помощью ИФА наличие анти-HCV-антител к вирусу гепатита С (для их выявления желательно использовать тест-системы второго — третьего поколения, отличающиеся большей специфичностью). Они указывают только на инфицированность вирусом гепатита С;
2) с помощью ПЦР наличие РНК вируса гепатита С — основного маркера репликации вируса.
Говоря о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями (ОГЗ), следует рассмотреть вопрос о применимости стандартных подходов к выявлению различных маркеров этих вирусов у данного контингента в связи с возможным нарушением процесса антителообразования на фоне глубокой иммуносу-прессии, развивающейся в ходе полихимиотерапии (ПХТ).
Исследования, в которых сделана попытка подтвердить или опровергнуть роль антительных маркеров у пациентов с онкологическими гематологическими заболеваниями, пока единичны.
Так, в отдельных работах сообщается, что при гепатите В иммуносупрессия нарушает обычную последовательность обнаружения в сыворотке крови антигенов и антител: у больных, которые до начала ПХТ были анти-НВs-позитивными, в процессе лечения могут вновь определяться HBsAg и HBeAg, свидетельствуя о несостоятельности анти-HBs в качестве протективных антител. Угнетение механизмов, ограничивающих вирусную репликацию, ведет к тому, что виремия нередко достигает высокого уровня.
Если антитела к столбняку, дифтерии и полиомиелиту сохраняются во время и после ПХТ, то титры антител к вирусам (ветряной оспы, кори и гепатита В) резко снижаются. Это в большей мере относится к детям с лейкозами, чем с солидными опухолями. Снижение или отсутствие выработки анти-HBs отметили также R. Repp и соавт. и R. Rokicka-Milewska и соавт.. Если при гепатите В эта особенность может отразиться только на ретроспективной диагностике, то для распознавания гепатита С, основанного чаще всего на обнаружении анти-HCV с помощью ИФА, такое положение может иметь принципиальное значение, препятствуя полному и своевременному выявлению всех инфицированных.
Антитела к вирусу гепатита С (анти-HCV) вообще образуются медленно, в течение 8—15 нед от момента инфицирования, но у иммунокомпетентных лиц персистируют в организме длительно и в большинстве случаев пригодны для выявления гепатита С, являясь в настоящее время рутинным и скрининговым маркером.
Некоторые авторы, проводившие немногочисленные и небольшие по объему исследования у иммунокомпрометированных пациентов, указывают на возможность отсроченного образования антител к вирусу гепатита С и считают недостаточным использование только ИФА для диагностики данного заболевания у этого контингента пациентов. В частности, С. Cornu и соавт. обнаружили, что у 5 из 6 обследованных ими иммунокомпрометированных пациентов анти-HCV начали обнаруживаться лишь спустя 14 мес и более от момента инфицирования, установленного с помощью ПЦР.
По данным М. Arico и соавт., антительная диагностика позволяет выявить около 70 % детей с ОЛЛ, инфицированных вирусом гепатита С. Значение ПЦР в выявлении пациентов, инфицированных вирусами гепатитов В и С, продемонстрировано при обследовании турецких детей: у 13,9 % больных с онкологическими гематологическими заболеваниями диагноз гепатита В установлен только при обнаружении ДНК вируса гепатита В, а 5,8 % анти-HCV-негативных детей оказались инфицированными вирусом гепатита С при тестировании РНК.
В то же время синтез анти-НВс IgM, сопутствующий в иммунокомпетентном организме вирусной репликации и являющийся одним из ее маркеров, у пациентов с онкологическими гематологическими заболеваниями почти отсутствует, а у пациентов без онкологических гематологических заболеваний происходит их активная наработка (7,7 % против 78,6 %).
С общебиологической точки зрения, выявленные феномены ждут объяснения, а в прикладном плане они демонстрируют особенности специфической диагностики инфицированности вирусом гепатита В у больных с онкологическими гематологическими заболеваниями и необходимость поиска других подходов к распознаванию болезни. Этой цели служит использование ПЦР, которая позволяет существенно повысить выявляемость пациентов с онкологическими гематологическими заболеваниями, инфицированных вирусом гепатита В: в 16 % случаев обнаружение ДНК этого вируса было единственным маркером инфицирования.
Более того, у 50 % детей, находившихся на полихимиотерапии и позитивных по каким-либо маркерам вируса гепатита В, вирусная ДНК выявлялась в отсутствие HBeAg, т. е. была единственным показателем репликации вируса, в то время как среди детей без онкологических гематологических заболеваний подобная ситуация встречалась лишь в 14,5 % случаев, т. е. в 3,5 раза реже.
При гепатите С также не обнаружено параллелизма между выявлением анти-HCV и РНК вируса гепатита С. Весьма демонстративным было преимущество тестирования РНК перед антительной диагностикой: у 44,4 % детей с онкологическими гематологическими заболеваниями РНК вируса гепатита С оказалась единственным маркером инфицирования.
Как и при гепатите В, диагностическая значимость генных и антительных маркеров зависит от фазы ПХТ. Период интенсивного и поддерживающего лечения онкологического гематологического заболевания при гепатите С — это время абсолютной репликативной активности и резкого снижения антителообразования, способность к которому частично восстанавливается по завершении полихимиотерапии. В наших наблюдениях у 74,9 % детей это сопровождалось продолжением вирусной репликации.
Практические выводы о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями сводятся к следующему:
1) рутинные подходы недостаточны для распознавания инфицированности пациентов с онкологическими гематологическими заболеваниями вирусами гепатитов В и С;
2) необходимо комплексное исследование всего известного спектра маркеров;
3) ведущую, определяющую роль в диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями играет тестирование ДНК вируса гепатита В и РНК вируса гепатита С в ПЦР;
4) только путем внедрения ПЦР-диагностики в учреждениях для больных с онкологическими гематологическими заболеваниями можно обеспечить полную и своевременную диагностику гепатитов В и С;
5) обязательность обследования всех пациентов с помощью современных маркеров:
— при поступлении;
— при повышении активности АЛТ на этапах ПХТ;
— каждые 3—6 мес в ходе и в течение года после ПХТ.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
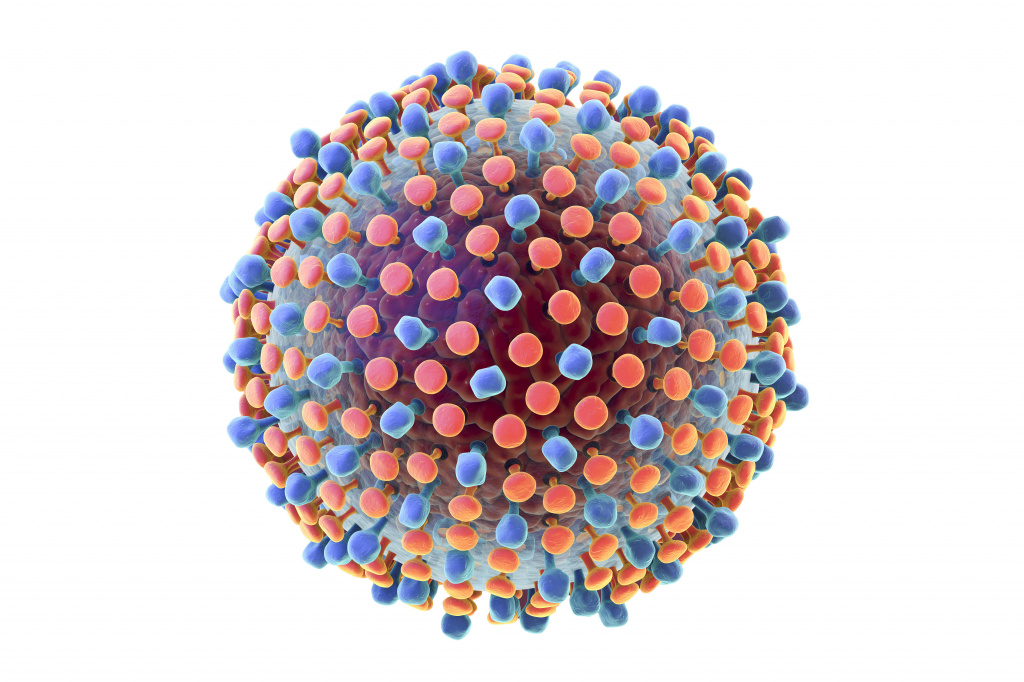
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

