Есть ли прививка от чумы для человека
Обновлено: 23.04.2024
Чумная болезнь вызывается зоонозной бактерией Yersinia pestis, обнаруживаемой обычно в организме мелких млекопитающих и в обитающих на них блохах. Между животными инфекция передается блохами. Заражение человека может иметь место в результате:
- укуса инфицированной блохи – переносчика болезни;
- незащищенного контакта с инфицированными биологическими жидкостями или зараженными материалами;
- вдыхания инфицированных мелких частиц/мелкодисперсных капель, выдыхаемых пациентом с легочной формой чумы (воздушно-капельным путем).
У человека чума, особенно ее септическая (в результате попадания бактерий в кровоток) и легочная формы, без лечения может быть очень тяжелым заболеванием с коэффициентом летальности 30-100%. Без раннего начала лечения легочная форма всегда приводит к смерти. Она носит особенно контагиозный характер и способна вызывать тяжелые эпидемии, передаваясь от человека человеку воздушно-капельным путем.
Признаки и симптомы
У человека, заразившегося чумой, по прошествии инкубационного периода от 1 до 7 дней обычно развивается острое лихорадочное состояние. Типичными симптомами являются внезапное повышение температуры, озноб, головная боль и ломота в теле, а также слабость, тошнота и рвота.
В зависимости от пути проникновения инфекции различаются две основные формы чумной инфекции: бубонная и легочная. Все формы чумы поддаются лечению, если выявляются достаточно рано.
Где встречается чума?
Как болезнь животных чума встречается повсеместно, за исключением Океании. Риск заболевания чумой человека возникает тогда, когда отдельно взятая популяция людей проживает на месте, где присутствует естественный очаг чумы (т.е. имеются бактерии, животные резервуары и переносчики).
Эпидемии чумы случались в Африке, Азии и Южной Америке, однако с 1990-х годов большая часть заболеваний человека чумой имела место в Африке. К трем наиболее эндемичным странам относятся: Мадагаскар, Демократическая Республика Конго и Перу. На Мадагаскаре случаи бубонной чумы регистрируются практически каждый год во время эпидемического сезона (сентябрь-апрель).
Диагностика чумы
Для подтверждения диагноза чумы требуется лабораторное тестирование. Образцовым методов подтверждения наличия чумы у пациента является изоляция Y. pestis из образца гноя из бубона, образца крови или мокроты. Существуют разные методы выявления специфического антигена Y. pestis. Одним из них является лабораторно валидированный экспресс-тест с использованием тест-полоски. Этот метод сегодня широко применяется в странах Африки и Южной Америки при поддержке ВОЗ.
Лечение
Профилактика
Профилактические меры включают в себя информирование населения о наличии зоонозной чумы в районе их проживания и распространение рекомендаций о необходимости защищать себя от укусов блох и не касаться трупов павших животных. Как правило, следует рекомендовать избегать прямого контакта с инфицированными биологическими жидкостями и тканями. При работе с потенциально инфицированными пациентами и сборе образцов для тестирования следует соблюдать стандартные меры предосторожности.
Вакцинация
ВОЗ не рекомендует проводить вакцинацию населения, за исключением групп повышенного риска (например, сотрудников лабораторий, которые постоянно подвергаются риску заражения, и работников здравоохранения).
Борьба со вспышками чумы
Эпиднадзор и контроль
Для осуществления эпиднадзора и контроля необходимо проводить обследование животных и блох, вовлеченных в чумной цикл в регионе, а также разработку программ по контролю за природными условиями, направленных на изучение природного зоонозного характера цикла инфекции и ограничение распространения заболевания. Активное продолжительное наблюдение за очагами проживания животных, сопровождаемое незамедлительными мерами реагирования во время вспышек заболевания среди животных, позволяет успешно уменьшить число вспышек заболевания чумой среди людей.
Для эффективного и результативного реагирования на вспышки чумы важным условием является наличие информированных и бдительных кадров здравоохранения (и местного сообщества), что позволит быстро диагностировать случаи болезни и оказывать надлежащую помощь инфицированным, выявлять факторы риска, вести непрерывный эпиднадзор, бороться с переносчиками и их хозяевами, лабораторно подтверждать диагнозы и передавать компетентным органам информацию о результатах тестирования.
Ответные действия ВОЗ
Целью ВОЗ является предупреждение вспышек чумы путем проведения эпиднадзора и оказания содействия странам повышенного риска в разработке планов обеспечения готовности. Поскольку резервуар инфекции среди животных может быть разным в зависимости от региона, что оказывает влияние на уровень риска и условия передачи инфекции человеку, ВОЗ разработала конкретные рекомендации для Индийского субконтинента, Южной Америки и стран Африки к югу от Сахары.
ВОЗ сотрудничает с министерствами здравоохранения для оказания поддержки странам, где происходят вспышки заболевания, в целях принятия на местах мер по борьбе со вспышками.
Со времен первых эпидемий чумы врачи-практики спорили о том, можно заразиться чумой от больного или нет и если можно, то каким способом. Мнения высказывались противоречивые. С одной стороны, утверждалось, что прикосновение к больным и их вещам опасно. С другой стороны, близость к больным, нахождение на инфицированной территории считались безопасными. Ясного ответа не было, поскольку втирание гноя больного в кожу или ношение его одежды далеко не всегда приводило к заражению.
Многие врачи усматривали связь между чумой и малярией. Первый опыт по самозаражению чумой провел в городе Александрия в 1802 году английский врач А. Уайт. Он хотел доказать, что чума может вызвать приступ малярии. Уайт извлек гнойное содержимое бубона чумной больной и втер себе в левое бедро. Даже когда на его собственном бедре появился карбункул и лимфатические узлы начали увеличиваться, врач продолжал утверждать, что заболел малярией. Лишь на восьмой день, когда симптомы стали очевидными, он поставил себе диагноз чумы и был доставлен в госпиталь, где и скончался.
Сейчас понятно, что от человека к человеку чума передается в основном воздушно-капельным путем, поэтому больные, особенно легочной формой чумы, представляют огромную опасность для окружающих. Также возбудитель чумы может проникнуть в организм человека через кровь, кожу и слизистые оболочки. Хотя причина болезни долгое время оставалась невыясненной, врачи давно искали способы защиты страшного заболевания. Задолго до начала эры антибиотиков, с помощью которых сегодня чуму довольно успешно вылечивают, и вакцинопрофилактики они предлагали различные способы повышения устойчивости организма к чуме.
Трагически закончился эксперимент, проделанный в 1817 году австрийским врачом А. Розенфельдом. Он уверял, что снадобье, приготовленное из костного порошка и высушенных лимфатических желез, взятых из останков умерших от чумы, при приеме внутрь полностью защищает от болезни. В одном из госпиталей Константинополя Розенфельд заперся в палате с двадцатью больными чумой, предварительно приняв рекламируемый им препарат. Сначала все шло хорошо. Шесть недель, отведенные для проведения эксперимента, заканчивались, и исследователь уже собирался покинуть госпиталь, когда внезапно заболел бубонной формой чумы, от которой и скончался.

Создатель первой в мире вакцины от чумы Владимир Хавкин проводит вакцинацию местного населения. Калькутта, 1893 год
Поиски средств профилактики и лечения чумы продолжались. Первую лечебную противочумную сыворотку приготовил Иерсен. После инъекции сыворотки больным чума протекала в более легкой форме, число смертельных случаев снижалось. До открытия антибактериальных препаратов эта вакцина была главным терапевтическим средством в лечении чумы, но при наиболее тяжелой, легочной, форме заболевания она не помогала.

В это же время на островах Ява и Мадагаскар французские ученые Л. Оттен и Г. Жирар тоже вели работы по созданию живой вакцины. Жирару удалось выделить штамм чумного микроба, который спонтанно потерял вирулентность, то есть перестал быть опасным для человека. Вакцину на основе этого штамма ученый назвал инициалами погибшей на Мадагаскаре девочки, у которой он был выделен, – EV. Вакцина оказалась безвредной и высоко иммуногенной, поэтому штамм ЕV и по сей день используется для приготовления живой противочумной вакцины.
Новую вакцину против чумы создал научный сотрудник Иркутского научно-исследовательского противочумного института Сибири и Дальнего Востока В.П. Смирнов, участвовавший в ликвидации 24 локальных вспышек чумы за пределами нашей страны. На основании многочисленных опытов на лабораторных животных он подтвердил способность микроба чумы вызывать легочную форму болезни при заражении через конъюнктиву глаза. Эти эксперименты легли в основу разработки конъюнктивального и комбинированного (подкожно-конъюнктивального) методов вакцинации против чумы. Чтобы убедиться в эффективности предложенного им метода, Смирнов сделал себе инъекцию новой вакцины и одновременно инфицировал себя вирулентным штаммом наиболее опасной, легочной, формы чумы. Для чистоты эксперимента ученый категорически отказался от лечения. На 16-й день после самозаражения он покинул изолятор. По заключению врачебной комиссии Смирнов перенес кожно-бубонную форму чумы. Эксперты констатировали, что предложенные В.П. Смирновым методы вакцинации оказались эффективными. Впоследствии в Монгольской Народной Республике при ликвидации вспышки чумы этими методами было привито 115 333 человека, из которых заболели лишь двое.
К 120-летию открытия А. Йерсеном и Ш. Китазато микроба чумы Yersinia pestis
Об авторе
Виктор Васильевич Сунцов — доктор биологических наук, ведущий научный сотрудник Института проблем экологии и эволюции им. А. Н. Северцова РАН. Занимается изучением происхождения и эволюции возбудителей природноочаговых инфекций, в частности чумы.
Диаграмма публикаций по проблеме чумы, фиксирующая скачок их числа с 2003 г.
Немного истории
Карта распространения чумы в Европе. Пандемия, начавшаяся в центральных районах Азии, достигла берегов Черного моря в 1347 г.
Когда появился микроб чумы?
Доказанное в 1980 г. молекулярными методами непосредственное родство псевдотуберкулезного (Y. pseudotuberculosis) и чумного (Y. pestis) микробов привело к выводу об их недавней дивергенции, правда, без указания времени и места, когда именно и где это случилось [5]. Высокое сходство их геномов позволяло некоторым авторам даже объединить их в один вид в качестве отдельных подвидов, хотя вызывают они совершенно разные болезни. И псевдотуберкулезного, и чумного микробов относят к семейству Enterobacteriaceae — возбудителям кишечных инфекций, но последний, будучи паразитом крови, не имеет к ним никакого отношения. У него иная адаптивная среда, и в принципе его нужно отнести к другому семейству [3].
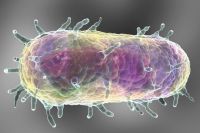
Микрофотография чумной палочки. Увел. ×200. Фото с сайта cdc.gov
Идея недавнего отделения чумного микроба от псевдотуберкулезного была неожиданной, но отнюдь не новой. В 1950–1970-х годах такие мысли высказывали В. Н. Беклемишев, В. А. Бибикова, А. И. Дятлов, Л. Н. Классовский, В. С. Петров, Н. М. Хрусцелевская. Но тогда подобные интуитивные ощущения эволюционной молодости возбудителя чумы выглядели теоретически чуждыми, паранаучными и деструктивными, поэтому они не нашли поддержки у ортодоксов.
Головокружение от успехов
В современных исторических реконструкциях в биологии доминирует новая филогенетика (молекулярная филогенетика, генофилетика). Отчасти это лидерство оправдано широкими возможностями, которые предоставляют молекулярные структуры и компьютерные технологии филогенетических построений, позволяющие сравнивать и обрабатывать миллионы признаков, — таких, как последовательности нуклеотидов. Все составляющие новой филогенетики полезны, они необходимы для создания естественных филогенетических схем, но недостаточны, особенно в отношении прокариот. Молекулярная генетика — молодая наука, и закономерности молекулярной эволюции пока не вполне ясны. Филогении можно выстраивать только по гомологичным признакам, а их выявление, в том числе и на молекулярном уровне, представляет немалую проблему. Выводы на основе применения разных молекулярно-генетических методов далеко не однозначны, порой не согласуются между собой и с данными других наук: экологии, биогеографии, микробиологии и др. Такая обескураживающая разноголосица свойственна и заключениям в отношении микроба чумы.
Происхождение Yersinia pestis: взгляд натуралиста
Знание экологии монгольского сурка и его блох позволяет понять селективные (адаптационные) процессы, проходившие в микробных популяциях в природе, и причинно-следственные связи в эволюционных филумах. Появление возбудителя чумы в Центральной Азии предопределили два природных фактора: аридность горно-степных ландшафтов, постепенно увеличивающаяся с олигоцена-миоцена, и максимальное похолодание в сартанское время последнего оледенения. Проще говоря, индуктором видообразования микроба чумы был сухой и холодный климат Центральной Азии в конце ледниковой эпохи. Кроме того, в возникновении чумного микроба важную роль играет физиология, точнее поведение монгольского сурка, связанное с устройством зимовочной пробки, а также особенности сурочьей блохи O. silantiewi.
В Центральной Азии, в горно-степных поселениях сурка тарбагана влажность почвы очень низкая, всего 2–7% [3], а грунт в зимовочной норе зверька сухой и щебнистый. Изготовить из него земляную пробку внутри норы, в вертикальном лазе диаметром 15–20 см, все равно, что замазать сухим песком отверстие в потолке размером с футбольный мяч. Из-за дефицита почвенной влаги у монгольского сурка выработалось специфичное поведение. При залегании в спячку он устраивает зимовочную пробку из специально подготавливаемой смеси мелкозема, щебня и влажных каловых масс, которые летом собираются в отнорках (уборных). Для перетаскивания камней, обвалянных в фекалиях, сурки используют зубы, при этом частицы фекалий, а с ними и возбудитель псевдотуберкулеза, попадают в ротовую полость. Итак, во рту спящих тарбаганов — экскременты, а в них — кишечный паразит, микроб псевдотуберкулеза!
Монгольский сурок тарбаган и его зимовочная (постоянная) нора. Вверху: зимовочная пробка, состоящая из смеси мелкозема, щебня и цементирующих их экскрементов (1); гнездовая камера (2); отнорки-уборные, в которых в летние месяцы сурки накапливают строительную смесь (3). Внизу: слой мелкозема и щебня (а); и коренные породы (б), приведены температуры грунта и спящих сурков во время раскопки (февраль 1979 г.)
Сурки — типичные семейно-колониальные животные. Группировки из 2–22 разновозрастных и разнополых зверьков совместно зимуют в одной постоянной, или зимовочной, норе. У каждого зверька в течение зимней спячки более длительные периоды глубокого сна (торпора) чередуются с короткими периодами бодрствования (эутермии). В торпорной фазе температура тела снижается до 2–5°C, в эутермной может достигать нормальной, у активных сурков — около 37°С. За осенне-зимне-весеннее время сурки не вполне синхронно просыпаются до 15 раз, примерно дважды в месяц. Таким образом, каждый зверек в течение периода подземной жизни имеет два гомеостатических состояния, между которыми лежит промежуток физиологической гетеротермии. Отсюда следствие: блохи в холодное время года питаются на сурках, температура тела которых лежит в диапазоне 5–37°C. Обратим внимание на непрерывность температур!
В 1970-х годах в тувинском очаге чумы, расположенном в Центральной Азии, мы изучали зимнюю спячку тарбагана. В феврале-марте, во время максимального зимнего промерзания грунта (до глубины более 2 м), раскопали три зимовочных норы. Из них изъяли восемь глубоко спящих и девять проснувшихся активных зверьков, среди которых были молодые, полувзрослые и взрослые особи. Из их шерсти собрали 230 личинок O. silantiewi, 60 живых и 452 пустых коконов, а из ротовой полости торпидных зверьков — дополнительно 20 личинок. Пустые коконы (от 4 до 87) обнаружили также на 22 зверьках, отловленных в первые две недели после весеннего пробуждения.
Тувинский природный очаг чумы, Монгун-Тайгинский мезоочаг. Снеговое покрытие в зимне-весенние месяцы не превышает 30–40%, грунт промерзает на глубину более 2 м к началу января, а оттаивает в июле
Отметим распределение коконов на шерсти: большая часть прикреплена на голове, у основания хвоста и на наружной стороне задних ног. Все личинки, извлеченные из ротовой полости, оказались с кровью и увеличенными в размерах за счет развития жирового тела, что свидетельствовало о полноценности пищи и об их готовности к окукливанию. У спящих зверьков поврежденная личинками слизистая ротовой полости и язык обильно кровоточили, изо рта заметно выступала кровяная пена, а рот, зубы, лапы были обильно испачканы экскрементами (следами устройства зимовочной пробки осенью). Незарубцевавшиеся раны в ротовой полости мы наблюдали у всех сурков, отловленных после выхода из нор в конце марта и начале апреля, что говорит о массовости описываемого явления, его общепопуляционном характере.
Отсюда понятна причина концентрации пустых коконов на голове, хвосте и наружной стороне задних ног у спящих и недавно пробудившихся сурков тарбаганов. Зимой грунт промерзает глубже гнездовых камер, и личинки переходят из гнездовой выстилки на более теплые тела спящих зверьков. При этом некоторые личинки, произвольно перемещаясь в шерсти, попадают в ротовую полость сурка, где, питаясь на слизистой, травмируют ее. Перед окукливанием личинки покидают ротовую полость и прикрепляются к шерсти близ рта. Зная позу свернувшегося в шар спящего сурка, у которого нос уткнулся в анус, а задние ноги прижаты к щекам, легко предсказать места прикрепления коконов.
На основе новых эколого-географических, палеоклиматических и генетических данных можно сформулировать основные постулаты теории происхождения и мировой экспансии микроба чумы.
Происхождение, естественное распространение в Евразии и антропогенная мировая экспансия микроба Y. pestis во время первой (I), второй (II) и третьей (III) пандемий. 1 — южная граница зоны многолетнемерзлых грунтов; 2 — граница доминантного распространения в природе микроба Y. pseudotuberculosis O:1b; 3 — ареал сурка-тарбагана, район происхождения микроба чумы; 4 — первичные природные очаги; 5 — вторичные природные очаги; gly + (gly − ) — способность (неспособность) штаммов ферментировать глицерин
Предковая форма возбудителя чумы — микроб псевдотуберкулеза 1-го серотипа (Y. pseudotuberculosis O:1b), который доминирует в северо-центрально-азиатских и дальневосточных районах с суровым климатом.
Метаморфоза микроба псевдотуберкулеза в чумную бактерию произошла в конце позднего плейстоцена. За весь четвертичный период глубокое промерзание грунта (2 м и более) в Центральной Азии отмечено только в сартанское время позднего плейстоцена и в голоцене, т. е. не ранее 22 тыс. лет назад [10].
В ультраконтинентальном районе зимнего антициклона в Центральной Азии личинки блох, паразитирующие на монгольском сурке тарбагане, зимой переходят к факультативной гематофагии, что приводит к устойчивому контакту крови сурков с псевдотуберкулезным микробом [3].
Теперь уже можно легко представить, как сапрозоонозный кишечный псевдотуберкулезный микроб постепенно эволюционировал в облигатный паразит крови незимоспящих грызунов: экскременты тарбагана → спящий сурок → активный сурок → незимоспящий грызун.
Знание молекулярно-генетических, популяционных и биоценотических факторов, а также их многообразных связей позволяет выделить в эволюционной истории возбудителя чумы основные вехи.
IV. Во время третьей пандемии с корабельными крысами микроб уже другого подвида (orientalis) из Азии вновь проник в Африку и впервые на быстроходных морских судах добрался до Нового Света, где закрепился в виде вторичных природных очагов в популяциях земляных белок, луговых собачек, полевок, морских свинок.
В поисках согласия
Экологический сценарий происхождения, эволюции и мировой экспансии возбудителя чумы весьма заметно расходится с гипотезами, построенными на основе генетических данных. Где же истина? Какой из них достоин большего одобрения?
В пользу экологического сценария говорит следующее:
Такие аргументы делают этот экологический сценарий наиболее правдоподобным в сравнении с другими, позволяют принять его за исходную гипотезу и наполнять его генетическими признаками. Биологическое содержание сценария, понятное широкому кругу исследователей, дает существенные гносеологические преимущества перед слишком редуцированными историческими реконструкциями. К примеру, некоторые авторы из-за сходства отдельных генетических признаков у кавказского подвида Y. pestis caucasica и псевдотуберкулезного микроба считают Кавказ родиной чумы и выстраивают соответствующую филограмму [11, 12]. Но на Кавказе, в относительно теплом климатическом регионе, нет псевдотуберкулезного микроба 1-го серотипа или он встречается крайне редко! Истоки чумы следует искать в холодных, суровых краях — как в предложенном сценарии.
Несмотря на разительное несходство экологической и генетической филогений, между ними нет непреодолимой пропасти, более того, есть безусловные точки соприкосновения. Экологический сценарий для молекулярных и генетических признаков очерчивает диапазон генетической изменчивости микробной популяции, вступившей на путь видообразования, выделяет рамки экологической достоверности генетических фактов, привлекаемых для филогенетических выводов [3, 13].
В китайском автономном районе Внутренняя Монголия, расположенном на севере страны и граничащем с Монголией и Россией, объявлен третий уровень эпидемиологической угрозы из-за бубонной чумы. До 2021 года там будут усилены меры безопасности.
Местные власти рекомендуют жителям избегать мест обитания грызунов, переносящих заболевание. Также предписывается обращаться в больницу в случае недомогания и высокой температуры.
Ранее в западной части Монголии, граничащей с КНР и российской Республикой Алтай, выявили два случая заражения бубонной чумой. Были госпитализированы два человека — 27-летний мужчина и девушка, которая на момент появления первых симптомов болезни непосредственно контактировала с 60 людьми. Монгольские власти заявили, что приняли все требуемые меры для того, чтобы не допустить проникновения чумы в соседние регионы и страны.
Что за болезнь бубонная чума?
Чумная палочка вызывает три различных вида чумы: бубонную, септическую и легочную. Бубонная чума распространяется через зараженных блох, живущих на тарбаганах, или монгольских сурках. Кроме того, подхватить инфекцию можно при поедании сырого мяса или его разделке.
Инкубационный период обычно составляет 2-6 дней. Если в ходе чумы развивается пневмония, то передача заболевания может происходить и воздушно-капельным путем.
В настоящее время болезнь лечат антибиотиками. При своевременном лечении в современных условиях смертность от бубонной чумы составляет не более 10 %, при других формах чумы смертность зависит от скорости начала лечения.
Существует ли прививка от бубонной чумы?
Впервые вакцину, эффективную против бубонной чумы, создал в начале XX века бактериолог, иммунолог и эпидемиолог Владимир Хавкин из убитых температурой чумных палочек. Живую вакцину против чумы создала и испытала на себе в 1934 году советский бактериолог Магдалина Покровская.
Сегодня для профилактики заболевания используется Вакцина чумная живая (Live plague vaccine). Она представляет собой живую культуру вакцинного штамма чумного микроба Yersinia pestis EV, высушенную методом лиофилизации в стабилизирующей среде. Вакцина вызывает развитие иммунитета к чуме длительностью до одного года.
Кого и как прививают от бубонной чумы?
Прививкам подлежат дети с двух лет и взрослые, проживающие на энзоотичных по чуме территориях, а также лица, работающие с живыми культурами возбудителя заболевания.
Вакцинацию проводят однократно подкожным, накожным, внутрикожным или ингаляционным способами и перорально, а ревакцинацию осуществляют через один год, при неблагоприятной эпидемической обстановке — через шесть месяцев. После вакцинации возможны недомогание, головная боль, повышении температуры до 38,5°С, реже до 40°С (при ингаляционном применении), тошнота, рвота. Продолжительность реакции может составлять 1-3 суток.

Прививку нельзя делать при острых инфекционных и неинфекционных заболеваниях, хронических заболеваниях в фазе обострения (вакцинацию проводят не ранее чем через месяц после выздоровления), на фоне лечения стероидными препаратами, при системных заболеваниях соединительной ткани, злокачественных новообразованиях и злокачественных заболеваниях крови, аллергических заболеваниях (бронхиальная астма, анафилактический шок, отек Квинке в анамнезе), беременности и т. д. Не допускается применение вакцины в сочетании с некоторыми антибиотиками, а также в течение 14 дней после других прививок.
Во Всемирной организации здоровья (ВОЗ) не рекомендуют проводить вакцинацию населения от чумы, за исключением групп повышенного риска (например, сотрудников лабораторий, которые постоянно подвергаются риску заражения, и работников здравоохранения).
Читайте также:

