Это как вирус а вакцины просто нет
Обновлено: 19.04.2024
Главная задача биологии — это развитие представлений у человека о живых организмах, о многообразии видов, обо всех закономерностях развития живых существ, а также об их взаимодействии с окружающей природой. Предмет основы безопасности жизнедеятельности (ОБЖ) позволяет получить знания и умения, которые помогут сохранить жизнь и здоровье в опасных ситуациях. Эти ситуации всегда возникают неожиданно, но, тем не менее, большинство из них предсказуемы и к ним можно подготовиться заранее. ОБЖ учит нас предвидеть возможные опасности и минимизировать потери от той или иной ситуации. Сегодня мы сталкиваемся с новым видом вирусной опасности COVID-19,о котором поговорим с точки зрения биологии и ОБЖ.
Что такое вирус?
Вирус — это неклеточный инфекционный агент. Сегодня нам известно около 6 тысяч различных вирусов, но их существует несколько миллионов. Вирусы не похожи друг на друга и могут иметь как форму сферы, спирали, так и форму сложного асимметричного сплетения. Размеры вирусов варьируются от 20 нм до 300 нм.
Как устроен вирус?
В центре агента находится генетический материал РНК или ДНК, вокруг которого располагается белковая структура — капсид.
Капсид служит для защиты вируса и помогает при захвате клетки. Некоторые вирусы дополнительно покрыты липидной оболочкой, т.е. жировой структурой, которая защищает их от изменений окружающей среды.
Вирусолог Дэвид Балтимор объединил все вирусы в 8 групп, из которых некоторые группы вирусов содержат 1-2 цепочки ДНК. Другие же содержат 1 цепочку РНК, которая может удваиваться или достраивать на своей матрице ДНК. При этом каждая группа вирусов производит себя в различных органеллах зараженной клетки.
Вирусы имеют определенный диапазон хозяев, т.е. он может быть опасен для одних видов и абсолютно безвреден для других. Например, оспой болеет только человек, а чумкой только некоторые виды плотоядных. Вирус не способен выжить сам по себе, поэтому активируется только в хозяйской клетке, используя ее ресурсы и питательные вещества. Цель вируса — создание множества копий себя, чтобы инфицировать другие клетки!
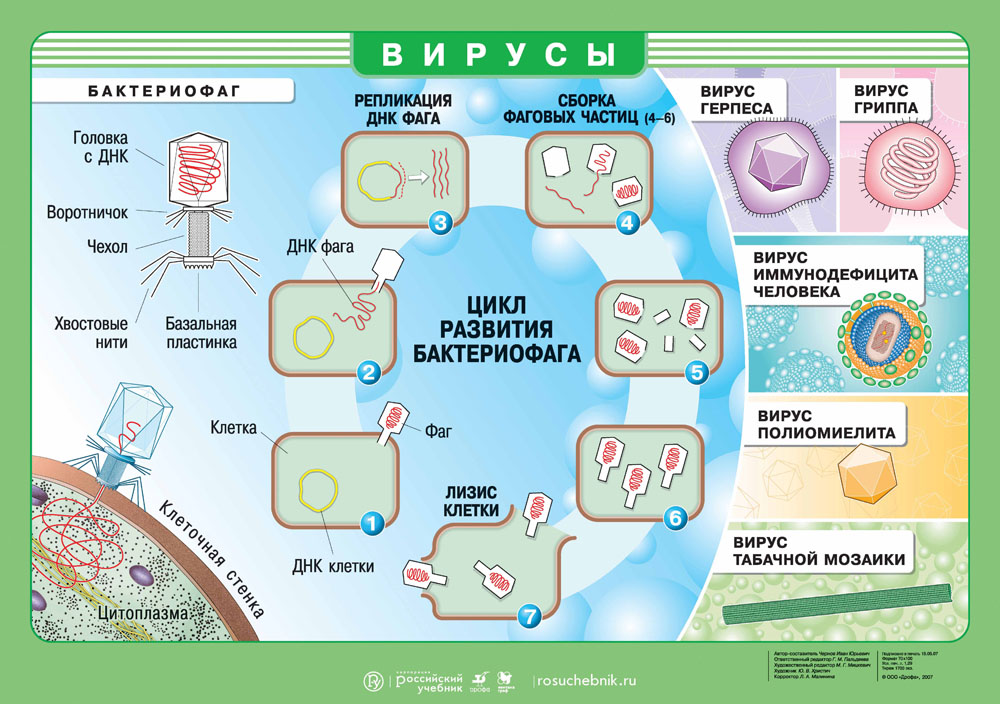
Как вирус попадает в организм?
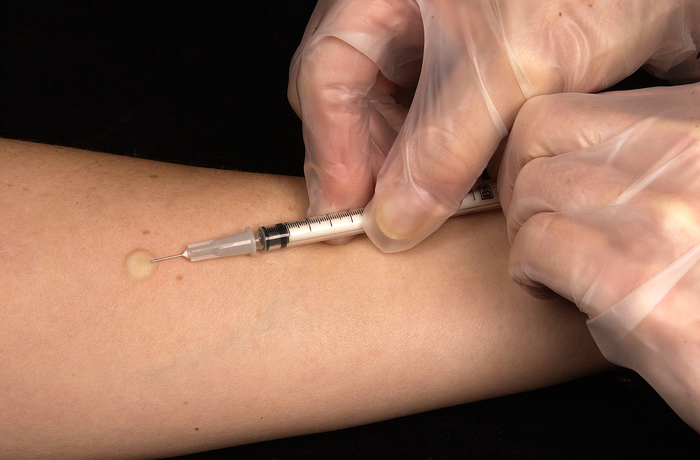
- через физические повреждения (например, порезы на коже)
- путём направленного впрыскивания (к примеру, укус комара)
- направленного поражения отдельной поверхности (например, при вдыхании вируса через трахею)
- к эпителию слизистых оболочек (это например вирус гриппа)
- к нервной ткани (вирус простого герпеса)
- к иммунным клеткам (вирус иммунодефицита человека)

Геном вируса встраивается в одну из органелл или цитоплазму и превращает клетку в настоящий вирусный завод. Естественные процессы в клетке нарушаются, и она начинает заниматься производством и сбором белка вируса. Этот процесс называется репликацией. И его основная цель — это захват территории. Во время репликации генетический материал вируса смешивается с генами клетки хозяина — это приводит к активной мутации самого вируса, а также повышает его выживаемость. Когда процесс репликации налажен, вирусная частица отпочковывается и заражает уже новые клетки, в то время как инфицированная ранее клетка продолжает производство.
Выход вируса
Вирус создал множество собственных копий, клетка оказывается изнуренной из-за использования ее ресурсов. Больше вирусу клетка не нужна, поэтому клетка часто погибает и новорожденным вирусам приходится искать нового хозяина. Это и есть заключительная стадию жизненного цикла вируса.
Скорость распространения вирусной инфекции
Размножение вирусов протекает с исключительно высокой скоростью: при попадании в верхние дыхательные пути одной вирусной частицы уже через 8 часов количество инфекционного потомства достигает 10³, а концу первых суток − 10²³.
Вирусная латентность
Как вирус распространяется?
- воздушно-капельный (кашель, чихание)
- с кожи на кожу (при прикосновениях и рукопожатиях)
- с кожи на продукты (при прикосновениях к пище грязными руками вирусы могут попасть в пищеварительную и дыхательную системы)
- через жидкие среды организма (кровь, слюну и другие)
Почему с вирусами так тяжело бороться?
Сегодня людям уже удалось победить некоторые вирусы, а некоторые взять под жесткий контроль. Например, Оспа (она же черная оспа). Болезнь вызывается вирусом натуральной оспы, передается от человека к человеку воздушно-капельным путем. Больные покрываются сыпью, переходящей в язвы, как на коже, так и на слизистых внутренних органов. Смертность, в зависимости от штамма вируса, составляет от 10 до 40 (иногда даже 70%), На сегодняшний день вирус полностью истреблен человечеством.
Кроме того, взяты под контроль такие заболевания, как бешенство, корь и полиомиелит. Но помимо этих вирусов существует масса других, которые требуют разработок или открытия новых вакцин.
Коронавирус
Виновником эпидемии, распространяющейся сегодня по миру, стал коронавирус, вирусная частица в 0,1 микрона. Свое название он получил благодаря наростам на своей структуре, своеобразным шипам. Внутри вируса спрятан яд, с помощью которого он подчиняет себе зараженный организм. Этот вирус воздействует не только на человека, но и на птиц, свиней, собак и летучих мышей. В настоящий момент выделяют от 30 до 39 разновидностей коронавирусной инфекции. Но для человека патогенно всего 6. И как любой другой вирус COVID-19 мутирует.

К наиболее распространенным симптомам COVID-19 относятся повышение температуры тела, сухой кашель и утомляемость. К более редким симптомам относятся боли в суставах и мышцах, заложенность носа, головная боль, конъюнктивит, боль в горле, диарея, потеря вкусовых ощущений или обоняния, сыпь и изменение цвета кожи на пальцах рук и ног. Как правило, эти симптомы развиваются постепенно и носят слабо выраженный характер. У некоторых инфицированных лиц болезнь сопровождается очень легкими симптомами.
Сколько же может жить этот вирус вне организма? Все зависит от типа вируса и от той поверхности, на которую вирусы попали. В качестве примера было рассмотрено 3 вируса, по которым велись исследования. Изучали время, на которое может задерживаться вирус на различных поверхностях. Данные приведены в таблице.

Поскольку пока не изобретено вакцины от COVID-19, в целях защиты от инфекции самым важным для нас является соблюдение гигиены.
Гигиена — раздел медицины, изучающий влияние жизни и труда на здоровье человека и разрабатывающая меры (санитарные нормы и правила), направленные на предупреждение заболеваний, обеспечение оптимальных условий существования, укрепление здоровья и продление жизни.
Сегодня следует соблюдать определенные правила гигиены:
- Соблюдение режима труда и отдыха, не допускающего развития утомления и переутомления.
- Выполнение условий, обеспечивающих здоровый и полноценный сон (свежий воздух, отсутствие шума, удобная постель, оптимальная продолжительность).
- Правильное здоровое питание в соответствии с потребностями организма.
- Комфортный микроклимат в жилище (температура, влажность и подвижность воздуха, естественная и искусственная освещенность помещений).
- Содержание в чистоте тела и тщательный уход за зубами.
- Спокойное и корректное поведение в конфликтных ситуациях.

Егор Воронин — нью-йоркский вирусолог, специалист в области вакцинопрофилактики. Более двадцати лет он занимался исследованиями ВИЧ, его эволюцией и репликацией. С 2018 по 2020 год он возглавлял биотехнологическую компанию Worcester HIV Vaccine, занимающуюся разработкой вакцины от ВИЧ. В своем блоге shvarz Егор публикует массу интересных фактов о вакцинах, ВИЧ, о вирусах в целом, а в последние полтора года и о новом коронавирусе: он умеет рассказывать простым языком о сложном.
— Наверное, тот факт, что сейчас все следят за вакцинами, позволит объяснить это проще.
— Это единственная проблема?
— Нет. Вторая проблема: как мы все уже знаем в отношении коронавируса — созданные против него вакцины хорошо предотвращают тяжелое течение болезни и смерть, но гораздо хуже защищают от заражения. Для COVID-19, как все же быстротечной болезни, это нормально: даже если вирус попадет в привитый организм, он не вызовет тяжелую болезнь, организм силами иммунной системы быстро его поборет, и человек скоро выздоровеет, вирус исчезнет.
С ВИЧ же совершенно другая ситуация. Он приспособлен к тому, чтобы жить в организме очень долго и ускользать от иммунной системы годами. Если мы не предотвратили его попадание в организм, то без терапии он будет в нем реплицироваться и в конце концов вызовет СПИД. Будучи привитыми от коронавируса, вы можете все равно им заразиться, но лишь чуть-чуть поболеете или даже не заметите, что вирус был, организм его вычистит, — а с ВИЧ это не работает. На ранних этапах разработки вакцин пытались измерять их эффективность именно по способности предотвращать не заражение ВИЧ, а последующее развитие СПИДа, но сейчас уже ясно, что если ВИЧ попал в организм, то без терапии СПИД неизбежно разовьется. Значит, в отношении ВИЧ нам нужна вакцина, которая будет полностью предотвращать само попадание вируса в организм, а это гораздо более высокая планка.
— Но с точки зрения обывателя все кажется просто: есть вирус ВИЧ, он выделен и хорошо известен. Так возьмите его, убейте, и убитый, обезвреженный вирус введите человеку — пусть организм вырабатывает иммунный ответ. Ведь так делались все классические вакцины. На каком этапе оказалось, что с ВИЧ это не работает?
— Над вакциной от ВИЧ работают уже не первый десяток лет. При этом были сделаны какие-то побочные открытия, которые можно применять в других областях? Например, в нынешней борьбе с коронавирусом?
— Попытки создать вакцины от ВИЧ начались сразу же, как только вирус был впервые выделен. Пытались сделать вакцины на основе убитого вируса, на основе рекомбинантных белков, продолжают активно работать над векторными вакцинами. А когда появился COVID-19, практически все мои коллеги, кто занимался вакцинами от ВИЧ, перекинулись в область коронавируса. Я смотрю на научные статьи о коронавирусе — там все знакомые имена.
Я уже упоминал, что технология стабилизации спайкового белка была разработана для ВИЧ, это был один из главных прорывов в вакцинологии за последние десять лет, и она нашла отличное применение в вакцинах от COVID-19.
Известный вирусолог Барни Грэм, который занимался именно стабилизацией вирусного белка у ВИЧ и у респираторно-синцитиального вируса, сыграл важную роль в разработке одной из самых популярных в мире вакцин от COVID-19 компании Moderna.
Мишель Нуссенцвайг, который выделил нейтрализующие антитела к коронавирусу, разработал технологию выделения этих антител в ходе многолетних исследований антител к ВИЧ и вирусу иммунодефицита обезьян. Памела Бьоркман, ведущий специалист Caltech по структуре вирусных белков, раньше изучала в том числе и ВИЧ.
— Это известные имена, но применяются ли отработанные на ВИЧ методики?
— Сами методы тестирования на нейтрализующие антитела были разработаны для ВИЧ, а теперь применяются для COVID-19. В области тестирования вакцин существует огромная сеть клинических центров и лабораторий и в США, и в Африке, и по миру — она была создана для ВИЧ-инфекции, после начала пандемии ее просто взяли и перепрофилировали под коронавирус, а заведуют ею те же самые ученые.
С другой стороны, технологии, нашедшие применение в вакцинах от COVID-19, сейчас интересуют и исследователей ВИЧ: технология мРНК вакцин разрабатывалась и для ВИЧ, но сейчас работы в этой области существенно активизировались.
— Кто-нибудь из российских ученых занимается разработками вакцины от ВИЧ?
— В России разработки вакцин от ВИЧ ведутся, но их немного. Есть три исследовательские группы: в Москве, Петербурге и в Новосибирске. У них есть определенные наработки, но пока они не прошли дальше первой фазы испытаний.
Вопрос в большей мере этический. Раз уж существуют эффективные методы предотвращения ВИЧ-инфекции, то нельзя не делать их доступными участникам клинических испытаний. Но если мы предоставляем их всем участникам клинических испытаний (и плацебо-группе, и группе, получающей вакцину), то количество новых инфекций будет чрезвычайно мало в обеих группах, и эффективность вакцины будет невозможно измерить. Или придется делать испытания еще обширнее и еще длинней, что еще больше повысит их стоимость.
Перспективы разработки вакцины от ВИЧ тают с каждым днем именно потому, что сложно их тестировать, не подвергая людей риску заразиться в ситуации, когда есть готовые способы избежать этого риска. Но нельзя сказать, что ученые полностью потеряли надежду. Уже ведутся активные обсуждения новых подходов к проведению клинических испытаний ВИЧ-вакцин в будущем.
Вакцины — это вообще зачем?

Я не общаюсь с больными, мне можно не прививаться?
по теме

Лечение
Прорыв: ученые создали вакцину против герпеса
От некоторых инфекций действительно нужно прививаться не всем. Например, прививку от желтой лихорадки нужно сделать, если вы собираетесь в Индию, а прививаться от туляремии и бруцеллеза в первую очередь необходимо работникам сельского хозяйства. Однако от большого количества инфекций должны быть привиты все люди, если у них нет индивидуальных медицинских противопоказаний. Это важно для сохранения коллективного иммунитета. Инфекция может распространяться в популяции только при наличии достаточного количества восприимчивых к ней людей.
Если человек привит и не может заболеть, через него инфекция не может распространяться дальше, а если таких людей много — эпидемия затухает вплоть до полного исчезновения болезни. Например, благодаря массовой вакцинации, удалось полностью искоренить натуральную оспу. В середине XX века от оспы привили так много людей по всему миру, что вирусу просто негде было жить, и он исчез. Сейчас оспой никто на планете не болеет, и вакцинация от нее больше не нужна.
Но нельзя вакцинировать все 100% населения — у некоторых есть медицинские противопоказания: аллергия на вакцину или некоторые заболевания. Таких людей может защитить только коллективный иммунитет. Поэтому прививаться нужно не только для сохранения собственного здоровья, но и для сохранения здоровья других людей.
От каких инфекций нужно прививаться всем, а от каких — только в некоторых случаях определено в Национальном календаре профилактических прививок. Он составлен исходя из соотношения потенциальных рисков заболевания инфекциями для разных групп населения и эффективности вакцинации. Также не забывайте проверять рекомендации ВОЗ по вакцинации для отдельных стран перед путешествиями.
В вакцинах же куча всякой химии, а еще и ртуть!
Каждая вакцина проходит многолетние тщательные клинические исследования, доказывающие эффективность и безопасность всех ее компонентов. Содержащий ртуть консервант тиомерсал (он же мертиолят) в современных вакцинах давно не применяют. Кроме того, его концентрация в вакцинах была так мала, что он не мог причинить вред прививаемому человеку. Конечно, каждая вакцина может иметь свои побочные эффекты, но их тяжесть и риск несоизмеримо малы по сравнению с тяжестью самих заболеваний, от которых они защищают.
Да это все не работает, вирусы и бактерии же постоянно мутируют!
Да, возбудители инфекций действительно меняются, как и все живое. Поэтому при разработке вакцины сначала долго изучают и подбирают штаммы возбудителей, чтобы они максимально соответствовали циркулирующим в популяции диким штаммам. Также эффективность вакцины — насколько хорошо она защищает от инфекции — постоянно мониторят на протяжении всего периода ее применения.
по теме

Эпидемия
Как изменит мир вакцина от ВИЧ-инфекции?
Нужно учитывать, что многие возбудители инфекций довольно стабильны. Например, вирус клещевого энцефалита остается неизменным уже десятки тысяч лет, поэтому вакцина от него не требует каких-то доработок, оставаясь эффективной.
Другие возбудители, например, вирус гриппа, меняются очень быстро. В таких случаях используют другую стратегию: перед каждым сезоном Всемирная организация здравоохранения (ВОЗ) строит прогноз, определяя наиболее вероятные штаммы, которые будут вызывать заболевание в грядущем сезоне, и именно эти штаммы используют для производства вакцины. То есть вакцину для профилактики гриппа каждый год делают из новых штаммов возбудителя, поэтому она остается эффективной, несмотря на изменчивость возбудителя.
Я привился от гриппа и все равно заболел.
А почему тогда от простуды до сих пор не сделали вакцину?
Почему нельзя сделать универсальную вакцину от всех инфекций?
Наша иммунная система распознает возбудителя инфекции, реагируя на его отдельные специфические фрагменты — антигены. Как правило, это крупные белковые молекулы, находящиеся на поверхности бактериальной клетки или в оболочке вируса. Именно опознавая эти молекулы, наша иммунная система понимает, с каким возбудителем она столкнулась и как его нейтрализовать.
по теме
Профилактика
В США разработана новая вакцина против туберкулёза
Сейчас существуют комбинированные вакцины, защищающие сразу от нескольких инфекций. В их состав входят характерные молекулы возбудителей разных инфекций, поэтому одна вакцина позволяет познакомить наш иммунитет сразу с пятью — шестью инфекциями и обеспечить защиту от них.
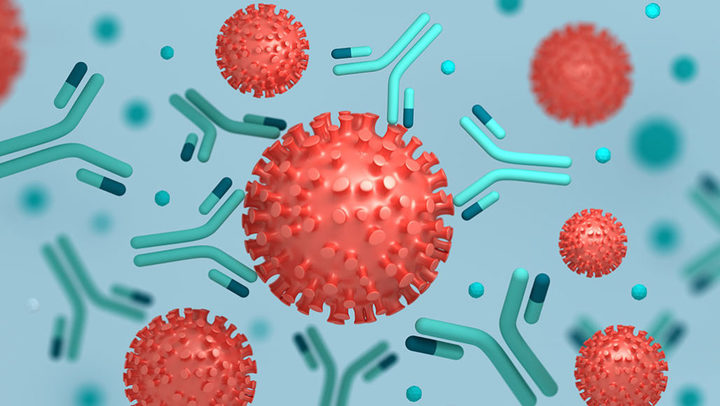
Как организм понимает, какие антитела вырабатывать?
Как антитела вырабатываются при вакцинации?
Продолжительность вакцинного иммунитета тоже зависит от иммунологической памяти и может отличаться от естественного иммунитета, возникшего после болезни. Когда иммунитет угасает, нужно вакцинироваться снова. Для вакцин от разных инфекций есть свои графики повторной вакцинации, их частота зависит от времени хранения иммунологической памяти.
Вакцины, полученные по различной технологии, могут отличаться по времени действия вакцинного иммунитета. Обычно эти различия не слишком велики, так как продолжительность иммунитета в гораздо большей степени зависит от вида самого возбудителя, чем от конкретной вакцины.
На формирование защитного иммунитета также влияет состояние самого организма. Например, при тяжелых заболеваниях иммунной системы (наследственные иммунодефициты, злокачественные новообразования) иммунный ответ на вакцину может быть снижен или не формироваться вообще. Как показывает многолетний опыт использования разных вакцин, в случае ВИЧ-инфекции иммунный ответ на вакцины, как правило, ничем не отличается от иммунного ответа у ВИЧ-негативных людей. Поэтому графики вакцинации и дозы вакцины для ВИЧ-позитивных пациентов не будут иметь никаких особенностей.
по теме
Лечение
Безумно дорогое лекарство, которое спасет мир от пандемии
Некоторые лекарства, например глюкокортикоиды и иммунодепрессанты, могут подавлять формирование вакцинного иммунитета. В таких случаях тактику вакцинации нужно обсудить с врачом.
Для вакцин от новой коронавирусной инфекции время действия вакцинного иммунитета остается одним из главных вопросов. Предсказать продолжительность защиты той или иной вакцины очень трудно. Обычно это выясняют на практике, регистрируя частоту инфекций у привитых во время массовой вакцинации людей спустя разное количество времени, а также измеряя титр защитных антител.
Титр? Какой еще титр?
Так как антитела — это сложные белки, определять их химическими методами крайне трудно. Поэтому для определения антител используют иммунологические реакции. Конкретных методов очень много, но в самом общем виде суть этих реакций очень простая. Мы берем раствор нужного антигена (например, того самого шиповидного белка коронавируса) и смешиваем его с сывороткой, в которой ищем антитела. Если антитела в сыворотке есть, то они связываются с антигеном и их соединение выпадает в виде осадка или раствор мутнеет. На практике проведение такой реакции выглядит сложнее, часто используют специальные гелевые среды и разные способы детектирования, но суть от этого не меняется.
Проблема в том, что такой подход отвечает нам только на вопрос, есть антитела в сыворотке или их нет, но ничего не говорит о количестве самих антител. Как в таком случае сравнить между собой две разные сыворотки? По количеству выпавшего осадка — не вариант, слишком большая погрешность. Но есть другой способ — можно разводить исследуемую сыворотку до тех пор, пока реакция (осадок) все еще будет обнаруживаться. И вот последнее, самое сильное разведение, при котором мы еще можем наблюдать реакцию сыворотки с раствором антигена, и называют титром этой сыворотки. То есть титр 1:50 говорит нам о том, что эту сыворотку можно развести в 50 раз и она еще будет давать реакцию с антигеном. Соответственно, чем больше вторая цифра в обозначении титра, тем выше концентрация антител в сыворотке.
Недостаток титра в том, что он указывает на относительное содержание антител. Если у нас есть две сыворотки с титрами 1:50 и 1:100, мы можем с уверенностью сказать, что во второй сыворотке антител в 2 раза больше, чем в первой. Но какая именно концентрация антител в каждой из этих сывороток, мы не знаем. На практике это часто бывает и не нужно: нам достаточно знать, с каким титром антител человек еще защищен от инфекции, а с каким — уже нет. Это легко выяснить, измеряя титр антител у вакцинированных людей, которые все же заразились.
В результатах лабораторных анализов обычно указывают концентрацию антител в международных единицах (МЕ) или относительных единицах (ОЕ). Результаты, полученные в МЕ, можно сравнивать между собой — значение не будет зависеть от лаборатории, тест-системы и условий анализа (для коронавируса таких пока нет). Результаты, выраженные в ОЕ, можно сравнивать между собой только для тестов одной марки, при этом сама лаборатория и время анализа роли не играют, то есть можно отслеживать динамику изменения уровня антител у одного человека.
Чтобы понять, нужна ли вакцина и подействовала ли она, достаточно измерить уровень антител? Какой нужен для ковида?
К сожалению, все немного сложнее. Антитела отвечают за гуморальный иммунитет — и это только лишь часть нашей иммунной системы. Помимо гуморального, есть еще клеточный иммунитет, работа которого не зависит от уровня антител. При защите от разных инфекций разные звенья иммунитета играют неодинаковые роли. В каких-то случаях ведущую роль имеет гуморальный иммунитет и антитела (например, в случае гепатита В, гриппа, столбняка и многих других инфекций). В других случаях — ведущая роль у клеточного иммунитета, например, при туберкулезе. По новой коронавирусной инфекции пока слишком мало данных, чтобы делать выводы о важности каждого из звеньев иммунитета и необходимом уровне антител. То есть даже если вы сделаете тест на антитела, эта информация практически ничего не даст по ряду причин.
Если вы еще не вакцинировались и тест на антитела будет положительным, что говорит о перенесенной инфекции в бессимптомной форме, это все равно не является противопоказанием к вакцинации. Мы не знаем, какова продолжительность естественного иммунитета, так что вакцина может продлить или усилить защиту.
Если вы делаете тест на антитела после вакцинации, сейчас нет надежных данных, с которыми можно было бы соотнести полученные результаты и сделать вывод о том, подействовала ли вакцина. Другими словами, пока никто не знает, сколько должно быть антител после вакцинации, чтобы гарантировать надежный уровень защиты. Плюс уровень антител ничего не говорит о состоянии клеточного иммунитета, а он тоже может быть очень важен для защиты.
Если вы наблюдаете за динамикой концентрации антител после вакцинации и видите ее снижение, это еще не говорит о снижении уровня защиты. Как мы выяснили выше, падение концентрации антител в крови с течением времени — это нормальное явление, а долговременную защиту обеспечивает иммунологическая память, которая с концентрацией антител не связана.
Не все антитела одинаково полезны
Для характеристики антител важно понимать их класс, тип и с каким антигеном они связываются.
Антитела бывают разных классов (A, M, G, E и др.). Основной класс защитных антител — G, в лабораторных исследованиях и тестах их обычно обозначают IgG. Наличие этих антител в крови говорит о наличие иммунитета после вакцинации или перенесенного заболевания. IgM — тоже защитные антитела, которые начинают вырабатываться первыми, раньше, чем IgG. Обычно IgM менее эффективны, чем IgG, и почти полностью исчезают к концу заболевания. Наличие этих антител обычно указывает на еще протекающее, или совсем недавно перенесенное заболевание, или на хроническую инфекцию. То есть, если нас интересует устойчивый иммунитет, в тестах ищем IgG.
И, наконец, антиген. Как мы разбирали выше, антитела обладают очень высокой специфичностью и связываются только с определенными белками. Когда иммунная система, столкнувшись с инфекцией, подбирает нужное антитело, она чаще всего начинает синтезировать сразу несколько разных видов, нацеленных на разные белки возбудителя. Ведь клетки, синтезирующие антитела, получают для анализа разные кусочки полупереваренного микроба — и поверхностные, и внутренние белки — и для каждого из них ищут антитело. Для эффективной защиты важны именно те антитела, которые связываются с белками на поверхности вируса или бактерии. Ведь антитела — это крупные молекулы, которые не могут поникать внутрь вирусных частиц или бактерий, для них доступны только поверхностные белки. Именно поэтому защитный иммунитет в первую очередь обеспечивают антитела к поверхностным антигенам. Например, в случае коронавирусной инфекции вырабатывается как минимум 2 вида антител — к S-белку (который на поверхности вирусной частицы) и к N-белку (он же нуклеокапсидный белок, который находится внутри вирусной частицы). Так как до N-белка антитела добраться не могут, защиту будут обеспечивать именно антитела к S-белку. То есть, если вы все же хотите определить уровень защитных антител после прививки от ковида, нужно искать тест на нейтрализующие IgG к S-белку.
Мы ждем вакцину от коронавируса через считанные месяцы, от силы год, и кажется, что она уже почти готова, осталось только ее испытать. Однако не всегда это бывает так быстро. Самую неуловимую вакцину на планете — от вируса иммунодефицита человека — ученые ищут уже без малого сорок лет, и до сих пор не нашли. Как так вышло? И что делать дальше: ждать, что она появится, искать обходные пути или научиться жить без нее?
Предчувствия
Для спасения человечества появился протокол. Шаг первый: выделить вирус. Шаг второй: вырастить его в культуре. Шаг третий: инактивировать (обезвредить) врага или отобрать его ослабленные варианты. Шаг четвертый: проверить, вызывают ли получившиеся вирусные частицы иммунный ответ на животных. Шаг пятый: проверить эффективность и безопасность на людях. Через полтора столетия после первых опытов Дженнера разработка противовирусных вакцин из творческой работы превратилась в техническую.

Вирус на Т-клетке человека под электронным микроскопом
NIADS / flickr / CC BY-SA 2.0
За 36 лет с заявления Хеклер и 39 лет с момента начала исследований HTLV-III в мире многое изменилось. Инактивированные вакцины вышли из моды, уступив свою популярность вирусным векторам, полиомиелит остался лишь в нескольких странах, а вакцину от гриппа научились обновлять каждый год. В мире начались и закончились эпидемии атипичной пневмонии и свиного гриппа, пандемия SARS-CoV-2 унесла уже больше полумиллиона жизней, а оставшиеся в живых надеются на скорое появление вакцины.
Тем временем от последствий заражения ВИЧ гибнут сотни тысяч людей и страдают десятки миллионов в год, а обещание Хеклер выполнить не удалось — ни за два года, ни за десять, ни за тридцать девять.
Погоня
Два года — это срок, за который можно успеть пройти по заранее проторенной тропе. В него можно уложиться, если у вас уже есть выделенный вирус, антитела из крови переболевших людей, примеры работающих вакцин того же типа (именно это помогло быстро стартовать разработчикам вакцин от SARS-CoV-2) и отработанная методика их производства — и все это при условии, что вакцина пройдет клинические испытания (которые длятся от нескольких месяцев до года) с первого раза. Иными словами, если сначала вы хорошо подготовились, а потом вам повезло.

Белок оболочки ВИЧ (Env) с размеченными мишенями для атаки антител
Dennis R Burton et al. / Nature Medicine. 2004
Через два года после обещания Хеклер первые вакцины на основе вирусных антигенов, действительно, уже испытывали на животных. Но к людям первой вышла другая вакцина — на основе вируса Vaccinia со встроенным участком генома ВИЧ. Клинические испытания 1986 года прошли на гражданах Заира и, как часто бывает в таких случаях, были этически спорными: оказалось, что в них участвовали дети. Кроме того, как выяснилось позже, некоторые из них умерли от побочного действия вакцины, и после этого никто уже не пытался оценить безопасность и эффективность пробной вакцины. С тех пор в мире прошло уже более двух сотен клинических испытаний разного рода вакцин, но до третьей фазы дошло менее десятка. Остальные не смогли заставить иммунную систему человека отреагировать на вторжение и принять своевременные меры.

Филогенетическое дерево вирусов иммунодефицита человека группы М, цветом обозначен недавно обнаруженный представитель подтипа L
Yamaguchi, Julie et al. / JAIDS, 2020
Строго говоря, это самый быстро мутирующий из известных нам биологических объектов. Таким образом, получается, что мы должны научить иммунную систему производить антитела к многоликому врагу, который вдобавок переобувается на бегу. Грубо говоря, если создание других вакцин — это стрельба по тарелочкам, то в случае с ВИЧ эта тарелочка летит быстрее звука.
Ситуация осложняется тем, что после первого же промаха ружье можно выкидывать. Поскольку ВИЧ — ретровирус, он встраивает свои гены в ядерную ДНК. И вычеркнуть их оттуда мы уже не можем — по крайней мере, до сих пор не научились. Это значит, что если вакцина не сразила врага первым ударом, то он, попав внутрь клеток, оттуда уже не уйдет. Можно приостановить его размножение, можно запретить ему выходить наружу (чем и заняты современные антиретровирусные лекарства), но он в любом случае останется внутри. С ним придется жить.
Собственно говоря, ровно поэтому у нас нет и естественных историй успеха. До сих пор не известно ни одного случая, в которых человек переболел бы ВИЧ-инфекцией в классическом смысле этого слова, то есть сначала носил в себе вирус, а потом перестал, без каких-либо вмешательств извне. И это в своем роде уникальная проблема. Обычно, когда ученые начинают искать вакцину, у них есть реальный пример того, как должна выглядеть их победа — то есть человек, который болел и излечился — его-то победу они и пытаются воспроизвести. Зная ответ заранее, ищут способ к нему прийти.
Принятие
Значит ли это, что люди стали меньше болеть? Увы, нет. Число инфицированных продолжает неумолимо расти, пусть и делает это медленнее, чем до 2000-х годов (Россия, увы — одно из немногих исключений в этом тренде).
Может быть, у нас наконец-то появилась вакцина? Тоже нет. Лучший результат, которым мы сегодня располагаем, получили еще в 2009 году — тогда в ходе испытаний в Таиланде в группе людей, получавших вакцину, вирусом заразились на 31 процент меньше человек, чем в контрольной группе. Сейчас в разгаре два других клинических исследования, в Африке (фаза 2b) и в США (фаза 3). В обоих используются мозаичные вакцины, которые содержат фрагменты белков от разных типов ВИЧ. Оба еще далеки от завершения.
Оптимизм Фаучи опирается не столько на научный прогресс, сколько на то, что мир постепенно учится соседствовать с ВИЧ-инфекцией, подобно тому, как организм пациентов понемногу привыкает жить с вирусом внутри. Не имея шансов оставить вирус позади, мы все еще можем бежать с ним бок о бок и пытаться опередить его хотя бы на полшага.
Другой способ обогнать вирус — профилактика. Если в крови постоянно поддерживается небольшая концентрация противовирусных средств, то ВИЧ не успевает проникнуть в клетки и в них размножиться. Защита от заражения при профилактике достигает 99 процентов — но таблетки придется пить каждый день, обезопасить себя раз и навсегда мы до сих пор не можем.
Даже в последнем программном тексте Фаучи вакцина упоминается лишь вскользь — как финальный штрих, без которого о полной победе над эпидемией говорить не получится. Но не она будет тем самым оружием и не она главная цель для борцов с ВИЧ — потому что она, вероятно, недостижима.
На этом фоне вирус SARS-CoV-2 кажется не таким опасным врагом - по крайней мере, из того, что мы знаем о нем сегодня. Он не столь разнообразен и мутирует медленнее. Многие люди выздоравливают после болезни и приобретают к вирусу иммунитет — а значит, нам есть на что ориентироваться. У нас даже есть наработки вакцин против его родственников и предшественников.
Так что задача выглядит легко решаемой — и если что-то пойдет не так, мы знаем способы договориться с эпидемией и без вакцины.
Читайте также:

