Ферментами вирусов может являться
Обновлено: 19.04.2024
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
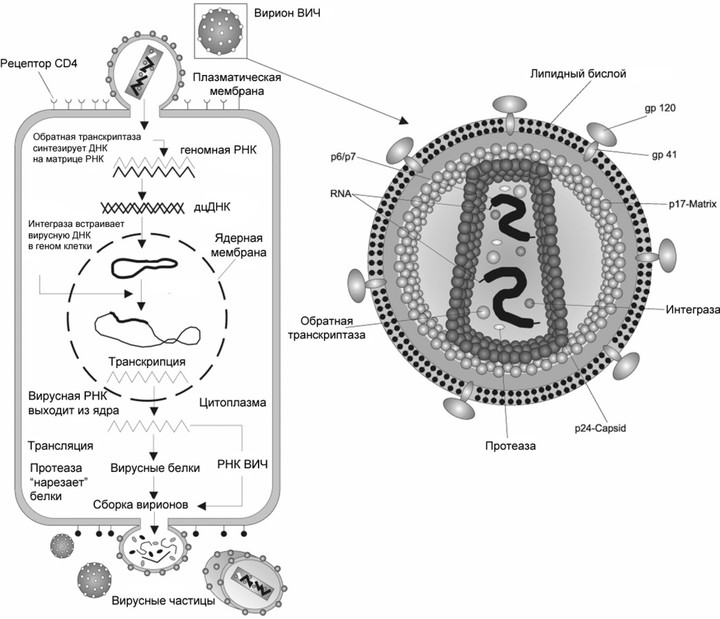
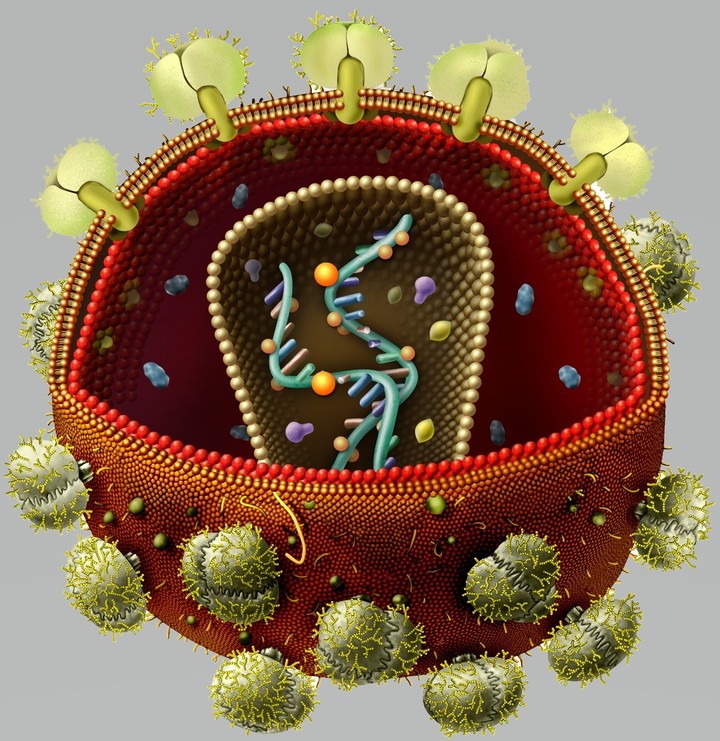
Жизненный цикл вируса, на примере вируса иммунодефицита
Как с ними бороться?
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
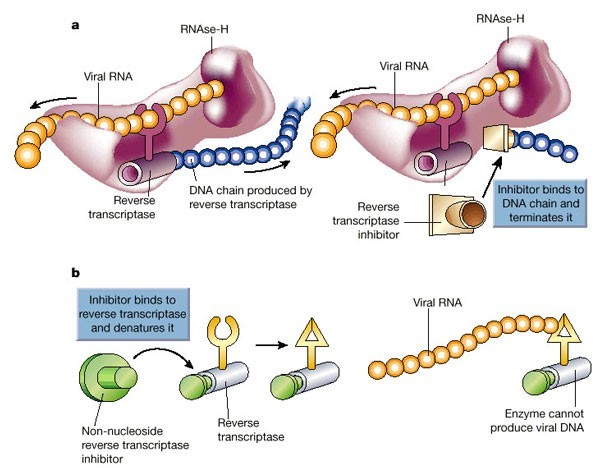
Механизм дейсвтия ингибиторов обратной транскриптазы
3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
4. Созревание
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.
в составе вирионов многих, особенно сложных вирусов, содержатся ДНК- и РНК-полимеразы, ферменты, разрушающие оболочку клетки-хозяина, модифицирующие концы иРНК. В процессе реализации вирусного генома в клетке синтезируется ряд Ф.в. с такими же или иными функциями. Однако набора Ф.в. недостаточно для самостоятельного внеклеточного размножения. В синтезе биополимеров вируса участие принимают ферменты клетки-хозяина.
Смотреть что такое "Ферменты вирусов" в других словарях:
Нуклеазы — ферменты, расщепляющие Нуклеиновые кислоты (НК) до моно и олигонуклеотидов; по характеру своего действия относятся к фосфодиэстеразам. Широко распространены в клетках микроорганизмов, растений и животных. Особенно много Н. в соке… … Большая советская энциклопедия
Медицина — I Медицина Медицина система научных знаний и практической деятельности, целями которой являются укрепление и сохранение здоровья, продление жизни людей, предупреждение и лечение болезней человека. Для выполнения этих задач М. изучает строение и… … Медицинская энциклопедия
НУКЛЕИНОВЫЕ КИСЛОТЫ — биополимеры, состоящие из остатков фосфорной кислоты, сахаров и азотистых оснований (пуринов и пиримидинов). Имеют фундаментальное биологическое значение, поскольку содержат в закодированном виде всю генетическую информацию любого живого… … Энциклопедия Кольера
Вирусы — (от лат. Virus яд) фильтрующиеся вирусы, ультравирусы, возбудители инфекционных болезней растений, животных и человека, размножающиеся только в живых клетках. В. мельче большинства известных микробов; почти все В. проходят через… … Большая советская энциклопедия
Дезоксирибонуклеиновая кислота — Двойная спираль ДНК Дезоксирибонуклеиновая кислота (ДНК) макромолекула(одна из трех основных, две другие РНК и белки), обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования… … Википедия
Ви́русы — (лат. virus яд) мельчайшие микроорганизмы, не имеющие клеточного строения, белоксинтезирующей системы и способные к воспроизведению лишь в клетках высокоорганизованных форм жизни. Они широко распространены в природе, поражают животных, растения и … Медицинская энциклопедия
Клетка — I Клетка (cytus) основная структурно функциональная единица, определяющая строение, жизнедеятельность, развитие и размножение животных и растительных организмов за исключением вирусов; элементарная живая система, способная к обмену веществ с… … Медицинская энциклопедия
ВИРУСЫ — мельчайшие возбудители инфекционных болезней. В переводе с латинского virus означает яд, ядовитое начало . До конца 19 в. термин вирус использовался в медицине для обозначения любого инфекционного агента, вызывающего заболевание. Современное… … Энциклопедия Кольера
ДНК — Двойная спираль ДНК Дезоксирибонуклеиновая кислота (ДНК) один из двух типов нуклеиновых кислот, обеспечивающих хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная… … Википедия
Двойная спираль — ДНК Дезоксирибонуклеиновая кислота (ДНК) один из двух типов нуклеиновых кислот, обеспечивающих хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная роль ДНК в… … Википедия

Оглавление
- Введение
- Обозначения и сокращения
- 1 История вирусологии, природа и происхождение вирусов
- 2 Химический состав вирусов
- 3 Морфология, морфогенез, биофизические свойства и генетика вирусов
Приведённый ознакомительный фрагмент книги Общая вирусология с основами таксономии вирусов позвоночных предоставлен нашим книжным партнёром — компанией ЛитРес.
2 Химический состав вирусов
Основными химическими соединениями, которые входят в состав всех вирусов, являются белки и нуклеиновые кислоты. В состав ряда вирусов входят липиды и углеводы.
Белки. Локализация вирусных белков. Белки, связанные с жизненным циклом вируса, разделяют на белки, детерминируемые геномом вируса и белки, имеющие клеточное происхождение. В качестве примера клеточных белков, которые обнаружены в составе некоторых вирионов, могут быть приведены белок цитоскелета — актин, и ядерные белки — гистоны. Белки клеточного происхождения, участвующие в процессе репликации вируса, будут рассмотрены в разделе взаимодействия вируса с клеткой.
По месту локализации белки, детерминируемые вирусным геномом, разделяют на две группы: 1) структурные белки — это белки, входящие в состав ВЧ, их обозначают как VP; 2) неструктурные белки — это предшественники структурных белков, регуляторные белки и ферменты, обслуживающие процесс внутриклеточной репродукции вируса и не входящие в состав ВЧ. Их обозначают как NS-белки.
Свойства вирусных белков. В состав вирионов входят белки с различной молекулярной массой (от 4 до 100 кД), состоящие из одной или нескольких полипептидных цепей. Количество этих белков также различно у разных вирусов. В состав нуклеокапсида ВТМ входит один белок. У других вирусов в состав вириона может входить несколько десятков белков, имеющих различные физико-химические свойства. Белки, формирующие капсид, нуклеокапсид и коровую оболочку, обладают одним общим свойством — способностью к самосборке.
В состав ВЧ могут входить низкомолекулярные белки, не участвующие в формировании капсида. Например, геномные белки пикорнавирусов и аденовирусов. Геномный белок ковалентно связан с нуклеиновой кислотой и участвует в ее репликации.
Сложные белки представлены гликопротеинами (обозначают как gp) и липопротеинами. Наличие гликопротеина определяет присутствие в вирионе углеводного компонента, который может быть представлен олигосахаридами маннозного типа, галактозой, N-ацетилглюкозамином или нейраминовой кислотой. Вирусные гликопротеины, как правило, экспонированы на наружной поверхности ВЧ и выполняют три основные функции: обеспечивают связывание вириона с клеточным рецептором (функция прикрепительного белка), обладают фузионной активностью (обеспечивают слияние мембран) и определяют антигенные свойства вирусов. В то же время, вирусные гликопротеины могут быть и неструктурными белками и, оставаясь в интегральной форме в мембране шероховатого эндоплазматического ретикулюма (ШЭР), выполнять функции транслоказ, обеспечивая транспорт вирусных компонентов в его просвет.
Вирусные липопротеины представлены белками, ацилированными, как правило, миристиновой (C14) кислотой. Остатки жирных кислот, соединенные с молекулой белка, выполняют функцию липофильного якоря.
Вирусные белки-ферменты могут входить в состав вирусной частицы или являться неструктурными белками и появляться в клетке после экспрессии вирусного генома. Наиболее оснащенным ферментами является вирион вируса оспы, который имеет практически полный набор энзимов, необходимых для независимой внутриклеточной репликации вируса. В то же время, мелкие просто организованные изометрические вирусы с позитивным РНК-геномом могут не иметь никаких ферментов в составе вириона.
Функционально активные белки вирусов представлены, в первую очередь, ферментами нуклеинового обмена, обеспечивающими сложные механизмы репликации/транскрипции вирусного генома; ферментами, осуществляющими посттрансляционный процессинг и модификацию белков, и ферментами, участвующими в проникновении вирионов в клетку хозяина.
Первая группа ферментов наиболее многочисленна и включает как аналоги клеточных ферментов, так и вирус-специфические ферменты.
ДНК-зависимая ДНК-полимераза — осуществляет синтез ДНК на матрице ДНК (вирус оспы).
ДНК-зависимая РНК-полимераза — осуществляет синтез мРНК на матрице ДНК (вирус оспы).
Обратная транскриптаза или ревертаза или РНК-зависимая ДНК-полимераза осуществляет синтез ДНК на матрице РНК. Впервые открыта в 1970 г. у ретровирусов Темином и Мизутани.
Хеликаза — осуществляет расплетете двухнитевой структуры ДНК. Кроме этого хеликазы обладают нуклеотидтрифосфат-зависимой РНК-хеликазной активностью, которая включает три процесса: связывание дезоксинуклеотидтрифосфата, его гидролиз и за счет этой энергии расплетение двухнитевой РНК.
мРНК-модифицирующие ферменты : поли-А-полимераза — аденилирует 3'конец РНК за счет энергии АТФ; Кэп-энзим и метилтрансферазный комплекс — катализирует образование на 5'-конце кэп-структуры.
АТФ-аза, ГТФ-аза — осуществляют гидролиз соответствующих энергетических субстратов.
Рибонуклеаза Н — разрушает РНК, находящуюся в дуплексе с ДНК. Вторая группа вирусных ферментов — ферменты белкового обмена.
Здесь мы приведем лишь некоторые из них:
Протеиназы — ферменты, участвующие в посттрансляционном процессинге полипротеинов. Являются NS-белками РНК-содержащих вирусов;
Протеинкиназы — ферменты, фосфорилирующие структурные белки вирионов. Обнаружены в составе вируса везикулярного стоматита, вируса бешенства, альфавирусов и ретровирусов. Примерами ферментов, участвующих в проникновении вирусов в клетку, являются лизоцим бактериофагов и нейраминидаза вируса гриппа.
Липиды. Все оболочечные РНК-содержащие почкующиеся вирусы имеют липиды клеточного происхождения, входящие в состав суперкапсида (от 15 % до 30 % от сухого веса). От 50 % до 60 % липидов представлены фосфолипидами, от 20 % до 30 % составляет холестерин.
У ДНК-геномных вирусов липиды содержат вирусы оспы, герпеса, гепатита B. Это непочкующиеся вирусы. У вируса оспы липиды не образуют дифференцированной оболочки, которая формируется в цитоплазме в процессе морфогенеза поксвириона. Липиды вируса гепатита B образуются путем инвагинации мембран эндоплазматического ретикулюма (ЭПР). Липидсодержащая оболочка вируса герпеса формируется при прохождении внутреннего компонента вириона через ядерную мембрану. Следовательно, в состав вирусной оболочки герпесвирусов входят липиды ядерной мембраны.
Нуклеиновые кислоты. Клетки всех живых организмов содержат два вида нуклеиновой кислоты — ДНК (двухнитевая ДНК клеточного генома) и РНК (мРНК, тРНК, рРНК). В отличие от клеток, вирионы содержат только один вид нуклеиновой кислоты — ДНК или РНК. И та и другая являются хранителями наследственной информации и выполняют функции генома. Однако следует учитывать, что наличие одного вида нуклеиновой кислоты является характеристикой вириона, но не вируса. В жизненном цикле вируса его геномная нуклеиновая кислота транскрибируется, то есть ДНК-содержащие вирусы образуют РНК. Ряд РНК-содержащих вирусов имеют в цикле репродукции стадию обратной транскрипции и синтезируют ДНК на матрице РНК. Примерно 20 % всех вирусов имеют ДНК-геном, 80 % — РНК-геном. Способность РНК хранить наследственную информацию — уникальное свойство вирусов. Размеры вирусных геномов (длина нуклеотидных последовательностей, выраженная в нуклеотидах) варьируют в широких пределах — от 1,7 тысяч нуклеотидов (т.н.) у цирковируса свиней до 300 т.н. у фикоднавирусов архибактерий.
Кроме того, что геном вирусов может быть представлен или ДНК или РНК, он может находиться в разных видах — в виде двухнитевой (дн) или однонитевой (он) формы, в виде линейной или кольцевой, в виде непрерывной или сегментированной формы.
Многообразие видов РНК геномов расширяется за счет существования последовательностей, отличающихся направлением связей сахаро-фосфатного остова.
Однонитевые РНК могут иметь позитивную полярность — (+) РНК, негативную полярность — (-) РНК или могут быть представлены обоюдозначащей цепью — (+, — ) РНК (амбисенс стратегия кодирования). В свою очередь, РНК позитивной полярности могут иметь разную структурную организацию: могут, являясь матричной РНК, иметь на 5'-конце кэп (7-метилгуанозин, Сар), а на 3'-конце — поли-А (poly-A) последовательность; могут не иметь кэпа или поли-А; могут иметь на 5'-конце геномный белок; могут иметь на 3'-конце тРНК-подобную или шпильковую структуру.
Виды геномов вирусов легли в основу их классификации. Однако следует учитывать, что вид генома в настоящее время не является формальным таксоном и используется для удобства ориентации в многообразии вирусов.
Углеводы. Углеводный компонент вирусов находится в составе гликопротеидов. Количество сахаров в составе гликопротеидов может быть достаточно большим, достигая от 10 % до 13 % от массы вириона. Химическая специфичность их полностью определяется клеточными ферментами, обеспечивающими перенос и присоединение соответствующих сахарных остатков. Обычными сахарными остатками, обнаруживаемыми в вирусных белках, являются фруктоза, сахароза, манноза, галактоза, нейраминовая кислота, глюкозамин. Таким образом, подобно липидам, углеводный компонент определяется клеткой-хозяином, благодаря чему один и тот же вирус, выращенный в клетках разных видов, может значительно отличаться по составу сахаров в зависимости от специфичности клеточных гликозилтрансфераз.
Углеводный компонент гликопротеидов играет существенную роль в структуре и функции белка. Он является каркасом для локальных участков гликопротеида, обеспечивая сохранение конформации белковой молекулы, и обусловливает защиту молекулы от протеаз. Возможны и другие функции углеводов, пока достоверно не установленные.
Компоненты клетки-хозяина. В составе вирионов могут находиться компоненты клетки-хозяина. К таким компонентам могут относиться белки, и даже целые клеточные структуры. Так, например, в составе ряда оболочечных вирусов может находиться белок цитоскелета актин, в составе паповавирусов содержатся клеточные гистоны. Ряд вирусов содержит клеточные ферменты, например, протеинкиназы. В составе аренавирусов обнаружены рибосомы.
Клеточные компоненты могут включаться в вирион случайно или закономерно, В некоторых случаях они играют существенную роль в репродукции вируса, как, например, гистоны в репродукции паповавирусов.
Одни вирусы способны интегрироваться в геном клетки-мишени и таким образом оставаться во всех дочерних клетках, которые будут в будущем получены после ее деления. К таким вирусам относятся гаммаретровирусы и лентивирусы. Другие делать этого не умеют (например, адено- и аденоассоциированные вирусы). Но для производства белков и репликации (размножения) все они используют клетку и ее синтетический аппарат.
Как это работает?
Для того чтобы вирус мог проникнуть в клетку, белки его оболочки должны связаться с мембранными белками клетки-мишени. Важно отметить, что проникает вирус только в те клетки, которые могут в дальнейшем помочь его репликации. Вирус ВИЧ живет в клетках иммунной системы, вирус гепатита С — в клетках печени. Есть особые вирусы, которые поражают только растения или даже только бактерии.
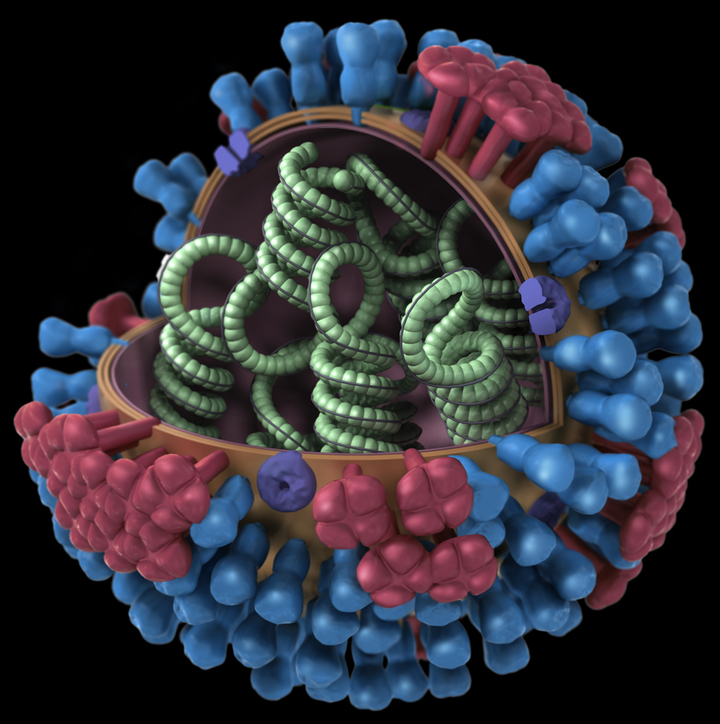
Строение вируса гриппа. Под оболочкой вириома - генетический материал вируса, необходимый для его воспроизводства в клетке.
Содержащие неактивный вирус и оставшиеся в живых клетки иногда сохраняют возможность нормального функционирования. В этом случае клетки могут быть заражены, но вирус проявит себя спустя длительный период времени. Так устроен герпес.
В зависимости от того, каким типом нуклеиновой кислоты представлен генетический материал, выделяют ДНК-содержащие вирусы и РНК-содержащие вирусы. И тут стоит остановиться на классификации.
Типы вирусов. Коротко о главном
Современная типология вирусов содержит 7 классов и была предложена Дэвидом Балтимором еще в 1971 году. С тех пор, впрочем, она была уточнена и расширена, в том числе советскими учеными. И выглядит в настоящее время таким образом:
Вирусы, содержащие двухцепочечную ДНК
Описание
Для репликации вирусу необходимо попасть в ядро клетки-мишени и воспользоваться ее ДНК-полимеразой. Иногда вирус вызывает незапланированное деление самое клетки, то есть становится онкогенным. Эти вирусы хорошо изучены.
Пример: Вирус герпеса, адено- и папилломавирусы
Вирусы, содержащие одноцепочечную ДНК
Описание
Попадая в ядро клетки, вирусы образуют двухцепочечную ДНК, после чего реплицируются так же, как вирусы класса I.
Пример: Парво- и цирковирусы
Вирусы, в которых РНК способна к репликации (редупликации)
Описание
Вирусы этого класса могут размножаться в цитоплазме клетки, им не нужна молекула ДНК. Каждый ген, находящийся в РНК вируса, кодирует только один вирусный белок.
Пример: Бирна- и реовирусы
Вирусы, содержащие одноцепочечную (+) РНК
Описание
Из геномной (+) РНК на рибосомах хозяина создаются вирусные белки. В одном фрагменте РНК могут быть закодированы разные белки, что увеличивает сложность вируса без удлинения генов.
Пример: Пикорнавирусы (полиомиелит, гепатит А) и коронавирусы
Вирусы, содержащие одноцепочечную (–) РНК
Описание
(–) РНК этих вирусов предварительно должна быть транскрибирована в (+) РНК вирусными РНК-полимеразами, после чего может начаться синтез вирусных белков. Вирусы этого класса делятся еще на две группы, в зависимости от их генома и места его репликации (цитоплазма или ядро).
Пример: Филовирусы, аренавирусы (геморрагическая лихорадка Ласса), ортомиксовирусы (вирусы гриппа) и так далее.
Вирусы, содержащие одноцепочечную (+) РНК, реплицирующиеся через стадию ДНК
Описание
Такие вирусы используют фермент обратную транскриптазу для превращения (+) РНК в ДНК, которая встраивается в геном хозяина ферментом интегразой. Дальнейшая репликация происходит при помощи полимераз клетки хозяина.
Пример: Ретровирусы (в том числе ВИЧ)
Вирусы, содержащие двухцепочечную ДНК, реплицирующиеся через стадию одноцепочечной РНК
Описание
Молекула ДНК замкнута в кольцо и является матрицей для синтеза мРНК и дополнительных молекул РНК, которые используются при репликации вирусного генома обратными транскриптазами.
Пример: Колимовирусы (вызывают инфекции растений) и гепаднавирусы (например, гепатит В)
Вакцинация и лечение
Как правило, организмы умеют бороться с паразитирующими на них вирусами. На примере млекопитающих и человека мы обычно говорим о главном инструменте — врожденном иммунитете.
Впрочем, наиболее эффективен этот вид защиты в отношении бактериальных инфекций и не может обеспечить продолжительную и надежную защиту, особенно от инфекций вирусных.
Именно поэтому огромное значение имеет приобретенный иммунитет, в результате которого клетки иммунной системы обучаются вырабатывать специфические к вирусу антитела, способные уничтожать как саму вирусную частицу, так и зараженные ею клетки.
Еще одна врожденная система борьбы с вирусными инфекциями — внутриклеточная. Как правило, клетка способна распознать чужеродную РНК в своей цитоплазме, куда ее сперва и доставляют многие вирусы, и имеет специальные комплексы для ее деградации. Но часть вирусов научились обходить и эту ловушку. К примеру, ротавирусы, которые даже внутри клетки сохраняют капсид с геномной РНК.
Миссия: уничтожить
Основная сложность в лечении вирусных заболеваний заключается в том, что они используют естественные функции клеток-мишеней для своего размножения, поэтому ученым зачастую оказывается не так-то просто придумать препарат, который будет токсичен для вируса и безопасен для самой клетки. Если такой безопасности достичь не удастся, лекарство будет иметь слишком много побочных эффектов, повреждающих сам организм, что окажется нецелесообразно для использования.

Сравнение жизненных циклов ВИЧ и вируса гриппа. Если первый использует обратную транскрипцию и живет в клетках иммунной стистемы, вирион второго, проникая в эпительные клетки дыхательных путей целиком - а именно там он и обитает - распадается уже внутри клетки, а репликация вирусной РНК происходит в ядре с помощью вирусных полимераз PA, PB1 и PB2 путем комплементарного копирования.
По принципу действия противовирусные препараты подразделяются на две группы: стимулирующие иммунную систему атаковать вирусы (например, за счет индукции синтеза белков-интерферонов) и атакующие вирусы напрямую. Препараты второй группы различаются по этапу жизненного цикла вируса, на котором они активны: это препараты, препятствующие проникновению вируса в клетку, препятствующие размножению вируса внутри клетки и препятствующие выходу копий вируса из клетки.
Еще один класс противовирусных препаратов блокирует ферменты, необходимые для создания и модификаций белков вируса. Такие лекарства называют протеазными ингибиторами.
Вместо заключения: а могут ли вирусы приносить пользу?
Безусловно, да. Несмотря на то, что вирусы ассоциируются у большинства людей с однозначным вредом, они могут приносить и пользу — если речь идет о так называемых вирусных векторах и терапевтических подходах на их основе.
Исследователи давно научились помещать в белковую оболочку вируса интересующие их нуклеиновые кислоты, чтобы доставлять нужный ген в клетки, а также убирать те гены, которые делают вирус опасным для организма.
Это позволило сделать возможной генную терапию, помогающую бороться с заболеваниями, вызванными известными генетическими мутациями. Создание вирусных векторов — достаточно непростая задача, к тому же ограниченная свойствами самих вирусных частиц: количеством помещающейся генетической информации, местом ее вставки, стабильностью. Кроме того, вирусный вектор, используемый в медицине, не должен вызывать иммунного ответа или критично влиять на жизнедеятельность клетки. Тем не менее эти сложности решаются, поэтому уже одобрен ряд вполне успешных и безопасных генных терапий. А в качестве основы для вирусных векторов чаще всего используются ретро-, ленти-, адено- и аденоассоциированные вирусы.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
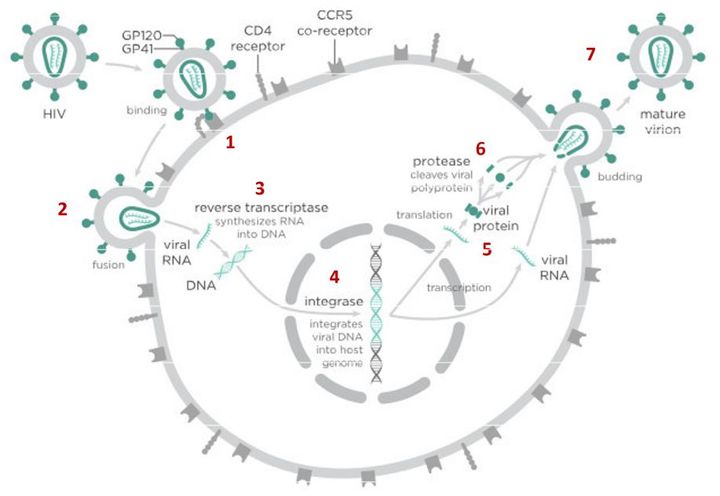
В случае с ВИЧ это выглядит так.
по теме

Лечение
Лучшие научпоп-статьи 2018 года
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
по теме

Лечение
Ошибка системы. Почему в регионах опять не хватает таблеток от ВИЧ
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.
Читайте также:

