Где лечат пневмоцистная пневмония у вич инфицированных
Обновлено: 24.04.2024
В статье представлены основные данные по эпидемиологии, распространению и патогенезу пневмоцистоза, а также рассматриваются его клинические проявления, методы современной диагностики и подходы к лечению и профилактике этого заболевания при ВИЧ-инфекции. Приводятся схемы лечения и профилактики пневмоцистной пневмонии основными (Бисептол, пентамидин) и резервными препаратами, а также необходимые компоненты патогенетической терапии.
Пневмоцистоз привлек в последние годы внимание многих исследователей в связи с пандемией ВИЧ-инфекции, хотя его изучением занимались и раньше – сначала как проблемой детской патологии, а затем и как проблемой внутрибольничных инфекций. Среди оппортунистических инфекций при СПИДе он занимает одно из лидирующих мест.
Со времени открытия возбудителя пневмоцистной пневмонии (ПП) в 1909 г. и вплоть до 1981 г. во всем мире было описано лишь несколько десятков случаев заболевания, в основном, у младенцев с недостаточностью питания и взрослых больных с гематологическими и онкологическими заболеваниями, получавших иммунодепрессанты [1]. Частота случаев ПП резко увеличилась, начиная с 1981 г. Это заболевание стало основным клиническим проявлением СПИДа, на основании которого были распознаны его первые случаи в США: ПП выявлялась при первом осмотре у 64% больных, а на более поздних стадиях регистрировалась еще у 20% пациентов.
Возбудителем заболевания является Рneumocystis carinii – микроорганизм, который большинство исследователей относят к простейшим (подтип Sporozoa, класс Haplospora). Это – внеклеточный паразит с преимущественным тропизмом к легочной ткани, поражающий пневмоциты 1 и 2 порядков.
До сих пор ведутся споры о таксономическом положении пневмоцист. Ряд специалистов относит их к грибам, так как имеются данные о сходстве между нуклеотидными последовательностями рибосомальной РНК P. carinii и аналогичными структурами у Saccharomyces cervisae и Neurospora crassae [2].
Пневмоцисты широко распространены во всех регионах мира и практически у всех животных – диких, синантропных и сельскохозяйственных. В многочисленных исследованиях показано широкое носительство пневмоцист среди людей в различных географических зонах как в общей популяции, так и у отдельных контингентов населения [1,3-7]. Нами было выявлено широкое носительство Р. carinii в отделении ВИЧ-инфекции у госпитализированных больных (92,9%) и у персонала (80%) [5].
Манифестные формы заболевания развиваются у ослабленных младенцев (преимущественно первых 4-6 месяцев жизни), а в старших возрастных группах они встречаются только при выраженном иммунодефиците, причем имеется четкая связь с характером последнего. Так, средняя частота ПП при ВИЧ-инфекции составляет в настоящее время более 50%, а при других иммунодефицитных состояниях – не превышает 1%.
Патогенез ПП связан с механическим повреждением стенок интерстиция легких. Весь жизненный цикл пневмоцист проходит в альвеоле, к стенке которой они очень плотно прикрепляются. Для развития пневмоцистам необходимо повышенное содержание кислорода. Постепенно размножаясь, они заполняют все альвеолярное пространство, захватывая все большие участки легочной ткани. При тесном контакте трофозоитов со стенками альвеол повреждаются фосфолипиды, постепенно нарушается растяжение легких, увеличивается толщина альвеолярных стенок (в 5-20 раз). Вследствие этого развивается альвеолярно-капиллярный блок, ведущий к тяжелой гипоксии. Отягощающим моментом является образование участков ателектаза, что усугубляет нарушение вентиляции и газообмена. Тяжелому течению болезни способствуют сопутствующие заболевания легких при ВИЧ-инфекции, чаще всего, цитомегаловирусная пневмония.
Наиболее характерными симптомами ПП у больных СПИДом являются: одышка (90-100%), лихорадка (60%), кашель (50%), в то время как у неинфицированных ВИЧ больных эти показатели несколько иные (например, кашель регистрируется гораздо чаще, в 80–95% случаев).
Одышка – наиболее ранний симптом ПП, наблюдающийся практически у всех больных. Вначале она бывает выражена при умеренной физической нагрузке, что особенно заметно при подъеме по лестнице. Если в этот период провести функциональные пробы (велоэргометрия), то после 5-минутной нагрузки дыхание становится более частым и поверхностным (а у здоровых людей – более глубоким), что свидетельствует о неэффективности внешнего дыхания. Этот период может быть растянут во времени и иногда достигает нескольких недель и даже месяцев. Мы наблюдали больного, у которого время от начала одышки при физической нагрузке до развернутой клинической картины с одышкой в покое до 50 в минуту, лихорадкой и кашлем составило 4 месяца. Постепенно одышка нарастает и начинает беспокоить больных уже в покое. Повышение температуры тела может сопровождаться ознобом, повышенной потливостью. В начале заболевания обычно наблюдается субфебрильная температура; в последующем она либо повышается (до 38–39°С), либо остается субфебрильной. Более высокие цифры регистрируются, как правило, у детей раннего возраста. Температурная кривая отличается постепенным нарастанием, постоянным, ремитирующим или неправильным характером. Кашель сухой, обычно, без отделяемого, хотя появление мокроты возможно у больных с сопутствующим бронхитом другой этиологии или у курильщиков. В начале болезни характерно навязчивое покашливание из-за постоянного ощущения раздражения за грудиной или в гортани. В дальнейшем кашель почти постоянный и приобретает коклюшеподобный характер, особенно он беспокоит в ночное время. Свойственных коклюшу приступов и реприз не бывает.
У взрослых ПП, как правило, проявляется более тяжело, отмечается затяжное и рецидивирующее (до 3-6 и более манифестаций) течение с высокой летальностью.
При клиническом обследовании в легких очень часто не удается выявить каких-либо характерных изменений. Перкуторно может определяться короткий оттенок легочного звука, аускультативно – жесткое дыхание, усиленное в передневерхних отделах, иногда рассеянные сухие хрипы. При исследовании других органов обычно наблюдается увеличение размеров печени, нередко отмечается и увеличение селезенки. В связи с возможной диссеминацией пневмоцист по органам (которая происходит все чаще) и вероятностью развития внелегочного пневмоцистоза обследование больного должно быть очень тщательным. Пневмоцисты могут поражать практически любой орган, за исключением суставных сумок и предстательной железы. Описаны поражения лимфатических узлов, селезенки, печени, костного мозга, слизистой оболочки желудочно-кишечного тракта, глаз, щитовидной железы, сердца, головного и спинного мозга, тимуса, брюшины и т.д.
При исследовании периферической крови специфических изменений при ПП не наблюдается. Часто регистрируются изменения, характерные для поздних стадий ВИЧ-инфекции: анемия, лейкоцитопения, тромбоцитопения и др. СОЭ всегда повышена и может достигать 40-60 мм/ч. Самым характерным биохимическим неспецифическим показателем является значительное повышение суммарной активности лактатдегидрогеназы (ЛДГ) как отражение дыхательной недостаточности. По наблюдениям зарубежных исследователей, неблагоприятными прогностическими признаками при ПП являются высокая активность ЛДГ (более 500 МЕ/л); продолжительное течение с развитием рецидивов; дыхательная недостаточность и/или сопутствующая цитомегаловирусная пневмония, а также низкий уровень гемоглобина (ниже 100 г/л), альбумина и Y-глобулина [8].
У больных ВИЧ-инфекцией развитие пневмоцистоза обычно наблюдается при уменьшении числа СD4-лимфоцитов ниже 0,2x10 9 /л.
Если больной не получает лечения, нарастают одышка (до 70 в минуту и более) и признаки легочно-сердечной недостаточности, могут развиться пневмоторакс и даже пневмомедиастинит, а в дальнейшем – отек легких. Нелеченое заболевание часто приводит к гибели больного.
Серологические методы диагностики ненадежны. Для выделения возбудителя из мокроты используют методы индуцированного ее получения (стимуляция кашлевых толчков 2-3% солевым раствором); в дальнейшем применяют прямую микроскопию окрашенных мазков. Используют также исследование бронхоальвеолярного смыва, что увеличивает возможность получения положительного результата с 60% до 90%. В последнее время для более точной диагностики разработаны и применяются методы ПЦР, иммунофлюоресцентные методы с моно- и поликлональными антителами [7].
Несмотря на то, что в настоящее время разработана эффективная терапия, летальность от ПП при ВИЧ-инфекции у больных, получающих лечение, превышает 10%, а при его отсутствии колеблется в пределах от 25% до 80%.
Лечение ПП обязательно должно сочетаться с терапией ВИЧ-инфекции (назначение комбинированной противоретровирусной терапии, если больной не получал ее ранее), а также с патогенетической и симптоматической терапией.
Бисептол, содержащий 480 мг действующих ингредиентов (80 мг триметоприма и 400 мг сульфометоксазола), назначают из расчета 20 мг/кг триметоприма в сутки. Эта доза делится на 4 части для приема каждые 6 часов. Обычно применяется таблетированная форма, но при тяжелом течении заболевания и при нарушении всасывания в желудочно-кишечном тракте препарат вводят внутривенно капельно. Для этого разовую дозу (1 ампула содержит 20 мг триметоприма) растворяют в 250 мл 5% раствора глюкозы. Курс лечения продолжается 21 день. В первые 3-4 дня приема возможно не только отсутствие эффекта, но и временное ухудшение – усиление одышки, повышение температуры тела. По завершении курса лечения проводится поддерживающая терапия – взрослые принимают Бисептол по 1 таблетке (480 мг) 1 раз в сутки.
В среднем, после перенесенной ПП выживают 75% больных, а в некоторых медицинских центрах этот показатель достигает 90%. При рецидивах выживают около 60% пациентов. Одним из критериев эффективности лечения является частота рецидивов, вероятность которых в первые 6 месяцев после первого эпизода ПП составляет около 35%, а в последующие 6 месяцев достигает 60%.
Побочные реакции, обычно, наблюдаются с 6 по 14 день приема ко-тримоксазола. Они могут проявляться повышением температуры тела, сыпью и зудом, тошнотой, увеличением печени, диареей, лейкоцитопенией, тромбоцитопенией, агранулоцитозом, повышением активности сывороточных трансаминаз, уровня креатинина и др. Кожные высыпания, поражения печени, нейтропения и тромбоцитопения чаще наблюдаются у больных со значительными нарушениями функции печени и почек (особенно, если клиренс креатинина ниже 15 мл/мин), поэтому этим категориям пациентов ко-тримоксазол назначать нельзя. Некоторые реакции могут исчезать на фоне продолжающегося лечения. После 2-недельного приема препарата необходимо провести контрольное исследование периферической крови. В случае обнаружения тяжелых нарушений показано назначение препаратов фолиевой кислоты.
За рубежом при непереносимости или недостаточной эффективности ко-тримоксазола больным назначают пентамидин парентерально (препарат не всасывается в желудочно-кишечном тракте). Его вводят внутривенно медленно в дозе 4 мг/кг/сут, разведенной в 250 мл 5% раствора глюкозы, или в форме аэрозоля (водный раствор в суточной дозе 4 мг/кг). При ингаляции пентамидина токсические реакции регистрируются реже и выражены в меньшей степени, чем при внутривенном введении (к наиболее тяжелым токсическим эффектам относятся гепато- и нефротоксичность, гипогликемия). Однако ингаляционный путь введения пентамидина при развившейся болезни имеет ряд ограничений: возможность бронхоспазма, раздражение слизистой оболочки глотки, неодинаковая вентиляция разных отделов легких и др. Чаще ингаляции пентамидина используют с профилактической целью, хотя этот метод профилактики также имеет ряд недостатков, основным из которых является вероятность развития внелегочного пневмоцистоза и пневмоторакса. Продолжительность внутривенного курса лечения составляет 21 день.
Третьим, наиболее часто применяемым при ПП препаратом, является дапсон (препарат резерва), обычно используемый для терапии лепры. Дапсон (100 мг 1 раз в сутки) рекомендуется сочетать с триметопримом (15-20 мг/кг/сут к 100 мг 1 раз в сутки каждые 8 часов). Продолжительность лечения – 21 день. Данная комбинация хорошо переносится. Ее основной побочный эффект – гемолиз у больных с дефицитом глюкозо-6-фосфатдегидрогеназы. Также возможно развитие метгемоглобинурии.
Другой резервной схемой лечения ПП умеренной степени тяжести является комбинация клиндамицина (1,2 г/день внутривенно или перорально) и примахина (0,03 г/день перорально), которую применяют в течение 21 дня. Эту схему также нельзя назначать больным с дефицитом глюкозо-6-фосфатдегидрогеназы, а на 2-3 неделе лечения необходим контроль уровня метгемоглобина.
При отсутствии угрожающих жизни осложнений, но при наличии дыхательной недостаточности применение кортикостероидов способствует более быстрому уменьшению гипоксии. С этой целью назначают преднизолон по 60 мг в сутки в 2-3 приема в первой половине дня в течение 7 дней с последующей постепенной отменой.
Короткий курс кортикостероидной терапии позволяет избежать диссеминации пневмоцист из легких в другие органы. Применение кортикостероидов нецелесообразно при легком течении заболевания и отсутствии отрицательной динамики. При наличии у больных других оппортунистических заболеваний кортикостероиды следует назначать с осторожностью, так как на фоне их применения возможно прогрессирование этих болезней и даже генерализация процесса (герпетическая инфекция, цитомегаловирусная инфекция).
Искусственную вентиляцию легких назначают по показаниям при наличии условий для ее проведения; 20–30% больных, которым она производится, выздоравливают и продолжают жить еще 6-12 месяцев.
При отсутствии первичного профилактического лечения ПП развивается на поздних стадиях ВИЧ-инфекции у 80% больных, а вероятность рецидива при отсутствии вторичной профилактики составляет 70% (в течение 1 года). У больных, получающих ко-тримоксазол, частота ПП составляет 3,5% в год. Кроме того, ко-тримоксазол действует на другие микроорганизмы, благодаря чему оказывает профилактический эффект в отношении ряда инфекций (токсоплазмоз, пневмококковая пневмония и др.).
В России профилактическое лечение ПП проводится у больных с уровнем CD4-лимфоцитов менее 0,2x10 9 /л (первичная профилактика) и пациентов, ранее перенесших ПП (вторичная профилактика). При неизвестном уровне CD4-клеток профилактика пневмоцистоза проводится больным со стадией IIIБ в период клинической активности при наличии легочной патологии, а также всем больным со стадией IIIВ (по клинической классификации ВИЧ-инфекции, 1989). За рубежом показаниями к проведению химиопрофилактики пневмоцистоза являются эпизоды ПП в анамнезе, уровень CD4-лимфоцитов менее 0,2x10 9 /л, а также лихорадка неясного генеза в течение 2 недель [10].
Для профилактики применяется ко-тримоксазол (3 дня в неделю взрослым по 2 таблетки по 480 мг, детям – в соответствии с массой тела). Альтернативный режим – аэрозоль пентамидина по 300 мг/мес или в/в по 4 мг/кг в течение 2-4 недель, или дапсон по 200 мг в сочетании с пириметамином по 75 мг и фолиновой кислотой по 25 мг в неделю.
Для вторичной профилактики в течение 4 недель после окончания курса лечения острого процесса рекомендуется принимать ежедневно по 1 таблетке (480 мг) ко-тримоксазола (поддерживающая терапия), а затем, в случае отсутствия отрицательной клинической и рентгенологической динамики, перевести больного на схему первичной профилактики. При появлении признаков активации болезни переходят на ежедневный прием препарата в соответствии со схемой лечения.
Пневмоцистная пневмония – сложное в плане диагностики и лечения заболевание. Его вызывает дрожжеподобный грибок Pneumocystis jirovecii. Здоровым людям он не причиняет вреда, а при иммунодефиците становится причиной воспаления в легких.
В Юсуповской больнице диагностикой и лечением данной патологии занимаются высококвалифицированные врачи-пульмонологи. Мы проводим все виды лабораторной и инструментальной диагностики. Обязательно выполняются анализы, направленные на выявление ВИЧ-инфекции и других причин иммунодефицита. Обследование проводится оперативно, без очередей, благодаря чему удается своевременно установить правильный диагноз и назначить эффективную терапию.
Лечение пневмоцистной пневмонии сложно в том плане, что препараты, эффективные против грибка, зачастую вызывают выраженные побочные эффекты. Наши врачи составляют программу терапии индивидуально и тщательно контролируют состояние пациента в процессе, при необходимости своевременно проводят коррекцию назначений.
Пневмоцистная пневмония - что это?
Пневмоцистная пневмония – это заболевание, возбудителем которого является дрожжеподобный гриб Pneumocystis jirovecii.
В Юсуповской больнице диагностику и лечение проводят доктора высшей категории с использованием современной медицинской аппаратуры.

array(6) < ["ID"]=>string(5) "26413" ["WIDTH"]=> int(1024) ["HEIGHT"]=> int(682) ["SRC"]=> string(62) "/upload/sprint.editor/a44/53f94955e022400271bede3af16ddb2b.jpg" ["ORIGIN_SRC"]=> string(62) "/upload/sprint.editor/a44/53f94955e022400271bede3af16ddb2b.jpg" ["DESCRIPTION"]=> string(0) "" >
Причины пневмоцистной пневмонии
Заболевание вызывает одноклеточный организм пневмоциста. Гриб обитает в легочной ткани человека и для здоровых людей является не опасным. Пневмонию гриб вызывает только у людей с иммунодефицитными состояниями.
Основной группой риска являются ВИЧ-инфицированные люди. У них пневмоцистную пневмонию диагностируют в 70% случаев. Именно эта патология позволяет заподозрить у пациента СПИД.
Риск развития заболевания существует и у другой категории людей, а именно:
- у людей преклонного возраста;
- у детей младше одного года, рожденных раньше положенного срока, имеющих аномалии развития, а также перенесших асфиксию;
- у людей с диагнозом цирроз печени, туберкулез, системная красная волчанка, цитомегаловирусная инфекция и др.;
- у людей любой возрастной категории, проходящих курс лучевой терапии и лечение при помощи препаратов, угнетающих иммунную систему (глюкокортикостероидов, цитостатиков).
Передача пневмоцисты может происходить трансплацентарным путем (то есть от матери к ребенку), либо воздушно-капельным. Инкубационный период в среднем составляет неделю.
После перенесенной пневмоцистной пневмонии возможны повторные случаи заражения. К формированию стойкого иммунитета заболевание не приводит.

array(6) < ["ID"]=>string(5) "26416" ["WIDTH"]=> int(410) ["HEIGHT"]=> int(1024) ["SRC"]=> string(96) "/upload/sprint.editor/5c8/%D0%BB%D0%B5%D1%87%D0%BF%D0%BD%D0%B5%D0%B2%D0%B3%D1%80%D0%B0%D1%84.jpg" ["ORIGIN_SRC"]=> string(96) "/upload/sprint.editor/5c8/%D0%BB%D0%B5%D1%87%D0%BF%D0%BD%D0%B5%D0%B2%D0%B3%D1%80%D0%B0%D1%84.jpg" ["DESCRIPTION"]=> string(0) "" >
Симптомы пневмоцистной пневмонии
Симптомы проявления заболевания у взрослых и детей отличаются.
Патология у младенцев проявляется примерно на шестом месяце и характеризуется тремя стадиями:
- отечная. Это первые 7-10 дней. Наблюдается накопление слизи в альвеолоцитах. Характерными признаками данной стадии являются:
- нормальная или повышенная температура тела до 38° Цельсия;
- слабость;
- сухой кашель;
- снижение аппетита;
- потеря веса.
Ателектатическая (4 недели) – развивается альвеолярно-капиллярный блок. На данной стадии наблюдаются следующие симптомы:
- кашель с густой прозрачной мокротой;
- синюшность и бледность кожных покровов;
- появление одышки – до 80 дыханий в минуту.
У детей старшего возраста и взрослых пневмоцистная пневмония не имеет разделений по стадиям и проявляется характерными симптомами в виде:
- потери веса;
- снижения аппетита;
- одышки после физической нагрузки;
- потливости в ночное время суток;
- сухого кашля;
- тахикардии.
Особо тяжело заболевание протекает у пациентов с иммунодефицитными состояниями. Его проявлениями выступают:
- общая слабость;
- лихорадка;
- боли в области грудной клетки с втягиванием межреберных промежутков;
- сильный сухой кашель с пенистой мокротой.
array(6) < ["ID"]=>string(5) "26414" ["WIDTH"]=> int(1024) ["HEIGHT"]=> int(682) ["SRC"]=> string(62) "/upload/sprint.editor/386/19440b7b07bed6cb623e7a9b855236c3.JPG" ["ORIGIN_SRC"]=> string(62) "/upload/sprint.editor/386/19440b7b07bed6cb623e7a9b855236c3.JPG" ["DESCRIPTION"]=> string(0) "" >
Диагностика пневмоцистной пневмонии
Заболевание диагностируют на основании комплекса мероприятий, включающих:
- физикальное обследование;
- сбор анамнеза;
- лабораторные анализы;
- инструментальные методы.
Всем известно, что чем раньше диагностировано заболевание, тем легче и эффективнее проходит лечение. В случае любого недомогания следует в обязательном порядке обращаться за консультацией к доктору. В Юсуповской больнице практикуют ведущие специалисты в области медицины, они поставят точный диагноз и подберут индивидуальную программу лечения.
К сожалению, низкая квалификация врачей и плохая оснащенность государственных клиник приводят к тому, что пациентов лечат от заболеваний, которых у них никогда не было. Такие истории не редкость, и каждый слышал их от своих знакомых, друзей и родственников.
Чтобы не усугублять течение болезни и не лечить несуществующую патологию, следует обращаться за медицинской помощью только к профессионалам своего дела.
Высококвалифицированные доктора Юсуповской больницы безошибочно ставят диагноз на основании доказательной медицины, проводят необходимые исследований и ежедневно спасают жизни десяткам пациентов.
Лечение пневмоцистной пневмонии
Лечение заболевания осложняется тем фактом, что пневмоциста устойчива ко многим антибиотикам. Препараты, к которым возбудитель заболевания сохраняет устойчивость, очень часто имеют ряд побочных эффектов в виде нейропатии, лихорадки, сыпи и пр.
Врачи Юсуповской больницы разрабатывают для каждого пациента индивидуальный план терапии, сводя к минимуму проявления побочных явлений. Курс лечения составляет 14 дней, у ВИЧ-инфицированных – 21 день.
Чтобы записаться на прием к доктору в Юсуповскую больницу, где медицинские услуги предоставляются на высоком европейском уровне, достаточно позвонить телефону. Визит к врачу будет подобран в любое удобное для Вас время.
Пневмоцистная пневмония – это тяжелая форма интерстициального легочного воспаления, вызываемая пневмоцистами и развивающаяся на фоне выраженных иммунодефицитных состояний. Клиническое течение характеризуется нарастающей одышкой, непродуктивным кашлем, фебрильной лихорадкой, болями в груди, развитием сердечно-легочной недостаточности. Диагноз ставится на основании рентгенологических признаков, состояния иммунного статуса, лабораторной идентификации патогена в крови, БАЛ, мокроте, биоптате (ПЦР, серологические тесты, РНИФ). Для этиотропной терапии используются сульфаниламидные, противопротозойные, иммуномодулирующие средства.
МКБ-10


Общие сведения
Пневмоцистная пневмония (ПП) относится к оппортунистическим инфекциям, поражающим лиц с иммунодефицитом и иммуносупрессией. При этом большинство людей с нормальным уровнем иммунитета переносит пневмоцистную инфекцию в виде ОРВИ. Антитела к возбудителю имеют около 90% взрослого населения, около 10% являются бессимптомными носителями пневмоцист – именно они представляют наибольшую угрозу для иммунокомпрометированных пациентов. Пневмоцистная пневмония является самой тяжелой клинической формой пневмоцистоза.

Причины
Характеристика возбудителя
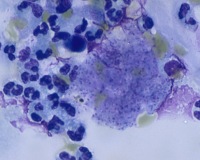
Pneumocystis jirovecii – микроорганизм, вызывающий пневмоцистную пневмонию и другие виды пневмоцистоза у человека. До недавнего времени пневмоцисты считались простейшими, однако в 1988 г. на основании ряда характерных генетических, морфологических и биохимических признаков были отнесены к грибам семейства актиномицетов. Пневмоцисты обладают тропизмом к легочной ткани, весь их жизненный цикл протекает внутри альвеол и проходит 4 стадии:
- Трофозоит. Представляет собой вегетативную стадию P. Jirovecii. Имеет амебоидную форму, диаметр 1-5 мкм, одно ядро и тонкую двухслойную мембрану. Прикрепляется к альвеолоцитам, где увеличивается в размерах и делится.
- Прециста. Имеет овальную форму, диаметр 5 мкм. В ранней стадии содержит одно ядро, окруженное митохондриями, на поздней – 2-6 ядер с мембранами.
- Циста. Зрелая циста округлой формы, с 3-слойной стенкой, диаметром 7-8 мкм. Внутри цисты содержится четное количество (обычно 8 шт.) внутрицистных телец ‒ спорозоитов.
- Спорозоит. При разрыве зрелых цист из них высвобождаются спорозоиты, часть которых обладает одинарным набором хромосом (являются гаплоидными). Сливаясь, они вновь образуют трофозоиты, и жизненный цикл патогена повторяется.
В описанном цикле различают две фазы: неполовую, или асексуальную (деление трофозоита), и половую, или сексуальную (спорозоит-трофозоит-прециста-циста).
Пути передачи
Источниками P. jirovecii являются носители (бессимптомные или больные ОРЗ) и больные пневмоцистной инфекцией. В 30% случаев выявляется вовлеченность в эпидемический процесс медицинских работников. При кашле и чихании носители выделяют мелкодисперсный аэрозоль, содержащий патогены. Заражение восприимчивого макроорганизма происходит при вдыхании контаминированного воздуха (воздушно-капельным, воздушно-пылевым путем). Воротами для входящей инфекции служат дыхательные пути. Редко реализуется трансплацентарный путь передачи.
Характерны внутрисемейные и внутрибольничные эпидемические вспышки пневмоцистной пневмонии. Последние чаще происходят в отделениях недоношенных, домах престарелых, инфекционных стационарах. Пик детской заболеваемости пневмоцистной пневмонией приходится на конец лета – начало осени, взрослые болеют круглогодично.
Группы риска
Пневмоцисты являются типичными оппортунистами, поскольку вызывают манифестную инфекцию только при выраженном дефиците клеточного и гуморального иммунитета у определенного контингента пациентов. К группам риска по заболеваемости пневмоцистной пневмонией относятся:
- ВИЧ-инфицированные и больные СПИДом;
- пациенты с ЦМВ-инфекцией;
- недоношенные дети и младенцы с ЗВУР;
- дети, страдающие гипотрофией, рахитом;
- больные, получающие иммуносупрессивную терапию (по поводу лейкозов, миеломной болезни, других видов рака, трансплантации органов, коллагенозов);
- пациенты с первичными иммунодефицитами, болезнями крови (анемией, полицитемией), туберкулезом, патологией почек.

Патогенез
Пневмоцисты присутствуют в дыхательных путях здоровых людей, но вызывают пневмоцистную пневмонию только у лиц с нарушением гуморального и клеточного звена иммунитета. Экспериментально доказано, что ведущую роль в механизме пневмоцистоза играет снижение Т-хелперов (критическим является снижение СД4+ лимфоцитов ˂300-200 клеток/мкл), увеличение количества цитотоксических лимфоцитов СД8+.
P. Jirovecii с помощью особых выростов – филоподий – прикрепляется к альвеолоцитам первого порядка и альвеолярным макрофагам. Клеточной адгезии также способствуют гликопротеины пневмоцистов, которые взаимодействуют с фосфолипидами, апопротеинами, мукополисахаридами, сурфактантом альвеолярного эпителия. В условиях иммунокомпрометации цисты размножаются, используя сурфактант-ассоциированные белки, выделяют токсические метаболиты.
Происходит разрушение альвеолоцитов, заполнение альвеол пенистым экссудатом, содержащим большое количество пневмоцист на разных стадиях развития, воспалительные клетки, детрит. Интерстициальная ткань инфильтрируется плазматическими клетками. Развивается интерстициальная плазмоклеточная пневмония. Межальвеолярные перегородки гипертрофируются, что приводит к резкому снижению диффузии газов (альвеолярно-капиллярный блок), формированию дыхательной недостаточности и тяжелой гипоксии.
Классификация
В соответствии с патоморфологическими критериями в современной пульмонологии выделяют три стадии пневмоцистной пневмонии:
- I стадия. Происходит прикрепление пневмоцист к альвеолярной стенке. Воспалительная реакция и клинические проявления отсутствуют.
- II стадия. Отмечается десквамация альвеолоцитов, увеличение числа возбудителей в форме цист в макрофагах. В эту стадию появляются начальные клинические проявления пневмоцистной пневмонии.
- III стадия. Развивается альвеолит, плазмоцитарная инфильтрация интерстиция, гигантские скопления пневмоцист в макрофагах и альвеолах. Соответствует разгару заболевания.
Этапы развития пневмоцистной пневмонии:
- отечная фаза ‒ длится 7-10 дней, характеризуется нарастанием симптоматики;
- ателектатическая фаза ‒ продолжается в течение 4-х недель, сопровождается выраженной легочной недостаточностью;
- эмфизематозная фаза – имеет различную длительность, знаменуется обратным развитием симптоматики.
Симптомы пневмоцистной пневмонии
Инкубационный период вариабелен – от 7-10 дней до 2-4 недель (у больных СПИДом – до 10 недель). В отечную стадию клинические признаки пневмоцистной пневмонии легко спутать с обычной респираторной инфекцией. Симптомы нарастают постепенно: вначале беспокоит слабость, недомогание, субфебрилитет. Затем появляется одышка при умеренной нагрузке, боли в грудной клетке, сухой кашель.
В ателектатической стадии лихорадка принимает фебрильный характер, усиливается интоксикационный синдром (отсутствие аппетита, снижение веса, потливость по ночам). Кашель становится коклюшеподобным, постоянным, особенно беспокоит в ночное время суток. Одышка до 30-50 дыхательных движений в минуту выражена в покое. Отмечаются бледность кожных покровов с носогубным цианозом, тахикардия. В этот период пациент может погибнуть от сердечно-легочной недостаточности (СЛН).
У выживших пациентов наступает эмфизематозная стадия. Температура тела снижается, дыхательные расстройства исчезают. В исходе пневмоцистной пневмонии формируется эмфизема легких, легочное сердце. Пневмоцистная пневмония часто протекает в ассоциации с туберкулезом легких.
Четкая стадийность при пневмоцистозе прослеживается в основном у детей раннего возраста. У ВИЧ-инфицированных болезнь имеет стертое затяжное течение, у ВИЧ-негативных лиц с иммунодефицитом – более активное, с быстрым нарастанием СЛН.
Осложнения
Типичными осложнениями, развивающимися в разгар болезни, являются пневмоторакс, подкожная эмфизема, пневмомедиастинум, возникающие вследствие разрыва мелких кистозных образований. Возможно развитие абсцедирующей пневмонии. Эти состояния еще более усугубляют дыхательную недостаточность, повышают летальность. При значительном подавлении иммунитета может произойти генерализация пневмоцистной инфекции с мультиорганным поражением печени, селезенки, ЖКТ, щитовидной железы, органов зрения и слуха, лимфоузлов, костного мозга.

Диагностика
Из-за неспецифичности и стертости симптоматики существенной проблемой является гиподиагностика пневмоцистной пневмонии. Иногда патология диагностируется только посмертно. Все больные с подозрением на ПП должны быть в срочном порядке проконсультированы врачом-пульмонологом, инфекционистом. При выставлении диагноза опираются на следующие данные:
Дифференциальная диагностика
Комплексное клинико-лабораторное, рентгенологическое и бронхологическое обследование позволяет отличить пневмоцистную пневмонию от других поражений легких:
- легочного кандидоза;
- криптококковой пневмонии;
- цитомегаловирусной пневмонии;
- микоплазменной пневмонии;
- хламидийной пневмонии;
- туберкулеза легких;
- респираторного криптоспоридиоза;
- саркомы Капоши;
- бактериальной пневмонии.
Лечение пневмоцистной пневмонии
Стандартные антибактериальные средства при ПП неэффективны. В настоящее время препаратами первой линии считаются комбинированные сульфаниламиды, оказывающие противомикробное, бактерицидное и противопротозойное действие. Могут назначаться как перорально, так и внутривенно. Курс лечения составляет 1-3 недели.
При выраженных токсических эффектах и резистентности подбираются другие антибиотики, активные в отношении пневмоцист (линкозамиды, противолепрозные, противомалярийные, антипротозойные препараты). Из-за массовой гибели патогенов в первые дни терапии состояние пациентов с пневмоцистной пневмонией может ухудшиться, в связи с чем целесообразно назначение кортикостероидов.
Прогноз и профилактика
Смертность от пневмоцистной пневмонии достигает 50% среди недоношенных детей, 25-40% ‒ среди больных СПИДом. У 10-30% иммунокомпрометированных пациентов через несколько месяцев после излечения возникают рецидивы ПП. При отсутствии лечения летальность 100%.
Профилактическая работа реализуется в двух направлениях: эпидемиологическом и медикаментозном. Первый аспект предполагает широкое тестирование на пневмоцистную инфекцию представителей групп риска: пациентов с ВИЧ, онкопатологией, иммунодефицитами, недоношенных детей, сотрудников роддомов и стационаров. Второе направление – это фармакопрофилактика пневмоцистной пневмонии у лиц с количеством СД4+ клеток ˂200. Она заключается в приеме сульфаниламидов в профилактических дозах длительными курсами.
1. Пневмоцистная пневмония. Этиология, патогенез, клиника, дифференциальная диагностика, лечение (лекция)/ Боровицкий В.С.// Проблемы медицинской микологии. – 2012.
2. Пневмоцистная пневмония: исторические, эпидемиологические, клинико-морфологические аспекты/ Марковский В. Д., Плитень О. Н., Мирошниченко М. С., Мирошниченко А. А.// Annals of Mechnikov Institute, - 2012. - №3.
3. Особенности пневмоцистной пневмонии у ВИЧ-инфицированных лиц/ Пузырёва Л.В., Сафонов А.Д., Мордык А.В.// Медицинский вестник Северного Кавказа. – 2016. – Т.11, №3.
4. Пневмоцистоз. Современное состояние проблемы/ Каражас Н.В.// Альманах клинической медицины. – 2010.
Пневмоцистоз – оппортунистическая инфекция дыхательных путей, чаще поражающая детей раннего возраста, а также лиц с ослабленным иммунитетом. Пневмоцистоз может протекать в форме ОРЗ, ларингита, обструктивного бронхита, обострения ХЗЛ, интерстициальной пневмонии. Диагностика пневмоцистоза основана на обнаружении пневмоцист в мокроте и бронхиальном секрете с помощью микроскопии и ПЦР; данных гистологического исследования биоптатов бронхов; рентгенографии и КТ легких, сцинтиграфии, спирографии. Для проведения противопневмоцистной терапии используются препараты сульфаметоксазол+триметоприм, пентамидин, комбинация триметоприма с дапсоном и другие схемы лечения.
МКБ-10
Общие сведения
Пневмоцистоз – легочная инвазия, вызываемая пневмоцистами и протекающая преимущественно в виде пневмоцистной пневмонии. Пневмоцистоз является иммунодефицит-ассоциированным инфекционным заболеванием, которым чаще всего болеют недоношенные дети, а также пациенты с первичными и вторичными иммунодефицитами. Смертельную опасность пневмоцистоз представляет для больных ВИЧ/СПИДом: при отсутствии лечения заболевание неизбежно заканчивается летальным исходом. Пневмоцистоз может возникать как спорадическая или внутрибольничная инфекция в отделениях педиатрии, гемобластозов, пульмонологии, противотуберкулезных инфекционных стационарах.

Причины пневмоцистоза
На сегодняшний день вопрос с видовой принадлежностью возбудителя пневмоцистоза окончательно не решен. В течение длительного времени микроорганизм Pneumocystis Carinii относили к простейшим класса споровиков. Однако в настоящее время доминирует точка зрения, что пневмоцисты занимают промежуточное положение между низшими и высшими грибами. В своем развитии пневмоцисты претерпевают 4 стадии: трофозоита, предцисты, цисты и спорозоита, протекающие на альвеоцитах. При разрыве оболочки созревшей цисты из нее выходят спорозоиты, которые проникают в легочные альвеолы, запуская очередной цикл стадийного развития пневмоцист новой генерации.
Источником эпидемиологической опасности выступает инвазированный человек (больной или носитель), выделяющий спорозоиты с частицами слизи во внешнюю среду при кашле или чихании. Передача возбудителей пневмоцистоза происходит по аспирационному механизму, воздушно-капельным, воздушно-пылевым, ингаляционным или аэрогенным путями. Считается, что среди клинически здоровых лиц до 10% являются носителями пневмоцист, однако у людей с нормально функционирующей иммунной системой инвазия протекает бессимптомно. Риску заболеваемости манифестными формами пневмоцистоза, главным образом, подвержены недоношенные новорожденные; дети с гипогаммаглобулинемией, гипотрофией, рахитом; больные ВИЧ/СПИДом и туберкулезом; пациенты, получающие иммуносупрессивную терапию по поводу коллагенозов, злокачественных новообразований, гематологических и лимфопролиферативных заболеваний, трансплантации органов и пр.
Пневмоцистоз развивается при снижении количества СД4+ клеток (Т-хелперов) в 4 и более раз по сравнению с нормой и достижении уровня менее 200 клеток в 1 мкл. При нарушении клеточного и гуморального иммунитета пневмоцисты начинают активно размножаться в альвеолах, вызывая развитие реактивного альвеолита, образование пенистого альвеолярного экссудата, содержащего пневмоцисты, лейкоциты, клеточный детрит и фибрин. При прогрессировании патологического процесса возникают участки ателектазов в легких, буллезное вздутии легочной ткани, что сопровождается нарушением вентиляции и газообмена, развитием дыхательной недостаточности.
Симптомы пневмоцистоза
В клиническом течении пневмоцистоза выделяют отечную (1-7 недель), ателектатическую (около 4-х недель) и эмфизематозную стадии. У части больных пневмоцистоз может протекать в виде ларингита, обструктивного или астматического бронхита, бронхиолита; в остальных случаях развивается пневмоцистная пневмония.
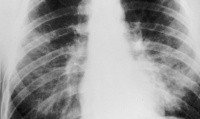
Инкубационный период пневмоцистоза занимает от 10 дней до 2-5 недель. Проявления отечной стадии развиваются постепенно и на ранних этапах включают в себя субфебрилитет, слабость, вялость. В конце первого периода присоединяется сухой кашель, тахипноэ, одышка. Признаками развивающегося пневмоцистоза у грудных детей может служить вялое сосание, отказ от кормления, плохая прибавка в массе тела, цианоз носогубного треугольника. Рентгенологические изменения в легких в отечной стадии пневмоцистоза отсутствуют; аускультативно определяется жестковатое дыхание, мелко- и среднепузырчатые хрипы; перкуторно - тимпанит в верхних отделах грудной клетки.
В ателектатической стадии пневмоцистоз может осложниться развитием пневмоторакса, экссудативного плеврита, легочного сердца, отека легких, а в случае присоединения бактериальной или грибковой инфекции – абсцессом легких. Летальные исходы в этот период обычно обусловлены дыхательной и сердечной недостаточностью. Третья, эмфизематозная стадия пневмоцистоза характеризуется уменьшением одышки и улучшением общего состояния больных. В исходе пневмоцистоза развивается эмфизема легких, сопровождающаяся значительным снижением показателей функции внешнего дыхания.
Диагностика
Клинические, физикальные и рентгенологические данные при пневмоцистозе не являются патогномоничными, что затрудняет своевременную диагностику заболевания. Между тем, пневмоцистную пневмонию всегда следует исключать у иммунокомпрометированных пациентов. С целью верификации пневмоцистоза проводится комплекс лабораторных и инструментальных исследований.
Для подтверждения диагноза пневмоцистоза выполняется бронхоскопия с забором бронхиального секрета, трансбронхиальная биопсия легкого, сцинтиграфия легких с галлием-67. Для лабораторной детекции P.carinii микроскопически исследуются окрашенные мазки мокроты, бронхиальный и трахеальный аспират; выполняется гистологическое исследование биоптатов, исследование мокроты методом ПЦР. Проводится иммунологическая диагностика: определение титра противопневмоцистных IgG и IgM в сыворотке крови с помощью РИФ и ИФА. Дифференциальную диагностику пневмоцистоза необходимо проводить с цитомегаловирусной, хламидийной, уреаплазменной, бактериальной пневмонией, туберкулезом легких, саркомой Капоши и др.
Лечение пневмоцистоза
Лечение пневмоцистоза проводится в стационаре. Лица с иммунодефицитом и недоношенные дети должны быть помещены в отдельные стерильные палаты с ламинарным воздушным потоком. В большинстве случаев для проведения специфической фармакотерапии пневмоцистоза используется комбинированные препараты (сульфаметоксазол+триметоприм, триметоприм+дапсон), пентамидин, эфлорнитин, атоваквон в течение 2-3 недель. Для устранения побочных эффектов терапии назначают фолиевую кислоту, глюкокортикоиды. Проводится инфузионная терапия (введение гамма-глобулина, солевых растворов, глюкозы, плазмы крови, альбумина и др.), кислородотерапия. У больных ВИЧ-инфекцией этиотропная терапия пневмоцистной пневмонии сочетается с высокоактивной антиретровирусной терапией.
Прогноз
Выживаемость при пневмоцистозе составляет 75-90%, а при повторном развитии пневмоцистной пневмонии – 60%. У 25-60% ВИЧ-инфицированных в течение года отмечаются рецидивы заболевания, поэтому больные нуждаются в проведении противорецидивного курса химиотерапии.
Читайте также:

