Гепатит с лечение рекомендации 2014
Обновлено: 18.04.2024
Проведен анализ существующих схем комбинированной противовирусной терапии хронического гепатита С. Комбинирование агентов с прямым противовирусным действием значительно снижает риск резистентности, увеличивая вероятность эрадикации вируса. Проведена оценк
This article contains analysis of current combination treatment regimens for chronic hepatitis C. Combination of agents with direct antiviral effect considerably reduces risk of resistance, increasing probability of virus eradication. A critical estimation of interferon-free modes of antiviral therapy of chronic hepatitis C according to the analysis of clinical studies. Interferon-free variants of treatment have certain advantages over modes of interferon-? based treatment.
Значимость проблемы хронического гепатита С (ХГС) определяется не только самим заболеванием, но и ростом риска формирования отдаленных неблагоприятных последствий в исходе заболевания, что влечет за собой огромные человеческие, социальные и экономические затраты. Около 170 млн человек инфицированы вирусом гепатита С (ВГС), в 10 раз больше, чем ВИЧ; более 350 тысяч человек умирают ежегодно от болезней, связанных с гепатитом C [1, 2]. Показано, что хроническая форма инфекции вызывает формирование цирроза (ЦП) до 20% случаев, а гепатоцеллюлярной карциномы у 1–5% пациентов [2, 3].
ХГС является одной из наиболее серьезных проблем здравоохранения РФ в связи с широким распространением, потенциальной угрозой жизни, а также отсутствием государственных программ противовирусного лечения. Общее число больных ХГС в Российской Федерации оценивается на сегодняшний день в 2,5–3,2 млн, из которых более половины инфицировано 1-м генотипом вируса [4, 5]. В настоящее время установить индивидуальный для пациента риск развития прогрессирующего заболевания печени невозможно, поэтому все больные ХГС (при компенсированной ее функции), ранее не получавшие лечения, вне зависимости от исходной биохимической активности, должны рассматриваться как кандидаты для проведения противовирусной терапии (ПВТ). Причинная связь между заболеванием печени и инфекцией ВГС должна быть доказана. Перед началом ПВТ необходимо оценить тяжесть поражения печени (стадию заболевания) и базовые вирусологические параметры (уровень вирусной нагрузки, генотип ВГС, а также субтип 1-го генотипа ВГС). Особого внимания требует стадия заболевания, поскольку жизненный прогноз и вероятность ответа на ПВТ у пациента с циррозом существенно отличаются от таковых у пациентов без ЦП [1, 5, 6].
Долгое время золотым стандартом терапии ХГС считалась комбинированная двойная терапия пегилированными интерферонами с рибавирином, которая наименее эффективна у больных с 1-м генотипом и продвинутым фиброзом печени [1, 5–7]. Появление за рубежом, а затем и в России препаратов прямого противовирусного действия (ПППД) привело к революционным изменениям в терапии больных ХГС и расширило показания к лечению пациентов, ранее не имевших шансов [8, 9]. Включение ПППД в схемы тройной терапии ХГС, вызванного вирусом 1-го генотипа, значительно повысило эффективность (до 69–85%), но не улучшило безопасность и качество жизни пациентов во время терапии [9–11]. Появившиеся в 2012 г. данные об эффективности ПППД дали начало новой безинтерфероновой эры лечения ХГС, а с 2014 г. по результатам клинических исследований началась регистрация безинтерфероновых режимов противовирусной терапии во всем мире. В настоящем обзоре представлены данные об основных классах ПППД, а также наиболее актуальные режимы безинтерфероновой ПВТ для лечения больных с ХГС без ЦП.
Препараты прямого противовирусного действия — это вещества, которые специфическим образом нарушают репликацию вируса за счет прямого взаимодействия с вирусными протеинами или нуклеиновыми кислотами [8, 9, 12]. За основу их классификации взяты белки-мишени, с которыми непосредственно взаимодействуют препараты (табл. 1). Выделяют классы ингибиторов протеазы NS3/4A, ингибиторов NS5A, ингибиторов полимеразы NS5B и другие (табл. 1).
Ингибиторы полимеразы NS5B (табл. 1), связываясь с РНК-зависимой РНК-полимеразой, нарушают жизненный цикл вируса [14, 19]. Данный класс препаратов делится на две группы: нуклеоз(т)идные и ненуклеозидные ингибиторы полимеразы NS5B. Мишенью нуклеоз(т)идных аналогов является высококонсервативный для всех генотипов ВГС каталитический сайт фермента; они прекращают синтез РНК, характеризуются мощной противовирусной активностью в отношении всех генотипов (1–6), высоким барьером резистентности, низким потенциалом межлекарственных взаимодействий [15]. Софосбувир — это уридиновый нуклеозидный аналог, единственный из этой группы ПППД, для которого завершены клинические исследования (КИ) третьей фазы, и в настоящее время он одобрен для применения в США, европейских и других странах, а с марта 2016 г. и в РФ [14, 16, 21]. В КИ софосбувиром было пролечено в общей сложности около 3 тысяч пациентов, в том числе с ЦП и ожидающих трансплантации печени. При клиренсе креатинина более 30 мл/мин, а также при тяжелом поражении печени (тяжелый фиброз и цирроз) коррекции дозы софосбувира не требуется. Прием пищи не оказывает существенного влияния на фармакокинетику [16, 21]. Софосбувир, как препарат с высоким барьером резистентности, может применяться в качестве основного препарата в комбинациях ингибиторов протеазы с NS3/4A, ингибиторами NS5A, рибавирином. Ненуклеозидные аналоги (ННА), мишенью для которых является один из четырех аллостерических сайтов полимеразы NS5B, ингибируют начальную стадию синтеза РНК, обладают узкой направленностью (в основном действуют на 1b генотип), меньшей противовирусной активностью и низким барьером резистентности. В связи с чем дальнейшая разработка некоторых препаратов данной группы (делеобувир (BI), филибувир, тегобувир) была остановлена [12, 15].
Ингибиторы NS5A блокируют репликацию вируса, вирусную сборку и высвобождение из клетки. Двойной механизм действия обеспечивает быстрое снижение вирусной нагрузки непосредственно после начала приема препаратов [17–19]. Ингибиторы первого поколения (табл. 1) эффективны в отношении 1-го и 4-го генотипов, некоторые активны и в отношении 2-го и/или 3-го генотипов, характеризуются низким барьером резистентности, особенно в отношении 1а и 3-го генотипов. Даклатасвир, первый в своем классе, обладает высокой противовирусной активностью, может применяться в составе интерферон-содержащих и безинтерфероновых режимов [19–21].
Эффективность безинтерфероновой ПВТ зависит от высокой противовирусной активности комбинации ПППД и их барьера резистентности. Препараты прямого действия всех классов имеют выраженную противовирусную активность и обеспечивают выраженное снижение вирусной нагрузки в первые три дня приема препарата и ее дальнейшее постепенное снижение во вторую фазу. В то же время их профиль резистентности существенно отличается. Высокий барьер резистентности является отличительной чертой всех представителей класса нуклеоз(т)идных ингибиторов NS5B. Ингибиторы NS3/4А, ингибиторы NS5A второго поколения характеризуются уже значительно более высоким барьером резистентности [21]. В процессе исследований возникло понимание необходимости применения комбинаций ПППД для преодоления вирусной резистентности, которая может стать значимой проблемой в связи с особенностями репликации возбудителя. Сочетая препараты ПППД разных классов, можно предотвратить развитие лекарственной устойчивости [21].
С 2015 г. доступные безинтерфероновые режимы терапии более предпочтительны за счет эффективного вирусологического ответа, простоты применения и хорошей переносимости [1, 5, 21]. Показания к терапии зависят от генотипа/субтипа ВГС, тяжести заболевания печени и/или результатов предшествующей терапии (табл. 2).
Полный анализ результатов лечения 513 больных ХГС с 1-м генотипом и компенсированным ЦП, прошедших лечение комбинированным препаратом с рибавирином и без него, выявил, что средняя частота УВО 12 недель составила 95% (305/322) после 12 недель лечения и 90% после 24 недель терапии (188/191). Отмечено, что ни продолжительность лечения, ни включение рибавирина в схему терапии не оказали действия на частоту достижения УВО у пациентов без предшествующей терапии в анамнезе. В группе с предшествующей интерферонотерапией частота УВО12 была достигнута в 90% случаев после 12 недель лечения без рибавирина и в 96% случаев с рибавирином. После 24 недель терапии УВО был в 98% случаев лечения без рибавирина и в 100% случаев с рибавирином этой комбинации. Результаты исследования показали равную эффективность схем с рибавирином и без него при длительности лечения 8 и 12 недель у больных без ЦП. Исключение из схемы лечения рибавирина снижало частоту НЛЯ [26–28].
Таким образом, в настоящее время для лечения ХГС в мире и в России начали успешно применяться безинтерфероновые режимы с высокой эффективностью, минимальным влиянием на качество жизни и существенным повышением безопасности и переносимости. Частота достижения УВО при назначении комбинаций препаратов прямого противовирусного действия практически не зависит от негативных факторов пациента и вируса, которые определяли эффективность терапии пегелированным интерфероном и рибавирином. Это позволило полностью исключить интерфероны из схемы и достигнуть значительного повышения эффективности лечения. При этом сократилась продолжительность терапии, повысилось удобство, исчезли правила отмены, отпала необходимость оценки большинства предикторов эффективности, появилась возможность назначать лечение пациентам, не ответившим на ПВТ, с ЦП и без него, с сопутствующей патологией [27]. Удачный опыт использования безинтерфероновых режимов вселяет оптимизм и позволяет с надеждой смотреть на перспективу более широкого применения комбинаций препаратов прямого противовирусного действия в терапии больных хроническим гепатитом С.
Литература
Ж. Б. Понежева, доктор медицинских наук
И. В. Семенова 1 , доктор медицинских наук
ФБУН ЦНИИ эпидемиологии Роспотребнадзора РФ, Москва
РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ВЗРОСЛЫХ БОЛЬНЫХ ГЕПАТИТОМ С
СОСТАВ РАБОЧЕЙ ГРУППЫ МИНЗДРАВА РОССИИ И АВТОРСКИЙ КОЛЛЕКТИВ
Сопредседатели рабочей группы:
академик РАН, профессор Ивашкин Владимир Трофимович, ГБОУ ВПО "Первый Московский государственный медицинский университет им.И.М.Сеченова" Минздрава России, кафедра пропедевтики внутренних болезней;
академик РАН, профессор Ющук Николай Дмитриевич, ГБОУ ВПО "Московский государственный медико-стоматологический университет им.А.И.Евдокимова" Минздрава России, кафедра инфекционных болезней и эпидемиологии.
Ответственные исполнители:
профессор Климова Елена Анатольевна, ГБОУ ВПО "Московский государственный медико-стоматологический университет им.А.И.Евдокимова" Минздрава России, кафедра инфекционных болезней и эпидемиологии;
профессор Маевская Марина Викторовна, ГБОУ ВПО "Первый Московский государственный медицинский университет им.И.М.Сеченова" Минздрава России, кафедра пропедевтики внутренних болезней.
ГБОУ ВПО "Московский государственный медико-стоматологический университет им.А.И.Евдокимова" Минздрава России
Кафедра инфекционных болезней и эпидемиологии:
Знойко Ольга Олеговна, доктор медицинских наук, профессор;
Максимов Семен Леонидович, доктор медицинских наук, профессор.
Кафедра пропедевтики внутренних болезней и гастроэнтерологии:
Маев Игорь Вениаминович, член-корреспондент РАН, доктор медицинских наук, профессор.
ГБОУ ВПО "Первый Московский государственный медицинский университет им.И.М.Сеченова" Минздрава России
Кафедра пропедевтики внутренних болезней:
Павлов Чавдар Савович, доктор медицинских наук, профессор.
ГУЗ г.Москвы "Инфекционная клиническая больница N 1" ДЗ г.Москвы
Малышев Николай Александрович, доктор медицинских наук, профессор;
Блохина Наталья Петровна, доктор медицинских наук, профессор.
ГБОУ ВПО "Российский национальный исследовательский медицинский университет им.Н.И.Пирогова" Минздрава России
Никитин Игорь Геннадьевич, доктор медицинских наук, профессор.
ГБОУ ВПО "Санкт-Петербургский медицинский университет им. акад. И.П.Павлова" Минздрава России
Рахманова Аза Гасановна, доктор медицинских наук, профессор.
ФБУН "Центральный научно-исследовательский институт эпидемиологии" Роспотребнадзора
Чуланов Владимир Петрович, доктор медицинских наук.
ФГБУ "Научно-исследовательский институт вирусологии им.Д.И.Ивановского" Минздрава России
Шахгильдян Иосиф Васильевич, член-корреспондент РАН, доктор медицинских наук, профессор.
ФГБУ "Институт хирургии им.А.В.Вишневского" Минздрава России
Чжао Алексей Владимирович, доктор медицинских наук, профессор;
Андрейцева Ольга Ивановна, кандидат медицинских наук.
СПИСОК СОКРАЩЕНИЙ
- сердцевинный протеин вируса гепатита С
- поверхностный антиген вируса гепатита В
- неструктурный белок 3 ВГС
- неструктурный белок 4 ВГС
- неструктурный белок 5 ВГС
- антитела к вирусу гепатита D
- антитела к вирусу гепатита А
- антитела к вирусу гепатита С
- антитела к вирусу гепатита Е
- активированное частичное тромбопластиновое время
- быстрый вирусологический ответ
- вирус гепатита С
- вирус гепатита В
- вирус гепатита D
- вирус иммунодефицита человека
- индекс массы тела
- медленный вирусологический ответ
- международное нормализованное отношение
- острый гепатит С
- продленный быстрый вирусологический ответ
- пункционная биопсия печени
- полимеразная цепная реакция
- пегилированный интерферон альфа-2а
- пегилированный интерферон альфа-2b
- ранний вирусологический ответ
- устойчивый вирусологический ответ
- хронический гепатит С
- обозначение торговых наименований препаратов
ВВЕДЕНИЕ
К настоящему времени накоплен большой опыт ведения и лечения пациентов с гепатитом С, который положен в основу представленных рекомендаций.
Вирус гепатита С (ВГС) был открыт более 20 лет назад. В настоящее время абсолютно очевидны серьезные проблемы, связанные с данной инфекцией: высокая частота формирования хронических форм, длительное бессимптомное течение, манифестация заболевания на поздних стадиях (цирроз печени), четкая ассоциация с развитием гепатоцеллюлярной карциномы.
Известно, что вирус гепатита С имеет 6 генотипов и большое число подтипов. В Российской Федерации распространены по убывающей частоте генотипы 1, 3, 2. Среди подтипов чаще встречается 1в, чем 1а, что аналогично европейской популяции, а также 3а. Генотипы 4-6 практически не встречаются в популяции Российской Федерации.
В структуре гепатита С отмечено увеличение числа больных с генотипом 3а. Выявлена значительная частота сочетания гепатита С с гепатитом В. Маркеры вируса гепатита В (ВГВ) обнаруживаются у пациентов с ХГС в 22% случаев, что делает обоснованной целесообразность вакцинации против ВГВ больных ХГС.
Установлена низкая частота перинатальной передачи ВГС от матерей с ХГС родившимся у них детям (3,5%), в то время как у женщин с сочетанием ХГС с ВИЧ-инфекцией перинатальная передача ВГС составила 14-16% [5-7, 22, 23, 25-27, 32].
Рекомендации по диагностике и лечению взрослых больных гепатитом С разработаны экспертной группой по вопросам вирусных гепатитов в соответствии с поручением министра здравоохранения Российской Федерации от 6 августа 2012 г. N 68 и служат руководством для практических врачей, осуществляющих ведение и лечение таких пациентов на разных стадиях заболевания. Рекомендации включают в себя разделы, посвященные скринингу и диагностике острого и хронического гепатита С, алгоритмы обследования пациентов и этиотропного лечения острого и хронического гепатита С. Подробно рассмотрены показания и противопоказания к терапии, противовирусное лечение с применением двойной и тройной схемы терапии, нежелательные явления лекарственной терапии и методы их коррекции, реакции взаимодействия между лекарственными средствами, лечение отдельных групп пациентов и др.
Что такое гепатит Е? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит Е — это острое (и редко хроническое) инфекционное заболевание, которое вызывает вирус гепатита Е. Клинически проявляется синдромом общей инфекционной интоксикации, энтерита (воспаления тонкой кишки) и холестаза (застоя желчи), желтухой, увеличением и нарушением работы печени. Болезнь протекает доброкачественно, за исключением беременных, у которых заболевание имеет катастрофические последствия в любом триместре беременности.
Этиология
Вид — вирус гепатита Е (HЕV)
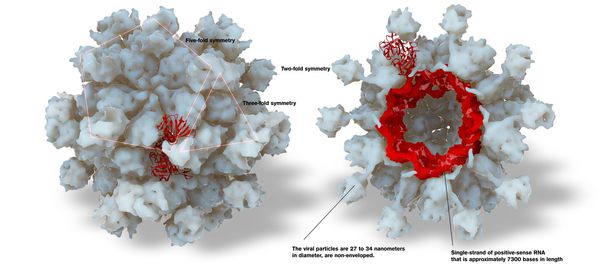
Данный вирус представляет собой одноцепочечный РНК-вирус округлой формы диаметром 30-35 нм. Он лишён наружной оболочки. На поверхности вириона есть вдавления, напоминающие чаши.
Чтобы вирус внедрился в клетку, в процессе жизни он кодирует трансмембранный белок и такие ферменты, как РНК-зависимую РНК-полимеразу, РНК-хеликазу, метилтрансферазу и папаин-подобную протеазу.
Существует пять генотипов вируса:
- I и II — только человеческие;
- III и IV — есть также у животных, т. е. может передаваться от них людям; вызывает хронические формы, если есть предрасположенность;
- V — птичий.
При температуре от 0°C быстро инактивируется. Длительно сохраняется в воде и при отрицательных температурах. Неплохо себя чувствует в ЖКТ человека. Хорошо сохраняется в плохо прожаренном мясе. При нагревании воды до 71°C погибает в течение 20 минут, при кипячении — практически мгновенно [1] [2] [3] [8] [10] .
Эпидемиология
Источник инфекции — вирусоноситель или человек, который уже болен какой-либо формой гепатита Е, в особенности острой. Вирус распространяется с последней недели инкубационного периода и до 30 дней от начала заболевания.
Каждый год повсеместно регистрируется около 3,3 млн случаев заболевания. При этом количество людей с гепатитом Е, который протекает пока без симптомов или совсем себя не проявляет, по предварительным оценкам может достигать 20 млн. Смертность — около 4 %, преимущественно умирают беременные.
В окружающую среду вирус выделяется с экскрементами инфицированных людей. Иногда человек заражается при употреблении недостаточно приготовленного мяса свиней, оленей и моллюсков.
- фекально-оральный — через заражённые вирусом руки (контактно-бытовой путь), воду или пищу;
- парентеральный — при переливании крови (встречается редко);
- половой путь — при орально-анальном контакте;
- вертикальный — от матери к плоду.

Наибольшее значение имеет водный путь передачи. Часто он связан с сезоном дождей и наводнениями, когда вода загрязняется фекалиями.
Восприимчивость к гепатиту Е высокая. Преимущественно болеют люди 15-44 лет. К группе повышенного риска относятся работники животноводческих ферм и боен.
Факторы риска заражения:
- высокая плотность населения, особенно в бедных странах;
- антисанитария, несоблюдение правил личной гигиены, неправильное хранение, обработка и приготовление пищи;
- нарушения санитарно-технических требований на объектах водоснабжения — заражение воды;
- бытовой очаг заболевания.
Заболевание обычно возникает в осенне-весенний период. В основном распространено в странах Восточной и Южной Азии.
После перенесённой болезни формируется стойкий иммунитет, чаще пожизненный [1] [3] [7] [9] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Е
Болезнь начинается постепенно. Инкубационный период длится от 2 до 10 недель.
Как и в случае гепатита А, заболевание обычно протекает в бессимптомной и субклинической (предсимптомной) форме.
При возникновении явных клинических признаков (т. е. при манифестации), преобладают случаи лёгкого и среднетяжёлого течения. Симптоматика медленно нарастает. Появляется немотивированная слабость, подташнивание, снижение аппетита, повышение температуры до 37,1-38,0°С (субфебрилитет), дискомфорт и тяжесть в правом подреберье, дискомфорт в суставах, возможна рвота.
Вслед за этими симптомами через 3-7 дней наступает желтушный период, который длится максимум один месяц. Он сопровождается пожелтением кожи и слизистых оболочек, потемнением мочи и обесцвечиванием кала. Общее состояние больных не улучшается, сохраняется плохое самочувствие, выраженный дискомфорт в правом подреберье, увеличение размеров печени и селезёнки, желтушность кожных покровов, нарастает зуд кожи.
При неосложнённом и нетяжёлом течении начинает медленно регрессировать в течение нескольких недель. Как правило, после этого человек полностью выздоровливает, иногда развиваются непродолжительные остаточные явления в виде астении (бессилия) и дискомфорта в правом подреберье.
Раньше считалось, что гепатит Е — лишь острое заболевание. Однако в последнее время накоплен ряд данных, позволяющих выделить небольшую группу больных, переносящих хронический вариант болезни. Он встречается у ВИЧ-инфицированных людей в стадии СПИДа, после пересадки органов, а также у тех, кто получает мощную иммуносупрессивную терапию.
Специфичной симптоматики у хронического гепатита А нет. Больные жалуются на повышенную утомляемость, артралгии, неустойчивый стул, тяжесть в правом подреберье, субфебрилитет, иногда устойчивый лёгкий зуд кожи. Если не лечить это состояние, может развиться цирроз печени.
Гепатит Е у беременных
При заражении беременной в I и II триместрах происходит 100 % гибель плода. Летальность самих беременных невелика.
При заражении беременной в III триместре ребёнок может родиться живым, но 50 % из них умирают в первые месяцы жизни. Смертность самих женщин достигает 25-30 %. А если беременные живут в районах, которым не свойственно данное заболевание, то летальность может достигать 80 %.
Тяжесть течения Гепатита А при беременности связана со специфической аутоиммунной перестройкой организма женщины. В этом случае заболевание часто протекает по фульминантному типу (острой печеночной недостаточности) — на фоне начальных симптомов болезни резко нарастает желтуха, развивается тяжёлая интоксикация, некупируемая рвота, кровотечения (ДВС-синдром), нарушается сознание. Роды (преждевременные или выкидыш) стремительно ухудшают состояние больной: развиваются массивные послеродовые кровотечения, острая почечная недостаточность, печеночная энцефалопатия. Из-за такого состояния в острый период искусственно прерывать беременность нельзя [1] [5] [6] [8] [9] .
Патогенез гепатита Е
В цитоплазме гепатоцитов внешняя оболочка вируса вируса раскрывается, и запускается выработка вирусных белков. Одновременно с этим происходит подготовка клетки-хозяина к этому процессу.
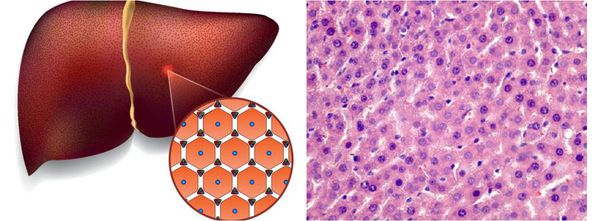
Во время своей жизни вирус напрямую провоцирует дегенеративные изменения в гепатоцитах, в т.ч. вызывая их гибель по типу баллонной дистрофии — переполнение клетки жидкостью. После этого готовые вирусные частицы распространяются и заражают новые здоровые клетки.
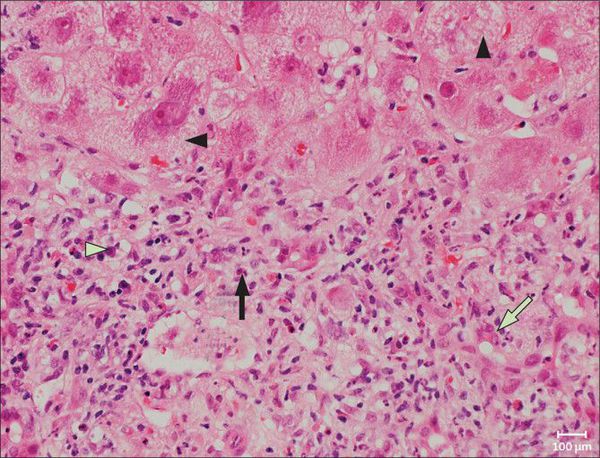
Со временем в организме формируются специфические антитела, которые позволяют полностью вывести вирус из организма человека (за исключением случаев выраженного угнетения иммунитета).
Тяжёлое течение гепатита Е у беременных не связано со свойствами вируса напрямую. Оно вызвано лишь иммунологической перестройкой иммунной защиты беременных. Из-за этого развивается каскад иммунопатологических и гормональных реакций, которые приводят к массированному некрозу гепатоцитов, дефициту плазменных факторов свёртывания и внутрисосудистому гемолизу — разрушению эритроцитов крови [1] [2] [3] [5] [10] .
Классификация и стадии развития гепатита Е
По клиническим признакам выделяют два варианта заболевания:
- безжелтушная форма — до появления симптомов или при освобождении организма от вируса и формировании стойкого иммунитета;
- желтушная форма — при нарастании симптомов.
По тяжести процесса гепатит Е делят на четыре степени:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная, гепатит у беременных).
Факторы риска развития тяжёлого течения болезни:
- беременность любого триместра (наиболее неблагоприятно заболевание протекает в III триместре);
- пожилой возраст:
- мужской пол;
- иммуносупрессивная терапия (на фоне трансплантации органов); ;
- комбинированная соматическая патология (сахарный диабет, ишемическая болезнь сердца, аутоиммунный гепатит, пациенты на гемодиализе);
- наличие хронической вирусной патологии печени (вирусные гепатиты В и С);
- алкоголизм.
По исходу заболевание бывает трёх типов:
- с выздоровлением (полным, с остаточными явлениями);
- с хронизацией;
- с неблагоприятным прогнозом (у беременных) [4][5][6] .
Осложнения гепатита Е
Осложнения при гепатите Е можно разделить на три группы:
- Истинные (печёночные) осложнения:
- острая печёночная недостаточность — осложнение с неблагоприятным исходом, при котором быстро развивается массивное повреждение ткани печени (до 90 %), резкое нарушаются её функции, возникает печёночная энцефалопатия (нарушение работы мозга), геморрагический синдром (повышенная кровоточивость) и коагулопатия (нарушение свёртывания крови);
- холестаз — нарушение синтеза и выведения желчи (желтуха), осветление кала и потемнение мочи, появление выраженного кожного зуда и чувства горечи во рту;
- тромбо-геморрагический синдром у беременных (ДВС-синдром) — кровотечения и кровоизлияния различной интенсивности и направленности;
- преждевременные роды или выкидыш у беременных.
- Внепечёночные осложнения: — острое неврологическое заболевание, которое сопровождается нарушением чувствительности в руках и ногах, мышечной слабостью и иногда параличом.
- острый поперечный миелит — нарушение всех функций спинного мозга;
- различные нейропатии и полирадикулопатии;
- панкреатит — тошнота, рвота, опоясывающие боли в животе; — боли в поясничной области, нарушение мочеобразования, повышенная потеря эритроцитов и белка с мочой;
- повышение вероятности развития рака кожи и заболеваний кровеносной системы.
- Резидуальные (постгепатитные) явления:
- дискинезия (нарушение моторики) желчевыводящих путей — застой желчи, чувство тошноты, отрыжка, горечь во рту;
- постгепатитная гепатомегалия — увеличение печени в связи с разрастанием соединительной ткани;
- постгепатитный синдром — повышенная утомляемость, астения, раздражительность, чувство тошноты и дискомфорта в правом подреберье [1][2][6][7][8] .
Диагностика гепатита Е
Лабораторная диагностика:
- Клинический анализ крови — нормальный объём эритроцитов или умеренная лейкопения, повышение количества лимфоцитов, моноцитов и снижение нейтрофилов в крови, сниженная или нормальная СОЭ.
- Биохимический анализ крови — повышенный уровень общего билирубина за счёт прямой и непрямой фракции, увеличение АЛТ и АСТ, сниженый индекс протромбина (ПТИ), повышение тимол-вероналоовой пробы (уменьшение альбуминов и увеличение гамма-глобулинов), повышение ГГТ и щелочной фосфатазы.
- Общий анализ мочи — появление гематурии, протеинурии и цилиндрурии (обнаружение эритроцитов, белка и цилиндров в моче).
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина.
- Серологические тесты — обнаружение антител в сыворотке крови:
- анти-HЕV IgM — выявляются при острой инфекции с конца первой недели от момента заражения, могут сохраняться до двух лет, иногда бывают ложноположительными при активной ЦМВ-инфекции;
- анти-HЕV IgG — выявляются с 41 дня в течение 15 лет методом иммуноферментного анализа (ИФА);
- HЕV RNA — выявляются при острой инфекции, начиная с 22 дня, а также при хронизации в течение долгого времени благодаря полимеразной цепной реакции (ПЦР).
- УЗИ органов брюшной полости — увеличение печени с реактивным изменением структуры её ткани, увеличение лимфоузлов в воротах печени, иногда увеличена селезёнка.
Дифференциальная диагностика с другими заболеваниями:
- Вирусные гепатиты В и С — связь с парентеральными вмешательствами (например, с переливанием крови), более длительный преджелтушный период, характерные серологические тесты. , желтушная форма — выраженный синдром общей инфекционной интоксикации, увеличение лимфоузлов, тонзиллит, специфические изменения общей крови и серологические тесты.
- Жёлтая лихорадка — острое начало, высокая температура, гиперемия и отёчность лица, временное улучшение, а затем ухудшение состояния. — острое начало, высокая температура, частое поражение почек, выраженные боли в икроножных мышцах, изменения общей крови бактериального характера.
- Псевдотуберкулёз — умеренно высокая температура, мезаденит (воспаление лимфоузлов брыжейки кишечника), терминальный илеит (воспаление подвздошной кишки), симптомы носков и капюшона (мелкоточечные высыпания), скарлатиноподобная сыпь, бактериальные изменения крови, специфические маркеры.
- Острые кишечные инфекции, например, сальмонеллёз — острое начало, выраженный синдром поражения ЖКТ (энтерит, колит, высокая температура).
- Листериоз — высокая температура, увеличение лимфоузлов, поражения железистой ткани ротоглотки, бактериальная кровь.
- Сепсис — гектическая (изнуряющая) лихорадка, выраженные полиорганные нарушения.
- Амебиаз — характерные симптомы поражения кишечника, эозинофилия крови, выявления возбудителя.
- Токсические поражения печени — связь с употреблением токсинов, отсутствие синдрома общей инфекционной интоксикации.
- Опухоли гепатобилиарной области — длительное постепенное начало, отсутствие яркой выраженной симптоматики, умеренное повышение АЛТ или АСТ, резкое повышение СОЭ, характерные изменения на УЗИ, КТ или МРТ. — типичные болевые приступы, умеренное повышение АЛТ или АСТ, данные инструментальных исследований [1][2][6][8][10] .
Лечение гепатита Е
При лёгкой степени гепатита Е лечение проводится в амбулаторных условиях (на дому). Во всех остальных случаях показано стационарное лечение в инфекционном отделении больницы. Режим постельный или полупостельный.
Чтобы снизить нагрузку на поражённую печень, необходимо придерживаться механически и химически щадящей диеты № 5 по Певзнеру. Она подразумевает употребление витаминов и повышенного количества воды (более 1,5 л в сутки), исключение алкогольных и газированных напитков, жаренной и острой пищи, грибов, сдобного теста и других продуктов.
Специфического лечения, которое бы устраняло причины гепатита Е, нет. В основном все методы направлены на устранение симптомов, интоксикации и восстановление нормальной функции печени.
Показан приём сорбентов и препаратов, которые повышают энергетические ресурсы. Иногда назначают гепатопротекторы. Если случай тяжёлый, то проводится терапия гормональными средствами и препаратами крови, а также гипербарическая оксигенация (использование кислорода под высоким давлением) и плазмаферез.
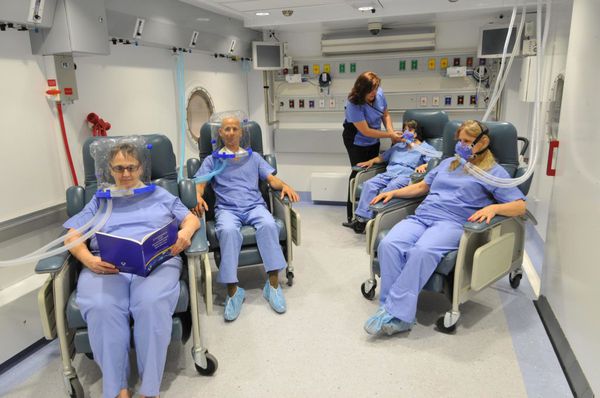
Назначение инфузионной терапии — внутривенного введения глюкозо-солевых растворов и витаминов — зависит от степени тяжести и определённых симптомов.
При тяжёлом течении и хронизации возможно применение препаратов общевирусного действия. Они позволяют снизить вирусную нагрузку.
Людям, получающим цитостатическую (противоопухолевую) терапию по возможности следует снизить дозу на 30 %. Это повышает вероятность спонтанной гибели вируса.
Беременные с гепатитом Е должны находиться в условиях реанимации инфекционного стационара. В острый период болезни лечение проводится по общим принципам, преждевременное родоразрешение противопоказано.
Выписывать больных можно в том случае, если в ходе лечения у них стойко улучшается клиническая картина и лабораторные показатели. После выписки пациенты, которые идут на поправку после неосложнённых форм болезни, находятся под наблюдением врача в течение шести месяцев. Осмотр и обследования проводятся минимум один раз в месяц [5] [6] [8] [9] .
Прогноз. Профилактика
Прогноз гепатита Е зачастую благоприятный, за исключением случаев заболевания при беременности. После выписки из больницы окончательное выздоровление наступает спустя 2-3 месяца. Крайне редко болезнь может стать хронической и затяжной.
Чтобы снизить количество случаев инфицирования, необходимо придерживаться следующих правил:
- создавать все условия для того, чтобы потребляемая питьевая вода была безопасной (касается водоснабжения);
- соблюдать правила утилизации сточных вод (канализационное хозяйство);
- соблюдать правила личной гигиены (всегда мыть руки);
- следить за качеством обследования работников, которые связаны с пищевой промышленностью;
- соблюдать технологию хранения, приготовления и транспортировки продуктов питания и воды;
- беременным на любом сроке стоит воздержаться от поездок в потенциально опасные в эпидемиологическим плане места (тёплые страны, особенно Азиатского региона).

Для предотвращения развития болезни разработана специфическая профилактика — вакцинация против гепатита Е. С этой целью применяется вакцина Hecolin (Китай). Она вырабатывает иммунитет к одному генотипу у 95 % трехкратно привитых людей [1] [2] [3] [5] [8] .
Изучена эффективность различных схем лечения больных вирусным гепатитом С (HCV-инфекция). Результаты позволяют признать приоритетное право использования противовирусной терапии у больных с сопутствующей соматической патологией и при тяжелых побочных эффек
По прогнозам ВОЗ, в ближайшие 10–20 лет ведущей проблемой в здравоохранении будет борьба с гепатитом С (HCV-инфекция), распространение которого приведет к тому, что на 60% увеличатся хронические гепатиты, на 70% увеличится заболеваемость раком печени, на 280% будет увеличиваться печеночная декомпенсация и в два раза возрастет смертность [1].
Правительство РФ предпринимает ряд мер, направленных на снижение угрозы заражения вирусными гепатитами и лечение больных вирусными гепатитами. Таким образом, проблема вирусных гепатитов заслуживает самого глубокого и комплексного изучения.
Современный подход к лечению вирусного гепатита С
Среди более чем 20 подтипов ИФН-α наиболее биологически значимы α2, рекомбинантными аналогами которого являются препараты Роферон-А (α2а), Интрон А (α2b), а также отечественный Реаферон-ЕС. Все вышеперечисленные препараты обладают высокой эффективностью. Однако препараты вводятся в организм больного парентеральным путем (внутривенно, внутримышечно, подкожно) и, как правило, в высоких дозах (3–10 млн ME в сутки). При этом наблюдаются побочные эффекты: гриппоподобный синдром, сильные головные боли, артралгия, депрессивное состояние, галлюцинации, выпадение волос, диарея [4, 5].
В результате фундаментальных исследований, проведенных в отделе интерферонов ФГБУ НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи МЗ РФ (Москва) под руководством проф. Малиновской В. В., была найдена реальная возможность обойти сложности, возникающие при парентеральном применении препаратов интерферонов. В процессе углубленных исследований функционирования системы интерферона в онтогенезе [6] был выявлен ряд закономерностей, позволивший решить стоявшие перед разработчиками задачи: снижение дозировки интерферона при однократном его введении; пролонгирование действия интерферона; устранение побочных эффектов, характерных для парентерального введения препаратов интерферона; обеспечение возможности применения препаратов интерферона не только для лечения взрослых, но и в педиатрической (неонатологической) и акушерской практике. Результатом проведенной работы стал препарат Виферон®, производимый в четырех различных дозировках в зависимости от содержания интерферона (150 тыс. МЕ, 500 тыс. МЕ, 1 млн МЕ, 3 млн МЕ) [7–9, 29].
Выбранная лекарственная форма — суппозитории обеспечивает простой, безопасный и безболезненный способ введения, что особенно актуально для педиатрии (неонатологии), а также при амбулаторном лечении и самостоятельном приеме препарата больными [9–11].
В качестве действующего начала был выбран человеческий рекомбинантный ИФН-α2b — один из наиболее распространенных в клинической практике. Кроме того, в состав препарата Виферон® помимо рекомбинантного ИФН-α2b вошли мембрано-стабилизирующие препараты — антиоксиданты α-токоферола ацетат (витамин Е) и аскорбиновая кислота (витамин С) в терапевтически эффективных дозах [7, 12, 13].
Комбинированная терапия (КТ) ИФН с рибавирином в настоящее время является мировым стандартом в лечении HCV-инфекции [14–17].
Важно отметить, что свой противовирусный эффект при хроническом вирусном гепатите С рибавирин оказывает только в присутствии ИФН (монотерапия рибавирином неэффективна) и препятствует формированию резистентности вируса гепатита C к терапии.
Рандомизированное контролируемое исследование КТ рибавирина и ИФН в качестве первичной терапии HCV-инфекции показало увеличение устойчивого ответа в 2 раза. Причем у пациентов с высокой репликативной активностью — более 3 млн gE/мл — выявлено 10-кратное возрастание частоты постоянного ответа по сравнению с монотерапией ИФН (41% и 4% соответственно). У пациентов с низкой концентрацией вирусной РНК — менее 3 млн gE/мл — не наблюдали преобладания эффективности КТ по сравнению с монотерапией ИФН. Частота постоянного ответа составляла 29% и 25% соответственно [3, 18–20].
У больных HCV-инфекцией с исходно высоким уровнем виремии удлинение сроков КТ с 24 до 48 нед на 10% увеличивает эффективность, тогда как у пациентов с низким уровнем виремии существенной разницы между эффективностью курсов выявлено не было [21].
Немаловажным звеном в лечении HCV-инфекции является применение озонотерапии (ОТ). При этом используется доказанный многими авторами выраженный антивирусный эффект [22], который проявляется как через непосредственное воздействие озона на вирус, так и опосредованно — через воздействие на вирус пероксидов, образующихся в результате взаимодействия озона с биологическими структурами организма, иммуномодулирующим действием озона [22]. Важным оказывается и то, что озон стимулирует фагоцитоз, оказывает защитный эффект на здоровые клетки, в то же время повышая элиминацию клеток, пораженных вирусом.
Основным методом применения ОТ при гепатитах является внутривенное капельное введение 400 мл озонированного физиологического раствора в дозировке 4–6 мг/л, несколькими процедурами в зависимости от формы ВГ. Различие в дозах при остром и хроническом гепатите связано с тем, что при этом используются различные эффекты ОТ. При остром гепатите необходимо антивирусное воздействие, а при хроническом важны иммуномодулирующий, протективный, стимуляция репарации [22–24, 26].
Целью данной работы было изучить эффективность различных схем лечения HCV-инфекции с последующим сравнительным анализом.
Материалы и методы исследования
Проведено лечение 96 больных хроническим вирусным гепатитом С с высоким уровнем репликации (РНК HСV более 2 млн копий в 1 мл). Из них 55 мужчин и 41 женщина, средний возраст больных составил 33 ± 6 лет. При генотипировании HCV генотип 1b был выявлен у 83 человек, 1а — у 5 больных, 2а — у 1 больного и 3а — у 7 больных. Все больные были разделены на 3 группы. Длительность заболевания составила 5 ± 2,5 года, из всех обследованных HCV впервые выявлен был у 29 человек, 28 обследованных получали ранее противовирусную терапию в виде монотерапии α-интерферонами, длительностью не более 6 месяцев, первичный ответ был у 12 из этих больных. Лица, получавшие лечение ранее, были равномерно распределены в 2-й и 3-й группах. В 1-ю группу вошли больные с сопутствующей соматической патологией, а также 8 человек, ранее получавшие лечение, у которых были отмечены выраженные побочные эффекты интерферонотерапии (в том числе у 5 больных наблюдалась лейко- и тромбопения, вследствие чего ранее полученное лечение было прервано). Больные с генотипами 1а, 2а и 3а HCV были равномерно распределены в группах больных.
Первая группа больных (26 человек) получала лечение препаратом Виферон®, суппозитории ректальные в суточной дозировке 6 млн МЕ на двукратный прием, в течение 3 месяцев, далее трехкратно в неделю, в течение 48 недель в комбинации с Рибаверином из расчета 15 мг/кг массы тела ежедневного приема на протяжении всего периода терапии.
Вторая группа больных (32 человека) получала стандартную базисную терапию: диету № 5, противовирусную терапию препаратами Реаферон-ЕС (интерферон α2b) или Роферон-А (интерферон α2a) по схеме: 6 млн МЕ внутримышечного или подкожного введения ежедневно в течение месяца, далее трехкратно в неделю в течение 48 недель в сочетании с постоянным приемом противовирусного препарата Рибаверин из расчета 15 мг/кг массы тела ежедневного приема на протяжении всего периода терапии.
Третья группа больных (38 человек), изъявивших добровольное согласие, получали комплексное лечение, включавшее диету № 5 с расширением рациона, содержащего пищевые волокна, витаминотерапию и ИФТ (Реаферон-ЕС или Роферон-А в дозе 6 млн МЕ внутримышечного или подкожного введения ежедневно в течение месяца, далее трехкратно в неделю в течение 48 недель) в сочетании с постоянным приемом противовирусного препарата Рибаверин из расчета 15 мг/кг массы тела ежедневного приема на протяжении всего периода терапии. В дополнение к комбинированной противовирусной терапии все больные получали ОТ, проводимую двумя курсами по 10 инфузий озонированного физиологического раствора с концентрацией озона 4–5 мг/л трижды в неделю на курс лечения в начале и спустя три месяца от начала интерферонотерапии.
Эффективность терапии оценивалась по степени выраженности побочных эффектов терапии, биохимическому ответу, вирусологическому (первичному и стойкому) ответу, а также по истечении трех месяцев от начала курса терапии была оценена внешнесекреторная функция печени путем проведения этапного хроматического дуоденального зондирования (ЭХДЗ) [27, 28].
Статистическая обработка полученных результатов проводилась с использованием программы Primer of Biostatistics (v 4.03). Для анализа качественных признаков таблиц сопряженности использовался критерий хи-квадрата (χ 2 ). Анализ эффективности лечения проводился с помощью критерия Стьюдента, используемого в непараметрической статистике при сравнении двух статистических выборок.
Результаты исследования и их обсуждение
В ходе проведенного исследования были получены следующие результаты. Все больные прошли полный курс терапии (48 недель), прерывания курса лечения в связи с выраженными побочными эффектами не было.
Оценка переносимости противовирусной терапии
Все больные HCV-инфекцией прошли полные курсы противовирусной терапии. В начале лечения были отмечены следующие побочные эффекты (рис. 1).
Как видно из данных, представленных на рис. 1, у всех больных HCV-инфекцией были отмечены побочные эффекты проводимой терапии, наиболее часто наблюдался астенический синдром, реже лихорадка и в отдельных случаях лейко- и тромбоцитопения. По частоте выявленных побочных эффектов — во 2-й группе наблюдались: астения — у 28 больных (87,5%), лихорадка — у 24 (75%) и лейко- и тромбоцитопения — у 5 (15,6%) больных HCV-инфекцией; в 3-й группе: астения — у 26 больных (68,4%), лихорадка — у 25 (65,8%) и лейко- и тромбоцитопения — у 4 (10,5%) больных; в 1-й группе, получавшей Виферон®, побочные эффекты выявлены: астения — у 11 больных (42,3%), лихорадка — у 5 (19,2%), лейко- и тромбоцитопении — не наблюдались. Полученные результаты, безусловно, положительно характеризуют препарат Виферон®, а использование озонотерапии снижает уровень возможных побочных явлений терапии, однако в группе, получавшей Виферон®, уровень побочных эффектов достоверно ниже.
Оценка биохимического ответа
У всех больных HCV-инфекцией проводилось изучение основных биохимических показателей. Результаты основных из них приведены в табице.
Из данных, приведенных в таблице, видно, что у всех групп больных HCV-инфекцией достоверно увеличены основные биохимические показатели печеночного метаболизма, после проведенного курса терапии у всех групп также достоверно улучшились все исследуемые критерии. В 1-й группе больных HCV-инфекцией результаты статистически сопоставимы с результатами во 2-й и 3-й группах, что положительно характеризует все использованные методы терапии.
Оценка вирусологического ответа при лечении вирусных гепатитов
Оценка вирусологических показателей проводилась с учетом первичного ответа (исчезновение РНК HCV и ДНК вируса гепатита В (HBV)), зафиксированные не менее 2 раз с интервалом не менее 2 недель) и стойкого ответа (исчезновение РНК HCV и ДНК HBV, зафиксированное через 6 месяцев после окончания курса лечения). Результаты представлены на рис. 2.
Как видно из результатов, представленных на рис. 2, у всех групп больных HCV-инфекцией получены достоверные результаты, так, в 1-й группе первичный ответ наблюдался у 14 (53,8%), стойкий — у 6 (23,1%) больных во 2-й группе; первичный ответ — у 18 (56,3%) больных, стойкий — у 9 (28,1%) больных, у больных в 3-й группе первичный ответ был — у 21 (55,3%) больного, стойкий — у 12 (31,6%) больных.
В 1-й группе, несмотря на более низкие показатели первичного и стойкого вирусологического ответа в лечении HCV-инфекции, нежели в группах больных, получавших парентеральные интерфероны, результаты сопоставимы с результатами во 2-й и 3-й группах, что заставляет признать приоритетное право использования препарата Виферон® у больных с сопутствующей соматической патологией и при тяжелых побочных эффектах лечения HCV-инфекции.
Оценка внешнесекреторной функции печени у больных HCV-инфекцией
При оценке внешнесекреторной функции печени путем проведения ЭХДЗ учитывалось наличие билиарной недостаточности (БН) (уменьшение количества желчи и желчных кислот, поступающих в кишечник за 1 час после введения раздражителя, меньше 1,2 ммоль/час [28]). Результаты представлены на рис. 3.
Из данных, представленных на рис. 3, видно, что у подавляющего большинства больных HCV-инфекцией присутствует синдром БН, при проведении противовирусной терапии отмечено достоверное купирование последнего, так, в 1-й группе до лечения БН присутствовала у 25 (96,2%), после — у 19 (73,1%) больных, во 2-й группе до лечения — 30 (93,8%), после — у 24 (75%) больных, в 3-й группе до лечения БН присутствовала — у 37 (97,4%) больных HCV-инфекцией, после — у 26 (68,4%).
Полученные результаты свидетельствуют о результативном использовании озонотерапии в комплексном лечении синдрома БН у больных HCV-инфекцией.
Выводы
- Введение больным озонированного физиологического раствора при лечении HCV-инфекции способствует уменьшению проявлений побочных эффектов интерферонотерапии (лихорадки, астении, лейко- и тромбоцитопении), однако уровень побочных проявлений лечения остается достоверно повышенным по сравнению с группой получавших ректальные интерфероны (Виферон®).
- Несмотря на более низкие показатели биохимического и вирусологического ответа, Виферон® является единственным альтернативным препаратом в лечении HCV-инфекции у лиц с сопутствующей соматической патологией и тяжелыми побочными проявлениями лечения парентеральными препаратами интерферонов.
Литература
В. А. Максимов* , 1 , доктор медицинских наук, профессор
А. Л. Чернышев*, доктор медицинских наук, профессор
В. А. Неронов*, доктор медицинских наук
Е. Е. Шелемов*, кандидат медицинских наук
Г. Г. Евстигнеева**
Abstract. Different schema of treatment patients with viral hepatitis type C (HCV) have been examined. Results prove priority right to use antiviral therapy for patients with attended somatic pathology and in case of severe side effects of HCV treatment.
Читайте также:

