Гепатита печени при малярии
Обновлено: 24.04.2024
На эритроцитарной стадии паразит поглощается ретикулоэндотелиальными клетками печени. Поражение печени развивается вследствие токсемии и гипертермии.
На преэритроцитарной стадии (экзоэритроцитарной) в печени обнаруживаются шизогонии, которые не оказывают заметного действия на её функции. Гепатоциты поражаются при инвазии спорозоитов. Ядро паразита многократно делится, и в конце концов (за 6-12 дней в зависимости от вида возбудителя) формируется сферическое или неправильной формы тело, содержащее тысячи зрелых мерозоитов. Такие преэритроцитарные шизонты лопаются, мерозоиты высвобождаются в синусоиды и проникают в эритроциты. При четырёхдневной или доброкачественной трёхдневной малярии лишь отдельные мерозоиты вновь проникают в клетки печени, запуская таким образом новый экзоэритроцитарный или рецидивный цикл. При злокачественной трёхдневной малярии этого не происходит, поэтому при ней не бывает истинных рецидивов. До сих пор в печени людей обнаруживали только Plasmodium falciparum и Р. vivax. У человека тканевая стадия малярии ограничивается только поражением печени.
Морфологические изменения
В печени наблюдается пролиферация клеток ретикулоэндотелиальной системы, как клеток Купффера, так и клеток зоны 3. В синусоидах выявляется очаговое накопление гистиоцитов с формированием специфического гранулематозного воспаления. В клетках Купффера обнаруживают коричневый малярийный пигмент (железо и гемофусцин). Малярийные паразиты не выявляются. Изменения гепатоцитов незначительны. Гепатоциты могут быть набухшими, с ядрами разного размера и формы, наблюдается увеличение количества митозов.
Описываемый при злокачественной малярии (P.falciparum) некроз зоны 3, вероятно, представляет собой посмертные изменения. В синусоидах могут выявляться скопления эритроцитов, содержащих паразитов.
Таким образом, в печени на возбудителя малярии реагируют преимущественно клетки ретикулоэндотелиальной системы; при этом возбудитель оказывает минимальное воздействие на гепатоциты. Фиброз печени не развивается. Широкая распространённость цирроза печени в эндемичных регионах может быть связана с другими действующими в них факторами.
Клиническая картина
Как правило, при малярии не наблюдается специфических проявлений поражения печени. В отдельных случаях при остром злокачественном течении малярии могут развиться слабовыраженная желтуха, гепатомегалия и болезненность в области печени.
Нарушение функций печени
Повышение уровня билирубина в сыворотке крови больных малярией в редких случаях превышает 51 мкмоль/л (3 мг%). Наблюдается небольшое повышение активности сывороточных трансаминаз.
Пролиферация ретикулоэндотелиальной ткани сопровождается повышением концентрации глобулинов в сыворотке.
Кала-азар (лейшманиоз)
Лейшманиоз представляет собой поражение ретикулоэндотелиальной ткани. В печени наблюдаются перипортальная клеточная инфильтрация и скопления макрофагов, в которых можно обнаружить тельца Лейшмана-Донована, а также фиброз портальной зоны. Клиническая картина сходна при американском, средиземноморском и азиатском типах заболевания.
При лейшманиозе наблюдаются лихорадка, спленомегалия, плотная болезненная печень, панцитопения, анемия и высокий уровень глобулинов в сыворотке. Результаты, полученные при исследовании аспирата костного мозга, обычно положительны.
Эхинококкоз
Возбудителем эхинококкоза является цепень Echinococcus granulosus на стадии личинки или кисты, который паразитирует у собак. Промежуточные хозяева паразита - человек, овца и крупный рогатый скот.
Биологические особенности
Инфицирование людей происходит при контакте с фекалиями собак, чаще в детском возрасте. Собаки заражаются, поедая внутренности овец с эхинококковыми кистами. Содержащиеся в кисте сколексы прикрепляются к стенке тонкой кишки собаки и вырастают во взрослые гении. Каждый червь откладывает в кишке 500 яиц. Инфицированные фекалии собак загрязняют траву, землю; яйца попадают в кишечник овец, свиней, верблюдов или человека, на шерсть собак. Человек может заразиться, гладя собаку, употребляя в пищу загрязнённые овощи.
Яйца имеют хитиновую оболочку, которая растворяется желудочным соком. Высвободившиеся яйца пробуравливают слизистую оболочку кишечника и через воротную вену попадают в печень, где развиваются в зрелую кисту. Большинство кист задерживается в печёночных синусоидах, поэтому 70% эхинококковых кист формируется в печени. Отдельные яйца проходят через печень и сердце и задерживаются в лёгочном капиллярном русле, что приводит к образованию лёгочных кист. При попадании яиц в большой круг кровообращения образуются кисты в селезёнке, головном и костном мозге.
Развитие эхинококковой кисты в печени
Из яйца медленно развивается зрелая киста, вызывающая в тканях хозяина клеточную реакцию, в которой можно выделить три зоны: периферический слой фибробластов, средний слой эндотелиальных клеток и внутреннюю зону круглых клеток и эозинофилов. Периферическая зона развивается из тканей хозяина, превращаясь в адвентицию, или эктоцисту (фиброзную оболочку), которая может кальцифицироваться. Средняя и внутренняя зоны гиалинизируются (слоистая оболочка, хитиновый слой). Изнутри кисту выстилает герминативный слой, дающий начало узлам на ножке, которые состоят из размножающихся клеток и выступают в просвет кисты как выводковые капсулы. Сколексы развиваются из выводковых капсул и в конце концов разрывают их. Ножка, прикрепляющая выводковую капсулу к герминативному слою, постепенно становится всё тоньше до тех пор, пока капсула не разрывается, высвобождая сколексы в наполняющую кисту жидкость. Под действием гравитации они оседают на дно кисты и образуют так называемый эхинококковый песок. После того как киста поедается собакой, цикл начинается снова.
Эхинококковая жидкость представляет собой транссудат сыворотки крови. Она содержит белки и обладает антигенными свойствами. При попадании её в кровеносную систему у больного могут развиться эозинофилия или анафилактический шок.
Дочерние или даже внучатые кисты образуются при фрагментировании герминативного слоя. В связи с этим у взрослых больных большая часть кист состоит из нескольких пузырей.
Эндемичные регионы
Эхинококкоз широко распространён в странах, где разводят овец и собаки могут поедать их заражённые внутренности. К эндемичным регионам относятся Южная Австралия, Новая Зеландия, Африка, Южная Америка, Южная Европа, особенно Кипр, Греция и Испания, а также районы Среднего и Дальнего Востока. В Великобритании это заболевание встречается редко, за исключением некоторых районов Уэльса.
Расположение кист в печени
Обычно эхинококковые кисты располагаются в правой доле печени на её передненижней или задненижней поверхности. Если киста располагается на передней поверхности правой доли, рёберный край выступает вперёд, если на задней - диафрагма поднимается вверх. Если заболевание поражает левую долю печени, наблюдается выбухание в эпигастральной области.
Клиническая картина
Клиническая картина зависит от расположения кисты, стадии её развития, наличия живого или мертвого паразита.
Непоражённая часть печени гипертрофируется, в результате развивается гепатомегалия.
Неосложнённая эхинококковая киста может быть бессимптомной и обнаруживаться случайно при аутопсии. Её наличие можно предположить, если у пациента без явных признаков заболевания печени обнаруживается округлое гладкое опухолевидное образование в печёночной ткани. Единственной жалобой при этом могут быть тупая боль в правом верхнем квадранте живота и иногда чувство распирания в животе. В кисте создается большое давление, поэтому никогда не наблюдается симптом флюктуации.
Осложнения
Разрыв кисты. При эхинококкозе часто происходит перфорация кисты в брюшную полость с образованием множественных кист брюшной полости, нарушением проходимости кишечника и значительным увеличением живота.
Давление в кисте во много раз превышает давление жёлчи в жёлчных путях, поэтому часто наблюдается прорыв кисты в жёлчные пути. Это может привести к спонтанному излечению или развитию холестатической желтухи, сопровождающейся рецидивирующим холангитом.
Прорыв кисты в просвет толстой кишки ведёт к элиминации возбудителя через прямую кишку и вторичной инфекции.
Кисты могут прикрепляться к диафрагме и прорываться в лёгкое, что приводит к появлению в мокроте дочерних кист. Сдавление печёночных вен и прорыв кисты в их просвет приводят к развитию синдрома Бадда-Киари. За ним может последовать вторичное поражение лёгких.
Инфекция. Прорыв кисты в жёлчные протоки может сопровождаться вторичной инфекцией пиогенными микроорганизмами с развитием гнойного абсцесса; при этом паразит погибает. В отдельных случаях содержимое целой кисты подвергается асептическому некрозу и паразит также погибает. Образующиеся при этом аморфные жёлтые остатки необходимо отличать от гноя, возникающего при вторичной инфекции.
Другие органы. Кисты могут выявляться в лёгких, почках, селезёнке, головном или костном мозге, однако у человека такая обширная инвазия наблюдается редко; как правило, печень представляет собой единственный поражённый орган. В тех случаях, когда эхинококковые кисты обнаруживаются в других органах, имеется сопутствующее поражение печени.
Аллергия к эхинококку. В жидкости, содержащейся в эхинококковой кисте, находятся чужеродные белки, которые сенсибилизируют организм хозяина. Это может привести к развитию тяжёлого анафилактического шока, однако чаще наблюдается рецидивирующая уртикарная сыпь (крапивница).
Мембранозный гломерулит может быть связан с отложением эхинококковых антигенов в клубочках почек.
Диагноз
Серологические исследования
Эхинококковая жидкость содержит специфические антигены, попадание которых в организм сенсибилизирует больного; при этом образуются антитела.
Положительные результаты ИФА эхинококковой жидкости наблюдаются приблизительно в 85% случаев.
Все серологические реакции могут давать ложноположительные и ложноотрицательные результаты.
Результаты серологических реакций могут быть отрицательными, если эхинококковая жидкость не попадает в организм хозяина и отсутствуют сколексы, а также в случае гибели паразита.
Приблизительно у 30% больных в крови обнаруживается эозинофилия более 7%.
Рентгенологические изменения
Рентгенологические изменения включают высокое стояние и ограничение подвижности правого купола диафрагмы, гепатомегалию, кальцификацию. Кальций откладывается в эктоцисте, что на рентгенограмме проявляется как отчётливое круглое или овальное затемнение или просто как отдельные затемнённые участки. При этом необходимо исключить кальцификацию в соседних тканях и органах, таких как надпочечники, почки, жёлчный пузырь, брюшина, диафрагма, рёберные хрящи и старые поддиафрагмальные абсцессы. Обнаруживаемые в эхинококковой кисте подвижные тела свидетельствуют о наличии дочерних кист. В инфицированных кистах, содержащих газ, может определяться уровень жидкости.
Эхинококковые кисты печени могут вызвать смещение желудка или печёночного изгиба ободочной кишки.
Характерные рентгенологические изменения могут обнаруживаться в лёгких, селезёнке, почках или костном мозге.
При помощи селективной целиакографии обнаруживают выпрямление и удлинение печёночных артерий с наличием аваскулярного участка.
При УЗИ или КТ обнаруживаются одиночные или множественные кисты, которые могут быть одно-или многокамерными, тонко- и толстостенными. Инфицированные кисты плохо различимы.
При МРТ можно обнаружить характерный интенсивный контур, дочерние кисты и расслоение оболочек кисты. При помощи этого метода можно определить внутри- и внепеченочные разрывы кист.
Прогноз
Неосложнённый эхинококкоз печени имеет довольно благоприятный прогноз. Однако всегда имеется риск развития осложнений. Тяжёлым осложнением являются разрывы кист в брюшную и плевральную полости. Прорыв кисты в жёлчные протоки не столь опасен, поскольку за жёлчными коликами может последовать спонтанное излечение. Это заболевание может привести к летальному исходу, однако в результате применения антибиотиков прогноз стал более благоприятным. Если предполагается хирургическое лечение, кальцификация кисты играет неблагоприятную роль, так как возникают трудности при ликвидации полости кисты.
Лечение
Необходимо предотвращать доступ собак к заражённым внутренностям животных, мыть руки после контакта с собаками, регулярно проводить дегельминтизацию собак в эндемичных районах.
Хирургическое лечение
Угроза разрыва и вторичного инфицирования кист столь велика, что, если их немного, они имеют крупные размеры и позволяет состояние пациента, необходимо хирургическое лечение.
Полностью удовлетворяющего всех оперативного доступа не существует, и такую операцию лучше выполнять квалифицированному специалисту. Цель операции заключается в полном удалении кисты и полной облитерации остаточной полости; при этом нельзя допустить загрязнения и инфицирования брюшной полости. Для того чтобы не разлить содержимое кисты, её удаляют полностью, вместе с эктоцистой.
Вначале производят аспирацию содержимого кисты через её наиболее поверхностный участок (определяется при помощи сканирования), для уничтожения сколексов в кисту вводят 90% этиловый спирт, 20% гипертонический раствор натрия хлорида или нитрата серебра, формалина. Введение этих растворов может осложниться развитием склерозирующего холангита, особенно в тех случаях, когда используется формалин.
Обычно производят цистэктомию с удалением герминативного и хитинового слоев с сохранением эктоцисты, развившейся из организма хозяина. Оставшуюся после удаления эндоцисты паразита полость трудно облитерировать. Такую полость можно оставить открытой, с дренированием или без него, плотно закрыть её, предварительно наполнив гипертоническим раствором, или выполнить оментопластику.
Радикальная перицистэктомия включает удаление перицисты и характеризуется высокой летальностью.
Летальность при этих операциях составляет 2,2%, частота развития осложнений - 23,7%.
В отдельных случаях для удаления кисты производят гемигепатэктомию или сегментэктомию.
Медикаментозное лечение
Мебендазол проникает через оболочку кисты и влияет на метаболизм глюкозы и функции микротрубочек паразита. Однако даже через 12 мес после лечения могут оставаться жизнеспособные кисты. Нередко наблюдаются рецидивы, и неизвестно, достигается ли нужная концентрация препарата в больших кистах.
Албендазол легко диффундирует через оболочку паразита и более эффективен, чем мебендазол. При применении его в дозе 10 мг/кг в сутки в течение 3 мес кисты становятся нежизнеспособными. Албендазол можно применять в качестве начальной терапии неосложнённого эхинококкоза. При бессимптомных мелких кистах терапия может быть эффективной, однако большие кисты требуют хирургического лечения.
Аспирация
Формально аспирация противопоказана в связи с риском диссеминации и развития анафилактического шока. Однако производимая под контролем ультразвука аспирация иглой №22 диаметром 0,7 мм признана в настоящее время безопасной и используется как с диагностическими, так и с терапевтическими целями. Аспирированную жидкость можно окрасить для выявления фрагментов хитиновой оболочки, крючьев и сколексов. Достаточно безопасна и эффективна транспечёночная аспирация с введением в полость кисты 95% этилового спирта или гипертонического раствора натрия хлорида под прикрытием албендазола.
При этом киста должна быть однокамерной (тип I или II Гарби). Жидкость не должна быть окрашена жёлчью, так как снижение давления в кисте может препятствовать закрытию жёлчной фистулы. Такую процедуру в основном назначают больным, которые отказываются от операции или которым она противопоказана.
Чрескожное дренирование с албендазолом в большей степени приводит к уменьшению размеров кисты, чем изолированное применение албендазола или выполнение аспирации.
(495) 50-253-50 - информация по заболеваниям печени и жёлчных путей

Лечение печени в Германии
Германская медицина по праву может считаться одной из лучших во всем мире, благодаря высококвалифицированным специалистам, ультрасовременному диагностическому и лечебному оборудованию, а также постоянному участию в процессе разработки новых методов диагностики и лечения.

Лечение печени в Израиле
В клиниках Израиля проводится лечение всех видов патологии печени, в том числе, вирусных гепатитов, цирроза печени, фиброза печени, гепатитов невирусного происхождения, в том числе вызванных медикаментозной терапией и аутоиммунных гепатитов, а также холециститов, печеночной недостаточности, желчекаменной болезни и других заболеваний желчевыводящих путей.
Паразитарные поражения печени. Механизмы
Паразитарные болезни с поражением печени нередко вызывают трудности диагностики, в основном связанные с недостаточной информацией клиницистов. Представления об ареалах распространения заболеваний не учитывают миграционных процессов населения и риска завоза возбудителей в среднюю климатическую полосу. Примерами служат случаи малярии, амебиаза, стронгилоидоза, гименолипедоза.
Паразитарные болезни включают в себя заболевания, вызванные протозойной инфекцией и глистной инвазией. При большинстве таких заболеваний в патологигеский процесс вовлекается печень.
К протозойным инфекциям с поражением печени относятся прежде всего амебиаз, малярия, лейшманиоз, токсоплазмоз.
К гельминтозам относят нематодозы, трематодозы и цестодозы.
Нематодозы (паразиты — круглые черви): аскаридоз, токсокароз, стронгилоидоз, трихинеллез.
Трематодозы (сосальщики): описторхоз, клонорхоз и фасциолез. Цестодозы (ленточные черви): эхинококкоз и альвеококк.
Вариантность и динамика клинических проявлений болезней, вызванных гельминтами и простейшими, обусловлены многообразием стационарной локализации, циклами развития паразитов, стадиеспецифической локализацией мигрирующих личинок, а также иммунным ответом организма хозяина. Гельминтозы, поражающие печень, как правило, приводят к развитию механической желтухи. Синдромы поражения желгных протоков характерны для описторхоза, клонорхоза, фасциолеза. Сосальщики паразитируют в желчных протоках, желчном пузыре, протоках поджелудочной железы.
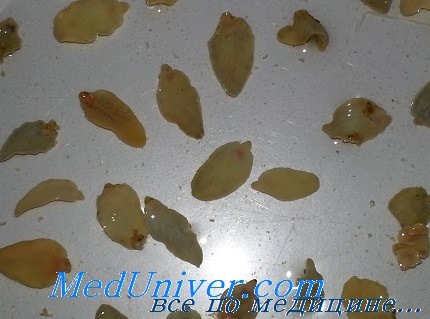
Вследствие механического повреждения стенок присосками образуются эрозии, железистая гиперплазия и кистозные изменения желчных протоков, холестаз, вторичное инфицирование с исходом в ангиохолит. Личинки фасциол прежде, чем проникнуть в гепатобилиарную систему, мигрируют двумя путями: по сосудам системы воротной вены и через брюшную полость в ткань печени, затем в желчные протоки, где превращаются во взрослых особей. В процессе дальнейшей миграции паразиты травмируют ткань печени и желчные протоки, вызывая микроабсцессы, микронекрозы, холестаз.
Поражением желчных путей может сопровождаться аскаридоз.
Объемные поражения печени образуют личиночная стадия эхинококков (киста печени), трофозоиты кишечной амебы.
Фиброз печени формируется при кишечных шистосомозах.
При малярии, висцеральном лейшманиозе, трипаносомозе наряду с гепатомегалией (гепатоспленомегалией), нарушением портального кровообращения, в тяжелых случаях манифестируют признаки поражения паренхимы печени, печеногной недостатогности.
Своеобразие поражений печени при паразитарных и протозойных болезнях определяется в первую очередь жизненным циклом паразита.
В целом поражения печени при большинстве гельминтозов и протозоозов имеют иммунную природу и свидетельствуют о неспецифигеской природе развивающегося процесса в виде лимфоидно-плазматигеской пролиферации, грануломатоза и своеобразных сосудистых поражений. Иммунологические реакции, переходя границы адекватного физиологического ответа, принимают характер иммунопатологических, приводящих к тяжелым органным поражениям. Ведущая роль в развитии иммунопатологических реакций принадлежит сенсибилизации организма ребенка соматическими, экскреторными и секреторными антигенами гельминтов.
В острой фазе гельминтозов происходит фиксация иммунных комплексов антиген — антитело на тучных клетках, что приводит к выделению биологически активных веществ: гистамина, гепарина, серотонинов и других. В результате наступают микроциркуляторные расстройства, нарушения проницаемости гистогематологических барьеров и клеточных мембран, что определяет развитие органной патологии.
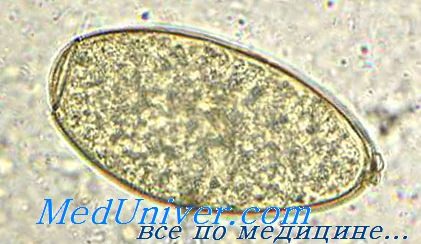
Иммунные комплексы фиксируются на мембранах тромбоцитов, вызывают лизис нейтрофилов, происходит освобождение лизосомальных ферментов, вазоактивных аминов, отложение фибрина и другие нарушения коагуляции, которые приводят к тяжелым сосудистым поражениям, нарушениям микроциркуляции, тромбозам, геморрагиям, отложению фибрина на базальной мембране сосудистых стенок с исходом в геалиноз или фибриноидный некроз. Повышенная проницаемость сосудистых стенок под действием вазоактивных аминов способствует проникновению иммунных комплексов в ткани и развитию органных поражений.
Личинки гельминтов оказывают также воздействие выделяемыми ими ферментами: гиалуронидазой, протеолитическими ферментами, способствующими активации системы комплемента, выделению простогландинов клетками окружающих гельминта тканей хозяина. Эти процессы провоцируют развитие воспалительных реакций. Таким образом, запускается каскадный механизм развития фиброза печени, начинающийся с регулярно повторяющегося повреждения ткани печени, следствием чего является преобладание процессов чрезмерного синтеза и накопления экстрацеллюлярного матрикса. В острой фазе фибриногенез контролируется и уравновешивается фибринолизом. В хронической фазе процессы фиброгенеза начинают превалировать.
Образование гранулем при гельминтозах обусловлено аллергической реакцией замедленного типа. Гранулемы появляются вокруг личиночных форм, а также вокруг взрослых паразитов, внедрившихся в ткани.
Кроме того, в патогенезе ряда инфекционных и паразитарных болезней существенная роль отводится системе цитокинов геловека. Цитокины — эндогенные биологически активные медиаторы, продуцируемые и секретируемые активированными клетками иммунной системы, в синтезе которых принимают участие фибробласты, эндотелиальные, эпителиальные и другие клетки. Клинически значимы интерлейкины (ИЛ 1-25), интерфероны (ИФН альфа, бета, гамма); факторы некроза опухоли (ФНО альфа, бета); колониостимулирующие факторы; факторы роста; хемокины.
В развитии и течении паразитарных болезней с поражением печени принимают активное участие следующие цитокины.
Интерлейкин 1 бета (ИЛ 1 бета) продуцируется макрофагами, моноцитами, лимфоцитами, фибробластами, эпителиоцитами.
ИЛ-1-бета регулирует синтез фактора роста гепатоцитов (ФРГ —HGF). Продуцируют HGF фибробласты, сосудистый эндотелий, активированный в результате повреждения печени, макрофагами и активированные Т-лимфоциты. Фактор является сильным митогеном для гепатоцитов и участвует в регенерации ткани печени. HGF супрессирует ген экспрессии тромбоцитарного фактора роста, повышает коллагеназную активность и угнетает апоптоз гепатоцитов, стимулирует их пролиферацию.
В повседневной клинической практике педиатра диагностика поражений печени при гельминтозах и протозоозах сопряжена с определенными трудностями. Задача усложнилась в последие годы в связи с миграцией детей из других регионов, эндемичных по различным контагиозным болезням, отсутствием информации об эпидемиологической ситуации в местах прежнего пребывания и посещаемых ребенком, отсутствием медицинской документации и достоверных анамнестических данных.
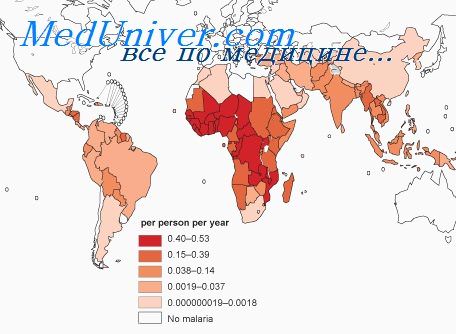
Стадии малярийного приступа. Печень при малярии
Малярии свойственна смена периодов лихорадочных приступов и межприступного латента, когда исчезает лихорадка и смягчаются другие признаки болезни. При тропической малярии в межприступ-ном периоде ряд клинических проявлений может быть более выражен, чем при других формах малярии.
Наиболее характерным клиническим признаком малярии является лихорадка. Иногда периоду высокой лихорадки предшествуют недомогание, чувство слабости, разбитости, головные боли, нарушение аппетита и др. Лихорадочные приступы возникают после инкубационного периода в 8—10 дней при тропической, 10—14 дней при трехдневной (с короткой инкубацией) и 20—25 дней при четырехдневной малярии. В первые дни лихорадка может носить неправильный, ремиттирующий, иногда даже (при тропической малярии) постоянный характер. Эта так называемая начальная (инициальная) лихорадка наблюдается только при свежем первожизненном заболевании малярией. Через несколько дней устанавливается правильное чередование лихорадочных приступов и периодов нормальной температуры.
В малярийном приступе различают три стадии: периоды озноба, жара к пота. Выраженность озноба и пота у больного связана с быстротой подъема и снижения температуры. При мягком течении болезни, а также при тяжелой малярии с лихорадкой неправильного, постоянного или послабляющего типа озноби пот могут быть мало выражены, а иногда и совсем отсутствовать.
Малярийные приступы, как правило, возникают в первой половине суток, максимум температуры обычно приходится на утренние часы. Эта особенность служит дифференциально-диагностическим признаком малярийной лихорадки. Однако нужно помнить, что для трехдневной малярии, вызываемой P. ovale, характерны вечерние н ночные приступы, С началом снижения температуры и появлением сильного пота состояние больного постепенно улучшается, больной успокаивается и засыпает. Продолжительность приступа обычно не превышает 8— 12 часов. Иногда, особенно при переводе правильного типа лихорадки в ежедневный, приступы могут длиться больше суток.
При правильном чередовании малярийных приступов (при трехдневной малярии через день и четырехдневной через 2 дня) в дни, свободные от приступов, состояние больного может быть удовлетворительным, возвращается аппетит, работоспособность. Однако по мере нарастания количества приступов и в дни апирексии состояние больного может оставаться тяжелым. Более тяжелое течение наблюдается при ежедневных лихорадочных приступах, что часто имеет место при тропической малярии.
Вторым характерным признаком малярии является увеличение к болезненность печени и селезенки. Увеличение печени обычно определяется раньше; селезенка в свежих случаях малярии отчетливо увеличивается только после перенесения нескольких приступов малярии. Вместе с тем увеличение селезенки остается более длительно, чем увеличение печени. Последнее связано с тем, что печень увеличивается главным образом за счет повышенного кровенаполнения и в меньшей степени за счет прироста ретикуло-эндотелиальной ткани. Увеличение селезенки обусловлено не только гиперемией, но и гиперплазией.
Во время малярийного приступа печень и селезенка становятся особенно болезненными. Это связано с повышенным кровенаподнением и растяжением капсулы органов. Размеры печени й селезенки с каждым приступом увеличиваются. При затянувшемся лихорадочном периоде переполнение селезенки кровью и растяжение ее капсулы могут привести к разрыву селезенки. При правильном лечении размеры обоих органов быстро уменьшаются, причем печень сокращается быстрее селезенки.
Диффузное поражение печени при малярии встречается редко; исключительно редко возникает острая или подострая атрофия печени. Частота хронических поражении печени у населения эндемичных по малярии колониальных или развивающихся стран связана прежде всего с постоянным белковым голоданием, гельминтозами, гепатотропными вирусными инфекциями и др.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
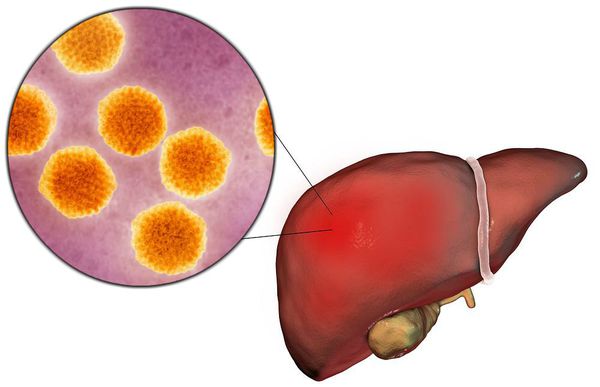
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
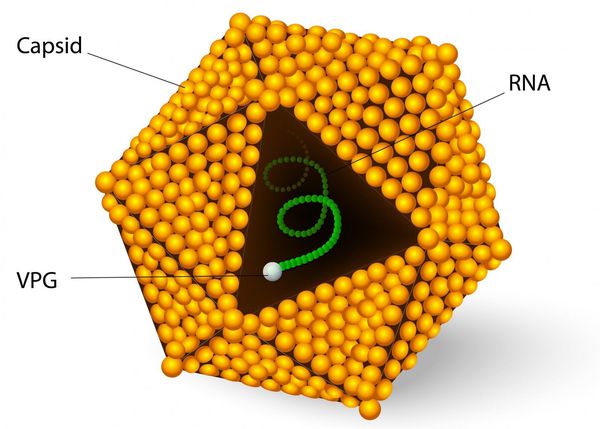
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
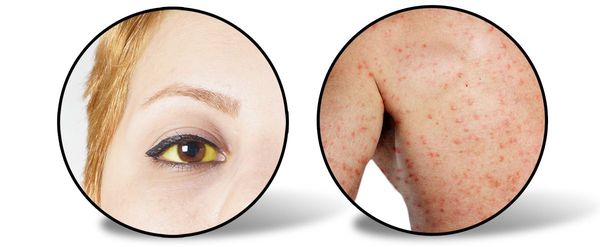
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
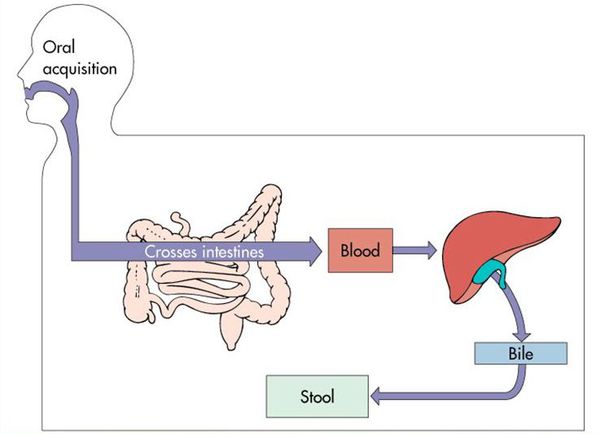
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
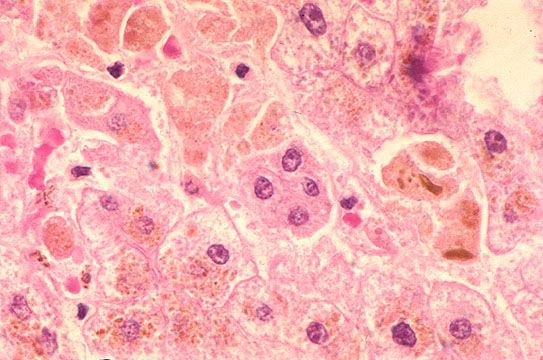
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
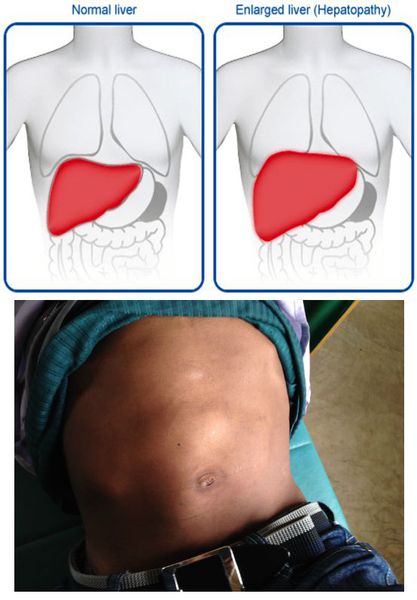
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
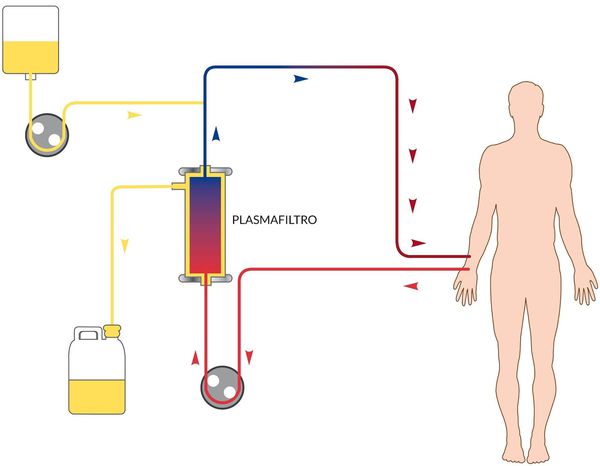
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
Что такое гепатит Е? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит Е — это острое (и редко хроническое) инфекционное заболевание, которое вызывает вирус гепатита Е. Клинически проявляется синдромом общей инфекционной интоксикации, энтерита (воспаления тонкой кишки) и холестаза (застоя желчи), желтухой, увеличением и нарушением работы печени. Болезнь протекает доброкачественно, за исключением беременных, у которых заболевание имеет катастрофические последствия в любом триместре беременности.
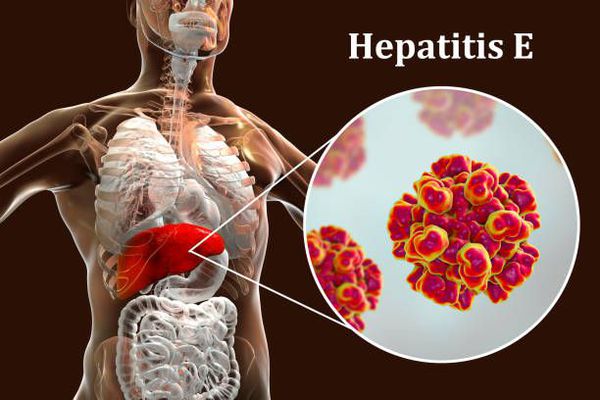
Этиология
Вид — вирус гепатита Е (HЕV)
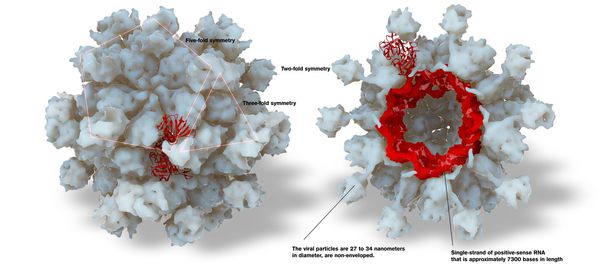
Данный вирус представляет собой одноцепочечный РНК-вирус округлой формы диаметром 30-35 нм. Он лишён наружной оболочки. На поверхности вириона есть вдавления, напоминающие чаши.
Чтобы вирус внедрился в клетку, в процессе жизни он кодирует трансмембранный белок и такие ферменты, как РНК-зависимую РНК-полимеразу, РНК-хеликазу, метилтрансферазу и папаин-подобную протеазу.
Существует пять генотипов вируса:
- I и II — только человеческие;
- III и IV — есть также у животных, т. е. может передаваться от них людям; вызывает хронические формы, если есть предрасположенность;
- V — птичий.
При температуре от 0°C быстро инактивируется. Длительно сохраняется в воде и при отрицательных температурах. Неплохо себя чувствует в ЖКТ человека. Хорошо сохраняется в плохо прожаренном мясе. При нагревании воды до 71°C погибает в течение 20 минут, при кипячении — практически мгновенно [1] [2] [3] [8] [10] .
Эпидемиология
Источник инфекции — вирусоноситель или человек, который уже болен какой-либо формой гепатита Е, в особенности острой. Вирус распространяется с последней недели инкубационного периода и до 30 дней от начала заболевания.
Каждый год повсеместно регистрируется около 3,3 млн случаев заболевания. При этом количество людей с гепатитом Е, который протекает пока без симптомов или совсем себя не проявляет, по предварительным оценкам может достигать 20 млн. Смертность — около 4 %, преимущественно умирают беременные.
В окружающую среду вирус выделяется с экскрементами инфицированных людей. Иногда человек заражается при употреблении недостаточно приготовленного мяса свиней, оленей и моллюсков.
- фекально-оральный — через заражённые вирусом руки (контактно-бытовой путь), воду или пищу;
- парентеральный — при переливании крови (встречается редко);
- половой путь — при орально-анальном контакте;
- вертикальный — от матери к плоду.

Наибольшее значение имеет водный путь передачи. Часто он связан с сезоном дождей и наводнениями, когда вода загрязняется фекалиями.
Восприимчивость к гепатиту Е высокая. Преимущественно болеют люди 15-44 лет. К группе повышенного риска относятся работники животноводческих ферм и боен.
Факторы риска заражения:
- высокая плотность населения, особенно в бедных странах;
- антисанитария, несоблюдение правил личной гигиены, неправильное хранение, обработка и приготовление пищи;
- нарушения санитарно-технических требований на объектах водоснабжения — заражение воды;
- бытовой очаг заболевания.
Заболевание обычно возникает в осенне-весенний период. В основном распространено в странах Восточной и Южной Азии.
После перенесённой болезни формируется стойкий иммунитет, чаще пожизненный [1] [3] [7] [9] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Е
Болезнь начинается постепенно. Инкубационный период длится от 2 до 10 недель.
Как и в случае гепатита А, заболевание обычно протекает в бессимптомной и субклинической (предсимптомной) форме.
При возникновении явных клинических признаков (т. е. при манифестации), преобладают случаи лёгкого и среднетяжёлого течения. Симптоматика медленно нарастает. Появляется немотивированная слабость, подташнивание, снижение аппетита, повышение температуры до 37,1-38,0°С (субфебрилитет), дискомфорт и тяжесть в правом подреберье, дискомфорт в суставах, возможна рвота.
Вслед за этими симптомами через 3-7 дней наступает желтушный период, который длится максимум один месяц. Он сопровождается пожелтением кожи и слизистых оболочек, потемнением мочи и обесцвечиванием кала. Общее состояние больных не улучшается, сохраняется плохое самочувствие, выраженный дискомфорт в правом подреберье, увеличение размеров печени и селезёнки, желтушность кожных покровов, нарастает зуд кожи.
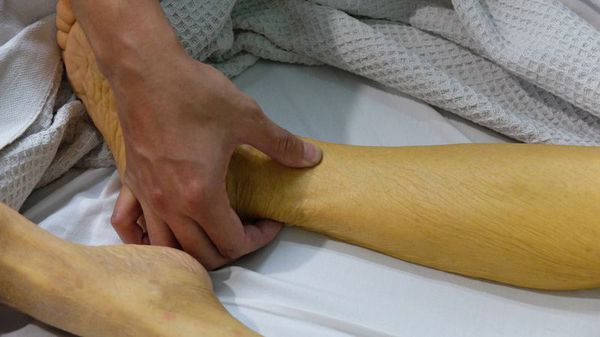
При неосложнённом и нетяжёлом течении начинает медленно регрессировать в течение нескольких недель. Как правило, после этого человек полностью выздоровливает, иногда развиваются непродолжительные остаточные явления в виде астении (бессилия) и дискомфорта в правом подреберье.
Раньше считалось, что гепатит Е — лишь острое заболевание. Однако в последнее время накоплен ряд данных, позволяющих выделить небольшую группу больных, переносящих хронический вариант болезни. Он встречается у ВИЧ-инфицированных людей в стадии СПИДа, после пересадки органов, а также у тех, кто получает мощную иммуносупрессивную терапию.
Специфичной симптоматики у хронического гепатита А нет. Больные жалуются на повышенную утомляемость, артралгии, неустойчивый стул, тяжесть в правом подреберье, субфебрилитет, иногда устойчивый лёгкий зуд кожи. Если не лечить это состояние, может развиться цирроз печени.
Гепатит Е у беременных
При заражении беременной в I и II триместрах происходит 100 % гибель плода. Летальность самих беременных невелика.
При заражении беременной в III триместре ребёнок может родиться живым, но 50 % из них умирают в первые месяцы жизни. Смертность самих женщин достигает 25-30 %. А если беременные живут в районах, которым не свойственно данное заболевание, то летальность может достигать 80 %.
Тяжесть течения Гепатита А при беременности связана со специфической аутоиммунной перестройкой организма женщины. В этом случае заболевание часто протекает по фульминантному типу (острой печеночной недостаточности) — на фоне начальных симптомов болезни резко нарастает желтуха, развивается тяжёлая интоксикация, некупируемая рвота, кровотечения (ДВС-синдром), нарушается сознание. Роды (преждевременные или выкидыш) стремительно ухудшают состояние больной: развиваются массивные послеродовые кровотечения, острая почечная недостаточность, печеночная энцефалопатия. Из-за такого состояния в острый период искусственно прерывать беременность нельзя [1] [5] [6] [8] [9] .
Патогенез гепатита Е
В цитоплазме гепатоцитов внешняя оболочка вируса вируса раскрывается, и запускается выработка вирусных белков. Одновременно с этим происходит подготовка клетки-хозяина к этому процессу.
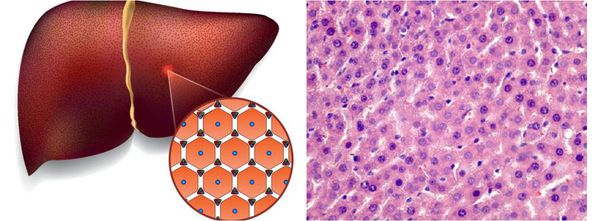
Во время своей жизни вирус напрямую провоцирует дегенеративные изменения в гепатоцитах, в т.ч. вызывая их гибель по типу баллонной дистрофии — переполнение клетки жидкостью. После этого готовые вирусные частицы распространяются и заражают новые здоровые клетки.
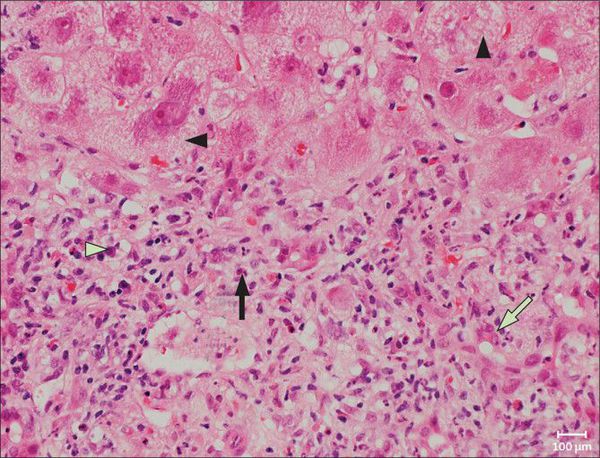
Со временем в организме формируются специфические антитела, которые позволяют полностью вывести вирус из организма человека (за исключением случаев выраженного угнетения иммунитета).
Тяжёлое течение гепатита Е у беременных не связано со свойствами вируса напрямую. Оно вызвано лишь иммунологической перестройкой иммунной защиты беременных. Из-за этого развивается каскад иммунопатологических и гормональных реакций, которые приводят к массированному некрозу гепатоцитов, дефициту плазменных факторов свёртывания и внутрисосудистому гемолизу — разрушению эритроцитов крови [1] [2] [3] [5] [10] .
Классификация и стадии развития гепатита Е
По клиническим признакам выделяют два варианта заболевания:
- безжелтушная форма — до появления симптомов или при освобождении организма от вируса и формировании стойкого иммунитета;
- желтушная форма — при нарастании симптомов.
По тяжести процесса гепатит Е делят на четыре степени:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная, гепатит у беременных).
Факторы риска развития тяжёлого течения болезни:
- беременность любого триместра (наиболее неблагоприятно заболевание протекает в III триместре);
- пожилой возраст:
- мужской пол;
- иммуносупрессивная терапия (на фоне трансплантации органов); ;
- комбинированная соматическая патология (сахарный диабет, ишемическая болезнь сердца, аутоиммунный гепатит, пациенты на гемодиализе);
- наличие хронической вирусной патологии печени (вирусные гепатиты В и С);
- алкоголизм.
По исходу заболевание бывает трёх типов:
- с выздоровлением (полным, с остаточными явлениями);
- с хронизацией;
- с неблагоприятным прогнозом (у беременных) [4][5][6] .
Осложнения гепатита Е
Осложнения при гепатите Е можно разделить на три группы:
- Истинные (печёночные) осложнения:
- острая печёночная недостаточность — осложнение с неблагоприятным исходом, при котором быстро развивается массивное повреждение ткани печени (до 90 %), резкое нарушаются её функции, возникает печёночная энцефалопатия (нарушение работы мозга), геморрагический синдром (повышенная кровоточивость) и коагулопатия (нарушение свёртывания крови);
- холестаз — нарушение синтеза и выведения желчи (желтуха), осветление кала и потемнение мочи, появление выраженного кожного зуда и чувства горечи во рту;
- тромбо-геморрагический синдром у беременных (ДВС-синдром) — кровотечения и кровоизлияния различной интенсивности и направленности;
- преждевременные роды или выкидыш у беременных.
- Внепечёночные осложнения: — острое неврологическое заболевание, которое сопровождается нарушением чувствительности в руках и ногах, мышечной слабостью и иногда параличом.
- острый поперечный миелит — нарушение всех функций спинного мозга;
- различные нейропатии и полирадикулопатии;
- панкреатит — тошнота, рвота, опоясывающие боли в животе; — боли в поясничной области, нарушение мочеобразования, повышенная потеря эритроцитов и белка с мочой;
- повышение вероятности развития рака кожи и заболеваний кровеносной системы.
- Резидуальные (постгепатитные) явления:
- дискинезия (нарушение моторики) желчевыводящих путей — застой желчи, чувство тошноты, отрыжка, горечь во рту;
- постгепатитная гепатомегалия — увеличение печени в связи с разрастанием соединительной ткани;
- постгепатитный синдром — повышенная утомляемость, астения, раздражительность, чувство тошноты и дискомфорта в правом подреберье [1][2][6][7][8] .
Диагностика гепатита Е
Лабораторная диагностика:
- Клинический анализ крови — нормальный объём эритроцитов или умеренная лейкопения, повышение количества лимфоцитов, моноцитов и снижение нейтрофилов в крови, сниженная или нормальная СОЭ.
- Биохимический анализ крови — повышенный уровень общего билирубина за счёт прямой и непрямой фракции, увеличение АЛТ и АСТ, сниженый индекс протромбина (ПТИ), повышение тимол-вероналоовой пробы (уменьшение альбуминов и увеличение гамма-глобулинов), повышение ГГТ и щелочной фосфатазы.
- Общий анализ мочи — появление гематурии, протеинурии и цилиндрурии (обнаружение эритроцитов, белка и цилиндров в моче).
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина.
- Серологические тесты — обнаружение антител в сыворотке крови:
- анти-HЕV IgM — выявляются при острой инфекции с конца первой недели от момента заражения, могут сохраняться до двух лет, иногда бывают ложноположительными при активной ЦМВ-инфекции;
- анти-HЕV IgG — выявляются с 41 дня в течение 15 лет методом иммуноферментного анализа (ИФА);
- HЕV RNA — выявляются при острой инфекции, начиная с 22 дня, а также при хронизации в течение долгого времени благодаря полимеразной цепной реакции (ПЦР).
- УЗИ органов брюшной полости — увеличение печени с реактивным изменением структуры её ткани, увеличение лимфоузлов в воротах печени, иногда увеличена селезёнка.
Дифференциальная диагностика с другими заболеваниями:
- Вирусные гепатиты В и С — связь с парентеральными вмешательствами (например, с переливанием крови), более длительный преджелтушный период, характерные серологические тесты. , желтушная форма — выраженный синдром общей инфекционной интоксикации, увеличение лимфоузлов, тонзиллит, специфические изменения общей крови и серологические тесты.
- Жёлтая лихорадка — острое начало, высокая температура, гиперемия и отёчность лица, временное улучшение, а затем ухудшение состояния. — острое начало, высокая температура, частое поражение почек, выраженные боли в икроножных мышцах, изменения общей крови бактериального характера.
- Псевдотуберкулёз — умеренно высокая температура, мезаденит (воспаление лимфоузлов брыжейки кишечника), терминальный илеит (воспаление подвздошной кишки), симптомы носков и капюшона (мелкоточечные высыпания), скарлатиноподобная сыпь, бактериальные изменения крови, специфические маркеры.
- Острые кишечные инфекции, например, сальмонеллёз — острое начало, выраженный синдром поражения ЖКТ (энтерит, колит, высокая температура).
- Листериоз — высокая температура, увеличение лимфоузлов, поражения железистой ткани ротоглотки, бактериальная кровь.
- Сепсис — гектическая (изнуряющая) лихорадка, выраженные полиорганные нарушения.
- Амебиаз — характерные симптомы поражения кишечника, эозинофилия крови, выявления возбудителя.
- Токсические поражения печени — связь с употреблением токсинов, отсутствие синдрома общей инфекционной интоксикации.
- Опухоли гепатобилиарной области — длительное постепенное начало, отсутствие яркой выраженной симптоматики, умеренное повышение АЛТ или АСТ, резкое повышение СОЭ, характерные изменения на УЗИ, КТ или МРТ. — типичные болевые приступы, умеренное повышение АЛТ или АСТ, данные инструментальных исследований [1][2][6][8][10] .
Лечение гепатита Е
При лёгкой степени гепатита Е лечение проводится в амбулаторных условиях (на дому). Во всех остальных случаях показано стационарное лечение в инфекционном отделении больницы. Режим постельный или полупостельный.
Чтобы снизить нагрузку на поражённую печень, необходимо придерживаться механически и химически щадящей диеты № 5 по Певзнеру. Она подразумевает употребление витаминов и повышенного количества воды (более 1,5 л в сутки), исключение алкогольных и газированных напитков, жаренной и острой пищи, грибов, сдобного теста и других продуктов.
Специфического лечения, которое бы устраняло причины гепатита Е, нет. В основном все методы направлены на устранение симптомов, интоксикации и восстановление нормальной функции печени.
Показан приём сорбентов и препаратов, которые повышают энергетические ресурсы. Иногда назначают гепатопротекторы. Если случай тяжёлый, то проводится терапия гормональными средствами и препаратами крови, а также гипербарическая оксигенация (использование кислорода под высоким давлением) и плазмаферез.
Назначение инфузионной терапии — внутривенного введения глюкозо-солевых растворов и витаминов — зависит от степени тяжести и определённых симптомов.
При тяжёлом течении и хронизации возможно применение препаратов общевирусного действия. Они позволяют снизить вирусную нагрузку.
Людям, получающим цитостатическую (противоопухолевую) терапию по возможности следует снизить дозу на 30 %. Это повышает вероятность спонтанной гибели вируса.
Беременные с гепатитом Е должны находиться в условиях реанимации инфекционного стационара. В острый период болезни лечение проводится по общим принципам, преждевременное родоразрешение противопоказано.
Выписывать больных можно в том случае, если в ходе лечения у них стойко улучшается клиническая картина и лабораторные показатели. После выписки пациенты, которые идут на поправку после неосложнённых форм болезни, находятся под наблюдением врача в течение шести месяцев. Осмотр и обследования проводятся минимум один раз в месяц [5] [6] [8] [9] .
Прогноз. Профилактика
Прогноз гепатита Е зачастую благоприятный, за исключением случаев заболевания при беременности. После выписки из больницы окончательное выздоровление наступает спустя 2-3 месяца. Крайне редко болезнь может стать хронической и затяжной.
Чтобы снизить количество случаев инфицирования, необходимо придерживаться следующих правил:
- создавать все условия для того, чтобы потребляемая питьевая вода была безопасной (касается водоснабжения);
- соблюдать правила утилизации сточных вод (канализационное хозяйство);
- соблюдать правила личной гигиены (всегда мыть руки);
- следить за качеством обследования работников, которые связаны с пищевой промышленностью;
- соблюдать технологию хранения, приготовления и транспортировки продуктов питания и воды;
- беременным на любом сроке стоит воздержаться от поездок в потенциально опасные в эпидемиологическим плане места (тёплые страны, особенно Азиатского региона).

Для предотвращения развития болезни разработана специфическая профилактика — вакцинация против гепатита Е. С этой целью применяется вакцина Hecolin (Китай). Она вырабатывает иммунитет к одному генотипу у 95 % трехкратно привитых людей [1] [2] [3] [5] [8] .
Читайте также:

