Герпес ассоциированная многоформная экссудативная эритема
Обновлено: 05.05.2024
ОПРЕДЕЛЕНИЕ
Многоформная эритема (МЭ) – острая иммуноопосредованная воспалительная реакция кожи и, в ряде случаев, слизистых оболочек на различные стимулы, характеризующаяся мишеневидными очагами поражения с периферической локализацией, склонная к рецидивированию и саморазрешению.
Классификация
Общепринятой классификации МЭ не существует.
Этиология и патогенез
В большинстве случаев развитие МЭ связано с герпетической инфекцией; также возможно развитие заболевания под влиянием вирусов гепатитов В и С, Эпштейна-Барра, аденовирусов, Mycoplasma pneumonia, бактериальных и грибковых микроорганизмов.
Причинами заболевания могут являться прием лекарственных препаратов (сульфаниламиды, пенициллины, барбитураты, аллопуринол, фенилбутазон), системные заболевания (саркоидоз, узелковый периартериит, гранулематоз Вегенера, лимфома, лейкоз).
МЭ наблюдается у пациентов всех возрастов, но чаще – у подростков и молодых людей. Среди больных преобладают мужчины (соотношение мужчин и женщин составляет 3:2). Примерно в 30% случаев заболевание рецидивирует. В детском возрасте встречается нечасто (20% случаев).
Клиническая картина
Cимптомы, течение
В зависимости от выраженности клинических проявлений выделяют две формы МЭ:
- легкую, при которой отсутствует поражение слизистых оболочек, общее состояние больного не нарушено;
- тяжелую, характеризующуюся распространенными кожными высыпаниями, поражением слизистых оболочек, общим недомоганием.
Клиническая картина МЭ характеризуется острым началом. Заболевание часто начинается с продромальных явлений (повышение температуры тела, недомогание, боли в мышцах и суставах, боль в горле).
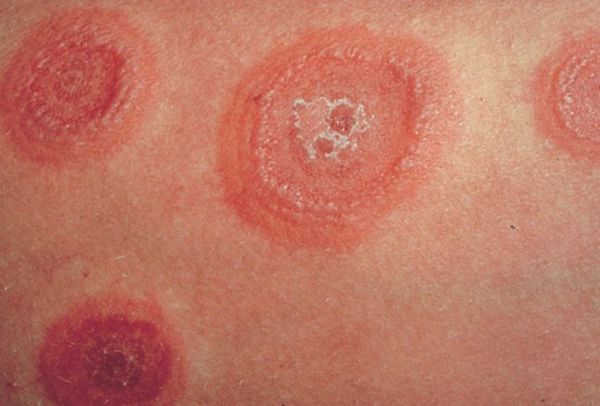
После продромального периода толчкообразно (в течение 10–15 суток и более) появляются полиморфные высыпания на коже – эритемы, папулы, пузырьки. Для МЭ характерны мишеневидные очаги менее 3 см в диаметре с четко очерченными краями, в структуре которых выделяют три различные зоны: центральный диск темной эритемы или пурпуры, который может стать некротическим или трансформироваться в плотную везикулу; кольцо пальпируемого бледного отечного участка; наружное кольцо эритемы. Встречаются и атипичные очаги поражения.
Вторичными морфологическими элементами при МЭ являются эрозии, корки, чешуйки, гиперпигментные пятна, не имеющие клинических особенностей.
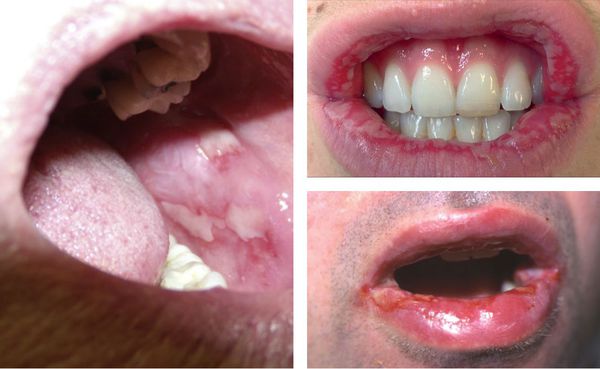
На слизистых оболочках могут образовываться пузыри, которые вскрываются с образованием болезненных эрозий.
Высыпания обычно появляются внезапно, располагаются чаще по периферии, симметрично на коже тыльной поверхности стоп и кистей, разгибательных поверхностях предплечий и голеней, красной кайме губ с образованием корочек, слизистой оболочке полости рта. Поражение глаз и гениталий наблюдается реже.
Разрешение высыпаний продолжается в течение 2–3 недель, не оставляя рубцов. Пигментные пятна, появляющиеся на месте бывших папул, отличаются желтовато-коричневой окраской.
Диагностика
Диагностика типичной МЭ основывается на данных анамнеза заболевания и характерной клинической картине. Отклонения в лабораторных показателях – повышение СОЭ, умеренный лейкоцитоз наблюдаются при тяжелом течении заболевания.
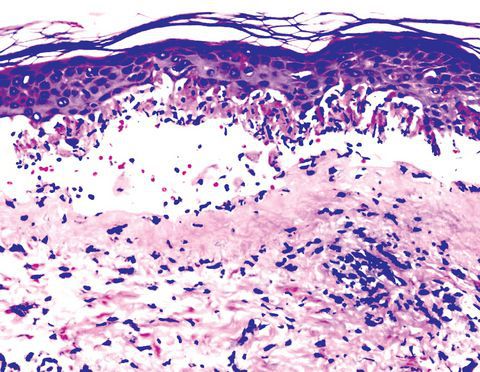
В случае затруднений в диагностике проводят гистологическое исследование биоптата кожи. При гистологическом исследовании наблюдаются отек сосочкового слоя, инфильтрация дермы различной интенсивности. Инфильтрат состоит из лимфоцитов, нейтрофилов и эозинофилов. В базальных клетках эпидермиса наблюдается вакуольная дистрофия. В некоторых участках клетки инфильтрата могут проникать в эпидермис и в результате спонгиоза образовывать внутриэпидермальные пузырьки. Вакуольная дистрофия и выраженный отек сосочкового слоя дермы могут приводить к образованию субэпидермальных пузырей.
Дифференциальный диагноз
Дифференциальную диагностику МЭ необходимо проводить с узловатой эритемой, кольцевидной эритемой Дарье, токсидермиями, вторичным сифилисом, синдромом Свита, пузырными дерматозами, системной красной волчанкой, герпетическим стоматитом, болезнью Кавасаки, уртикарным васкулитом, эрозивной формой красного плоского лишая.
Лечение
- уменьшение тяжести общеинфекционных симптомов и высыпаний;
- сокращение срока госпитализации;
- предупреждение возможных осложнений.
Схемы лечения
Наружная терапия [1]:
1. Растворы анилиновых красителей (метиленовый синий, фукорцин, бриллиантовый зеленый) (D) применяются для обработки эрозий.
2. Глюкокортикостероидные препараты (D):
- метилпреднизолона ацепонат 0,1%, крем 2 раза в сутки наружно на очаги поражения в течение 2 недель
или
- гидрокортизона бутират 0,1% 2 раза в сутки наружно на очаги поражения в течение 2 недель
или
- бетаметазона валерат 0,1% 2 раза в сутки наружно на очаги поражения в течение 2 недель.
3. Комбинированные глюкокортикостероидные препараты + антибактериальные препараты (D):
- бетаметазона валерат + гентамицина сульфат 2 раза в сутки наружно на очаги поражения в течение 2 недель.
Системная терапия
1. При вторичном инфицировании или ассоциации МЭ с Mycoplasma pneumoniae показаны системные антибактериальные препараты:
- эритромицин (D), таблетки 0,5–1,0 г перорально 3 раза в сутки в течение 2 недель.
2. Антигистаминные препараты (D):
- хлоропирамин 25 мг перорально или внутримышечно 2–3 раза в сутки в течение 7–10 дней
или
- мебгидролин 0,1 г перорально 1–3 раза в сутки в течение 7–10 дней
или
- хифенадин 20–50 мг перорально 3–4 раза в сутки в течение 7–10 дней
или
- клемастин 1 мг перорально 2–3 раза в сутки или внутримышечно в течение 7–10 дней
или
- диметинден 4 мг перорально 1 раз в сутки в течение 7–10 дней
или
- лоратадин 10 мг перорально 1 раз в сутки в течение 7–10 дней
или
- цетиризин 10 мг перорально 1 раз в сутки в течение 7–10 дней
или
- левоцетиризин 5 мг перорально 1 раз в сутки в течение 7–10 дней.
3. Глюкокортикостероидные препараты системного действия назначаются при тяжелой форме МЭ:
- преднизолон (C) 30–50 мг в сутки перорально или 0,5–1 мг на кг массы тела с постепенным снижением дозы в течение 2 недель
или
- дексаметазон (C) 4–8 мг в сутки перорально [2].
При регрессе высыпаний дозу глюкокортикостероидных препаратов постепенно снижают до полной отмены.
4. При ассоциации МЭ с вирусом простого герпеса назначают один из противовирусных препаратов:
- ацикловир (A) 200 мг перорально 5 раз в сутки в течение 5–7 дней [3, 4]
или
- валацикловир (A) 500 мг перорально 2 раза в сутки в течение 5–10 дней [5]
или
- фамцикловир (A) 250 мг перорально 2 раза в сутки в течение 7 дней [5].
В случае торпидного течения МЭ рекомендуется профилактическое, противорецидивное, превентивное лечение: ацикловир 400 мг перорально 2 раза в сутки длительными курсами.
5. У больных МЭ без ассоциации с инфекцией простого герпеса возможно использование дапсона 100–150 мг в день (D), гидроксихлорохина 200- 400 мг в день (D) или азатиоприна 100–150 мг в день (D) [6].
Особые ситуации
Лечение детей
У детей раннего детского возраста с обширными поражениями слизистой полости рта необходимо обеспечить достаточное поступление жидкости в организм, проводить инфузионную терапию.
Требования к результатам лечения
- клиническое выздоровление;
- предупреждение развития рецидивов.
ПРОФИЛАКТИКА
Курсовой прием противовирусных препаратов, особенно в весенний период, снижает вероятность рецидивов МЭ, обусловленных вирусом простого герпеса.
Госпитализация
- тяжелое течение МЭ;
- отсутствие эффекта от амбулаторного лечения.
Информация
Источники и литература
- Клинические рекомендации Российского общества дерматовенерологов и косметологов
- 1. Katsambas A.D., Lotti T.M. European handbook of dermatological treatments. Springer. 2003; 515–517. 2. Martinez A.E., Atherton D.J. High-dose systemic corticosteroids can arrest recurrences of severe mucocutaneous erythema multiforme. Pediatr Dermatol 2000; 17: 87–90. 3. Tatnall F.M., Schofield J.K., Leigh I.M. A double-blind, placebo-controlled trial of continuous acyclovir therapy in recurrent erythema multiforme. Br J Dermatol 1995; 132: 267–270. 4. Kerob D., Assier-Bonnet H., Esnault-Gelly P. et al. Recurrent erythema multiforme unresponsive to acyclovir prophylaxis and responsive to valacyclovir continuous therapy. Arch Dermatol 1998; 134 (7): 876–877. 5. Inoue K., Kano Y., Kagawa H. et al. Herpes virus-associated erythema multiforme following valacyclovir and systemic corticosteroid treatment. Eur J Dermatol 2009; 19 (4): 386–387. 6. Schofield J.K., Tatnall F.M., Leigh I.M. Recurrent erythema multiforme: clinical features and treatment in a large series of patients. Br J Dermatol 1993; 128: 542–545.
Информация
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.Методы, использованные для оценки качества и силы доказательств:
· Консенсус экспертов;
· Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).Рейтинговая схема для оценки силы рекомендаций:
Уровни доказательств Описание 1++ Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ) или РКИ с очень низким риском систематических ошибок 1+ Качественно проведенные мета-анализы, систематические, или РКИ с низким риском систематических ошибок 1- Мета-анализы, систематические, или РКИ с высоким риском систематических ошибок 2++ Высококачественные систематические обзоры исследований случай-контроль или когортных исследований. Высококачественные обзоры исследований случай-контроль или когортных исследований с очень низким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи 2+ Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи 2- Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи 3 Неаналитические исследования (например: описания случаев, серий случаев) 4 Мнение экспертов Методы, использованные для анализа доказательств:
· Обзоры опубликованных мета-анализов;
· Систематические обзоры с таблицами доказательств.Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.Рейтинговая схема для оценки силы рекомендаций:
Сила Описание А По меньшей мере один мета-анализ, систематический обзор или РКИ, оцененные как 1++ , напрямую применимые к целевой популяции и демонстрирующие устойчивость результатов
или
группа доказательств, включающая результаты исследований, оцененные как 1+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатовВ Группа доказательств, включающая результаты исследований, оцененные как 2++, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов
или
экстраполированные доказательства из исследований, оцененных как 1++ или 1+С Группа доказательств, включающая результаты исследований, оцененные как 2+, напрямую применимые к целевой популяции и демонстрирующие общую устойчивость результатов;
или
экстраполированные доказательства из исследований, оцененных как 2++D Доказательства уровня 3 или 4;
или
экстраполированные доказательства из исследований, оцененных как 2+Индикаторы доброкачественной практики (Good Practice Points – GPPs):
Рекомендуемая доброкачественная практика базируется на клиническом опыте членов рабочей группы по разработке рекомендаций.Экономический анализ:
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.Метод валидизации рекомендаций:
· Внешняя экспертная оценка;
· Внутренняя экспертная оценка.Рабочая группа:
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы.Основные рекомендации:
Сила рекомендаций (A–D) приводится при изложении текста рекомендаций.Что такое многоформная экссудативная эритема (МЭЭ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Фоминых С.Ю., дерматолога со стажем в 23 года.
Над статьей доктора Фоминых С.Ю. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Многоформная экссудативная эритема (МЭЭ) — это острое аллергическое заболевание, при котором на коже и слизистых оболочках появляются различные по виду высыпания — пятнистые, папулёзные и пузырные.
![Как выглядит многоформная экссудативная эритема]()
МЭЭ обычно болеют люди молодого и среднего возраста. У пациентов мужского пола это заболевание встречается несколько чаще, чем у женщин.
Известны две основные разновидности МЭЭ:
- инфекционно-аллергическая (идиопатическая или истинная) — составляет около 80 % всех случаев МЭЭ и является следствием аллергической реакции на хронический очаг инфекции в организме;
- токсико-аллергическая — развивается, как правило, на фоне применения некоторых лекарственных средств, таких как амидопирин, барбитураты, сульфаниламиды и тетрациклины [7] .
Для инфекционно-аллергической МЭЭ характерна весенне-осенняя сезонность. Одного очага хронической инфекции недостаточно, чтобы данное заболевание развилось или обострилось. Для этого необходимо определённое сочетание триггерных, т. е. провоцирующих факторов, например:
- иммунодефицит (обратимый, преходящий, циклический);
- переохлаждение;
- ультрафиолетовое облучение;
- некоторые консерванты в составе пищевых продуктов (бензоаты, формальдегид и т. д.);
- психоэмоциональный стресс;
- патология пищеварительного тракта (хронический гастрит, дисбактериоз);
- аутоиммунные заболевания и онкопатология; , ангина и другие заболевания.
Не исключается и наличие наследственной предрасположенности к ММЭ.
Причиной инфекционно-аллергической МЭЭ, которая приводит к развитию болезни, чаще всего является герпесвирус человека, вирус Эпштейна — Барр, цитомегаловирус, а также возбудители вирусных гепатитов, микобактерии, микоплазменная, стрептококковая и грибковые инфекции, паразиты. Наиболее распространённый вид инфекционно-аллергической МЭЭ — герпес-ассоциированная МЭЭ [4] [12] [13] .
![Герпес-ассоциированная МЭЭ]()
Считается, что герпесвирусная инфекция [1] [2] [5] становится причиной подавляющего большинства случаев МЭЭ. Чаще всего обнаруживается связь с вирусом простого герпеса первого типа [8] [10] [11] , реже — второго.
В пользу инфекционно-аллергической формы МЭЭ свидетельствует наличие продромального периода (предшествующего болезни), склонности к сезонности высыпаний и хроническое рецидивирующее течение.
Эксперты ВОЗ отмечают, что рост заболеваемости простым герпесом в настоящий момент заставляет рассматривать его в числе первоочередных проблем, наряду с ВИЧ-инфекцией и гриппом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы многоформной экссудативной эритемы
Для инфекционно-аллергической МЭЭ, включая герпес-ассоциированную [13] , характерно острое начало заболевания. Оно может проявляться повышением температуры, общей слабостью, ломотой в теле, головной болью, болезненными ощущениями в горле и другими симптомами.
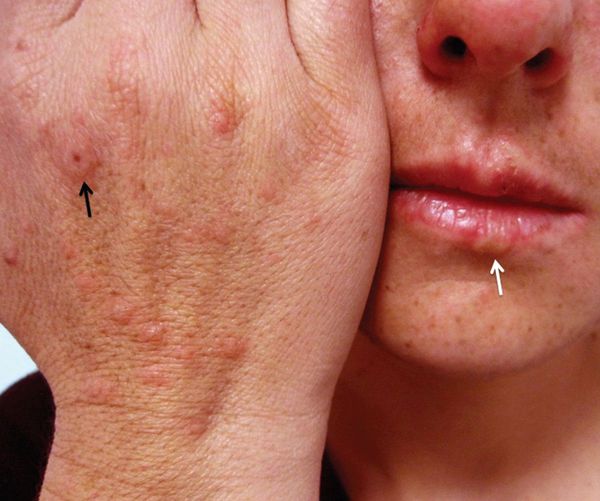
Нередко за несколько дней до обострения МЭЭ у пациентов активируется герпетическая инфекция — проявляется герпес на губах или возникает рецидив генитального герпеса [8] .
Высыпания, характерные для МЭЭ, обычно начинают появляться через 1-2 дня после начала продромальных явлений. При этом общие симптомы обычно идут на спад.
Локализация сыпи весьма разнообразна. Она может появиться как на коже, так и на слизистых оболочках.
Кожные проявления
На коже обычно отмечаются чётко очерченные округлые красно-розовые пятна и плоские отёчные папулы, которые увеличиваются в размерах от 2-3 мм до 3 см в диаметре. При инфекционно-аллергической форме пятна обычно несколько мельче и не склонны к слиянию. Они могут доставлять зуд и жжение.
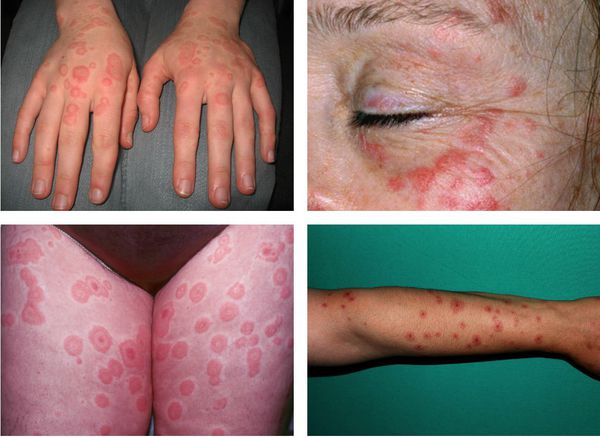
Преимущественная локализация высыпаний — на разгибательной стороне рук и ног, тыльной стороне стоп и кистей, на лице и в области гениталий. В основном они располагаются на теле симметрично, часто группами в виде дуг, гирлянд.
![Преимущественное расположение ММЭ]()
По мере роста папулы её центр начинает западать и менять окраску на более синюшную, по периферии остаётся красно-розовый ободок — таким образом элементы сыпи приобретают характерный вид "мишени" (иногда их сравнивают с "бычьим глазом" или "кокардой") [4] .
После в их центре образуются пузыри — везикулы и буллёзные элементы. Они содержат серозный или кровянистый экссудат. Лопаясь, пузыри формируют желтоватые или коричнево-бурые корочки, эрозированные поверхности.
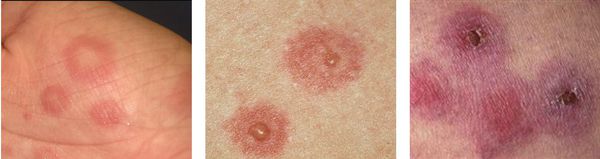
В итоге на теле пациента одновременно присутствуют элементы разной степени развития — пятна, папулы и пузыри, переходящие в корочки и эрозии. Именно поэтому эритема именуется многоформной.
![Этапы развития сыпи]()
С интервалами в несколько дней могут образовываться новые группы высыпаний. Это может затянуть процесс. Но обычно окончательный регресс наступает приблизительно в течение двух недель.
Частота обострений может варьировать от 1-2 до 5-12 раз в год. В редких тяжёлых случаях одно обострение может переходить в другое, практически без светлого промежутка. За это время предыдущие высыпания полностью не разрешаются.
Высыпания на слизистых оболочках
Могут появляться единичные элементы на слизистой полости рта, который не причиняют особого беспокойства. В более тяжёлых случаях поражения бывают настолько обширными и болезненными. Они затрудняют речь и приём даже однородной и жидкой пищи [12] [13] .
Образующиеся пузыри лопаются довольно быстро, поэтому пациент не успевает их заметить — обычно обнаруживаются уже эрозии, на которых иногда можно увидеть плёнчатые фибринозные налёты светлого или бурого оттенка.
![Эрозии и фиброзный налёт]()
В области красной каймы губ могут возникнуть весьма болезненные, растрескивающиеся кровянистые корки, которые не позволяют больному полноценно открывать рот.
Реже высыпания обнаруживаются на слизистых глаз и половых органов. В осложнённых случаях возможно присоединение вторичной инфекции, образование рубцов и синехий (спаек).
Патогенез многоформной экссудативной эритемы
На современном этапе любая разновидность мультиформной экссудативной эритемы рассматривается как сдвиг адаптации защитных механизмов в сторону гиперчувствительности [4] .
МЭЭ — это смешанная аллергическая реакция, в которой просматриваются особенности, характерные для гиперчувствительности как немедленного, так и замедленного типа. Зачастую у пациента явно прослеживается так называемая общая атопическая предрасположенность — исходно у него могут отмечаться, к примеру, признаки пищевой аллергии, атопический ринит, бронхиальная астма и дерматит.
При герпес-ассоциированной МЭЭ у пациентов резко повышается уровень иммуноглобулинов класса Е (IgE) и снижается продукция иммуноглобулинов класса А (IgA), которые обеспечивают "первую линию" защиты кожи и слизистых оболочек. Также отмечается понижение выработки альфа- и гамма-интерферона и образование циркулирующих иммунных комплексов с вирусом простого герпеса.
Вирус повреждает генетический аппарат не только клеток эпидермиса, но и иммунокомпетентных клеток, изменяет состояние их рецепторов, выработку специфических ферментов и провоспалительных цитокинов. В то же время может наблюдаться Т-клеточный и нейтрофильный иммунодефицит, повышение количества В-лимфоцитов. Всё это нарушает связь между различными звеньями иммунитета, искажает нормальный иммунный ответ, заставляет организм проявлять агрессию к собственным тканям, в данном случае — к клеткам эпидермиса и эндотелия сосудов кожи.
Всё вышеперечисленное приводит к образованию лимфоцитарного инфильтрата вокруг кровеносных сосудов кожи, иногда с признаками геморрагии. В базальном слое эпидермиса развивается внутри- и внеклеточный отёк. Сам слой расслаивается, в нём возникают некротические изменения с образованием толстостенных булл.
![Изменение кожи при МЭЭ]()
Степень тяжести патологических проявлений при герпес-ассоциированной МЭЭ во многом зависит от выраженности имеющихся иммунных сдвигов, которые, в свою очередь, могут являться причиной наличия хронического инфекционного очага в организме.
Классификация и стадии развития многоформной экссудативной эритемы
В зависимости от степени выраженности симптомов [3] [12] выделяют две формы МЭЭ:
- малая — поражений слизистых нет или они очень слабо выражены, почти нет общих симптомов;
- большая — протекает с тяжёлым поражением слизистых оболочек, ярко выраженными общими симптомами.
По первичным элементам сыпи, преобладающим в клинической картине МЭЭ, различают пять форм заболевания:
- эритематозная — ограниченное покраснение кожи;
- папулёзная — появление красноватых плотных узелков;
- эритематозно-папулёзная — образование папул с ярко-красными краями и потемневшим центом;
- везикуло-буллёзная — формирование эритематозных бляшек с пузырьком в центре;
- буллёзная — превращение пузырьков в эрозии, которые покрываются корочками.
Воспалительный процесс в зависимости от гистопатологической картины поражения кожи разделяют на три типа [3] :
- эпидермальное воспаление — нарушается наружный слой кожи;
- дермальное воспаление — изменяется толстый слой кожи под эпидермисом;
- смешанное (эпидермо-дермальное) воспаление.
По степени тяжести МЭЭ может быть лёгкой, средней, среднетяжёлой и тяжёлой. В качестве критериев тяжести рассматривают количество и размер буллёзных элементов, наличие поражений слизистых оболочек полости рта и гениталий, температуру тела. Отдельно выделяют часто рецидивирующую форму.
Общепринятой классификации герпес-ассоциированной МЭЭ в настоящее время не существует. В её развитии, как и в развитии МЭЭ, различают два периода:
- продромальный — период активации вирусного процесса;
- буллёзный — период разгара заболевания.
Осложнения многоформной экссудативной эритемы
Осложнения чаще всего развиваются при тяжёлых формах заболевания, а также у людей, организм которых по различным причинам ослаблен [12] [13] .
При обширных поражениях слизистой полости рта резкая болезненность высыпаний затрудняет нормальный гигиенический уход. Когда во рту изначально присутствовали очаги инфекции, возможно развитие такого осложнения, как фузоспирохетоз. Это стоматологическое заболевание характеризуется образованием толстого желтоватого дурно пахнущего налёта на слизистой полости рта, языке и зубах.
Затруднённый приём пищи при генерализованном поражении слизистой полости рта может приводить к истощению пациента.
При локализации высыпаний на слизистой носа возможно развитие ринита с носовыми кровотечениями.
Эрозии на слизистой половых органов могут заживать с образованием синехий (спаек, сращений).
В 22% случаев через эрозивные дефекты покровов проникает вторичная бактериальная инфекция. Это чревато гнойно-септическими осложнениями, образованием более глубоких поражений, на месте которых в редких случаях могут образовываться рубцы.
Поражение слизистой оболочки глаз может осложняться конъюнктивитом и кератитом (кератоконъюнктивитом) [3] .
К числу редких и наиболее серьёзных осложнений можно также отнести постгерпетическую невралгию, пневмонию, почечную недостаточность.
Диагностика многоформной экссудативной эритемы
Для постановки диагноза "МЭЭ" в типичном случае врачу-дерматологу достаточно характерной клинической картины и данных опроса пациента. Имеют значение сведения о хронических очагах инфекции, недавних рецидивах герпетических высыпаний и провоцирующих факторах.
Лабораторные анализы (например, общий анализ крови) в нетяжёлых случаях могут не показать никаких отклонений. При тяжёлых формах отмечается повышение СОЭ и умеренный лейкоцитоз — небольшое повышение уровня лимфоцитов в крови.
Для уточнения диагноза нужно исключить другие, схожие по симптоматике заболевания — пузырчатку, узловатую эритему, системную красную волчанку, вторичный сифилис и другие. С этой целью выполняют цитологическое исследование мазков-отпечатков, взятых с поверхности высыпаний, а также изучение клеток поражённой ткани под микроскопом.
Наличие герпетической инфекции в организме при необходимости можно подтвердить несколькими способами:
- ПЦР-диагностика на инфекции, передающиеся половым путём;
- серологическое обследование на наличие антител к вирусу простого герпеса;
- оценка иммунного статуса.
Дифференциальную диагностику герпес-ассоциированной МЭЭ необходимо проводить с узловатой и кольцевидной эритемой Дарье, токсидермиями, вторичным сифилисом, системной красной волчанкой, герпетическим стоматитом, болезнью Кавасаки, уртикарным васкулитом, красным плоским лишаем (эрозивной формой).
Лечение многоформной экссудативной эритемы
Основные задачи лечения:
- уменьшить тяжесть общих проявлений и количество высыпаний во время обострений;
- сократить длительность рецидивов;
- предотвратить осложнения;
- в межрецидивный период повысить сопротивляемость организма, сократить частоту рецидивов.
При любой форме МЭЭ используют десенсибилизирующую терапию и антигистаминные (противоаллергические) препараты.
При поражении слизистых оболочек рта и половых органов назначаются орошения и полоскания составами, успокаивающими воспаление и подавляющими инфекцию — "Ротокан", настой ромашки и т. п.
Ускорить очищение эрозий от налётов и некротических тканей помогают местные ферментные препараты. Также применяются кератопластические средства и препараты, способствующие регенерации и ускорению эпителизации повреждений.
Показаниями для госпитализации может послужить тяжёлое течение заболевания, а также неэффективность амбулаторного лечения. В нетяжёлых случаях вполне допустимо лечение в домашних условиях, без особых ограничений.
Изоляции больного не требуется, так как он не представляет опасности для здоровья окружающих. Пациенту рекомендуется гипоаллергенная диета, химически и термически щадящая, гомогенная пища (особенно при высыпаниях на слизистой рта), пить достаточное количество воды.
Лечение герпес-ассоциированной МЭЭ
Тактика лечения при герпес-ассоциированной МЭЭ зависит от степени выраженности тех или иных симптомов, стадии развития процесса, частоты и тяжести обострений [3] [4] . Например, если рецидивы возникают часто, высыпания обильны и им характерны некротические изменения, то нередко применяются глюкокортикоиды [14] .
Когда в возникновении заболевания очевидна роль герпесвируса, показан приём синтетических ациклических нуклеозидов — ацикловир, валацикловир [14] , фамцикловир.
В случае торпидного (вялого) течения герпес-ассоциированной МЭЭ рекомендовано профилактическое, противорецидивное и превентивное (предупреждающее) лечение. Для этого длительными курсами применяют препараты, содержащие ацикловир.
Применение антибиотиков в лечении герпес-ассоциированной МЭЭ оправдано лишь при наличии признаков вторичной бактериальной инфекции — нарастание интоксикации и появление гнойного отделяемого.
Чтобы предупредить присоединение вторичной инфекции, эрозированные участки и пузыри обрабатывают растворами антисептиков, например, фукорцином, фурацилином или хлоргексидином.
Прогноз. Профилактика
В большинстве случаев МЭЭ прогноз для жизни и здоровья благоприятный, за исключением редких особо тяжёлых форм болезни у людей с пониженной резистентностью организма.
Рубцы при заживлении повреждений не образуются, за редким исключением. Иногда на месте бывших элементов сыпи изменяется окрас кожи.
Рецидивировать МЭЭ может приблизительно в 30 % случаев. Особое внимание следует уделять тяжёлым поражениям слизистой оболочки и бактериальной суперинфекции [15] .
В качестве первичной профилактики рекомендуется минимизировать риск заражения герпетической инфекцией:
- соблюдать нормы личной гигиены;
- избегать случайных половых связей;
- практиковать защищённый секс.
Чтобы сохранить сопротивляемость организма инфекциям в норме, нужно рационально питаться, соблюдать оптимальный режим труда и отдыха, полноценно спать, регулярно закаляться, отказаться от вредных пристрастий.
Меры неспецифической вторичной профилактики формируются с учётом возможных триггерных факторов. Целесообразно обратить внимание на следующие моменты:
- регулярное прохождение профилактических осмотров и своевременная санация (очищение) хронических очагов инфекции, при ассоциации с герпесвирусной инфекцией — противовирусная терапия;
- защита от избыточного облучения солнечным светом и ультрафиолетового облучения;
- уменьшение вероятности переохлаждения;
- исключение стрессовых воздействий и т. п.
Для предупреждения рецидивов герпес-ассоциированной МЭЭ применяется герпетическая поливакцина, которая вводится по особой схеме. Её эффективность достигает более 70 %: она в 2-4 раза уменьшает частоту рецидивов.
Сокращению числа рецидивов также способствует длительный превентивный приём синтетических ациклических нуклеозидов, препаратов интерферона [6] , его индукторов и целого ряда неспецифических иммуномодуляторов [9] .
Клинические проявления заболевания
Патогенетические и иммунологические аспекты
Многоформная экссудативная эритема относится к заболеваниям, которые имеют характерные клинические проявления, но при этом вызываются разными причинами (об их составе речь пойдет ниже). Постоянная симптоматика, характерная для этого дерматоза, является естественным следствием единства патогенетических механизмов, которые на определенном этапе протекают одинаково при всех формах МЭЭ. Каков их морфологический субстрат? Он описывается в основном как лимфоцитарный инфильтрат вокруг сосудов, с небольшой примесью эозинофилов или нейтрофилов. Этот быстро накапливающийся инфильтрат имеет вид сине-розовых папул. В базальном слое наблюдается внутри- и внеклеточный отек, эпидермис может отслоиться с образованием пузыря, покрышку которого образуют все слои эпидермиса; соответственно, покрышка может сохраняться один-два дня неповрежденной, даже под одеждой или при большом диаметре пузыря. Могут встречаться экстравазаты, внешне проявляющиеся геморрагическими элементами. В целом, так как клиника МЭЭ достаточно типична, потребность в биопсии возникает редко. Патогистологическое исследование может оказаться серьезным подспорьем в диагностике, если клиническая картина МЭЭ представлена в основном пузырями. Мазки-отпечатки позволяют исключить акантолиз и, соответственно, пузырчатку, а малое число эозинофилов в пузырной жидкости снижает вероятность наличия герпетиформного дерматита и буллезного пемфигоида.
В заключение вышеуказанного можно отметить, что в любом случае МЭЭ — это проявление сдвига адаптивных механизмов иммунного ответа в сторону гиперчувствительности, т. е. представляет собой аллергическую реакцию — вне зависимости от причинного фактора.
Предрасположенность и триггерные факторы развития МЭЭ
Инфекционно-аллергическая форма дерматоза встречается чаще и создает больше терапевтических затруднений. Известно много бактериальных и вирусных агентов, которые провоцируют развитие МЭЭ. Как правило, это возбудители, которые формируют в организме очаг хронической персистенции с периодическими обострениями, что способствует сенсибилизации к инфекту. Роль бактериальной аллергии неоднократно находила объективные подтверждения в разного рода исследованиях [2, 13, 14, 15]. Локализация очага может быть любая. Наличие хронической инфекции в организме, уже являющееся следствием тех или иных дефектов иммунной системы, усугубляет их и может вызывать повреждение защитной противоинфекционной реакции, в том числе способствуя выработке медиаторов иммунного ответа, среди эффекторов которых есть клоны клеток, формирующих реакции гиперчувствительности. У наблюдавшихся у нас пациентов мы находили очаги инфекции чаще в области носоглотки, придаточных пазух и дыхательной системы, реже она имела урогенитальную локализацию. Как правило, очаг инфекции не удается определить при первой беседе с пациентом, в большинстве случаев поиск инфекта требует осмотра смежными специалистами, а также лабораторно-инструментального обследования. Впервые развившаяся острая инфекция также может провоцировать МЭЭ, однако в этом случае это происходит спустя одну-две недели. В то же время МЭЭ на обострение хронического очага может проявляться в первые дни его активации.
Патология пищеварительного тракта, которую принято считать одной из причин развития МЭЭ, также не носила явного характера, у всех пациентов при опросе и обследовании выявлялись минимальные симптомы хронического колита, дискинезии желчевыводящих путей, чаще по гипомоторному типу, признаки хронического гастрита, дисбиоз кишечной микрофлоры первой-второй степени. Однако у всех пациентов был снижен уровень IgА, конечный этап синтеза которого происходит в кишечной стенке.
Клинические особенности МЭЭ в зависимости от этиологического агента
Герпесассоциированная многоформная экссудативная эритема
По данным статистики, до 80% МЭЭ вызывается вирусом простого герпеса (ВПГ) [16], поэтому мы провели работу по оценке клинических и иммунологических параметров именно этой формы, как наиболее часто встречающейся в практике. Среди обратившихся к нам пациентов с МЭЭ 73% составила герпесассоциированная экссудативная эритема (ГАМЭЭ).
Следует отметить, что диагноз ГАМЭЭ мы ставили на базе клинических данных. Это были типичные проявления МЭЭ, развившиеся в сроки от 12 ч до 12 дней от начала рецидива простого герпеса (ПГ), имевшего клинически очевидную форму — сгруппированные везикулы на отечно-эритематозном фоне. Проявления ГАМЭЭ характеризовались в основном очагами небольшого размера — до 2,5 см в диаметре, и представлены были всем спектром возможных при МЭЭ элементов. Мономорфную сыпь мы наблюдали всего несколько раз: у двух человек папулезную сыпь, представленную одинаковыми розовыми уплощенными папулами диаметром 1-1,3 см, группировавшимися в локтевых областях у одной пациентки и на всей разгибательной поверхности рук, в небольшом количестве на ногах и туловище у второго пациента. У 54-летней женщины была выявлена буллезная форма — крупные пузыри диаметром от 2 до 7 см, располагавшиеся на боковой поверхности туловища. В основном сыпь при ГАМЭЭ была представлена уплощенными сине-розовыми папулами до 3 см в диаметре, которые разрешались с центра, в центре очагов в ряде случаев формировались пузыри с плотной покрышкой, встречались мелкие пустулы и единичные геморрагические очаги. Особенностью ГАМЭЭ явилось редкое вовлечение в патологический процесс области гениталий. Эволюционная динамика сыпи в целом не имела отличий от МЭЭ. Частота рецидивирования ГАМЭЭ была высокой, 5—12 раз в год, что, вероятно, обусловлено особенностями этиологического фактора — ПГ, при нарушениях противовирусного звена иммунитета, склонного к частому рецидивированию.
Иммунологические параметры ГАМЭЭ
Наряду с клиническими особенностями ГАМЭЭ, интерес представляют ее иммунологические параметры. Выявляемая иммунологически предрасположенность к ГАМЭЭ может в некоторой степени свидетельствовать о предрасположенности к развитию у пациентов с ПГ герпесассоциированных заболеваний. Ведь вирусная репликация может изменять генный аппарат как резидентных клеток, например эпидермоцитов (в этом случае это ведет к ограниченным эпидермисом поражениям), так и иммунокомпетентных клеток, тогда могут наблюдаться системные заболевания, например СКВ. Данное предположение свидетельствует о пользе активной терапии пациентов с соответствующими изменениями. Согласно этой же гипотезе меняться может как рецепторный аппарат клеток, так и ферментный или иммуномедиаторный (цитокиновый) профиль [7].
Для ГАМЭЭ характерны повышение IgE, снижение IgА, понижение числа NK-клеток и g-интерферона, резкое повышение спонтанной выработки ИЛ-4 и ИЛ-6 над индуцированной продукцией, которая истощена, снижение рецепторов к ИЛ-2.
ГАМЭЭ представляет собой смешанную реакцию гиперчувствительности с иммунокомплексным компонентом той или иной степени выраженности.
Терапия многоформной экссудативной эритемы
Лечение данного заболевания включает как купирование рецидива, так и профилактику дальнейших обострений. Следует учитывать, что экссудативная эритема представляет собой аллергическую реакцию, независимо от этиологического фактора. При выявлении триггера добавляются соответствующие мероприятия.
При купировании рецидива мы брали за основу тип протекания дерматоза. Если при первичном обращении пациент сообщает, что у него наблюдаются частые рецидивы и (или) обильные высыпания, имеются участки некроза в центре элементов, поражены слизистые, выражен эпидермолитический компонент, мы применяем однократную инъекцию 2 мл дипроспана (раствор для инъекций, включающий β-метазон в форме динатрия фосфата и диприпионата).
Лечение МЭЭ включает купирование рецидива, чаще с использованием дипроспана, без которого можно обойтись при самолимитирующемся течении дерматоза и воздействии на триггер, которое варьирует в зависимости от его природы.
Терапия ГАМЭЭ
В дальнейшем для профилактики ГАМЭЭ мы применяли герпетическую поливакцину: два курса по пять инъекций в дозе 0,1-0,2-0,3-0,3-0,3 с двухнедельным перерывом между курсами; ревакцинация проводилась через шесть месяцев, и через год — для закрепления результата. Ревакцинацию целесообразно осуществлять в случае, если первый курс оказался эффективным. Если же первая инъекция вызывает обострение процесса, вероятнее всего, она назначена слишком рано. Важно определить момент, когда целесообразно начинать вакцинацию. Мы рассматривали в качестве критерия нормализацию уровней спонтанной и индуцированной выработки ИЛ-4 и ИЛ-6. В ходе этого процесса, который может оказаться довольно длительным, мы назначали фамцикловир по 250 мг два раза в сутки, или валацикловир 500 мг два раза в сутки, либо ацикловир 200 мг четыре раза в сутки. Если при исходном тестировании иммунного статуса повышены уровни других цитокинов, участвующих в формировании воспалительной реакции, например ИЛ-1 или ФНО, для начала вакцинации необходима нормализация уровня их выработки, поскольку повышение данных показателей увеличивает риск поствакцинальных осложнений.
Эффективность вакцинации составила 71%, что заключалось в сокращении числа рецидивов ПГ и, соответственно, уменьшении ГАМЭЭ в два—четыре раза. У нескольких пациентов рецидивы отсутствовали в течение всего периода наблюдения (один год). В целом чем мягче протекает ГАМЭЭ, тем лучше прогноз при вакцинации, поскольку выраженное поражение кожи наблюдается при максимальном компоненте гиперчувствительности, и тем больше времени занимает нормализация цитокинового профиля. В заключение можно напомнить, что применение дипроспана и вакцинация имеют свои противопоказания, такие, как сахарный диабет, язвенная болезнь или глаукома (для дипроспана), поэтому необходим тщательный сбор анамнеза для их выявления. Вакцинация также должна проводиться с учетом всех требований безопасности лечения и при наличии средств для купирования поствакцинальных осложнений, сведения о которых можно найти в соответствующих руководствах по медицинской вакцинологии.
Литература
О. Л. Иванов, доктор медицинских наук, профессор
М. В. Халдина
ММА им. И. М. Сеченова, МоскваРассмотрены причины возникновения и клинические проявления токсикодермий. Указывается, что реакции на лекарства с проявлениями на коже чрезвычайно разнообразны. В некоторых случаях врач не может отменить лекарство, и тогда задача врача — назначить лечение
Reasons of appearance and clinical manifestations of toxicodermia were considered. It was indicated that drug reactions with skin manifestations are extremely versatile. In some cases, the doctor cannot cancel the drug, and then the doctor should prescribe the treatment in order to mitigate the side effects of the drug, or find a substitute for this preparation. Regression in the eruptions after the preparation is cancelled also helps find the reason of the disease.
Высыпания на коже как проявление реакции на лекарства встречаются часто и составляют около 6% из всех случаев госпитализаций. Кожа является органом, который чаще всего участвует в реакции на лекарство. Тяжесть повреждения кожи варьирует от легких макулопапулезных высыпаний до тяжелых реакций, потенциально опасных для жизни [1].
Высыпания очень разнообразны по своим проявлениям и часто имитируют другие заболевания кожи. В связи с этим, наряду с сифилисом, грибовидным микозом, чесоткой и саркоидозом кожи, лекарственно-индуцированный дерматит можно назвать великим имитатором.
Как с современных позиций объясняют развитие токсикодермий? Патогенез токсикодермии
В развитии кожных реакций на лекарства могут участвовать любые из известных типов гиперчувствительности:
- I тип — гиперчувствительность немедленного типа: иммунологическая уртикария и отек Квинке; анафилаксия.
- II тип — антителозависимые клеточные цитотоксические реакции: эксфоллиативная эритродермия; многоформная экссудативная эритема/синдром Стивенса–Джонсона/синдром Лайелла (МЭЭ/ССД/СЛ); фиксированная эритема; эрозии и язвы как проявления реакции на лекарства.
- III тип — реакции иммунных комплексов: лейкоцитокластический васкулит; красная волчанка; дерматомиозит; вульгарная пузырчатка; буллезный пемфигоид; IgA буллезный дерматоз; синдром гиперчувствительности с эозинофилией и системными симптомами (Drug Reaction with Eosinophilia and Systemic Symptoms, DRESS) (иногда); гепариновый некроз; возможно — фиксированная эритема.
- IV тип — гиперчувствительность замедленного типа: аллергический контактный дерматит и системный контактный дерматит; морбилиформная токсикодермия; DRESS; фотоаллергическая токсидермия.
Однако не всегда развитие токсикодермии можно объяснить одним из типов гиперчувствительности по классификации Кумбса. Существует несколько иных объяснений этиопатогенеза токсикодермий в научной литературе.
Теория гаптена
Согласно данной теории, лекарство захватывается специфическим белком, который взаимодействует с рецепторами главного комплекса гистосовместимости (MHC) иммунокомпетентных клеток, вызывая воспалительные реакции.
P-i-теория
Генетическая теория
Предполагаtт, что генетические факторы могут способствовать развитию тяжелых токсикодермий, особенно в генах МНС. К лекарствам, связанным с сильным генетическим фактором риска, относятся противоэпилептические препараты, аллопуринол, абакавир, невирапин, сульфаниламиды, дапсон, нестероидные противовоспалительные препараты (НПВП) и анальгетики. Однако генетические ассоциации различаются между разными этническими группами, возможно, из-за различной распространенности аллелей человеческого лейкоцитарного антигена (HLA) [1]. Варфариновый некроз проявляется при врожденном дефиците протеинов С и S [3]. Врожденные нарушения системы Р450, а также мутации в локусе HLA-B могут способствовать развитию СЛ и ССД [4].
Вирусная теория
Токсикодермия, вызванная аминопенициллиновыми антибиотиками при инфекционном мононуклеозе, известна много лет. Такие высыпания при инфекционном мононуклеозе первоначально рассматривали как неаллергические проявления, поскольку они не рецидивировали после прекращения острой фазы инфекции, вызванной вирусом Эпштейна–Барр (ЭБВ) [2]. Однако позже выяснилось, что ЭБВ может способствовать развитию сенсибилизации к амоксициллину и ампициллину [5]. В связи с этим желательно по возможности избегать в дальнейшем назначения этих препаратов.
Повышенный риск лекарственной токсикодермии имеют ВИЧ-инфицированные, у которых может возникать реактивация цитомегаловируса, ЭБВ, вируса герпеса 6 типа. В нескольких исследованиях выявлена тесная взаимосвязь между вирусами герпеса и DRESS.
Есть несколько объяснений вирусной теории этиопатогенеза токсикодермий: возможно, вирус изменяет метаболизм препарата; или сам препарат может индуцировать вирусную реактивацию, которая вызывает высыпания; вирус вызывает распознавание лекарственного средства в качестве антигена; или вирусная инфекция изменяет нормальную иммуносупрессию и тем самым способствует появлению высыпаний [2].
Некоторые другие механизмы патогенеза
Фототоксические реакции развиваются вследствие изменений молекулы лекарственного препарата под воздействием световой энергии в коже с последующим повреждением кожи. Возникает дестабилизация электронов и образование свободных радикалов либо изменения самих молекул лекарственных препаратов, которые ведут к повреждению тканей организма.
Фотоаллергический дерматит возникает при участии механизмов гиперчувствительности замедленного типа в ответ на изменения лекарства, происходящих под воздействием света или ультрафиолетовых лучей. Например, под воздействием солнечных лучей у пациентов, принимающих дилтиазем, может формироваться супероксид дилтиазема, который вызывает аллергию IV типа [6].
Понять, какое лекарство вызвало ту или иную реакцию, а зачастую вообще понять, что мы имеем дело именно с реакцией на лекарство, бывает сложно. Тем более что возможности лабораторной диагностики реакции на лекарство очень ограничены.
Большую помощь может оказать гистологическое исследование кожи. Однако специфических гистологических признаков, характерных для реакций на лекарства, нет [7]. Исключение составляет фиксированная эритема [8]. Тем не менее есть признаки, которые с большой вероятностью могут указывать на этот диагноз. Разумеется, разные формы токсикодермии имеют различную гистологическую картину. Ниже представлены особенности наиболее часто встречающейся формы заболевания — морбилиформной токсикодермии:
1) периваскулярный и, особенно, интерстициальный воспалительный инфильтрат в дерме, преимущественно поверхностный. При этом периваскулярный инфильтрат неплотный и состоит из лимфоцитов (100%), эозинофилов (60%) и нейтрофилов (50%). В сосочковом слое дермы нейтрофилы часто превалируют над эозинофилами;
2) кластеры нейтрофилов и эозинофилов в просвете расширенных кровеносных сосудов без признаков поражения сосудов (если это не васкулит, вызванный лекарством);
3) токсикодермии, вызванные противосудорожными средствами и анксиолитиками, характеризуются преобладанием нейтрофилов и крупных лимфоцитов;
4) характерен отек сосочкового слоя дермы;
5) извитые пучки коллагеновых волокон, или фиброз, в сосочковом слое дермы встречаются очень редко [9], в отличие от начальных проявлений грибовидного микоза [10].Возможности лабораторной диагностики реакций на лекарства
Диагностическая ценность иммунологических методов исследования реакций на лекарства ограничена. Исключение составляют лишь тесты в случае IgE-опосредованной лекарственной аллергии. Другие методы исследования, такие как реакция бласт-трансформации лимфоцитов, реакция дегрануляции эозинофилов, тест индукции ИФН-g [11] и др., проводятся в основном с целью научных исследований и недоступны многим лабораториям.
Такие провокационные тесты, как прик-тест или патч-тест, для подтверждения лекарства как причины высыпаний, также имеют ограниченную ценность. Накожные тесты могут быть опасны для пациентов с тяжелыми реакциями. За исключением острого генерализованного экзантематозного пустулеза (Acute Generalized Exanthematous Pustulosis, AGEP), патч-тесты имеют низкую чувствительность и специфичность и часто не являются полезными [12]. При подозрении на фотоаллергический дерматит можно провести фотопатч-тесты, однако этот метод исследования в России недоступен.
В связи с этим чаще всего приходится полагаться на знания, которые помогут врачу понять, преимущественно какой вид реакции вызывает тот или иной препарат. Следует опираться также на литературные данные, а также собственный опыт и придерживаться определенной логики в постановке диагноза.
Клинические проявления кожных реакций на лекарства
Мы не затрагиваем в нашей статье лечение токсикодермий. Чаще всего выбор метода лечения не вызывает вопросов, за исключением самого тяжелого варианта, СЛ.
Ниже кратко рассмотрим наиболее характерные проявления кожных реакций на лекарства.
Клинические проявления токсикодермии можно условно разделить на типичные формы токсикодермии и токсикодермии, имитирующие другие дерматозы. В первом случае мы знаем, что в качестве этиологического фактора следует искать лекарство. Во втором — есть сомнения в постановке правильного диагноза из-за недостаточно типичной клинической картины, различных проявлений токсикодермии и т. п.
Типичные формы токсикодермии
К ним можно отнести: морбилиформную (кореподобную) токсикодермию; МЭЭ/ССД/СЛ; фиксированную эритему; DRESS; AGEP.
Токсико-аллергическая форма многоформной экссудативной эритемы, синдром Стивенса–Джонсона и токсический эпидермальный некролиз, или синдром Лайелла
Токсико-аллергическая форма многоформной экссудативной эритемы, синдром Стивенса–Джонсона и токсический эпидермальный некролиз, или синдром Лайелла, по своей природе являются одним и тем же заболеванием. Главное отличие каждого из них — площадь поражения кожи. При этом есть и клинические особенности заболевания (табл. 1). Токсико-аллергическая форма МЭЭ в случае реакции на лекарство отличается от герпес-ассоциированной МЭЭ наличием поражения слизистых, и прежде всего — слизистой полости рта.
При большей площади поражения — до 10% поверхности тела — возникает ССД. Как и в случае МЭЭ, при этом есть пятна, напоминающие мишень, но они более крупные. Кроме того, при МЭЭ они трехцветные, зачастую отечные или даже с поверхностным пузырем, а при ССД — двухцветные и без признаков экссудации или отека. При этом поражение слизистых при ССД очень выражено, характерно образование пузырей, помимо слизистых полости рта поражается также слизистая оболочка гениталий.
При площади поражения кожи от 10% до 30% считается, что это переходная форма между ССД и СЛ. При поражении кожи более 30% развивается СЛ. Как известно, СЛ — самое тяжелое проявление токсикодермии, при котором до сих пор летальность может достигать 30% и даже 60% [13]. Прогноз СЛ зависит от различных факторов, и прежде всего — от наличия сопутствующей злокачественной опухоли, возраста и некоторых показателей лабораторных исследований. Для того чтобы предсказать смертность пациентов, Batuji-Garin et al. предложили систему подсчета очков для СЛ, назвав ее SCORTEN (Severity-of-illness score for Toxic Epidermal Necrolysis) [14] (табл. 2, 3).
В отличие от ССД, на коже при СЛ появляются не столько пузыри, сколько имеет место отторжение эпидермиса на фоне интенсивной эритемы. Название заболевания — токсический эпидермальный некролиз — достаточно точно отражает этот процесс.
Одним из лекарств, которые чаще всего вызывают СЛ (табл. 4), по данным литературы, является ламотриджин. Так, 1 из 1000 взрослых и 1 из 50–100 детей, получавших ламотриджин, развивали тяжелую реакцию на лекарство [15]. Нет другого лекарства, для которого СЛ был бы столь типичным, как для этого антиконвульсанта. Неотложные меры, предпринятые уже при первых проявлениях реакции на ламотриджин, могут предотвратить развитие тяжелого течения заболевания. Первые симптомы реакции, генерализованный зуд и невыраженная распространенная эритема, требуют немедленной отмены ламотриджина и введения системного кортикостероида в достаточно высокой дозе.
Синдром гиперчувствительности с эозинофилией и системными симптомами
Нередко в литературе используется синоним этого заболевания, Drug-induced Hypersensitivity Syndrome (DIHS). Широкий спектр клинических признаков и длительный латентный период, которые характерны для DRESS, часто приводят к задержке постановки диагноза. Как правило, у пациента с лихорадкой, сыпью, лимфаденопатией, лейкоцитозом и повышенным уровнем печеночных ферментов врачи сначала предполагают инфекционное заболевание. Однако оценка высыпаний и характера изменений показателей периферической крови предположительно указывают на то, что заболевание вызвано лекарственным препаратом [16]. Синдром обычно развивается через 2–6 недель после начала приема лекарств. Вначале у пациента повышается температура и появляются макулопапулезные (кореподобные, то есть морбилиформные) высыпания, которые могут прогрессировать до эксфолиативной эритродермии. Лимфаденопатия, гепатит, почечная дисфункция и гематологические нарушения наблюдаются в разной степени, реже вовлекаются другие органы и системы организма. Для этого заболевания очень характерен отек лица, порой грубый. Следует помнить о том, что эти симптомы иногда могут возникать даже через несколько недель после отмены лекарства [17]. Типичным для DRESS является реактивация герпес-вирусной инфекции. Tetsuo Shiohara с соавт. считают, что этот синдром следует рассматривать как реакцию, вызванную сложным взаимодействием между несколькими герпесвирусами (ЭБВ, герпесвирус 6 или 7 типа, цитомегаловирус), антивирусным иммунным ответом и специфической реакцией организма на лекарство [18]. Наиболее типичные лекарства, способные вызвать DRESS, — антиконвульсанты, аллопуринол, дапсон, НПВС, сульфаниламиды (табл. 4).
Острый генерализованный экзантематозный пустулез
Острый генерализованный экзантематозный пустулез (AGEP) развивается наиболее часто как следствие лечения бета-лактамными пенициллинами. Были также описаны случаи AGEP при приеме тербинафина [19]. Это своеобразная реакция на лекарство, которая проявляется в виде распространенных мелких эпидермальных пустул, напоминающих генерализованный пустулезный псориаз. Иногда наблюдаются повышение температуры, озноб, нейтрофильный лейкоцитоз в периферической крови.
Морбилиформная (кореподобная, или макулопапулезная) токсикодермия
Морбилиформная (кореподобная, или макулопапулезная) токсикодермия составляет около 95% случаев среди всех токсидермий. Проявляется в виде симметричных зудящих макулопапулезных высыпаний без вовлечения слизистой оболочки, которые появляются через 1–14 дней после начала лечения. В основном причиной морбилиформной токсикодермии являются β-лактамные антибиотики, сульфаниламиды, аллопуринол, антиконвульсанты, НПВС.
Фиксированная эритема
Фиксированная эритема представляет собой эритему округлой формы с четкими границами, иногда возникает эпидермальный пузырь в центральной части эритемы. Реакция возникает в течение суток после введения препарата. Кроме того, при повторном приеме лекарства, вызвавшего это заболевание, эритема возникает на том же месте. Изредка возможна распространенная фиксированная эритема. Обычно после прекращения приема препарата, вызвавшего фиксированную эритему, остается гиперпигментация кожи. Типичные лекарства, вызывающие фиксированную эритему: гидроксазин, гистазин, НПВС, парацетамол, псевдоэфедрин (не оставляет гиперпигментации), сульфаниламиды, тетрациклин, эритромицин. В литературе описан случай фиксированной эритемы на цетиризин [20] и левоцетиризин [21].
Клинические проявления токсикодермий, имитирующие другие дерматозы
Синдром Свита (острый фебрильный нейтрофильный дерматоз) может быть вызван такими препаратами, как гранулоцитарный колониестимулирующий фактор, гормональные контрацептивы, триметоприм/сульфаметоксазол, третиноин, изотретиноин. Чаще всего высыпания в виде эритемы, инфильтрированных болезненных бляшек и узлов возникают на лице, верхних конечностях и верхней части туловища, на фоне кратковременной высокой температуры и озноба. В периферической крови обнаруживается нейтрофильный лейкоцитоз.
Фоточувствительные лекарственные дерматиты
На сегодня известно много разных лекарственных препаратов, которые могут быть причиной фоточувствительных дерматозов. Однако, по мнению канадских дерматологов A. M. Drucker и C. F. Rosen, среди них есть только десять препаратов, которых следует рассматривать в качестве мощных фотосенсибилизаторов. К ним относятся: амиодарон, хлорпромазин, доксициклин, гидрохлортиазид, налидиксовая кислота, напроксен, пироксикам, тетрациклин, тиоридазин и вориконазол [22].
Фототоксический дерматит
Фототоксический дерматит наиболее часто встречается среди других фоточувствительных дерматитов, вызванных лекарственными средствами (табл. 5). Такая реакция, как и простой ирритантный контактный дерматит, развивается в течение нескольких минут — нескольких часов: границы очагов четкие и соответствуют локализации облучения в соответствии с краями одежды. Субъективно пациента беспокоит жжение и болезненность кожи. Сила побочного эффекта зависит от дозы препарата и от пороговой чувствительности кожи человека к световым или ультрафиолетовым лучам. Механизмы развития фоточувствительности на лекарства [33] представлены на рис.
Фотоаллергическая токсикодермия
Фотоаллергическая токсикодермия классически представляет собой зудящую экзематозную сыпь. Фотоаллергия встречается гораздо реже, чем фототоксические реакции. Некоторые лекарства могут вызывать как фототоксический, так и фотоаллергический дерматит (табл. 5).
Псевдопорфирия
Псевдопорфирия возникает в ответ на лечение некоторыми НПВС (чаще напроксен), а также тетрациклином и реже — гормональными контрацептивами (табл. 4, 5). Клинически она неотличима от поздней кожной порфирии, но не имеет специфических биохимических маркеров этого заболевания.
Системная красная волчанка (СКВ)
Некоторые лекарства взаимодействуют с гистоном ядер, являясь гаптенами, в результате в организме вырабатываются антигистоновые антитела, которые при участии комплемента запускают механизм красной волчанки как проявление реакции на лекарство. Типичные лекарства: антиконвульсанты, гризеофульвин, пеницилламин, прокаинамид.
Окончание статьи читайте в следующем номере.
Ю. Г. Халиулин 1 , кандидат медицинских наук
Д. Ш. Мачарадзе, доктор медцинских наук, профессорФГАОУ ВО РУДН, Москва
Кожные реакции на лекарства. Как распознать? (Часть 1)/ Ю. Г. Халиулин, Д. Ш. Мачарадзе
Для цитирования: Лечащий врач № 10/2018; Номера страниц в выпуске: 67-72
Теги: антибиотики, кожные проявления, гиперчувствительностьЧитайте также: