Герпес на плече при воспалении плечевого нерва
Обновлено: 23.04.2024
Профессор А.С. Никифоров, к.м.н. О.И. Мендель
РГМУ, Москва
На сегодняшний день плечелопаточный болевой синдром принято считать симптомокомплексом полиэтиологического типа. Его клинические проявления могут быть обусловлены поражением связочно-мышечного аппарата, окружающего плечевой сустав, самого плечевого сустава (артрит), а также патологическими изменениями на уровне шейного отдела позвоночника (шейный остеохондроз и спондилоартроз).
Наиболее частой причиной острой, подострой и хронической боли в области плеча являются дегенеративно-воспалительные поражения сухожилий глубоких мышц плеча. В этой связи выделяют поражение мышц, окружающих сустав (дегенерация, кальцификация, частичные или полные разрывы, воспаление), патологию ключично-акромиального сустава, поражения капсулы сустава, субакромиальной сумки и комплексное поражение структур, расположенных под акромионом (субакромиальный синдром).
В Международной классификации болезней 10-го пересмотра (1995 г.) все периартикулярные поражения области плечевого сустава представлены в виде отдельных нозологических форм, в основном соответствующих классификации, предложенной T. Thornhill (табл. 1)
Таблица 1.
Классификация периартикулярных поражений области плечевого сустава (Т. Thornhill, 1989)
| 1. Тендинит мышц вращательной манжеты (с указанием конкретной мышцы) 2. Тендинит двуглавой мышцы плеча 3. Кальцифицирующий тендинит 4. Разрыв (частичный или полный) сухожилий мышц области плечевого сустава 5. Ретрактильный капсулит |
Следует отметить, что в данную классификацию вошли далеко не все состояния, проявляющиеся болью в области плеча. Что касается связи плечелопаточного синдрома с патологией позвоночных структур, то на сегодняшний день здесь нет единого мнения. Большинство зарубежных исследователей признают самостоятельность и локальность процессов в плечевом поясе, считая их лишь совпадающими по времени с прогрессированием остеохондроза. Отечественными неврологами рассматривается возможность неврогенной этиологии плечелопаточного синдрома и предлагается следующий механизм его развития: поражение спинномозговых корешков в позвоночнике и нервных стволиков в капсуле плечевого сустава вызывают формирование очагов нейроостеофиброза по рефлекторным механизмам. В качестве доказательства правомочности этой теории свидетельствуют следующие аргументы: данный синдром развивается на фоне уже имеющихся симптомов шейного остеохондроза или спондилоартроза; в некоторых случаях наблюдается развитие двухстороннего процесса (с вовлечением плечевых суставов); дерецепция пораженного диска купирует проявления плечелопаточного синдрома. Ряд авторов высказывают мнение, что, возможно, имеет место сочетание двигательной дисфункции в шейном отделе позвоночника и болей в нем с плечелопаточной патологией, обусловленной мышечно-тоническим и мио-фасциальным синдромами плечевого пояса.
Помимо вышеуказанных нужно иметь в виду и другие, различные по этиологии и патогенезу причины болевых проявлений и двигательных расстройств в плечевом суставе и в шейном отделе позвоночника. Среди них - различные варианты поражения плечевого сплетения, отдельных сосудисто-нервных пучков, как это бывает при тоннельных синдромах, развитие дегенеративных и деструктивных процессов, в основе которых могут быть общие сосудистые заболевания, ведущие к локальным гемо-динамическим нарушениям, а также неопластические процессы.
Клиническая картина и топическая диагностика периартикулярных поражений области плеча
Наиболее частой причиной боли и ограничения движений в плечевом суставе признается дегенеративно-воспалительное поражение сухожилий глубоких мышц, участвующих в движениях плеча - тендиниты. Это обусловлено анатомическими особенностями строения плечевого сустава - с прохождением сухожилий в узких анатомических каналах, и с большой нагрузкой, приходящейся на эти мышцы. К этиологическим факторам тендинитов относят микротравматизацию, кальцификацию, нарушения обменных процессов. Нередко имеет место сочетание нескольких факторов, из которых трудно выделить главный. Так, дегенеративные изменения сухожилий вращательной манжеты плеча, с одной стороны, могут быть проявлением естественного процесса инволюции, с другой - результатом микротравм, последствия которых накапливаются в течение всей жизни Появление боли при поражении сухожилий области плечевого сустава в большинстве случаев связано с присоединением к первичному дегенеративному процессу воспалительной реакции.
Микроскопические изменения в тканях при тендинитах. На начальных стадиях выявляются очаговый некроз или частичные разрывы сухожильных волокон, асептическое воспаление сухожилий и серозных сумок. На поздних стадиях - фиброзные изменения, ведущие к развитию контрактур. При кальцифицирующем периартрите в околосуставных тканях определяются отложения солей кальция, чаще гидроксиапатита.
Стадии прогрессирования тендинита:
Стадия 1 - отек и геморрагии бурсы и сухожилия
Стадия 2 - фиброз и воспаление бурсы и сухожилия
Стадия 3 - разрывы сухожилия и костные изменения
Тендинит мышц вращающей манжетки плеча. Для тендинита мышц вращающей манжетки плеча характерна боль в верхне-наружном отделе плеча, иногда иррадиирущая в локоть. Боль, как правило, возникает после значительных и непривычных физических нагрузок, например, после работы с высоко поднятыми руками.
Тендинит сухожилия длинной головки двуглавой мышцы плеча (бицепса). При этом состоянии возникает боль в верхне-передних отделах плеча. Боль проявляется после физических нагрузок, связанных с перенапряжением двуглавой мышцы (поднятие тяжестей). При пальпации определяется болезненность в межбугорковой борозде. Отведение и ротация плеча, как правило, не нарушены. Для выявления поражения сухожилия бицепса проводят тест сопротивления активной супинации кисти. Положение руки больного такое же, как при исследовании вращающей манжеты (плечо прижато к туловищу). Врач обеими руками обхватывает кисть больного и просит его совершить активную супинацию кисти, а сам оказывает сопротивление этому движению. При поражении длинной головки двуглавой мышцы плеча возникает боль.
Для поражения сухожилия надостной мышцы или ткани субакромиальной сумки характерна боль в среднем секторе верхней дуги плечевого сустава, а также боль при сопротивлении активному отведению плеча, но его маятникообразные движения вперед и назад при этом остаются безболезненными.
При поражении подостной и малой круглой мышц положительна проба сопротивления активной наружной ротации плеча. Во время ее проведения больной сгибает руку в локтевом суставе на 90 градусов. Врач одной рукой прижимает локоть больного к туловищу, другой рукой фиксирует предплечье, и просит больного отводить плечо, оказывая сопротивление этому движению. У больного при этом затруднено причесывание головы. В момент выполнения пробы возникает боль в верхнем отделе плеча.
При поражении подлопаточной мышцы положительна проба сопротивления активной внутренней ротации. Производится при положении руки больного в позиции аналогично той же, что и при проведении описанной выше пробы, только в этом случае боль возникает при внутренней ротации плеча, например, при попытке завести руку за спину. Иногда определяется болезненность при пальпации места проекции поврежденных сухожилий. Пальпация проводится следующим образом: больного просят положить руку на противоположное плечо. Врач под выступающим участком акромиона по направлению к большому бугорку последовательно пальпирует сухожилия надостной, подостной, малой круглой мышц. Затем больной заводит руку за спину, а врач под передним отделом акромиального отростка по направлению к малому бугорку плечевой кости пальпирует сухожилие подлопаточной мышцы.
Для вовлечения в патологический процесс ключично-акромиального сустава выявляется ограничение максимального отведения руки (более, чем на 90 градусов) из-за болевого синдрома. Пальпаторная болезненность в проекции ключично-акромиального сустава подтверждает диагноз.
Таблица 2.
Определение пораженных структур области плечевого сустава на основании жалоб пациента (по А.Г. Беленькому)
| Боль, ограничение движения | Пораженная структура |
| Отведение руки | Сухожилие надостной мышцы, субакромиальная сумка |
| Максимальный подъем руки вверх | Ключично-акромиальный сустав |
| Наружная ротация (попытка причесаться) | Сухожилия подостной и малой круглой мышц |
| Внутренняя ротация (попытка завести руку за спину) | Сухожилие подлопаточной мышцы |
| Сгибание в локтевом суставе и супинация предплечья (подъем тяжести, поворот ключа в двери кнаружи) | Сухожилия двуглавой мышцы плеча |
| Нарушены (болезненны и/или ограничены) все движения | Поражение капсулы (или собственно плечевого сустава) |
Нередко при шейном остеохондрозе, цервикалгии и шейном радикулите возникает ночная дизестезия рук -брахиалгия Вартенберга или ночная брахиалгия Путмена-Шультца. Для этого синдрома характерны боль, дизестезии, парестезии, возникающие в зоне С6- С8 дерматомов во время сна, ведущие к пробуждению и исчезающие обычно при активных движениях руками. Расценивается как следствие растяжения плечевого сплетения или вторичных гемодинамических расстройств в нем. Чаще проявляется у женщин в период менопаузы.
Синдром передней и средней лестничных мышц, мышцы, поднимающей лопатку, малой грудной мышцы также проявляются болью в области плечевого пояса. Их диагностика базируется на данных пальпации мышц, выявлении характерных триггерных точек и двигательных расстройств. Пациентов нередко больше беспокоит боль, чем ограничение движений. Особенностью клинической картины синдрома передней лестничной мышцы, помимо наличия болей в плече, надплечье, иногда - в кисти, являются признаки компрессии нервно-мышечного пучка в межлестничном промежутке. Характерны разной степени выраженности сенсорные и вазомоторные расстройства, а также усиление болей при наклоне головы в здоровую сторону, отведении и ротации плеча.
Медикаментозное лечение. Медикаментозное лечение при плечелопаточном синдроме, в первую очередь, направлено на уменьшение боли, отека тканей, снятие мышечного спазма и увеличение функционального состояния плечевого сустава. Однако современные представления о преимущественно дегенеративном характере поражения сухожильно-связочных структур при плечелопаточном синдроме, предполагают возможность повышения эффективности терапии за счет использования препаратов, способных повлиять на процесс дегенерации.
Системная противовоспалительная и обезболивающая терапия. Для купирования болей в плечелопаточной области широко применяются простые аналгетики (парацетамол), нестероидные противовоспалительные препараты (НПВП) и мышечные релаксанты. В классическом варианте используют как неселективные (диклофенак 100-150 мг/сут., ибупрофен 1200 мг/сут. и т.д.), так и селективные (мелоксикам до 15 мг/сут, целекоксиб 100-200 мг/сут.) НПВП. При выраженном болевом синдроме в некоторых случаях приходится прибегать к применению наркотических анальгетиков - трамадола или его сочетания с парацетамолом. При мышечно-тоническом синдроме эффективно использование мышечных релаксантов (тизанидин 6-12 мг/сут., толперизон 150-300 мг/сут.). Миорелаксанты снижают патологическое мышечное напряжение, уменьшают боль и облегчают движения в позвоночнике и суставах. Доказано, что при болевом синдроме, возникающем вследствие мышечного спазма, сочетанное применение НПВП и миорелаксантов приводит к более быстрому регрессу боли и восстановлению функциональных способностей. НПВП назначаются на срок не более, чем 1-2 недели. Длительное проведение противовоспалительной терапии не рекомендуется в связи с возможностью развития нежелательных эффектов, в первую очередь, со стороны желудочно-кишечного тракта. Определенный лечебный эффект можно ожидать и от применения локальных лекарственных средств, содержащих обезболивающие и противовоспалительные средства в виде мазей, геля, кремов и т.д. Они удобны тем, что в случае их применения существенно сокращается вероятность развития побочных эффектов от применения НПВП.
Терапия, направленная на улучшение регенеративных процессов в структурах опорно-двигательного аппарата. В большинстве случаев в основе клинических проявлений плечелопаточного синдрома лежит поражение связочно-сухожильного аппарата, преимущественно дегенеративного характера. В то же время, одним из важнейших факторов, предопределяющих вероятность хронического течения боли при плечелопаточном болевом синдроме, могут быть нарастающие в степени выраженности дегенеративные процессы в хрящевой ткани различных структур позвоночника.
Таким образом, в комплексном лечении плечелопаточного синдрома целесообразно применение фармакологических средств, стимулирующих продукцию составляющих соединительной ткани (тканей сухожильно-связочного аппарата) и хрящевой ткани (в том числе структур позвоночника), замедляющих их разрушение, и тем самым препятствующих прогрессированию дегенеративных заболеваний всех структур опорно-двигательного аппарата.
Большинство клинических исследований ХС и Г, проведенных в мире, связано с изучением их действия при остеоартрозе периферических суставов. Эффективность ХС и Г в отношении подавляющего влияния на дегенерацию суставного хряща, а также наличие у них достоверного противовоспалительного эффекта, подтверждены в исследованиях на моделях ОА у животных и в клинической практике. В двойных слепых плацебоконтролируемых исследованиях доказано, что при остеоартрозе ХС и Г способствуют более быстрому купированию болевого синдрома, восстанавливают подвижность пораженных суставов, а также способны предупреждать повторные обострения и улучшать состояние суставного хряща, обеспечивая существенное замедление дальнейшего развития дегенеративного процесса. Имеется целый ряд работ как зарубежных, так и отечественных авторов, посвященных исследованиям эффективности ХС, Г и их комбинации при остеохондрозе и спондилоартрозе. По этим данным ХС и Г оказывают положительное влияние на обмен в хрящевой ткани МПД и межпозвонковых суставов, способствуя замедлению прогрессирования остеохондроза и спондилоартроза.
Исследования in vivo и in vitro продемонстрировали наличие синергических отношений между ХС и Г, связанных с улучшением регуляции синтеза матричных протеогликанов и деактивацией активности металлопротеаз, что свидетельствует о целесообразности их совместного применения для получения более достоверного лечебного эффекта. Более высокий лечебный эффект комбинации ХС и Г на болевой синдром при остеоартрозе коленных суставов подтвержден в двойном слепом плацебо контролируемом исследовании, проведенном в 2003-2005 гг. на базе нескольких научно-клинических центрах США.
Комбинированный хондропротектор АРТРА (500 мг хондроитина сульфата и 500 мг глюкозамина гидрохлорида) уже в течение нескольких лет успешно применяется в лечении дегенеративных заболеваний опорно-двигательного аппарата. Клинические исследования, проведенные в ведущих медицинских центрах России, показали, что препарат АРТРА оказывает достоверное обезболивающее и противовоспалительное действие (уменьшает боль и скованность в пораженных суставах и позвоночнике (рис. 1, 2), улучшает функциональное состояние суставов и позвоночника, позволяет снизить дозу или полностью отменить принимаемые больным НПВП. Эффективность АРТРА с клинической точки зрения подтверждена данными МРТ, которое выявило на фоне лечения АРТРА увеличение площади суставной поверхности и высоты хряща в исследуемых точках у пациентов с ОА коленных суставов. АРТРА обладает прекрасной переносимостью и высокой безопасностью. На фоне приема АРТРА в два раза снижается частота НПВП-гастропатий и снижается риск обострений заболеваний сердечно-сосудистой системы (АГ, ИБС).
Рис. 1. Динамика боли (WOMAC) на фоне лечения АРТРА + диклофенак vs диклофенак. Различия между группами: через 1 месяц лечения p=0,0003
Рис. 2. Динамика болевого синдрома в спине (WOMAC боли) у пациентов с остехондрозом и спондилоартрозом через 6 месяцев на фоне терапии АРТРА
Таким образом, включение препаратов ХС и Г (АРТРА) в схемы лечения больных с плечелопаточным болевым синдромом, обусловленным дегенеративными изменениями (тендиниты сухожилий глубоких мышц плеча, в том числе на фоне травмы, поражение ключично-акромиального сустава, остеохондроз шейного отдела позвоночника и т.д.), позволит позитивно повлиять на болевой синдром, уменьшить дегенеративные изменения во всех тканях плечелопаточной области и ускорить их восстановление.
Вирус герпеса третьего типа varicella zoster (VZV) вызывает два клинически обособленных заболевания - ветряную оспу и опоясывающий герпес (Баринский И.Ф. и др., 1986; Haanpaa M., 2001). Оба заболевания, прежде всего, характеризуются везикулярной сыпью. Первичная инфекция манифестирует в форме ветряной оспы (ветрянки), а реактивация латентного VZV обусловливает появление локализованных высыпаний - опоясывающего лишая (Хахалин Н.Н., 2002). Мысль о связи между ветрянкой оспой и опоясывающим лишаем впервые была высказана в 1888 венским врачом Яношом Бокеем (von Bokay J., 1909).
Эпизод ветряной оспы в детстве способствует формированию специфической клеточной и гуморальной иммунной защиты. Считается, что рецидив инфекции у таких пациентов может развиться только на фоне недостаточности иммунной защиты, вследствие снижения активности специфических натуральных киллеров, Т-киллеров и системы интерферонов (Fleming D.M. et al., 2004). После первичной инфекции излюбленным местом персистенции VZV являются ганглий тройничного нерва и спинномозговые ганглии чувствительных корешков грудного отдела спинного мозга, где VZV находится в латентном состоянии. В течение этого времени вирус не размножается и не проявляет патогенных свойств. По-видимому, время латентного состояния вируса определяется уровнем специфических антител к VZV. Снижение их количества ведет к реактивации вируса, вирусной репликации (размножению), что на клиническом уровне и проявляется в виде опоясывающего лишая (Arvin A., 2005). Данный вывод подтверждается высокой корреляцией между вероятностью возникновения опоясывающего лишая у людей пожилого возраста и возрастным ослаблением активности клеточного звена иммунитета (Gilden et al., 2000)., На это также указывают данные, свидетельствующие о более высокой заболеваемости опоясывающим герпесом среди лиц, инфицированных вирусом иммунодефицита человека (Gilson I.H. et al., 1989), однако точные механизмы, лежащие в основе перехода вируса из латентного состояния в активное неизвестны.
В случае реактивации VZV ганглии чувствительных нервов становятся местами репликации вируса, именно в них обнаруживаются наиболее выраженные дегенеративные повреждения нейронов (Zerboni L. et al., 2005; Reichelt M. et al., 2008). В результате развивается ганглионит, сопровождаемый распространением инфекции вниз по нервным аксонам к коже. Каким образом происходит транспортировка вируса в поврежденных аксонах неизвестно. Инфекция также может распространяться центрально, приводя к воспалению оболочек в области передних и задних рогов спинного мозга (Gray F. et al. 1994). Отдельные патолого-анатомические наблюдения также свидетельствуют о наличии воспалительных изменений и в контралатеральных спинномозговых ганглиях (Miller S. E. et al., 1997), отмечается снижение количества нейронов и наличие воспалительных инфильтратов в ганглиях, периферических нервах, и спинномозговых корешках (Gowrishankar K. et al., 2007). В некоторых случаях отмечается выраженные некротические изменения в спинномозговых ганглиях. Большинство изменений в периферическом нерве протекает по типу Валлериановской дегенерации, имеющей место, как в толстых, так и в тонких волокнах. (Denny-Brown et al., 1944).
Острая VZV инфекция клинически характеризуется стадией продрома и стадией везикулярных высыпаний (Arvin A., 2005).
Сыпь обычно локализуется в одном или нескольких смежных дерматомах и сопровождается развитием острой невропатической боли. У 50% больных сыпь встречается на туловище, у 20% - на голове, у 15% - на руках, и у 15% - на ногах (Arani R.B. et al., 2001).
Клинический диагноз опоясывающего лишая в типичных случаях достаточно прост. Однако иногда требуется проведение лабораторной диагностики с целью идентификации вируса. Наиболее быстрым и высокочувствительным методом является полимеразная цепная реакция.
В остром периоде болезни или после него возможно развитие осложнений, захватывающих различные системы организма. Наиболее серьезными считаются неврологические осложнения. В структуре неврологических расстройств ведущее место занимает поражение периферической нервной системы. При данном заболевании воспалительный процесс затрагивает региональные, чувствительные ганглии с развитием ганглиолитов. Наличие у больных корешковых болей, парастезий, сегментарных нарушений чувствительности отмечается практически у каждого больного (Stankus S. et al., 2000; Thyregod H. G. et al., 2007). Болевой синдром имеет выраженную вегетативную окраску в виде жгучих, приступообразных, резких болей, усиливающихся в ночное время. В головном мозге при опоясывающем герпесе могут быть обнаружены явления отека, выраженная диффузная инфильтрация подпаутинного пространства, геморрагии в белом веществе, базальных ганглиях (Sissoko D. et al., 1998). Следует заметить, что осложнения со стороны головного и спинного мозга в настоящее время встречаются редко. В случаях развития VZV-инфекции в области тройничного нерва часто наблюдаются осложнения со стороны глаз - кератит, ирит, ретинит, офтальмит. Ранее, при отсутствии специфической противогерпетической терапии, к частым осложнениям VZV-инфекции относились пневмонии, энцефалиты или гепатиты, иногда приводившие к летальному исходу.
Вместе с тем, из всех перечисленных осложнений VZV инфекции самым распространенным считается постгерпетическая невралгия (Dworkin R.H., Portenoy R.K., 1996).
Различают острую герпетическую невралгию (в течение 30 дней после начала заболевания) и постгерпетическую невралгию (Choo P. et al.,1997). К ПГН относят упорные боли в областях, затронутых герпесной инфекцией после заживления кожи (Dworkin R. et al. 2003). Наиболее хорошо установленными факторами риска для ПГН являются пожилой возраст, большая распространенность высыпаний на коже и выраженная боль перед везикулярной сыпью (Desmond R.A. et al., 2002; Fleming D.M. et al., 2004). Все эти факторы находятся во взаимосвязи, поэтому пациенты 50 лет и старше в большинстве случаев испытывают тяжелую, нестерпимую боль и значительные кожные высыпания, что гораздо чаще приводит к развитию ПГН. У пациентов со всеми этими факторами риск развития ПГН превышает 50-75 % (Gnann J., Whitley R. 2002; Jung B.F., 2004). Постгерпетическая невралгия может развиться в любом возрасте, однако для нее характерна прямая корреляция частоты встречаемости и длительности ПГН с возрастом. Более 50% всех пациентов с ПГН - старше 60 лет, 75% больных с указанной патологией приходится на возрастную группу старше 75 лет (Nurmikko T.J., 2001). Половина всех пациентов с ПГН старше 60 лет испытывает постоянную боль более 6 месяцев, в то время как в возрастной группе 30-50 лет ПГН более 6 месяцевь наблюдается у 10% больных (Whitley R. et al. 1996). В США ежегодно регистрируется 100-200 тыс. новых случаев ПГН (Nurmikko T.J., 2001). Однако, истинная распространенность ПГН не известна, не только потому, что эпидемиологические данные недостаточны, но также из-за отсутствия конценсусса по определению ПГН. Некоторые авторы относят к ПГН боли, возникающие в любой период герпесной инфекции, другие считают, что ПГН - это боль, сохраняющаяся спустя 3 месяца после заживления кожи. В первом случае определения ПГН ее распространенность составляет 8%, во втором - 4,5% (Choo P. et al. 1997). Постоянную боль в течение 1 мес после сыпи испытывают до 15% пациентов и около 4% пациентов от общего количества перенесших опоясывающий лишай отмечают сохранение боли в течение года (Lancaster T. et al. 1995).
Классическое проспективное исследование, проведенное Hope-Simpson (1975), продемонстрировало, что из 321 пациента с опоясывающим лишаем 10 % имеют выраженную боль спустя 3 месяца после острой герпетической инфекции, а 4 % - и через 12 месяцев. Подобные результаты были получены и в других проспективных исследованиях (Helgason S. et al. 1996; 2000; Scott F.T. et al., 2006), в которых также было показано, что наибольший риск пролонгации болевого синдрома после перенесенного опоясывающего лишая имеют пациенты в возрасте около 60 лет.
Постгерпетическая невралгия занимает третье место по частоте встречаемости среди различных типов невропатической боли и уступает только болям в нижней части спины и диабетической невропатии (Montero H.J. et al., 2005; Breivik H. et al, 2006; Torrance N. et al., 2006).
Локализация болевого синдрома практически всегда соответствует зоне кожных высыпаний. Интенсивность болевого синдрома как правило высокая. Кроме глубоких ноющих и стреляющих болей очень характерны поверхностные жгучие боли и наличие стимулозависимых болей - динамической гипералгезии и аллодинии (Baron R., 2004).
При клиническом осмотре в зоне болей выявляются нарушения поверхностной чувствительности. Качество боли в острый период опоясывающего лишая и при ПГН различно. Вместе с тем, несмотря на разный выбор дескрипторов из МакГилловского болевого вопросника, пациенты с опоясывающим лишаем и ПГН для описания своих болевых ощущений выбирают похожие по смыслу слова, например, горячая и жгучая боль или пронзающая и простреливающая боль (Bennett M., 2001).
Схожие проявления наблюдаются и при описании вызванной боли пациентами с опоясывающим лишаем и ПГН. И те, и другие отмечают наличие схожих типов гипералгезии и аллодинии (Haanpaa M. et al., 2000; Berry J.D., Rowbotham M.C., 2004).
У большинства пациентов боль, связанная с ПГН, уменьшается в течение первого года. Однако у части больных она может сохраняться годами и даже в течение всей оставшейся жизни, причиняя немалые страдания (Cunningham A.L., Dworkin R.H., 2000). Затяжной, тяжелый характер заболевания с длительным, выраженным болевым синдромом способствует формированию расстройств психики (Dworkin R.H., et al., 1992). У таких пациентов выявляются тревожно-депрессивные расстройства, когнитивные нарушения - снижение активного внимания, памяти, затруднения осмысления происходящего, отмечается некритичность, нетерпеливость, неряшливость, страх боли, неуверенность в завтрашнем дне, отмечается снижение социальной активности (Haythornthwaite J.A. et al., 2003). ПГН оказывает значительное отрицательное влияние на качество жизни и функциональный статус пациентов особенно пожилого возраста (Lydick E. et al., 1995). У пациентов с ПГН отмечается хроническая усталость, снижение массы тела, физической активности, нарушения сна (Morin C.M., Gibson D., Wade J., 1998).
В основе боли, связанной с ПГН, лежат воспалительные изменения или повреждения ганглиев задних корешков спинного мозга и периферических нервов в пораженных зонах тела. Такие боли относят к невропатическим болям, их выделяют в отдельную самостоятельную группу и определяют как боли, возникающие вследствие первичного повреждения соматосенсорной нервной системы (Treede R.D. et al., 2008).
Патофизиологической основой невропатических болевых синдромов являются нарушения генерации и проведения ноцицептивного сигнала в нервных волокнах, а также механизмов контроля возбудимости ноцицептивных нейронов в структурах спинного и головного мозга (Кукушкин М.Л., Хитров Н.К., 2004; Baron R. 2000).
Лечебная тактика при опоясывающем лишае включает два основных направления: противовирусная терапия и купирование невропатической боли, как в острый период заболевания, так и в стадии постгерпетической невралгии. Результаты нескольких рандомизированных контролируемых испытаний свидетельствуют о том, что раннее начало лечения простого герпеса может предотвратить развитие постгерпетической невралгии или способствовать ее скорейшему разрешению (Исаков В.А. и др., 2004; Helgason S. et al., 1996; Jackson J.L. et al., 1997 ; Volmink J. et al., 1996).
Наиболее широкое применение нашли такие специфические противогерпетические препараты, как ацикловир, фамцикловир и валацикловир, которые, являясь нуклеозидными аналогами, блокируют вирусную репликацию (Романцев М.Г., 1996; Beutner K. et al., 1995; Bruxelle J., 1995). Важно, что противовирусное лечение проявляет наивысшую активность, если назначено в течение 72 ч от начала герпетических высыпаний (Johnson R., 2001; Johnson R., Dworkin R.H., 2003). В ряде исследований доказана высокая эффективность ацикловира в уменьшении тяжести, продолжительности острой герпесной инфекции и профилактике ПГН, особенно при его раннем назначении. Оценка эффективности фамцикловира также продемонстрировала уменьшение времени до разрешения сыпи (Dworkin R.H. et al., 1998). В сравнительном исследовании ацикловира и валацикловира показана эквивалентная эффективность в сокращении продолжительности невропатической ПГН (Beutner K. et al. 1995). В другом клиническом испытании установлена терапевтическая эквивалентность фамцикловира и валацикловира для неосложненного герпеса (Tyring S. et al. 2000). Возможно также сочетанное использование противовирусной терапии и глюкокортикостероидов (Whitley R. et al. 1999). Выявлено, что такая комбинация эффективнее монотерапии противовирусными препаратами, особенно для лечения острой боли и коррекции различных аспектов качества жизни пациентов. Комбинация ацикловир+преднизолон значительно быстрее купирует острую невралгию и возвращает пациента к обычной жизнедеятельности, но существенно не влияет на течение ПГН, то есть она наиболее показана в остром периоде в старших возрастных группах для терапии острого болевого синдрома. Доказано, что хотя преднизолон является иммуносупрессором, его использование не увеличивает частоты развития ПГН и в этом смысле его действие сравнимо с влиянием плацебо, то есть данная комбинация может быть спокойно использована в старших возрастных группах. Для некупируемых тяжелых случаев ПГН некоторые исследователи рекомендуют интратекальное введение метилпреднизолона (Kost R., Straus S., 1996).
В настоящее время в США делается акцент на профилактику герпетической инфекции. С 1995 г. в США проводится всеобщая вакцинация от ветряной оспы, особенно пожилых лиц, и с 1999 г. отмечается резкое снижение заболеваемости (Hambleton S., Gershon A., 2005; Oxman M.N. et al., 2005).
При постгерпетической невралгии препаратами с доказанной эффективностью (класс А - терапия первой линии) являются: пластины с 5% лидокаином, габапентин, прегабалин, трициклические антидепрессанты, трамадол (Attal et al., 2006).
На сегодняшний день эффективность применения пластин с 5% лидокаином (Версатис, Grunenthal Gmbh) убедительно доказана при лечении ПГН. Так, в нескольких рандомизированных клинических исследованиях установлено, что применение пластин с 5% лидокаином статистически достоверно более значимо облегчает проявления болевого синдрома у пациентов с постгерпетической невралгией по сравнению с плацебо (Rowbotham M.C., 1996; Galer B.S., 1999, 2002). На основании полученных данных FDA одобрило применение данного препарата в качестве стартовой терапии у пациентов с постгерпетической невралгией. (Richard L. et al., 2004)
Версатис - это топический анальгетик, который действует непосредственно там, где болит. Он выпускается в виде мягких пластин размером 10х14 см, которые наклеиваются на неповрежденную кожу без признаков воспаления. Медленно высвобождающийся из пластины лидокаин создает более или менее значительную концентрацию лишь в поверхностных слоях кожи, где проходят тонкие волокна, обеспечивающие болевую и температурную чувствительность (Gammaitoni AR, Davis MW. 2002.). Лидокаин лишь в незначительной степени проникает в более глубокие слои кожи, где проходят кровеносные сосуды, поэтому его попадание в системный кровоток сведено к минимуму. У пациентов, использовавших пластины Версатис, не наблюдалось никаких известных системных эффектов лидокаина (влияние на деятельность ЦНС и сердечно-сосудистой системы). Таким образом, важнейшим преимуществом пластин Версатис служит отсутствие системного действия, что гарантирует безопасность лечения. Практически полное отсутствие системного эффекта позволяет назначать Версатис совместно с любыми другими препаратами для лечения нейропатической боли.
Механизм лечебного эффекта препарата Версатис не ограничивается только действием высвобождающегося из них лидокаина. Важное значение имеет также то, что пластина выполняет роль механического барьера, препятствуя раздражению участка кожи с измененной чувствительностью (аллодиния), а также оказывает не него легкое охлаждающее действие (Galer BS, Gammaitoni AR, Oleka N et al., 2004)
Пластины Версатис рекомендуется прикреплять на 12 ч в течение суток, затем следует 12-часовой перерыв. Обезболивающий эффект часто начинается в течение 30 мин после прикрепления пластины, но может проявляться и позже, нарастает в течение 4 ч и затем поддерживается в течение длительного времени, пока пластина прикреплена к коже. Более того, он может сохраняться и после ее удаления.
Для объективной оценки эффективности каждого из препаратов при лечении ПГН используется показатель NNT (number needed to treat - количество больных, которых нужно пролечить, чтобы получить у одного 50% снижение боли). Чем ниже NNT, тем более эффективен препарат при данной патологии. NNT для пластин с 5% лидокаином при лечении пациентов с ПГН составляет 2,0; для амитриптилина - 2,6; габапентина - 4,4; прегабалина - 4,6 (Wu C.L., Raja S.N., 2008); для трамадола - 3,9 (Kalso E., 2006).
Кроме того, в клинической практике очень важен показатель NNH (number needed to harm - число пациентов, которых необходимо пролечить данным препаратом, чтобы получить развитие 1 случая неблагоприятной побочной реакции, приводящей к отмене препарата). Он показывает, насколько безопасен данный препарат при его использовании. Величина NNH для трамадола, рассчитанная по результатам нескольких клинических исследований, составила 9.0, для ТЦА 14.7, для габапентина 26.1. Рассчитать показатель NNH для пластин с 5% лидокаином не представляется возможным в связи благоприятным профилем безопасности препарата, сравнимым с плацебо.
Таким образом, оценка препарата Версатис с позиций доказательной медицины делает его препаратом выбора при лечении постгерпетической невралгии, что подтверждено в соответствующих рекомендациях.
СПИСОК ЛИТЕРАТУРЫ

Часто, даже легкий тычок или кратковременное переохлаждение, приводят к развитию неврита плечевого сустава. Другими словами – воспаляются нервные волокна, следствием чего становится сдавливание, защемление стволов. Медики применяют термин “плексит плеча”.
Причина в том, что плечевой сустав создан природой с большим диапазоном движений. И рядом с ним располагается плечевое сплетение – узел нервных волокон, от которого отходят нервы руки. Из-за особенностей расположения, сплетение крайне уязвимо к воздействию извне.
Главным симптомом патологии становится сильная боль и дискомфорт, распространяющиеся по всем областям, куда идут веточки от этого нервного пучка. То есть – как на руку, так и на часть спины, ухудшая самочувствие больного человека, ограничивая его трудоспособность.
Попытки самостоятельного лечения или просто прием обезболивающего без обращения к врачу, создают риск усугубления болезни.
Сначала боль станет постоянной, привычные средства перестанут на нее влиять.
Затем постепенно разовьется паралич руки, лишив человека возможности пользоваться конечностью. Такое тяжелое осложнение возникает из-за гибели нервных волокон.
Восстановление утраченных функций руки, в запущенных случаях, весьма затруднено или невозможно.
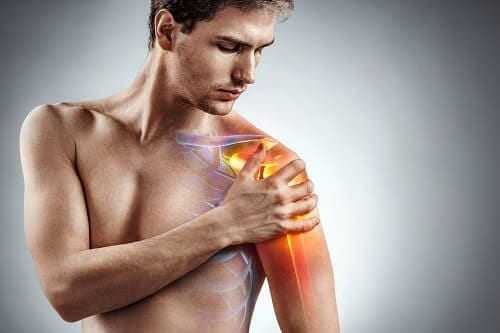
Причины
Невропатия плечевого сустава – распространенное явление в жизни человека, какой бы образ жизни мы бы не вели. Спровоцировать патологию, неврит любой локализации, могут как чрезмерные физические нагрузки, так и их отсутствие. Как и неправильный прием отдельных лекарств и другие факторы.
Типичными причинами для симптомов неврита плеча, требующих немедленного лечения, являются:
- травмы сустава или костей ключицы;
- бактериальные или вирусные инфекции мягких тканей этой области;
- пережатие волокон и сосудов из-за неправильно наложенного гипса или жгута;
- остеохондроз шейного отдела позвоночника;
- растяжение связок (манжеты плечевого сустава), приводящее к воспалению, отеку и сжатию нервных окончаний;
- опухоли различного типа, образующиеся около шеи, в подмышках, на плече;

- переохлаждение, застуживание;
- чрезмерные регулярные физические нагрузки, связанные с работой или спортивными тренировками;
- нарушения кровообращения в сосудах, питающих сустав и кости плечевой области;
- некомпенсированный сахарный диабет.
Частой причиной плексита плеча становится застуживание. Получить его возможно не только в сырую или холодную погоду, наиболее часто проблемы начинаются именно в теплое время года из-за неудачного расположения рядом с кондиционером, на сквозняке или слишком долгом пребывании в холодной воде.
В диагностике, выявление первопричины плексита крайне важно. Так как без устранения источника проблемы, ожидаются регулярные рецидивы. Встречается и трансформация в хроническое течение воспаление.
Симптомы
Даже при нерегулярных, периодически возникающих неприятных ощущениях в области плеча или руки, нужно обратиться для проверки к неврологу. Сами собой, боли, коль уж возникли, не уйдут, а со временем только усилятся.
Лечение неврита нерва плечевого сустава начинается при симптомах и признаках следующего типа:
- Ноющая боль в плече, усиливающаяся при движениях. В периоде покоя может проходить, возвращаясь после физической нагрузки или воздействия холода на пораженный участок.
- Снижается чувствительность кожи плеча и соседствующих областей.
- Периодически возникают неприятные покалывания без причины в плече-лопаточной области, коже руки.
- Чувство онемения кожи и руки при отсутствии движений ею в течение 30 минут, пары часов.
- Возникновение отека в месте локализации болевых ощущений.
- Снижение или полная утрата мышечного тонуса. Рука кажется свисающей, недвижимой.

Проблемы с двигательной способностью означают, что откладывать визит к врачу нельзя! Сначала появляются легкие нарушения, затем они нарастают, в итоге способность двигать рукой прекращается!
Если не обратиться к доктору при появлении первых симптомов, то со временем деградация нервных волокон приводит к параличу плечевого сустава, руки. Устранить такое нарушение, даже оперативным путем, бывает невозможно. То есть пациент на всю дальнейшую жизнь останется инвалидом.
Диагностика
В первую очередь, при первичном осмотре, невролог устанавливает степень поражения нервной ткани. С помощью специальных тестов определяются тонус мышц, подвижность руки. Уточняют болезненность движений, когда пациент сам двигает рукой или, когда это делает за него врач.
Собирают анамнез, чтобы первично определить возможную причину состояния. Затем больного направляют на сдачу анализов и аппаратные исследования, которые смогут подтвердить предположения доктора, показать, в каком состоянии находятся нервные корешки.
Пациенту необходимо пройти такие лабораторные и инструментальные обследования:
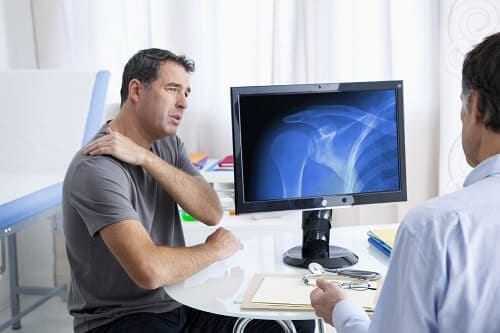
- анализы крови и мочи для выявления возможных системных заболеваний;
- рентгенографию плеча в разных ракурсах, что покажет наличие травм, смещение костей, новообразования, способные влиять на узел нервной ткани;
- электромиографию – исследование функции нервных волокон, насколько сохранена их проводимость и способность передавать мышцам сигналы;
-
;
- МРТ, при необходимости, помогает выявить микротравмы или патологические изменения структуры костей и мягких тканей.
После получения результатов исследований возможна постановка точного диагноза с указанием первопричины подобного состояния.
Лечение
При симптомах воспаления плечевого нерва назначают лечение исходя из результатов обследования и особенностей организма пациента.
Пускать плексит на самотек, заниматься самолечением с применением обезболивающего или народных методов, при подобном воспалении нельзя. Это может усугубить двигательные и чувствительные нарушения, сделает их необратимыми.
Список рекомендуемых медикаментов, физиопроцедур и методик рефлексотерапии, составляется для отдельного больного. Применяются следующие группы лекарств:
- нестероидные противовоспалительные препараты;
- обезболивающие, анальгетики внутрь и в виде мазей;
- мочегонные для уменьшения отека;
- обезболивающие блокады (инъекции в очаг) при длительном лечении;
- препараты для улучшения питания нервных волокон;
- стимулирующие кровообращение лекарства;
- антибиотики в случае инфекций;
- витамины группы B.
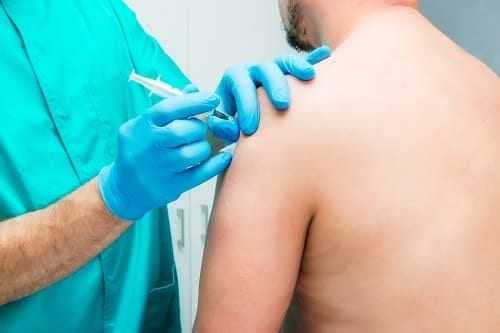
На весь курс рекомендуется покой для руки и фиксация конечности в удобном положении с помощью лонгеты.
При травматическом происхождении заболевания или в случае наличия опухоли применяется оперативное вмешательство.
В период восстановления, нейрореабилитации, для постепенной разработки руки и возвращения трудоспособности, организовывают курсы физиотерапии. Занятия ЛФК проводят под руководством тренера, который научит выполнять все движения правильно, так, чтобы не ухудшить состояние.
Постгерпетическая невралгия – это осложнение опоясывающего лишая, заболевания, которое вызывает вирус ветряной оспы. Во время инфекции на ограниченном участке кожи, соответствующем пораженному нерву, возникает покалывание, спустя некоторое время появляется болезненная сыпь с пузырьками.


Когда на месте пузырьков образуется корочка, и они заживают, возникает жгучая боль, которая может сохраняться в течение длительного времени (в течение нескольких лет, месяцев или всю жизнь).
Против постгерпетической невралгии не существует эффективного лечения. Врачи-неврологи могут лишь назначить препараты, которые помогут управлять болевым синдромом.
Постгерпетическая невралгия в цифрах и фактах:
- Согласно американской статистике, постгерпетическая невралгия возникает у 10-18% людей, перенесших опоясывающий лишай.
- После перенесенного опоясывающего лишая у людей младше 60 лет это осложнение развивается менее чем в 10% случаев.
- После 60 лет риски сильно повышаются, и эта цифра поднимается до 40%.
Симптомы герпетической невралгии
Нарушения возникают на ограниченном участке тела, как правило, с одной стороны, там, где проходит пораженный вирусом нервный ствол. Для заболевания характерно сочетание трех признаков:
- Боль. Может быть жгучей, колющей, ноющей. Как правило, сохраняется 3 месяца и дольше после выздоровления от опоясывающего лишая.
- Аллодиния. Это сложное слово обозначает состояние, когда боль возникает от воздействий, которые у здоровых людей к ней не приводят. При герпетической невралгии болевые ощущения могут возникать от легких прикосновений к коже, одежде.
- Зуд и чувство онемения. Более редкие симптомы.
Заболевание не представляет большой опасности, но из-за постоянных болей со временем человек начинает испытывать повышенную утомляемость, депрессию, у него снижается аппетит, он не может нормально выспаться.
Для того чтобы предотвратить осложнение, нужно обращаться к врачу при первых признаках герпеса. Чем раньше заболевший человек начал принимать противовирусные средства, тем ниже риск того, что в будущем его будут беспокоить боли.
Чаще всего врач устанавливает диагноз после осмотра пациента. Дополнительные исследования и анализы не нужны.
Лечение постгерпетической невралгии
Для борьбы с болевыми ощущениями используют разные средства. Не все они одинаково хорошо помогают разным пациентам. Задача врача – подобрать препарат или их сочетание, которое сможет эффективно держать болезнь под контролем у конкретного пациента.
Чаще всего используют следующие средства:
- Лидокаин – наносят местно на пораженный участок кожи.
- Нестероидные противовоспалительные средства, например, парацетамол, аспирин.
- Опиоидные (наркотические) анальгетики – более мощные обезболивающие, также обладают успокоительным эффектом.
- Противосудорожные препараты. Некоторые лекарства из этой группы, например, прегабалин и габапентин, помогают лечить боли при постгерпетической невралгии.
- Антидепрессанты. Эти препараты оказывают влияние на головной мозг и изменяют восприятие боли. Их назначают в меньших дозах, чем при депрессии.
Иногда медикаментозное лечение дополняют альтернативными методами, такими как иглорефлексотерапия, разные практики релаксации.
Причина герпетической инфекции - 8 вирусов, два вируса простого герпеса, а ещё Эпштейна-Барра и цитомегаловирус, опоясывающего лишая и безымянные под номерами. Вирус простого герпеса 1 типа вызывает поражение кожи красной каймы губ, 2 типа – слизистую гениталий, но в жизни строгой локализации нет, и генитальный вирус живёт на губах и лабиальный – на половых органах.


Какие вирусы становятся причиной возникновения разных видов герпеса?
Какие виды герпеса возникают у взрослых?
Инфекционный агент легко сосуществует с родственниками, так почти все переболевшие ветряной оспой имеют возбудителей 1 и 2 типа. Если заражение произошло одновременно, то это коинфекция, если последовательно – суперинфекция.
И это типичные виды герпетической инфекции, потому что атипичными считаются проявления с менее или более выраженными симптомами.
Какое лечение герпеса показано взрослым?
На первом этапе во время обострения необходимы специфические противовирусные препараты, их несколько групп и разные формы, требуется индивидуальный подбор. Обязательно стараются уменьшить тягостные проявления и предотвратить осложнения и вторичное бактериальное инфицирование.
На втором этапе проводится иммунотерапия и пренебрегать ею не стоит, поскольку рецидивы – обычное для дело для этой разноликой инфекции.
Насколько заразен герпес?
В международной клинике Медика24 не только в кратчайший срок и с минимальными затратами установят правильный диагноз, но и проведут оптимальное лечение по мировым клиническим стандартам.
Позаботьтесь о себе, запишитесь на консультацию сейчас
Какие симптомы при герпесе у взрослых?
- Первый признак заболевания - локальный отёк кожи или слизистой, до этого может появиться в этом месте зуд и жжение, эта стадия держится несколько часов.
- Постепенно на фоне покраснения начинается рост крохотных пузырьков, наполняющихся желтоватым секретом.
- Пузырьки легко травмируются, лопаются и на их месте расползается эрозия - как будто ободрана кожа, боль интенсивная, но терпимая.
- Эрозии покрываются серым налётом, из которого образуются коричневые корочки, они стягивают кожу, часто лопаются и кровоточат. Полное излечение наступает через 3 – 7 дней.
- На стороне поражения может прощупываться увеличенный и болезненный лимфатический узел.
- При обильных высыпаниях может развиться общая реакция организма: умеренное повышение температуры, ломота в мышцах и суставах, головная боль.
Всё течение довольно болезненно, и не только в месте кожного поражения, но при генитальном герпесе боли с онемением могут распространяться на внутреннюю поверхность бедра, пах и ягодичную область. Пузырьки на слизистой мочеиспускательного канала вызывают жгучую боль при каждом мочеиспускании.
Вылечить герпетическую инфекцию невозможно, но между рецидивами могут проходить годы, вирусоноситель заразен. Наши врачи-инфекционисты центра инфекционных заболеваний подскажут, что нужно делать, чтобы не стать источником проблем для других людей, помогут облегчить проявления заболевания и предотвратить рецидивы.
Всегда ли необходимо делать анализы на вирус герпеса? В большинстве случаев для диагностики опытному врачу достаточно наблюдать клинические проявления. Симптоматика герпеса довольно типична:
- Появление неврологической боли до кожных поражений;
- Цикличность кожных изменений от зудящего пятнышка, через растущий пузырек с постепенно мутнеющим содержимым, до корочки;
- Развитие общей интоксикации на фоне кожных высыпаний;
- Неоднократное возникновение похожих изменений в течение жизни;
- Более или менее типичная локализация на губах и половых органах, крыльях носа и в межреберных промежутках;
- При опоясывающем герпесе патологические изменения располагаются полосой и только на одной половине.
В международной клинике Медика24 в кратчайший срок проведут обследование и поставят правильный диагноз, что повысит эффективность лечения и сократит период реабилитации.
Наши врачи вам помогут
Когда крайне необходимо сделать анализ на вирус?
Во всех случаях, когда есть сомнения, что это симптомы именно герпетической инфекции, то есть для выявления истинной причины и дифференциальной диагностики герпеса от других патологических состояний. Лабораторная диагностика проводится:
- Больным герпесом беременным и их супругам или половым партнерам, потому что без адекватного лечения герпетической инфекции на раннем сроке может произойти выкидыш или сформироваться уродства, а при заболевании во второй половине ребенок может родиться с тяжелой врожденной инфекцией.
- ВИЧ-инфицированным и пациентам с приобретенным на фоне хронического заболевания дефицитом иммунной защиты поможет установить причину инфекции.
- При тяжело протекающей инфекции с нетипичными проявлениями, когда поражаются внутренние органы или практически весь организм – генерализованный герпес, и возможны сомнения в правильности диагноза или вообще неясно, какая это болезнь.
- При появлении симптомов поражения центральной нервной системы для принятия срочных терапевтических мер.
- При лечении бесплодия, потому что герпес у мужчин вызывает нарушение сперматогенеза.
Какая диагностика при герпесе необходима?
Существуют несколько тестов, позволяющих определить сам вирус и вырабатываемые на него антитела разных типов в биологических жидкостях человека: в крови, слюне, выделениях из половых и мочевыводящих путей, в кожном дефекте. Стандартными являются такие тесты, как ИФА – иммуноферментный анализ определение наличия вирусной ДНК в крови при ПЦР – полимеразной цепной реакции.
Мы вам перезвоним
Как клинически проявляются рецидивы?
Характерно, что рецидивы протекают мягче первичного эпизода. Для развития кожного поражения бывает достаточно стресса, высыпания как саморегулируемая организация: где хотят, там и появляются, когда сочтут нужным, тогда и вылезут.
При рецидивах чаще отмечается атипичное течение. К примеру, болезнь как будто замирает на стадии отёка и покраснения кожи, сопровождаясь зудом или лёгким жжением, но пузырьков не образуется. Продолжительность таких проявлений короче.
Какие опасности несёт заболевание?
Кожные симптомы довольно болезненно, но хуже то, что герпетическая инфекция селится в нервной ткани, пересиживая там между рецидивами, при обострении вызывая невриты лицевого и затылочного нервов, седалищного и тройничного. Эти страдания могут тянуться неделями, выводя вирусоносителя из строя.
И самое опасное проявление: способность на раннем сроке беременности вызывать самопроизвольные аборты, не исключают, что вирус ответственен за каждый 2-3 выкидыш.
Специалисты центра Международная клиника Медика24 при комплексном обследовании выявляют факторы риска и объективные причины, которые могут привести к развитию непрерывно рецидивирующего заболевания, что позволяет начать профилактические мероприятия.
Лечить надо кожные проявления герпетической инфекции и симптомы невритов, ни один из препаратов: ацикловир, ганцикловир, валацикловир, фамцикловир – не имеет клинических преимуществ, но все высокоэффективны. Лечение способствует существенному сокращению продолжительности заболевания и уменьшает клинические проявления.
При постоянном приёме таблеток в течение нескольких месяцев можно избежать рецидива, программу лечения способен составить только высококвалифицированный специалист.
Читайте также:

