Грипп и другие орви в практике участкового терапевта
Обновлено: 24.04.2024
ВОЗ — Всемирная организация здравоохранения
СО — слизистая оболочка
ОРВИ — острые респираторные вирусные инфекции
Острые респираторные вирусные инфекции (ОРВИ) — наиболее распространенная патология, на долю которой приходится около 90% всех инфекционных болезней. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно заболевает каждый третий житель планеты [1—4].
В Российской Федерации ежегодно болеют ОРВИ и гриппом более 30 млн человек, а суммарный экономический ущерб от респираторных вирусных инфекций оценивается в 40 млрд руб. в год. Большие экономические потери обусловлены вовлечением в эпидемический процесс трудоспособного населения, развитием осложнений, особенно в раннем детском и старческом возрасте, непродолжительным нестойким иммунитетом, определяющим повторные случаи заболевания [4—8].
Вирусы, вызывающие респираторные инфекции, не являются эндемичными для какого-либо региона или страны и распространены повсеместно. Чаще эпидемии возникают в зимнее время, однако вспышки наблюдаются и в осенне-весенний период, а спорадические случаи ОРВИ — круглый год. Известно около 300 возбудителей респираторных инфекций, более 200 из них представители 4 семейств РНК-содержащих вирусов (ортомиксовирусы, парамиксовирусы, коронавирусы и пикорнавирусы) и 2 семейств ДНК-содержащих вирусов (аденовирусы и герпесвирусы) [4].
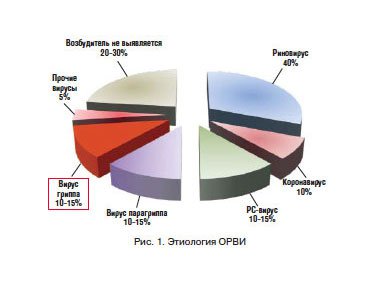
По данным различных эпидемиологических исследований, лидирующие позиции в этиологическом рейтинге занимают вирусы парагриппа, риновирусы и возбудители микстинфекции; при этом частота инфицирования вирусами гриппа составляет 5—15%.
Локализация очага поражения во многом зависит от вида возбудителя. Однако клиническая дифференциация ОРВИ часто затруднена из-за схожей симптоматики, в связи с чем этиологический фактор без применения методов лабораторной диагностики часто остается неустановленным. ОРВИ и грипп занимают значительное место в практике врачей первого контакта (участковых терапевтов, врачей общей практики, педиатров и т. д.). Чаще всего подобный диагноз ставится на основании совокупности клинико-эпидемиологических данных. Для клинической диагностики большое значение имеет эпидемиологическая ситуация в регионе. Подтверждение диагноза ОРВИ лабораторными методами проводится в эпидемических очагах и в стационарах при лечении тяжелых форм течения болезни [9—11].
Характерной особенностью гриппа является острое начало с повышением температуры тела, которая в течение нескольких часов может достигать 39—40 °С и выше. Лихорадка при неосложненном гриппе продолжается от 2 до 5 дней, затем температура тела снижается ускоренным лизисом. Основной ведущий признак интоксикации — головная боль, преимущественно в лобной части. Кроме того, пациенты часто отмечают общее недомогание и слабость, мышечные и суставные боли. В тяжелых случаях отмечается адинамия, головокружение, обморочные состояния, нарушения сознания; у детей возможны судорожный синдром и явления менингизма.
При парагриппозной инфекции виремия малоинтенсивна, поэтому интоксикация выражена слабо и непродолжительна. Взрослые переносят болезнь легко, лихорадка выражена незначительно. У детей часто развивается ларингит, при этом в результате отека СО гортани может развиться синдром ложного крупа. Основными клинико-дифференциальными признаками при парагриппе служат поражение дыхательных путей, насморк с набуханием СО носа, затруднение носового дыхания, развитие ларингита, умеренные признаки поражения гортани с болью в горле, упорным, чаще сухим кашлем, иногда грубым и напоминающим лающий при крупе у детей. Часто меняется тембр голоса, появляется охриплость вплоть до афонии. Кроме стеноза гортани частым осложнением у них является пневмония.
В клинической картине риновирусной инфекции ведущим симптомом является ринорея. Наблюдаются также сухость, першение и боль в горле, кашель.
Отличительной особенностью коронавирусной инфекции является высокий удельный вес смешанных форм инфекции. Коронавирусная инфекция может также протекать по типу гастроэнтерита.
При аденовирусной инфекции воспалительный процесс наиболее часто локализуется во входных воротах на СО верхних дыхательных путей и конъюнктиве. Размножение вируса в дальнейшем может происходить в ткани кишечника, лимфатических узлах. Это обусловливает широкий диапазон клинических проявлений, в том числе нехарактерных для большинства ОРВИ, таких как лимфаденопатия, диарея, гепатоспленомегалия.
К основным клинико-дифференциальным признакам при аденовирусной инфекции относится экссудативный характер поражения дыхательных путей, который проявляется набуханием, отечностью СО полости глотки и носа. Ринит протекает с обильным серозно-слизистым отделяемым, значительным затруднением дыхания (из-за выраженной заложенности носовых ходов). В процесс постоянно вовлекается задняя стенка глотки и миндалины. Фарингит характеризуется гиперплазией лимфоидных образований. Миндалины увеличены, отечны, может быть обострение хронического тонзиллита в виде лакунарной и фолликулярной ангины. Конъюнктивит — катаральный, фолликулярный, пленчатый, чаще односторонний.
Клиническую картину респираторных заболеваний могут вызывать вирусы Коксаки В, реовирусы, цитомегаловирусы, микоплазмы и большое число бактериальных агентов.
Среди осложнений выделяют ларингит, тонзиллит, фарингит и трахеит бактериальной природы, различные формы синуситов (гайморит, этмоидит, фронтит), отит, евстахиит. Возможно также развитие бронхита и пневмонии.
Для профилактики и лечения гриппа в настоящее время используются специфические вакцины и противогриппозные химиопрепараты, однако для борьбы с другими многочисленными видами респираторных вирусов средств специфической защиты и этиотропной терапии не существует. Поэтому заболеваемость ОРВИ среди вакцинированных лиц против гриппа в осенне-зимний период остается высокой.
Многообразие возбудителей ОРВИ делает практически невозможным организацию масштабных профилактических мероприятий, аналогичных проводимым в отношении вируса гриппа [12, 13]. В связи с этим во всем мире возрастает интерес медицинских работников к неспецифическим средствам профилактики гриппа и ОРВИ. Экспертами ВОЗ подчеркивается важность выполнения простых и доступных общегигиенических рекомендаций, таких как проветривание помещений, полноценное питание, прием витаминно-минеральных комплексов, закаливание, мытье рук, использование индивидуальных марлевых масок при общении с больными людьми, ограничение посещения мест большого скопления народа в периоды эпидемии и др. [12—14].
В предэпидемический период на первый план выступает весь комплекс санитарно-оздоровительных мероприя-тий (что особенно актуально для групп повышенного риска), включающий использование наряду со средствами специфической профилактики (вакцинации против гриппа) многочисленных средств, повышающих естественную резистентность организма, например иммуномодуляторов, адаптогенов, поливитаминов и др. [2, 14, 15].
В настоящее время для профилактики и терапии ОРВИ и гриппа активно используются препараты интерферона [16, 17]. Широкий спектр действия данной группы лекарственных средств обусловлен универсальным противовирусным эффектом интерферона — активацией синтеза специфических внутриклеточных ферментов, нарушающих размножение вирусов. Кроме того, интерферон стимулирует экспрессию антигенов I и II классов главного комплекса гистосовместимости. В результате изменяется топография цитомембран, что препятствует прикреплению вирусов к клеточной оболочке и нарушает их проникновение внутрь клеток. Активизируя цитотоксическую активность Т-лимфоцитов, интерфероны также стимулируют лизис клеток, инфицированных вирусами. Таким образом, они не только препятствуют вирусному инфицированию, но и подавляют репродукцию вирусов на стадии синтеза специфических белков.
Среди препаратов интерферона выделяют природные интерфероны первого поколения (интерферон человеческий лейкоцитарный) и рекомбинантные, полученные генно-инженерным способом. С конца 50-х годов прошлого века в клинической практике применялся только лейкоцитарный интерферон, полученный в культуре клеток человека. Однако его использование даже при самых совершенных системах контроля не может со 100% вероятностью гарантировать отсутствие в полученном препарате вирусов иммунодефицита человека, гепатита, А и В и др. В настоящее время, согласно рекомендациям ВОЗ, лекарственные средства, содержащие лейкоцитарные интерфероны, применяются только по жизненным показаниям. Отличительной же особенностью рекомбинантных интерферонов является то, что они получены вне организма человека (продуцируются бактерией Escherichia coli, в ДНК которой встроен ген интерферона человека), что сводит к нулю вероятность передачи какой-либо инфекции от донора.
Среди эффективных и безопасных лекарственных средств для лечения и профилактики гриппа и ОРВИ выделяют отечественный препарат Гриппферон (содержащий интерферон человеческий рекомбинантный альфа-2b), обладающий выраженной активностью в отношении большинства респираторных вирусов. Препарат выпускается в виде назальных капель и дозированного назального спрея и может быть использован как средство профилактики (в том числе экстренной) гриппа и ОРВИ в детских и других организованных коллективах [18—27], а также в группах риска развития данных заболеваний (у медицинских и фармацевтических работников, обслуживающего персонала общественных учреждений, транспорта и т. д.) [17, 28—31].
С целью экстренной профилактики ОРВИ и гриппа препарат Гриппферониспользуется следующим образом: при контакте с больным и/или при переохлаждении препарат закапывают (капли) или впрыскивают (спрей) в разовой возрастной дозировке 2 раза в день; при сезонном повышении заболеваемости применяют в возрастной дозировке однократно утром с интервалом 24—48 ч. При необходимости профилактические курсы повторяют.
В различных работах показан выраженный профилактический эффект Гриппферона при использовании в период сезонного повышения заболеваемости гриппом и ОРВИ; так, применение препарата в организованных коллективах обеспечивало снижение заболеваемости в 2,4—3,5 раза [16, 17, 29].
Большой опыт применения Гриппферона показал также высокую эффективность при лечении гриппа и ОРВИ у всех возрастных групп, в том числе у детей 1-го года жизни [21, 24—26, 29—32]. Препарат может быть использован у пациентов с сопутствующими фоновыми заболеваниями, лиц, страдающих хроническими инфекциями, а также теми или иными вариантами аллергозов, независимо от состояния их иммунного статуса [16, 17, 28—31]. Гриппферон при первых признаках заболевания применяют в течение 5 дней в возрастной дозировке. Так, пациентам старше 15 лет и взрослым рекомендуется принимать препарат по 3 капли/дозы в каждый носовой ход 5—6 раз в день (разовая доза при этом составляет 3000 ME, суточная доза — 15 000—18 000 ME).
Гриппферон является приоритетным средством для лечения и профилактики гриппа и других ОРВИ у беременных в любом гестационном периоде, поскольку не вызывает побочных эффектов, в том числе эмбриотоксических и тератогенных [29, 30, 33, 34]. В суточной дозе 15 000—18 000 ME в течение 2 нед препарат существенно снижает заболеваемость беременных в очаге пандемии и обусловливает более благоприятное течение инфекционного процесса [33], значительно уменьшая вероятность развития тяжелых осложненных форм гриппа у беременных [34].
Такие симптомы ОРВИ, как отек СО, заложенность носа, ринорея, в одинаковой степени характерны и для аллергического ринита. Они развиваются под влиянием медиаторов воспаления, среди которых одним из наиболее важных является гистамин. При ОРВИ инфекционные агенты атакуют клетки СО дыхательных путей, что собственно и приводит к развитию воспалительного процесса [35, 36].
Комбинированный оригинальный препарат, содержащий интерферон человеческий рекомбинантный альфа-2b и лоратадин (препарат Аллергоферон), зарекомендовал себя в качестве эффективного и безопасного лекарственного средства для лечения аллергических заболеваний, в том числе в офтальмологической практике [40—42].
Нами оценены эффективность и безопасность Гриппферона с лоратадином в профилактике ОРВИ и гриппа в период эпидемического подъема заболевае-мости.
Материалы и методы
Во время первого визита (в сентябре 2015 г.) собирали анамнез, включавший данные о средней частоте ОРВИ/гриппа в течение 3 предшествующих лет, длительности заболеваний и их симптомов, а также о наличии сопутствующих аллергических заболеваний (вазомоторный ринит, поллиноз, крапивница) и пищевой аллергии.
Пациентов проинформировали о возможности использования изучаемого препарата в эпидемический (осенне-зимний) период с целью профилактики и лечения ОРВИ и гриппа. Были выданы соответствующие рекомендации по применению препарата: в профилактических целях после контакта с заболевшим препарат используют однократно утром, для лечения — 5 раз в день. Мазь наносят на СО носа, выпустив по 1 см в каждый носовой ход. В обоих случаях курс применения составлял 7 дней. Кроме того, во время первого визита даны рекомендации по заполнению карты наблюдения, в которой пациенты в течение эпидемического периода фиксировали частоту профилактического использования изучаемого препарата, частоту заболевания ОРВИ или гриппом, длительность и степень тяжести ОРВИ (продолжительность температуры, интоксикационного синдрома, катаральных симптомов, насморка). Пациенток проинформировали, что не проводилось исследований по безопасности препарата Гриппферон с лоратадином у беременных, поэтому при возникновении беременности рекомендовали использовать назальные капли или спрей Гриппферон, разрешенные к применению в течение всего периода гестации.
Результаты
По средней частоте случаев заболевания ОРВИ/гриппом в предшествующие 3 года пациентов разделили на 2 группы: 1-я — 68 человек, у которых отмечено 1—2 случая ОРВИ/гриппа, 2-я — 35 человек с 3 и более эпизодами ОРВИ/гриппа в осенне-зимний период. На профилактическое использование назальной мази Гриппферон с лоратадином указали все пациенты, однако в соответствии с рекомендациями 7-дневный курс профилактики проводили только 34 (33%) пациента, остальные не соблюдали предписания: 33 (32%) пациента применяли препарат в течение 5 дней, еще 25 (24,3%) — в течение 3 дней. Оставшиеся 11 (10,7%) пациентов применяли мазь не более 1—2 дней.
Во 2-й группе среднее число случаев ОРВИ/гриппа в предшествующие годы составило 3,69±0,29, за период наблюдения при использовании назальной мази Гриппферон с лоратадином 2,49±0,22 дня; (р<0,05). На отсутствие эпизодов заболевания указали 2 человека, проходившие 7-дневный курс профилактики. Средняя частота применения назальной мази Гриппферон с лоратадином в этой группе составила 6,57±0,42.
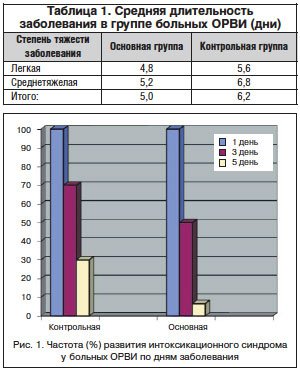
Длительность и степень тяжести ОРВИ (продолжительность периода с повышенной температурой тела, интоксикационного синдрома, катаральных симптомов, насморка) сравнивали у 80 пациентов (имевших случаи заболевания в течение наблюдения) по данным анамнеза за предыдущий год и по данным карт наблюдения в текущем эпидемическом сезоне. Длительность эпизода ОРВИ/гриппа на фоне применения Гриппферона с лоратадином (в составе комплексной терапии) составила 5,05±0,34 дней и была достоверно ниже чем в предшествующем сезоне (6,92±0,39; р<0,05). Продолжительность клинических симптомов представлена в табл. 1. Обращает внимание позитивная динамика показателей основных симптомов ОРВИ и гриппа, свидетельствующая о сокращении продолжительности лихорадки, интоксикации и катаральных явлений в области носо- и ротоглотки при использовании изучаемого препарата.

Таблица 1. Продолжительность клинических симптомов при ОРВИ/гриппе на фоне применения назальной мази Гриппферон с лоратадином Примечание. Здесь и в табл. 2: данные представлены в виде М±m. *— р
Среди 103 пациентов, включенных в исследование, у 31 имелся отягощенный аллергологический анамнез. По частоте эпизодов ОРВИ и гриппа пациентов разделили на 2 группы: в 1-ю группу вошли 12 человек, во 2-ю — 19. Результаты эффективности применения у этих пациентов назальной мази Гриппферон с лоратадином непосредственно для профилактики и лечения ОРВИ/гриппа представлены в табл. 2. По итогам проведенного исследования на отсутствие эпизодов заболевания указали 6 пациентов, проводившие 7-дневный курс профилактики. При этом средняя частота профилактического применения назальной мази Гриппферон с лоратадином пациентами с отягощенным анамнезом в течение эпидемического сезона составила 6,77±0,38.

Таблица 2. Эффективность применения назальной мази Гриппферон с лоратадином для профилактики и лечения ОРВИ/гриппа у пациентов с отягощенным аллергологическим анамнезом
В процессе лечения не отмечено выраженных нежелательных явлений. В единичных случаях пациенты отмечали кратковременный зуд в месте нанесения мази, самостоятельно проходящий в течение нескольких минут, а также чихание.
Заключение
Таким образом, результаты исследования позволяют рассматривать отечественный комбинированный лекарственный препарат Гриппферон с лоратадином, мазь назальная, в качестве эффективного и безопасного препарата для профилактики и лечения ОРВИ и гриппа в составе комплексной терапии у взрослых, в том числе у пациентов с отягощенным аллергологическим анамнезом.
Многолетний опыт применения Гриппферона (в виде капель назальных и спрея) свидетельствует об эффективности и безопасности препарата при использовании у новорожденных, детей и взрослых пациентов, включая беременных, при лечении и профилактике ОРВИ и гриппа. Появление новой формы — назальной мази Гриппферон с лоратадином — в соответствии с результатами нашего наблюдения и исследования С.Е. Ушаковой и соавт. [43] расширяет профилактические и терапевтические возможности участковых терапевтов и врачей общей практики при ОРВИ и гриппе у взрослых пациентов, особенно с аллергическим ринитом.
Острые респираторные вирусные заболевания являются самыми распространенными заболеваниями во всем мире. На их долю приходится большая часть общей заболеваемости. При этом не все врачи общей практики одинаково оценивают значимость проблемы борьбы с респираторными инфекциями. В отличие от педиатров, для которых проблема профилактики и лечения ОРВИ является одной из первоочередных, терапевты более редко оценивают данные вопросы, как остро стоящие в своей практике. Отчасти, это связано с тем, что в отличие от хронических заболеваний и бактериальных инфекций, ОРВИ характеризуются в целом более легким течением. Кроме того, в виду низкой санитарной культуры, характерной даже для мегаполисов, представители взрослого населения намного более склонны к самолечению развившихся ОРВИ, и практически не настроены на проведение профилактических мероприятий. Поэтому для терапевтов проблема лечения и профилактики респираторных вирусных инфекций в целом не является столь актуальной.
Однако, есть категории пациентов, которые особо привлекают внимание терапевтической службы в отношении заболеваемости ОРВИ. И прежде всего к ним следует отнести пациентов, страдающих хроническими сердечно-сосудистыми и бронхолегочными заболеваниями, у которых ОРВИ и грипп могут приводить к развитию осложнений, а нередко и к летальным исходам.
Обусловленное вирусными возбудителями снижение иммунологической резистентности, глубокое подавление функциональной активности различных звеньев иммунной системы приводят к обострению многих хронических заболеваний, а также к возникновению вторичных бактериальных осложнений (Ершов Ф.И. и соавт.) (1).
С другой стороны, хроническая патология ведущих систем жизнеобеспечения формирует серьезные изменения в деятельности системы противоинфекционной защиты, что приводит к снижению резистентности к различным инфекционным агентам.
Так, у пациентов с атеросклерозом в возрасте 40–46 лет выявляются снижение содержания в крови гуморального тимического фактора, количества Т-лимфоцитов, особенно функционально активной субпопуляции, количества Т-супрессоров, что в итоге приводит к извращению регуляторного индекса и нарушению иммунного ответа. Отмечено, что у пациентов с ИБС и высоким коронарным риском снижена фагоцитарная способность клеток. При сочетании атеросклероза с гипертонической болезнью отмечаются признаки еще более глубокого угнетения функций иммунной системы.
У больных с хроническими заболеваниями легких и бронхов наблюдается выраженное расстройство местного иммунитета, характер которого зависит от вида заболевания. Например, при бронхиальной астме существенно снижается уровень секреторного IgA. У больных с хроническим бронхитом с гнойной легочной инфекцией наблюдается ослабление функции альвеолярных макрофагов, уменьшение количества лимфоцитов, увеличение количества нейтрофилов в бронхоальвеолярном секрете, что совпадает со снижением бактерицидной активности этих клеток. К системным иммунным реакциям при бронхолегочной патологии следует отнести супрессию Т-зависимых иммунных реакций по количественным и качественным критериям. У больных также формируется дисиммуноглобулинемия. Поглотительная и метаболическая активность фагоцитов нередко оказывается подавленной. При хроническом бронхите выявляется снижение уровня общих Т-лимфоцитов, дефицит содержания IgM и IgA, уменьшение количества В-клеток. Бронхиальная астма характеризуется снижением содержания Т- и В-лимфоцитов, недостаточностью Т-хелперов 1 типа, что характеризуется снижением выработки ИФН-γ. При формировании кортикозависимости данные изменения достигают предельных величин (Земсков А.М. и соавт., Куделя Л.М. и соавт.) (2, 10, 11).
Следует отметить, что довольно часто традиционное лечение кортикостероидами, антибиотиками и сульфаниламидами широкого спектра действия, антигистаминными препаратами и особенно их комбинацией не исправляет, а усугубляет иммунную недостаточность (Земсков А.М.) (1).
С другой стороны, респираторные вирусные заболевания сами оказывают существенное негативное влияние на течение сердечно-сосудистой патологии и бронхолегочных заболеваний (Лусс Л.В. и соавт., Куделя Л.М. и соат.) (10, 11, 12).
У пациентов с ИБС на фоне гриппа и других ОРВИ отмечаются нарушения микроциркуляции и гемореологии, особенно сильно проявляющиеся к периоду реконвалесценции. Данные изменения объясняют развитие обострений ИБС, а также провоцируют развитие инфарктов миокарда уже после перенесенной вирусной инфекции. Группами риска по развитию являются больные с ангинозными болями, изменениями конечной части желудочкового комплекса на ЭКГ, нарушениями ритма и проводимости и особенно больные с постинфарктным кардиосклерозом (Богомолов Б.П. и соавт.) (3). Известно, что у больных с гипертонической болезнью в острый период гриппа чаще возникают гипертонические кризы, острые нарушения мозгового кровообращения (Малый В.П. и соавт.) (4).
Отсроченная летальность у пациентов с кардиопатологией после перенесенных ОРВИ зачастую не рассматривается как следствие респираторной инфекции и не связывается с методами лечения ОРВИ у данной категории больных. Следствием этого является недооценивание истинных исходов ОРВИ, а также тактики лечения каждого конкретного пациента.
Согласно литературным данным, около 20-30% обострений хронических обструктивных болезней легких и бронхиальной астмой вызваны острыми респираторными вирусными инфекциями (Ершов Ф.И. и соавт., Хаитов Р.М. и соавт., W.W. Busse, P.J. Sterk) (13, 14, 15, 16).
Все выше перечисленное, определяет необходимость внедрения в клиническую практику лекарственных средств, активирующих неспецифические факторы противовирусной защиты организма, и в первую очередь систему интерферонов, которой принадлежит ключевая роль в противовирусной защите (Л.В. Лусс и соавт.) (12).
Принципам ведения пациентов с отягощенным анамнезом был посвящен симпозиум, проходивший в рамках III-го Национального Конгресса терапевтов, проходившего в г. Москве с 5 по 7 ноября 2008 г.
Председатель симпозиума д.м.н. Хитров Н.А., открывая симпозиум, сказал, что количество пациентов с хроническими заболеваниями неуклонно растет. Это требует соответствующего подхода к выбору лечебной тактики и профилактических мероприятий с учетом тех нарушений, которые имеются у пациентов с отягощенным анамнезом.
Анаферон обладает разносторонним действием на иммунную систему, оказывая влияние на все механизмы противоинфекционной защиты. Механизм действия Анаферона заключается в воздействии на систему эндогенных интерферонов (ИФН). За счет комплексного влияния на выработку разных пулов интерферонов (ИФН-α и ИФН-γ) Анаферон обладает двойным действием. Повышая выработку ИФН-α Анаферон проявляет противовирусную активность широкого спектра, а за счет воздействия на выработку ИФН-γ – оказывает модулирующее воздействие на иммунный ответ (5–9). При этом препарат способствует повышению функциональной активности макрофагов и NK-клеток (цитотоксические лимфоциты), которые лизируют уже зараженные клетки. Действующим веществом Анаферона являются сверхмалые дозы антител к гамма-интерферону (ИФН-γ) человека. Технология производства препарата обеспечивает его высокую фармакологическую активность при сверхнизком содержании действующего вещества, что обеспечивает его выдающийся профиль безопасности.
Доцентом кафедры инфекционных болезней Уральской государственной медицинской академии д.м.н. Веревщиковым В.К. были доложены результаты, проведенного на кафедре, открытого сравнительного рандомизированного исследования по изучению клинической эффективности Анаферона для лечения ОРВИ у пациентов с отягощенным кардиологическим анамнезом.
Под наблюдением находилось 55 пациентов, поступивших в клинику инфекционных болезней с диагнозом ОРЗ.
У всех пациентов имелись в анамнезе хронические сердечно-сосудистые заболевания: ишемическая болезнь сердца, гипертоническая болезнь, стенокардия, постинфарктный кардиосклероз.
Методом рандомизации было сформировано 2 группы: основная (n=30) и группа сравнения (n=25). Пациенты основной группы в дополнение к дезинтоксикационной, симптоматической, патогенетической терапии получали Анаферон по лечебной схеме с первого дня госпитализации.
Эффективность применения Анаферона оценивалась по данным клинико-лабораторных и инструментальных исследований, с обязательной оценкой иммунологических параметров и ЭКГ-мониторингом.
По данным исследования было отмечено, что применение Анаферона в комплексной терапии ОРЗ у пациентов с хроническими заболеваниями сердечно-сосудистой системы способствовало сокращению продолжительности периода лихорадки в 1,4 раза, интоксикации – в 2 раза, сокращало продолжительность катаральных явлений и сухого кашля в 1,6 раза, что способствовало сокращению пребывания пациентов в стационаре.
Исследование иммунного статуса пациентов показало, что стимулированная продукция ИФН-α и ИФН-γ в период реконвалесценции была в 1,9 раз выше в группе, получавшей Анаферон.
Исследование в динамике показателей ЭКГ у пациентов, получавших Анаферон, не выявило существенных изменений, за исключением синусовой тахикардии, которая коррелировала с выявляемой в этот период гипертермией. Тогда как в группе сравнения в период разгара заболевания отмечались усугубление признаков ишемии миокарда.
Важно отметить, что в результате включения Анаферона в схему лечения ОРВИ у пациентов, страдающих сердечно-сосудистой патологией, сократилась продолжительность пребывания в стационаре. В основной группе средняя продолжительность пребывания в отделении составила 6,4 ± 1,1 дня, в группе сравнения этот показатель был выше и составил 8,6 ± 0,8 дня, а у пациентов с бактериальными осложнениями сроки пребывания в стационаре увеличивались еще на 3–5 дней в связи с проведением антибактериальной терапии.
Профилактике ОРВИ и гриппа у больных с бронхолегочной патологией был посвящен доклад доцента кафедры факультетской терапии Казанского государственного медицинского университета, д.м.н. Копылова А.Н. На кафедре было проведено открытое, сравнительное, рандомизированное исследование по изучению профилактической эффективности Анаферона по отношению к ОРВИ у больных с бронхолегочной патологией. В исследование были включены 89 пациентов в возрасте от 18 до 69 лет с хроническими заболеваниями бронхолегочной системы (бронхиальная астма, хронический бронхит, ХОБЛ).
Благодаря проведению рандомизации пациенты были разделены на две группы, сопоставимые по тяжести и хронической патологии. Основная группа (n=57) получала Анаферон по 1 таблетке в день на протяжении 3 месяцев.
В контрольной группе (n=32) неспецифическая профилактика ОРВИ не проводилась. Пациенты обеих групп также получали препараты для лечения основного заболевания. В ходе исследования было отмечено, что в группе, получавшей Анаферон в течение периода наблюдения (90 дней) в 3 раза сократилось число случаев ОРВИ (рРис. 1. Структура заболеваемости ОРВИ в группах
* – различия между аналогичными показателями в группах статистически значимы, р
В группе, получавшей Анаферон, течение ОРВИ было более легким, также отмечено сокращение продолжительности симптомов интоксикации, уменьшение на 3 дня периода гипертермии, снижение интенсивности и длительности катаральных явлений.
Докладчик подчеркнул, что на фоне профилактического приема Анаферона увеличивается временной интервал между эпизодами ОРВИ, а также сокращается количество обострений бронхолегочной патологии (табл. 1), что согласуется с данными других авторов (Куделя Л.М. и соавт.) (10, 11).
Таблица 1. Характеристика заболеваемости ОРВИ в группах.
| Параметр | Основная группа (n=57) | Контрольная группа (n=32) | p (T Стьюдента, для долей – Х2) |
| Среднее количество ОРВИ | 0,32 ± 0,08 | 1,13 ± 0,14 | 0,000005 |
| Средняя продолжительность одного ОРВИ (сутки) | 6,8 ± 0,99 | 6,83 ± 0,7 | 0,98 |
| Доля ОРВИ с гипертермией % (абс.) | 33,3 (6) | 67 (24) | 0,0215 |
Подводя итоги, важно отметить, что назначение Анаферона пациентам, страдающим хронической сердечнососудистой и бронхолегочной патологией, способствует сокращению заболеваемости ОРВИ и гриппом, снижает продолжительность и выраженность острой вирусной респираторной патологии, уменьшает количество бактериальных осложнений. И что очень актуально: предупреждает развитие обострения хронической патологии на фоне простудных заболеваний у пациентов из групп риска, а также улучшает показатели иммунитета.
Таким образом, можно сделать вывод о целесообразности применения Анаферона в комплексной терапии ОРВИ и гриппа у данной категории больных. Учитывая положительное комплексное влияние на все звенья иммунного ответа Анаферон рекомендован для включения в программы профилактики простудных заболеваний у пожилых пациентов и пациентов из групп риска.
Для цитирования: Колбасников С.В., Медведева С.О. Эффективность комбинированной терапии острых респираторных вирусных инфекций у взрослых в амбулаторной практике. РМЖ. Медицинское обозрение. 2015;23(4):236.
Острые респираторные вирусные инфекции (ОРВИ) – группа вирусных заболеваний верхних дыхательных путей, которые относятся к числу самых распространенных болезней человека и составляют половину от общего числа острых заболеваний [1, 2]. В целом на одного взрослого человека приходится 3–4 случая заболевания в год. При этом доля острых респираторных заболеваний составляет 30–40% среди болезней, приводящих к потерям рабочего времени среди взрослого населения, и 60–80% – среди болезней, приводящих к потерям учебного времени среди детей школьного возраста [3, 4].
Коварство ОРВИ состоит не только в снижении качества жизни, возникновении временной утраты трудоспособности, увеличении потребления лекарств в период заболевания, но и в развитии осложнений и обострении хронических неинфекционных заболеваний [6]. Актуальность проблемы ОРВИ обусловлена значительной распространенностью и высокой вероятностью осложненного течения, а также быстрым формированием на этом фоне бактериально-ассоциированных заболеваний верхних дыхательных путей [5]. В связи с этим требуется изучение новых подходов к комплексному лечению ОРВИ на уровне первичного звена здравоохранения.
К достоинствам ингаляционного метода терапии относятся: безопасность и удобство применения, что позволяет использовать его пациентами всех возрастов; максимально физиологичное введение вещества – вместе с вдыхаемым воздухом; прямое действие на слизистую оболочку органов дыхания; купирование застойных и воспалительных реакций; смягчающее действие микрочастиц масел на слизистые оболочки; возможность избежать мацерации кожных покровов и раздражения слизистой, которое развивается при длительном применении лекарственных средств в полости носа [8].
Целями данного исследования явились оценка эффективности и безопасности масла Дыши в комбинированной терапии больных ОРВИ трудоспособного возраста и анализ целесообразности его назначения в амбулаторной практике по сравнению с традиционной терапией.
Материал и методы исследования
В открытое сравнительное исследование были включены 120 больных в возрасте 18–59 лет с различными нозологическими формами острых инфекционных воспалительных заболеваний дыхательных путей, не принимавших масло Дыши по меньшей мере за 14 дней до включения, не имевших критериев исключения и подписавших информированное согласие.
Критерии включения: установленный диагноз ОРВИ или гриппа согласно клиническим, диагностическим критериям; наличие интоксикации, катаральных явлений со стороны верхних дыхательных путей в период не более чем 48 ч от начала заболевания; течение респираторного заболевания легкой или средней степени тяжести; отсутствие тяжелой сопутствующей терапевтической и прочей патологии, признаков бактериальной инфекции верхних и нижних дыхательных путей или другой локализации, требующей назначения антибиотиков.
Критерии исключения: тяжелое или гипертоксическое течение ОРВИ или гриппа, сроки заболевания более 48 ч от появления симптомов заболевания; индивидуальная непереносимость компонентов масла Дыши; наличие клинически значимых аллергических реакций в анамнезе, острого тонзиллита любой степени выраженности, физикальных изменений в бронхах и легких во время отбора больных; тяжелых клинически значимых неврологических, эндокринологических, сердечно-сосудистых, желудочно-кишечных, печеночных, почечных заболеваний в анамнезе; иммуносупрессивные больные, получающие гормоны, цитостатики, иммуносупрессоры; алкоголизм, наркомания, токсикомания.
Обследуемые были разделены на 2 группы (по 60 человек в каждой) так, чтобы они были репрезентативны по удельному весу различных клинических форм ОРВИ, степеням тяжести, полу, возрасту. Контрольная группа получала только стандартную терапию ОРВИ, включающую противовирусные, жаропонижающие препараты, при необходимости – антигистаминные средства и антиоксиданты. В рамках исследования при наличии сопутствующих заболеваний применялись лекарства, не принадлежащие к числу не разрешенных к использованию в ходе исследования. Основная группа в дополнение к стандартной терапии получала в течение 5 дней масло Дыши: 2–3 капли наносились на салфетку или любую тканевую поверхность и помещались рядом с обследованным для вдыхания аромата. Масло наносилось на салфетку каждые 3–4 ч. Состав композиции масло Дыши: масло мятное (Оleum mеnthае) – 35,45%, масло эвкалиптовое (Oleum eucalypti) – 35,45%, масло каепутовое (Oleum cajuputi) – 18,5%, левоментол (Levomenthol) – 4,1%, масло винтергриновое (Oleum wintergreen) – 3,7%, масло можжевеловое (Oleum juniperi) – 2,7%, масло гвоздичное (Oleum caryophylli) – 0,1%. Деконгестанты и другие препараты эфирных масел не использовались.
Мониторинг больных осуществлялся на протяжении 7 дней (период активной терапии изучаемым препаратом – 5 дней), в течение которых предусматривалось 4 визита пациента к врачу. При 1-м визите проводился сбор данных анамнеза заболевания, в т. ч. эпидемиологического, сбор жалоб, а также осуществлялись объективный осмотр и проба на переносимость препарата. На 2-м и 3-м визитах (соответственно на 3-й и 5-й дни лечения) врачом проводились стандартный опрос и осмотр по протоколу, оценивалось выполнение пациентом всех предписаний и режима применения препаратов. Визит 3 (5-й день лечения) был окончательным для пациентов с легкой степенью тяжести ОРВИ и гриппа, а для пациентов со среднетяжелым течением в случае нетрудоспособности был предусмотрен визит 4 (на 7-е сут болезни). На каждом этапе исследования врачом обязательно уточнялась индивидуальная переносимость препарата.
Критерии клинической эффективности применения масла Дыши: динамика клинической картины (выраженность симптомов интоксикационного и катарального синдромов по системе баллов и их продолжительность), продолжительность острого периода (лихорадки), длительность заболевания, количество дней временной нетрудоспособности, отсутствие осложнений ОРВИ.
Динамика основных симптомов интоксикационного и катарального синдромов оценивалась во время всех визитов.
Оценка клинических симптомов проводилась по 4-балльной шкале:
0 – нет симптома;
1 – слабая выраженность симптома;
2 – умеренная выраженность симптома;
3 – сильная выраженность симптома.
Помимо этого, по 4-балльной шкале оценивались температура тела и общее самочувствие пациента (общая слабость).
Результаты исследования

Таким образом, при добавлении к терапии ОРВИ масла Дыши уменьшаются выраженность и длительность интоксикационного и катарального синдромов, что приводит к сокращению сроков временной нетрудоспособности на 1,2 сут и уменьшению экономических затрат на терапию респираторных инфекций. Следует отметить, что при применении масла Дыши осложнений ОРВИ ни у одного больного не наблюдалось, в то время как в контрольной группе течение ОРВИ осложнилось отитом у 2 обследованных.
Выводы
1. Добавление масла Дыши к стандартной терапии респираторных инфекций позволяет:
– устранить интоксикационный синдром у 93,4% пациентов на 5-й день применения препарата (в контрольной группе синдром устранен у 70% пациентов);
– устранить катаральный синдром у 90% пациентов на 5-й день применения препарата (в контрольной группе синдром устранен у 70% больных).
2. Применение масла Дыши в комплексной терапии респираторных инфекций сокращает продолжительность клинических проявлений заболевания: лихорадки – на 30%, головной боли – на 42,9%, ринита – на 29,6%, катаральных явлений – на 27,1%, общей слабости – на 18,4% (по сравнению с больными, не применявшими масло Дыши в комплексной терапии ОРВИ).
3. Применение масла Дыши в комплексной терапии респираторных инфекций сокращает длительность заболевания на 19,4% и, следовательно, уменьшает экономические затраты на терапию респираторных инфекций.
4. Отмечаются хорошая переносимость масла Дыши и отсутствие побочных эффектов при его применении.
5. При применении масла Дыши в комплексной терапии ОРВИ снижается вероятность возникновения осложнений.
6. Рекомендуется шире использовать масло Дыши в практике участкового врача-терапевта, врача общей практики в комплексной терапии респираторных инфекций, в т. ч. для профилактики осложнений.
Для цитирования: Усенко Д.В., Горелова Е.А., Каннер Е.В. Рациональный подход к терапии ОРВИ и гриппа в клинической практике врача-педиатра. РМЖ. 2015;3:174.
ОРВИ по заболеваемости и распространенности занимают лидирующие позиции среди всех инфекций у взрослых и детей, являются самым частым поводом для обращения к врачу и в аптечные учреждения, самолечения.
Согласно официальной статистике, в России ежегодно регистрируют до 30–60 млн и более случаев ОРВИ, более половины из них — у детей. Заболеваемость ОРВИ не имеет тенденции к снижению, растет во всех возрастных группах, несмотря на значительные успехи фармакологии и фармакотерапии [1, 2]. Ситуация осложняется еще и тем, что в последнее время врачам все чаще приходится иметь дело с ее осложненными вариантами — . Таким образом, вопросы эффективной терапии и профилактики ОРВИ не теряют своей актуальности.
Ежегодно, по данным ВОЗ, дети в среднем переносят от 5 до 8 острых заболеваний верхних дыхательных путей, большей частью легкого течения [3]. Столь частые заболевания респираторного тракта объясняются многообразием этиологических факторов и высокой контагиозностью респираторных вирусов [4].
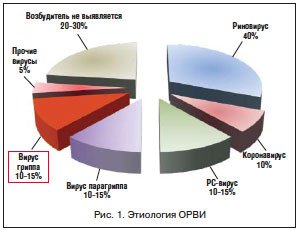
ОРЗ включают в себя инфекции, вызываемые как вирусами, в основном респираторными, так и пневмотропными бактериями, нередко вегетирующими в дыхательных путях [5]. Общее число вирусов и их серотипов, вызывающих ОРЗ, достигает 200, и на их долю приходится 95% всех случаев поражений дыхательных путей у детей. Вирусами гриппа вызываются только 10–15% заболеваний (рис. 1).
Вирусные инфекции нередко осложняются бактериальной инфекцией, обостряют течение хронических заболеваний, представляют серьезную угрозу здоровью ребенка [6, 7]. У 70–80% детей, особенно младшего возраста, в воспалительный процесс вовлекаются : околоносовые пазухи, среднее ухо, трахея, бронхи, следствием чего могут быть поражения глазной орбиты и мозговых оболочек. Поэтому начинать рациональное лечение необходимо уже в первые часы заболевания [8–10].
Ежегодная высокая заболеваемость острыми респираторными инфекциями и гриппом, риск осложнений, постоянно меняющаяся мозаика возбудителей, а также наносимый этими инфекциями экономический и социальный ущерб делают разработку и внедрение в практику эффективных способов профилактики гриппа и острых респираторных инфекций приоритетными задачами современной медицины [2, 11, 12].
Несомненно, наиболее эффективной является специфическая профилактика, применяемая в отношении вирусов гриппа. Доказано, что своевременно проведенная вакцинация способна защитить от гриппа до 80% взрослых и детей [11, 13–15]. Разработка специфических вакцин против всего спектра возбудителей ОРВИ нецелесообразна огромного многообразия серотипов респираторных вирусов и их ежегодно изменяющегося соотношения в структуре заболеваемости на разных континентах, в различных странах и городах. Осложняет ситуацию наблюдающаяся в последние годы резистентность ряда респираторных вирусов к химиопрепаратам, одной из причин которой является нерациональная фармакотерапия [16].
Помимо того, практическим врачам известно, что в ряде случаев существуют объективные причины, не позволяющие достичь оптимального соотношения вакцинированных людей в популяции, что снижает индекс защищенности от вируса гриппа [8, 15, 17]:
- абсолютные и относительные противопоказания к назначению вакцин (коморбидные заболевания, аллергия к белковым компонентам вакцин, обострение хронических воспалительных процессов, неоплазии и др.);
- запаздывание производства необходимого количества вакцинных препаратов к началу эпидсезона;
- появление новых типов и серотипов вирусов;
- немотивированный отказ взрослых людей и родителей детей от проведения вакцинации.
- Поэтому вполне понятен и обоснован интерес медиков различных стран к неспецифическим средствам профилактики гриппа и ОРВИ.
Экспертами ВОЗ подчеркивается важность выполнения простых и доступных общегигиенических рекомендаций: проветривание помещений, полноценное питание, прием комплексов, закаливание, мытье рук, использование масок при общении с больными, ограничение посещения мест большого скопления людей в периоды эпидемии и др. [11–13, 18].
Таким образом, поиск и внедрение лекарственных средств для профилактики и лечения ОРВИ продолжаются и относятся к числу приоритетных задач клинической педиатрии. Выбор рациональной фармакотерапии различных ОРВИ, в первую очередь гриппа, а также оптимальной схемы и длительности лечения — актуальная проблема медицины на протяжении многих десятилетий и постоянная тема для дискуссий в медицинском сообществе.
Спектр лекарственных средств, применяемых пациентами для лечения и профилактики гриппа и ОРВИ как по рекомендации врача, так и самостоятельно, весьма разнообразен. Но какие из этих лекарств действительно приносят пользу?
На сегодняшний день не вызывает сомнения целесообразность раннего применения при гриппе этиотропной противовирусной терапии, особенно при наличии риска развития осложнений. Это единственная группа препаратов, рекомендации по применению которых при гриппе основаны на результатах международных рандомизированных контролируемых клинических исследований. К ним относятся рекомендуемые ВОЗ препараты осельтамивир и занамивир. Эти препараты продемонстрировали высокую эффективность при начале лечения в первые 48 ч заболевания. Однако в реальной практике пациент обращается к врачу только на 3–4 сут, когда характер и тяжесть симптомов не оставляют сомнений в том, что он болен гриппом. Для профилактики гриппа в связи с высокой частотой развития резистентности ВОЗ не рекомендует применять осельтамивир. Поэтому ключевым показанием к назначению осельтамивира является грипп, верифицированный в первые 2 сут от начала заболевания, особенно у пациентов из группы риска.
Грипп и другие ОРВИ часто являются поводом для полипрагмазии и нерационального использования лекарственных средств. Для облегчения симптомов заболевания родители по рекомендации врача или самостоятельно прибегают к применению симптоматических препаратов, например, жаропонижающих, обезболивающих, муколитических, противоотечных, сосудосуживающих назальных капель Результаты клинических испытаний показали, что их использование в ряде случаев может облегчить течение заболевания, но не оказывает существенного влияния на его исходы [20–23]. Клиническая эффективность адаптогенов, общеукрепляющих средств, традиционно популярных среди населения, не доказана, и применение их при ОРВИ нецелесообразно.
Данные Кокрейновских систематических обзоров и клинических руководств говорят о том, что антибиотики, также часто применяемые при ОРВИ, не только не улучшают исходы заболевания, но и могут привести к таким неблагоприятным последствиям, как удлинение сроков выздоровления, повышение частоты нежелательных лекарственных реакций и рост антибиотикорезистентности [20, 24, 25].
Данные клинических и фармакоэпидемиологических исследований убедительно показали нецелесообразность применения антигистаминных препаратов, которые также не только не улучшают исходы ОРВИ, но и достаточно часто приводят к нежелательным лекарственным реакциям [21].
Число лекарств, предлагаемых для лечения и профилактики ОРВИ и гриппа, с каждым годом увеличивается. Проблемами противовирусной терапии являются снижение эффективности лечения при позднем начале приема препарата, возрастные ограничения, узкая специфичность и снижение эффективности ряда лекарственных средств за счет роста резистентности, отсутствие устойчивой доказательной базы по целому ряду препаратов, токсичность большинства препаратов, низкая комплаентность. Кроме того, при назначении индукторов интерферона необходимо учитывать, что концентрация интерферонов в сыворотке крови у больных ОРВИ в разгар заболевания существенно повышается, сам вирус является мощным интерфероногеном, а дополнительная искусственная стимуляция выработки интерферонов чревата срывом компенсаторных возможностей иммунной системы организма.
В этом аспекте определенный интерес вызывают гомеопатические этиотропные лекарственные средства для лечения респираторных вирусных инфекций, которые практически не имеют противопоказаний и возрастных ограничений, лишены побочных эффектов и могут использоваться в комплексе с другими препаратами [26]. Несомненным достоинством гомеопатических средств является возможность их длительного приема на фоне терапии сопутствующей патологии.
Развитие данного метода лечения обусловило отход от традиции отказа от использования параллельно аллопатических препаратов и создание комплексных гомеопатических лекарств. Эти препараты являются безрецептурными, их могут применять врачи любых специальностей, не владеющие основами гомеопатии. Различные формы таких препаратов — таблетки, гранулы, сиропы, мази — не вызывают сложностей в определении дозировки и сроков лечения и широко используются во всех возрастных группах без ограничения, и в период эпидемических подъемов ОРВИ, особенно гриппа [27, 28].
Эффективность Оциллококцинума в лечении гриппа и ОРВИ известна на протяжении более полувека. Препарат продается в более чем 50 странах, особенно он популярен во Франции, где производится около 70 лет и является самым продаваемым в стране безрецептурным средством против гриппа. В США объемы продажи лекарства достигают 15 млн долларов в год. В России Оциллококцинум рекомендован в качестве лекарственного средства для профилактики и лечения гриппа и вирусных респираторных заболеваний [30–34]. Показания к применению определены как грипп и простудные заболевания, противопоказанием является только повышенная индивидуальная чувствительность к отдельным компонентам препарата.
Оциллококцинум рекомендовано принимать за 15 мин до приема пищи или через 1 ч после него, средство необходимо держать во рту до полного растворения. В начальной стадии заболевания следует как можно раньше принять 1 дозу препарата, затем при необходимости повторить 2–3 раза с интервалом 6 ч. В более поздние сроки рекомендован прием по 1 дозе утром и вечером в течение 1–3 дней. Желательно начинать лечение как можно раньше, при появлении первых проявлений простуды, в этом случае использование препарата наиболее эффективно. При нарастании симптомов в течение суток на фоне использования Оциллококцинума и при значительно выраженной интоксикации следует обратиться к врачу. Препарат может быть использован пациентами любого возраста, беременными и кормящими женщинами. Дозировка Оциллококцинума определяется только стадией заболевания и целью назначения. Оциллококцинум может применяться для профилактики в период распространения ОРВИ и гриппа, в этом случае рекомендуется принимать 1 дозу в неделю.
Явные преимущества препарата подтверждены данными, полученными при проведении многочисленных клинических наблюдений во многих странах мира.
В многоцентровом рандомизированном исследовании, выполненном во Франции, эффективность Оциллококцинума оценивалась при лечении 300 больных гриппом. Пациенты основной группы при появлении первых симптомов заболевания (озноб, ломота, высокая температура тела) принимали Оциллококцинум в течение 3–4 дней до исчезновения симптомов. Пациентам контрольной группы назначали плацебо. Температура тела, примерно одинаковая в обеих группах больных до начала лечения, быстрее снижалась у пациентов, получавших Оциллококцинум, и нормализовалась к 4 дню. Озноб, исходно имевший место в обеих группах, исчез к 4 дню у 55% больных, принимавших активный препарат, и только у 26,5% пациентов, получавших плацебо [28].
В другом исследовании, проведенном в Германии в период эпидемического подъема ОРВИ с осени 1990 до весны 1991 г., также оценивалась эффективность применения Оциллококцинума для лечения гриппа. При этом 188 пациентов (93 женщины и 95 мужчин, средний возраст — 35,1±12,7 года) получали Оциллококцинум, а 184 (88 женщин и 96 мужчин, средний возраст — 34,9±12,1 года) — плацебо. Оценка состояния больных проводилась в начале лечения, через 2 сут и в период с по день. Дважды в день измерялась температура тела, регистрировались изменения 9 симптомов (кашель, насморк, мышечные боли, боли в горле и др.). Кроме того, регистрировалось возможное использование других лекарственных средств [35]. Препарат признавался эффективным, если число пациентов из принимавшей его группы, у которых все гриппоподобные симптомы исчезали в течение первых 2 сут, превышало число выздоровевших пациентов из группы плацебо, и/или если период полного выздоровления был менее продолжительным при использовании Оциллококцинума, чем при приеме плацебо. У всех пациентов регистрировались точность, с которой они следовали всем необходимым предписаниям, полнота и регулярность заполнения анкет и развитие побочных явлений. В результате нарушения условий протокола 21 пациент из основной группы и 17 из контрольной были выведены из исследования. Таким образом, в каждой из групп оценивалось состояние 167 пациентов.
Результаты исследования подтвердили эффективность Оциллококцинума в лечении гриппа и показали, что в течение первых 2 сут у 19,2% лиц, принимавших препарат, симптомы гриппа исчезли полностью, и они смогли полноценно трудиться. На 5 сут некоторые симптомы гриппа оставались у 26,4% лиц основной группы и 32,3% контрольной. Через 7–10 дней после начала лечения у 133 (80,1%) пациентов, принимавших Оциллококцинум, симптомов гриппа не наблюдалось. В группе, получавшей плацебо, к этому сроку выздоровели 128 (76,6%) человек.
Авторы особо подчеркивают положительное действие препарата на тяжесть течения заболевания. Через 2 сут после начала лечения значительное улучшение состояния отмечали 43,7% больных, принимавших Оциллококцинум, и 33,5% из группы плацебо. В контрольной группе к этому моменту у 5,4% пациентов отмечено ухудшение состояния, связанное, , с присоединением вторичной инфекции, которое потребовало дополнительных лечебных мероприятий.
Пациенты, принимавшие плацебо, в 1,5 раза чаще по сравнению с основной группой прибегали к применению сопутствующих лекарственных средств (анальгетиков, отхаркивающих, противокашлевых препаратов и др.). Исследователи отметили, что процент работоспособных пациентов в группе активного лечения был несколько выше, чем в группе плацебо: соответственно 16,3 и 9,2% — через 2 дня после начала лечения и 48,9 и 46,7% — через 4 дня. У 5 пациентов, участвовавших в этом исследовании, наблюдались нежелательные явления. Согласно заключению авторов, у 4 из них они не были связаны с действием исследуемого препарата. У 1 пациента отмечалась головная боль, связанная, возможно, с его приемом.
Таким образом, применение Оциллококцинума способствует более быстрому купированию клинических симптомов гриппа и сокращает продолжительность заболевания.
В России и соавт. подтвердили высокую эффективность препарата в нескольких исследованиях, проведенных у медицинского персонала (2006) и у молодых людей в возрасте от 16 до 22 лет (2007) [17].
Высокая эффективность и безопасность Оциллококцинума в лечении и профилактике респираторных вирусных инфекций подтверждены в многочисленных отечественных и зарубежных исследованиях. Несмотря на множество вопросов о противовирусном механизме действия гомеопатических препаратов, эффективность Оциллококцинума показана в клинических исследованиях, с использованием плацебо.
Воздействуя на организм на и электромагнитном уровне, индивидуальном для данного вещества, гомеопатический препарат Оциллококцинум не имеет побочных эффектов, работает тонко, избирательно, не перегружая организм. Результаты приведенных наблюдений позволяют сделать вывод об эффективности гомеопатического препарата Оциллококцинум в лечении ОРВИ и гриппа.
Оциллококцинум хорошо переносится, может быть использован как средство монотерапии при ОРВИ и гриппе. Отсутствие побочных эффектов и ограничений в сроках начала лечения и по возрасту позволяет рекомендовать данное средство к широкому использованию для лечения ОРВИ в амбулаторной практике. Применение Оциллококцинума в качестве профилактического средства позволяет снизить уровень заболеваемости и риск формирования патологии у детей.
Читайте также:

