Грипп патогенез и иммунитет
Обновлено: 24.04.2024
Этиология гриппа
Грипп — острое респираторное вирусное заболевание, этиологически связанное с представителями трех родов — Influenza A virus (вирусы гриппа А), Influenza В virus (вирусы гриппа В) и Influenza С virus (вирусы гриппа С) — из семейства Orthomyxoviridae [2, 26].
Вирус гриппа А был впервые изолирован от свиней американским вирусологом Ричардом Шоупом (1901–1966) в 1930 г.; от людей — тремя годами позже группой английских ученых: Вильсоном Смитом (1897–1965), Кристофером Эндрюсом (1896–1987) и Патриком Лейдлоу (1881–1940) [26].
| Рис. 1. Структура вириона вируса гриппа А (Orthomyxoviridae, Influenza A virus) |
На поверхности вириона (вирусной частицы) вируса гриппа А имеются две функционально-важные молекулы (рис. 1): гемагглютинин (с помощью которого вирион прикрепляется к поверхности клетки-мишени); нейраминидаза (разрушающая клеточный рецептор, что необходимо при почковании дочерних вирионов, а также для исправления ошибок при неправильном связывании с рецептором) [2, 24, 26].
В настоящее время известны 16 типов гемагглютинина (обозначаемые как Н1, Н2, …, Н16) и 9 типов нейраминидазы (N1, N2, …, N9). Комбинация типа гемагглютинина и нейраминидазы (например, H1N1, H3N2, H5N1 и т. п.) называется субтипом: из 144 (16 × 9) теоретически возможных субтипов на сегодняшний день известны 115 [24].
Природным резервуаром вируса гриппа А являются дикие птицы водно-околоводного экологического комплекса (в первую очередь, речные утки, чайки и крачки), однако вирус способен преодолевать межвидовой барьер, адаптироваться к новым хозяевам и длительное время циркулировать в их популяциях [9–12]. Эпидемические варианты вируса гриппа А вызывают ежегодный подъем заболеваемости и раз в 10–50 лет — опасные пандемии [1, 11, 16].
Вирус гриппа В был открыт в 1940 г. американским вирусологом Томасом Фрэнсисом-младшим (1900–1969). Вирус гриппа В не вызывает пандемии, но является возбудителем крупных эпидемических вспышек [26].
Вирус гриппа С был открыт в 1947 г. американским вирусологом Ричардом Тейлором (1887–1981). Вирус гриппа С вызывает локальные эпидемические вспышки в детских коллективах. Наиболее тяжело инфекция протекает у детей младшего возраста [26].
Вирусы гриппа занимают важное место в структуре заболеваемости людей острыми респираторными вирусными инфекциями (ОРВИ), составляющими до 90% от всех других инфекционных болезней. По данным Всемирной Организации Здравоохранения (ВОЗ), только тяжелыми формами гриппа в мире ежегодно заболевают 3–5 млн человек. Заболевает ежегодно гриппом и другими ОРВИ в РФ — 25–35 млн, из них 45–60% — дети. Экономический ущерб РФ от сезонного эпидемического гриппа составляет до 100 млрд руб./год, или порядка 85% экономических потерь от инфекционных болезней [2–8, 20–23].
История гриппозных пандемий
В первый постпандемический эпидсезон 2010–2011 гг. пандемический грипп А(H1N1) swl стал причиной более 70% случаев ОРВИ в мире, грипп А(H3N2) — 1–5%, грипп В — 10–20%.
Состав противогриппозных вакцин в эпидсезоне 2011–2012 гг. (как и в 2010–2011 гг.): A/California/07/2009 (H1N1) swl; A/Perth/16/2009 (H3N2); B/Brisbane/60/2008.
Пандемический вирус гриппа А(H1N1) swl резистентен к Ремантадину и Амантадину, но чувствителен к Тамифлю, Релензе, Ингавирину, Арбидолу и Рибавирину [13–16, 18, 19, 23].
Высоковирулентный грипп А(H5N1) птиц — возможный возбудитель очередной пандемии.
Вероятность преодоления вирусом гриппа А межвидового барьера и проникновения в человеческую популяцию с опасными последствиями резко увеличивается в период эпизоотий 3 . Поэтому высоковирулентный вирус гриппа А(H5N1) птиц, ставший причиной современной масштабной эпизоотии среди диких и домашних птиц Старого Света и имеющий повышенную способность репродуцироваться в клетках млекопитающих, рассматривается как наиболее вероятный возбудитель очередной пандемии гриппа [10, 11, 17]. Дальнейшее распространение этого вируса может иметь катастрофические последствия в случае появления у него эпидемического потенциала (способности передаваться от человека к человеку), так как, во-первых, у человечества отсутствует коллективный иммунитет к вирусам гриппа А (Н5), а во-вторых, из 563 лабораторно подтвержденных случаев заболевания людей в 15 странах мира в результате заражения вирусом гриппа А(H5N1) птичьего происхождения за 2003–2011 гг. 330 умерли, т. е. летальность приближается к 60% [11, 24].
Патогенез гриппа
У человека вирусы гриппа поражают эпителиальные клетки слизистой оболочки респираторного тракта, а также бокаловидные клетки (секретирующие слизь), альвеолоциты и макрофаги [3, 4, 7]. Все эти клетки имеют на своей поверхности рецептор, с которым связывается вирусный гемагглютинин (рис. 1), — концевой остаток сиаловой, или N-ацетилнейраминовой, кислоты (Neu5Ac) (рис. 2), в составе полисахаридных цепочек, входящих в состав ганглиозидов и гликопротеинов. Концевой остаток сиаловой кислоты может связываться со следующим моносахаридом двумя способами: с помощью альфа2-3- или альфа2-6-связи (рис. 2) [14, 18].
Рис. 2. Структурные формулы сиаловой, или N-ацетилнейраминовой кислоты (Neu5Ac) и двух способов ковалентной связи со следующим моносахаридом (в данном случае — галактозой, Gal): альфа2-3- или альфа2-6-связью
Клетки эпителия верхних отделов респираторного тракта человека содержат, в основном, альфа2-6-сиалозиды; нижних отделов — альфа2-3-сиалозиды (рис. 3). Поэтому эпидемические штаммы вирусов гриппа, имея альфа2-6-специфичность, легко репродуцируются в верхних отделах респираторного тракта человека, активно выделяются в окружающую среду при речи, чихании, кашле и эффективно заражают других людей капельно-воздушным путем.
Варианты вируса гриппа А, адаптированные к птицам, имеют альфа2-3-специфичность (рис. 3). Концевые альфа2-3-сиалозиды содержатся у птиц, в основном, на поверхности эпителиальных клеток слизистой кишечника, поэтому у птиц грипп протекает в форме энтерита; вирус выделяется во внешнюю среду с фекалиями, а заражение происходит алиментарным путем. Альфа2-3-специфичность птичьих вариантов вируса гриппа А объясняет их неспособность эффективно поражать эпителий верхних отделов респираторного тракта человека и, как следствие, — передаваться капельно-воздушным путем в человеческой популяции. Вместе с тем, если высоковирулентный вирус гриппа А птиц каким-либо образом сумел вызвать продуктивную инфекцию в человеческом организме, то он будет эффективно поражать нижние отделы респираторного тракта, становясь причиной тяжелой первичной вирусной пневмонии (по данным ВОЗ, в 60% случаев — летальной).
Эпителиоциты свиней одновременно содержат и альфа2-6-, и альфа2-3-сиалозиды (рис. 3), поэтому в организме могут одновременно циркулировать и эпидемические, и птичьи варианты вируса гриппа А. Вследствие этого в свиных популяциях могут, во-первых, формироваться реассортанты 4 человеческих и птичьих штаммов с новыми биологическими свойствами; во-вторых, селектироваться штаммы со смешанной альфа2-6/альфа2-3-специфичностью. Именно такой смешанной альфа2-6/альфа2-3-специфичностью обладают штаммы пандемического вируса гриппа А(H1N1) swl, и, как следствие, они обладают способностью распространяться капельно-воздушным путем и вызывать тяжелые пневмонии [13–15, 18, 19, 23].
Рис. 3. Сиалозиды-рецепторы вирусов гриппа А на поверхности эпителиоцитов людей (альфа2-6 — на слизистой верхних, альфа2-3 — на слизистой нижних отделов респираторного тракта), свиней (альфа2-6/альфа2-3-смесь на слизистой респираторного тракта) и птиц (альфа2-3 — на слизистой кишечника)
Инфицирование эпителиоцитов имеет следствием быстрый рост вирусной нагрузки, апоптоз, дегенерацию и некроз этого типа клеток с последующим развитием токсических и токсико-аллергические реакций. У людей характерно повреждение клеток цилиндрического эпителия трахеи и бронхов. Главным звеном в патогенезе гриппа А является поражение сосудистой и нервной систем, возникающее вследствие токсического действия вируса. При этом одним из основных механизмов влияния вируса гриппа А на сосудистую систему является образование активных форм кислорода, которые взаимодействуют с фосфолипидами клеточных мембран, вызывая в них процесс перекисного окисления липидов, нарушение мембранного транспорта и барьерных функций, способствуя дальнейшему развитию вирусной инфекции. Лизосомальные ферменты дополнительно повреждают эпителий капилляров, базальную мембрану клеток, что способствует распространению гриппозной инфекции и виремии. Повышение проницаемости сосудов, ломкость их стенок, нарушение микроциркуляции является причиной возникновения геморрагических проявлений — от носовых кровотечений до геморрагического отека легких и кровоизлияний в вещество головного мозга. Циркуляторные расстройства, в свою очередь, вызывают поражения ЦНС: патоморфологическая картина характеризуется наличием лимфомоноцитарных инфильтратов вокруг мелких и средних вен, гиперплазией глиальных элементов и очаговой демиелинизацией, что свидетельствует о токсико-аллергической природе патологического процесса в ЦНС при гриппе [3–8, 23].
Важным фактором патогенеза при гриппе является продукция вирусного белка PB1-F2, который вызывает апоптоз тканевых макрофагов легких и тем самым способствует развитию вторичных бактериальных пневмоний (у современного пандемического варианта вируса гриппа А(H1N1) swl продукция PB1-F2, к счастью, отсутствует, что снижает — но не отменяет! — вероятность развития вторичных пневмоний, оставляя в силе опасность первичных вирусных пневмоний — см. далее) [2, 26].
Клиническая картина гриппа у людей
Начало острое, с озноба, быстрого повышения температуры до высоких цифр, резкого нарастания симптомов интоксикации. Температура достигает максимальных значений (39,0–40,0 °С) в первые сутки заболевания. В этот же период нарастают признаки интоксикации: озноб, сильная головная боль, головокружение, миалгии, артралгии, выраженная слабость. При внешнем осмотре: лицо гиперемировано, одутловато, сосуды склер инъецированы, определяется гиперемия конъюнктив, цианоз губ и слизистой оболочки ротоглотки, возможны точечные геморрагии на мягком небе. Цианоз вообще является важным симптомом при гриппе: следует обращать внимание не только на цианоз губ, но и на цианотичный оттенок язычка, миндалин, небных дужек на фоне яркой гиперемии слизистой ротоглотки; слизистая оболочка мягкого неба также имеет цианотичный оттенок, хорошо видна мелкая зернистость, инъекция сосудов и мелкоточечные геморрагические элементы; на задней стенке глотки — умеренная гиперплазия лимфоидной ткани.
Локализация головной боли: в лобно-височной области и в глазных яблоках (при легком надавливании на них или при их движении). Нередко определяются менингеальные знаки, которые постепенно исчезают с уменьшением интоксикации и снижением температуры тела. Диапазон клинических проявлений со стороны нервной системы достаточно широкий: от функциональных расстройств до серозных менингитов и тяжелых менингоэнцефалитов.
При развитии вторичных пневмоний на фоне вирусной инфекции определяются признаки бактериального воздействия, подтверждаемого обнаружением в мокроте бактерий Streptococcus pneumoniae, Staphylococcus aureus и др. Как правило, вторичная пневмония развивается после 5–7 сут гриппа и характеризуется повторным подъемом температуры до фебрильных значений, усилением кашля, появлением слизисто-гнойной мокроты, часто с прожилками крови, рентгенологически — очаговыми и очагово-сливными инфильтратами, нередко с признаками деструкции и абсцедирования. Позже 10 сут пневмония имеет, как правило, бактериальную этиологию и чаще всего связана с грамотрицательной микрофлорой.
Одним из главных факторов, способствующих тяжелому течению гриппа, является сопутствующая патология. В частности, у пациентов, умерших в период двух последних эпидсезонов 2009–2011 гг., преобладали болезни сердца и сосудов, сахарный диабет, метаболический синдром (ожирение), алкоголизм и табакокурение. Особую группу риска составляют беременные, у которых пневмония может развиваться стремительно, а потому они требуют особого внимания клиницистов и безотлагательной терапии.
Литература
М. Ю. Щелканов, доктор биологических наук, доцент
Л. В. Колобухина, доктор медицинских наук, профессор
Д. К. Львов, доктор медицинских наук, профессор, академик РАМН
1 Для сравнения: в результате военных действий за 5 лет Первой мировой войны (1914–1918 гг.) погибли 8,3 млн человек.
3 Эпизоотия — процесс распространения инфекционного заболевания в популяциях животных.
4 Вирус гриппа А имеет геном, состоящий из 8 отдельных молекул РНК. Реассортацией называется формирование штамма, у которого источником различных генетических сегментов стали различные родительские штаммы, одновременно инфицировавшие одну и ту же клетку.
Что такое острые респираторные заболевания (ОРЗ)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Острые респираторные заболевания (ОРЗ) — группа острых инфекционных заболеваний, при которых возбудители проникают в организм человека через дыхательные пути и вызывают синдром поражения респираторного тракта и общей инфекционной интоксикации. Употребление термина ОРВИ (острое респираторное вирусное заболевание) при отсутствии лабораторно подтверждённой этиологической расшифровки является некорректным.
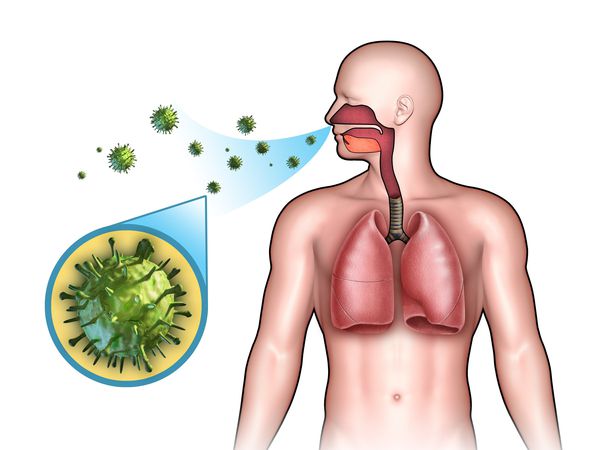
Этиология
ОРЗ — полиэтиологический комплекс заболеваний, т. е. они могут быть вызваны различными видами возбудителей:
- бактерии (стафилококки, стрептококки, пневмококки, гемофильная палочка, моракселла катаралис и др.);
- вирусы (риновирусы, аденовирусы, респираторно-синцитиальный вирус, реовирусы, коронавирусы, энтеровирусы, герпесвирусы, вирусы парагриппа и гриппа);
- хламидии (х ламидия пневмония , хламидия пситаки, хламидия трахоматис );
- микоплазмы (м икоплазма пневмония ).
Чаще всего возбудителем ОРЗ являются вирусы, поэтому термин ОРВИ используют небезосновательно. В последнее время иногда встречается употребление термина ОРИ (острая респираторная инфекция) [2] [4] .
Эпидемиология
ОРЗ — это преимущественно антропонозы, т. е. болезни, способные поражать только человека . Являются самой многочисленной и частой группой заболеваний у человека (до 80 % всех болезней у детей). Поэтому они представляют серьёзную проблему для здравоохранения различных стран вследствие наносимого ими экономического ущерба.
Источник инфекции — больной человек с выраженными или стёртыми формами заболевания. Восприимчивость всеобщая, иммунитет к некоторым возбудителям (аденовирусы, риновирусы) стойкий, но строго типоспецифичный. Это значит, что заболеть ОРЗ, вызванным одним видом возбудителя, но разными серотипами (их могут быть сотни), можно многократно. Заболеваемость повышается в осенне-зимний период, может принимать вид эпидемических вспышек, довлеет к странам с прохладным климатом. Чаще болеют дети и лица из организованных коллективов (особенно в период адаптации).
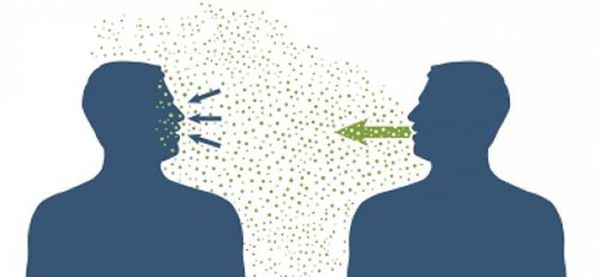
Основной механизм передачи — воздушно-капельный (аэрозольный, в меньшей степени воздушно-пылевой путь), но может также играть роль контактно-бытовой механизм (контактный — при поцелуях, бытовой — через загрязнённые руки, предметы или воду) [2] [7] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы острых респираторных заболеваний (ОРЗ)
Инкубационный период различен и зависит от вида возбудителя, может варьироваться от нескольких часов до 14 дней (аденовирус).
Для каждого возбудителя ОРЗ имеются свои специфические особенности протекания заболевания, однако все их объединяет наличие синдромов общей инфекционной интоксикации (СОИИ) и поражения дыхательных путей в той или иной степени. СОИИ проявляется общей слабостью, адинамией, быстрой утомляемостью, повышенной температурой тела, потливостью и др.
Синдром поражения респираторного тракта (СПРТ) — основной синдром для данных заболеваний, он включает:
- Ринит — воспаление слизистой оболочки носа. Характеризуется заложенностью носа, снижением обоняния, чиханием, выделениями из носа — сначала прозрачными слизистыми, затем слизисто-гнойными (более плотные выделения жёлто-зелёного цвета появляются в результате присоединения вторичной бактериальной флоры). — воспаление слизистой оболочки глотки. Основные симптомы: першение и боли в горле различной интенсивности, сухой кашель — "горловой".
- Ларингит — воспаление слизистых оболочек гортани. Проявляется осиплостью голоса, иногда афонией (отсутствием голоса), кашлем и болью в горле.
- Трахеит — воспаление трахеи. Сопровождается мучительным, преимущественно сухим кашлем, саднением и болями за грудиной.
- Бронхит — воспаление слизистой оболочки бронхов. При этом возникает кашель с наличием мокроты и без, сухие хрипы, редко крупнопузырчатые хрипы при аускультации (выслушивании).
- Бронхиолит — воспаление бронхиол (мелких бронхов). Характеризуется наличием кашля различной интенсивности и хрипов разных калибров.
Дополнительными синдромами могут быть:
- синдром экзантемы (высыпания на кожных покровах);
- тонзиллита (воспаления миндалин);
- лимфаденопатии (ЛАП) — увеличения лимфатических узлов ; ( воспаления слизистой оболочки глаза) ;
- гепатолиенальный синдром (увеличение печени и селезёнки);
- геморрагический синдром ( повышенная кровоточивость) ;
- синдром энтерита (воспаления слизистой оболочки тонкого кишечника) .
Алгоритм по распознаванию ОРЗ различной этиологии:
Наиболее распространенным заболеванием, имеющим тяжёлое течение и высокий риск развития осложнений является грипп. Инкубационный период гриппа длится от нескольких часов до 2-3 дней. В отличие от других острых респираторных заболеваний, при гриппе сначала появляется синдром общей инфекционной интоксикации (высокая температура, озноб, сильная головная боль, слезотечение, боль при движении глазных яблок, ломота в мышцах и суставах). На 2-3-день присоединяются симптомы поражения респираторного тракта: першение в горле, насморк, сухой надсадный кашель.
Типичное ОРЗ начинается с чувства дискомфорта, першения в носу и горле, чихания. В течение непродолжительного периода симптоматика нарастает, першение усиливается, появляется чувство интоксикации, повышается температура тела (обычно не выше 38,5 ℃), появляется насморк, неярко-выраженный сухой кашель. В зависимости от вида возбудителя и свойств микроорганизма могут последовательно появляться все перечисленные синдромы ОРЗ в различных сочетаниях и степени выраженности. Возможно появление осложнений и неотложных состояний [6] [7] .
Патогенез острых респираторных заболеваний (ОРЗ)
- у аденовирусов — гликопротеином (фибриллы);
- у парамиксо- или ортомиксовирусов шипами гемагглютинина;
- у коронавирусов — S-белком соединения и гликолипидами.
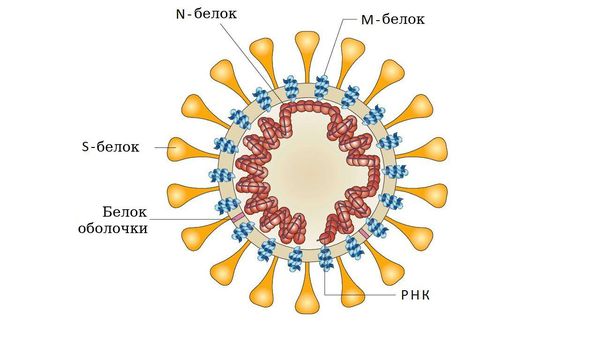
Взаимодействие болезнетворного агента с клеточными рецепторами необходимо не только для прикрепления его к клетке, но и для запуска клеточных процессов, подготавливающих клетку к дальнейшей инвазии. Т. е. наличие соответствующих рецепторов на поверхности клеток — это один из важнейших факторов, определяющих возможность или невозможность возникновения инфекционного процесса. Внедрение возбудителя в клетку хозяина вызывает поток сигналов, активирующих целый ряд процессов, с помощью которых организм пытается от него освободиться, например, ранний защитный воспалительный ответ, а также клеточный и гуморальный иммунный ответ. Повышение метаболизма клеток представляет собой защитный процесс, но с другой стороны в результате накопления свободных радикалов и факторов воспаления запускается патологический процесс:
- нарушается липидный слой клеточных мембран эпителия верхних отделов респираторного тракта и лёгких;
- нарушаются матричные и барьерные свойства внутриклеточных мембран, увеличивается их проницаемость;
- развивается дезорганизация жизнедеятельности клетки вплоть до её гибели.
Второй этап инфицирования характеризуется вирусемией — попаданием вируса в кровь и распространением по всему организму. В совокупности с повышением деятельности защитных механизмов и появлением в крови продуктов распада клеток этот процесс вызывает интоксикационный синдром.
Третий этап характеризуется усилением выраженности реакций иммунной защиты, элиминацию (выведение) микроорганизма и восстановление строения и функции поражённой ткани хозяина [5] [7] .
Классификация и стадии развития острых респираторных заболеваний (ОРЗ)
По вовлечению отдельных частей дыхательной системы:
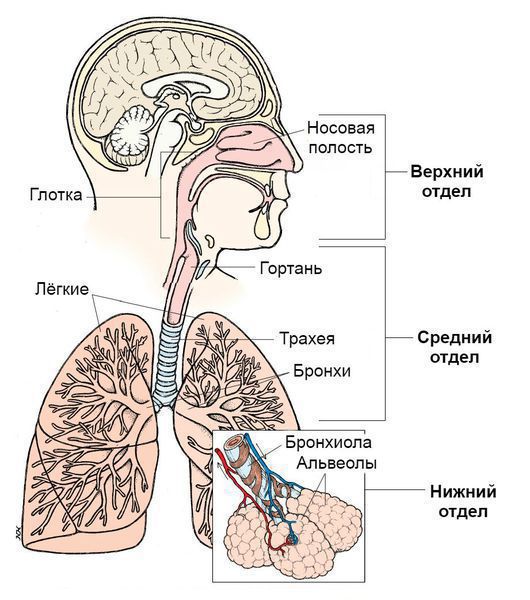
- Инфекции верхних дыхательных путей. Верхние дыхательные пути начинаются с носа и включают голосовые связки в гортани, придаточные пазухи носа и среднее ухо.
- Инфекции нижних дыхательных путей. Нижние дыхательные пути начинаются с трахеи и бронхов и заканчиваются бронхиолами и альвеолами.
По клинической форме:
- Типичная.
- Атипичная:
- акатаральная (отсутствие признаков поражения дыхательных путей при наличии симптомов общей инфекционной интоксикации);
- стёртая (маловыраженная клиника);
- бессимптомная (полное отсутствие клинической симптоматики).
По течению:
По степени тяжести:
По длительности течения:
- острое (5-10 дней);
- подострое (11-30 дней);
- затяжное (более 30 дней) [8] .
Осложнения острых респираторных заболеваний (ОРЗ)
Если острое респираторное заболевание не пролечить вовремя, могут появиться различные более серьёзные заболевания:
- Связанные с ЛОР-органами: отит, синуситы, бактериальный ринит, ложный круп.
- Связанные с лёгочной тканью: вирусные пневмонии, вирусно-бактериальные и бактериальные пневмонии, абсцесс лёгкого ( ограниченный очаг гнойного воспаления в лёгочной ткани) , эмпиема плевры ( скопление гноя в плевральной полости) . Пневмония проявляется значимым ухудшением общего состояния, выраженным кашлем, усиливающимся на вдохе, при аускультации звуком крепитации ( потрескиванием или похрустыванием) , влажными мелкопузырчатыми хрипами, иногда одышкой и болями в грудной клетке.

- Связанные с поражением нервной системы: судорожный синдром, неврит ( воспаление нерва) , менингит ( воспаление оболочек головного и спинного мозга) , менингоэнцефалит (воспаление оболочек и вещества головного мозга), синдром Гийена—Барре и др. [10]
- Связанные с поражением сердца: миокардит (воспаление сердечной мышцы).
- Связанные с обострением хронических заболеваний: обострение ревматизма, тонзиллита, туберкулёза, пиелонефрита (воспаление почки) и др. [7]
Диагностика острых респираторных заболеваний (ОРЗ)
В широкой рутинной практике лабораторная диагностика ОРЗ (особенно при типичном неосложнённом течении) обычно не проводится. В отдельных случаях могут использоваться:
- Развёрнутый клинический анализ крови. При этом может обнаружиться лейкопения ( снижение количества лейкоцитов) и нормоцитоз ( нормальный размер эритроцитов) , лимфо- и моноцитоз ( увеличение числа лимфоцитов и моноцитов) , при наслоении бактериальных осложнений — нейрофильный лейкоцитоз со сдвигом влево (увеличение количество нейтрофилов и появление их незрелых форм );
- Общеклинический анализ мочи (изменения малоинформативны, указывают на степень интоксикации).
- Биохимические анализы крови. Может выявляться С-реактивный белок (указывает на наличие инфекции). При некоторых системных возбудителях, например аденовирусной инфекции, характерно повышение АЛТ.
- Серологические реакции. Возможна ретроспективная диагностика методами РСК, РА, ИФА, однако она редко используется в практической деятельности. В настоящее время широко применяется ПЦР-диагностика мазков-отпечатков, но её применение ограничено в основном стационарами и научно-исследовательскими группами.
При подозрении на развитие осложнений проводят соответствующие лабораторные и инструментальные исследования (рентген придаточных пазух носа, органов грудной клетки, КТ и др.) [3] [5] .
Лечение острых респираторных заболеваний (ОРЗ)
ОРЗ встречается очень часто и в большинстве случаев протекает в лёгкой и средней степени тяжести, поэтому обычно больные проходят лечение дома. При тяжёлых формах (с риском развития или развившимися осложнениями) пациенты должны проходить терапию в условиях инфекционного стационара до нормализации процесса и появления тенденций к выздоровлению. В домашних условиях лечением ОРЗ занимается терапевт или педиатр (в некоторых случаях инфекционист).
Пища должна быть разнообразной, механически и химически щадящей, богатой витаминами, рекомендуются мясные нежирные бульоны (идеально подходит негустой куриный бульон и т. п.), обильное питьё до — 3 л/сут. (тёплая кипячёная вода, чай, морсы). Хороший эффект оказывает тёплое молоко с мёдом, чай с малиной, отвар брусничных листьев.
Медикаментозная терапия ОРЗ включает в себя этиотропную (т. е. воздействующую на возбудителя заболевания), патогенетическую (дезинтоксикация) и симптоматическую (уменьшение беспокоящих симптомов) терапию.
Этиотропная терапия имеет смысл лишь при назначении в раннем периоде и лишь при ограниченном спектре возбудителей (в основном при гриппе). Использование средств отечественной фарминдустрии ("Арбидол", "Кагоцел", "Изопринозин", "Амиксин", "Полиоксидоний" и т. п.) не обладают никакой доказанной эффективностью и могут иметь эффекта, лишь в качестве плацебо.
В качестве симптоматической терапии могут быть использованы препараты следующих групп:
- жаропонижающие при температуре у взрослых свыше 39,5, у детей — свыше 38,5 ℃ (парацетамол, ибупрофен);
- противовирусные и антибактериальные глазные капли при конъюнктивите;
- сосудосуживающие капли в нос при заложенности носа и насморке (не более 5 дней);
- солесодержащие капли в нос при рините для разжижения слизи;
- противоаллергические препараты при аллергическом компоненте ОРЗ;
- средства противовоспалительного и противомикробного действия местного действия (таблетки, пастилки и др.);
- средства для улучшения образования, разжижения и выделения мокроты (муколитики);
- антибиотики широкого спектра действия (при отсутствии улучшения в течении 4-5 дней, присоединении вторичной бактериальной флоры и развитии осложнений) [2][6] .
Прогноз. Профилактика
Прогноз при ОРЗ — положительный. Больные обычно выздоравливают в течение 5-10 дней без неблагоприятных последствий. Осложнения респираторных заболеваний могут возникнуть при гриппе, другие возбудители менее агрессивны. Также неблагоприятные последствия возможны у пациентов с ослабленным иммунитетом. После выздоровления организмом вырабатывается иммунитет к той инфекции, которой человек переболел .
Ведущую роль в профилактике распространения ОРЗ (исключая грипп) является:
Переборов сопротивление ослабленных ресничек, возбудитель попадает в носоглотку и поддается действию высокоактивного секрета клеток. Белки секрета слизистых желез способны неспецифически ингибировать гемагглютинирующую и инфекционную активность вируса гриппа. Это действие обусловлено наличием в секрете гликопротеидов, которые содержат значительное количество N-ацетилнейраминовой кислоты. Существуют сезонные колебания содержания ингибиторов. Наиболее активны они в летне-осенний период, а в период эпидемии гриппа (зима) содержание ингибиторов снижается. Погибшие клетки отрываются и захватываются макрофагами, а также удаляются с секретом дыхательных путей. В подслизистом слое в результате высвобождения биологически активных веществ (гистамин, серотонин, кинины, простагландины) возникает реакция сосудов, форменных элементов крови, образование мелких тромбов и кровоизлияний, диапедез мо-нонуклеаров и нейтрофильных лейкоцитов, отек, местные нарушения метаболизма, изменения рН среды в кислую сторону и тому подобное. При этом патологический воспалительный процесс наиболее выражен в трахее и бронхах.
Наличие токсикоза при гриппе является существенной особенностью патогенеза. Симптомы интоксикации являются следствием резорбции токсичных субстанций вирусов, продуктов нарушенного обмена веществ, что прямо или опосредованно влияет на органы и системы. Вирус обладает токсическим действием на сосудистую систему, значительно повышая проницаемость и ломкость сосудов, что в комплексе с расстройствами микроциркуляции может приводить к развитию геморрагического синдрома. В возникновении циркуляторных расстройств, кроме прямого действия на сосудистую стенку, большое значение имеет нейротропность вируса. Характерны фазовые повреждения вегетативной нервной системы, касающиеся двух ее частей (симпатической и парасимпатической): гипертензия изменяется гипотензией, тахикардия — брадикардией, повышается секреция слизи в дыхательных путях, появляется потливость.
Проникая в более глубокие слои эпителия, вирус встречается со второй линией специфической обороны (интерферон, циркулирующие антитела классов IgM, IgG, IgE, температурная реакция). Механизмы иммунного ответа при гриппе представлены на рис. 3.
Рис. 3. Механизмы иммунного ответа при гриппе
При гриппе в ответ на инфицирование развиваются ранние цитокиновые реакции (РЦР) как наиболее быстрый ответ на вирус. Здесь мы имеем дело с естественным (врожденным) и наиболее распространенным вариантом РЦР на вирус гриппа как на внутриклеточного паразита, когда вирус сам включает систему интерферона, играя роль природного индуктора.
Каскад внутриклеточных событий, который наблюдается после внедрения вируса, обусловлен индукцией образования ИФН и в последующем разрушением вирусных информационных РНК, благодаря действию 2'-5'-олигоаденилсинтетазы и активации эндонуклеазы. Параллельно активированная протеинкиназа фосфорилирует а-субъединицу фактора, который инициирует трансляцию, что приводит к блокировке синтеза вирусных белков. Все это приводит к угнетению репродукции широкого спектра РНК и ДНК-содержащих вирусов за счет прямого внутриклеточного антивирусного эффекта. Эти явления происходят в течение первых часов после проникновения вируса гриппа в организм.
Интерфероны (в первую очередь ИФН-b или так называемые интерфероны I типа) имеют способность к активации естественных киллеров (ЕК) и цитотоксических лимфоцитов. В результате на этом этапе вирусного инфицирования локально осуществляются три взаимосвязанных действия:
- внутриклеточная ингибиция интерферонами репродукции вирусов;
- удаление посредством ЕК и ЦТЛ инфицированного материала;
- защита вновь образованным интерфероном окружающих незараженных клеток от возможного заражения.
Интерферон распределяется по организму, связывается со специфическими рецепторами здоровых неповрежденных клеток и делает их невосприимчивыми к вирусу. С интерферонсвязанных неинфицированных клеток вокруг очага вирусной инфекции образуется заслон для последующего распространения инфекции. Кроме того, интерферон активирует почти все иммунные реакции (модуляция взаимосвязи между эндокринной и иммунной системами, активация макрофагов, повышение цитотоксичности, стимуляция экспрессии антигенов ГКГ I и II классов).
Однако описанные эффекты ИФН нередко являются недостаточными для завершения инфекционного процесса. Подобное имеет место при сниженном сопротивлении организма, дефектности системы ИФН и иммунитета, неблагоприятной экологической ситуации, действии стрессов и др.
В итоге развивается острое заболевание, которое сопровождается продукцией каскада ранних цитокинов (второй этап РЦР), активацией CD4+ и CD8+ Е-клеток с последующим развитием специфического, опосредствованного Т- и В-клеточного иммунитета. В этих случаях кроме ИФН 1-го типа синтезируются такие ранние цитокины, как фактор некроза опухоли, образуются интерлейкины (IL) 1b, 6, 10 и 15, а также трансформирующий фактор роста (TGF). На этом этапе уже отмечается вариабельность РЦР при разных вирусных инфекциях. Продукция ИФН-b считается ключевым доминантным признаком инфицирования вирусом.
ИФН а/b вызывает лейкопению, лимфаденопатию, миграцию клеток из красной пульпы селезенки в белую пульпу, то есть происходит перераспределение клеток для последующих иммунорегуляторных эффектов. ИФН а/b могут усилить специфический иммунный ответ при гриппе в период первичной инфекции за счет притягивания популяции В- и Е-клеток в места воспаления для антигенной презентации.
Первыми на инфекцию начинают реагировать макрофаги, в них происходит расщепление вирусной частицы на отдельные пептиды, которые продвигаются к поверхности клетки, здесь (на мембране макрофага) они контактируют с молекулами ГКГ I и II классов. ИФН, который секретируется ИЛ-1, усиливает экспрессию антигена ГКГ. Выраженное синергичное действие ИЛ-1 и ИЛ-2 способствует пролиферации предшественников Т-клеток в вилочковой железе. В очаг инфекции направляются Т-лимфоциты (хелперы), которым и предоставляются фрагменты антигена в комплексе с молекулами ГКГ. В активации Т-хелперов принимают участие ИЛ-4, ИЛ-6 и ФНО. Возможна ситуация, когда Т-лимфоциты способны непосредственно связывать вирусные антигены при участии антигенов II класса ГКГ. Потом подключаются ЦТЛ и NK-клетки, которые являются основными факторами ликвидации инфицированных вирусом клеток. Но роль CD8+ ЦТЛ двойственна: с одной стороны, они более эффективно по сравнению с другими субпопуляциями элиминируют вирус из отделов нижних дыхательных путей, с другой — усиливают реакции локального воспаления, вызывая в эксперименте синдром респираторного дистресс-синдрома. Результатом этого взаимодействия может стать победа вируса, тогда макроорганизм подключает факторы гуморального иммунитета (местного и общего).
Основу специфического местного иммунитета составляет секреторный IgA. В его синтезе принимают участие клетки реснитчатого эпителия, макрофаги, Т-лимфоциты, клетки секреторного эпителия. Макрофаги, локализованные в пространствах между эпителиальными клетками, захватывают обломки разрушенных вирусом клеток, метаболизируют их. Антигены, подготовленные макрофагами, активизируют Т- и В-лимфоциты, которые превращаются в плазмоциты, продуцируют антитела класса IgA. Выполняя важные эффекторные функции, IgA играет роль молекулы, которая регулирует функции клеток иммунной системы, в частности альвеолярных макрофагов, несущих рецепторы к Fc-фрагменту этого Ig. Так, иммунные комплексы, которые содержат антитела класса А, индуцируют в моноцитах-макрофагах синтез ФНО-а и СЗ-комплемента С. Секреторные IgA связывают вирус и препятствуют его выходу из организма в активной форме, что ограничивает циркуляцию вируса среди людей.
При первой встрече с вирусом через 3-5 дней образуются антитела класса IgM. Повышение их содержания свидетельствует об остроте инфекционного процесса. Высокое содержание Ig в крови является показателем устойчивости организма к инфекции. IgE — единственный тип антител, который вступает во взаимодействие с мембраной тучных клеток (в клинической картине наблюдаются приступы бронхоспазма).
Иммунные механизмы при первичной встрече с вирусом запоминаются организмом в виде информации, заложенной в клетки памяти (иммунологическая память), и при повторной встрече с вирусом той же антигенной разновидности иммунные реакции протекают быстрее и более эффективно. Создание иммунной памяти об антигене является целью применения вакцин. С их помощью создается и поддерживается защитная концентрация противогриппозных антител. Антитела, вступая во взаимосвязь с антигеном, образуют иммунные комплексы. Иногда вместе с защитными функциями они могут стать причиной тяжелых иммунопатологических состояний. Циркулируя по всему организму, они оседают в тканях, вызывая воспалительные реакции в капиллярах клубочков почек и синовиальных оболочек суставов. Частично вирус из организма выделяется почками, что, возможно, и обусловливает тот факт, что в эпителии дистальных канальцев, как и в эндотелии капилляров клубочков, оказывается значительное количество антигена вируса. Почками также выделяются иммунные комплексы, фрагменты клеток, что приводит к сенсибилизации тканей почки и впоследствии, через несколько недель и даже месяцев после перенесенного заболевания, может послужить причиной возникновения гломерулонефрита. Инициатором в этом случае может быть фактор, который имеет антигенную природу (например, переохлаждение).
Находясь в окружении антител, вирус может сохранять свою структуру и при разрушении комплекса опять поражать чувствительные клетки. Длительная циркуляция комплексов приводит к инфицированию все большего количества клеток, к поддержке инфекции и к персистенции. В данное время не исключается возможность длительной персистенции вируса гриппа в ЦНС по типу медленной инфекции с развитием впоследствии такого патологического состояния, как паркинсонизм. Это изменяет представление о гриппе как об острой инфекции. Установлено, что в 50% случаев антиген вируса гриппа сохраняется в периферических лимфоидных клетках и в крови до 120-200 и более дней.
При гриппе роль антигена могут играть не только структура вируса, но и измененные вирусом структуры клеток, и уже к ним синтезируются антитела, с которыми начинают вступать во взаимодействие нормальные клетки, в результате чего возникает угроза развития аутоиммунопатологического состояния.
Изменения во внутренних органах однотипны, обусловлены генерализованной вазодилятациеи. При массивной вирусемии, которая быстро развивается в первые часы болезни, может возникнуть инфекционно-токсический шок с развитием сердечно-сосудистой недостаточности. В его основе лежат несколько факторов: сосудистый (непосредственное действие вируса на сосуды с повышением их проницаемости, вазодилятациеи), геморрагический синдром с повреждением надпочечников и дефицитом гормонов, нарушение функции миокарда. У таких больных смерть может наступить в ближайшие часы от начала заболевания.
В результате токсического повреждения сосудистого аппарата ЦНС наступает гиперсекреция спинномозговой жидкости, нарушается ликвородинамика, что приводит к повышению внутричерепного давления, может наступить отек мозга. Чаще все-таки повреждаются мягкие мозговые оболочки, сосудистое сплетение, где можно выявить антигены вируса гриппа.
Инфекционно-алергический процесс после перенесенной гриппозной инфекции может возникнуть также в эндокарде. Изменения в миокарде, определенные на ЭКГ как миокардиодистрофия, обусловлены токсикозом и циркуляторными расстройствами.
В патогенезе отека легких имеют значение много факторов: нарушения гемодинамики, связанные с токсикозом, воспалительные процессы в бронхах и легких, снижение сократительной функции левого желудочка, что чаще развивается у лиц с сопутствующими заболеваниями сердечно-сосудистой системы. Необходимо подчеркнуть, что начальные стадии отека легких, на которых повреждается интерстициальная ткань, определяются лишь рентгенологически в виде нерезких, расплывчатых теней, которые сливаются и распространяются от корней к периферии легочных полей.
В механизмах устойчивости организма к генетически инородной информации принимают участие два основных феномена: наследственная резистентность и приобретенный иммунитет:
- природная видовая наследственная резистентность, связанная с врожденной стойкостью организма, которая развивается с возрастом, к возбудителям инфекций, основанная на отсутствии чувствительных клеток или повышении их резистентности к репродукции вируса, а также на их биологической инактивации при участии интерферона, фагоцитарных факторов, нормальной температуры тела или неспецифических ингибиторов крови;
- приобретенный иммунитет создается после болезни или искусственной иммунизации вакцинами.
Приобретенный иммунитет опирается на формирование местной секреторной защиты. Секреторный иммунитет предупреждает или смягчает тяжесть заболевания во входных воротах гриппозной инфекции при участии антител класса IgA, которые синтезированы в процессе кооперации между В-лимфоцитами и эпителиальными клетками. Секреторные антитела избирательно адсорбируются на поверхности клеток мерцательного эпителия, эффективно защищая их от инвазии вируса.
Длительность противогриппозного иммунитета ограничена не дву-мя-тремя годами, как это считалось бесспорным до 1977 г. (в этот год особенно тяжело болели молодые люди, рожденные после 1957 г., когда вирус A (H1N1) исчез из циркуляции и появился снова в 1977 г.). В случае возвращения к активной циркуляции уже известного подтипа через 20 и более лет — выявляется сохранение специфической невосприимчивости к возбудителю, который вернулся, у части населения, которая контактировала с ним раньше. Такая длительная иммунологическая память обусловлена, конечно, не антителами (их титры в крови падают ниже защитного порога через 6-12 месяцев, а в секрете дыхательных путей — еще быстрее). Длительный постинфекционный иммунитет обеспечивают клеточные механизмы (Т- и В-лимфоциты), в том числе местные, во входных воротах возбудителя инфекции. Существует четко выраженная корреляция невосприимчивости к гриппу с концентрацией антител в крови (в основном IgG) и в секрете дыхательных путей (IgA). Однако в частных случаях гриппом могут заболеть люди с высоким исходным уровнем гуморального иммунитета и не заболевают инфицированные лица с низким начальным титром антител. Такие примеры подчеркивают сложность и многогранность иммунной защиты организма, где роль отдельных факторов интегрирована в общем результате.
Между специфическими механизмами противогриппозного иммунитета существует распределение защитных функций:
- секреторные антитела, которые подавляют репродукцию вируса во входных воротах инфекции, обеспечивают противоэпидемическую защиту, направленную на ограничение рассеивания и передачи возбудителя от инфицированных лиц здоровому окружению; в связи с широким диапазоном нейтрализующего эффекта секреторные антитела способны подавлять любые антигенные варианты вируса гриппа А в пределах своего подтипа;
- сывороточные антитела нейтрализуют токсичные продукты вируса и регулируют клиническую тяжесть болезни;
- клеточно-обусловленные факторы иммунитета устраняют резервуар вируса в инфицированных клетках, малодоступных влиянию антител.
Напряженность противовирусного иммунитета зависит от уровня циркулирующих антител и образования цитотоксических лимфоцитов. Цитотоксические лимфоциты вызывают лизис инфицированных вирусом клеток.
Повторное заболевание гриппом обусловлено высокой изменчивостью вируса гриппа и формированием иммунитета только к конкретному штамму, что и объясняет необходимость ежегодной вакцинации.
Резервуаром вируса и источником инфекции, как правило, является больной человек, возможно, вирусоноситель. Условия формирования вирусоносительства мало изучены. Известно, что фактором, который способствует персистенции вируса, является иммунодефицитное состояние хозяина. В последние годы не исключается также возможность развития хронической гриппозной инфекции. Последние вспышки гриппа (например, в Гонконге) дают основания предполагать, что возможна передача вируса типа А от животного к человеку.
Эпидемиологическую опасность человека, который инфицирован вирусом гриппа, определяют два фактора: количество вируса в слизи верхних дыхательных путей и выраженность катарального синдрома. Доза вируса, который инфицирует, для человека составляет около 0,0001 мл носоглоточного секрета. В инкубационном периоде вирусы гриппа выделяются в единичных случаях из-за отсутствия катарального синдрома. В разгар заболевания вирусы выделяются достаточно интенсивно. Частое выделение вируса сохраняется и в периоде реконвалесценции после нормализации температуры, что обеспечивается наличием остаточных катаральных явлений в дыхательных путях. Для определения сроков изоляции больных необходимо знать о сроках выделения возбудителя. Так, срок выделения вируса A (H1N1) составляет 21-26 дней, вируса A (H2N2) — 25 дней, A (H3N2) — 22 дня, вируса В — до 30 дней. Описаны случаи выявления вируса через 20-40 и даже 150-180 дней после начала заболевания. Большую эпидемическую опасность представляют больные, которые при заболевании гриппом не остаются дома, а продолжают посещать общественные места. Продолжая вести активный образ жизни, они успевают заразить большое количество людей.
Механизм передачи возбудителя при гриппе — аэрогенный, который реализуется воздушно-капельным, воздушно-пылевым и, реже, бытовым путем передачи, например заражением через предметы быта.
Рис. 2. Рассеивание аэрозольных частиц при чихании

Более мелкие частицы аэрозоля способны проникать в отделы дыхательных путей и вызывать инфицирование. Частицы размером более 30 мкм оседают на слизистой оболочке носа, гортани и трахеи; размером 3-10 мкм — проникают в бронхиолы; 0,3-1 мкм — могут достигать альвеол. Репродукция вирусов происходит с исключительно высокой скоростью: при попадании в верхние дыхательные пути одной вирусной частицы уже через 8 часов количество инфекционного потомства достигает 103, а до конца первых суток — 1023. Высокая скорость размножения вируса гриппа объясняет такой короткий инкубационный период — 1-2 суток. Скорости репродукции вируса способствует распространение многих сотен вирионов, которые подготовлены лишь одной инфицированной клеткой.
Для гриппа свойственным является то, что первая встреча с вирусом гриппа остается в иммунной памяти человека на всю жизнь. Каким бы новым подтипом он и заразился, через много лет первыми в крови появляются антитела не к этому новому вирусу, который вызвал болезнь сегодня, а к тому, который вызывал еще первое заболевание много лет тому назад. Иммунологическая память В-лимфоцитов фиксирует пожизненно все встречи с вирусами гриппа. Но достаточно наименьших изменений в структуре нейраминидазы и (или) гемагглютинина, чтобы вспыхнула болезнь. Против таких новых вирусов анамнестические антитела не срабатывают. Именно этой способностью к изменчивости определяется время эпидемий и пандемий. Об эпидемии говорят тогда, когда одновременно заболевает гриппом большое количество людей в одной стране. Длительность эпидемии гриппа обычно составляет 3-6 недель. За последние годы большинство эпидемий в Украине было не завозного, а эндогенного характера. В случае пандемии грипп будет поражать одновременно большое количество людей в разных странах мира. В этом случае заболевание вызывается новыми серотипами вируса гриппа, к которым восприимчива большая часть населения. Поэтому вирус распространяется с очень высокой скоростью и вызывает заболевание в очень тяжелой форме.
Восприимчивость к гриппу очень высокая у людей всех возрастных групп, но наибольшее количество заболеваний наблюдается у детей в возрасте от 1 до 14 лет (37%), что в четыре раза выше, чем у пожилых (10%). Относительно редкими являются случаи гриппа только среди детей первых месяцев жизни, которые получили пассивный иммунитет от матери, с 6 месяцев дети могут легко инфицироваться гриппом.
Для наблюдения за гриппом в масштабе всей планеты еще в 1947 г. на международной конференции в Копенгагене Всемирная организация здравоохранения (ВОЗ) приняла решение о создании сети лабораторий для изучения гриппа во всех областях земного шара. Учреждениями, которые координируют проведение исследовательских работ, стали Всемирный центр гриппа в Лондоне и соответствующая лаборатория в США. В России функции национального центра по гриппу выполняет Научно-исследовательский институт гриппа Российской академии медицинских наук, руководимый академиком РАМН, профессором О. И. Киселевым.
План заключался в том, чтобы лаборатории разных стран выделяли вирусы и пересылали их в Лондонский центр или другие центральные лаборатории для сравнительного изучения. В свою очередь, центры должны поставлять региональным лабораториям информацию и образцы новых выделенных вирусов гриппа. В данное время по программе ВОЗ в наблюдении за гриппом принимают участие ПО национальных лабораторий в 79 странах, задачей которых является выделение вируса гриппа от больных, предварительная характеристика изолятов и их передача в один из центров, что сотрудничает с ВОЗ, для более детального исследования. Такая система наблюдения за гриппом обеспечивает центральные лаборатории ВОЗ штаммами вируса гриппа для изучения эволюции этого возбудителя в масштабах всей планеты, а также позволяет осуществлять выбор штаммов для современных вакцин.
Гриппу подвержены все возрастные группы. В 2002 г. в России зарегистрировали 1 млн 719 тыс. 106 случаев гриппа (1 190,6 случаев на 100 000 человек), что в структуре инфекционных заболеваний составило 6,2% [2]. Дети болеют гриппом в 4,6 раза чаще, чем взрослые. Пик заболеваемости в детском возрасте отмечен в группе 7–14-летних. Смертность от гриппа и его осложнений занимает первое место в структуре смертности среди всех инфекционных и паразитарных заболеваний.
Во время эпидемий частота госпитализаций по поводу гриппа и его осложнений среди пациентов моложе 65 лет с одним и более сопутствующим заболеванием составляет 56–63,5 случая на 100 000 человек, а у пациентов без сопутствующей патологии — 13–60 случаев на 100 000 человек [3]. В структуре смертности ведущее место занимают пациенты старше 65 лет — 80–90%, тогда как смертность среди пациентов 45–64 лет без сопутствующей патологии составляет примерно 2 случая на 100 000 человек [4].
Вирусология. Вирус гриппа относится к семейству ортомиксовирусов. Выделяют, в зависимости от содержания отдельных протеинов, три серологических типа вируса: А, В и С. При электронной микроскопии вирус выглядит как сферическая частица с располагающимися на поверхности гликопротеинами: гемагглютинином (Н) и нейраминидазой (N) [5].
Природным резервуаром вируса гриппа А являются птицы, редко — животные. Вирус гриппа В встречается только у людей, вирус гриппа С — у людей, свиней и, возможно, собак. Периодические пандемии и частые эпидемии, ассоциированные с высокой заболеваемостью и смертностью, связывают с вирусом гриппа А, реже — с вирусом гриппа В, а грипп С, как правило, протекает в инаппарантной (бессимптомной) форме и почти не влияет на уровень заболеваемости [1].
С учетом антигенных различий поверхностных гликопротеинов вирус гриппа А подразделяется на подтипы. Различают 15 подтипов гемагглютининов (Н1–Н15) и 9 подтипов нейраминидаз (N1–N9). Каждое изменение антигенной структуры поверхностных гликопротеинов в результате мутаций вируса вызывает развитие новых пандемий и эпидемий. Существенная группа антигенных разновидностей вируса гриппа А (Н5 и Н7) циркулирует только в пределах природного резервуара, вызывая заболевание исключительно у птиц и, в редких случаях, у свиней. Наибольшую проблему в последние годы представляют те вирусы, которые смогли преодолеть межвидовой барьер вследствие мутаций с образованием новых, высокопатогенных, подтипов.
В зависимости от степени генных изменений выделяют антигенный дрейф (drift) и антигенную трансформацию (shift) [1].
Антигенный дрейф представляет собой генные мутации в виде перемещений участков генома внутри одного подтипа вируса А или В. Изменяются гены, кодирующие поверхностные гликопротеины (чаще Н). Антигенная природа вируса меняется. В результате один и тот же подтип вируса распознается иммунной системой человека как новый. С антигенным дрейфом связывают вспышки заболеваемости в межпандемический период.
Антигенная трансформация состоит в перемещении генных участков между геномами двух разных подтипов вируса гриппа А (причем не только между человеческими подтипами, но также между птичьим и человеческим). Антигенная трансформация вызывает значительные изменения Н и, возможно, N. С антигенной трансформацией связывают развитие пандемий гриппа А.
N, в свою очередь, облегчает высвобождение вирусных частиц с поверхности инфицированных клеток и предотвращает их слипание. В силу способности N расщеплять сиаловую кислоту терминальных участков протеинов, находящихся на поверхности эпителиальных клеток, а также содержащихся в N и Н вновь синтезированных вирусных частиц, вирус распространяется в организме. Если же N ингибирована (медикаментозно) или разрушена (например, у чувствительных штаммов при изменении температуры), то вновь синтезированные вирусные частицы слипаются, образуя крупные агрегаты на поверхности эпителиальных клеток, и распространение инфекции прекращается [1]. N облегчает продвижение вируса через мукополисахаридный слой, выстилающий эпителий верхних дыхательных путей. Кроме тогo, изменения N при антигенном дрейфе способствуют выживаемости вируса, защищая его от распознавания иммунной системой макроорганизма.
Репликация вируса происходит в эпителиальных клетках респираторного тракта. Цикл репликации составляет 4–6 ч. После этого вирусные частицы высвобождаются с поверхности эпителиальных клеток и инфицируют близлежащие клетки. Таким образом, за короткий период многие клетки эпителия верхних дыхательных путей оказываются пораженными, высвобождая вирус или погибая.
В присутствии рибонуклеиновой кислоты (РНК) вируса лейкоциты вырабатывают интерфероны, способные блокировать репликацию вируса. Однако вирус гриппа противостоит этому защитному механизму вследствие наличия NS1-протеина. Последний частично нарушает синтез белка в клетке макроорганизма путем блокирования транспорта матричной РНК из ядра, в результате чего снижается выработка интерферона [8]. На основе этих данных, используя генно-инженерные методы, можно создать культуру вируса, в которой бы отсутствовал эффекторный участок NS1-протеина, а значит создать и новый тип вакцины.
Исследования выделенного в 1997 г. вируса А (H5N1) показали наличие ряда факторов, которые делают вирус высоковирулентным. К ним относятся измененный H, облегчающий слияние вирусной оболочки с клеточной мембраной, а также специфические протеины, пролонгирующие репликацию вируса и повышающие его резистентность к компонентам противовирусного иммунитета (интерферону, фактору некроза опухоли a, макрофагам и др.) [10]. Однако относительно низкая заболеваемость у людей, несмотря на широко распространенные контакты с больной домашней птицей, свидетельствует о достаточно высокой прочности межвидового барьера.
Эпидемиология. Инфицирование происходит при вдыхании микрокапель секрета дыхательных путей, образующихся при кашле или сморкании. Цикл репликации длится 4–6 ч. Выделение вируса из дыхательных путей инфицированного человека начинается за 1–2 дня до появления симптомов и прекращается через 5–7 дней после исчезновения клинических проявлений болезни. Эти сроки могут увеличиваться у детей и пациентов с иммуносупрессией.
Высокая вирулентность, короткий инкубационный период, массивное выделение с назофарингеальным секретом способствуют быстрому распространению вируса гриппа, особенно в изолированных группах людей. Так, например, грипп является важной причиной внутрибольничных вспышек, увеличивая заболеваемость и смертность в отделениях интенсивной терапии, неонатальных и гериатрических отделениях.
Заболеваемость гриппом носит четкий сезонный характер, что может быть связано с несколькими причинами: скоплением людей в закрытых помещениях в плохую погоду, учебными занятиями в школах и институтах с начала осени до конца весны и, возможно, лучшей выживаемостью вируса в аэрозоле в зимние месяцы. Вспышки гриппа совпадают с повышением заболеваемости другими респираторными инфекциями, вызываемыми, в частности, респираторным синцитиальным вирусом, коронавирусом, риновирусом, аденовирусом. Летом вспышки гриппа наблюдаются в Южном полушарии, зимой — в Северном.
Короткие вспышки инфекции обычно начинаются внезапно и длятся 5–6 нед. Число заболевших быстро растет, достигая максимума и сохраняясь на этом уровне 2–3 нед, а затем идет на убыль. При уровне еженедельной заболеваемости более 100 случаев на 100 000 человек констатируются эпидемии гриппа [13], продолжительность которых может достигать 3 мес. Высок риск заболеть у детей до 1 года, лиц старше 65 лет, имеющих сопутствующие заболевания (сердечно-сосудистые и хронические легочные заболевания, сахарный диабет, почечная недостаточность, неврологические расстройства, иммуносупрессии), а также у беременных [14].
С 1948 г. активность вируса гриппа ежегодно оценивается национальными отделениями ВОЗ по изучению этой инфекции более чем в 80 странах. Определяются время и место циркуляции тех или иных подтипов вируса, степень их активности и особенности течения вызванной ими инфекции, изучаются новые антигенные варианты вируса. На основании этих данных специальное подразделение ВОЗ (WHO Collaborating Center for Reference and Research on Influenza at CDC) дает рекомендации по профилактике, лечению и ограничению распространения гриппа в предстоящем сезоне. В феврале каждого года ВОЗ рекомендует соответствующие штаммы вируса для включения в вакцину на следующий сезон в Северном полушарии. Так, на 2007–2008 гг. эксперты ВОЗ рекомендуют такие штаммы: A/Solomon Islands/3/2006 (H1N1), A/Wisconsin/67/2005 (H3N2) и B/Malaysia/2506/2004 [15].
Клинические проявления. Клиническая картина гриппозной инфекции включает широкий спектр проявлений — от бессимптомного течения до развития вторичной бактериальной или первичной вирусной пневмонии и полиорганных осложнений. Это зависит от возраста, иммунного статуса, наличия сопутствующей патологии, беременности (у женщин детородного возраста) [1, 16, 17].
Инкубационный период продолжается 1–4 дня (в среднем 2 дня). При гриппе А (H5N1) инкубационный период может увеличиваться до 8 дней. Пациенты могут быть заразны для окружающих за 1 день до появления клинических симптомов и до 5 дней после их исчезновения. Дети могут быть заразны более длительное время.
Неосложненный грипп у взрослых. Характерны острое начало таких системных и респираторных проявлений, как лихорадка, головная боль, озноб, суставная и мышечная боли, анорексия, саднение в горле, непродуктивный кашель, ринит со слизистыми выделениями. Лихорадка до 38–40 °С — наиболее частый системный симптом — может длиться от 1 до 5 дней. Разрешение симптомов наступает обычно через 3–5 дней, хотя слабость и кашель могут сохраняться в течение 2 нед после нормализации температуры тела. Для дебюта гриппа А (H5N1) более характерны диарея, рвота, абдоминальная и плевральная боли, носовые и десневые кровотечения (иногда даже при отсутствии респираторных проявлений).
Грипп у детей. Обычно клинические проявления гриппа у детей схожи с таковыми у взрослых, но наблюдаются и некоторые возрастные особенности. Так, например, сонливость встречается у каждого второго болеющего ребенка в возрасте до 4 лет. Высокая лихорадка — признак, отмечаемый более часто у детей, нежели у взрослых. На высоте лихорадки у детей могут возникать судороги (фебрильные судороги). Гастроинтестинальные расстройства — тошнота, рвота, боли в животе, диарея — встречаются у 40% детей, причем в некоторых случаях симптомы могут быть столь выраженными, что симулируют аппендицит. Миалгии (чаще — боли в ногах и спине) возникают в ранние сроки болезни. Миозит — нечастое осложнение (чаще всего гриппа В), возникающее в период реконвалесценции; проявляется болями и слабостью в ногах, может сопровождаться миоглобинурией (с нарушением функции почек или без такового), длится 1–5 дней.
Частота госпитализаций у детей в период эпидемий гриппа колеблется в зависимости от возраста и наличия факторов риска. У детей 0–4 лет частота госпитализаций составляет 100–500 на 100 000, достигая максимума в возрастной группе 0–6 мес — до 1040 на 100 000 [18].
Грипп у пожилых. Если учитывать распространенность сопутствующих заболеваний, то пожилые люди составляют группу высокого риска развития осложнений гриппа. Частота госпитализаций по поводу обострения/декомпенсации сопутствующих заболеваний у лиц старше 65 лет в период эпидемий гриппа составляет 200–1000 на 100 000 [19].
При гриппе у пациентов пожилого и старческого возраста чаще, чем у молодых, поражаются нижние отделы дыхательного тракта, что клинически проявляется экспекторацией мокроты, свистящими хрипами или болями в грудной клетке.
Осложнения со стороны органов дыхания. Наиболее частые респираторные осложнения гриппа включают острый бронхит, ларинготрахеобронхит, бронхиолит, пневмонию, абсцесс легкого, эмпиему плевры, пневмоторакс, обострение хронического бронхита/хронической обструктивной болезни легких, бронхиальной астмы и муковисцидоза.
Пневмония развивается у 5–38% пациентов с гриппом А и у 10% с гриппом В [1]. Различают первичную вирусную пневмонию (в результате непосредственного вирусного поражения легких) и вторичную бактериальную пневмонию (она может сочетаться с первичной вирусной или быть самостоятельным поздним осложнением гриппа).
Другие респираторные осложнения гриппа [1, 20]:
- острый средний отит;
- обострение фиброзирующего альвеолита (вирусная инфекция верхних дыхательных путей и развитие вторичной бактериальной инфекции вызывает прогрессирование заболевания);
- абсцесс легкого;
- эмпиема плевры;
- инвазивный легочный аспергиллез.
Нереспираторные осложнения. Вирус гриппа редко обнаруживается за пределами бронхолегочной системы, и развитие нереспираторных осложнений обычно связывается с патоиммунными механизмами, а не с непосредственным цитопатическим действием вируса.
Синдром Рейе. Синдром острой энцефалопатии и жировой инфильтрации внутренних органов развивается у детей и подростков 2–18 лет. В этом случае через 5–6 дней после начала вирусной инфекции появляется неукротимая рвота, сопровождающаяся внезапным изменением психического статуса. Прием салицилатов во время гриппозной инфекции увеличивает риск развития синдрома Рейе.
Осложнения со стороны сердечно-сосудистой системы. Изменения электрокардиограммы без клинических проявлений встречаются у 81% госпитализированных больных с гриппом и y 43% амбулаторных больных [1]. Чаще всего эти изменения не сопровождаются клиническими проявлениями и продолжаются короткое время (до 24 ч), реже — месяцы и годы. Иногда у пациентов с латентно протекающей сердечной патологией переносимая гриппозная инфекция является провоцирующим фактором для развития тяжелых нарушений ритма или рестриктивной кардиомиопатии. Миокардит — характерное осложнение гриппа — протекает, как правило, бессимптомно. Грипп часто вызывает ухудшение течения уже имеющихся у пациентов сердечно-сосудистых заболеваний, и прежде всего сердечной недостаточности.
Сахарный диабет. Больные сахарным диабетом 2 типа умирают от гриппа и пневмонии в 1,7 раз чаще, чем в популяции. Во время эпидемий гриппа А в 1968–1970 и 1972–1973 гг. смертность среди пациентов только с сердечно-сосудистыми заболеваниями составила 104 на 100 000, а среди пациентов с сердечно-сосудистыми заболеваниями и диабетом — 481 на 100 000 человек [1].
Другие нереспираторные осложнения:
- неврологические расстройства (фебрильные судороги, токсическая энцефалопатия, вирусный энцефалит, иммунный параинфекционный энцефалит);
- бактериальный менингит;
- цереброваскулярные заболевания;
- психические расстройства.
Поражения нижних дыхательных путей, встречающиеся у большинства пациентов, проявляются уже в ранние сроки заболевания. В среднем на 6-е сутки появляются одышка, продукция мокроты, выслушивается инспираторная крепитация. Почти у всех пациентов диагностируется пневмония. Ограниченные микробиологические данные свидетельствуют о первичном вирусном характере воспаления легких. Рентгенологические симптомы разнообразны и включают диффузные, многофокусные или локальные инфильтраты (сегментарные или дольковые), а также интерстициальную инфильтрацию. Плевральный выпот не является характерным.
Часто инфекция приобретает прогрессирующее течение с развитием острого респираторного дистресс-синдрома, полиорганной недостаточности с поражением почек и сердца. Реже развиваются другие тяжелые осложнения: вентилятор-ассоциированная пневмония, легочное кровотечение, пневмоторакс, панцитопения, синдром Рейе.
Большинство госпитализированных пациентов уже в ранние сроки нуждались в респираторной поддержке. В некоторых случаях требовалось проведение интенсивных мероприятий в связи с выраженной гипотензией и развивающейся полиорганной недостаточностью.
Продолжение читайте в следующем номере.
По вопросам литературы обращайтесь в редакцию.
А. И. Синопальников, доктор медицинских наук, профессор
Ю. Г. Белоцерковская
ГИУВ МО РФ, Москва
Читайте также:

