Грипп после пересадки почки
Обновлено: 25.04.2024
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение хирургии пороков сердца Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. акад. Б.В. Петровского, Москва
Лаборатория клинической биохимии Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Вакцинация пациентов с хронической почечной недостаточностью в пред- и посттрансплантационном периоде
Журнал: Терапевтический архив. 2015;87(12): 32‑35
Резюме Цель исследования. Выяснить, провоцирует ли вакцинация развитие отторжения трансплантированной почки. Материалы и методы. 92 больным с хронической почечной недостаточностью — ХПН до и после пересадки почки выполнено 131 введение вакцин: 7 больным вакцины вводили до трансплантации почки, 85 — в различные сроки после трансплантации почки. Для обследования больных использованы пункционная биопсия трансплантата, измерение уровня протеинурии, оценка динамики уровня креатинина в крови и скорости клубочковой фильтрации. Результаты. Выявлено, что вакцинация не провоцирует развитие отторжения, о чем свидетельствовали результаты пункционной биопсии аллопочек и исследование их функции. Заключение. Вакцинация безопасна для больных с ХПН, так как не вызывает развитие эпизодов отторжение.
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение трансплантации почки Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. акад. Б.В. Петровского РАМН, Москва
Отделение хирургии пороков сердца Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
Российский научный центр хирургии им. акад. Б.В. Петровского, Москва
Лаборатория клинической биохимии Российского научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
ПБТ — пункционная биопсия трансплантата
СКФ — скорость клубочковой фильтрации
ХТН — хроническая трансплантационная нефропатия
Кандидаты на трансплантацию и реципиенты трансплантированных органов входят в группу повышенного риска развития инфекционных осложнений. Иммунодепрессивная терапия подвергает этих пациентов более высокому риску развития инфекционных заболеваний. Вакцинация может предупредить развитие указанных заболеваний и снизить репликацию и диссеминацию этих микроорганизмов. Следовательно, рекомендуется специфическая вакцинация, включающая пневмококки, вирусы гриппа, гепатита, А и В и столбняк/дифтерию. В исключительных случаях показана вакцинация против столбняка, дифтерии и гемофильной палочки типа В.
Однако эффективность, безопасность и протоколы введения некоторых вакцин у пациентов данной популяции мало изучены. В силу того, что иммунодепрессия имеет нескольких протоколов, возникает ряд вопросов: 1) каково воздействие иммунодепрессии на продолжительность предтрансплантацинной вакцинации, проводимой как на ранней, так и в терминальной стадии заболевания; 2) эффективны ли вакцинации, проводимые как в раннем, так и отдаленном посттрансплантационном периоде; 3) каковы побочные действия живых и инактивированных вакцин у пациентов на фоне иммунодепрессии и каково воздействие таких вакцин на функцию пересаженной почки. Но главным остается вопрос, не спровоцирует ли вакцинация развитие отторжения, приведя, таким образом, к гибели пересаженной почками [1—4]. Именно поэтому мы сосредоточили основное внимание на данном аспекте проблемы.
Материалы и методы
В отделении трансплантации почки РНЦХ им. акад. Б.В. Петровского РАМН вакцинацию начали проводить с сентября 2010 г. За период с сентября 2010 по февраль 2011 г. 92 больным выполнено 131 введение вакцины, из них 64 больным однократно, 28 больным проведены 62 вакцинации: 1 пациентке — 4 раза, 5 больным — 3 раза; 22 — 2 раза. Возраст больных от 2 до 67 лет (в среднем 22,8±15,2 года). Мужчин было 54, женщин — 38, детей — 43, взрослых — 49.
Во всем мире принято считать, что оптимальный период для вакцинации — предтрансплантационный не только потому, что введение вакцины реципиентам аллотрансплантированных органов чревато развитием отторжения [5, 6], но и в связи с тем, что иммуносупрессия препятствует работе вакцины. В связи со сложившейся ситуацией вакцинированы за 0,4—12 мес (в среднем 2,78±3,85 мес) до трансплантации почки только 7 (6,52%) больных (1-я группа), остальные 85 (93,48%) вакцинированы в различные сроки после пересадки почки (от 0,8 до 144 мес, в среднем 35,13±29,14 мес): 57 больных — однократно (2-я группа) и 28 — неоднократно (3-я группа). Возраст больных, у которых вакцинация проводилась в посттрансплантационном периоде, составил от 2 до 69 лет (в среднем 22,6±15,2 года). Показанием к вакцинации служила профилактика таких инфекционных осложнений, как гепатит, А и В, пневмококковая инфекция, грипп и др.
В 1-ю группу вошли 7 пациентов в возрасте от 3 до 40 лет (в среднем 15,7±13,4 года; всего 3 пациента женского пола, 4 мужского, 6 из 7 в возрасте от 2 до 19 лет). Проводилась вакцинация в сроки за 0,2—12 мес до трансплантации (в среднем 2,78±3,85 мес). У 2 пациентов вакцинация проведена 2 раза с интервалом между введениями 7 и 14 дней. Одному больному введена противогриппозная вакцина, а через 7 дней — пентаксим и пневмо23, другому больному 3 раза введена сыворотка против гепатита В, а через 2 нед — пневмо23. Четверым больным вакцинация проведена в виде однократной инъекции, при которой каждому пациенту введено по одной вакцине (ваксигрипп, пентаксим и церварикс); одному пациенту последовательно ввели пентаксим, затем пневмо23.
Однократная вакцинация в посттрансплантационном периоде выполнена 57 больным (2-я группа) в сроки от 0,82 до 144 мес после трансплантации (в среднем 36,4±33,7 мес). У всех больных перед вакцинацией оценивали уровень креатинина в крови, скорость клубочковой фильтрации (СКФ), суточную экскрецию белка с мочой. Затем эти же параметры оценивали через 2—4 и 6—8 нед после вакцинации (см. рисунок, а). Кроме того, у 16 больных проведена сравнительная оценка результатов пункционной биопсии трансплантатов (ПБТ) до и после вакцинации. Оценку биоптатов по Banff проводили количественно по 10 морфологическим параметрам, степень выраженности которых оценивали по шкале от 0 до 3 баллов. Сумма оценок тех или иных параметров (если они больше 1 балла) отражает степень выраженности процесса в нем от 0 (норма) до 9—11 баллов (острое отторжение 2b).

Динамика показателей функции аллотрансплантированных почек до и после однократной вакцинации (а) и неоднократных вакцинаций (б).
В 3-й группе у 28 пациентов вакцинация проводилась многократно, число введений вакцины варьировало от 2 до 6 (в среднем 3,44±1,39). Использовали такие же вакцины, как и у пациентов 1-й и 2-й групп. Оценку функции трансплантированных почек проводили по тому же принципу, что и у больных 2-й группы (см. рисунок, б).
Результаты и обсуждение
В 1-й группе побочные действия вакцин наблюдали только у больного, которому вводили пентаксим и пневмо23, — развилась гипертермия до 37,5 °С с ознобом. Перечисленные явления купированы введением антигистаминных препаратов. У остальных больных побочных явлений не было. У 3 больных данной группы выполнены ПБТ. Во всех случаях отторжение отсутствовало. При оценке функции трансплантированной почки уровень креатинина в крови колебался от 0,5 до 1,8 мг% (в среднем 1,00±0,46 мг%), СКФ составляла 22,4—148,8 мл/мин (в среднем 63,18±48,38 мл/мин). Можно считать, что функция трансплантированной почки во всех случаях была удовлетворительной.
Небольшое число больных, которых вакцинировали в предтрансплантационном периоде, не дает нам права делать основополагающие выводы, но с их помощью наглядно показано, что проведенная вакцинация не спровоцировала иммунный конфликт между донорским органом и реципиентом, а также не оказала отрицательного влияния на состоянии аллотрансплантированной почки.
Во 2-й группе после вакцинации отрицательной динамики показателей функции аллотрансплантированной почки не наблюдалось. При сравнительной оценке результатов ПБТ до и после вакцинации отрицательная динамика не выявлена (табл. 1). Это дает основание утверждать, что вакцинация не провоцирует развитие криза отторжения и не оказывает отрицательного воздействия на функцию пересаженной почки.

Таблица 1. Сравнительная оценка результатов ПБТ до и после вакцинации Примечание. ХТН — хроническая трансплантационная нефропатия.
Статистическая обработка данных показала, что математическая разница между данными до и после вакцинации статистически недостоверная (t=0,52; p>0,1). Следовательно, это служит еще одним подтверждением тому, что однократная посттрансплантационная вакцинация не провоцирует развитие отторжения.
У пациентов 3-й группы на протяжении всего периода исследования функция трансплантированных почек не ухудшилась (см. рисунок, б). На основании этого можно сделать вывод, что и многократные вакцинации не ухудшают функцию аллотрансплантированных почек.
ПБТ в поствакцинальном периоде выполнена только у 6 пациентов 3-й группы (табл. 2). При этом не у кого из них не отмечено отрицательной динамики морфологии аллогенных почек. Однако недостаточное число больных, которым выполнена ПБТ после вакцинации, не дает нам право делать выводы по всей группе в целом.

Таблица 2. Сравнительная оценка результатов ПБТ до и после вакцинации
Протокол вакцинации и побочные действия вакцин. Наш опыт проведения вакцинаций реципиентов трансплантированных почек дает основание считать внутримышечный способ введения вакцин оптимальным. Мы не всегда имели возможность соблюдать протокол 0—1—6 мес, поскольку у определенного процента больных с момента первого введения вакцины до момента написания данной работы прошло не более 4 мес. Кроме того, не был соблюден протокол и у тех больных, для которых мы были вынуждены ограничиться однократным введением.
Подобно любому биологически активному препарату вакцины могут вызывать различные побочные реакции как местного, так и общего характера.
Из местных реакций мы наблюдали у 9 (9,8%) из 92 больных болезненность в месте инъекции, гиперемию, отечность, гиперемию в области инъекции у 2 (2,2%), инфильтрат в области введения вакцины у 1 (1,1%). Из общих явлений отмечена только головная боль у 2 (2,2%) больных. Таким образом, можно утверждать, что вакцинация у наших пациентов прошла без серьезных последствий и ее можно считать безопасной.
Выживаемость в группе вакцинированных пациентов. На момент написания данной работы все вакцинированные пациенты живы, ни одной трансплантированной почки не потеряно. Анализ уровня креатинина в крови, его клиренса и суточной экскреции белка с мочой представлен на рисунке, в. На протяжении всего поствакцинального периода ухудшения функции аллотрансплантированных почек не наступило. Следовательно, проведение вакцинации реципиентам трансплантированных почек не вызывает у них развития отторжения пересаженных органов. Это может быть связано с тем, что нами использованы только импортные вакцины. Выбор именно импортных вакцин обусловлен тем, что в их состав не входят полиоксидоний и интерферон, оказывающие выраженное иммуностимулирующее действие.
Несмотря на очевидность того, что вакцинация безопасна и эффективна у пациентов, получающих иммунодепрессию, большинство вакцин у больных данной категории используются недостаточно [7]. Следует придерживаться следующих принципов при иммунизации реципиентов трансплантированных органов: 1) эффективность вакцинации, измеренная путем определения титра антител, обычно снижена по сравнению с таковой у здоровых лиц; 2) эффективный противоинфекционный иммунитет может исчезнуть раньше, чем у здоровых людей; 3) профили безопасности модифицированы и специфические осложнения такие, как отторжение и дисфункция трансплантата, существуют по крайней мере теоретически; 4) живые ослабленные вакцины обычно противопоказаны; 5) иммунная реакция лучше, когда вакцинация начата до начала иммунодепрессивной терапии.
Заключение
Таким образом, реципиентам трансплантированных органов проведение вакцинации полезно исходя из общепринятой практики иммунизации. У пациентов этой группы следует использовать инактивированные вакцины, так как их побочные влияния минимальны и ограничены.
Рекомендовано продолжение исследований для улучшения имеющихся протоколов для данной популяции больных, так как большинство исследований проводится с ограниченным числом пациентов.
Инфекции после трансплантации почки ребенку
Инфекции остаются важнейшей причиной заболеваемости и смертности у больных с пересаженными почками.
1. Бактериальные инфекции после трансплантации почки. Чаще всего встречаются пневмония и инфекции мочевых путей. Последние могут быстро переходить в уросепсис и иногда бывают ошибочно приняты за острое отторжение трансплантата.
2. Вирусные инфекции после трансплантации почки. Особую опасность представляют герпесвирусы (цитомегаловирус, вирус простого герпеса, вирус varicella-zoster и вирус Эпштейна—Барр). У детей младшего возраста первый контакт с этими вирусами часто бывает уже после трансплантации почки, и тогда первичная инфекция на фоне иммунодепрессантов может протекать у них очень тяжело.
Частота этих заболеваний существенно возрастает после лечения антилимфоцитарными препаратами или пульс-терапии большими дозами глюкокортикоидов. В таких случаях показана профилактика герпесвирусных инфекций.
а) Цитомегаловирус. Цитомегаловирусная инфекция может протекать в виде носительства (вирус персистирует в лимфоидной ткани). Серологические пробы на цитомегаловирус положительны приблизительно у 30% детей старше 5 лет и у 60% подростков. Следовательно, чем младше ребенок, тем выше риск первичной цитомегаловирусной инфекции при трансплантации почки от инфицированного донора.
Она может проявляться лихорадкой, лейкопенией, тромбоцитопенией, пневмонией, язвами ЖКТ, гепатитом, гломерулопатией и почечной недостаточностью, острым отторжением трансплантата и подавлением иммунитета. Установлена связь между цитомегаловирусной инфекцией и хроническим отторжением при трансплантации любых органов. Для лечения и профилактики применяют иммуноглобулин против цитомегаловируса, нормальный иммуноглобулин для в/в введения в высоких дозах и противовирусные препараты — ацикловир, валацикловир, ганцикловир и валганцикловир.
Профилактическое лечение ганцикловиром показано серонегативным реципиентам почки от серопозитивного донора.
б) Вирус varicella-zoster. У детей старшего возраста, перенесших трансплантацию почки, вирус varicella-zoster чаще всего вызывает опоясывающий лишай — локальные пузырьковые высыпания в пределах одного дерматома. У детей младшего возраста возможна быстропрогрессирующая тяжелейшая инфекция с энцефалитом, пневмонией, печеночной недостаточностью, панкреатитом и ДВС-синдромом.
Серонегативным детям в течение 72 ч с момента случайного контакта с больным необходимо ввести иммуноглобулин против вируса varicella-zoster, в 75% случаев это существенно облегчает протекание инфекции. До трансплантации ребенка следует вакцинировать против вируса varicella-zoster. При появлении ветряночной сыпи у ребенка с пересаженной почкой необходимо немедленно ввести ацикловир парентерально. Опоясывающий лишай менее склонен к диссеминации, но ацикловир все же показан.
в) Вирус Эпштейна—Барр. Примерно 50% детей серонегативны в отношении вируса Эпштейна— Барр, и приблизительно 75% из них после трансплантации почки инфицируются. Инфекция вирусом Эпштейна—Барр даже на фоне иммунодепрессантов в большинстве случаев протекает бессимптомно. В то же время у 0,5—2% детей после трансплантации почки возникает лимфопролиферативный синдром, часто обусловленный инфекцией вирусом Эпштейна—Барр на фоне интенсивной иммуносупрессивной терапии.
Он может проявляться лихорадкой, потерей веса, гепатоспленомегалией, поносом, увеличением лимфоузлов, а при поражении ЦНС — неврологической симптоматикой. Лечение включает резкое снижение доз иммунодепрессантов, а при наличии очагов высокой степени злокачественности — химиотерапию и антилимфоцитарные средства.
г) Вирус простого герпеса. Типичные герпетические изъязвления около рта при применении иммунодепрессантов встречаются часто и обычно излечиваются при приеме ацикловира внутрь.
3. Пневмоцистная пневмония после трансплантации почки. Для профилактики пневмоцистной пневмонии после трансплантации показан 3—6-месячный курс триметоприма/сульфаметоксазола.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Осложнения трансплантации почек. Последствия иммуносупрессии
Самой частой причиной смерти в течение первого года после трансплантации является инфекция, особенно цитомегаловирусная. Определение титра антицитомегаловирусных антител должно входить в обязательную программу обследования донора и реципиента. ЦМВ-инфекция может быть как первичной (т. е. передаваться реципиенту с трансплантированной почкой или компонентами крови), так и связанной с реактивацией вируса у реципиента с положительными результатами серологических проб вследствие иммуносупрессивной терапии. В последнем случае заболевание проявляется через 1-3 мес. После трансплантации.
Иммуносупрессия остается необходимым условием трансплантации. К сожалению, применение иммунодепрессантов может вызывать репликацию вируса Эпштейна-Барр с развитием потенциально смертельного посттрансплантационного лимфопролиферативного заболевания в 1-2 % случаев. В 2001 г. в Северной Америке это наблюдалось у 121 из 7545 детей, которым с 1987 по 2000 г. проводилась трансплантация почки (1,7 %). Однако обследование на ВИЧ-инфекцию не проводилось. По данным одного французского центра, посттрансплантационное лимфопролиферативное заболевание наблюдалось у 16 из 1420 взрослых больных, не инфицированных ВИЧ (1,1 %; средний возраст — 45,5 года (27-64 лет)). Лимфопролиферативный процесс у маленьких детей в течение первого года после трансплантации остается основной причиной тяжелой заболеваемости и смертности.
Его необходимо диагностировать по возможности раньше, обращая пристальное внимание на лихорадку, лимфаденопатию, симптомы со стороны ЖКТ (объемные образования в животе, кровотечения, боль, непроходимость, перфорация, асцит), судороги и другие нарушения ЦНС, а также бессимптомные объемные образования в грудной клетке и средостении у перенесших трансплантацию больных. Помимо клинического обследования требуются биопсия тканей и все возможные лабораторные исследования: определение РНК вируса Эпштейна-Барр и ЦМВ в крови (с помощью ПЦР и саузерн-блоттинга), а также определение скрытой экспрессии мембранного белка 1 на парафиновых или замороженных тканевых срезах.
Лимфопролиферативное заболевание, возникшее менее чем через 1 год после трансплантации, обычно имеет более благоприятный прогноз и при снижении доз или отмене иммунодепрессантов может регрессировать. Из упомянутых выше 16 больных с тяжелым лимфопролиферативным заболеванием в поздние сроки после трансплантации 11 получали полную химиотерапию (протокол CHOP: циклофосфамид, доксорубицин, винкристин и преднизолон), у 6 пациентов наблюдалась полная и постоянная ремиссия. Лечение по этому протоколу не оказывало нефротоксического действия, и в тех случаях, когда после противоопухолевой терапии приходилось кратковременно снижать дозы или отменять иммунодепрессанты, реакция отторжения трансплантата не развивалась.
Улучшение прогноза для ВИЧ-инфицированных больных (в результате создания средств эффективной специфической терапии) позволяет рассматривать возможность трансплантации почки и им. Однако это требует соблюдение определенных условий. В течение 2 лет до трансплантации у ВИЧ-инфицированного больного не должно быть никаких оппортунистических инфеккций, его состояние должно быть стабильным, и должен хорошо переносить специфическую терапию. Обязательные условия включают также строгое соблюдение врачебных рекомендаций, отсутствие вирусной РНК в крови, достаточное колиство СD4-лимфоцитов и отсутствие осложнений.
Возобновление патологии клубочков в трансплантированной почке. В трансплантате возможны любые рекуррентные гломерулопатии, и в 5-10 % случаев потеря аллотранплантатов происходит именно по этой причине, наиболее часто, по-видимому, возобновляется фокально-сегментарный гломерулосклероз — с трудом поддающееся лечению заболевание, механизм развития которого остается неизвестным.
Гемолитико-уремический синдром (ГУС) не возобновляется, но может быть возникать de novo. В 1-3 % случаев его причиной является семейный вариант неинфекционного ГУС (вероято, наследственный), в остальных — использование ингибиторов кальциневрина (циклоспорина и др.). Однако зто более характерно для транспланции костного мозга, чем почки. Факторами риска неинфекционного ГУС после трансплантации почки является семейное заболевание (аутосомно-доминантное или рецессивное наследование), проведение трансплантации ранее 0,5-1 года после полной ремиссии заболевания у реципиента и использование циклоспорина (если этот синдром развился при предыдущей трансплантации, то рекомендуется применять лишь низкие дозы циклоспорина).
Известны также случаи de novo развития этого синдрома после трансплантации почки от живых родственников с семейным нарушением синтеза простациклина, после приема оральных контрацептивов и при посттрансплантационном лечении антилимфоцитарным иммуноглобулином.
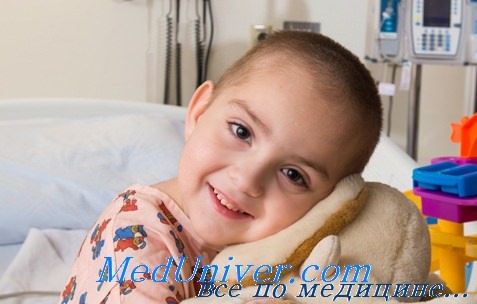
Техника трансплантации почки. Осложнения трансплантации почки
При гетеротопической пересадке почки в правую или левую подвздошную ямку делают косой разрез (при этом рана получается более широкой и удобной, легко обнажить подвздошные сосуды). Фасцию наружной косой мышцы живота рассекают по ходу волокон. После разведения краев этой фасции обнажают внутреннюю косую и прямую мышцы живота; разрез продолжают по фасциальной перемычке, соединяющей обе эти мышцы. Семенной канатик у мужчин нужно стремиться не пересекать, хотя это удается не во всех случаях; круглую связку матки у женщин всегда пересекают. Далее выделяют внутреннюю подвздошную артерию и наружную подвздошную вену. Артерию пересекают и анастомозируют с почечной артерией.
При пересадке почки от трупов берут почечную артерию вместе с участком аорты, выкраиваемым в виде своеобразного венчика. Этот венчик анастомози-руют с внутренней подвздошной артерией, которая в большинстве случаев по калибру бывает шире почечной артерии. При наличии у донора двух почечных артерий возможны различные варианты наложения артериального анастомоза: чаше всего целесообразно при наличии единой площадки из стенок донорской аорты, от которой отходят обе почечные артерии, анастомозировать ее с продольно надсеченной внутренней подвздошной артерией донора или дополнительный сосуд вшить в бок основного ствола.
При наличии двух почечных вен следует попытаться восстановить кровоток по ним. Для этого можно либо сшить обе вены по одной полуокружности, а затем анастомозировать их с наружной подвздошной веной реципиента, либо иссечь почечные вены единым блоком вместе со стенкой нижней полой вены и затем этот участок вшить в подвздошную вену реципиента.
Важный этап операции — восстановление непрерывности мочевыводящих путей и пассажа мочи. С этой целью применяют анастомозы между мочеточником донора и мочевым пузырем реципиента (уретеронеоцистостомия), а также между мочеточниками донора и реципиента. Наибольшее распространение получила уретеронеоцистостомия. При выполнении этой операции мочеточник проводит в подслизистом туннеле длиной 2—3 см для создания искусственного клапана, препятствующего рефлюксу мочи. Однако при этом ни слизистую оболочку, ни мышечный слой мочевого пузыря широко не вскрывают. Другая возможность восстановления непрерывности мочевыводящнх путей заключается в наложении уретеро-урстероанастомоза или уретеролоханочного анастомоза. При применении этих анастомозов практически исключается возможность возникновения рефлюкса.
Но такие анастомозы чаще осложняются стенозированием или несостоятельностью швов.
После трансплантации трупной почки функция трансплантата в первые дни бывает резко сниженной или отсутствует; реже наблюдается полиурическая форма функционирования трансплантата. С лечебной и диагностической точки зрения наиболее сложной является анурическая фаза, при которой в течение нескольких суток, а иногда 2 — 3 нед из пересаженной почки моча не выделяется. Чаше всего анурия бывает вызвана ишемическими повреждениями трансплантата обратимого характера. Однако при дифференциальной диагностике необходимо учитывать, что в ряде случаев возможна анурия вследствие необратимого ишемического некроза почки, тромбоза анастомозов сосудов, непроходимости мочеточника и, наконец, реакции отторжения.
Деятельность современного трансплантационного центра немыслима без большого и хорошо оснащенного центра гемодиализа; лишь единичным больным производят пересадки почки без применения аппарата искусственной почки. Гемодиализ обычно используют до трансплантации и в послеоперационном периоде. Эффективно комбинированное применение гемодиализа и сорбентов.
Большое значение имеет правильное проведение иммуносупрсссивной терапии, особенно в ближайшем послеоперационном периоде. Наибольшее распространение в клинике в качестве нммуносупрессоров получили глюкокортикоидные препараты (кортикостероиды) и азатноприн (имуран), а также местное рентгеновское облучение трансплантата. Реци пиентам назначают имуран или азатноприн (3—5 мг/кг в сутки) и преднизолон (1,5 мг/кг в сутки). В конце первого месяца дозы стероидов снижают до 0.75 мг/кг. При возникновении каких-либо диспепсических расстройств или наличии у больного язвенного анамнеза иредиизолон заменяют урбазоном в той же дозировке. При развитии инфекционно-септических осложнений (пневмония, нагноение раны) во всех случаях дозировку преднизалона резко снижают или заменяют этот препарат урбазоном, вводимым внутривенно.
В случае отсутствия функции трансплантат может быть либо удален во время повторной пересадки, либо, если он не оказывает отрицательного влияния на организм больного, оставлен ни месте. В последнее время предприняты попытки выключении отторгшегося трансплантата из кровотока путем эмболизации его сосудистой системы мнкросферамн. Тромбирование почечной артерии и выключение трансплантата из кровотока помогают избавить больных от лишней операции — удаления трансплантата.
Хирургическими осложнениями иммуносупрессивной терапии являются кишечные кровотечения, прободение желудка и другие поражения желудочно-кишечного тракта. Иногда возникают также разрывы трансплантатов: это осложнение с яркой клинической картиной отмечается чаше всего через 7—9 дней после операции. Раньше разорванные трансплантаты удаляли. В настоящее время в ряде случаев их удается сохранить, применяя для остановки кровотечения специальный клей.
В последнее время все большее применение получают повторные пересадки почки (вторые, третьи, четвертые и т. д.). К ним прибегают при неудачных первичных трансплантациях и непродолжительном функционировании пересаженной почки. Ретранснлантации трупной ночки являются альтернативой хронического гемодиализа после отказа первого трансплантата. Их результаты, как показывает специальный анализ, вполне сравнимы с результатами первичных операций.
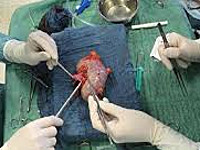
Осложнения трансплантации почки — это расстройства, этиологически связанные с пересадкой нефротрансплантата. В раннем периоде проявляются гипертермией, олигоанурией, артериальной гипертензией, болью в области трансплантата. Поздние осложнения длительно протекают бессимптомно, в последующем превалируют признаки почечной недостаточности и нарушений в работе других органов. Патология диагностируется с помощью исследований крови и мочи, УЗИ, УЗДГ, МРТ почек, пункционной биопсии. Для лечения применяют иммуносупрессоры, антибиотики, антиагреганты, антикоагулянты, проводят хирургическую ревизию раны, оперативные вмешательства на мочеточниках, нефротрансплантатэктомию.
МКБ-10
Общие сведения
Выживаемость пациентов, перенесших трансплантацию почки, на протяжении первого послеоперационного года достигает 94-98%, однако развитие осложнений существенно влияет на функциональность пересаженного органа и качество жизни реципиентов. В раннем и позднем посттрансплантационном периоде могут возникать как урологические заболевания, так и повреждения других органов, способные спровоцировать гибель пациента.
По результатам наблюдений, 33,2% смертей после трансплантации почек вызваны кардиальными причинами, из них 11,3% — острым инфарктом миокарда, 17,8% — инфекционными заболеваниями, 11,9% — опухолевым процессом, 6,9% — нарушением мозгового кровообращения, 30,3% — другими факторами. В течение первых 12 месяцев после вмешательства отторгается от 6 до 12% нефротрансплантатов, что требует возобновления заместительной почечной терапии и проведения повторной пересадки. До 36% реципиентов переносят инфекционные заболевания мочевыделительных органов и оппортунистические инфекции.

Причины
Несмотря на накопленный опыт и внедрение эффективных стандартов проведения операции, техническая сложность ее выполнения и использование аллотрансплантата повышают риск осложненного течения послеоперационного периода. Специалисты в сфере современной урологии, нефрологии и трансплантологии выделяют следующие группы причин, провоцирующих возникновение осложнений после нефротрансплантации:
- Возраст и состояние здоровья реципиента. Кроме абсолютных противопоказаний, при которых проведение трансплантации в большинстве случаев завершается неблагоприятным исходом, существуют относительные, существенно повышающие вероятность осложнений. В группу риска входят пациенты старше 65-70 лет, а также страдающие рядом сопутствующих заболеваний — активным гепатитом, циррозом печени, СКВ, васкулитом, гемолитико-уремическим синдромом, системными заболеваниями в активной фазе, сахарным диабетом, острыми инфекционными процессами, ХСН IIБ ст.
- Особенности трансплантируемой почки. Осложнения чаще возникают при AB0 и HLA-несовместимости тканей, пресенсибилизации реципиента. Приживление органа ухудшается при длительной (более 24 ч) холодовой ишемии почки, по результатам некоторых наблюдений этот фактор оказывается более значимым, чем гистосовместимость. Функциональность трупной почки зависит от причин смерти донора, электролитных нарушений, степени и длительности гипотонии, других особенностей агонального периода. На течение посттрансплантационного периода также влияет техника забора органа.
- Медицинские факторы. Исход трансплантации зависит от полноты предоперационного обследования реципиента и прижизненного донора, правильности оценки выявленных противопоказаний, проведения предтрансплантационной подготовки при обнаружении гистологической несовместимости тканей. На качество приживления почки оказывают влияние техническая точность пересадки, соблюдение требований асептики и антисептики, профилактика ишемического повреждения органа, качество наблюдения за пациентом, выбор оптимального режима иммуносупрессии (ИСТ).
- Иммунодефицит. Ряд постнефротрансплантационных осложнений связан с медикаментозным угнетением иммунитета реципиента. Назначение иммуносупрессивных препаратов — важное условие профилактики отторжения трансплантата. Однако на фоне иммунодефицита повышается вероятность возникновения ранних и отдаленных инфекционных заболеваний. Кроме того, иммуносупрессия является фактором риска онкогенеза. У части пациентов нарушения гуморального и клеточного иммунитета стимулируют возникновение аллергических и аутоиммунных реакций.
Патогенез
Механизм развития осложнений трансплантации почек зависит от этиологических факторов, спровоцировавших патологическое состояние. Зачастую в основе расстройства лежит иммунное или инфекционное воспаление. В первом случае наблюдается отторжение нефротрансплантата вследствие Т-клеточного ответа или гуморальной реакции типа антиген-антитело. При попадании в рану инфекционных агентов воспалительная деструкция тканей происходит под действием бактериальных эндо- и экзотоксинов.
Ситуация часто усугубляется ишемическими нарушениями, возникшими на фоне расстройств микроциркуляции, артериальной окклюзии, венозного тромбоза. Отдельную роль в патогенезе постнефротрансплантационных осложнений играет иммуносупрессия, снижающая или извращающая нормальную защитную реакцию организма на действие повреждающих факторов. В отдаленные сроки преобладают процессы склерозирования почечной паренхимы.
Классификация
Систематизация вариантов осложнений после трансплантации почки создана с учетом времени возникновения, причин, механизма развития и клинической симптоматики расстройства. Такой подход соответствует принципам своевременной диагностики и адекватной этиопатогенетической терапии постнефротрансплантационных нарушений. Осложнения при нефротрансплантации могут быть ранними, возникшими остро в ходе операции или в первые месяцы после пересадки, и поздними, с постепенным нарастанием симптомов. Различают следующие формы патологии:
Симптомы
Ранние острые нарушения обычно отличаются бурной клинической картиной. Вскоре после трансплантации у пациента возникает ярко выраженный интоксикационный синдром с высокой температурой, ознобом, суставными и мышечными болями, тошнотой, рвотой, кожным зудом, резкой слабостью. При внутреннем кровотечении наблюдается головокружение, бледность кожных покровов, возможна потеря сознания.
У большинства реципиентов о появлении осложнений свидетельствует значительное уменьшение мочеотделения вплоть до его полного прекращения в сочетании с высоким артериальным давлением. В области трансплантированной почки может пальпироваться болезненное уплотнение. Распространенным признаком инфекционного воспаления является наличие обильного раневого отделяемого. При вовлечении в воспалительный процесс брюшины и развитии перитонита возникает резкая боль в брюшной полости, живот становится напряженным, доскообразным, отмечается учащение пульса, резкое падение АД, часто отсутствует стул.
Проявлением поздних осложнений обычно становится прогрессирующее снижение фильтрационной способности почек. Клиническая симптоматика длительное время отсутствует. В последующем пациент начинает предъявлять жалобы на быструю утомляемость, снижение работоспособности. Уменьшается суточный диурез. Утром на лице преимущественно в области век появляются отеки, которые по мере развития почечной недостаточности сохраняются в течение дня и распространяются на другие части тела. Часто повышается артериальное давление.
Возникают и нарастают симптомы уремии — заторможенность, апатичность, бледность и сероватый оттенок кожи, интенсивный кожный зуд, жажда, нарушения сна, низкая температура тела, отсутствие аппетита, тошнота, рвота, диарея. При сочетанном поражении других органов и систем отмечается соответствующая симптоматика. Из-за угнетения иммунитета реципиенты часто болеют ОРВИ, у них развиваются тяжелые длительные бронхиты, пневмонии. Возможны различные формы пиодермий.
Нарушение всасывания кальция приводит к остеопорозу, гиперплазии паращитовидных желез. Из-за недостаточного синтеза эритропоэтинов часто формируется анемия. У пациентов, длительно принимающих иммуносупрессоры, могут диагностироваться онкологические заболевания. При этом преобладают новообразования предположительно вирусного происхождения — плоскоклеточная (сквамозная) и базальноклеточная карциномы, лимфопролиферативная болезнь (преимущественно В-клеточная неходжкинская лимфома), аногенитальные неоплазии, в том числе рак шейки матки, саркома Капоши.
Диагностика
Диагностический поиск при подозрении на осложнение трансплантации почки направлен на уточнение характера расстройства, оценку жизнеспособности и функциональной состоятельности почечного трансплантата, выявление критических органных и метаболических нарушений, угрожающих жизни реципиента. Наиболее информативными методами обследования являются:
- Общий анализ крови. Вероятное развитие острых осложнений подтверждается значительным повышением уровня лейкоцитов, падением содержания тромбоцитов, ускорением СОЭ. В отдаленном периоде часто наблюдается снижение концентрации эритроцитов, гемоглобина, на фоне иммуносупрессии возможно возникновение лейкопении.
- УЗИ почечного трансплантата. Эхография почки является безопасным скрининговым методом, позволяющим выявить изменение размеров пересаженного органа, деструкцию паренхимы, наличие патологических изменений в паранефральном пространстве. Исследование дополняют УЗДГ почечных сосудов для комплексной оценки состояния кровотока.
- Биохимический анализ крови. О нарушении фильтрационной функции клубочков свидетельствует нарастание уровней креатинина, остаточного азота, мочевины, калия. Поражение гломерулярного аппарата подтверждается данными пробы Реберга, нефрологического комплекса. Характерен высокий уровень ЛДГ, С-реактивного белка.
В зависимости от типа осложнения в общем анализе мочи может обнаруживаться повышение или снижение удельной плотности, наличие эритроцитов, лейкоцитов, цилиндров, бактерий. Для исключения отторжения нефротрансплантата рекомендовано проведение расширенного комплексного иммунологического исследования, пункционной биопсии с последующим гистологическим анализом полученного материала. Исследования с введением рентгеновского контраста (экскреторная урография, КТ, МСКТ почек) производятся с осторожностью из-за возможного усугубления клинической ситуации за счет развития контраст-индуцированной нефропатии.
В качестве дополнительных методов может назначаться МРТ для выявления возможных структурных нарушений в тканях трансплантата и нефросцинтиграфия, позволяющая уточнить функциональность пересаженной почки. Для мониторинга состояния пациента в раннем посттрансплантационном периоде оценивают волемический статус (гемогидробаланс, уровень ЦВД), электролитное состояние (уровни калия, натрия, кислотно-щелочного равновесия), коагулограмму, обеспечивают контроль диуреза, суточное мониторирование АД, регулярно выполняют ЭКГ.
Дифференциальную диагностику обычно проводят между различными видами осложнений. При поздних урологических последствиях трансплантации исключают развитие возвратного гломерулонефрита, рецидивирующей волчаночной нефропатии, пиелонефрита, гидронефроза. По назначению врача-нефролога или уролога пациента консультирует трансплантолог, анестезиолог-реаниматолог, абдоминальный хирург, инфекционист, ревматолог, иммунолог, онколог.
Лечение осложнений трансплантации почки
Основными врачебными задачами являются скорейшая коррекция возникших расстройств и поддержание основных жизненных функций реципиента. При отсутствии острых хирургических осложнений лечение обычно представлено комплексной медикаментозной терапией. С учетом выявленных нарушений пациентам, перенесшим трансплантацию почки, назначаются:
- Коррекция иммуносупрессорной терапии. Применение пульс-методов, изменение дозировки ингибиторов кальциневрина, антиметаболитов, глюкокортикоидов, ингибиторов интерлейкинов, биологических антилимфоцитарных агентов, замена одних препаратов другими зачастую позволяет купировать эпизод отторжения. Коррекция назначений также может потребоваться при связи осложнений с принимаемыми иммунодепрессантами.
- Лечение ишемии пересаженной почки. При возникновении сосудистых и тромботических нарушений используются дезагреганты, антикоагулянты, антигипоксанты, цитопротекторы, синтетические простагландины. С их помощью удается эффективно улучшить почечный кровоток, микроциркуляцию, перфузию тканей. Для увеличения кислородной емкости крови может назначаться гипербарическая оксигенация.
- Антибактериальные препараты. Показанием к проведению активной антибиотикотерапии служит наличие инфекционно-воспалительных осложнений. Предпочтительны противобактериальные средства с минимальным риском нефротоксического эффекта — хинолоны, комбинации диаминопиримидинов с синтетическими сульфаниламидами. При лечении оппортунистических инфекций учитывается чувствительность микроорганизмов.
Инфузионная терапия под контролем диуреза проводится при возникновении острых, угрожающих жизни состояний, метаболических расстройств. С учетом клинической картины реципиенту почки могут вливаться коллоидные и кристаллоидные растворы, отдельные электролиты, цельная кровь и ее компоненты. При нарастании признаков почечной недостаточности возобновляется заместительная терапия (гемодиализ, перитонеальный диализ, гемофильтрация, гемодиафильтрация). Лечение заболеваний, спровоцированных трансплантацией почки, осуществляется согласно протоколам для соответствующей патологии.
Оперативные методы лечения требуются при выявлении хирургических осложнений, деструкции мочеточника или почечного трансплантата. Объем вмешательств зависит от особенностей осложнения. Может выполняться ревизия и дренирование раны, ушивание поврежденных сосудов, лапароскопическая марсупиализация лимфоцеле. При повреждении мочеточника возможно проведение эндоскопического рассечения уретероцеле, уретеропластики, уретерокутанеостомии, наложение неоуретероцистоанастомоза. Необратимая деструкция трансплантированной почки служит показанием для нефротрансплантатэктомии с последующим назначением ЗПТ и возможной повторной пересадкой органа.
Прогноз и профилактика
Возникновение осложнений ощутимо ухудшает показатели выживаемости пациентов, однако своевременное выявление и грамотная коррекция расстройств делают прогноз более благоприятным. Профилактика возможных осложнений начинается с комплексного обследования больного перед операцией для определения всех абсолютных и относительных противопоказаний, оценки гистосовместимости с донором. При предстоящей AB0-несовместимой трансплантации требуется проведение предоперационной десенсибилизации. По показаниям на предтрансплантационном этапе может назначаться превентивная антибиотикотерапия.
С учетом вероятной компрометации заживления раны на фоне иммуносупрессивной терапии важна прецизионная хирургическая техника, повышенное внимание к деталям, строгое соблюдение правил асептики, тщательный гемостаз. После трансплантации ключевую роль играет правильный выбор индукционной и поддерживающей ИСТ, послеоперационный мониторинг состояния реципиента.
2. Инфекции после трансплантации почки (Обзор литературы)/ Кабулбаев К.А.// Нефрология и диализ. – 2009 – Т.11, №4.
3. Инфекционные осложнения раннего послеоперационного периода у пациентов после трансплантации почки/ Барканова О.Н., Перлин Д.В., Шепелева Ю.Б., Реброва Е.В., Ильченко О.В. // Вестник Волгоградского государственного медицинского университета. – 2016.
4. Этиология возбудителей инфекционных осложнений после трансплантации печени и почек и их резистентность к антибиотикам/ Габриэлян Н.И.// Российский медицинский журнал. – 2016.
Читайте также:

