Гуморальный фактор защиты который подавляет размножение вирусов
Обновлено: 24.04.2024
Гуморальный противовирусный иммуннитет. Клеточный противовирусный иммунный ответ.
Гуморальный противовирусный иммунный ответ в основном рассматривают как благоприятный для организма процесс, который в сочетании с клеточными иммунными механизмами, как правило, способствует выздоровлению. Однако существуют вирусы (герпесвирусы, гепатита В и др.), которые, несмотря на иммунный статус, длительно персистируют в организме хозяина. При некоторых вирусных инфекциях возможны иммунопатологические реакции. Так, антитела против вируса денге способствуют повышению его вирулентности у частично иммунных особей. Опосредованное антителами усиление репликации вируса денге в макрофагах объясняется повышенным связыванием иммунных комплексов с Fc-рецепторами клеточной поверхности. Иммунокомплексная патология лежит в основе патогенеза ряда вирусных инфекций, в том числе при лимфоцитарном хориоменингите и алеутской болезни норок. Следовательно, одним из важных аспектов защиты от данных инфекций является разработка высокоиммуногенных вакцин.
Проникновение вирусов в организм, как правило, сопровождается образованием вируснейтрализующих антител. Исключение составляют ряд вирусов и прежде всего, вирус африканской чумы свиней. Инфицирование этим вирусом не индуцирует синтез вируснейтрализующих антител, хотя в сыворотке крови выявляют комплементсвязывающие, преципитирующие и задерживающие гемадсорбцию антитела. Отсутствие вируснейтрализующих антител обусловливает неспособность организма связывать и элиминировать циркулирующий вирус, что сопровождается высокой летальностью и сводит на нет попытки создания эффективной вакцины.
Важное значение антител в защите от заболевания можно продемонстрировать следующим примером. Дети с тяжелой агаммаглобулинемией выздоравливают нормально от кори, но очень плохо защищены от паралитического полиомиелита, несмотря на прививку живой полиовирусной вакциной. Такие дети имели нормальный, опосредованный клетками и интерфероном иммунитет, нормальный фагоцитоз и нормальную систему комплемента, но не могли образовывать антитела, которые особенно важны, чтобы вирус с током крови не попал в нервную систему. Следует отметить, что полиовирус имеет два органа-мишени: кишечник и центральную нервную систему, которые поражаются в указанной последовательности.
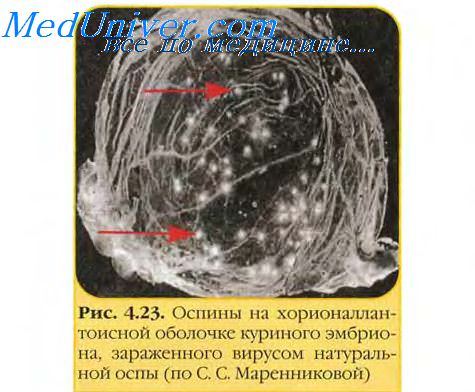
Кроме того, иммунизация живыми вакцинами через слизистые покровы может приводить и к выраженному местному синтезу антител, которые способны эффективно предотвращать локальную колонизацию (например, кишечника энтеропатогенными вирусами, а дыхательного тракта респираторными вирусами), блокируя таким образом развитие инфекции уже на уровне места проникновения и репликации вируса. С учетом указанной взаимосвязи, несомненный интерес представляют вирусы со строго дифференцированным тропизмом в отношении клеток слизистого покрова, в защите которых главенствующая роль принадлежит факторам иммунной системы слизистых покровов.
Среди секреторных и сывороточных антител наибольшее значение имеют вирусспецифические антитела к поверхностным гликопротеинам и, главным образом, к НА. Если антитела к НА нейтрализуют инфекционность вируса, то антитела к NA в основном ограничивают распространение инфекции, снижая ее интенсивность.
Помимо антител к гликопротеинам при респираторной инфекции образуются антитела к внутренним белкам вируса, в основном к нуклеопротеину (NP) и матриксному (М) белку. В отличие от поверхностных штаммоспецифических гликопротеинов, внутренние белки являются типоспецифическими антигенами, то есть индуцируют синтез антител, образующих иммунные комплексы со всеми штаммами вируса одного типа. Несмотря на индукцию гуморального и клеточного ответа, NP-белок вируса гриппа не создавал протективного иммунитета. Протективный эффект при пассивном переносе сывороточных IgG (особенно анти-НА) подтверждает их главную роль в гуморальном иммунитете при гриппе и других респираторных вирусных инфекциях.
Полагают, что свойством различать антигенные детерминанты обладает особый клон Тц-лимфоцитов, наделенный иммунологической памятью, которая усиливается при естественном инфицировании организма. Время полужизни вирусспецифических Тц-лимфоцитов у человека составляет 2—3 года. К специфическим факторам клеточного иммунитета относят также Тц-клетки с гиперчувствительностью замедленного типа. Антителозависимая цитотоксичность определяется всецело наличием антител и является своеобразным связующим звеном между клеточным и гуморальным иммунитетом. Это же положение подтверждается на примере Т-хелперов, которые способствуют продукции как Тц-лимфоцитов, так и антител.
При первичном инфицировании, когда еще не развились специфические факторы защиты, в борьбу с возбудителем включаются клеточные и гуморальные факторы неспецифической резистентности. Индуцируемая вирусом гриппа активность естественных киллеров (NK) обусловлена главным образом НА- и NA-антигенами.
Таким образом, иммунитет при гриппе ассоциируется с развитием гуморального ответа, а также формированием вирусспецифического клеточного иммунитета. Основные факторы гуморального иммунитета - вируснейтрализующие антитела секретов и сыворотки - обеспечивают защитный эффект в основном при реинфекции вирусом, проявляющейся даже спустя много лет после первичного инфицирования. Наибольшее значение для защиты имеют штаммспецифические антитела к НА вируса.
Иммунитет, индуцированный инактивированными гриппозными вакцинами, связывают с действием сывороточных антител. Живые вакцины обеспечивают длительный местный иммунитет слизистых оболочек с синтезом секреторных антител и, кроме того, транзиторный ответ сывороточных антител. Устойчивость организма к респираторным вирусам, как, впрочем, и ко многим другим вирусам, представляет собой многофакторный феномен, обусловленный как специфическими факторами иммунитета, так и неспецифической резистентностью.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Местный иммунитет (барьерная защита от инфекций)
Первой линией обороны против инфекционных агентов служат кожа и слизистые оболочки, которые препятствуют проникновению микробов в ткани и выделяют вещества, оказывающие бактерицидное действие.
Важным фактором является механическая защита. Так бактерии, попавшие на кожу, удаляются при слущивании эпидермиса (образование перхоти, шелушение при некоторых инфекционных заболеваниях). Слизь, выделяемая стенками многих внутренних органов, действует как защитный барьер, препятствующий прикреплению бактерий к эпителиальным клеткам. Микробы и чужеродные частицы, захваченные слизью, удаляются механическим путем – за счет движения ресничек эпителия, с кашлем и чиханьем. К другим механическим факторам, защищающим поверхности эпителия, можно отнести вымывающее действие слез, слюны и мочи.
Механическая защита дополняется секреторной (выделительной) деятельностью кожных желез: потовых и сальных. Молочная кислота пота и ненасыщенные жирные кислоты сальных желез обладают противомикробным действием. Во многих жидкостях, производимых организмом (секретах организма), также содержатся бактерицидные компоненты:
- лизоцим в слезах, носовых выделениях и слюне,
- кислота в желудочном соке,
- продукты расщепления жирных кислот в тонкой кишке,
- спермин и цинк в сперме,
- лактопероксидаза в молоке.
Специфическую функцию защиты во внешних секретах организма выполняет секреторный иммуноглобулин А (IgA). Он содержится в секретах и на слизистых оболочках слюнных желез, носа, рта, бронхов, влагалища, кишечника, мочеточников, мочевого пузыря. Секреторный иммуноглобулин А блокирует накопление и размножение на слизистой оболочке бактерий путем блокады поверхностных антигенов бактерий, с помощью которых они прикрепляются к слизистой оболочки органов.
Неспецифическая иммунная защита (защита на все возбудители)
Любой повреждающий агент-фактор, который по силе и длительности превосходит барьерные возможности ткани, вызывает ответную защитную реакцию организма – воспаление. Воспалительная реакция представлена единством трех явлений:
- повреждение и распознавание возбудителей;
- сосудистая реакция – нарушение микроциркуляции крови;
- клеточная реакция – миграция клеток иммунной системы в очаг воспаления.
Основная задача воспалительной реакции – уничтожение возбудителя и/или освобождение от собственных разрушенных клеток.
Можно выделить два типа уничтожения возбудителей:
- Внеклеточное разрушение возбудителя гуморальными факторами защиты (активными белками сыворотки крови).
- Внутриклеточная нейтрализация (фагоцитоз) (поглощение инфицированных клеток нейтрофилами и макрофагами с дальнейшим ферментативным разрушением структуры).
Внеклеточные механизмы защиты реализуются несколькими путями:
Клеточные и гуморальные факторы активно дополняют друг друга.
Специфическая иммунная защита (иммунный ответ на конкретный возбудитель)
За реакциями воспаления, если они не смогли нейтрализовать возбудителей, развивается более специализированная линия обороны – иммунный ответ, который последовательно запускает многоуровневую иммунную реакцию на возбудителя. Развитие специфических иммунных реакций требует взаимодействия практически всех видов клеток иммунной системы.
На первом этапе иммунного ответа захваченный в процессе фагоцитоза возбудитель перерабатывается макрофагом и в иммуногенной форме выводится его антиген на поверхность (презентация антигена). Особая роль в дальнейшем принадлежит активации Т-хелперов, которая происходит при распознавании Т-хелпером соответствующего антигенного комплекса на поверхности макрофага (антигенпрезентирующей клетки). В результате данного контакта Т-хелперы начинают делиться и после нескольких делений разделяются на две популяции. Одна активизирует развитие гуморального иммунного ответа (выработку иммуноглобулинов и антител), а другая популяция является необходимым компонентом в активации клеточного иммунитета (цитотоксические Т-лимфоциты).
Гуморальный иммунный ответ обеспечивается иммуноглобулинами или антителами, производимыми В-лимфоцитами. Продвигаясь по кровяному или лимфатическому руслу, антитела поражают чужеродные вещества на любой дистанции от лимфоцита. За счет гуморального иммунного ответа происходит уничтожение самих возбудителей и нейтрализация их токсинов, находящихся в межклеточном пространстве и на слизистых. Специфическая нейтрализация осуществляется за счет присоединения антител к антигенам с образованием растворимых и нерастворимых циркулирующих комплексов (ЦИК), которые активируют защитную систему белков комплемента, повышают фагоцитарную активность макрофагов и нейтрофилов, усиливают специфическое цитотоксическое действие Т-лимфоцитов (то есть повышается активность естественных киллеров).
Установлен ряд закономерностей динамики накопления антител после первого и повторного внедрения антигена. Первый пик концентрации антител появляется через несколько дней (скрытый период иммунного ответа) и обусловлен усиленным синтезом главным образом иммуноглобулина М (IgM). После второго внедрения того же антигена амплитуда ответа больше, он продолжается дольше и обусловлен возрастанием преимущественно синтеза иммуноглобулина G (IgG). Формирование стойкого иммунитета к возбудителям связано с образованием антител иммуноглобулина класса G.
Клеточный иммунный ответ. Гуморальный иммунный ответ. Защитные функции иммуноглобулинов ( антител ).
Клеточный иммунный ответ направлен против внутриклеточно паразитирующих микроорганизмов, основная защитная роль в нем принадлежит активированным макрофагам и цитотоксическим лимфоцитам (CD8+ CTL).
Макрофаги, инфицированные микроорганизмами, получают от Thl в качестве сигналов активации цитокины: гамма-интерферон и туморнекротизирующий фактор (ТНФ), которые действуют через свои рецепторы, вызывая усиленную продукцию макрофагами супероксидных и нитроксидных радикалов, убивающих внутриклеточные паразиты.
Цитотоксические CD8+ CTL способны убивать зараженные вирусами клетки при непосредственном контакте с ними. В месте контакта из CTL в мембрану клетки-мишени проникают порообразующие белки — перфорины, формирующие в мембране микроканалы, через которые в клетку-мишень проникают ферменты — фрагментины, вызывающие разрушение ядра клетки и ее гибель.
Гуморальный иммунный ответ
Гуморальный иммунный ответ защищает преимущественно против внекле-точно паразитирующих микроорганизмов, которые доступны действию специфических антител. Продуцентами антител (иммуноглобулинов) являются потомки активированных В-лимфоцитов — плазматические клетки.
В-лимфоцит получает сигнал активации при соединении его антиген-распознающего рецептора с антигеном. Для активной пролиферации и дифференцировки в плазматические клетки потомки В-лимфоцита получают дополнительные сигналы активации — продуцируемые Th2 цитокины: интерлейкины-4, -5, -6, -10, -13. Те же цитокины усиливают продукцию и секрецию специфических для данного антигена антител зрелыми плазматическими клетками.
Таблица 8.5. Защитные функции иммуноглобулинов (антител) разных изотипов
| Изотипы (классы) иммуноглобулинов | Локализация | Защитные функции |
| Иммуноглобулин G | Кровяное русло и ткани | Нейтрализация токсинов и вирусов, активация системы комплемента, усиление фагоцитоза |
| Иммуноглобулин М | Только кровяное русло | Активация системы комплемента |
| Иммуноглобулин А (секреторный) | Секреты на слизистых оболочках, грудное молоко | Препятствие адгезии бактерий и вирусов на слизистых оболочках, их связывание |
Специфические антитела — иммуноглобулины против конкретных антигенов бактерий (стафилококки, стрептококки, возбудители дифтерии, кишечных инфекций, клостридии и др.), связываясь с бактериальными токсинами, вызывают их нейтрализацию, т. е. утрату токсического действия на организм. Сами бактерии, связавшиеся со специфическими антителами, быстрее и легче захватываются и убиваются фагоцитирующими клетками или лизируются активированной системой комплемента.
Иммуноглобулины делятся на пять классов (изотипов): IgG, IgM, IgA, IgE, IgD. В нормальной сыворотке крови 80 % всех иммуноглобулинов составляют IgG, на долю IgM приходится 6 %, на долю IgA— 13 %, а на долю IgE и IgD — сотые или тысячные доли процента. Главными защитными иммуноглобулинами являются IgG. У иммуноглобулинов разных изотипов различаются защитные свойства (табл. 8.5).
Гуморальная иммунная реакция, то есть гуморальный иммунитет — это набор различных действий, которые выполняет наш организм, когда существует риск заболевания. Иммунная система работает так, что человеческий организм начинает вырабатывать антитела, которые помогают ему бороться с микроорганизмами. Существует ряд действий, при правильном выполнении которых, организм эффективно борется с угрозой и не заболевает. Что именно представляет собой деятельность иммунной системы ?
Чтобы понять, как именно человеческий организм защищается от болезней, необходимо разобраться в таком понятии как гуморальный иммунитет.
Что такое гуморальный иммунитет?
Гуморальный иммунитет входит в так называемый специфический иммунитет организма. Перед тем, как он начинает работать, срабатывает другой, первый ответ — неспецифический. В чем разница между ними и почему так важен специфический иммунитет?
Неспецифический и специфический иммунитет — особенности и отличия
В ситуации, когда есть риск заразиться инфекцией, организм запускает иммунный ответ. Первый этап, предшествующий ему, — это неспецифический иммунитет, нейтрализация действия опасного возбудителя.
Неспецифический иммунитет — это особенности организма, которые влияют на его способность защищаться от инфекции. Например, кожный барьер, который предотвращает проникновение патогена в организм, или пот, который является кислым и убивает некоторые бактерии. Слизистые оболочки и содержащиеся в них ферменты также обладают неспецифическим иммунитетом.
Гуморальный ответ, или специфический иммунитет, работает иначе. Он — второй защитник, который действует, когда первый терпит неудачу и не может побороть патогенный микроорганизм. В игру вступают лимфоциты, которые оценивают, нужна ли соответствующая иммунная реакция, то есть диагностируют, имеет ли данный патоген, попадая в организм, чужеродный антиген (характеристика данной клетки) или, наоборот, — это собственный антиген организма, и поэтому полностью безопасен. При обнаружении угрозы происходит соответствующая иммунная реакция, так называемый гуморальный иммунный ответ.
Распознавание чужеродных антигенов — в игру вступает гуморальный
Когда лимфоциты-помощники распознают антиген как чужеродный, вступает гуморальный ответ, направленный на уничтожение вредных клеток, патогенов. В хорошем варианте развития ситуации болезнь не наступает, поскольку организм справился с проблемой.
Что делать, если гуморальный и клеточный ответы не работают?
Гуморальный и клеточный ответ не всегда работает успешно и не всегда могут уберечь организм от болезней. В мире много людей, чьи гуморальные и клеточные реакции не работают должным образом. Организм теряет иммунитет, что делает его более восприимчивым к разного рода инфекциям.
Иногда гуморальный иммунитет разрушается под действием сильнодействующих препаратов, иногда из-за аллергии, во время которой человеческий организм считает безопасные вещества вредными и реагирует на них совершенно без надобности, т. е. тоже не работает должным образом.
Людям с ослабленным гуморальным ответом стоит сосредоточиться на том, как эффективно повысить иммунитет, чтобы усилить работу всей иммунной системы.
Эффективные способы укрепить ослабленный иммунитет
Как уже сказано, иммунная система не всегда работает идеально. Иммунитет может быть снижен в определенное время, особенно в осенне-зимний период, необходимо сделать все, чтобы его укрепить.
Если вы хотите повысить свой иммунитет, нужно вести здоровый образ жизни (правильное питание, занятия спортом, достаточное количество сна, соблюдение правил гигиены) и принимать лекарства, стимулирующие иммунную систему — стоит использовать те, которые содержат водный экстракт алоэ, африканской герани или эхинацеи.
Знание того, как работает иммунная система, помогает понять ту важную роль, которую она играет в организме. Ведя правильный образ жизни, человек помогает своему организму бороться с патогенами и снижает количество и тяжесть болезней.
Типы гуморального иммунного ответа при вирусной инфекции. Иммуноглобулин A.
Иммунная система организма на вирусные инфекции или иммунизацию вирусными вакцинами отвечает выработкой антител, обладающих специфичностью к различным вирусным компонентам и принадлежащих к разным классам иммуноглобулинов.
Важнейшая биологическая функция иммуноглобулинов - специфическое связывание с антигеном. Антитела против некоторых эпитопов на поверхности вирионов нейтрализуют инфекционность, они могут также действовать как опсонины, облегчая поглощение и разрушение макрофагами. Кроме того, антитела могут прикрепляться к вирусным антигенам на поверхности инфицированных клеток, вызывая их разрушение вследствие активации классического или альтернативного действия комплемента или с помощью активации Fc-рецепторсвязывающих клеток, таких как NK-клетки, полиморфноядерные лейкоциты и макрофаги (антителозависимая цитотоксичность).
Различают четыре основных класса антител: два мономера IgG и IgE и два полимера IgM и IgA. Все иммуноглобулины имеют подобную структуру, но широко варьируют по аминокислотной последовательности антигенсвязывающего сайта, который определяет их специфичность для данной антигенной детерминанты. N-концевая последовательность L- и Н-цепей образует антигенсвязывающий центр, то есть антидетерминанту. Чем больше антидетерминант на поверхности иммуноглобулина, тем выше его активность.
Авидность характеризует прочность связи антитела с соответствующим антигеном. Афинность - прочность связи между отдельными антидетерминантами и детерминантами.
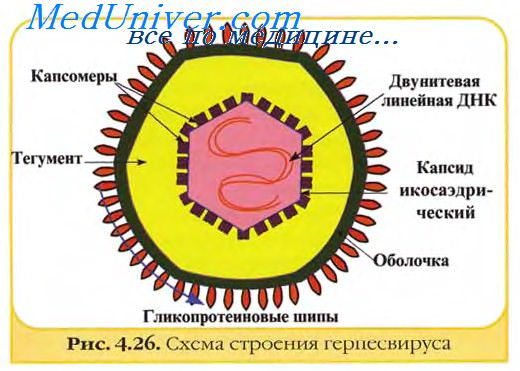
IgG является основным классом антител в крови. Он состоит из двух Н- и L-цепей, каждая из которых содержит постоянные и вариабельные участки. Молекулы IgG содержат два идентичных антигенсвязывающих Fab-фрагмента и Fc-фрагмент, выполняющий эффекторные функции (связывание комплемента, прикрепление к фагоцитам и плацентарному или колостральному трансферу).
В результате системной вирусной инфекции IgG синтезируется в течение длительного периода и является главным фактором защиты от реинфекции. Субклассы IgG отличаются константной областью их V-цепей и, соответственно, биологическими свойствами, такими как фиксация комплемента и прикрепление к фагоцитам.
Первоначально антитела относятся к классу IgM, но соматические рекомбинации (транслокации) затем рождают класс, обусловленный связыванием V-генных сегментов различными постоянными участками Н-цепей. В изменении изотипов (переход изотипов на другой путь) важная роль принадлежит различным цитокинам. Таким образом, через несколько дней IgG , IgA и иногда IgE-антите-ла той же самой специфичности становятся доминантными в иммунном ответе.
Тц-клетки достигают своего пика обычно через неделю после инфекции, а антитела — через 2—3 недели. NK-клетки максимально активируются через два дня, а активность интерферона совпадает с пиком концентрации вируса.
Динамика гуморального иммунного ответа проявляется, в первую очередь, в смене синтеза антител различных классов. В начальной фазе иммунного ответа синтезируется преимущественно IgM с относительно слабым сродством к антигену (авидный класс антител). IgM является пентамером с 10 Fab-фрагментами. Синтез IgM сменяется синтезом IgG, а затем IgA. IgM-антитела находятся в большинстве случаев в плазме крови и лимфе, обладая способностью преципитировать, агглютинировать и лизировать антигены.
Устойчиво высокие титры антител могут отражать также персистенцию вирусной инфекции (например, вирусов герпеса, кори) или повторную стимуляцию вирусным антигеном, однако антитела к некоторым вирусам могут персистировать и без явных признаков заболевания. IgG -антитела содержатся в сыворотке крови в наиболее высокой концентрации (~12г/л), откуда они поступают в тканевую жидкость. В отличие от других иммуноглобулинов, у человека и приматов они способны проникать через плаценту и снабжать плод материнскими антителами. Период полураспада их равен 10-35 дням.
Иммуноглобулин A (IgA) является димером с 4 Fab-фрагментами. Проходя через эпителиальные клетки, IgA приобретает J-фрагмент (секреторный фрагмент), становясь секреторным slgA, который секретируется через эпителий респираторного, кишечного и урогенитального трактов. Секреторный IgA более устойчив к протеазам, чем другие иммуноглобулины, и является основным иммуноглобулином на слизистых поверхностях, в молозиве и молоке многих видов млекопитающих. Поэтому IgA-антитела играют важную роль в защите от инфекции респираторного, кишечного и урогенитального трактов. Иммунизация через слизистые при некоторых инфекциях является более эффективной, чем системное введение вакцины.
Секреторные антитела появляются на 4-7-й день после инфицирования и представлены в основном IgA, IgG и IgM. Они считаются менее специфичными, чем сывороточные. Динамика накопления антител в сыворотке крови и секретах практически одинакова.
В отличие от сывороточного IgA, большая часть которого является мономером, молекула секреторного IgA представляет собой димер. Мономерный IgA синтезируется плазматическими клетками костного мозга, периферических лимфатических узлов, селезенки и других органов. Димерные формы sIgA с соединительной j-цепью синтезируются лимфоидной тканью желудочно-кишечного, респираторного и урогенитального трактов.
Добавочный структурный компонент секреторного IgA, вероятно, функционирует как поверхностный рецептор клеток секреторного эпителия и придает устойчивость sIgA к действию протеаз. Биологическая функция sIgA состоит в основном в местной защите слизистых оболочек от инфекции. Формирование местных секреторных IgA на поверхности слизистых оболочек имеет особое значение для формирования устойчивости организма к вирусам, обычно проникающим через дыхательный, кишечный или урогенитальный эпителий. Для индукции секреторных IgA в кишечнике вирус должен вступить в контакт с лимфоидной тканью кишечника. После формирования местного ответа В-клетки памяти, образующие IgA, мигрируют в другие участки кишечника. Аналогичный механизм индукции IgA функционирует в респираторном тракте.
Система секреторного иммунитета функционирует и регулируется иначе, чем иммунная система в целом. Она может коррелировать с общей иммунной реакцией или быть независимой от нее. Кроме секреторного IgA, существенное значение для иммунитета слизистых оболочек имеют содержащиеся в секретах у человека IgM и IgG. IgM также представляет секреторный иммуноглобулин, однако он не так прочно, как sIgA, связывает секреторный компонент. В пищеварительном тракте IgM играет более важную роль, чем IgG, а в носоглотке - наоборот.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

