Harmony лекарство от гепатита с
Обновлено: 12.05.2024
ОПИСАНИЕ И ЭФФЕКТИВНОСТЬ ПРЕПАРАТА ХАРВОНИ ДЛЯ ЛЕЧЕНИЯ ГЕПАТИТА С
Успешное терапия для гепатита С 1-го и 4-го генотипов HCV
На фармацевтическом рынке в ноябре 2014 года впервые появилось высокоэффективное инновационное лекарственное средство нового поколения Harvoni от американской компании Gilead Sciences, применение которого одобрено в США и странах Евросоюза. Препарат эффективно лечит гепатит С как 1-го так и 4-го генотипов HCV . Терапия препаратом Харвони это первая, одобренная FDA схема лечения, которая не предполагает одновременного сочетания препарата с интерфероном-альфа и значительно упрощает выбор курса терапии.
Гепатит С – очень серьезная болезнь с необратимыми нарушениями: циррозом печени, печеночной недостаточностью, гепатоцеллюлярной карциномой (ГЦК, раком печени), инфекциями брюшной полости, онкологическими проблемами. С момента начала применения этого новейшего противовирусного лекарства предотвращать развитие вышеперечисленных тяжелых состояний и заболеваний стало значительно проще и неприятных последствий у пациентов становится значительно меньше.

Состав инновационного препарата
Харвони имеет вид таблеток ромбовидной формы, покрытых оболочкой оранжевого (реже белого) цвета. Каждая таблетка содержит 90 мг препарата Ледипасвир и 400 мг препарата Cофосбувир . Среди вспомогательных ингредиентов – моногидрат лактозы, микрокристаллическая целлюлоза, кроскармеллоза натрия, стеарат магния, коповидон. Хранят лекарственное средство в темном и сухом, недоступном детям месте. Срок годности препарата – 2 года .
Фармакологическое воздействие
Активные действующие компоненты препарата – ледипасвир и софосбувир – при попадании в организм человека способны блокировать ферменты, необходимые для размножения вируса гепатита С и предотвращать инфицирование здоровых клеток. Степень эффективности Харвони подтвердили клинические испытания с участием более 1.500 добровольцев , разделенных в случайном порядке на 2 группы. В каждой из групп оказались люди, которые впервые проходили курс лечения, пациенты с циррозом печени и больные, у которых применение других лекарственных средств было малоэффективным. В одной группе пациенты 12 недель получали Harvoni с Рибавином, в другой – просто Harvoni.

Рис. 2. Харвони / Harvoni побеждает вирус гепатита С!
Кому назначают препарат
Научная презентация о препарате Харвони от нашего центра
Противопоказания
Если имеется почечная и печеночная недостаточность, курс лечения проводится под контролем специалиста. Среди других ограничений:
- аллергия на компоненты препарата;
- беременность и лактация;
- возраст до 18 лет;
- одновременный прием другого средства, в состав которого входит молекула Софосбувир (во избежание передозировки);
- запрещено сочетать прием Харвони с так называемыми Ингибиторами протонной помпы, Эльвитегравиром, Тенофовиром, Эмтрицитабином;
- Карбамазепин, Розувастатин, зверобой, Рифампицин, Типранавир, Фенитоин при одновременном применении сокращают лечебный эффект от приема Harvoni.
Женщине на время приема Харвони необходимо применять надежные контрацептивы, так как влияние Harvoni на течение самой беременности и плод до конца не изучено. Если курс назначен в период лактации, от грудного вскармливания надо отказаться, так как лекарство способно проникать в материнское молоко. Детям это лекарство не назначают, так как его воздействие на детей не изучалось. Принимают Harvoni по рекомендации врача строго в указанной дозе . Если в период лечения приходится принимать и другие препараты, врач должен об этом знать и обязательно контролировать возможные неблагоприятные межлекарственные взаимодействия. Доктору необходимо сообщать и о побочных реакциях, если они возникли во время или после приема Харвони.

Рис. 3. Харвони – фото оригинальной упаковки
Побочные эффекты
Препарат обладает сравнительно низкой токсичностью, но при высокой чувствительности к компонентам возможны:
- признаки общего недомогания;
- головная боль;
- в крайних случаях – аллергическая реакция.
Особенно внимательным к своим ощущениям надо быть в течение первых недель приема лекарства . Если появилась желтуха, асцит, одышка, отеки, сильный зуд следует немедленно обратиться к лечащему врачу и быстро пройти обследование.
После начала приема Харвони могут возникать незначительные расстройства в виде упадка сил или головных болей. Такая реакция организма только подтверждает эффективность лечения, поэтому довести курс до конца очень важно. При лечении гепатита C в комплексе с Рибавирином процент побочных эффектов может увеличиться.
Для пациентов с циррозом печени лекарство безопасно и эффективно, если соблюдать все меры предосторожности. Абсолютным большинством пациентов препарат переносится нормально и дает хороший результат.
Как применять Харвони
Харвони принимают во время еды, всего лишь одну таблетку в день. Жевать ее не рекомендуют – надо просто запить водой. Максимальный эффект от лекарства получается при приеме таблеток в одно и то же время . Если пришлось пропустить время приема, можно принять и позже или пропустить дозу, чтобы принять ее в обычный час. Главное – не допускать приема двойной дозы.
Принимать лекарство надо при любом самочувствии. Для больных с гепатитом С курс лечения составляет 12 недель, для пациентов с суб- и декомпенсированным циррозом печени срок терапии может быть увеличен до 24 недель и обязателен дополнительный прием Рибавирина. Аналогичные рекомендации и для пациентов при повторном лечении. С учетом особенностей здоровья пациента лечащий врач может скорректировать схему лечения препаратом. При случайной передозировке надо пройти обследование. Медицинской статистики о последствиях передозировки нет.
В период лечения Harvoni его воздействие на возможность управления автомобилем не наблюдалось, но все же надо быть внимательным из-за возможной общей усталости.
Харвони эффективен и в сочетании с другими препаратами от гепатита С. Для людей с аллергической реакцией на Интерферон и Рибавирин может быть настоящим спасением, так как его можно использовать отдельно от этих лекарств.
Сколько стоит Харвони и где его купить в России?
Харвони одобрили еще не во всех странах мира, препарат пока невозможно найти в российских аптеках. Но ведь он уже сегодня способен спасти жизнь и здоровье миллионам пациентов! Получить консультацию по этому препарату можно в клинике ЭКСКЛЮЗИВ по телефону горячей линии. Для Харвони цена одной упаковки на 4 недели лечения (всего 28 таблеток, каждая из которых содержит 90 мг препарата ледипасвир и 400 мг препарата софосбувир) может достигать $29.400 .
По информации PZ Online – Фармацевтической газеты Германии, стоимость лечения Harvoni в Европе в среднем составляет €20.000 в месяц. В соответствии с данными службы помощи больным СПИДом, терапия с применением Харвони в США обходится 25.000 долларов в месяц.
На сегодняшний день препарат Harvoni входит в число самых эффективных лекарственных препаратов, которые применяют для лечения пациентов с гепатитом С. Применение его в комплексной терапии вместо Интерферона, обладающего целым рядом побочных эффектов, значительно повышает эффективность и качество лечения и шансы на полное выздоровление.
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Софбувир
Таблетки, покрытые пленочной оболочкой белого цвета, капсуловидные, двояковыпуклые; на изломе таблетка белого или почти белого цвета.
| 1 таб. | |
| софосбувир | 400 мг |
Вспомогательные вещества: гипролоза - 80 мг, кремния диоксид коллоидный - 6 мг, мальтитол - 134 мг, натрия стеарилфумарат - 6 мг, повидон К30 - 14 мг.
Состав пленочной оболочки: титана диоксид - 2 мг, макрогол 3350 - 2.1 мг. поливиниловый спирт - 4.2 мг, тальк - 1.7 мг.
7 шт. - упаковки ячейковые контурные (4) - пачки картонные.
10 шт. - упаковки ячейковые контурные (3) - пачки картонные.
28 шт. - банки - пачки картонные.
Фармакологическое действие
Противовирусное средство, пан-генотипический ингибитор РНК-зависимой РНК-полимеразы NS5B вируса гепатита С. Софосбувир - нуклеотидное пролекарство, подвергается внутриклеточному метаболизму, в процессе которого формируется фармакологически активный аналог уридинтрифосфата (GS-461203). С помощью NS5B полимеразы GS-461203 может встраиваться в строящуюся цепочку РНК вируса гепатита С и действовать как обрыватель цепи. Этот активный метаболит софосбувира (GS-461203) подавляет активность полимеразы генотипов 1b, 2а, 3а и 4а вируса гепатита С в концентрациях, вызывающих 50% ингибицию (IC 50 ), в диапазоне от 0.7 до 2.6 мкмоль.
Фармакокинетика
После приема внутрь софосбувир быстро всасывается, C max в плазме крови достигается через 0.5-2 ч вне зависимости от величины принятой дозы. С max неактивного метаболита (GS-331007) в плазме крови достигалась через 2-4 ч после приема препарата. По результатам популяционного анализа фармакокинетических данных у пациентов с генотипами 1-6 вируса гепатита С, значения AUC 0-24 софосбувира и неактивного метаболита (GS-331007) в равновесном состоянии равны 1010 нг×ч/мл и 7200 нг×ч/мл соответственно. По сравнению со здоровыми добровольцами, AUC 0-24 софосбувира и неактивного метаболита (GS-331007) у пациентов с хроническим гепатитом С на 57% выше и на 39% ниже соответственно.
Прием софосбувира в однократной дозе с пищей с высоким содержанием жиров замедляет скорость всасывания софосбувира. Полнота всасывания софосбувира увеличивается примерно в 1.8 раз, при этом наблюдается незначительное влияние на C max . Прием пищи с высоким содержанием жиров не влияет на экспозицию неактивного метаболита (GS-331007). Установлено, что при приеме натощак софосбувира в дозах от 200 мг до 400 мг AUC софосбувира и неактивного метаболита (GS-331007) практически пропорциональна дозе.
Софосбувир примерно на 85% связывается с белками плазмы крови человека (данные ex vivo), степень связывания не зависит от концентрации препарата в диапазоне 1-20 мкг/мл. Неактивный метаболит (GS-331007) в минимальной степени связывается с белками плазмы крови. После однократного приема [ 14 С]-софосбувира в дозе 400 мг здоровыми добровольцами соотношение радиоактивности 14 С в крови/плазме составляло приблизительно 0.7.
Софосбувир интенсивно метаболизируется в печени с формированием фармакологически активного нуклеозидного (уридинового) аналога трифосфата (GS-461203). Метаболический путь активации включает последовательный гидролиз молекулы карбоксилэстеразы катепсином A (CatA) или карбоксилэстеразой 1 (CES1) и расщепление фосфорамидата нуклеотид-связывающим белком 1 с гистидиновыми триадами (HINT1) с последующим фосфорилированием путем биосинтеза пиримидинового нуклеотида. Дефосфорилирование приводит к образованию нуклеозидного неактивного (>90%) метаболита, который не может быть полностью рефосфорилирован, и не обладает активностью против HCV in vitro.
После однократного приема внутрь [ 14 С]-софосбувира в дозе 400 мг системная экспозиция софосбувира и неактивного метаболита (GS-331007) составляла примерно 4 и >90% соответственно от системной экспозиции материала, связанного с препаратом (сумма AUC софосбувира и его метаболитов с коррекцией на молекулярную массу).
После однократного приема внутрь [ 14 С]-софосбувира в дозе 400 мг среднее общее выведение радиоактивной дозы составляло более 92%, при этом приблизительно 80%, 14% и 2.5% выводилось почками, кишечником и легкими соответственно. Большая часть дозы софосбувира, выводимая почками, представляла неактивный метаболит (GS-331007) (78%), тогда как 3.5% выводилось в виде софосбувира. Эти данные показывают, что почечный клиренс является основным путем выведения неактивного метаболита (GS-331007) с преимущественной активной секрецией. Средний Т 1/2 софосбувира и неактивного метаболита (GS-331007) составляет 0.4 ч и 27 ч соответственно.
Фармакокинетика в особых клинических случаях
По сравнению с пациентами с нормальной функцией почек (КК >80 мл/мин), не инфицированными вирусом гепатита С, при почечной недостаточности легкой, средней и тяжелой степени тяжести, AUC 0-inf софосбувира была выше соответственно на 61%, 107% и 171%, a AUC 0-inf неактивного метаболита (GS-331007) была выше на 55%, 88% и 451% соответственно. У пациентов с хронической почечной недостаточностью по сравнению с пациентами с нормальной функцией почек AUC 0-inf софосбувира была на 28% выше, если софосбувир принимали за 1 ч до сеанса гемодиализа, и на 60% выше, если софосбувир принимали через 1 ч после сеанса гемодиализа. Основной неактивный метаболит (GS-331007) может быть эффективно удален с помощью гемодиализа (клиренс составляет около 53%). После 4-часового сеанса гемодиализа выводится примерно 18% от принятой дозы препарата.
По сравнению с пациентами с нормальной функцией печени AUC 0-24 софосбувира была на 126% и 143% выше у пациентов с печеночной недостаточностью средней и тяжелой степени тяжести, AUC 0-24 неактивного метаболита (GS-331007) была выше на 18% и 9% соответственно.
Показания активных веществ препарата Софбувир
Лечение хронического гепатита С у взрослых пациентов (в комбинации с другими лекарственными препаратами).
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Произведено:
Вторичная упаковка и выпускающий контроль качества:
Активные вещества
Лекарственная форма
Форма выпуска, упаковка и состав препарата Гарвони ®
Таблетки, покрытые пленочной оболочкой оранжевого цвета, ромбовидные, с гравировкой "GSI" на одной стороне и "7985" на другой.
| 1 таб. | |
| ледипасвир | 90 мг |
| софосбувир | 400 мг |
Вспомогательные вещества: коповидон, лактозы моногидрат, целлюлоза микрокристаллическая, кроскармеллоза натрия, кремния диоксид коллоидный, магния стеарат.
Состав оболочки: Опадрай II оранжевый 85F13912 (поливиниловый спирт, титана диоксид, макрогол, тальк, краситель солнечный закат желтый (E110)).
28 шт. - флаконы из полиэтилена высокой плотности (1) - пачки картонные × .
× с контролем первого вскрытия или без него.
Фармакологическое действие
Комбинированное противовирусное средство.
Ледипасвир является ингибитором вируса гепатита С (ВГС), который воздействует на неструктурный 5А (NSSА) протеин ВГС, необходимый для репликации РНК и формирования вирионов ВГС. Биохимическое подтверждение ингибирования NSSА ледипасвиром в настоящее время не представляется возможным, поскольку NSSА не имеет ферментативной функции. Выборочные исследования резистентности и перекрестной резистентности in vitro показывают, что механизм действия ледипасвира - это воздействие на NSSА.
Софосбувир является пангенотипным ингибитором РНК-зависимой РНК-полимеразы ВГС NSSB, необходимой для репликации вируса. Софосбувир - это нуклеотидное пролекарство, которое в результате внутриклеточного метаболизма преобразуется в фармакологически активный трифосфат (GS-461203), аналог уридина, который встраивается в РНК вируса гепатита С с помощью NSSВ-полимеразы и действует как терминатор цепи. GS-461203 (активный метаболит софосбувира) не является ингибитором ДНК и РНК-полимераз человека, а также не является ингибитором митохондриальной РНК-полимеразы.
Фармакокинетика
После приема внутрь комбинации ледипасвир/софосбувир пациентами, инфицированными ВГС, средняя C max ледипасвира в плазме крови наблюдалась через 4 ч после приема. Софосбувир быстро всасывался, и его средняя C max в плазме крови наблюдалась приблизительно через 1 ч после приема. Средняя C max GS-331007 в плазме крови наблюдалась через 4 ч после приема.
По результатам популяционных фармакокинетических исследований у пациентов, инфицированных ВГС, в равновесном состоянии значения AUC 0-24 ледипасвира (n=2113), софосбувира (n=1542) и GS-331007 (n=2113) были 7290 н×гч/мл, 1320 н×гч/мл и 12000 н×гч/мл соответственно. В равновесном состоянии C max ледипасвира, софосбувира и GS-331007 составили 323 нг/мл, 618 нг/мл и 707 нг/мл соответственно. AUC 0-24 и C max софосбувира и GS-331007 совпадали у взрослых здоровых добровольцев и у пациентов, инфицированных ВГС. Показатели AUC 0-24 и C max ледипасвира были на 24% и 32% ниже у пациентов, инфицированных ВГС, чем у здоровых добровольцев (n=191). В диапазоне доз от 3 мг до 100 мг значения AUC ледипасвира пропорциональны принятой дозе. Значения AUC софосбувира и GS-331007 приблизительно пропорциональны принятой дозе в диапазоне доз от 200 мг до 400 мг.
Связывание ледипасвира с белками плазмы крови человека составляет >99.8%. После однократного приема дозы 90 мг [ 14 С]-ледипасвира здоровыми добровольцами коэффициент соотношения [ 14 С]-радиоактивности крови и плазмы был в диапазоне от 0.51 до 0.66.
Наблюдался медленный окислительный метаболизм, механизм которого неизвестен. После однократного приема 90 мг [ 14 С]-ледипасвира системная экспозиция была почти полностью связана с ледипасвиром в неизмененном виде (>98%). В кале ледипасвир в основном определяется в неизмененном виде.
После однократного приема внутрь [ 14 С]-ледипасвира в дозе 90 мг средняя величина общего выведения дозы [ 14 С]-радиоактивного компонента с калом и мочой составляла 87%, при этом большая часть содержалась в кале (86%). 70% ледипасвира выводилась с калом в неизмененном виде, а на окислительный метаболит М19 приходилось 2.2% дозы. Эти данные свидетельствуют о том, что экскреция неизмененного ледипасвира с желчью является основным путем выведения, а почечная экскреция - вторичным (приблизительно 1%). Средний T 1/2 ледипасвира у здоровых добровольцев после приема комбинации ледипасвир/софосбувир натощак составил 47 ч
После однократного приема внутрь [ 14 С]-софосбувира в дозе 400 мг средняя величина общего выведения дозы составляла более 92%, из которой приблизительно 80%, 14% и 2.5% выводилось с мочой, калом и выдыхаемым воздухом соответственно. Большую часть софосбувира, выводимого с мочой, составлял метаболит GS-331007 (78%) и лишь 3.5% выводилось с неизмененном виде. Эти данные показывают, что почечный механизм является основным путем выведения GS-331007, а большая его часть выводится в результате активной секреции. Средний T 1/2 софосбувира и GS-331007 после приема комбинации ледипасвир/софосбувир составил 0.5 и 27 ч соответственно.
Показания активных веществ препарата Гарвони ®
Лечение хронического гепатита С (ХГС) у взрослых и подростков в возрасте от 12 до 18 лет.
Приведенная научная информация является обобщающей и не может быть использована для принятия решения о возможности применения конкретного лекарственного препарата.
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Софосбувир-ТЛ
Таблетки, покрытые пленочной оболочкой светло-желтого с коричневатым оттенком цвета, овальные, двояковыпуклые; на поперечном разрезе ядро от белого до светло-желтого цвета.
| 1 таб. | |
| софосбувир | 400 мг |
Вспомогательные вещества: маннитол, целлюлоза микрокристаллическая 102, кроскармеллоза натрия, магния стеарат, кремния диоксид коллоидный.
Состав оболочки: Опадрай II 85F220031 желтый [поливиниловый спирт, титана диоксид, макрогол 4000, тальк, краситель железа оксид желтый].
28 шт. - банки полимерные (1) - пачки картонные.
84 шт. - банки полимерные (1) - пачки картонные.
Фармакологическое действие
Противовирусное средство, пан-генотипический ингибитор РНК-зависимой РНК-полимеразы NS5B вируса гепатита С. Софосбувир - нуклеотидное пролекарство, подвергается внутриклеточному метаболизму, в процессе которого формируется фармакологически активный аналог уридинтрифосфата (GS-461203). С помощью NS5B полимеразы GS-461203 может встраиваться в строящуюся цепочку РНК вируса гепатита С и действовать как обрыватель цепи. Этот активный метаболит софосбувира (GS-461203) подавляет активность полимеразы генотипов 1b, 2а, 3а и 4а вируса гепатита С в концентрациях, вызывающих 50% ингибицию (IC 50 ), в диапазоне от 0.7 до 2.6 мкмоль.
Фармакокинетика
После приема внутрь софосбувир быстро всасывается, C max в плазме крови достигается через 0.5-2 ч вне зависимости от величины принятой дозы. С max неактивного метаболита (GS-331007) в плазме крови достигалась через 2-4 ч после приема препарата. По результатам популяционного анализа фармакокинетических данных у пациентов с генотипами 1-6 вируса гепатита С, значения AUC 0-24 софосбувира и неактивного метаболита (GS-331007) в равновесном состоянии равны 1010 нг×ч/мл и 7200 нг×ч/мл соответственно. По сравнению со здоровыми добровольцами, AUC 0-24 софосбувира и неактивного метаболита (GS-331007) у пациентов с хроническим гепатитом С на 57% выше и на 39% ниже соответственно.
Прием софосбувира в однократной дозе с пищей с высоким содержанием жиров замедляет скорость всасывания софосбувира. Полнота всасывания софосбувира увеличивается примерно в 1.8 раз, при этом наблюдается незначительное влияние на C max . Прием пищи с высоким содержанием жиров не влияет на экспозицию неактивного метаболита (GS-331007). Установлено, что при приеме натощак софосбувира в дозах от 200 мг до 400 мг AUC софосбувира и неактивного метаболита (GS-331007) практически пропорциональна дозе.
Софосбувир примерно на 85% связывается с белками плазмы крови человека (данные ex vivo), степень связывания не зависит от концентрации препарата в диапазоне 1-20 мкг/мл. Неактивный метаболит (GS-331007) в минимальной степени связывается с белками плазмы крови. После однократного приема [ 14 С]-софосбувира в дозе 400 мг здоровыми добровольцами соотношение радиоактивности 14 С в крови/плазме составляло приблизительно 0.7.
Софосбувир интенсивно метаболизируется в печени с формированием фармакологически активного нуклеозидного (уридинового) аналога трифосфата (GS-461203). Метаболический путь активации включает последовательный гидролиз молекулы карбоксилэстеразы катепсином A (CatA) или карбоксилэстеразой 1 (CES1) и расщепление фосфорамидата нуклеотид-связывающим белком 1 с гистидиновыми триадами (HINT1) с последующим фосфорилированием путем биосинтеза пиримидинового нуклеотида. Дефосфорилирование приводит к образованию нуклеозидного неактивного (>90%) метаболита, который не может быть полностью рефосфорилирован, и не обладает активностью против HCV in vitro.
После однократного приема внутрь [ 14 С]-софосбувира в дозе 400 мг системная экспозиция софосбувира и неактивного метаболита (GS-331007) составляла примерно 4 и >90% соответственно от системной экспозиции материала, связанного с препаратом (сумма AUC софосбувира и его метаболитов с коррекцией на молекулярную массу).
После однократного приема внутрь [ 14 С]-софосбувира в дозе 400 мг среднее общее выведение радиоактивной дозы составляло более 92%, при этом приблизительно 80%, 14% и 2.5% выводилось почками, кишечником и легкими соответственно. Большая часть дозы софосбувира, выводимая почками, представляла неактивный метаболит (GS-331007) (78%), тогда как 3.5% выводилось в виде софосбувира. Эти данные показывают, что почечный клиренс является основным путем выведения неактивного метаболита (GS-331007) с преимущественной активной секрецией. Средний Т 1/2 софосбувира и неактивного метаболита (GS-331007) составляет 0.4 ч и 27 ч соответственно.
Фармакокинетика в особых клинических случаях
По сравнению с пациентами с нормальной функцией почек (КК >80 мл/мин), не инфицированными вирусом гепатита С, при почечной недостаточности легкой, средней и тяжелой степени тяжести, AUC 0-inf софосбувира была выше соответственно на 61%, 107% и 171%, a AUC 0-inf неактивного метаболита (GS-331007) была выше на 55%, 88% и 451% соответственно. У пациентов с хронической почечной недостаточностью по сравнению с пациентами с нормальной функцией почек AUC 0-inf софосбувира была на 28% выше, если софосбувир принимали за 1 ч до сеанса гемодиализа, и на 60% выше, если софосбувир принимали через 1 ч после сеанса гемодиализа. Основной неактивный метаболит (GS-331007) может быть эффективно удален с помощью гемодиализа (клиренс составляет около 53%). После 4-часового сеанса гемодиализа выводится примерно 18% от принятой дозы препарата.
По сравнению с пациентами с нормальной функцией печени AUC 0-24 софосбувира была на 126% и 143% выше у пациентов с печеночной недостаточностью средней и тяжелой степени тяжести, AUC 0-24 неактивного метаболита (GS-331007) была выше на 18% и 9% соответственно.
Показания активных веществ препарата Софосбувир-ТЛ
Лечение хронического гепатита С у взрослых пациентов (в комбинации с другими лекарственными препаратами).
Лечение гепатита с в СПб в клинике ЭКСКЛЮЗИВ позволяет с гарантией более 95 процентов избавиться от вируса HCV, который вызывает серьезную хроническую патологию печени. Практически у всех вновь инфицированных болезнь протекает скрытно, без каких-либо симптомов.

Как передается вирус
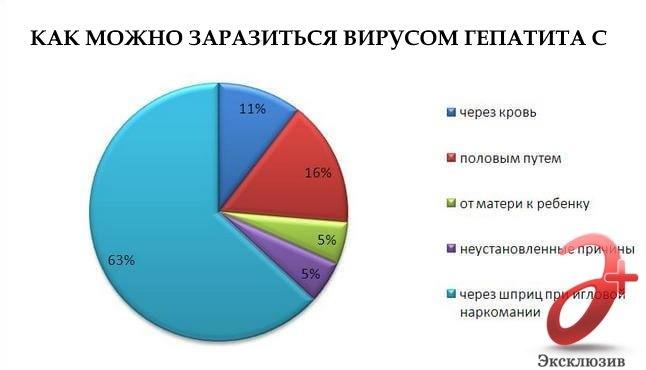
Гепатит С возникает вследствие передачи вируса через кровь следующими путями:
- из-за плохой обработки шприцев;
- ребенку от матери во время родов;
- в результате сексуальных контактов без презерватива;>
- при переливании зараженной вирусом крови или препаратов крови;
- если один шприц для инъекций используют сразу несколько человек – обычно именно так гепатитом С заражаются наркоманы.
Важно запомнить: при поцелуях, объятиях и через пищу вирус HCV не передается.
Как действует ВГС на печень
Сразу же после заражения человека иммунная система начинает активно реагировать на вирус и все свои силы направляет на борьбу с зараженными клетками организма. Ответ иммунной системы проявляется в первую очередь гибелью печеночных клеток, на месте которых образуются соединительная и жировая ткани – так формируются фиброз и стеатоз печени. Печень постепенно теряет свою эластичность и становится все более и более плотной – так формируется цирроз печени.
- отсутствие аппетита и потеря массы тела;
- астения и слабость.
Позже, когда развивается цирроз, появляются такие характерные признаки цирроза как:
- отеки нижних конечностей и асцит;
- быстро появляющиеся синяки на коже даже при несильных ушибах мягких тканей;
- снижение памяти, нарушение сна, агрессия, головная боль.
Характер и исход длительного воздействия HCV-инфекции на организм при хронической болезни печени заранее предсказать невозможно. У некоторых больных будут быстро развиваться фиброз и стеатоз печени (жировая дистрофия), у других может не быть вообще никаких патологических изменений в печени. Бывает так, что через 6-8 лет после момента заражения у больного развивается тяжелый цирроз печени, а в некоторых случаях даже рак печени.
Читайте также:

