Hepadnaviridae вирусы гепатита в
Обновлено: 19.04.2024
Вирус гепатита В ( HBV ), представляет собой частично двухцепочечной ДНК вируса , [1] а виды рода Orthohepadnavirus и членом Hepadnaviridae семейства вирусов. [2] [3] Этот вирус вызывает заболевание гепатитом . [4]
СОДЕРЖАНИЕ
Несмотря на то, что существует вакцина для предотвращения гепатита B, HBV остается глобальной проблемой здравоохранения. Гепатит B может быть острым, а затем перейти в хронический, приводя к другим заболеваниям и состояниям здоровья. [5] Помимо гепатита, инфекция HBV может привести к циррозу и гепатоцеллюлярной карциноме . [6]
Также было высказано предположение, что это может увеличить риск рака поджелудочной железы . [4]
Вирусная инфекция, вызванная вирусом гепатита В (HBV), вызывает множество изменений гепатоцитов из-за прямого действия белка, кодируемого вирусом, HBx , и косвенных изменений из-за значительного увеличения количества внутриклеточных активных форм кислорода (ROS) после заражения. HBx, по-видимому, нарушает регуляцию ряда клеточных путей. HBx вызывает нарушение регуляции частично за счет связывания с геномной ДНК , изменения паттернов экспрессии miRNA, воздействия на гистоновые метилтрансферазы, связывания с белком SIRT1 для активации транскрипции и взаимодействия с гистоновыми метилазами и деметилазами для изменения паттернов клеточной экспрессии. [7] HBx частично ответственен за приблизительно 10 000-кратное увеличение внутриклеточных ROS при хронической инфекции HBV. [8] Повышение АФК может быть частично вызвано локализацией HBx в митохондриях, где HBx снижает потенциал митохондриальной мембраны. [9] Кроме того, другой белок HBV , HBsAg , также увеличивает количество АФК за счет взаимодействия с эндоплазматическим ретикулумом . [9]
Увеличение количества активных форм кислорода (АФК) после инфицирования ВГВ вызывает воспаление, что приводит к дальнейшему увеличению АФК. [8] АФК вызывают более 20 типов повреждений ДНК. [10] Окислительное повреждение ДНК является мутагенным. [11] Кроме того, восстановление повреждений ДНК может вызвать эпигенетические изменения в месте повреждения во время восстановления ДНК. [12] Эпигенетические изменения и мутации могут вызывать дефекты клеточного аппарата, которые затем способствуют заболеванию печени . К тому времени, когда накапливающиеся эпигенетические и мутационные изменения в конечном итоге вызывают прогрессирование рака , эпигенетические изменения, по-видимому, играют в этом большую роль. канцерогенез, чем мутации. Только один или два гена, TP53 [13] и, возможно, ARID1A , [14] мутированы более чем в 20% случаев рака печени, в то время как каждый из 41 гена имеет гиперметилированные промоторы (репрессирующие экспрессию генов) более чем в 20% случаев рака печени, из них семь из этих генов гиперметилируются более чем в 75% случаев рака печени. [13] В дополнение к изменениям в участках репарации ДНК, эпигенетические изменения также вызваны тем, что HBx рекрутирует ферменты ДНК-метилтрансферазы , DNMT1 и / или DNMT3A , в определенные локусы генов, чтобы изменить их метилирование. уровни и экспрессия генов. [15] HBx также изменяет ацетилирование гистонов, что может влиять на экспрессию генов. [15]
Несколько тысяч генов, кодирующих белок, по-видимому, имеют сайты связывания HBx. [7] [16] Помимо генов, кодирующих белок, около 15 микроРНК и 16 длинных некодирующих РНК также подвержены влиянию связывания HBx с их промоторами. [16] Каждая измененная микроРНК может влиять на экспрессию нескольких сотен информационных РНК (см. МикроРНК ).
Вирус гепатита B классифицируется как типовой вид в Orthohepadnavirus , который содержит восемь других видов. [3] Род классифицируется как часть семейства Hepadnaviridae , которое включает четыре других рода: Avihepadnavirus , Herpetohepadnavirus , Metahepadnavirus и Parahepadnavirus . [3] Это семейство вирусов является единственным членом вирусного отряда Blubervirales . [3] Вирусы, похожие на гепатит В, были обнаружены у всех человекообразных обезьян ( орангутанги , гиббоны , горилл и шимпанзе ), в обезьян Старого Света , [17] и в Новый Свет шерстистый обезьян ( шерстистые обезьяны вируса гепатита В ), что указывает на древнее происхождение этого вируса в приматах.
Вирус делится на четыре основных серотипа (adr, adw, ayr, ayw) на основе антигенных эпитопов, присутствующих на его белках оболочки . Эти серотипы основаны на общем детерминанте (а) и двух взаимоисключающих парах детерминант (d / y и w / r). Вирусные штаммы также были разделены на десять генотипов (A – J) и сорок субгенотипов в соответствии с общими вариациями нуклеотидной последовательности генома. [18] Генотипы имеют четкое географическое распределение и используются для отслеживания эволюции и передачи вируса. Различия между генотипами влияют на тяжесть заболевания, течение и вероятность осложнений, а также реакцию на лечение и, возможно, вакцинацию. [19] [20] Серотипы и генотипы не обязательно совпадают.
Генотип D имеет 10 субгенотипов. [21] [18]
От летучих мышей был выделен ряд еще не классифицированных разновидностей вируса гепатита B. [22]

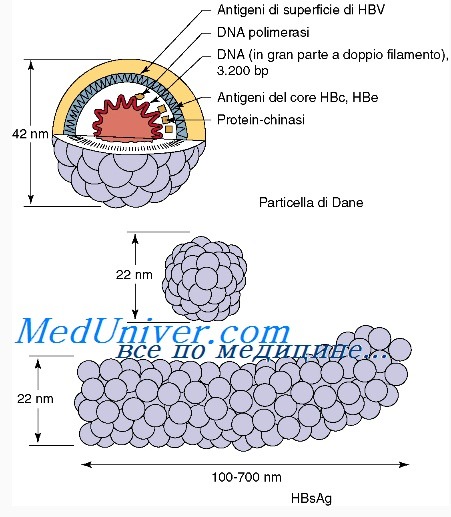
Вирус гепатита B является членом семейства Hepadnavirus . [23] Вирусная частица, называемая частица Дэйна [24] ( вирион ), состоит из внешней липидной оболочки и ядра икосаэдрического нуклеокапсида, состоящего из белка . Нуклеокапсид включает вирусную ДНК и ДНК-полимеразу, которая имеет активность обратной транскриптазы, аналогичную ретровирусам. [25] Внешняя оболочка содержит встроенные белки, которые участвуют в связывании вируса и проникновении в чувствительные клетки. Вирус является одним из самых маленьких оболочечных вирусов животных с диаметром вириона 42 нм, но плеоморфным. формы существуют, в том числе нитевидные и сферические тела без ядра. Эти частицы не являются инфекционными и состоят из липидов и белков, которые образуют часть поверхности вириона, называемого поверхностным антигеном ( HBsAg ), и вырабатываются в избытке в течение жизненного цикла вируса. [26]
Вирус гепатита D требует, чтобы частицы оболочки HBV стали вирулентными. [38]
Трудно установить раннюю эволюцию гепатита B, как и всех вирусов.
Дивергенция ортогепаднавируса и авихепаднавируса произошла ~ 125 000 лет назад (95% интервал 78 297–313 500). [39] И вирусы Avihepadnavirus, и Orthohepadna начали диверсифицироваться около 25 000 лет назад. [39] Ветвление в это время привело к появлению генотипов Orthohepadna A – H. У человеческих штаммов самый недавний общий предок датируется от 7000 (интервал 95%: 5 287–9 270) до 10 000 (интервал 95%: 6 305–16 681) лет назад.
У Avihepadnavirus отсутствует белок X, но в геноме гепаднавируса уток присутствует рудиментарная рамка считывания X. [40] Белок X, возможно, произошел от ДНК-гликозилазы .
Частота несинонимичных мутаций в этом вирусе оценивается примерно в 2 × 10 -5 замен аминокислот на сайт в год. [41] Среднее количество замен нуклеотидов на сайт в год составляет ~ 7,9 × 10 -5 .
Вторая оценка происхождения этого вируса предполагает, что он был самым недавним общим предком человеческих штаммов, появившихся около 1500 лет назад. [42] Самый недавний общий предок птичьих линий был установлен 6000 лет назад. Частота мутаций составила ~ 10-6 замен на сайт в год.
Другой анализ с большим набором данных предполагает, что гепатит В инфицировал людей 33 600 лет назад (на 95% выше задняя плотность 22 000-47 100 лет назад [43]. Расчетная скорость замещения составляла 2,2 × 10 -6 замен / сайт / год. Значительное увеличение в популяции отмечалось в течение последних 5 000 лет, межвидовое заражение орангутангов и гиббонов произошло в течение последних 6 100 лет.
Изучение последовательностей у зебровых вьюрков отодвинуло происхождение этого рода назад, по крайней мере, на 40 миллионов лет назад и, возможно, на 80 миллионов лет назад . [44] Шимпанзе , горилла , орангутанг и гиббоны объединяются в группу изолятов человека. К неприматам относились вирус гепатита сурков, вирус гепатита сусликов и вирус гепатита арктических белок. Также был описан ряд видов, заражающих летучих мышей. Было высказано предположение, что вид летучих мышей Нового Света может быть источником видов приматов. [45]
Исследование изолятов из циркумполярной арктической популяции людей показало, что предок субгенотипа B5 ( эндемический тип, обнаруженный в этой популяции), что предковый вирус возник в Азии около 2000 лет назад (95% HPD 900 г. до н.э. - 830 г. н.э.). [46] Слияние произошло около 1000 г. н.э. Этот субгенотип сначала распространился из Азии в Гренландию, а затем за последние 400 лет распространился на запад.
Самые старые свидетельства инфекции гепатита В относятся к бронзовому веку . [47] [48] Доказательства были получены из человеческих останков возрастом 4500 лет. [48] Согласно исследованию 2018 года, вирусные геномы, полученные путем секвенирования с дробовиком, стали самыми старыми из когда-либо извлеченных из образцов позвоночных. [48] Также было обнаружено, что некоторые древние штаммы вируса гепатита все еще инфицируют людей, а другие вымерли. [48] Это опровергло мнение о том, что гепатит B возник в Новом Свете и распространился в Европе примерно в 16 веке. [48]
Геном В выполнен из круглой ДНК , но это необычно , потому что ДНК не является полностью двухцепочечными. Один конец полноразмерной цепи связан с вирусной ДНК-полимеразой . Длина генома составляет 3020–3320 нуклеотидов (для полной цепи) и 1700–2800 нуклеотидов (для короткой цепи). [49]
Негативная (некодирующая) цепь комплементарна вирусной мРНК. Вирусная ДНК обнаруживается в ядре вскоре после заражения клетки. Частично двухцепочечная ДНК становится полностью двухцепочечной за счет завершения (+) смысловой цепи клеточными ДНК-полимеразами (вирусная ДНК-полимераза используется на более поздней стадии) и удаления белка вирусной полимеразы (P) из (- ) смысловой цепи и короткой последовательности РНК из (+) смысловой цепи. Некодирующие основания удаляются с концов (-) смысловой цепи, и концы соединяются заново.
Вирусные гены транскрибируются клеточной РНК-полимеразой II в ядре клетки из матрицы ковалентно замкнутой кольцевой ДНК (кзкДНК). В геноме HBV были идентифицированы два энхансера, обозначенные как энхансер I (EnhI) и энхансер II (EnhII). Оба энхансера проявляют большую активность в клетках печеночного происхождения и вместе они управляют и регулируют экспрессию полных вирусных транскриптов. [50] [51] [52] Существует четыре известных гена, кодируемых геномом: C, P, S и X. Основной белок кодируется геном C (HBcAg), а его стартовый кодон предшествует восходящему внутрикадровый стартовый кодон AUG из которого производится pre-core белок. HBeAg продуцируется протеолитическим процессингом пре-корового белка. ДНК-полимераза кодируется геном P. Ген S - это ген, кодирующий поверхностный антиген (HBsAg). Ген HBsAg представляет собой одну длинную открытую рамку считывания, но содержит три кодона в "стартовой" рамке (ATG), которые делят ген на три части: пре-S1, пре-S2 и S. Из-за множественных стартовых кодонов полипептиды трех производятся разные размеры, называемые большим, средним и малым (pre-S1 + pre-S2 + S, pre-S2 + S или S). [53] Функция белка, кодируемого геном X, полностью не изучена [54], но некоторые данные свидетельствуют о том, что он может действовать как транскрипционный трансактиватор.
В геноме HBV было идентифицировано несколько некодирующих элементов РНК . К ним относятся: HBV PREalpha , HBV PREbeta и сигнал инкапсидации РНК HBV эпсилон . [55] [56]
Генотипы различаются по крайней мере на 8% последовательности и имеют четкое географическое распределение, и это было связано с антропологической историей. Внутри генотипов описаны подтипы: они различаются на 4–8% генома.
Известно восемь генотипов, обозначенных от А до Н. [19]
С тех пор были признаны еще два генотипа. [59] В текущем (2014 г.) листинге от A до J. Также распознаются несколько подтипов.
Есть как минимум 24 подтипа.
Различные генотипы могут по-разному реагировать на лечение. [60] [61]
Тип F, который отличается от других геномов на 14%, является наиболее дивергентным из известных типов. Тип А распространен в Европе , Африке и Юго-Восточной Азии , включая Филиппины . Типы B и C преобладают в Азии ; тип D распространен в Средиземноморье, на Ближнем Востоке и в Индии ; тип E локализован в Африке к югу от Сахары; тип F (или H) ограничен Центральной и Южной Америкой . Тип G был обнаружен во Франции и Германии . Генотипы A, D и F преобладают в Бразилии, и все генотипы встречаются в Соединенных Штатах. с частотами, зависящими от этнической принадлежности.
Штаммы E и F, по-видимому, произошли от коренных народов Африки и Нового Света соответственно.
Тип A имеет два подтипа: Aa (A1) в Африке / Азии и на Филиппинах и Ae (A2) в Европе / США.
Тип B имеет два различных географических распределения: Bj / B1 ('j' - Япония) и Ba / B2 ('a' - Азия). Тип Ba был далее подразделен на четыре клады (B2 – B4).
Тип C имеет два географических подтипа: Cs (C1) в Юго-Восточной Азии и Ce (C2) в Восточной Азии. Подтипы C были разделены на пять клад (C1 – C5). Шестая клада (C6) была описана на Филиппинах, но на сегодняшний день только в одном изоляте. [62] Тип C1 связан с Вьетнамом , Мьянмой и Таиландом ; тип C2 с Японией , Кореей и Китаем ; тип C3 с Новой Каледонией и Полинезией ; C4 с Австралией ; и C5 с Филиппинами . Другой подтип был описан в Папуа , Индонезия . [63]
Тип D разделен на 7 подтипов (D1 – D7).
Тип F подразделяется на 4 подтипа (F1 – F4). F1 был дополнительно разделен на 1a и 1b. В Венесуэле подтипы F1, F2 и F3 встречаются у индейцев Восточной и Западной Америки. Среди южноамериканских индейцев был обнаружен только F3. Подтипы Ia, III и IV имеют ограниченное географическое распространение (Центральная Америка, Север и Юг Южной Америки соответственно), в то время как клады Ib и II встречаются во всех Америках, за исключением Северной Южной Америки и Северной Америки соответственно.

Жизненный цикл вируса гепатита В сложен. Гепатит B - один из немногих известных неретровирусных вирусов, которые используют обратную транскрипцию как часть процесса репликации.
Вложение Вирус проникает в клетку, связываясь с рецепторами на поверхности клетки и проникая в нее посредством эндоцитоза, опосредованного клатрином или кавеолином-1 . [64] HBV первоначально связывается с протеогликаном сульфата гепарина . Затем пре-S1-сегмент белка L HBV прочно связывается с рецептором клеточной поверхности, котранспортирующим тауроколат натрия, котранспортным полипептидом (NTCP), кодируемым геном SLC10A1 . [65] НПБТ встречается в основном в синусоидальной мембраны из клеток печени . Присутствие NTCP в клетках печени коррелирует с тканевой специфичностью инфекции HBV. [64] Проникновение После эндоцитоза вирусная мембрана сливается с мембраной клетки-хозяина, высвобождая нуклеокапсид в цитоплазму. [66] Непокрытие Поскольку вирус размножается с помощью РНК, созданной ферментом-хозяином, вирусная геномная ДНК должна быть перенесена в ядро клетки. Считается, что капсид транспортируется по микротрубочкам к ядерной поре . Основные белки отделяются от частично двухцепочечной вирусной ДНК, которая затем становится полностью двухцепочечной (ДНК-полимеразами хозяина) и трансформируется в ковалентно замкнутую кольцевую ДНК ( кзкДНК ), которая служит матрицей для транскрипции четырех вирусных мРНК . Репликация Самая большая мРНК (которая длиннее вирусного генома) используется для создания новых копий генома и для создания белка ядра капсида и вирусной РНК-зависимой ДНК-полимеразы . сборка Эти четыре вирусных транскрипта подвергаются дополнительной обработке и продолжают формировать вирионы потомства, которые высвобождаются из клетки или возвращаются в ядро и рециклируются, чтобы произвести еще больше копий. [53] [67] Релиз Затем длинная мРНК транспортируется обратно в цитоплазму, где белок Р вириона синтезирует ДНК за счет своей активности обратной транскриптазы.
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
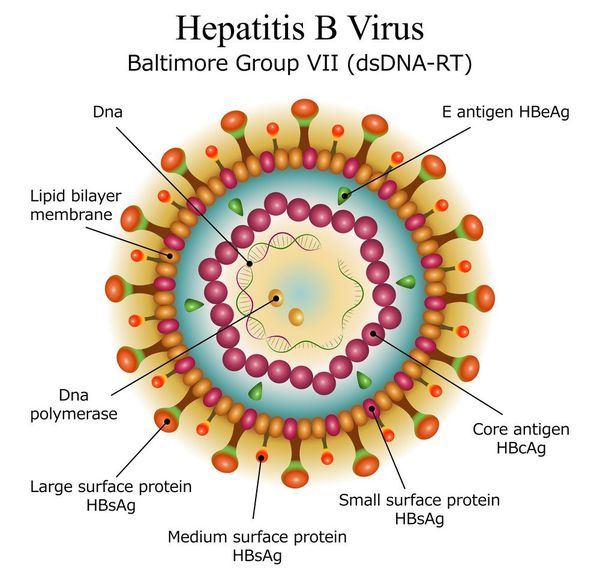
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
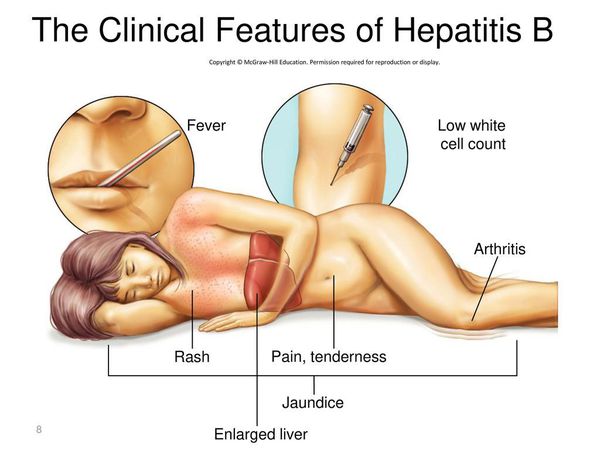
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
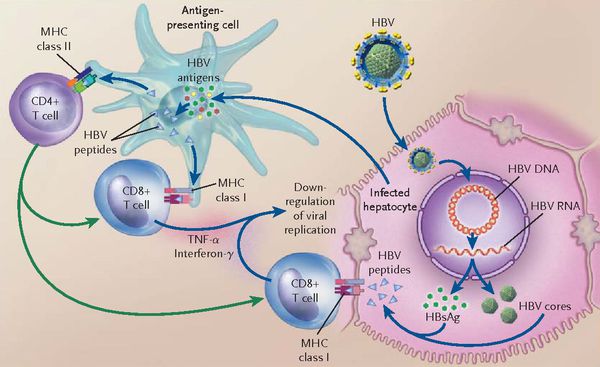
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Гепатит В. Вирус гепатита В. Эпидемиология гепатита В.
Гепатит В — инфекционное заболевание с кровяно-коптактным механизмом передачи, клинически и морфологически характеризующееся поражением печени с развитием симптомокомплекса острого и хронического гепатита.
Возбудитель гепатита В впервые обнаружили Д. Дёйн и соавт. (1970). Вирус гепатита В включён в состав рода Orthohepadnavirus семейства Hepadnaviridae.
В состав сердцевины гепатита В также входит ДНК-зависимая ДНК-пол имераза. Для эффективной репродукции необходим синтез ДНК-полимеразы, так как вирусная ДНК образуется на матрице РНК; в динамике процесса вирусная ДНК интегрирует в ДНК клетки.
В крови больных гепатитом В циркулируют частицы трёх морфологических типов. Наиболее часто обнаруживают сферические частицы около 22 в диаметре; реже - нитевидные формы около 22 нм в диаметре и 50-230 нм в длину.
Вирусные частицы гепатита В этих типов не проявляют инфекционных свойств. Лишь 7% частиц представлены комплексными двухслойными сферическими образованиями с полной структурой — частицы Дейна, проявляющие выраженную инфекционность. Их оболочку на 70% поверхности образуют белки.

Эпидемиология гепатита В
Резервуар возбудителя гепатита В — инфицированный человек. Механизм передачи инфекции гепатита В — кровяно-контактный. Основные пути передачи вируса гепатита В — инъекционный, гемотрансфузионный и половой.
Также показана возможность вертикальной передачи вируса гепатита В от матери к плоду. 7-10% инфицированных становятся хроническими носителями. Ежегодно заболевает не менее 50 млн человек. В РФ отмечают 10-15% рост заболеваемости.
Основные группы риска гепатита В — медицинские работники; лица, получающие гемотрансфузии или препараты крови; наркоманы, вводящие наркотики внутривенно; больные гемофилией; лица, находящиеся на гемодиализе; дети матерей-носителей HBsAg; половые партнёры носителей вируса.
Инфекции вируса гепатита В: диагностика, лечение, профилактика
Гепаднавирус — возбудитель гепатита В (HBV) — мелкий оболочечный вирус (3,2 тыс. пар нуклеотидов) с частично двунитевой ДНК, кодирующей три поверхностных белка (поверхностный антиген — HBsAg, ядерный антиген — HBcAg, преядерный белок — HBEAg), активный полимеразный белок и трансактивирующий белок. Передача инфекции осуществляется посредством парентерального, вертикального и полового механизмов.
Клинические признаки инфекции вируса гепатита В. Основной фазе заболевания предшествует длительный инкубационный период (до 6 мес), после которого начинается острая стадия (от лёгких до тяжёлых форм).
При молниеносном (фульминантном) гепатите смерть наступает в 1—2% случаев. У 10% пациентов болезнь переходит в хроническую форму, осложнения которой — цирроз печени или гепатоцеллюлярная карцинома. При врождённой инфекции — высокий риск развития гепатоцеллюлярной карциномы.
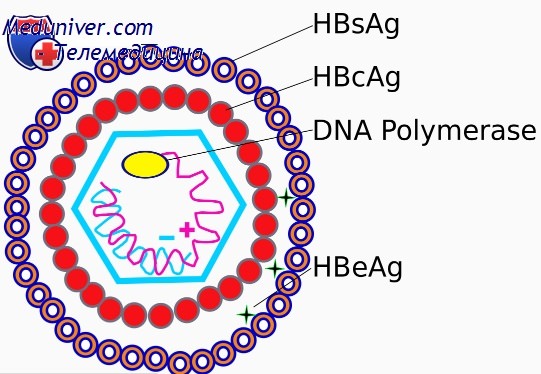
Диагностика инфекции вируса гепатита В:
• ИФА (обнаружение HBsAg, HBEAg, HBcAg и антител к ним).
• Молекулярно-генетический метод (измерение вирусной нагрузки).
• Секвенирование (определение резистентных штаммов для правильного выбора лекарственного препарата).
Лечение и профилактика инфекции вируса гепатита В. Слабый терапевтический эффект оказывает применение интерферона альфа, однако его пегилированные формы считают основным средством для подавления активности вируса без развития резистентных штаммов. Вирусную нагрузку помогает снизить нуклеозидный ингибитор ламивудин, но к нему быстро развивается устойчивость.
Более новые препараты (адефовир, энтекавир, тенофовир, телбивудин и клевудин) обладают равным или даже превосходящим ламивудин по силе противовирусным эффектом. Их применяют против ламивудинустойчивых штаммов вируса гепатита В.
Подавление вирусной репликации на протяжении 2—5 лет способно остановить прогрессирование фиброза печени, предотвращает развитие цирроза, а при его возникновении — улучшает функцию печени, предупреждает развитие печёночной недостаточности и снижает риск развития рака печени. Признак успешного лечения — сероконверсия HBEAg (появление антител к HBeAg).
Для иммунизации людей, входящих в группу риска, применяют рекомбинантную вакцину для профилактики вирусного гепатита В. С целью снижения риска заражения от матери новорождённым вводят вакцину для профилактики вирусного гепатита В и иммуноглобулин человека против гепатита В. Для профилактики парентерального заражения все доноры обязаны проходить обследование. Большое значение придают программам сексуального воспитания населения и пропаганде использования одноразовых шприцев.
Варианты HBsAg гепатита В и их распространение
Серологическая гетерогенность вируса гепатита В установлена в 1971 году G. L. Le Bouvier, когда им были описаны две взаимоисключающие субдетерминанты d и у. В 1972 году W. Н. Bancroft et al. выявили еще две дополнительные субдетерминанты — w и r.
Наличие общей детерминанты a HBsAg и двух пар взаимоисключающих детерминант d или у и w или r приводит к существованию 4 серотипов или, как их еще называют, субтипов: adw, ayw, adr, ayr. Общеизвестные серотипы вируса иногда ошибочно называют генотипами.
Между тем, генетический анализ вирусов четырех вышеупомянутых серотипов не выявил четкого соответствия между определенными генотипами и серотипами. В настоящее время известно 6 генотипов (A-F) и 9 серотипов HBV.
Сегодня, с учетом данных о ряде аминокислотных замен, приводящих к образованию нескольких минорных субдетерминант, выделено девять основных субтипов HBsAg — ayw1, ayw2, ayw3, ayw4, ayr, adw2, adw4, adrq-v, adrq-. В различных регионах мира структура циркулирующих субтипов HBsAg неодинакова.
В Северной и Южной Америке, Европе и значительной части Азии преобладают субтипы adw2, ayw3, ayr. Субтипы ayw2, ayw4, adw2 часто встречаются в Африке, adrq+ широко распространен в Юго-Восточной Азии, adrq- — в Австралии. К. Madalinski et al., 1977 показали преимущественное распространение субтипа adw, который был обнаружен в Польше и Венгрии соответственно в 80,7% и 72,2% случаев.
Исследования, проведенные в Финляндии, зафиксировали у 77-100% лиц с HBs-антигенемией субтип ау. По данным G. Gerna et al., 1976, на севере Италии субтип ayw преобладает (83,1%). Представляют значительный интерес данные К. Katsuki et al., 1980 о различиях в частоте обнаружения одного и того же субтипа в различных этнических группах Японии.
В качестве антигена важнейшее значение имеет детерминанта a HBsAg, которая является доминирующим кластером эпитопов HBV, обеспечивает выработку протективного иммунитета и взаимодействует с подавляющим большинством антител к HBV, присутствующих в гипериммунной сыворотке. Кроме того, детерминанта а весьма консервативная структура у всех серотипов HBV, что делает HBsAg важнейшим компонентом всех ныне применяемых вакцин.
Детерминанта а представляет собой часть большого гидрофильного региона HBsAg. Антигенность а детерминанты обусловлена ее третичной структурой. Детерминанта состоит из 23 аминокислотных остатков, локализованных в положении 124-147 пептидной цепочки HBsAg, и образует 2 петли, выступающие над наружной поверхностью вируса.
Большинство антител, вырабатываемых в ответ на вакцинацию, взаимодействует с участком, состоящим из 9 аминокислотных остатков в положении 139-147. С другой стороны, показано, что детерминанта а является конформационным кластером эпитопов, включающим область 120-124 аминокислотных остатков. Так, замены аминокислотных остатков в позициях 139-147 способны влиять на связывание антител с эпитопом в позиции 122, а замены аминокислотных остатков в позициях 120-124 в свою очередь влияют на связывание антител с эпитопом в позиции 139-147. Диагностические методы, разработанные для выявления HBsAg, основаны на применении антител, полученных к удлиненной детерминанте а.
Читайте также:

