Идентификация вируса гепатита с
Обновлено: 18.04.2024
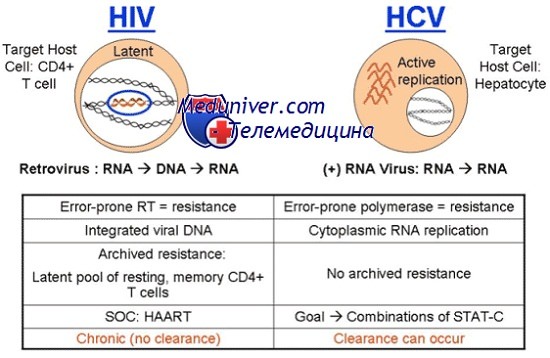
Вирус гепатита С (HCV) представляет собой небольшой вирус, покрытый липидной оболочкой, содержащей одноцепочечную РНК. HCV относится к флавивирусам, роду семейства тогавирусов. Между 5' и 3' терминальными участками генома вируса располагаются структурные и неструктурные гены (рис. 1). 6 Структурные гены (С - core, Е1, Е2) кодируют ядерный и оболочечные гликопротеиды, в то время как неструктурные гены (NS2, NS3, NS4, NS5) - ферменты, участвующие в репликации вируса. Внутри генома имеются вариабельные и гипервариабельные участки, 6, 7 и в зависимости от их строения выделяют по крайней мере 6 различных генотипов HCV (возможно, их 12 или больше). 5, 8, 9 Генотипы вируса, по-видимому, различаются по иммуногенности, географическому распределению и, вероятно, влияют на течение HCV-инфекции и результаты лечения (см. также "Зависимость тяжести течения от генотипа HCV", "Ответ на лечение ИФН альфа-2b, влияние генотипа HCV"). 5, 7, 8 Вариабельность генома также может снижать чувствительность имеющихся диагностикумов для тестирования донорской крови и осложнять разработку вакцин против вируса. 10 (В настоящее время все усилия направлены на разработку вакцин на основе core региона, являющегося относительно стабильным участком у всех генотипов). 11, 12
Разные генотипы могут выявляться на протяжении инфекции у одного и того же больного. 13, 14 Исходя из этого было предположено, что наличие более вариабельных участков генома может отражать стратегию ускользания вируса от механизмов защиты хозяина. 5, 13, 15 По мнению других исследователей, данный феномен не имеет значения для репликации вируса. 13
Рис. 1 Организация генома HCV (По Van der Poel и соавт., 6 воспроизведено с разрешения)
ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ ПРИ HCV-ИНФЕКЦИИ
Anti-HCV и HCV РНК
По мере расширения представлений о структуре HCV методы выявления вируса становятся все более чувствительными. В настоящее время нет тест-систем для прямого определения антигенов HCV и больные тестируются на антитела к вирусу (anti-HCV). Скрининговым тестом обычно является иммуноферментный анализ (ELISA) (описан ниже). Положительные результаты контролируются более чувствительными методами рекомбинантного иммуноблоттинга (RIBA). По возможности необходимо исследование HCV РНК (с помощью полимеразной цепной реакции или метода амплификации разветвленной ДНК) для подтверждения наличия или отсутствия вируса в сыворотке.
Скрининговые тесты. Первые тест-системы для выявления anti-HCV основывались на обнаружении антител к вирусному антигену c 100 (anti-c100) с помощью ELISA первого поколения (табл. 1). 16 Однако anti-c100 могут появляться через много лет после инфицирования HCV; при этом наблюдается высокая частота ложноположительных результатов в популяциях низкого риска (таких как доноры), 14, 17-20 при исследовании длительно хранившихся образцов крови и у больных с гипергаммаглобулинемией. 21-23
Второе поколение тест-систем ELISA является более чувствительным, позволяя обнаруживать антитела к другим вирусным белкам, включая с22 и с33 (табл. 1). 24-26 Антитела к данным антигенам обнаруживаются чаще, чем anti-c100, и появляются в более ранние сроки. Они могут использоваться в диагностике как острой, так и хронической HCV-инфекции. 26-28
Третье поколение тест-систем ELISA сейчас широко используется для скрининга донорской крови, является более чувствительным и специфичным по сравнению с тест-системами ELISA предыдущих поколений 29-30 и дает почти 100% гарантию предотвращения заражения реципиентов донорской крови. Однако антитела могут быть не обнаружены у больных, инфицированных менее 6 месяцев назад, и у больных с иммуносупрессией. Возможны ложноположительные результаты (часто среди доноров). В связи с этим положительные результаты ELISA должны подтверждаться дополнительными тестами.
Табл. 1 Методы выявления антител к вирусу гепатита С (anti-HCV)
| Метод | Выявляемые антитела (кодирующий ген) |
| Скрининговые тесты | |
| I поколения ELISA | anti-c100 (NS4) |
| II поколения ELISA | anti-c22(C), anti-c33+anti-c100[anti-c200] (NS3/NS4) |
| II поколения ELISA | (С, NS3, NS4, NS5) |
| Дополнительные тесты | |
| I поколения RIBA | anti-c100 (NS4), anti-5-1-1 (белки NS3/NS4 регионов) |
| II поколения RIBA | anti-c22(C) ,anti-c33 (NS3), anti-c100 (NS4), anti-5-1-1 (NS3/NS4) |
| II поколения RIBA | (С, NS3, NS4, NS5) |
*Полимеразная цепная реакция (ПЦР), позволяющая выявить, клонировать и определить последовательность генома вируса, имеет наибольшую чувствительность из принятых тестов, позволяя определять РНК вируса даже при низком уровне виремии. ПЦР пока не доступна для широкого применения, имеет ограничения, связанные с возможностью загрязнения и количественным определением; в то же время амплификация вирусного генома дает большое преимущество в выявлении низких концентраций вируса и различий в нуклеотидной последовательности между разными генотипами. Количественное определение HCV РНК стало возможным благодаря адаптированию ПЦР с использованием метода серийных разведений или коамплификации РНК. 5 Новейший метод количественного определения основан на амплификации разветвленной ДНК (bDNA, Chiron). 36-39 Данный метод, выявляющий линейную корреляцию между тест-сигналом и титром вируса (более 3-4 log), более прост в исполнении, 40 но менее чувствителен, 5, 37 чем ПЦР. Результаты исследования могут различаться в зависимости от генотипа вируса. 38 Указанные тесты имеют важное значение при установлении связи титра HCV РНК с инфекциозностью, уровнем аминотрансфераз, тяжестью заболевания и ответом на противовирусную терапию.
HCV РНК. Тест-системы для прямого определения антигенов HCV в сыворотке еще не разработаны, и в настоящее время HCV РНК является лучшим маркером виремии, инфекциозности и активности болезни (см. "Хронический гепатит С. Биохимические показатели, сывороточные маркеры HCV"). Тестирование на HCV РНК проводится в основном в специализированных центрах, однако недавно появились коммерческие наборы для ПЦР. 32 Выявление HCV РНК с помощью ПЦР может подтвердить наличие виремии при отрицательных результатах исследования anti-HCV методами ELISA и RIBA. HCV РНК появляется в крови гораздо раньше других маркеров, обнаруживаясь спустя несколько дней после инфицирования. 33, 34 Следует, однако, отметить, что при циркуляции вируса в низких, подпороговых концентрациях HCV РНК может периодически не определяться. Поэтому суждение об отсутствии виремии на основании единичного отрицательного результата ПЦР не является окончательным.
Гепатит С. Вирус гепатита С. Диагностика гепатита С. Лечение гепатита С. Профилактика гепатита С.
Гепатит С обычно протекает хронически и характеризуется преимущественным развитием хронических форм гепатита с исходом в цирроз и первичную карциному печени. Вирус гепатита С включён в состав рода семейства Flaviviridae.
Резервуар возбудителя гепатита С — инфицированный человек. Основной путь передачи вируса гепатита С — парентеральный. Основное отличие от эпидемиологии вируса гепатита В — более низкая способность вируса гепатита С к передаче от беременной к плоду и при половых контактах.
Больной выделяет вирус гепатита С за несколько недель до появления клинических признаков и в течение 10 нед после начала проявлений. Заболевание чаще регистрируют в США (до 90% всех трансфузионных гепатитов) и Африке (до 25%).
Для клинической симптоматики вирусного гепатита С характерны изменение консистенции и размеров печени. При активном процессе печень обычно увеличена и болезненна при пальпации, её консистенция умеренно плотная. Другие проявления включают спленомегалию, диспепсический и астенический синдромы, желтуху, артралгии и миалгии, кардиты, васкулиты, лёгочные поражения, анемии и др. Осложнения хронического процесса — цирроз и первичная карцинома печени.

Принципы микробиологической диагностики гепатита С
Маркёры репликации вируса гепатита С — AT [IgM) к Аг вируса гепатита С и вирусная РНК. Маркёры гепатита С выявляют методами ИФА и ПЦР.
Показание для поиска AT или РНК вируса гепатита С — любое воспалительное заболевание печени. Вирусспецифические AT появляются в среднем через 3 мес и указывают на возможное инфицирование вирусом гепатита С или на перенесённую инфекцию. В серонегативный период выявляют РНК вируса гепатита С. Для подтверждения результатов ИФА, а также при обследовании пациентов, не относящихся к основным группам риска, применяют метод рекомбинантного иммуноблотинга, позволяющий эффективно исключить ложноположительные результаты ИФА.
Лечение и профилактика гепатита С
Средства этиотропной терапии гепатита С отсутствуют; при хронических инфекциях можно использовать а-ИФН. На фоне терапии ИФН у 40-70% больных отмечают стихание воспалительного процесса (на что указывает снижение содержания концентрации аминотрансфераз в сыворотке), однако по окончании курса у 40-50% пациентов наблюдают рецидив воспаления.
Средства специфической иммунопрофилактики гепатита С не разработаны.
Белки и антигены вируса гепатита С. Диагностика ВГС
Сегодня известно минимум 10 структурных и неструктурных белков, кодируемых геномом HCV. К структурным белкам относят core, envelop 1 и envelop 2. Белок core является белком нуклеокапсида, тогда как envelop 1 и envelop 2 — гликопротеины внешней оболочки вируса. В структурной зоне кодируется также белок р7, функция которого не ясна, однако аналогия с другими представителями семейства Flaviviridae позволяет предположить, что его функция связана с высвобождением вириона из инфицированной клетки.
Этот белок отщепляется клеточной пептидазой от envelop 2, но не во всех случаях, что обусловливает существование envelop 2 в виде двух форм более и менее протяженной.
Неструктурная область генома HCV кодирует 6 белков — NS2, NS3, NS4A, NS4B, NS5A и NS5B. Белок NS2 является вирусной металлозависимой протеиназой. Белок NS4A действует как эффектор или кофактор для NSЗ-протеолитической активности в NS4A/NS4B, NS4B/NS5A, NS5A/NS5B сайтах нарезания полипротеина вируса.
В настоящее время фрагменты структурных и неструктурных белков, полученных генноинженерным путем (рекомбинантные белки) или с помощью химического синтеза, используют в качестве антигенов при конструировании иммуноферментных тест-систем. Первое поколение иммуноферментных тест-систем появилось на рынке в 1989 году и было основано на прямом ИФА. В качестве иммуносорбента были использованы фрагменты двух белков, NS3 и NS4, обозначаемых как 5-1-1 и С100-3.
Одновременно были разработаны и подтверждающие тесты на основе иммуноблота с рекомбинантными белками (RIBA). Чувствительность этих тест-систем первого поколения составляла только 64% для ИФА и 55% для иммуноблота. Тест-системы второго поколения появились на рынке в 1991 году. В качестве антигенов, сорбированных на твердой фазе, в этих тест-системах использовали капсидные белки (фрагмент с22-3) и антигены неструктурных регионов NS3 (фрагменты с200 и сЗЗс) и NS4, что позволило повысить чувствительность и специфичность исследований. Поскольку гуморальный иммунный ответ на капсидные антигены (структурные белки) нагинается быстрее, гем на неструктурные белки, период от инфицирования до выявляемой сероконверсии удалось уменьшить до двух месяцев.
Подтверждающие тест-системы на основе иммуноблота позволяли идентифицировать участвующие в реакции антигены. Результаты, полученные при помощи этих тест-систем, интерпретировали как положительные лишь при реакции антител, находящихся в исследуемом субстрате, по крайней мере, с двумя антигенами, тогда как при наличии реакции лишь с одним из антигенов результат считали неопределенным. Было установлено, что специфичность второго поколения тест-систем зависела от источника антигенов. В 1993 году на рынке появилось третье поколение тест-систем. В дополнение к вышеупомянутым антигенам в этих тест-системах используются также антигены, аминокислотная последовательность которых соответствует иммунодоминантным участкам NS5 белков.
В тест-системах первого, второго и третьего поколений в качестве антигенов использовались или рекомбинантные, или синтетические пептиды. В настоящее время можно выделить также тест-системы четвертого поколения, в которых в качестве иммуносорбента используют сочетания рекомбинантных и синтетических пептидов.
Опыт применения тест-систем различных поколений в мире очень большой. Было установлено, что если с помощью тест-систем первого или второго поколения у больных с острым вирусным гепатитом С антитела выявляли на 10-16, а в ряде случаев и 25-30 неделе от начала заболевания, то диагностикумы третьего поколения позволяли сократить этот срок до 2-3 недель. Согласно обобщенным данным чувствительность тест-систем первого, второго и третьего поколений составляет соответственно 70-80%, 92-95% и 97%.
В то же время, по данным С. Colin, 2001, чувствительность тест-систем третьего поколения составила 98,9% у пациентов с хроническими заболеваниями печени и 97,2% на специальных контрольных панелях сывороток. Достижение высокой чувствительности иммуноферментных тест-систем 3 и 4 поколения сопряжено с некоторыми проблемами в обеспечении специфичности исследований, что в ряде случаев может приводить к появлению ложноположительных результатов. В литературе имеются данные о возможных погрешностях в специфичности ELISA 3 тест-систем. Они являются общими для всех ELISA тест-систем, включая тест-системы для диагностики СПИДа.
Ложнопозитивные результаты могут быть следствием повышенного содержания в образцах гамма-глобулинов (сыворотки пациентов африканской расы, миеломная болезнь, ревматоидные факторы), заболеваний печени (цирроз, рак), аутоиммунных заболеваний (коллагенозы, аутоиммунные гепатиты), других вирусных инфекций (ВИЧ, гепатит В) и длительного хранения сывороток в меняющихся температурных условиях. Проведение какой-либо иммунизации также может сопровождаться повышением частоты ложнопозитивных реакций. Рекомендуемые в настоящее время меры по устранению этой проблемы следующие: а) повторная постановка образца в этой же ИФТС; б) повторная детекция anti-HCV в другой ИФТС; в) использование подтверждающих тестов на основе ИФА и иммуноблота.
Однако использование предлагаемых способов подтверждения результатов зачастую приводят к расхождениям в их итоговой трактовке, что показано исследованиями российских и зарубежных исследователей.
В настоящее время производители ИФТС для детекции anti-HCV достигают высокой чувствительности или за счет более полного выявления антител к NS3 или антител к антигенам core. Сравнительные исследования, выполненные на различных группах риска и специальных контрольных панелях показали, что тест-системы, лучше выявлявшие антитела к NS3, оказались несколько более чувствительными, чем тест-системы, лучше выявлявшие антитела к антигенам core. Их чувствительность составляла, соответственно 99,9% и 98,6%.
Диагностика гепатитов В и С у гематологических больных - анализы, особенности
Современная этиологическая диагностика вирусных гепатитов основана на обнаружении специфических маркеров соответствующих вирусов. Один из методов их выявления — тестирование различных антигенов вируса и антител к ним в ИФА. Наиболее прогрессивна и информативна так называемая генная диагностика: обнаружение вирусной РНК или ДНК с помощью ПЦР.
Для диагностики гепатита В в ИФА исследуют:
1) HBsAg-поверхностный антиген гепатита В, ранее называвшийся австралийским. Он указывает на факт инфицированности гепатитом В;
2) HbeAg — антиген инфекционности, свидетельствующий об активной вирусной репликации;
3) анти-НВс —антитела к ядерному антигену вируса гепатита В: класса IgM—ранние антитела острого периода, класса IgG—поздние антитела к ядерному антигену;
4) анти-НВе — антитела к HBeAg, чаще всего характеризующие прекращение активной репликации вируса (так называемая сероконверсия);
5) анти-HBs—антитела к HBsAg, обеспечивающие протективный иммунитет.
С помощью ПЦР для диагностики гепатита В тестируют ДНК вируса гепатита В — основного маркера репликации вируса.
Для диагностики гепатита С исследуют:
1) с помощью ИФА наличие анти-HCV-антител к вирусу гепатита С (для их выявления желательно использовать тест-системы второго — третьего поколения, отличающиеся большей специфичностью). Они указывают только на инфицированность вирусом гепатита С;
2) с помощью ПЦР наличие РНК вируса гепатита С — основного маркера репликации вируса.
Говоря о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями (ОГЗ), следует рассмотреть вопрос о применимости стандартных подходов к выявлению различных маркеров этих вирусов у данного контингента в связи с возможным нарушением процесса антителообразования на фоне глубокой иммуносу-прессии, развивающейся в ходе полихимиотерапии (ПХТ).
Исследования, в которых сделана попытка подтвердить или опровергнуть роль антительных маркеров у пациентов с онкологическими гематологическими заболеваниями, пока единичны.
Так, в отдельных работах сообщается, что при гепатите В иммуносупрессия нарушает обычную последовательность обнаружения в сыворотке крови антигенов и антител: у больных, которые до начала ПХТ были анти-НВs-позитивными, в процессе лечения могут вновь определяться HBsAg и HBeAg, свидетельствуя о несостоятельности анти-HBs в качестве протективных антител. Угнетение механизмов, ограничивающих вирусную репликацию, ведет к тому, что виремия нередко достигает высокого уровня.
Если антитела к столбняку, дифтерии и полиомиелиту сохраняются во время и после ПХТ, то титры антител к вирусам (ветряной оспы, кори и гепатита В) резко снижаются. Это в большей мере относится к детям с лейкозами, чем с солидными опухолями. Снижение или отсутствие выработки анти-HBs отметили также R. Repp и соавт. и R. Rokicka-Milewska и соавт.. Если при гепатите В эта особенность может отразиться только на ретроспективной диагностике, то для распознавания гепатита С, основанного чаще всего на обнаружении анти-HCV с помощью ИФА, такое положение может иметь принципиальное значение, препятствуя полному и своевременному выявлению всех инфицированных.
Антитела к вирусу гепатита С (анти-HCV) вообще образуются медленно, в течение 8—15 нед от момента инфицирования, но у иммунокомпетентных лиц персистируют в организме длительно и в большинстве случаев пригодны для выявления гепатита С, являясь в настоящее время рутинным и скрининговым маркером.
Некоторые авторы, проводившие немногочисленные и небольшие по объему исследования у иммунокомпрометированных пациентов, указывают на возможность отсроченного образования антител к вирусу гепатита С и считают недостаточным использование только ИФА для диагностики данного заболевания у этого контингента пациентов. В частности, С. Cornu и соавт. обнаружили, что у 5 из 6 обследованных ими иммунокомпрометированных пациентов анти-HCV начали обнаруживаться лишь спустя 14 мес и более от момента инфицирования, установленного с помощью ПЦР.
По данным М. Arico и соавт., антительная диагностика позволяет выявить около 70 % детей с ОЛЛ, инфицированных вирусом гепатита С. Значение ПЦР в выявлении пациентов, инфицированных вирусами гепатитов В и С, продемонстрировано при обследовании турецких детей: у 13,9 % больных с онкологическими гематологическими заболеваниями диагноз гепатита В установлен только при обнаружении ДНК вируса гепатита В, а 5,8 % анти-HCV-негативных детей оказались инфицированными вирусом гепатита С при тестировании РНК.
В то же время синтез анти-НВс IgM, сопутствующий в иммунокомпетентном организме вирусной репликации и являющийся одним из ее маркеров, у пациентов с онкологическими гематологическими заболеваниями почти отсутствует, а у пациентов без онкологических гематологических заболеваний происходит их активная наработка (7,7 % против 78,6 %).
С общебиологической точки зрения, выявленные феномены ждут объяснения, а в прикладном плане они демонстрируют особенности специфической диагностики инфицированности вирусом гепатита В у больных с онкологическими гематологическими заболеваниями и необходимость поиска других подходов к распознаванию болезни. Этой цели служит использование ПЦР, которая позволяет существенно повысить выявляемость пациентов с онкологическими гематологическими заболеваниями, инфицированных вирусом гепатита В: в 16 % случаев обнаружение ДНК этого вируса было единственным маркером инфицирования.
Более того, у 50 % детей, находившихся на полихимиотерапии и позитивных по каким-либо маркерам вируса гепатита В, вирусная ДНК выявлялась в отсутствие HBeAg, т. е. была единственным показателем репликации вируса, в то время как среди детей без онкологических гематологических заболеваний подобная ситуация встречалась лишь в 14,5 % случаев, т. е. в 3,5 раза реже.
При гепатите С также не обнаружено параллелизма между выявлением анти-HCV и РНК вируса гепатита С. Весьма демонстративным было преимущество тестирования РНК перед антительной диагностикой: у 44,4 % детей с онкологическими гематологическими заболеваниями РНК вируса гепатита С оказалась единственным маркером инфицирования.
Как и при гепатите В, диагностическая значимость генных и антительных маркеров зависит от фазы ПХТ. Период интенсивного и поддерживающего лечения онкологического гематологического заболевания при гепатите С — это время абсолютной репликативной активности и резкого снижения антителообразования, способность к которому частично восстанавливается по завершении полихимиотерапии. В наших наблюдениях у 74,9 % детей это сопровождалось продолжением вирусной репликации.
Практические выводы о специфической диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями сводятся к следующему:
1) рутинные подходы недостаточны для распознавания инфицированности пациентов с онкологическими гематологическими заболеваниями вирусами гепатитов В и С;
2) необходимо комплексное исследование всего известного спектра маркеров;
3) ведущую, определяющую роль в диагностике гепатитов В и С у пациентов с онкологическими гематологическими заболеваниями играет тестирование ДНК вируса гепатита В и РНК вируса гепатита С в ПЦР;
4) только путем внедрения ПЦР-диагностики в учреждениях для больных с онкологическими гематологическими заболеваниями можно обеспечить полную и своевременную диагностику гепатитов В и С;
5) обязательность обследования всех пациентов с помощью современных маркеров:
— при поступлении;
— при повышении активности АЛТ на этапах ПХТ;
— каждые 3—6 мес в ходе и в течение года после ПХТ.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое гепатит Е? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит Е — это острое (и редко хроническое) инфекционное заболевание, которое вызывает вирус гепатита Е. Клинически проявляется синдромом общей инфекционной интоксикации, энтерита (воспаления тонкой кишки) и холестаза (застоя желчи), желтухой, увеличением и нарушением работы печени. Болезнь протекает доброкачественно, за исключением беременных, у которых заболевание имеет катастрофические последствия в любом триместре беременности.
Этиология
Вид — вирус гепатита Е (HЕV)
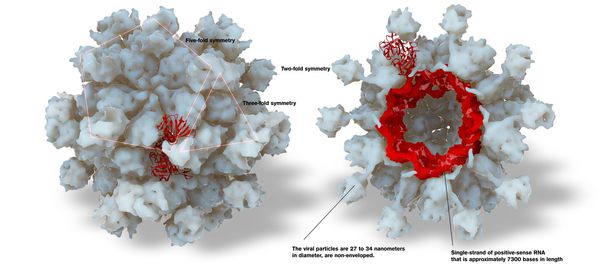
Данный вирус представляет собой одноцепочечный РНК-вирус округлой формы диаметром 30-35 нм. Он лишён наружной оболочки. На поверхности вириона есть вдавления, напоминающие чаши.
Чтобы вирус внедрился в клетку, в процессе жизни он кодирует трансмембранный белок и такие ферменты, как РНК-зависимую РНК-полимеразу, РНК-хеликазу, метилтрансферазу и папаин-подобную протеазу.
Существует пять генотипов вируса:
- I и II — только человеческие;
- III и IV — есть также у животных, т. е. может передаваться от них людям; вызывает хронические формы, если есть предрасположенность;
- V — птичий.
При температуре от 0°C быстро инактивируется. Длительно сохраняется в воде и при отрицательных температурах. Неплохо себя чувствует в ЖКТ человека. Хорошо сохраняется в плохо прожаренном мясе. При нагревании воды до 71°C погибает в течение 20 минут, при кипячении — практически мгновенно [1] [2] [3] [8] [10] .
Эпидемиология
Источник инфекции — вирусоноситель или человек, который уже болен какой-либо формой гепатита Е, в особенности острой. Вирус распространяется с последней недели инкубационного периода и до 30 дней от начала заболевания.
Каждый год повсеместно регистрируется около 3,3 млн случаев заболевания. При этом количество людей с гепатитом Е, который протекает пока без симптомов или совсем себя не проявляет, по предварительным оценкам может достигать 20 млн. Смертность — около 4 %, преимущественно умирают беременные.
В окружающую среду вирус выделяется с экскрементами инфицированных людей. Иногда человек заражается при употреблении недостаточно приготовленного мяса свиней, оленей и моллюсков.
- фекально-оральный — через заражённые вирусом руки (контактно-бытовой путь), воду или пищу;
- парентеральный — при переливании крови (встречается редко);
- половой путь — при орально-анальном контакте;
- вертикальный — от матери к плоду.

Наибольшее значение имеет водный путь передачи. Часто он связан с сезоном дождей и наводнениями, когда вода загрязняется фекалиями.
Восприимчивость к гепатиту Е высокая. Преимущественно болеют люди 15-44 лет. К группе повышенного риска относятся работники животноводческих ферм и боен.
Факторы риска заражения:
- высокая плотность населения, особенно в бедных странах;
- антисанитария, несоблюдение правил личной гигиены, неправильное хранение, обработка и приготовление пищи;
- нарушения санитарно-технических требований на объектах водоснабжения — заражение воды;
- бытовой очаг заболевания.
Заболевание обычно возникает в осенне-весенний период. В основном распространено в странах Восточной и Южной Азии.
После перенесённой болезни формируется стойкий иммунитет, чаще пожизненный [1] [3] [7] [9] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Е
Болезнь начинается постепенно. Инкубационный период длится от 2 до 10 недель.
Как и в случае гепатита А, заболевание обычно протекает в бессимптомной и субклинической (предсимптомной) форме.
При возникновении явных клинических признаков (т. е. при манифестации), преобладают случаи лёгкого и среднетяжёлого течения. Симптоматика медленно нарастает. Появляется немотивированная слабость, подташнивание, снижение аппетита, повышение температуры до 37,1-38,0°С (субфебрилитет), дискомфорт и тяжесть в правом подреберье, дискомфорт в суставах, возможна рвота.
Вслед за этими симптомами через 3-7 дней наступает желтушный период, который длится максимум один месяц. Он сопровождается пожелтением кожи и слизистых оболочек, потемнением мочи и обесцвечиванием кала. Общее состояние больных не улучшается, сохраняется плохое самочувствие, выраженный дискомфорт в правом подреберье, увеличение размеров печени и селезёнки, желтушность кожных покровов, нарастает зуд кожи.
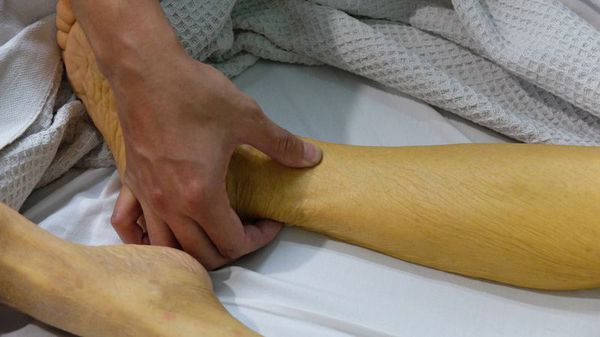
При неосложнённом и нетяжёлом течении начинает медленно регрессировать в течение нескольких недель. Как правило, после этого человек полностью выздоровливает, иногда развиваются непродолжительные остаточные явления в виде астении (бессилия) и дискомфорта в правом подреберье.
Раньше считалось, что гепатит Е — лишь острое заболевание. Однако в последнее время накоплен ряд данных, позволяющих выделить небольшую группу больных, переносящих хронический вариант болезни. Он встречается у ВИЧ-инфицированных людей в стадии СПИДа, после пересадки органов, а также у тех, кто получает мощную иммуносупрессивную терапию.
Специфичной симптоматики у хронического гепатита А нет. Больные жалуются на повышенную утомляемость, артралгии, неустойчивый стул, тяжесть в правом подреберье, субфебрилитет, иногда устойчивый лёгкий зуд кожи. Если не лечить это состояние, может развиться цирроз печени.
Гепатит Е у беременных
При заражении беременной в I и II триместрах происходит 100 % гибель плода. Летальность самих беременных невелика.
При заражении беременной в III триместре ребёнок может родиться живым, но 50 % из них умирают в первые месяцы жизни. Смертность самих женщин достигает 25-30 %. А если беременные живут в районах, которым не свойственно данное заболевание, то летальность может достигать 80 %.
Тяжесть течения Гепатита А при беременности связана со специфической аутоиммунной перестройкой организма женщины. В этом случае заболевание часто протекает по фульминантному типу (острой печеночной недостаточности) — на фоне начальных симптомов болезни резко нарастает желтуха, развивается тяжёлая интоксикация, некупируемая рвота, кровотечения (ДВС-синдром), нарушается сознание. Роды (преждевременные или выкидыш) стремительно ухудшают состояние больной: развиваются массивные послеродовые кровотечения, острая почечная недостаточность, печеночная энцефалопатия. Из-за такого состояния в острый период искусственно прерывать беременность нельзя [1] [5] [6] [8] [9] .
Патогенез гепатита Е
В цитоплазме гепатоцитов внешняя оболочка вируса вируса раскрывается, и запускается выработка вирусных белков. Одновременно с этим происходит подготовка клетки-хозяина к этому процессу.
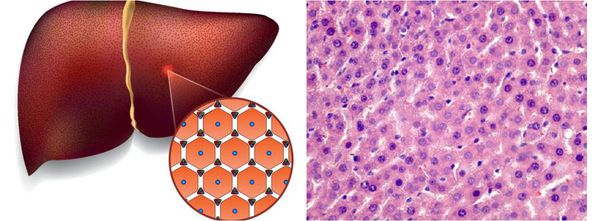
Во время своей жизни вирус напрямую провоцирует дегенеративные изменения в гепатоцитах, в т.ч. вызывая их гибель по типу баллонной дистрофии — переполнение клетки жидкостью. После этого готовые вирусные частицы распространяются и заражают новые здоровые клетки.
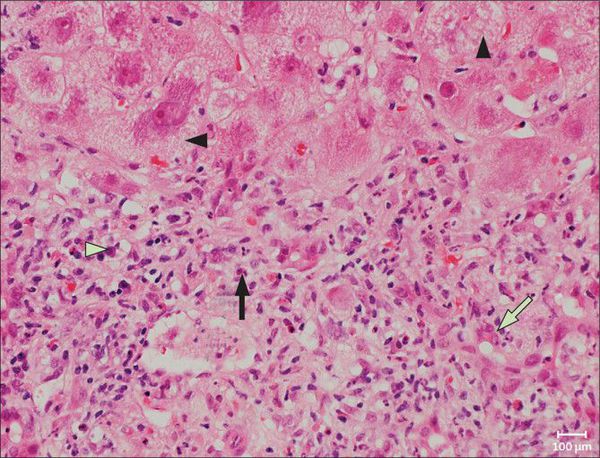
Со временем в организме формируются специфические антитела, которые позволяют полностью вывести вирус из организма человека (за исключением случаев выраженного угнетения иммунитета).
Тяжёлое течение гепатита Е у беременных не связано со свойствами вируса напрямую. Оно вызвано лишь иммунологической перестройкой иммунной защиты беременных. Из-за этого развивается каскад иммунопатологических и гормональных реакций, которые приводят к массированному некрозу гепатоцитов, дефициту плазменных факторов свёртывания и внутрисосудистому гемолизу — разрушению эритроцитов крови [1] [2] [3] [5] [10] .
Классификация и стадии развития гепатита Е
По клиническим признакам выделяют два варианта заболевания:
- безжелтушная форма — до появления симптомов или при освобождении организма от вируса и формировании стойкого иммунитета;
- желтушная форма — при нарастании симптомов.
По тяжести процесса гепатит Е делят на четыре степени:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная, гепатит у беременных).
Факторы риска развития тяжёлого течения болезни:
- беременность любого триместра (наиболее неблагоприятно заболевание протекает в III триместре);
- пожилой возраст:
- мужской пол;
- иммуносупрессивная терапия (на фоне трансплантации органов); ;
- комбинированная соматическая патология (сахарный диабет, ишемическая болезнь сердца, аутоиммунный гепатит, пациенты на гемодиализе);
- наличие хронической вирусной патологии печени (вирусные гепатиты В и С);
- алкоголизм.
По исходу заболевание бывает трёх типов:
- с выздоровлением (полным, с остаточными явлениями);
- с хронизацией;
- с неблагоприятным прогнозом (у беременных) [4][5][6] .
Осложнения гепатита Е
Осложнения при гепатите Е можно разделить на три группы:
- Истинные (печёночные) осложнения:
- острая печёночная недостаточность — осложнение с неблагоприятным исходом, при котором быстро развивается массивное повреждение ткани печени (до 90 %), резкое нарушаются её функции, возникает печёночная энцефалопатия (нарушение работы мозга), геморрагический синдром (повышенная кровоточивость) и коагулопатия (нарушение свёртывания крови);
- холестаз — нарушение синтеза и выведения желчи (желтуха), осветление кала и потемнение мочи, появление выраженного кожного зуда и чувства горечи во рту;
- тромбо-геморрагический синдром у беременных (ДВС-синдром) — кровотечения и кровоизлияния различной интенсивности и направленности;
- преждевременные роды или выкидыш у беременных.
- Внепечёночные осложнения: — острое неврологическое заболевание, которое сопровождается нарушением чувствительности в руках и ногах, мышечной слабостью и иногда параличом.
- острый поперечный миелит — нарушение всех функций спинного мозга;
- различные нейропатии и полирадикулопатии;
- панкреатит — тошнота, рвота, опоясывающие боли в животе; — боли в поясничной области, нарушение мочеобразования, повышенная потеря эритроцитов и белка с мочой;
- повышение вероятности развития рака кожи и заболеваний кровеносной системы.
- Резидуальные (постгепатитные) явления:
- дискинезия (нарушение моторики) желчевыводящих путей — застой желчи, чувство тошноты, отрыжка, горечь во рту;
- постгепатитная гепатомегалия — увеличение печени в связи с разрастанием соединительной ткани;
- постгепатитный синдром — повышенная утомляемость, астения, раздражительность, чувство тошноты и дискомфорта в правом подреберье [1][2][6][7][8] .
Диагностика гепатита Е
Лабораторная диагностика:
- Клинический анализ крови — нормальный объём эритроцитов или умеренная лейкопения, повышение количества лимфоцитов, моноцитов и снижение нейтрофилов в крови, сниженная или нормальная СОЭ.
- Биохимический анализ крови — повышенный уровень общего билирубина за счёт прямой и непрямой фракции, увеличение АЛТ и АСТ, сниженый индекс протромбина (ПТИ), повышение тимол-вероналоовой пробы (уменьшение альбуминов и увеличение гамма-глобулинов), повышение ГГТ и щелочной фосфатазы.
- Общий анализ мочи — появление гематурии, протеинурии и цилиндрурии (обнаружение эритроцитов, белка и цилиндров в моче).
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина.
- Серологические тесты — обнаружение антител в сыворотке крови:
- анти-HЕV IgM — выявляются при острой инфекции с конца первой недели от момента заражения, могут сохраняться до двух лет, иногда бывают ложноположительными при активной ЦМВ-инфекции;
- анти-HЕV IgG — выявляются с 41 дня в течение 15 лет методом иммуноферментного анализа (ИФА);
- HЕV RNA — выявляются при острой инфекции, начиная с 22 дня, а также при хронизации в течение долгого времени благодаря полимеразной цепной реакции (ПЦР).
- УЗИ органов брюшной полости — увеличение печени с реактивным изменением структуры её ткани, увеличение лимфоузлов в воротах печени, иногда увеличена селезёнка.
Дифференциальная диагностика с другими заболеваниями:
- Вирусные гепатиты В и С — связь с парентеральными вмешательствами (например, с переливанием крови), более длительный преджелтушный период, характерные серологические тесты. , желтушная форма — выраженный синдром общей инфекционной интоксикации, увеличение лимфоузлов, тонзиллит, специфические изменения общей крови и серологические тесты.
- Жёлтая лихорадка — острое начало, высокая температура, гиперемия и отёчность лица, временное улучшение, а затем ухудшение состояния. — острое начало, высокая температура, частое поражение почек, выраженные боли в икроножных мышцах, изменения общей крови бактериального характера.
- Псевдотуберкулёз — умеренно высокая температура, мезаденит (воспаление лимфоузлов брыжейки кишечника), терминальный илеит (воспаление подвздошной кишки), симптомы носков и капюшона (мелкоточечные высыпания), скарлатиноподобная сыпь, бактериальные изменения крови, специфические маркеры.
- Острые кишечные инфекции, например, сальмонеллёз — острое начало, выраженный синдром поражения ЖКТ (энтерит, колит, высокая температура).
- Листериоз — высокая температура, увеличение лимфоузлов, поражения железистой ткани ротоглотки, бактериальная кровь.
- Сепсис — гектическая (изнуряющая) лихорадка, выраженные полиорганные нарушения.
- Амебиаз — характерные симптомы поражения кишечника, эозинофилия крови, выявления возбудителя.
- Токсические поражения печени — связь с употреблением токсинов, отсутствие синдрома общей инфекционной интоксикации.
- Опухоли гепатобилиарной области — длительное постепенное начало, отсутствие яркой выраженной симптоматики, умеренное повышение АЛТ или АСТ, резкое повышение СОЭ, характерные изменения на УЗИ, КТ или МРТ. — типичные болевые приступы, умеренное повышение АЛТ или АСТ, данные инструментальных исследований [1][2][6][8][10] .
Лечение гепатита Е
При лёгкой степени гепатита Е лечение проводится в амбулаторных условиях (на дому). Во всех остальных случаях показано стационарное лечение в инфекционном отделении больницы. Режим постельный или полупостельный.
Чтобы снизить нагрузку на поражённую печень, необходимо придерживаться механически и химически щадящей диеты № 5 по Певзнеру. Она подразумевает употребление витаминов и повышенного количества воды (более 1,5 л в сутки), исключение алкогольных и газированных напитков, жаренной и острой пищи, грибов, сдобного теста и других продуктов.
Специфического лечения, которое бы устраняло причины гепатита Е, нет. В основном все методы направлены на устранение симптомов, интоксикации и восстановление нормальной функции печени.
Показан приём сорбентов и препаратов, которые повышают энергетические ресурсы. Иногда назначают гепатопротекторы. Если случай тяжёлый, то проводится терапия гормональными средствами и препаратами крови, а также гипербарическая оксигенация (использование кислорода под высоким давлением) и плазмаферез.
Назначение инфузионной терапии — внутривенного введения глюкозо-солевых растворов и витаминов — зависит от степени тяжести и определённых симптомов.
При тяжёлом течении и хронизации возможно применение препаратов общевирусного действия. Они позволяют снизить вирусную нагрузку.
Людям, получающим цитостатическую (противоопухолевую) терапию по возможности следует снизить дозу на 30 %. Это повышает вероятность спонтанной гибели вируса.
Беременные с гепатитом Е должны находиться в условиях реанимации инфекционного стационара. В острый период болезни лечение проводится по общим принципам, преждевременное родоразрешение противопоказано.
Выписывать больных можно в том случае, если в ходе лечения у них стойко улучшается клиническая картина и лабораторные показатели. После выписки пациенты, которые идут на поправку после неосложнённых форм болезни, находятся под наблюдением врача в течение шести месяцев. Осмотр и обследования проводятся минимум один раз в месяц [5] [6] [8] [9] .
Прогноз. Профилактика
Прогноз гепатита Е зачастую благоприятный, за исключением случаев заболевания при беременности. После выписки из больницы окончательное выздоровление наступает спустя 2-3 месяца. Крайне редко болезнь может стать хронической и затяжной.
Чтобы снизить количество случаев инфицирования, необходимо придерживаться следующих правил:
- создавать все условия для того, чтобы потребляемая питьевая вода была безопасной (касается водоснабжения);
- соблюдать правила утилизации сточных вод (канализационное хозяйство);
- соблюдать правила личной гигиены (всегда мыть руки);
- следить за качеством обследования работников, которые связаны с пищевой промышленностью;
- соблюдать технологию хранения, приготовления и транспортировки продуктов питания и воды;
- беременным на любом сроке стоит воздержаться от поездок в потенциально опасные в эпидемиологическим плане места (тёплые страны, особенно Азиатского региона).

Для предотвращения развития болезни разработана специфическая профилактика — вакцинация против гепатита Е. С этой целью применяется вакцина Hecolin (Китай). Она вырабатывает иммунитет к одному генотипу у 95 % трехкратно привитых людей [1] [2] [3] [5] [8] .
Читайте также:

