Ифа гепатит в производители
Обновлено: 07.05.2024
Набор предназначен для одновременного выявления антител классов G и М к вирусу гепатита С (ВГС) в сыворотке или плазме крови человека “in vitro” методом непрямого твердофазного иммуноферментного анализа.
2.1 Состав набора:
Положительный контрольный образец (К + )
Отрицательный контрольный образец (К – )
Раствор для разведения конъюгата (РР-К)
2 флакона по 13 мл
Раствор для разведения сывороток (РР-С)
Буферный раствор для субстрата (БРС)
2 флакона по 13 мл
25-кратный концентрат фосфатно-солевого буферного раствора с твином (ФСБ-Т×25)
2 флакона по 28 мл
Комплект ванночки для реагентов с наконечниками для многоканальных пипеток
2.2 Основные компоненты набора "ИФА-антиHСV" – иммуносорбент и конъюгат (раствор конъюгата).
Иммуносорбент представляет собой полистирольный планшет, в лунках которого сорбирована смесь рекомбинантных антигенов “core”, “NS3” и “NS5” и синтетических пептидов “NS4”, являющихся аналогами антигенов NS3, NS4, NS5 и Сore вируса гепатита С:
а) антиген “core” представляет собой синтезированный в E. coli рекомбинантный антиген, содержащий аминокислотную последовательность антигенных детерминант корового (нуклеокапсидного) белка ВГС;
б) антиген “NS3” представляет собой синтезированный в E. coli рекомбинантный антиген, содержащий аминокислотную последовательность антигенных детерминант неструктурного белка NS3 ВГС;
в) антиген “NS4” представляет собой синтетический пептид, соответствующий антигенным детерминантам NS4 ВГС, характерный для генотипов 1в, 2в, 3а;
г) антиген “NS5” представляет собой синтезированный в E. coli рекомбинантный антиген, содержащий аминокислотную последовательность антигенных детерминант неструктурного белка NS5 ВГС.
Конъюгат (раствор конъюгата) представляет собой смесь моноклональных антител мыши к IgG человека, конъюгированных с пероксидазой хрена и моноклональных антител мыши к IgМ человека, конъюгированных с пероксидазой хрена.
Положительный контрольный образец – сыворотка крови человека, содержащая антитела к ВГС и не содержащая антитела к ВИЧ-1 и ВИЧ-2 и НВs-антиген, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Отрицательный контрольный образец – сыворотка крови человека, не содержащая антитела к ВГС, ВИЧ-1, ВИЧ-2 и НВs-антиген, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Принцип работы набора. При внесении в лунки планшета образцов исследуемых сывороток антитела, специфические к вирусу гепатита С, связываются с антигенами на твердой фазе, образуя иммунные комплексы антиген-антитело. Образовавшиеся комплексы выявляют при помощи специфического иммуноферментного конъюгата. После отмывания несвязавшихся компонентов в лунки планшета добавляют раствор субстрата пероксидазы (перекись водорода) и хромогена ТМБ.
Пероксидазную реакцию останавливают, добавляя стоп-реагент (0,9 М раствор серной кислоты), и интенсивность окрашивания раствора в лунках измеряют на спектрофотометре как величину оптической плотности (ОП) при длине волны 450 нм.
Величина ОП прямо пропорциональна концентрации специфических антител в образце сыворотки или плазмы крови человека. Чем выше содержание антител в образце сыворотки, тем выше интенсивность окрашивания.
2.3 Набор рассчитан на проведение 24 постановоки ИФА: 1 постановка – 1 стрип (8 лунок). Всего – 192 определения, включая контрольные образцы.
3.1 Все компоненты набора в используемых концентрациях являются нетоксичными. Однако работа со всеми исследуемыми образцами сыворотки (плазмы) крови человека, которые следует рассматривать как потенциально инфицированные, способные сохранять и передавать ВИЧ, вирус гепатита В или любой другой возбудитель вирусной инфекции, с отработанными растворами и жидкостями, различным оборудованием, которое может быть загрязнено в процессе анализа, требует определенных мер безопасности при использовании набора:
- работу необходимо проводить в специально оборудованном помещении;
- работать необходимо с применением средств индивидуальной защиты и с соблюдением мер предосторожности в соответствии с требованиями [1], [2], и [3].
3.2 Стоп-реагент, содержащий серную кислоту, обладает раздражающим действием. При попадании на кожу и слизистые немедленно промыть большим количеством воды.
3.3 При работе с набором рабочие места должны быть обеспечены приточно-вытяжной вентиляцией.
3.4 Все лица, работающие в лаборатории с наборами, должны проходить обязательный медицинский осмотр в соответствии с требованиями [4].
3.5 Утилизация медицинских отходов и/или неиспользованных наборов с истекшим сроком годности должна производиться в соответствии с требованиями [5].
4.1 Для исключения ложных результатов исследуемые образцы необходимо готовить и хранить в условиях, предотвращающих бактериальный пророст. Необходимо осветлять образцы сывороток, содержащие агрегированные компоненты сыворотки или осадок, при помощи центрифугирования в течение 15 мин при скорости вращения 3000 об/мин. Образцы сывороток можно хранить при температуре (2-8) °С не более 48 ч. Замороженные образцы (желательно до температуры не менее минус 20 °С) можно хранить не более 3 месяцев. Необходимо избегать повторных циклов замораживания-оттаивания образцов.
Необходимо помнить, что образцы с гемолизом, гиперлипидемией, бактериальным проростом, а также длительно хранившиеся без замораживания не пригодны для анализа.
Надежность результатов зависит от выполнения следующих правил:
- не допускается использование набора после окончания срока годности, а также смешивание компонентов наборов разных серий;
- для приготовления каждого реагента должна использоваться отдельная емкость;
- всю используемую для приготовления реагентов посуду не обрабатывать дезрастворами и моющими средствами. В случае необходимости промыть водой питьевой проточной, а затем пять раз ополоснуть дистиллированной водой;
- для работы с хромогеном ТМБ и РХ необходимо использовать отдельные емкости для растворов, наконечники для пипеток, посуду.
- необходимо обратить внимание на тщательное перемешивание реагентов;
- время между заполнением и опорожнением лунок планшета растворами и реагентами должно быть не менее 30 с. Не допускается подсыхание лунок на всех этапах постановки ИФА;
- при использовании промывателя следить за состоянием емкости для раствора для промывания планшета и соединительных шлангов: в них не должно быть признаков бактериального или грибкового роста;
- необходимо использовать пипетки автоматические со сменными наконечниками, аттестованные по значению средней дозы и сходимости результатов пипетирования (погрешность не более 3%);
- дозаторы и рабочие поверхности обрабатывать раствором с объемной долей спирта этилового 70 %. Не использовать хлорамин и другие хлорсодержащие вещества;
- для работы с исследуемыми сыворотками и контрольными образцами рекомендуется использовать одноразовые наконечники для пипеток. Каждый образец сыворотки, а также реагенты набора необходимо отбирать отдельным наконечником.
- во время проведения анализа следует избегать попадания прямых солнечных лучей на рабочую поверхность.
5.1 Спектрофотометр вертикального сканирования, позволяющий проводить измерения оптической плотности растворов в лунках планшета при длине волны 450 нм;
- полу- или автоматическое устройство для промывания планшетов (вошер);
- суховоздушный термостат типа ТС-80 М2, поддерживающий температуру (37±1) °С, или аналогичный ему по характеристикам;
- пипетки одноканальные автоматические со сменными наконечниками, позволяющие отбирать объемы жидкости от 0,02 до 5,0 мл;
- мерный цилиндр вместимостью 1000 мл;
- колба лабораторная вместимостью 1000 мл;
- флаконы стеклянные вместимостью 20 мл;
- ванночки для реагентов или чашки Петри (диаметр 100 мм);
- вата медицинская гигроскопическая;
- перчатки резиновые хирургические;
- раствор с объемной долей спирта этилового 70 %;
- раствор с массовой долей перекиси водорода 6 %;
- вода деионизированная или дистиллированная;
- контейнер для сбора твердых отходов;
- контейнер для слива жидких отходов.
Все образцы сыворотки (плазмы) крови человека и реагенты перед проведением анализа тщательно перемешать.
Расход реагентов набора для постановки анализа, который определяется количеством используемых стрипов, приведен в таблице А1 Приложения А.
6.2 Подготовка иммуносорбента
Иммуносорбент готов к использованию.
Открыть пакет и установить на рамку необходимое количество стрипов. Оставшиеся стрипы хранить в плотно закрытом пакете с влагопоглотителем при температуре (2-8) °С в течение 3 месяцев.
6.3 Приготовление раствора для промывания планшета
Внимание! Раствор для промывания планшета готовить за 15 мин до начала проведения анализа!
Если флакон с ФСБ-Т×25 содержит осадок, его необходимо прогреть перед использованием при температуре (37±1) °С до полного растворения осадка.
В мерный цилиндр вместимостью 1000 мл внести содержимое флакона с ФСБ-Т×25, затем добавить дистиллированной воды до метки 700 мл и аккуратно перемешать раствор. Раствор можно хранить при температуре (2-8) °С в течение 72 ч.
В случае использования одного или несколько стрипов содержимое флакона с ФСБ-Т×25 интенсивно встряхнуть в течение (20-30) с, отобрать необходимый объем раствора (таблица А.1 Приложения А) в мерный стакан или цилиндр, добавить необходимое количество дистиллированной воды и перемешать раствор.
Неиспользованный ФСБ-Т×25 можно хранить в закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.4 Подготовка К + , К – ,РР-К, РР-С, БРС и стоп-реагента
К + , К – ,РР-К, РР-С, БРС и стоп-реагент готовы к использованию.
Внимание! Во флаконах с РР-С и РР-К возможно выпадение осадка. Перед использованием содержимое флаконов тщательно перемешать, не допуская образования пены.
Неиспользованные РР-С, РР-К, БРС и стоп-реагент после вскрытия флаконов можно хранить в закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
Остаток К + и К - после вскрытия флакона можно хранить в закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
6.5 Приготовление раствора Кг в рабочем разведении
Из флакона с Кг отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с РР-К. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон отобрать необходимое количество РР-К, добавить Кг в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Остаток Кг можно хранить в закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.6 Приготовление рабочего раствора субстрата
Если флакон с хромогеном ТМБ содержит кристаллы, его необходимо прогреть перед использованием в течение (3-5) мин при температуре (37±1) °С до полного растворения кристаллов.
Из флакона с хромогеном ТМБ отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с БРС. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон из темного стекла или пластика (прозрачный флакон обернуть флакон) отобрать необходимое количество БРС, добавить хромоген ТМБ в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Раствор необходимо предохранять от попадания света и контакта с металлами или ионами металлов. Перед использованием раствор субстрата должен быть бесцветным. Посуду, которая будет в ходе реакции контактировать с раствором субстрата, отмывать без применения синтетических моющих средств. Использовать только новую ванночку для реагентов и новые наконечники!
Остаток хромогена ТМБ можно хранить в закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
- на всех этапах промывания необходимо контролировать заполнение всех лунок и полное удаление (аспирацию) жидкости из них;
- необходимо при каждом промывании все лунки заполнить раствором до краев (0,30-0,35 мл в лунку), без переполнения и перетекания жидкости из соседних лунок;
- необходимо выдерживать лунки, заполненными раствором для промывания планшета, в течение 30 с;
- при каждой аспирации тщательно удалять остатки жидкости из лунок постукиванием рамкой со стрипами в перевернутом положении по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена;
- некачественное промывание планшета приводит к получению некорректных результатов.
8.1 Промыть лунки планшета раствором для промывания планшета (п 6.3) один раз. При промывании во все лунки необходимо внести (0,30-0,35) мл раствора. По окончании промывания тщательно удалить остатки жидкости из лунок, постукивая планшетом в перевернутом положении по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена.
8.2 В любые две лунки планшета внести по 0,1 мл (100 мкл) К + , в три другие лунки планшета – по 0,1 мл (100 мкл) К – , в одну лунку внести 0,1 мл (100 мкл) РР-С для контроля конъюгата (ККг).
Внимание! При постановке ИФА на одном стрипе допускается использовать для К – – две лунки, для К + – одну лунку, для ККг – одну лунку.
В остальные лунки планшета внести по 0,06 мл (60 мкл) РР-С, затем внести по 0,04 мл (40 мкл) исследуемых образцов сыворотки (плазмы) крови человека. Содержимое лунок перемешать пять раз пипетированием, при этом при этом цвет РР-С должен измениться.
Внимание! Время внесения контрольных и исследуемых образцов не должно превышать (5-10) мин! Каждый образец необходимо отбирать одноразовым наконечником!
8.3 Планшет заклеить пленкой или закрыть крышкой и инкубировать в термостате при температуре (37±1) °С в течение 30 мин.
Внимание! За (1-2) мин до окончания инкубации приготовить раствор Кг в рабочем разведении (п 6.5).
8.4 Удалить содержимое лунок с помощью промывателя, затем промыть лунки планшета раствором для промывания планшета (п 6.3) пять раз.
8.5 Внести во все лунки планшета по 0,1 мл (100 мкл) раствора РК или раствора Кг в рабочем разведении (п 6.5) в зависимости от комплектации набора.
8.6 Планшет заклеить пленкой или закрыть крышкой и инкубировать в термостате при температуре (37±1) °С в течение 30 мин.
8.7 Удалить содержимое лунок планшета с помощью промывателя, затем промыть лунки планшетов раствором для промывания планшета (п 6.3) пять раз.
8.8 Во все лунки планшета внести по 0,1 мл (100 мкл) рабочего раствора субстрата (п 6.6) или РХ в зависимости от комплектации набора.
8.9 Планшет заклеить пленкой или закрыть крышкой и инкубировать в термостате при температуре (37±1) °С в защищенном от света месте в течение 15 мин.
Внимание! По окончании инкубации в лунках с образцами сывороток, содержащими антитела к ВГС, произойдет изменение окраски раствора различной интенсивности в зависимости от концентрации антител в исследуемом образце сыворотки: от бесцветной до голубой (при использовании рабочего раствора субстрата) или от розовой до синей (при использовании РХ).
8.10 Остановить пероксидазную реакцию путем внесения во все лунки по 0,05 мл (50 мкл) стоп-реагента.
Внимание! В лунках с образцами сывороток, содержащими антитела к ВГС, произойдет изменение окраски раствора: с голубой на желтую (при использовании рабочего раствора субстрата) или с синей на желтую (при использовании РХ).
8.11 Не позже чем через 40 мин после остановки реакции определить значение ОП раствора в лунках:
- при использовании РХ – в двухволновом режиме: 450 нм относительно (620-700) нм. Допускается измерение ОП в одноволновом режиме при длине волны 450 нм.
- при использовании рабочего раствора субстрата – в одноволновом режиме при длине волны 450 нм.

На нашем YouTube-канале опубликована серия видео по ИФА-диагностике респираторных инфекций. Подробнее
Новый набор для дифференциального выявления IgG к S- и N-белкам SARS-CoV-2. Подробнее
HBsAg-ИФА-БЕСТ (комплект 1/авто)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-ИФА-БЕСТ (комплект 2)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-ИФА-БЕСТ (комплект 3)
Набор реагентов для иммуноферментного выявления HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
HBsAg-подтверждающий-ИФА-БЕСТ
Набор реагентов для иммуноферментного подтверждения присутствия HBs-антигена вируса гепатита В.
Срок годности: 12 месяцев
Вектогеп B-HBs-антиген-авто (комплект 1)
Набор реагентов для иммуноферментного выявления HBsAg для автоматических ИФА анализаторов.
Вектогеп B-HBs-антиген-авто (комплект 2/Чароит)
Набор реагентов для иммуноферментного выявления HBsAg для автоматических ИФА анализаторов.
Вектогеп B-HBs-антиген (комплект 1)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 2)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 3)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп B-HBs-антиген (комплект 4)
Набор реагентов для иммуноферментного выявления HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 1)
Набор реагентов для иммуноферментного подтверждения наличия HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
Вектогеп В-HBs-антиген-подтверждающий тест (комплект 2)
Набор реагентов для иммуноферментного подтверждения наличия HBsAg. Одностадийная постановка.
Срок годности: 24 месяцев
HBsAg-ИФА-БЕСТ-количественный
Набор реагентов для иммуноферментного количественного определения HBs-антигена вируса гепатита В в сыворотке (плазме) крови
Диапазон измерений: 0 - 10 МЕ/мл (нг/мг)
ВектоHBsAg-антитела
Набор реагентов для иммуноферментного качественного и количественного определения антител к HBs-антигену вируса гепатита В в сыворотке (плазме) крови.
ВектоHBcAg-IgМ
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса М к core-антигену вируса гепатита В.
ВектоHBcAg-антитела
Набор реагентов для иммуноферментного выявления суммарных антител к core-антигену вируса гепатита В.
ГепаБест анти-HBc-IgG
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к core-антигену вируса гепатита В в сыворотке (плазме) крови.
ВектоHBe-антиген
Набор реагентов для иммуноферментного выявления E-антигена вируса гепатита В в сыворотке (плазме) крови.
ВектоHBe-IgG
Набор реагентов для иммуноферментного выявления иммуноглобулинов класса G к HВe-антигену вируса гепатита В.
Набор для внутрилабораторного контроля качества ИФА "Сыворотка, содержащая НВsАg".
HBsAg-стандартная панель сывороток
Набор образцов сывороток крови, содержащих разные субтипы и мутантные формы HBsAg вируса гепатита В.
Вирус гепатита B (HBV) принадлежит к новому семейству ДНК вирусов Hepadnaviridae. К его особенностям относятся поразительный гепатотропизм и уникальный способ репликации с использованием механизма обратной транскрипции. Собранный вирион или частица Дейна состоит из кольцевой молекулы ДНК, защищенной ядерным капсидом/коровым антигеном (HBcAg). Внешняя оболочка вируса образована поверхностным антигеном (HBsAg). HBsAg также обнаруживается в сыворотке в виде неинфекционных сферических частиц или нитей. Малые компоненты HBV- нуклеакапсиды, HBe антиген (HBeAg) также можно обнаружить в крови во время репликативной фазы вируса.
HBV является широко распространенным по всему миру вирусом. В Москве, как и в целом по России, в последние годы отмечается рост заболеваемости парентеральными вирусными гепатитами [158].
Основные пути заражения: горизонтальный - половое и парентеральное заражение, и вертикальный - перинатальная передача от инфицированной матери плоду. Клинические последствия от заражения гепатитом B варьируют от полностью неразличимых (70% случаев) до острых гепатитов. Большинство пациентов полностью выздоравливают в течение 6 месяцев с начала заболевания. У небольшой доли инфицированного населения (<1.5%) могут развиться скоротечные гепатиты, часто с фатальным исходом. У значительной части (до 10%) взрослого населения HBV может сохраниться, постепенно развиваясь в хронический гепатит, конечным этапом развития которого будет цирроз и / или карцинома печени. Хронические носители вируса гепатита B (350 миллионов по всему миру) составляют основной его резервуар вируса и являются основным источником распространения болезни.
Перинатальная передача HBV инфекции от инфицированной матери к ее ребенку является одним из наиболее значимых путей распространения гепатита В. Около 70-95% случаев перинатальной передачи происходит во время родов, однако, 5% новорожденных детей заражаются антенатально, т.е. еще в утробе матери [159]. Перинатальная передача HBV возможна: -через поврежденную плаценту, когда может происходить смешивание крови матери и плода; -во время прохождения ребенка через родовые пути в результате повреждения кожи и слизистых оболочек, или при заглатывании материнской крови; - в результате контакта ребенка с кровью матери при родах путем кесарева сечения.
Все беременные женщины должны обследоваться на наличие HBs Ag 2 раза в течение беременности: 1-ый раз – в первом триместре, 2- ой раз – в третьем триместре.
Выявление HBsAg у беременной женщины не является показанием к искусственному прерыванию беременности или родоразрешению с помощью кесарева сечения.
Сроки заболевания HBV-инфекцией во время беременности и наличие маркеров высокой инфекционности (HBsAg) являются важными факторами, определяющими перинатальную передачу ВГВ. У HBsAg-положительных матерей вероятность перинатального инфицирования своего ребенка составляет от 70 до 90% [158]. Почти 90% из этих перинатально инфицированных детей могут стать хроническими носителями или развить в будущем хронический гепатит В (30-35%). У детей, родившихся от матерей, не имеющих маркера высокой инфекционности (HBsAg), риск перинатальной передачи значительно ниже - менее 10%.
Горизонтальная передача HBV-инфекции возможна при тесных контактах матери и ребенка, особенно в первые месяцы, годы жизни и связана с микротравматизацией слизистых и кожных покровов. Следует учитывать, что при отсутствии повреждений молочной железы у родильницы, ребенок может находиться на грудном вскармливании.
Дети, родившиеся от матерей с HBs-антигеном, относятся к группе высокого риска должны быть вакцинированы. Биохимические исследования крови и исследования на HBs-антиген назначаются ребенку в 6-12 месяцев.
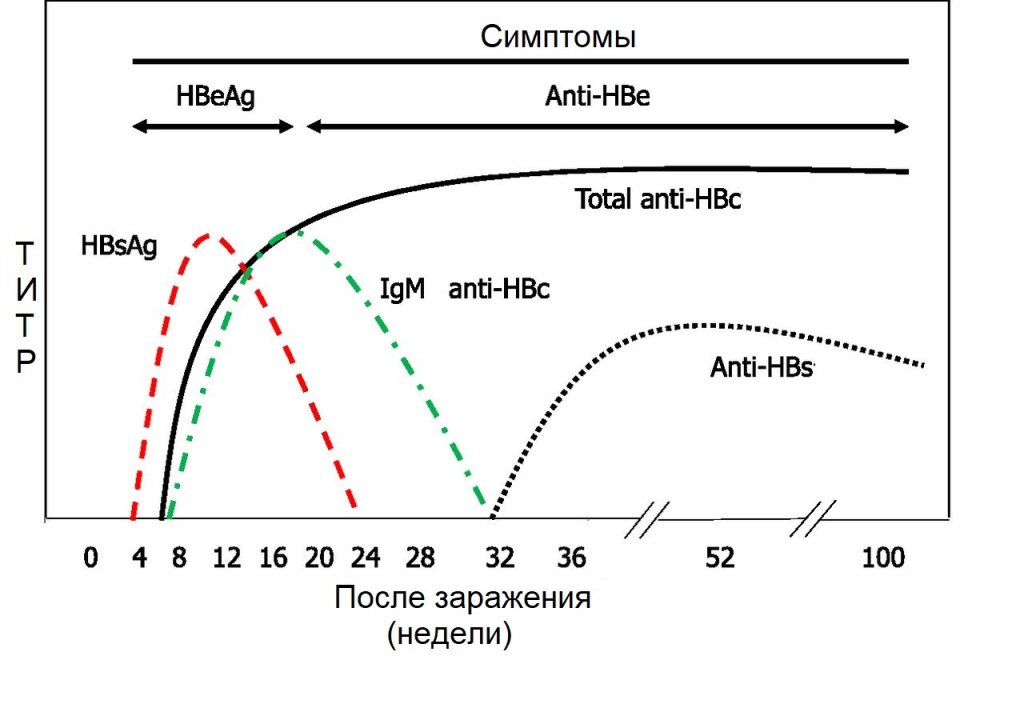
В типичных случаях острой HBV инфекции HBsAg, часто в сопровождении HBcAg, появляется в крови за 2-6 недель до появления симптомов или биохимических признаков гепатита и достигает максимума во время острой фазы заболевания. Присутствие HBsAg в сыворотке более 6 месяцев отражает статус хронического носителя HBV. Поэтому, скрининг по HBsAg, позволяет выявлять HBV инфицированных пациентов и помогает в диагностировании и прогнозировании течения болезни (Рис. 10).
Рисунок 10. Относительная концентрация маркеров гепатита B в сыворотке хронического носителя, в зависимости от времени инфицирования
Высокие титры (> 1:1000) IgM антител на HBcAg появляются во время острой фазы HBV инфекции, совпадая с появлением IgG и ростом аминотрансфераз. Так как уровень анти-HBc IgM быстро уменьшается, высокий титр этих антител является свидетельством острой фазы гепатита B. Поэтому тестирование на анти-HBc IgM является полезным инструментом при диагностике острой HBV инфекции, позволяющим различать острые и хронические гепатиты B.
Во время активной фазы болезни в организме появляются как IgM, так и IgG антитела к вирусному коровому антигену. В то время как анти-HBc IgM быстро исчезает, анти-HBc IgG сохраняются годы. Поэтому анти-HBc IgG являются удобным индикатором для подтверждения предшествующих контактов с HBV. Более того, анти-HBc IgG является единственным маркером, который можно обнаружить во время так называемого серологического окна острого гепатита B, периода, когда анти-HBs антитела, указывающие на элиминацию вируса, еще не обнаруживаются, а специфические IgM уже исчезли (Рис. 11).
Рисунок 11. Относительная концентрации маркеров гепатита B при острой инфекции в зависимости от времени инфицирования
Антитела к HBsAg (анти-HBs) являются основными нейтрализующими HBV антителами, которые защищают против повторного инфицирования и сохраняются в течение всей жизни. Поэтому обнаружение анти-HBs служит индикатором выздоровления от гепатита B или успеха вакцинации с использованием HBsAg частиц. Концентрация антител ? 10 IU/L указывает на иммунитет к HBV.
В 1999-2001 гг. ВОЗ провела сравнительные испытания быстрых простых тестов 10 производителей (Determine HBsAg, DoubleCheck HBs Antigen, ImmunoComb II HBs Ag 90’, Serodia-HBs.PA, GLD Rapid HBsAg, Hepacard, AQ One HBsAg Test, Uni-Cold HBsAg, Genedia HBsAg, Hep B Stark-Pack) для обнаружения поверхностного антигена вирусного гепатита B [160]. При этом оценивалась не только чувствительность и специфичность, но и результаты, полученные на сероконверсионных и низкотитражных панелях. В качестве образцов сравнения, референс-тестов, выступали ELISA тест-системы MonolisaAgHBs Plus и Hepanostika HBsAg. Результаты испытаний представлены на рисунке. Столбцы диаграммы характеризуют количество выявленных положительных образцов низкотитражной и сероконверсионных панелей. Как видно из диаграммы (Рис.12), тесты ИммуноКомб продемонстрировали результаты, близкие или превосходящие результаты ИФА референс-тестов на сероконверсионных и низкотитражных панелях.
Рисунок 12. Сравнительная характеристика тестов при диагностике образцов сероконверсионных и низкотитражных панелей
Количество образцов низкотитражной панели, идентифицированных тестом ИммуноКомб как содержащие HBsAg, совпадает с количеством образцов, выявленных референс-тестом Hepanostika и на один образец меньше, чем референс-тестом Monolisa. Количество образцов сероконверсионной панели, диагностированых тест-системами ИммуноКомб, превышает показатель референс-тестов. Все остальные тесты отставали от референс-тестов в определении положительных образцов этих панелей. Как видно из данных, представленных на рисунке 13 ИммуноКомб HBsAg 90’ диагностирует HBsAg в среднем на 1 сутки раньше, чем референс-тест Monolisa Ag HBs Plus. Все остальные тесты обнаруживают HBsAg, отставая от референс-теста, по крайней мере, на 2 суток.
Рисунок 13. Образцы сероконверсионной панели, определяемые каждым из тестов относительно референс-теста Monolisa Ag HBs Plus (0 соответсует первому образцу, определяемому референс-тестом)
Эффективность быстрых простых тестов по выявлению поверхностного антигена вируса Гепатита В не уступает аналогичным характеристикам ELISA тестов. ИммуноКомб диагностирует HBsAg на более ранних стадиях и в более низких концентрациях, чем другие участвующие в испытаниях тесты.
Данный диагностический препарат позволяет диагностировать антиген различных субтипов в концентрации 0,25 нг/мл и проводить индивидуальное и групповое тестирование.
В таблице 24 представлены результаты международных испытаний БПТ ИммуноКомб HBS AG 90' [13].
Таблица 24. Качество тестов ИммуноКомб HBS AG 90'
| Год | Страна | Место проведения | Образцы и панели | Хар-ки панелей и референс-тесты | Чув- стви- тель- ность | Специ- фич- ность | |
| Кол-во | Характер Сывороток | ||||||
| 1991 | Франция | INSERM Lyon | 266 | 199 HBsAg полож. образца 72 отриц. образца | Austria II, Abbott | 99% | 97,2% |
| 1994 | Израиль | Вирусологическая лаборатория | 444 | 195 положит. 1 слабоположит. 248 отриц. образцов | Austria II, Abbott | 100% | 99,5% |
| 1995 | Франция | ADM, Париж, Национальный Институт Трансфузиологии | 30 | 19 положит. сыворо ток разл. субтипов вируса гепатита B, 2 отрицат.образца разбавленных, 3 образца от недавно вакцинир.индивидуумов( < 0,5 нг/мл) 6 сывороток хронич. носителей HBV | панели DECODAGE, PL21-PL30, Франция | 0,48 | не определялась. |
| 1998 | Израиль | Орженикс, Явна | 164 | положит. сыворотки: к HBsAg – 1 положит.сыворотки: к anti Toxo IgG - 21 положит.сыворотки: к anti Toxo IgM - 20 положит.сыворотки: к anti Toxo IgM - 20 положит.сыворотки: к anti CMV IgG - 20 положит.сыворотки: к anti CMV IgM - 18 положит.сыворотки: к anti HBc IgG - 18 положит.сыворотки: к anti Rubella IgG -15 положит.сыворотки: к anti Rubella IgM-14 положит.сыворотки: к anti HBs AB - 6 положит.сыворотки: к anti HCV - 18 положит.сыворотки: к HIV – 12 отрицат. сыворотки: к HBsAg - 1 | Панели BBI; США; сероконверсионная HIV, ADM панель, Франция | не определялась | 100% |
| 2001 | Франция | Вирусологическая Лаборатория, CERV2, Париж | 58 | 5 положит. сыворот. (0,4 – 0,9 нг/мл) 14 сильно положит. сывороток 8 слабо положит. сывороток. 12 отрицат. сыворо-ток, трудно опреде- ляемых согласно HBsAg, Abbott 19 отрицат. сыворот. | панель BBI; Axsym HBsAg, Abbott; Axsym HBsAg Confirma –tory AFFSAPS | ? 0,5 нг/мл, 100% | 100% |
| 2003 | Франция | Лаборатория Marquis Lanzenberg | 71 | 71 образец от бере- менных женщин и позитивных к HCG ? | Abbott | не опре делял. | 100% |
| 2003 | Франция | Федеральный медицинский Госпитальный Центр | 150 | 142 образца от беременных женщин 8 положит. сывороток | Platelia Ag HBs Biorad | не определял. | 100% |
Проведенные испытания показали, что аналитическая чувствительность тестов ИммуноКомб HBsAg соответствует Европейскому стандарту(меньше или равно 0,5нг/мл). Обладая высокой чувствительностью и специфичностью (100% и 99,7%) тест системы ИммуноКомб выявляют сероконверсионные и низкотетражные сыворотки в той же или более низкой концентрации, чем референс-тесты. Независимо от субтипа вируса гепатита В тесты ИммуноКомб достоверно диагностируют присутствие HBsAg.
В таблица 25 приведена схема постановки диагноза инфицированности вирусом гепатита В на основании результатов анализа с помощью ИФА БПТ ИммуноКомб.
Таблица 25. Использование тестов ИммуноКомб для более точной постановки диагноза гепатита B
| Результаты | Интерпретация | |||
| HBs Ag | HBc IgM | HBc IgG | Anti-HBs | |
| + | – | – | – | Ранняя активная фаза гепатита B |
| + | + | + | – | Активная фаза гепатита B или рецидив хронической инфекции. |
| + | – | + | – | Хронический носитель гепатита B (если HBsAg присутствует больше 6 месяцев) |
| – | + | + | – | Выздоравливающий после гепатита B (недавняя активная инфекция) |
| – | – | + | + | Выздоровление после гепатита B |
| – | – | + | – | Период окна HBV |
| – | – | – | + | Успешная вакцинация HBV |
| – | – | – | – | Отрицательный результат. Требуется проверка на другие этиологические агенты (HCV и т.п.) |
Качественное определение поверхностного антигена к вирусу гепатита В следует проводить с помощью ИФА БПТ ИммуноКомб HBS AG 90' согласно инструкции, прилагаемой к набору. Общую схему постановки анализа см. гл. 4.1, таблица 3, рисунок 3.
Результаты анализа проявляются в виде серо-голубых точек на поверхности зубца гребня. Качественная оценка результата осуществляется визуально, сравнением интенсивности окрашивания нижнего пятна каждого образца с интенсивностью окрашивания на зубце с положительным контролем, или автоматизировано на приборе КомбСкан III™(см. 4.1.6.). На твердую фазу нанесены моноклональные антитела к HBS AG, что позволяет диагностировать 0,25 нг/мл антигена.
Чувствительность и специфичность теста ИммуноКомб HBS AG 90' была оценена на панели из 203 образцов сывороток в сравнении с ИФА – референс тестом Abbot Axsym. Результаты приведены в таблице 26.
Таблица 26. Результаты испытаний
| Контрольный метод (ИФА) | ИммуноКомб HBS AG 90' | |
| положительные | отрицательные | |
| положительные | 112 | 1 |
| отрицательные | 0 | 90 |
Исходя из этих результатов, были вычислены следующие показатели теста:
- Чувствительность - 99%
- Специфичность – 100%
Чувствительность теста HBs Ag 90’ составляет 0,25 нг/мл.
Качественное определение IgM антител к коровому антигену вируса гепатита В следует проводить с помощью ИФА БПТ ИммуноКомб HBC IGM согласно инструкции, прилагаемой к набору. Ниже приведено краткое описание процедуры Общую схему постановки анализа см. гл. 4.1, таблица 3, рисунок 3.
Результаты анализа проявляются в виде серо-голубых точек на поверхности зубца гребня. Качественная оценка результата осуществляется визуально, сравнением интенсивности окрашивания нижнего пятна каждого образца с интенсивностью окрашивания на зубце с положительным контролем, или автоматизировано на приборе КомбСкан III™(см. 4.1.6.).
Чувствительность и специфичность теста ИммуноКомб HBC IGM была оценена на панели 773 образцов сыворотки. Результаты приведены в таблице 27.
Таблица 27. Результаты испытаний
| Контрольный метод | ИммуноКомб HBC IGM | |
| Реакция | положительная | отрицательная |
| положительная | 75 | 0 |
| отрицательная | 3 | 695 |
Исходя из этих результатов, были вычислены следующие показатели теста:
- Чувствительность - 100%
- Специфичность – 99,5%
Качественное определение IgG антител к коровому антигену вируса гепатита В следует проводить с помощью ИФА БПТ ИммуноКомб HBC IGG согласно инструкции, прилагаемой к набору. Общую схему постановки анализа см. гл. 4.1, таблица 3, рисунок 3.
Результаты анализа проявляются в виде серо-голубых точек на поверхности зубца гребня. Качественная оценка результата осуществляется визуально, сравнением интенсивности окрашивания нижнего пятна каждого образца с интенсивностью окрашивания на зубце с положительным контролем, или автоматизировано на приборе КомбСкан III™(см. 4.1.6.).
Чувствительность и специфичность теста Иммунокомб HBC IGG была оценена на панели 879 образцов сыворотки. Результаты приведены в таблице 28.
Таблица 28. Результаты испытаний
| Контрольный метод | Иммунокомб HBC IGG | |
| Реакция | положительная | отрицательная |
| положительная | 93 | 0 |
| отрицательная | 7 | 779 |
Исходя из этих результатов, были вычислены следующие показатели теста:
- Чувствительность - 100%
- Специфичность – 99,1%
Количественное определение антител к поверхностному антигену вируса гепатита В следует проводить с помощью ИФА БПТ ИммуноКомб ANTI HBS согласно инструкции, прилагаемой к набору. Общую схему постановки анализа см. гл. 4.1, таблица 3, рисунок 3.
Результаты анализа проявляются в виде серо-голубых точек на поверхности зубца гребня. Количественную оценку результатов осуществляют визуально с помощью шкалы CombScale или автоматически на приборе КомбСкан III™(см. 4.1.6.). Исследуемые образцы с концентрацией большей, либо равной 10 МЕ/л (IU/L) признаются положительными.
Чувствительность и специфичность теста Иммунокомб ANTI HBS была оценена на панели 170 образцов сыворотки по отношению к двум ИФА тестам. Результаты приведены в таблице 29.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Антитела к вирусу гепатита В: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показания к назначению исследования
Основным показанием к назначению исследования служит гепатит В – инфекционное заболевание, вызываемое ДНК-содержащим вирусом, относящимся к семейству Hepadnaviridae. Вирус гепатита В высококонтагиозен и устойчив к действию факторов окружающей среды.
Источником инфекции являются больные любой формой острого или хронического гепатита, а также вирусоносители. Инкубационный период составляет от 60 до 120 дней.
Непосредственно сам вирус не повреждает клетки печени (гепатоциты). Поражение клеток печени происходит в результате иммунного ответа организма через повреждающее действие Т-лимфоцитов, в меньшей степени за счет образования антител.
Болезнь начинается постепенно и характеризуется наличием у пациента слабости, повышенной утомляемости, редкой головной болью, нарушением сна, снижением аппетита, тошнотой, иногда рвотой, горечью во рту, тяжестью и тупыми болями в правом подреберье. Примерно у 20-30% больных отмечаются боли в крупных суставах, сыпь, реже кожный зуд.
Затем увеличивается печень, появляются темная моча и недостаточно окрашенный кал, желтушность кожных покровов (хотя безжелтушный вариант течения вирусного гепатита В встречается в 20-40 раз чаще желтушного). Период выздоровления может продолжаться до 6 месяцев.
Гепатит В у беременных нередко протекает тяжелее, особенно во второй половине беременности, осложняясь острой печеночной недостаточностью, отслойкой плаценты, гибелью плода и др.
У новорожденных и детей вирусный гепатит, как правило, протекает бессимптомно, без классической желтухи, но в 70-90% случаев переходит в хроническую форму.
Гепатит В у пожилых людей часто имеет тяжелое течение, значительную продолжительность болезни и признаки холестаза (нарушение выработки желчи или ее оттока в двенадцатиперстную кишку с повышением в крови экскретируемых с желчью веществ, появлением кожного зуда, тяжести в правом подреберье, желтушности кожных покровов, потемнение мочи и обесцвечивание кала).
Выделяют острый и хронический гепатит В. Хроническая форма гепатита В диагностируется при обнаружении HBsAg (поверхностного антигена вируса гепатита В) в сыворотке крови в течение 6 и более месяцев.
В структуре вируса выделяют следующие антигенные структуры:
- поверхностный антиген (HBsAg), входит в состав оболочки вируса, его обнаружение в крови пациента указывает на наличие инфекции;
- ядерный антиген (HBсAg) – белок внутренней оболочки вируса гепатита В, синтезируется в зараженной клетке, не проникает через клеточную мембрану и поэтому не обнаруживается в сыворотке крови больного человека;
- HBеAg – входит в состав ядра вируса гепатита В, наличие его в крови указывает на активное размножение вируса;
- HBхAg –расположен около оболочки вируса, его роль изучается.
- антитела к HBsAg - анти-HBsAg;
- антитела к HBсAg обнаруживаются двух видов: анти-HBсAg IgМ и анти-HBсAg IgG;
- антитела к HBеAg - анти-HBеAg.
- диагностика вирусного гепатита В (в процессе первичного клинико-лабораторного обследования; перед плановыми хирургическими операциями; беременные женщины в I и III триместрах беременности; реципиенты и доноры крови и ее компонентов, органов и тканей; персонал медицинских организаций; пациенты перед проведением химиотерапии; больные с хроническими заболеваниями, пациенты наркологических и кожно-венерологических диспансеров; персонал учреждений с круглосуточным пребыванием; контактные лица в очагах острого и хронического гепатита В; дети в возрасте до 12 месяцев, рожденные от инфицированных ВГВ матерей; больные с онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.);
- подготовка к вакцинации и оценка иммунитета после вакцинации.
Подготовка к процедуре
- Рекомендуется сдавать кровь утром с 8 до 11 часов, натощак (не менее 8 часов голода, пить воду можно в обычном режиме).
- Предварительно проконсультируйтесь с врачом по поводу целесообразности проведения исследования на фоне принимаемых лекарств или возможности отмены приема препарата перед исследованием.
- Исключить прием алкоголя накануне исследования, не курить в течение 1 часа до исследования.
- Исключить физические и эмоциональные перегрузки накануне исследования.
- После прихода в лабораторию отдохнуть 10-20 минут перед взятием крови.
- Нежелательно сдавать кровь для лабораторного исследования вскоре после физиотерапевтических процедур, инструментального обследования и других медицинских вмешательств.
- При контроле лабораторных показателей в динамике рекомендуется проводить повторные исследования в одинаковых условиях: в одной лаборатории (тем же методом), сдавать кровь примерно в одинаковое время суток и т. п.
Сроки исполнения
1 рабочий день, исключая день взятия крови.
Что может повлиять на результат
Кроме того, ложноположительный результат может быть у пациентов после переливания крови или компонентов плазмы.
Кровь на анализ берется из вены.
Метод определения: иммуноферментный анализ (ИФА).
Исследуемый материал: сыворотка крови.
Единицы измерения в лаборатории ИНВИТРО: мМЕ/мл.
Анализ крови на антитела к вирусу гепатита В может включать определение следующих показателей:
-
Anti-HBs (антитела к HBs-антигену вируса гепатита B);
Серологический маркёр острого процесса. Определяет присутствие антител класса M к HBcoreAg Антитела к HBсore антигену класса М начинают вырабатываться в период первого появления клинических симптомов гепатита В и сохраняются до периода выздоровления. Особенности инфекции. Гепатит B.
Свидетельство перенесённого острого гепатита В, показатель ремиссии. Определяет присутствие антител к HBеAg. Синтез антител к HBeAg в организме начинается после элиминации антигена инфекционности, они свидетельствуют о прекращении репликации (размножения) вируса в организме. К концу 9-й недели .
Определяет присутствие антител к HB-core Ag, независимо от класса M или G. Функции. Антитела к HB-core антигену появляются при остром гепатите В в крови вскоре после появления HBsAg, персистируют после исчезновения HBs-антигена перед появлением анти-HBs-антител и сохраняются длительное время после.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Нормальные показатели
Для контроля эффективности иммунитета при вакцинации против гепатита В используют количественное определение анти-HBs Ag.
Расшифровка показателей
Антитела к поверхностному антигену вируса гепатита В (Anti-HBs Ag) можно обнаружить в конце острого периода, чаще через 3 месяца от начала инфекции, но иногда и позже (до года). Антитела к поверхностному антигену нейтрализуют вирус, их наличие рассматривают как признак иммунитета.
Anti-HBs Ag выявляются длительное время, могут сохраняться пожизненно и свидетельствуют о наличии инфекции (текущей или перенесенной ранее) или поствакцинальном иммунитете.
При количественном определении анти-HBs Ag:
- Anti-HBs ниже 10 мМЕ/л - показана вакцинация против гепатита В;
- Anti-HBs 10-100 мМЕ/л - вакцинацию следует отложить на 1 год;
- Anti-HBs более 100 мМЕ/л - вакцинация не показана, рекомендовано повторное обследование через 5 лет.
Выявление анти-HBс IgМ свидетельствует об активном размножении вируса, о наличии острой инфекции, особенно при отрицательном результате на HBsAg, в некоторых случаях - о хроническом гепатите В.
Антитела к HBсAg класса IgG появляются в острый период практически одновременно с анти-HBс IgМ, достигают максимальных значений через 5-6 месяцев от момента обнаружения HBsAg и сохраняются на протяжении всей жизни. Анти-HBс IgG - маркер хронической или перенесенной инфекции, вызванной вирусом гепатита В.
Анти-HBе появляются в острый период, сохраняются до 5 лет после перенесенной инфекции и указывают на активное выведение вируса гепатита В из организма и незначительное инфицирование. Их появление считается признаком благоприятного течения болезни, свидетельствуя о снижении скорости размножения вируса.
Отрицательный результат на анти-HBе не исключает наличия острого или хронического гепатита.
Расшифровку результатов лабораторных исследований на антитела к вирусу гепатита В проводят только с учетом выявления других маркеров гепатита. В таблице представлены некоторые критерии лабораторной диагностики нескольких вариантов течения инфекции, вызванной вирусом гепатита В.
| Маркер | Острый гепатит В | Хронический гепатит В | Перенесенный гепатит В | Носительство гепатита В | Иммунитет после вакцинации |
| HBsAg | + | + | - | + | - |
| Anti-HBs Ag | - | - | + | - | + |
| анти-HBс Ag IgG | + | + | + | + | - |
| анти-HBс Ag IgМ | + | - | - | - | - |
| HBеAg | +/- | +/- | - | - | - |
| анти-HBеAg | -/+ | -/+ | + | - | - |
| ДНК вируса гепатита В | + | + | - | +/- | - |
| Активность АЛТ (аланинамино- трансфераза) | ↑ | норма | норма | норма | норма |
Дополнительное обследование
При наличии антител к вирусу гепатита В в крови для уточнения диагноза и определения дальнейшей тактики лечения может быть назначено дополнительное обследование:
HBsантиген вируса гепатита В – основной маркер вируса гепатита В. Синонимы: Анализ крови на австралийский антиген гепатита В; Поверхностный антиген гепатита В. Australia antigen (Au(1)); Australian antigen; Australia-Antigen. Краткое описание исследования HBs¬-антиге.
Характеристика и принцип работы набора
2.1 Состав набора:
Положительный контрольный образец (К + )
Отрицательный контрольный образец (К – )
Слабоположительный контрольный образец (Ксл + )
Раствор для разведения конъюгата №1 (РР-К1)
2 флакона по 6 мл
Раствор для разведения конъюгата №2 (РР-К2)
2 флакона по 6 мл
Буферный раствор для субстрата (БРС)
2 флакона по 13 мл
25-кратный концентрат фосфатно-солевого буферного раствора с твином (ФСБ-Т×25)
2 флакона по 28 мл
Комплект ванночки для реагентов с наконечниками для многоканальных пипеток
2.2 Основные компоненты набора "ИФА-HBsAg" – иммуносорбент, конъюгат №1 и конъюгат №2.
Иммуносорбент представляет собой полистирольный планшет, в лунках которого сорбированы поликлональные антитела к HВs-антигену.
Конъюгат №1 представляет собой меченые биотином моноклональные антитела к HBs-антигену.
Конъюгат №2 представляет собой стрептавидин, конъюгированный с пероксидазой хрена.
Положительный контрольный образец – сыворотка крови человека, содержащая НВs-антиген, не содержащая антитела к ВИЧ-1, ВИЧ-2 и вирусу гепатита С, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Отрицательный контрольный образец – сыворотка крови человека, не содержащая НВs-антиген, антитела к ВИЧ-1, ВИЧ-2, вирусу гепатита С, инактивированная прогреванием в течение 3 ч при температуре 56 ºC.
Слабоположительный контрольный образец – лиофилизированный препарат сыворотки крови человека, содержащей рекомбинантный НВs-антиген с концентрацией 0,25 нг/мл, не содержащей антитела к ВИЧ-1, ВИЧ-2, вирусу гепатита С и НВs-антиген, инактивированной прогреванием в течение 3 ч при температуре 56 ºC.
Принцип работы набора. При внесении в лунки планшета конъюгата №1 и образцов сывороток (плазмы) инфицированной крови HВs-антиген связывается как с поликлональными антителами к HВs-антигену, сорбированными на твердой фазе, так и с моноклональными антителами к HBs-антигену, входящими в состав конъюгата №1, образуя комплексы антитело-антиген-конъюгат. Иммунные комплексы антитело-антиген-конъюгат выявляются конъюгатом №2. После отмывания несвязавшихся компонентов связавшийся конъюгат №2 выявляют, добавляя в лунки планшета раствор субстрата пероксидазы (перекись водорода) и хромогена ТМБ.
Пероксидазную реакцию останавливают, добавляя стоп-реагент (0,9 М раствор серной кислоты), и интенсивность окрашивания раствора в лунках измеряют на спектрофотометре как величину оптической плотности (ОП) при длине волны 450 нм.
Величина ОП прямо пропорциональна концентрации HВs-антигена в образце сыворотки или плазмы крови человека. Чем выше содержание HВs-антигена в образце сыворотки, тем выше интенсивность окрашивания.
2.3 Набор рассчитан на проведение 24 постановоки ИФА: 1 постановка – 1 стрип (8 лунок). Всего – 192 определения, включая контрольные образцы.
3.1 Все компоненты набора в используемых концентрациях являются нетоксичными. Однако работа со всеми исследуемыми образцами сыворотки (плазмы) крови человека, которые следует рассматривать как потенциально инфицированные, способные сохранять и передавать ВИЧ, вирус гепатита В или любой другой возбудитель вирусной инфекции, с отработанными растворами и жидкостями, различным оборудованием, которое может быть загрязнено в процессе анализа, требует определенных мер безопасности при использовании набора:
- работу необходимо проводить в специально оборудованном помещении;
- работать необходимо с применением средств индивидуальной защиты и с соблюдением мер предосторожности в соответствии с требованиями [1], [2], и [3].
3.2 Стоп-реагент, содержащий серную кислоту, обладает раздражающим действием. При попадании на кожу и слизистые немедленно промыть большим количеством воды.
3.3 При работе с набором рабочие места должны быть обеспечены приточно-вытяжной вентиляцией.
3.4 Все лица, работающие в лаборатории с наборами, должны проходить обязательный медицинский осмотр в соответствии с требованиями [4].
3.5 Утилизация медицинских отходов и/или неиспользованных наборов с истекшим сроком годности должна производиться в соответствии с требованиями [5].
4.1 Для исключения ложных результатов исследуемые образцы необходимо готовить и хранить в условиях, предотвращающих бактериальный пророст. Необходимо осветлять образцы сывороток, содержащие агрегированные компоненты сыворотки или осадок, при помощи центрифугирования в течение 15 мин при скорости вращения 3000 об/мин. Образцы сывороток можно хранить при температуре (2-8) °С не более 7 суток. Замороженные образцы (желательно до температуры не менее минус 20 °С) можно хранить не более 6 месяцев. Необходимо избегать повторных циклов замораживания-оттаивания образцов.
Необходимо помнить, что образцы с гемолизом, гиперлипидемией, бактериальным проростом, а также длительно хранившиеся без замораживания не пригодны для анализа.
Надежность результатов зависит от выполнения следующих правил:
- не допускается использование набора после окончания срока годности, а также смешивание компонентов наборов разных серий;
- для приготовления каждого реагента должна использоваться отдельная емкость;
- всю используемую для приготовления реагентов посуду не обрабатывать дезрастворами и моющими средствами. В случае необходимости промыть водой питьевой проточной, а затем пять раз ополоснуть дистиллированной водой;
- для работы с хромогеном ТМБ необходимо использовать отдельные емкости для растворов, наконечники для пипеток, посуду.
- необходимо обратить внимание на тщательное перемешивание реагентов;
- при внесении в лунки стрипов раствора Кг-1 в рабочем разведении или раствора Кг-2 в рабочем разведении нельзя касаться наконечником пипетки поверхности планшета и раствора, находящегося в лунках во избежание случайного заноса образца из одного стрипа в другой через наконечники;
- время между заполнением и опорожнением лунок планшета растворами и реагентами должно быть не менее 30 с. Не допускается подсыхание лунок на всех этапах постановки ИФА;
- при использовании промывателя следить за состоянием емкости для раствора для промывания планшета и соединительных шлангов: в них не должно быть признаков бактериального или грибкового роста;
- необходимо использовать пипетки автоматические со сменными наконечниками, аттестованные по значению средней дозы и сходимости результатов пипетирования (погрешность не более 3 %);
- дозаторы и рабочие поверхности обрабатывать раствором с объемной долей спирта этилового 70 %. Не использовать хлорамин и другие хлорсодержащие вещества;
- для работы с исследуемыми сыворотками и контрольными образцами рекомендуется использовать одноразовые наконечники для пипеток. Каждый образец сыворотки, а также реагенты набора необходимо отбирать отдельным наконечником.
- во время проведения анализа следует избегать попадания прямых солнечных лучей на рабочую поверхность.
4.2 При вскрытии и растворении лиофилизированных компонентов необходимо следить, чтобы на крышке и стенках флаконов не оставалось сухого вещества.
5.1 Спектрофотометр вертикального сканирования, позволяющий проводить измерения оптической плотности растворов в лунках планшета при длине волны 450 нм;
- полу- или автоматическое устройство для промывания планшетов (вошер);
- суховоздушный термостат типа ТС-80 М2, поддерживающий температуру (37±1) °С, или аналогичный ему по характеристикам;
- пипетки одноканальные автоматические со сменными наконечниками, позволяющие отбирать объемы жидкости от 0,02 до 5,0 мл;
- мерный цилиндр вместимостью 1000 мл;
- колба лабораторная вместимостью 1000 мл;
- флаконы стеклянные вместимостью 20 мл;
- ванночки для реагентов или чашки Петри (диаметр 100 мм);
- вата медицинская гигроскопическая;
- перчатки резиновые хирургические;
- раствор с объемной долей спирта этилового 70 %;
- раствор с массовой долей перекиси водорода 6 %;
- вода деионизированная или дистиллированная;
- контейнер для сбора твердых отходов;
- контейнер для слива жидких отходов.
Содержимое флаконов с реагентами, входящими в состав набора, и все образцы исследуемых сывороток (плазмы) крови человека перед проведением анализа тщательно перемешать.
Расход реагентов набора для постановки анализа, который определяется количеством используемых стрипов, приведен в таблице А.1 Приложения А.
6.2 Подготовка иммуносорбента
Иммуносорбент готов к использованию.
Открыть пакет и установить на рамку необходимое количество стрипов. Оставшиеся стрипы хранить в плотно закрытом пакете с влагопоглотителем при температуре (2-8) °С в не более 3 месяцев.
6.3 Приготовление раствора для промывания планшета
Внимание! Раствор для промывания планшета готовить за 15 мин до начала проведения анализа!
Если флакон с ФСБ-Т×25 содержит осадок, его необходимо прогреть перед использованием при температуре (37±1) °С до полного растворения осадка.
В мерный цилиндр вместимостью 1000 мл внести содержимое флакона с ФСБ-Т×25, затем добавить дистиллированной воды до метки 700 мл и аккуратно перемешать раствор.
В случае использования одного или несколько стрипов содержимое флакона с ФСБ-Т×25 интенсивно встряхнуть в течение (20-30) с, отобрать необходимый объем раствора (таблица A.1 Приложения А) в мерный стакан или цилиндр, добавить необходимое количество дистиллированной воды и перемешать раствор.
Неиспользованный ФСБ-Т×25 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.4 Подготовка К + , К – , РР-К1, РР-К2, БРС и стоп-реагента
К + , К – , РР-К1, РР-К2, БРС и стоп-реагент готовы к использованию.
Неиспользованные РР-К1, РР-К2, БРС и стоп-реагент после вскрытия флаконов можно хранить в плотно закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
Остаток К + и К - после вскрытия флаконов можно хранить в плотно закрытых флаконах при температуре (2-8) °С в течение срока годности набора.
6.5 Приготовление раствора Ксл +
Внимание! Раствор Ксл + готовить за 15 мин до начала проведения анализа!
Восстановленный Ксл + можно хранить в закрытом флаконе при температуре (2-8) °С не более 1 месяца , при температуре минус 20 °С – в течение шести месяцев. Допускается однократное замораживание-оттаивание восстановленного Ксл + .
6.6 Приготовление раствора Кг-1 в рабочем разведении
Из флакона с Кг-1 отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с РР-К1. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон отобрать необходимое количество РР-К1, добавить Кг-1 в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Остаток Кг-1 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.7 Приготовление раствора Кг-2 в рабочем разведении
Из флакона с Кг-2 отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с РР-К2. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон отобрать необходимое количество РР-К2, добавить Кг-2 в соответствии с таблицей А.1 Приложения А и перемешать раствор, не допуская образования пены.
Остаток Кг-2 можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
6.8 Приготовление рабочего раствора субстрата
Флакон с хромогеном ТМБ необходимо прогреть перед использованием в течение (3-5) мин при температуре (37±1)° С до полного растворения кристаллов.
Из флакона с хромогеном ТМБ отобрать указанный в таблице А.1 Приложения А объем и перенести во флакон с БРС. Содержимое флакона тщательно перемешать, не допуская образования пены.
В случае использования одного или несколько стрипов в чистый флакон из темного стекла или пластика (прозрачный флакон обернуть флакон) отобрать необходимое количество БРС, добавить хромоген ТМБ в соответствии с таблицей A.1 Приложения А и перемешать раствор, не допуская образования пены.
Раствор необходимо предохранять от попадания света и контакта с металлами или ионами металлов. Перед использованием раствор субстрата должен быть бесцветным. Посуду, которая будет в ходе реакции контактировать с раствором субстрата, отмывать без применения синтетических моющих средств. Использовать только новую ванночку для реагентов и новые наконечники!
Остаток хромогена ТМБ можно хранить в плотно закрытом флаконе при температуре (2-8) °С в течение срока годности набора.
- на всех этапах промывания необходимо контролировать заполнение всех лунок и полное удаление (аспирацию) жидкости из них;
- необходимо при каждом промывании во все лунки планшета вносить не менее 380 мкл раствора для промывания планшета;
- необходимо выдерживать лунки, заполненными раствором для промывания планшета, в течение 30 с;
- при каждой аспирации тщательно удалять остатки жидкости из лунок постукиванием рамкой со стрипами в перевернутом положении по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена;
- некачественное промывание планшета приводит к получению некорректных результатов.
8.1 В лунки, предназначенные для контрольных образцов внести:
- в две лунки планшета – по 0,1 мл (100 мкл) К + ;
- в две лунки планшета – по 0,1 мл (100 мкл) Ксл + ;
- в две лунки планшета – по 0,1 мл (100 мкл) К – .
Во все остальные лунки планшета внести по 0,1 мл (100 мкл) исследуемых образцов сыворотки (плазмы) крови человека.
Внести во все лунки планшета по 0,05 мл (50 мкл) раствора Кг-1 в рабочем разведении (п 6.6).
Внимание! При постановке ИФА на одном или двух стрипах допускается использовать для К – – две лунки, для К + – одну лунку, для Ксл + – одну лунку.
Внимание! Время внесения контрольных и исследуемых образцов не должно превышать (5-10) мин! Каждый образец необходимо отбирать одноразовым наконечником!
Содержимое лунок перемешать осторожным постукиванием по краю планшета
8.2 Планшет заклеить пленкой или закрыть крышкой и инкубировать при температуре (37±1) °С в течение 60 мин в термостате.
Внимание! За (1-2) мин до окончания инкубации приготовить раствор Кг-2 в рабочем разведении (п 6.7).
8.3 По окончании инкубации внести во все лунки планшета по по 0,05 мл (50 мкл) раствора Кг-2 в рабочем разведении (п 6.7). Содержимое лунок перемешать осторожным постукиванием по краю планшета
8.4 Планшет заклеить пленкой или закрыть крышкой и инкубировать при температуре (37±1) °С в течение 30 мин в термостате.
8.5 Удалить содержимое лунок, затем промыть лунки планшета раствором для промывания планшета (п 6.3) семь раз. Для этого во все лунки планшета необходимо внести не менее 380 мкл раствора для промывания планшета, а затем удалить содержимое лунок в емкость с дезраствором.
По окончании промывания тщательно удалить остатки жидкости из лунок, активно постукивая планшетом в перевернутом положении (лунками вниз) по сложенной в несколько раз фильтровальной бумаге, положенной на лист полиэтилена.
8.6 Во все лунки планшета внести по 0,1 мл (100 мкл) рабочего раствора субстрата (п 6.8). При приготовлении рабочего раствора субстрата (п.6.8) флакон с хромогеном ТМБ необходимо прогреть перед использованием в течение (3-5) мин при температуре (37±1)° С до полного растворения кристаллов
8.7 Планшет заклеить пленкой или закрыть крышкой и инкубировать в термостате при температуре (37±1) °С в защищенном от света месте в течение 15 мин.
Внимание! По окончании инкубации в лунках с образцами сывороток, содержащими HBs-антиген, произойдет изменение окраски раствора различной интенсивности в зависимости от концентрации HBs-антигена в исследуемом образце сыворотки: от бесцветной до голубой.
8.8 Остановить пероксидазную реакцию путем внесения во все лунки по 0,05 мл (50 мкл) стоп-реагента.
Внимание! В лунках с образцами сывороток, содержащими HBs-антиген, произойдет изменение окраски раствора: с голубой на желтую.
8.9 Не позже чем через 10 мин после остановки реакции определить значение ОП раствора в лунках в двухволновом режиме: 450 нм относительно (620-700) нм. Допускается измерение ОП в одноволновом режиме при длине волны 450 нм.
Читайте также:

