Иммунитет к вирусам после болезни
Обновлено: 12.05.2024


Прусс: Практически это главное, что мы про него знаем. Недавно вышли очень интересные британские данные про спектр симптомов заболевания, насколько они изменились в сравнении с дельтой. Я должен сказать, что изменились они, по-видимому, не настолько сильно. Да, британцы видят больше больных с больным горлом, их с омикроном около половины, но и с дельтой был каждый третий. Также они видят меньше зараженных с потерей обоняния. Это фиксировалось у трети пациентов с дельтой и осталось у каждого восьмого с омикроном.
То есть для пациентов, которые не испытывают серьезных последствий от ковида, разница симптомов не такая большая.
А вот при тяжелом течении болезни уже есть существенные отличия. Для омикрона больше характерен бронхиолит средних дыхательных путей. А для дельты — более глубинное поражение самих легких, альвеол.
Ясно ли, какая длительность иммунитета после омикрона? Он действует против дельты?
До недавнего времени я рассказывал, что это будет понятно не раньше чем через три месяца. Традиционно считалось, что в первые месяцы после заболевания не всегда просто определить новое это заражение или вспышка старого. Чтобы не ошибиться, отсчитывали 90 дней и только потом выясняли, заразились люди снова или нет.
Сегодня я с большим удовлетворением вижу, что британцы начали смотреть повторное заражение начиная уже с 30-дневного срока. Они, конечно, пока не получили информацию о том, через какое время после омикрона можно заразиться, потому что большинство пациентов еще только-только выздоровели. Но британцы анализируют, насколько у болевших дельтой в осеннюю волну на 30-й день после выздоровления ослабла чувствительность к омикрону.
Теоретически можно предположить, что первые месяц-два, чем бы человек ни переболел, у него сохраняется значительная устойчивость ко всем штаммам, которыми можно заразиться. Иммунная система еще очень активная, в ней много всех активизированных компонентов: и Т-клетки циркулируют, и концентрация антител большая. Реально риски начинаются где-то после третьего месяца после выздоровления, а где-то и больше. Точнее мы об этом узнаем скорее всего в мае.
Омикрон сам по себе менее патогенен или вызывает более легкое течение болезни только у вакцинированных?
И то, и другое — правда. Поначалу это было очень трудно различить, потому что большинство жителей тех стран, по которым омикрон прокатился первым, были или вакцинированы, при этом хорошо, с ревакцинацией, как в Британии, или относительно недавно переболели, как в Южной Африке. По небольшим прослойкам населения, которые все-таки не вакцинированы в Дании и Великобритании
ученые делают вывод, что тяжесть заболевания заметно меньше и для тех, кто ни разу не был вакцинирован. Заметно — это, конечно, не в разы. В зависимости от того, что мы измеряем, — на 30-50 процентов
Хотя статистически установлено, что при омикроне ковид протекает легче, не стоит успокаиваться, это палка о двух концах. Даже уменьшенная в полтора-два раза в группах риска опасность, где она изначально была очень высокой, остается огромной.
В России уровень вакцинации меньше, чем в Европе. Но, мне кажется, найти непереболевших и непривитых уже очень трудно. Многие болели неофициально, поэтому не попали в статистику.
Так случилось в Англии, где трудно было до конца провести анализ, потому что значительная часть населения переболела без официального статуса. В расчетах они пытались применить условные поправочные факторы. Смотрели, у скольких людей нашли антитела к вирусу, больше ли их, чем официально болевших. Но это трудно верно рассчитать.

Фото: Maxim Shemetov / Reuters
Мне все-таки кажется, что именно среди людей пожилых, именно среди тех, кто склонен тяжело переносить ковид, доля болевших, но не имевших подтвержденного диагноза, небольшая. Потому что это гораздо чаще происходит с перенесшими болезнь легко, без дискомфорта, то есть с молодыми.
За счет чего снизились патогенные свойства вируса?
Люди часто думают, что вирусы становятся менее патогенными потому, что они не смогут существовать, убив всех своих носителей. Но никакие штаммы коронавируса не убивали так много людей. С точки зрения общества смертность от ковида очень большая, однако с точки зрения вируса — это не так много, чтобы помешать ему распространяться.
Как вирус изменяет свои свойства? Иммунная система наших организмов учится все лучше и лучше бороться против него. Вирус должен постоянно изменяться, чтобы противостоять давлению иммунитета. Не все изменения проходят вирусу даром. Иногда что-то меняется в белках, это позволяет избежать ему защитной реакции иммунной системы. Но для вируса это тоже вредно, может сделать его менее активным. Именно так произошло с омикроном.
Главное, почему он не проходит в глубину легких, а остается в верхних и средних дыхательных путях, это потому, что в процессе мутирования, чтобы избежать нашей иммунной системы, он утратил один из сайтов расщепления шиповидного белка на поверхности. И в результате больше не может войти в клетки так, как раньше
Но это не сам вирус стал менее патогенен, потому что ему захотелось оставить в живых человечество. Просто наша иммунная система загнала его в такой угол, что у него не осталось другого выхода.
На самом деле и дельта на начальной стадии первых волн резко молодела — гораздо больше заражала людей, которые были младше, чем болевшие до того. К концу волн эта динамика поменялась на противоположную — болело больше пожилых людей. Это связано скорее не с биологией вируса, а с социальными навыками тех, кто первыми или последними подхватывают инфекцию.
Первыми подхватывают вирус те, кто ходит в школу, на всякие гулянки, концерты. Пенсионеры как бы немножко более изолированы, их круг общения уже. А иногда они осторожничают и вообще сокращают его до полного минимума, поэтому к ним поздно приходит инфекция.
Биологический эффект трудно даже оценить, учитывая, что это проявляется на фоне социального аспекта. Перемены наблюдаются в такой стране, как Дания. Там волна омикрона дошла до пика и, возможно, начала спадать. За четыре недели до пика среди зараженных наблюдалось значительное преобладание молодых, особенно 20-24-летних. Но к последней неделе этот эффект начал сходить на нет. Теперь доля омикрона среди пожилых — практически такая же.
Дети стали чаще болеть?
В Дании дети попадали в статистику немного меньше, чем при дельте. Связано ли это с более легким течением болезни, честно говоря, не знаю. Дело в том, что детей тестируют не совсем по тем правилам, по которым тестируют взрослых. Очень многие страны делают программы тестирования в зависимости от уровня инфекции в школах. И получается, что дети охвачены тестированием гораздо шире. Взрослые, чтобы им сделали анализ, должны реально заболеть. А дети — всего лишь находиться в школе, где довольно много заболевших, в этом случае они сразу попадают под обязательное тестирование. Такая программа была и у нас в штате Юта. Сегодня ее отменили по причине того, что болеет столько детей, что тестов уже не хватает на всех.

Фото: Pavel Golovkin / AP
Есть ли вероятность, что омикрон к весне тоже уйдет, как и другие штаммы?
Дельту и омикрон от всех предыдущих штаммов отличает ускоренный жизненный цикл. Это делает более трудным прогноз, исчезнут эти штаммы напрочь или будут возвращаться периодически.
После волн высокой заболеваемости тем или иным штаммом два-три месяца, а то и больше у населения остается нейтрализующий иммунитет. Но постепенно его уровень спадает, и его уже недостаточно, чтобы предохранить людей.
Но буквально за считаные дни после новой инфекции иммунная система вспоминает, что она умеет бороться с этой угрозой, берется за дело и очень быстро останавливает вирус. Однако достаточно ли быстро, чтобы предотвратить новую волну?
Допустим, для альфы или для гаммы реально люди становились заразными на четвертый или на пятый день после инфицирования. К этому сроку иммунная система уже набирала обороты, вирус во внеклеточном пространстве весь инактивировался. И люди, переболевшие даже давно, все равно становились неспособными эффективно распространять эту заразу.
С дельтой было не так. Дельта уже парой волн прокатывалась по России. Хотя организм помнит, как с ней бороться, имеет иммунные клетки памяти, Т-клетки, В-клетки, но те 3-4-5 дней, которые требуются, чтобы на полную скорость раскрутить иммунную реакцию, недостаточны для предотвращения передачи дельты дальше. Жизненный цикл этого вируса быстрее, уже на третьи сутки после инфицирования зараженный человек способен заразить других.
Возможно, то же самое будет характерно и для омикрона. Предполагается, что у него тоже более быстрый жизненный цикл, но точных данных по этому поводу нет.
Пока эпидемия развивается при доминировании какого-то одного штамма. Есть ли опасность, что появятся разные виды вируса, которые будут параллельно ходить в популяции?
В принципе, новой волне подняться на фоне старой волны довольно сложно потому, что у недавно переболевших какое-то время сохраняется иммунитет. Омикрон в какой-то мере является исключением, так как он слишком несхож в иммунологическом плане с другими штаммами, иммунный ответ на него более узок.
Как правило, люди, которые переболели старыми штаммами или вакцинированы, формируют свой иммунный ответ против омикрона из того разнообразия антител, которые у них сформированы. Но в случае омикрона имеющиеся антитела в основном не подходят для решения новой задачи.
Такого биохимического, иммунологического механизма раньше не было. Поэтому есть некоторая вероятность, что будущие варианты вируса смогут изначально избегать нейтрализации. Так что, возможно, прямо на хвосте омикрона придет что-то еще.
Я сейчас внимательно наблюдаю за очень необычной разновидностью омикрона. Формально она считается омикроном, но на практике очень далека от него. Это штамм, который имеет международную номенклатуру ВА.2. Он сейчас очень распространен в Индии, на Филиппинах, в Дании, Швеции
И буквально в ближайшую неделю мы должны узнать, способен ли он распространяться как дополнительная волна на хвосте волны омикрона.

Фото: Kirill Braga / Reuters
Я правильно понимаю, что это преобразованный омикрон?
Месяц или чуть больше назад у них с обычным омикроном (обозначаемым BA.1) были общие предки. Но затем эти две ветки начали развиваться разными эволюционными путями. Штамм ВА.2 отличается от омикрона 20 мутациями. Можно решить, что это омикрон набрал дополнительные 20 мутаций. Но это не так. На самом деле у него нет десяти из мутаций, которые есть у омикрона, зато есть десять других.
Эта новость больше научная или на практике новый омикрон может оказать существенное влияние на пандемию?
Обычный омикрон (BA.1) начал завоевывать целые страны два месяца назад, и постепенно эпидемиологи и иммунологи разобрались в особенностях вызванного им ковида. Массовое распространение BA.2 началось только в последние дни, ясности с этим штаммом меньше.
Однако иммунологи уже предсказывают, что иммунитет у привитых сможет эффективно предотвращать тяжелое течение болезни у зараженных BA.2. И действительно, в Дании, где BA.2 уже преобладает, нагрузка на больницы стабилизировалась. Однако это совсем не означает безоблачную перспективу. Ведь большинство из нас рассчитывают, что волна омикрона закончится спустя считаные недели, и все снова откроется. А BA.2, возможно, удлинит волну, приведет к повторным заболеваниям и существенно замедлит возврат к норме.
С биологической точки зрения возможно ли создать универсальную вакцину от всех штаммов, которая бы обеспечивала длительный иммунитет?
Думаю, что можно. Но опыт показывает, что просто полагаться на широкий иммунитет против шиповидного S-белка вируса, видимо, невозможно. У меня есть своя неподтвержденная гипотеза. Неспроста иммунитет, вызываемый вакцинами или природной заболеваемостью, уходит довольно быстро, количество антител после непродолжительного времени снижается.
Поэтому иммунный ответ, который вызывается одной специфической разновидностью коронавируса, от природы не должен быть слишком долгим. Ведь наш организм ожидает, что придет другая разновидность вируса, против которого предыдущая версия ответа может быть не только неполезна, но даже вредна. Это, конечно, моя гипотеза, и она пока ничем не подтверждена. Но коронавирусы в истории человечества существуют давно, десятки тысяч лет. Ученые находят разнообразные следы эволюции в иммунной системе человека, которые примерно связаны с переселением людей в Восточную Азию, где коронавирусы были эндемичны. Так что не исключено.
Но если для вакцины выбрать другую мишень, не шиповидный белок, то, возможно, удастся найти универсальный ответ. Или выбрать какую-то более узкоспецифическую мишень. То есть такое место в геноме, которое вирус изменить принципиально не может, и оно у всех штаммов единое.
Такие разработки ведутся?
Пока мы идем по линии использования того, что есть. Это, конечно, эффективно, но не идеально. Вряд ли люди будут считать должным ревакцинироваться каждые несколько месяцев. Поэтому на повестке дня будет создание долгосрочных, более универсальных решений. Они точно разрабатываются, но в ближайший год мы этого не увидим.

Фото: Natacha Pisarenko / AP
Частая ревакцинация — с точки зрения биологии, есть ли вред для человека?
Вряд ли это вредно. При очередном столкновении с антигеном у нас не только увеличивается количество антител, но и улучшается их качество, улучшается их сродство, то есть сила связывания с вирусом, которая называется авидностью. Антитела немножко меняются. В Т-клетках, В-клетках происходят небольшие мутации, которые позволяют новым поколениям этих клеток узнавать не только те антигены, которые уже были им знакомы, но даже и родственные.
Определенная польза от этого есть. Но, конечно, эффективность может сходить на нет. Увеличивая количество доз, мы все меньше и меньше будем получать дополнительного эффекта. Особенно это касается векторных вакцин. По мере повторного их применения организм приучается бороться с вектором, на основе которого они сделаны. И тем самым аденовирусу, который используется как вектор, все труднее и труднее будет донести свой груз в виде коронавирусного гена в человеческие клетки, где он будет работать.
До сих пор все самые опасные штаммы коронавируса развивались параллельно — от одного уханьского предка. Почему не было постепенного перехода — от альфы к бете, а потом к дельте? Может быть, постепенная эволюция одного и того же штамма была бы лучше для человечества?
Главный упор в эволюции вируса был сделан на уход от иммунных реакций. Для этого вирусу нужны десятки мутаций. Создать их методом ступенчатой эволюции, одну за другой очень трудно. Поэтому реально оказывалось, что новые важные штаммы, которые вызывали озабоченность ВОЗ, возникали разом из глубинных корней.
Реально не было больших успехов, которые бы опасные штаммы смогли достичь методом постепенной эволюции. Возьмем ту же дельту, которой заболели сотни миллионов людей. В русле дельты постепенно возникли дополнительные, выгодные вирусу мутации, которые, возможно, позволяли ему распространяться быстрее. Но это было очень слабое, инкрементальное, как говорят у нас, изменение степени жизнеспособности вируса. Может быть, это давало пять-десять процентов дополнительной заразности по сравнению с двукратным перевесом, который дельта имела над альфой в самом начале.
Конечно, вирусы эволюционировали, когда было очень много переходов от одного больного к другому, при этом они чуть-чуть продолжали усовершенствоваться.
В свое время я уже был готов поставить точку на коронавирусе. Готов был сказать, что на основе наблюдений за дельтой, за тем, как она приходит круг за кругом, но меняется очень слабо, ступенчато приобретенные мутации дают ей очень копеечный выигрыш, виден конец эволюции вируса
Но с омикроном природа решила поставить нас на место.
Глядя на омикрон, уже нельзя увидеть конец эволюции вируса?
Думаю, что через пару-тройку месяцев мы увидим, насколько у переболевших омикроном сильна остаточная иммунная реакция, насколько долго она тянется, хватит ли ее, чтобы предотвратить новую волну омикрона. Я не берусь судить в долгосрочном плане, но есть надежда, что эффект иммунного обучения нашего организма при встрече с омикроном останется достаточно долгим. Это поможет предотвратить будущие волны, но стопроцентной гарантии нет.
У омикрона есть кое-какие качества, которые заставляют усомниться в таком ответе. Примерно известно, где омикрон выигрывает. Он может входить в клетки некоторых тканей организма через пузырьки эндосом. Считалось, что вирусам трудно так делать. Там очень опасная для вируса среда, там всякие ферменты, которые раскусывают, разгрызают вирусы. Но каким-то образом омикрон научился подавлять эти антивирусные процессы и выходить целехоньким из эндосом. То, что это происходит, достоверно известно, а вот как омикрон это делает — пока непонятно.
От изучения этого специфического процесса будет зависеть наше понимание, что вирусы смогут делать дальше, насколько легко им получить такие необычные изменения, позволяющие эффективно заражать клетки нашего организма. Ведь из-за стремления избежать антител, вся поверхность SARS-CoV-2 уже испорчена. Вирус может себя изменить, чтобы его не узнали, но ему от этого чаще больше вреда, чем пользы. Могу вспомнить русскую пословицу про то, что выбью себе глаз, чтобы у тещи был зять кривой. Наверное, так вирус борется с иммунной системой — что-нибудь портит себе на поверхности, иммунная система из-за этого его не узнает.
Вряд ли вирус умрет, скорее всего станет слабопатогенным. Такое происходит с коронавирусами обычной простуды.
Не может ли на место омикрона прийти еще более опасный новый штамм?
В октябре я бы сказал: да нет, мы уже столько прождали, и ничего опасного не приходило. Но омикрон, конечно, всех удивил, делать прогнозы побаиваюсь. Хотя считаю, что у вируса не должно быть слишком много эффективных решений задачи, как изменить свою поверхность, чтобы она не распознавалась иммунной системой, но при этом хорошо работала.

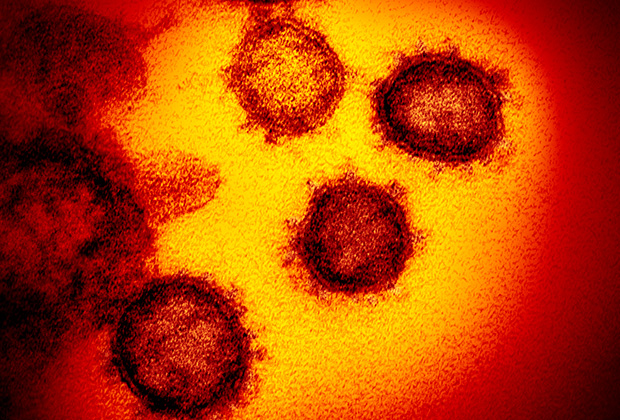
Неспецифическая защита
Существует два типа иммунитета: врожденный и приобретенный, каждый из которых по-разному реагирует на патогены и создает таким образом двухступенчатую систему защиты.
Врожденный иммунитет, как следует из названия, выдается нам с рождения и унаследован человеком от далеких предков. Комплекс реакций врожденного иммунитета сформировался в результате миллионов лет эволюции и сосуществования человека и патогенов. Но реакция эта — стандартная, одинаковая, вне зависимости от того, какой именно антиген попал в наш организм. За это его еще называют неспецифическим.
Система врожденного иммунитета (клетки иммунной системы и интерфероны) защищает организм от большинства возбудителей, например, гриппа и сезонных ОРВИ. Если она реагирует своевременно и правильно, то заболевание может не наступить вовсе.
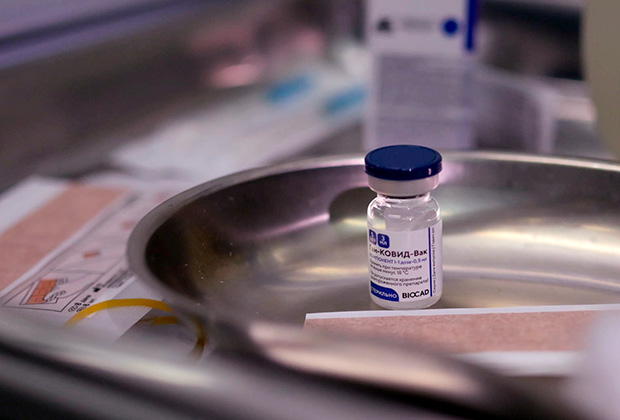
Приобретенный иммунитет
Иногда происходит так, что при всех усилиях врожденного иммунитета заболевание все-таки наступает. Это значит, что высокопатогенному микроорганизму все же удалось обойти систему защиты человека и начать размножаться. Человек реагирует на это повышением температуры, кашлем, насморком и другими болезненными симптомами. При всей неприятности повышение температуры тела также направлено на борьбу с вирусом, что в конечном итоге приводит к его уничтожению. Кроме того, через несколько дней после заражения на помощь врожденному приходит приобретенный иммунитет. Реагирует он гораздо медленнее, зато уже знает, с чем имеет дело, — атакует попавший в организм антиген специфическими, предназначенными именно для него антителами, или иммуноглобулинами, — особыми белковыми молекулами.
Таким образом, чтобы в организме развился приобретенный иммунитет к какому-либо патогену, необходимо перенести заболевание. Причем, по словам врачей, чем сложнее человек переносит заболевание, тем более сильный иммунитет у него сформируется. Ко многим болезням приобретенный иммунитет сохраняется практически бессрочно. Например, так называемыми детскими болезнями — ветрянкой, краснухой, корью — человек чаще всего болеет один раз. После этого даже через много лет в крови переболевшего можно выявить антитела к этим вирусам.

В случае тяжелого течения болезни, например, того же коронавируса, нагрузка на организм многократно возрастает. На борьбу с заболеванием организм тратит ресурсы и силы, для него это существенный стресс, который может привести к нарушениям в работе систем. В такой ситуации формируется приобретенный иммунитет к конкретной болезни, но из-за стресса повышается вероятность других заболеваний, растет уровень восприимчивости к ним. Тут вновь подспорьем могут быть индукторы интерферона, которые помогут снизить риски в этот непростой для организма период.
Более приятная альтернатива болезни — вакцинация, при которой в организме также вырабатываются антитела к распространенным и опасным инфекциям. Но вакцины, к сожалению, существуют не от всех болезней. Например, по словам врачей, создавать вакцины от многочисленных вирусов, вызывающих сезонные ОРВИ, — бессмысленно. С одной стороны, эти заболевания не настолько опасны, с другой — сезонные вирусы постоянно мутируют, что делает создание вакцины бесполезным и экономически невыгодным, ведь ее пришлось бы обновлять каждый год. Именно так, кстати, поступают с вакциной от гриппа, но тут речь идет только об одном типе вируса.
Исключение — новая коронавирусная инфекция, вакцины от которой в ускоренном порядке разрабатываются, тестируются или уже массово применяются в разных странах мира. Кстати, на этом актуальном примере можно наглядно разобрать работу приобретенного иммунитета.

Фото: Brittany Colette / Unsplash
Какие антитела важнее
Для борьбы с коронавирусом организм синтезирует три класса антител: иммуноглобулины A (IgA, вырабатываются первыми в острой фазе заболевания, но обладают низкой специфичностью), M (IgM, вырабатываются чуть позже, активно борются с вирусом и сохраняются в крови примерно месяц) и G (IgG, появляются через 3-4 недели после выздоровления и обеспечивают долгосрочный иммунитет, который, впрочем, в случае COVID-19 сохраняется всего 3-4 месяца).
IgG, как и антитела других классов, вырабатываются к различным частям (антигенам) оболочки вируса. Из всего объема выработанных антител IgG только часть способна блокировать расположенный на шипах вируса S-белок и препятствовать тем самым проникновению вируса в клетку. Именно эти антитела больше всего интересуют врачей.

Фото: Kelly Sikkema / Unsplash
Нейтрализовать вирус
На основе частей S-белка созданы все первые вакцины против коронавируса, в том числе и российская Sputnik V, разработанная центром имени Н. Ф. Гамалеи. При вакцинации организм начинает вырабатывать не все подряд антитела, а только те, которые наиболее эффективно защищают от вируса. Их называют вируснейтрализующими. По прогнозам, в результате вакцинации они сохранятся в организме до двух лет.
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
по теме

Мнение
Кто отвечает за работу различных видов иммунитета?
- Костный мозг. Это центральный орган иммуногенеза. В костном мозге образуются все клетки, участвующие в иммунных реакциях.
- Тимус (вилочковая железа). В тимусе происходит дозревание некоторых иммунных клеток (Т-лимфоцитов) после того, как они образовались в костном мозге.
- Селезенка. В селезенке также дозревают иммунные клетки (B-лимфоциты), кроме того, в ней активно происходит процесс фагоцитоза — когда специальные клетки иммунной системы ловят и переваривают проникших в организм микробов, фрагменты собственных погибших клеток и так далее.
- Лимфатические узлы. По своему строению они напоминают губку, через которую постоянно фильтруется лимфа. В порах этой губки есть очень много иммунных клеток, которые также ловят и переваривают микробов, проникших в организм. Кроме того, в лимфатических узлах находятся клетки памяти — это специальные клетки иммунной системы, которые хранят информацию о микробах, уже проникавших в организм ранее.
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.

по теме
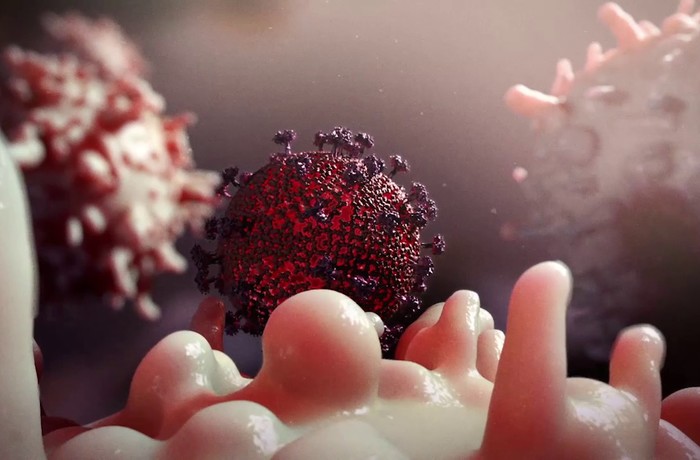
Эпидемия
Учёные выяснили, как вирусы обманывают иммунитет
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
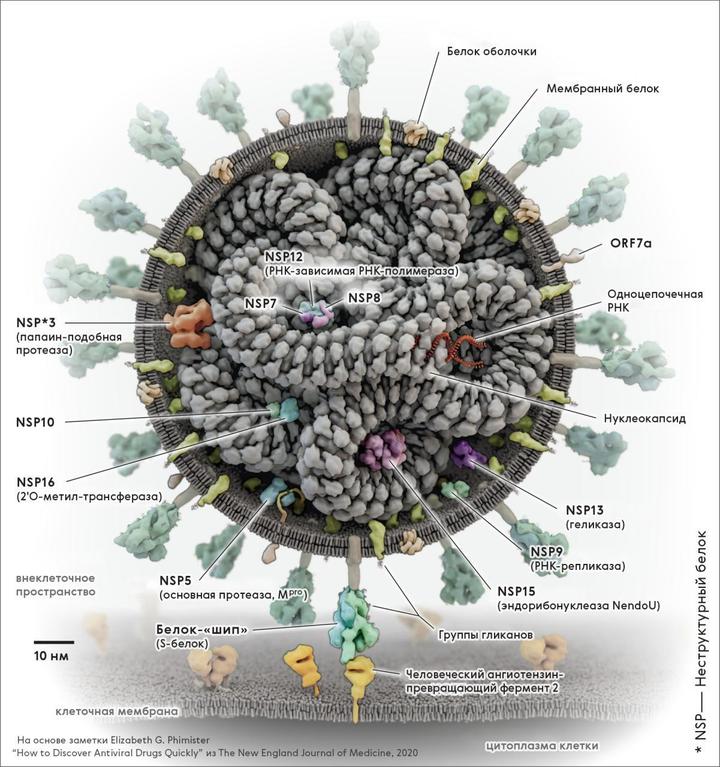
Антитела совершенно точно не являются плохим показателем. Но эксперты в области иммунологии и вирусологии, с которыми я беседовал, согласны с ВОЗ: наличия антител к COVID-19 недостаточно для заявления, что человек к нему больше не восприимчив. Потому что мы до сих пор до конца не знаем, как работает иммунитет к данному вирусу.
Но все это не значит, что тесты на антитела бесполезны. Они могут сыграть важную роль в понимании того, как победить нынешнюю пандемию.
Положительные результаты тестов на антитела, безусловно, указывают на возможное присутствие иммунитета, но не показывают полной картины. А вот, что покажет.
3D-модель коронавируса студии Visual.
Большинство тестов на антитела указывают на наличие антител, но не на их качество
В идеале врачи ищут у тех, кто переболел COVID-19, нейтрализующие антитела. Но на практике это не так просто.
по теме

Лечение
Второй тест называется реакцией сывороточной нейтрализации. Он гораздо сложнее, на его выполнение уходит несколько дней, и он реже используется. С его помощью можно не только обнаружить антитела, но и подвергнуть их воздействию вируса в клеточной структуре, чтобы понять, насколько эффективно антитела с ним борются.
В лучшем случае ученые соотнесут данные двух тестов и выяснят, какие концентрации антител обеспечивают наиболее высокий уровень иммунной защиты. Но исследования продолжаются, и пока неизвестно, какие уровни антител необходимы для продолжительной иммунной защиты, — говорит Меначери. Ученые также до сих пор пытаются выяснить, является ли наличие антител признаком того, что вы не можете передать вирус другому человеку.
Наблюдение за иммунитетом необходимо вести в течение длительного времени
Наблюдение за такими пациентами в течение долгого времени может помочь лучше понять, какое сочетание антител необходимо для развития устойчивого иммунитета.
Еще один вопрос, требующий ответа: как долго действует иммунитет?
По причинам, которые ученым до конца неясны, к некоторым инфекциям формируется пожизненный иммунитет. Например, люди с иммунитетом к оспе больше не могут ей заразиться. Антитела, защищающие организм от оспы, обнаруживались даже через восемьдесят восемь лет после вакцинации.
Оптимизма не добавляет и недавно опубликованное предварительное исследование ученых из Колумбийского университета, показавшее, что некоторые люди заражаются коронавирусом (тем, что вызывает обычную простуду) повторно в течение года.
Однако даже если антитела у вас пропадут, это вовсе не значит, что вы снова станете полностью восприимчивы к вирусу. Да, все не так просто.
Ученые провели несколько экспериментов, когда добровольцев подвергали воздействию штамма коронавируса, вызывающего обычную простуду. Результаты показали, что, как правило, уровень антител к данным штаммам снижается через год или около того.
Читайте также:

