Индикация вирусов на лабораторных животных
Обновлено: 24.04.2024
Для выявления (индикации) вирусов применяются следующие методы.
Индикация вирусов в культуре клеток осуществляется, прежде всего, по цитопатическому действию (ЦПД) вирусов, сроки и характер которого зависят от свойств вируса, проявляясь дегенеративными изменениями клеток с последующей их гибелью и отслаиванием от стекла (рис. 29).
Полная дегенерация клеток сопровождается значительными изменениями в виде пикноза ядра и цитоплазмы, отслаиванием клеточного монослоя от стекла. Частичная дегенерация культур клеток может протекать по следующим типам:
гроздеобразования (округление, увеличение и слияние клеток с образованием гроздевидных скоплений, типично для аденовирусов),
очаговой деструкции (очаги пораженных клеток на фоне в целом сохранившегося монослоя), характерной для вирусов гриппа;
симпластообразования (слияние клеток с образованием гигантских многоядерных клеток в виде симпластов или синцитиев, характерных для вирусов кори, паротита, парагриппа, респираторно-синцитиального, герпеса, иммунодефицита человека).
Пролиферативный тип ЦПД с трансформацией клеток в злокачественные, обладающие неограниченными потенциями к росту, способны вызывать онкогенные вирусы.
Сроки, в течение которых наступает ЦПД, вариабельны (например, 1-2 дня у полиовирусов, 7-14 суток у аденовирусов).


Рис. 29. Культура клеток почек обезьян (а – незараженная, б – цитопатическое действие вируса) х200
Индикация вирусов с помощью реакции гемадсорбции (РГад). Сущность этой реакции заключается в способности эритроцитов человека или животных адсорбироваться на поверхности клеток, инфицированных рядом вирусов (например, орто и парамиксовирусов и др.) в ранние сроки их репродукции (до развития ЦПД) в результате действия гемагглютининов – гликопротеидов, входящих в состав суперкапсида вируса. Для постановки РГад в культуру клеток добавляют 0,2 мл 0,5%-й взвеси эритроцитов, выдерживают 15-20 мин при температуре 4 0 , 20 0 или 37 0 С в зависимости от свойств вируса, после чего взвесь эритроцитов удаляют и производят учет реакции под малым увеличением микроскопа по скоплению эритроцитов на отдельных клетках или на всем монослое.
Индикация вирусов по цветной пробе. Принцип метода основан на определении кислых продуктов метаболизма, накаливающихся в клетке в процессе ее жизнедеятельности с помощью индикатора фенолового красного, меняющего свой цвет с красного в щелочной среде на оранжево-желтый в кислой среде. При заражении культуры клеток вирусами, вызывающими ЦПД (например, аденовирусы, энтеровирусы и др.), метаболизм клеток подавляется, рН среды не меняется и она остается окрашенной в красный цвет.
Индикация вирусов по внутриклеточным включениям. Репродукция некоторых вирусов (оспы, герпеса, бешенства) приводит к образованию внутриклеточных включений, локализующихся в цитоплазме или в ядре клеток и представляющих собой скопления вируса (или его антигенов). Включения выявляют путем световой микроскопии культур клеток, окрашенных по Романовскому- Гимзе или другими методами, а также с помощью прямого флюорохромирования (например акридиновым оранжевым) с последующей микроскопией препаратов в люминесцентном микроскопе.
Индикация вирусов с помощью прямой РИФ – выявление вирусных антигенов, находящихся в инфицированной клетке культуры ткани, с помощью антител диагностической иммунной сыворотки, специфических иммуноглобулинов или моноклональных антител, меченых флюорохромом, обычно флюоресцеином (рис. 30).
Индикация вирусов с помощью электронно-микроскопического метода (ЭММ) применяется, в основном, в научных исследованиях. Материал для ЭММ концентрируют различными методами (ультрацентрифугирование, хроматография на колонках, адсорбцией с помощью специальных сорбентов или антител – для метода иммунной электронной микроскопии). ЭММ позволяет обнаружить в ядре или цитоплазме клеток отдельные вирионы, а также их скопления. В практических целях ЭММ может быть полезен для индикации и идентификации вирусов с типичной морфологией (оспенные вирусы, ротавирусы, коронавирусы, ВИЧ и т.д.).

Рис. 30. Реакция иммунофлюоресценции (РИФ) – выявление вирус-специфических антигенов. х900
Индикация вирусов по образованию бляшек - очагов разрушенных вирусом монослоя культуры клеток под агаровым покрытием. Количество бляшек отражает инфекционную активность вируса.
Для постановки этой пробы вирусную суспензию в разных разведениях вносят в культуры ткани, находящиеся в плоских сосудах, после чего монослой клеток заливают гелем (слой агара или бентонита с индикатором нейтральным красным). Время бляшкообразования для большинства вирусов, обладающих ЦПД, варьирует от 36 до 48 ч. Бляшки выглядят в виде неокрашенных светлых пятен на розово-красном фоне окрашенного монослоя. В бентонитовом методе монослой клеток молочного цвета, бляшки прозрачные.
Индикация вирусов в куриных эмбрионах. Зараженные РКЭ инкубируют в термостате при 35- 37 0 С в течение 48 -72 ч., после чего производят их вскрытие, амниотическую и аллантоисную жидкость отсасывают шприцем, а оболочки и эмбрион извлекают и помещают в стерильные чашки Петри.
При репродукции некоторых вирусов (натуральной оспы, осповакцины, простого герпеса) на ХАО куриных эмбрионах появляются характерные бляшки - беловатые пятна диаметром 1-2 мм, количество которых соответствует числу инфекционных частиц.
В аллантоисной и амниотической жидкости зараженных эмбрионов ряд вирусов (например, ортомиксовирусы, парамиксовирусы, аденовирусы и т.д.) может быть выявлен с помощью реакция гемагглютинации (РГА). Принцип реакции состоит в способности гемагглютининов -поверхностных вирусных структур гликопротеидной природы этих вирусов склеивать (агглютинировать) эритроциты определенных видов животных, птиц или человека. РГА не относится к иммунологическим реакциям, поскольку в ее основе отсутствует взаимодействие АГ и AT.
Определение титра вирусов можно проводить также на хорионаллантоисной оболочке. Для этого в лунки стерильных полистироловых пластин помещают кусочки скорлупы 11-12-дневного куриного эмбриона с неповрежденной ХАО, добавляют вирусосодержащую жидкость в десятикратных разведениях на буфере, накрывают пластины фольгой и инкубируют при 35-37 0 С в течение 24-72 часов. После этого скорлупу удаляют, добавляют 0,5% взвесь куриных эритроцитов и производят учет реакции по эффекту гемагглютинации, который свидетельствует о репродукции вируса.
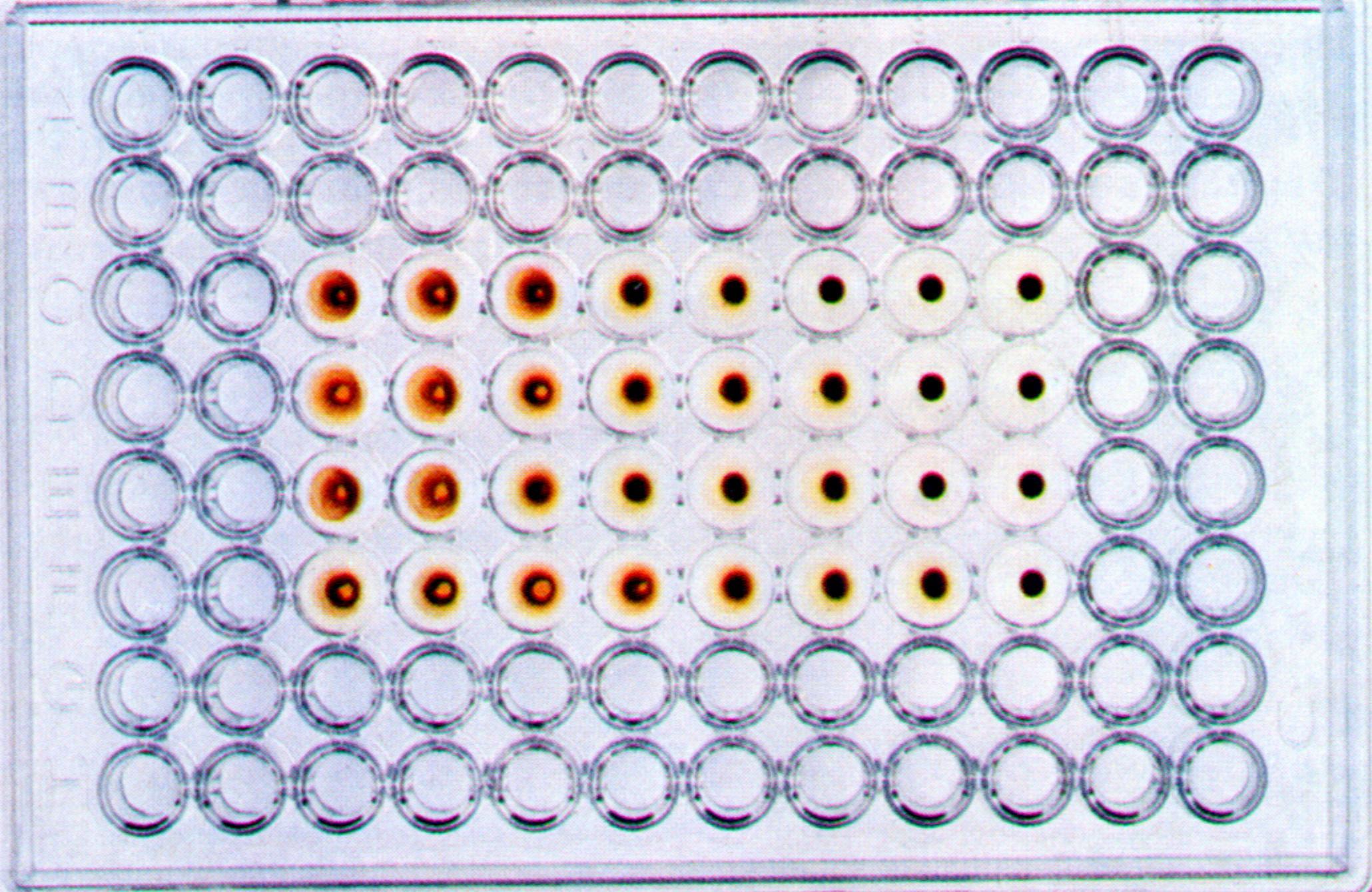
Рис. 31. Реакция гемагглютинации для выявления вируса гриппа в хорион-аллантоисной жидкости куриного эмбриона.
Индикация вирусов в организме лабораторных животных находится в зависимости от вируса и вида чувствительного лабораторного животного, будет описана в лабораторной диагностике конкретных вирусных инфекций.
Культивирование вирусов в организме лабораторных животных.
Выбор экспериментальных животных определяется целью работы и видовой чувствительностью к изучаемому вирусу. Для заражения используют обезьян, кроликов, морских свинок, хомячков, белых крыс и мышей.
- Для обнаружения вируса - биопроба.
- Для выделения вируса и получения вирус содержащего материала от положительной биопробы.
- Для поддержания вируса в лаборатории, т.е. для сохранения его в активной форме в течении многих лет. Это достигается путем чередований пассажей и хранений в консервирующих условиях. Пассаж - заражение живого объекта с последующим получением новой популяции вируса.
- Для накопления вирусной массы с целью исследования вируса и получения вакцин.
- Для титрования вирусов.
- Как тест-объект в реакции нейтрализации.
Лабораторных животных заражают различными способами в зависимости от тропизма вируса к определенным тканям. Так, например, для культивирования нейротропных вирусов заражение производят преимущественно в мозг (вирусы бешенства, клещевого энцефалита и др.), культивирование респираторных вирусов осуществляется при интраназальном инфицировании животных (вирусы гриппа), дерматотропных (вирус оспы) - путем накожного и внутрикожного заражения. Наиболее часто используются накожное, внутрикожное, внутримышечное, внутрибрюшинное и внутримозговое заражение.
При первичном заражении животные могут не заболеть, поэтому через 5-7 дней внешне здоровых животных убивают, а из их органов готовят суспензии, которыми заражают следующие партии животных. Эти последовательные заражения называются `пассажами'.
Индикацию, т.е. обнаружение факта размножения вируса, устанавливают на основании развития типичных признаков заболевания, патоморфологических изменений органов и тканей животных или положительной реакции гемагглютинации (РГА). РГА основана на способности некоторых вирусов вызывать агглютинацию (склеивание) эритроцитов различных видов животных, птиц и человека за счет поверхностного вирусного белка - гемагглютинина.В настоящее время использование животных для культивирования вирусов ограничено.
1. Гибель в характерные для данного вируса сроки.
2. Характерные клинические признаки.
3. Характерные патологоанатомические изменения.
- обнаружить характерные для данной вирусной патологии изменения во внутренних органах.
- взять материал для последующих пассажей (материал берется в зависимости от тропизма вируса).
Для выявления (индикации) вирусов применяются следующие методы.
Индикация вирусов в культуре клеток осуществляется, прежде всего, по цитопатическому действию (ЦПД) вирусов, сроки и характер которого зависят от свойств вируса, проявляясь дегенеративными изменениями клеток с последующей их гибелью и отслаиванием от стекла (рис. 29).
Полная дегенерация клеток сопровождается значительными изменениями в виде пикноза ядра и цитоплазмы, отслаиванием клеточного монослоя от стекла.
Частичная дегенерация культур клеток может протекать по следующим типам:
- гроздеобразования (округление, увеличение и слияние клеток с образованием гроздевидных скоплений, типично для аденовирусов),
- очаговой деструкции (очаги пораженных клеток на фоне в целом сохранившегося монослоя), характерной для вирусов гриппа;
- симпластообразования (слияние клеток с образованием гигантских многоядерных клеток в виде симпластов или синцитиев, характерных для вирусов кори, паротита, парагриппа, респираторно-синцитиального, герпеса, иммунодефицита человека).
Пролиферативный тип ЦПД с трансформацией клеток в злокачественные, обладающие неограниченными потенциями к росту, способны вызывать онкогенные вирусы.
Сроки, в течение которых наступает ЦПД, вариабельны (например, 1-2 дня у полиовирусов, 7-14 суток у аденовирусов).


А б
Рис. 29. Культура клеток почек обезьян (а – незараженная, б – цитопатическое действие вируса) х 200
Индикация вирусов с помощью реакции гемадсорбции (РГад).
Сущность этой реакции заключается в способности эритроцитов человека или животных адсорбироваться на поверхности клеток, инфицированных рядом вирусов (например, орто и парамиксовирусов и др.) в ранние сроки их репродукции (до развития ЦПД) в результате действия гемагглютининов – гликопротеидов, входящих в состав суперкапсида вируса. Для постановки РГад в культуру клеток добавляют 0,2 мл 0,5%-й взвеси эритроцитов, выдерживают 15-20 мин при температуре 4 0 , 20 0 или 37 0 С в зависимости от свойств вируса, после чего взвесь эритроцитов удаляют и производят учет реакции под малым увеличением микроскопа по скоплению эритроцитов на отдельных клетках или на всем монослое.
Индикация вирусов по цветной пробе.
Принцип метода основан на определении кислых продуктов метаболизма, накаливающихся в клетке в процессе ее жизнедеятельности с помощью индикатора фенолового красного, меняющего свой цвет с красного в щелочной среде на оранжево-желтый в кислой среде. При заражении культуры клеток вирусами, вызывающими ЦПД (например, аденовирусы, энтеровирусы и др.), метаболизм клеток подавляется, рН среды не меняется и она остается окрашенной в красный цвет.
Индикация вирусов по внутриклеточным включениям.
Репродукция некоторых вирусов (оспы, герпеса, бешенства) приводит к образованию внутриклеточных включений, локализующихся в цитоплазме или в ядре клеток и представляющих собой скопления вируса (или его антигенов). Включения выявляют путем световой микроскопии культур клеток, окрашенных по Романовскому - Гимзе или другими методами, а также с помощью прямого флюорохромирования (например акридиновым оранжевым) с последующей микроскопией препаратов в люминесцентном микроскопе.
Индикация вирусов с помощью прямой РИФ – выявлениевирусных антигенов, находящихся в инфицированной клетке культуры ткани, с помощью антител диагностической иммунной сыворотки, специфических иммуноглобулинов или моноклональных антител, меченых флюорохромом, обычно флюоресцеином (рис. 30).
Индикация вирусов с помощью электронно-микроскопического метода (ЭММ) применяется, в основном, в научных исследованиях. Материал для ЭММ концентрируют различными методами (ультрацентрифугирование, хроматография на колонках, адсорбцией с помощью специальных сорбентов или антител – для метода иммунной электронной микроскопии). ЭММ позволяет обнаружить в ядре или цитоплазме клеток отдельные вирионы, а также их скопления. В практических целях ЭММ может быть полезен для индикации и идентификации вирусов с типичной морфологией (оспенные вирусы, ротавирусы, коронавирусы, ВИЧ и т.д.).

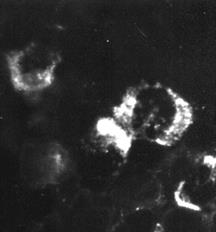
Рис. 30. Реакция иммунофлюоресценции (РИФ) – выявление вирус-специфических антигенов. х 900
Индикация вирусов по образованию бляшек - очагов разрушенных вирусом монослоя культуры клеток под агаровым покрытием. Количество бляшек отражает инфекционную активность вируса.
Для постановки этой пробы вирусную суспензию в разных разведениях вносят в культуры ткани, находящиеся в плоских сосудах, после чего монослой клеток заливают гелем (слой агара или бентонита с индикатором нейтральным красным). Время бляшкообразования для большинства вирусов, обладающих ЦПД, варьирует от 36 до 48 ч. Бляшки выглядят в виде неокрашенных светлых пятен на розово-красном фоне окрашенного монослоя. В бентонитовом методе монослой клеток молочного цвета, бляшки прозрачные.
Индикация вирусов в куриных эмбрионах.
Зараженные РКЭ инкубируют в термостате при 35- 37 0 С в течение 48 -72 ч., после чего производят их вскрытие, амниотическую и аллантоисную жидкость отсасывают шприцем, а оболочки и эмбрион извлекают и помещают в стерильные чашки Петри. При репродукции некоторых вирусов (натуральной оспы, осповакцины, простого герпеса) на ХАО куриных эмбрионах появляются характерные бляшки - беловатые пятна диаметром 1-2 мм, количество которых соответствует числу инфекционных частиц.
В аллантоисной и амниотической жидкости зараженных эмбрионов ряд вирусов (например, ортомиксовирусы, парамиксовирусы, аденовирусы и т.д.) может быть выявлен с помощью реакция гемагглютинации (РГА). Принцип реакции состоит в способности гемагглютининов - поверхностных вирусных структур гликопротеидной природы этих вирусов склеивать (агглютинировать) эритроциты определенных видов животных, птиц или человека. РГА не относится к иммунологическим реакциям, поскольку в ее основе отсутствует взаимодействие АГ и AT.
Гемагглютинационный титр (максимальное разведение вирусосодержащей жидкости, вызывающее агглютинацию эритроцитов - одна гемагглютинирующая единица вируса,1 ГЕ) соответствует концентрации вируса. Агглютинацию эритроцитов могут вызывать также некоторые бактерии (стафилококки, эшерихии, сальмонеллы, шигеллы, холерный вибрион Эль-Тор), что необходимо учитывать при трактовке результатов РГА при исследовании вирус-содержащего материала, загрязненного бактериальной микрофлорой.
Определение титра вирусов можно проводить также на хорионаллантоисной оболочке.Для этого в лунки стерильных полистироловых пластин помещают кусочки скорлупы 11-12-дневного куриного эмбриона с неповрежденной ХАО, добавляют вирусосодержащую жидкость в десятикратных разведениях на буфере, накрывают пластины фольгой и инкубируют при 35-37 0 С в течение 24-72 часов. После этого скорлупу удаляют, добавляют 0,5% взвесь куриных эритроцитов и производят учет реакции по эффекту гемагглютинации, который свидетельствует о репродукции вируса.
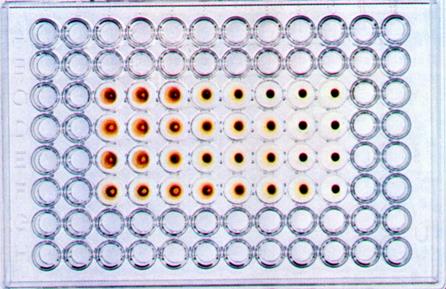
Рис. 31. Реакция гемагглютинации для выявления вируса гриппа в хорион-аллантоисной жидкости куриного эмбриона.
Индикация вирусов в организме лабораторных животных находится в зависимости от вируса и вида чувствительного лабораторного животного, будет описана в лабораторной диагностике конкретных вирусных инфекций.
Идентификация вирусов проводится с помощью следующих методов .
Учет вирусиндуцированных патологических изменений в чувствительных живых системах.
Изучение антигенных свойств вирусов в серологических реакциях с противовирусными сыворотками является основным методом идентификации вирусов. Для этого используют ряд иммунологических реакций.
Реакция нейтрализации основана на способности антител нейтрализовать инфекционную активность вирусов в культурах ткани, РКЭ, чувствительных лабораторных животных. Из вирус-содержащего материала готовят десятикратные разведения и добавляют к ним специфическую сыворотку в разведении в соответствии с титром, указанным на этикетке ампулы. Смеси вирус-сыворотка инкубируют 30 — 60 мин при 37 °С для обеспечения связывания антигенов с антителами, после чего смесью заражают культуру ткани, куриные эмбрионы или лабораторных животных. Контролем является чувствительная биосистема, зараженная вирусом без сыворотки.
Реакция считается положительной в случае нейтрализации ЦПД в культуре клеток, а также при отсутствии патологических изменений в куриных эмбрионах или в организме животных. По результатам РН высчитывается индекс нейтрализации (ИН - отношение титра вируса в контроле к титру вируса в опыте). При ИН менее 10 реакция расценивается как отрицательная, от 11 до 49 — сомнительная, от 50 и выше — положительная.
РН может быть поставлена в наиболее чувствительном варианте - подавления вирусного бляшкообразования под действием вирусспецифической антисыворотки. Для этого к вирус-содержащему материалу добавляют соответствующую искомому вирусу антисыворотку и после инкубации в термостате при 37 0 С течение 30-60 мин смесь вносят в культуру чувствительных клеток. Бляшкообразование выявляют в слое агара или бентонита. Идентичность вируса антителам сыворотки проявляется подавлением бляшкообразования.
Другим вариантом РН является цветная проба. Положительный результат пробы в случае соответствия вируса противовирусным антителам проявляется блокадой репродукции вируса, клетка при этом остается жизнеспособной, вырабатывая кислые продукты метаболизма, под влиянием которых цвет индикатора (фенолового красного) меняется с красного на желтый. Для постановки пробы в пробирки вносят по 0,25 мл рабочего разведения вируса и соответствующую антисыворотку.
Смесь выдерживают при комнатной температуре 30-60 мин, добавляют в каждую пробирку по 0,25 мл клеточной суспензии и закрывают их резиновыми пробками. Пробирки инкубируют в термостате при 37 0 С 6-8 дней, результаты реакции учитывают по изменению цвета индикатора (красный цвет индикатора соответствует щелочному характеру рН - 7,4 указывая на репродукцию вируса и подавление метаболизма клеток; желтый цвет свидетельствует о кислом рН - ниже 7,2 в результате нейтрализации вируса антителами и активном метаболизме клеток с выработкой кислых продуктов обмена).
Перед постановкой РТГА сыворотки обрабатывают периодатом калия, каолином, бентонитом, ацетоном или другими веществами для удаления неспецифических ингибиторов гемагглютинации. После этого к двукратным разведениям сыворотки добавляют равное количество вируссодержащей жидкости с активностью 4 ГЕ, смесь инкубируют 30-60 мин при оптимальной для данного вируса температуре (4 0 , 20 0 , 37 0 С), а затем добавляют равный объем 0,5-1,0% взвеси эритроцитов. Смесь снова инкубируют 30-45 мин и производят учет результатов реакции. Титром сыворотки считают ее наибольшее разведение, которое вызывает торможение гемагглютинации.
Реакция торможения гемадсорбции (РТГадс) основана на нейтрализации эффекта адсорбции эритроцитов на поверхности клеток, инфицированных вирусами, способными вызывать гемадсорбцию. Для постановки реакции по 0,2 мл специфической сыворотки, разведенной 1:5, вносят в пробирки, инкубируют 30-60 мин в термостате при оптимальной для данного вируса температуре, затем добавляют по 0,2 мл 0,5% взвеси эритроцитов. Контрольные пробы содержат неиммунную сыворотку и эритроциты. Пробирки снова инкубируют 20-30 мин, после чего производят учет реакции. Идентификация вируса основывается на признаке отсутствия адсорбции эритроцитов на клетках в присутствии иммунной сыворотки при наличии гемадсорбции в контрольных пробирках.
Для антигенной идентификации вирусов в клетках культур тканей используются также РПГ, РСК, РИФ, РОПГА ИФА, РИА со специфическими иммунными противовирусными сыворотками или моноклональными AT.
- выявление вирусной НК методами генодиагностики с помощью метода молекулярной гибридизации и ПЦР;
- электронно-микроскопическое изучение вирусов (см. выше).
Индикацию, т.е. обнаружение факта размножения вируса, устанавливают на основании развития типичных признаков заболевания, патоморфологических изменений органов и тканей животных или положительной реакции гемагглютинации (РГА).
26)Что такое цпд? Виды цпд?
ЦПД - (цитопатическое действие вирусов) - деструктивные изменения отдельных клеток и клеточного монослоя, возникающие в результате продуктивной вирусной инфекции клеток и цитотоксического действия вирионов. В клеточном монослое ЦПД проявляется в форме сплошной или очаговой круглой или полиморфноклеточной дегенерации, образовании многоядерных клеток или клеточных симпластов, а также в пролиферативном разрастании клеток. В пораженных вирусом клетках ЦПД проявляется в пикнозе ядра, маргинации и зернистости хроматина, появлении включений, телец, кристаллов; в цитоплазме появляются вакуоли, наступает ее сморщивание и дегенерация. ЦПД используют для индикации и идентификации вирусов.
Виды: 1. Равномерная мелкозернистая деструкция клеток
(полиовирусы , вирусы Коксаки).
2. Очаговая мелкозернистая дегенерация клеток
З. Гроздевидная дегенерация клеток (аденовирусы).
4. Крупнозернистая равномерная деструкция клеток
5. симластообразование (вирус кори).
27) Механизм рга и ргАдс
на поверхности эритроцитов имеются рецепторы мукопротеидной природы, способные адсорбировать вирионЫ , а на поверхности гемагглютинирующих вирусов располагаются гемагтлютинины - сложные белковые тела с энзиматической активностью. При смешивании эритроцитов с вирусосодержащей жидкостью гемагтлютинины вируса при помощи фермента муциназы вступают во взаимодействие с рецепторами эритроцитов, в результате чего происходит адсорбция вирусов на эритроцитах. Вирионы, адсорбированные на одном эритроците, способны свободными поверхностями соединяться с другими эритроцитами, образуя при этом мостики между ними, что и приводит к склеиванию (агглютинации) эритроцитов. Адсорбция вирусов на эритроцитах является энзимэтическим процессом
28)Цветная реакция механизмы
При репродукции в ткани вирусов клетки гибнут и цвет среды не меняется. Добавление специфической сыворотки нейтрализует вирус, гибель клетки не происходит и индикатор ( феноловый красный) в кислой среде меняет свой цвет с малинового на желтый. При росте клеток, не пораженных вирусом, происходит накопление кислых продуктов метаболизма что приводит к изменению рн среды и цвета индикатора
29)Метод бляшек механизм. В основе метода лежит образование в местах цитопатогенного действия вируса обесцвеченных пятен, так как пораженные клетки теряют способность сохранять или воспринимать витальные окрашивания. Пятна, или бляшки, представляют собой изолированные колонии вируса в однослойных культурах, видимые микроскопиически в виде неокрашенных округлых форм, четко выделяющиеся на фоне живых клеток, окрашенных в красный цвет.
30. Бактериофаги - бактериальные вирусы, вызывающие разрушение (лизис) бактерий и других микроорганизмов. Бактериофаги размножаются в клетках, лизируют их и переходят в др., как правило, молодые, растущие клетки. Бактериофаги состоят из головки округлой, гексагональной или палочковидной формы диаметром 45-140 нм и отростка толщиной 10-40 и длиной 100-200 нм (рис.). Другие Бактериофаги не имеют отростка; одни из них округлы, другие - нитевидны, размером 8х800 нм. Содержимое головки состоит преимущественно из РНК и небольшого количества белка. Отросток имеет вид полой трубки, окруженной чехлом, содержащим сократительные белки, подобные мышечным. У ряда Бактериофагов чехол способен сокращаться, обнажая часть стержня. На конце отростка у многих Бактериофаги имеется базальная пластинка с несколькими шиловидными или другие формы выступами. От пластинки отходят тонкие длинные нити, которые способствуют прикреплению фага к бактерии. Оболочки головки и отростка состоят из белков. Каждый Бактериофаг обладает специфическими антигенными свойствами, отличными от антигенов бактерии-хозяина и других фагов. Имеются антигены, общие для ряда фагов (особенно содержащих РНК). Некоторые фаги применяли для профилактики и лечения ряда бактериальных инфекционных болезней человека (дизентерия, брюшной тиф, холера, чума, стафилококковые и анаэробная инфекции и др.) и животных. Однако антибиотики и другие химиотерапевтические средства оказались эффективнее фагов, в связи с чем применение их с лечебной целью сузилось. Бактериофаги успешно применяются при определении вида бактерий, актиномицетов. Бактериофаги могут вредить производству антибиотиков, аминокислот, молочных продуктов, бактериальных удобрений и в других отраслях микробиологического синтеза.
32.Контаминация — попадание загрязнителей в образец или культуру;засорение (загрязнение) чистой культуры посторонними микроорганизмами. Деконтаминация—процесс уничтожения микробов в (на) каких-либо объектах. Д. осуществляют дезинфекцией или стерилизацией.Дезинфекция — комплекс мер по уничтожению патогенных микробов и резкое снижение общей микробной обсемененности материала или объекта. Стерилизация — обеспложивание, объектов, при кт уничтожаются все формы микроорганизмов. Асептика - совокупность мер, направленных на предупреждение попадания микробов в организм. Антисептика - комплекс мероприятий, направленных на уничтожение микробов в ране, патологическом очаге или организме в целом, на предупреждение или ликвидацию инфекционного воспалительного процесса.
33. Деконтаминация—процесс уничтожения микробов в (на) каких-либо объектах. Д. осуществляют дезинфекцией или стерилизацией. Цель в медицине – отрыв путей передачи, опосредованных мед.оборудованием или действиями врача, и снижение риска передачи инфекционных заболеваний.Воздействие на клеточные стенки гр+ бактерий и грибов должно состоять в разрушении оболочки из пептидогликана или хитина, так же в учете наличия в кл.стенкетейхоевых кислот. Разрушение пойдет по пептидным связям, по кислородным мостикам между гликозидными кольцами. Оболочка споры из денатурированного белка, следовательно мало нарушить структуру белка, надо разрушить вторичну структуру белка, по ковалентным связям: окислять амикислотные остатки или разрывать пептидные связи. У гр- над пептидогликановой оболочкой есть еще внешняя мембрана, где ЛПС, липопротеины и белки-порины. Необходимо определить мин.плотность необходимых нарушений хим.связей для нарушения целостности, стабильности и связаностикл.стенок. У вирусо надо не только разрушить белковую оболочку, но и уничтожить наследственную информацию. У вироидов белковой оболочки нет, только наслед.материал. Для уничтожения приона необходимо разрушить все молекулы, образующие его.
34. Физические факторы деконтаминации: температура, высушивание, фильтрование, лучистая энергия (уф и ионизирующее излучение), ультразвук, ионизированная плазма. Хим. Факторы: атибиотики, антисептики, дезинфектанты, консерванты, фенолы, галогены, спирты, ПАВ, соли тяж.металлов, красители, окислители, кислоты и щелочи, альдегиды.
35. Методы дезинфекции:
Механический, физический метод заключается в высокотемпературной обработке.Химический, биологический метод основан на использовании антагонизма различных видов микроорганизмов. Так, при использовании бактериофагов, то есть вирусов бактерий, уничтожаются стафилококки, синегнойная палочка, брюшнотифозные бактерии и т. д. Методы стерилизации: тепловая (прокаливание.Сухой жар, под давлением, текучий пар), газовая, химическая (перекись водорода, хлоргексидин, формальдегид, спирт), ультразвуком, уф и гамма-излучением, плазмой.
37. Автоклав: 1 атм 45 мин 120 0 , 2 атм 20 мин 132 0 . Газовый аппарат 30 мин. Р-ры хим. в-в. Ультразвук с моющим средством 15 мин. УФ и гамма-излучение 1 час. Плазмой 10-15 мин.
№38Современные методы стерилизации .контроль стерилизации. Физические методы: высокая тем.,ионизируещее излучение , фильтрование., глас- перленовый стерилизатор при тем=250гр.Комбенированные методы стерилизации:-газовая –изделия стерил от 4- 16 ч.контроль процесса ведут приборы.Плазменная стерилизация- 10 -15 мин, в зависимости от загрязнений.обьем камеры 1 л.Контроль: по показанию приборов.,с использованием физико – хим тестов.,биологические тесты, молекулярно-генетический метод контроля.( анаэробные, вирусы)
№ 39.правила техники безопасности при раб. С биоматериалом инф.ВИЧ. – заклеять открытые раны лейкопластырем.- использовать латексные перчатки однаразовые Во время работы перчатки обрабатывать 70% спиртом или другими дезинфектантами, - мыть руки с мылом немедленно после контакта с кровью или биологическими жидкостями организма; - защищать лицо – марлевой повязкой, глаза – очками или щитком. - обрабатывать поверхность рабочих столов, загрязненных кровью, немедленно 3% раствором хлорамина или 6% раствором перекиси водорода с 0,5% раствором моющего средства дважды с интервалом в 15 минут; - запрещать пипетирование ртом. Засасывание в капилляры производить только с помощью резиновых груш; - шприцы, иглы и катетеры сразу после использования помещают в специальный контейнер для дезинфекции и утилизации; - иметь на рабочем месте аптечки и достаточное количество дезинфицирующих средств.
№40. Микробный антагонизм- при котором один вид микробов угнетает развитие других, довольно широко распространен в природе.это -отношения между микроорганизмами выработались на протяжении длительного периода эволюции в борьбе за существование.
Хим факторы: Антибиотики- вещ-ва. Блокирующие ферментативный процесс в клетке,или разрушает основные ее структуры. Гликопротеиновой или протеиновая структура..Бактериоцины- в-ва, белковой природы,короткие пептидные цепочки, без ферментативной активности., действуя через специф. или неспециф. Клеточные рецепторы. Токсические продукты метаболизма- ислоты, эфиры, амины, сероводород, перекись. Формирование биопленки.
№41. Классификация антибиотиков по происхождению.1)из грибов, например рода Penicillium (пенициллин), рода Cephalosporium (цефалоспорины) 2)из актиномицетов; группа включает около 80% всех антибиотиков. Среди актиномицетов основное значение имеют представители рода Streptomyces, являющиеся продуцентами стрептомицина, эритромицина, левомицетина. 3)Антибиотики, продуцентами кт являются собственно бактерии.Bacillus и Pseudomonas,полимиксины, бацитрацины, грамицидин.4) животного происхождения; из рыбьего жира получают эктерицид, из молок рыб – экмолин, из эритроцитов – эритрин. 5) растительного происхождения. которые выделяют лук, чеснок, сосна, ель, сирень, другие растения. Антимикробным действием обладают многие растения, например, ромашка, шалфей, календула.




Рис. 2. Заражение куриного эмбриона на ХАО через естественную воздушную камеру
(по Николау)
Рис. 3. Заражение куриного эмбриона в аллантоисную полость (по Николау)
Заражение через искусственную воздушную камеру применяют чаще первого, так как оно обеспечивает контакт вируссодержащего материала с большей поверхностью ХАО и, следовательно, ведет к образованию большего количества вируса. Для заражения эмбриона этим методом его помещают в штатив горизонтально зародышем вверх. В скорлупе делают два отверстия: одно небольшое над центром воздушной камеры (предназначено для отсасывания из нее воздуха), а другое диаметром 0,2-0,5 см сбоку, со стороны зародыша. Сложность метода в том, что, делая второе отверстие, необходимо осторожно снять вначале кусочек скорлупы, затем скользящим движением, не повреждая ХАО, сдвинуть подскорлупную оболочку в сторону так, чтобы через образовавшийся дефект мог пройти воздух. После этого резиновой грушей через первое отверстие отсасывают воздух из естественной воздушной камеры (рис. 4, а). В результате через боковое отверстие наружный воздух устремляется внутрь, образуя искусственную воздушную камеру, дном которой является ХАО (рис. 4, б).

,
Рис. 4. Заражение куриного эмбриона на ХАО через искусственную воздушную камеру (по Николау и др.)
Через боковое отверстие на поверхность ХАО наносят инфекционную жидкость и отверстие закрывают кусочком лейкопластыря. Закрывать первое отверстие нет необходимости, так как внутренний листок подскорлупной оболочки при этом методе заражения не нарушается и продолжает выполнять роль барьера для микрофлоры окружающей среды.
Дальнейшую инкубацию эмбрионов, зараженных этим методом, проводят в горизонтальном положении боковым отверстием вверх.
Заражение в желточный мешок. Большей частью им пользуются для размножения хламидий, а также вирусов болезни Марека, ринопневмонии лошадей, катаральной лихорадки овец и др. Заражают эмбрионы 5-7-дневного, а иногда и 2-3-дневного возраста (вирус лихорадки долины РИФ). Используют два варианта заражения (рис. 6).


Рис. 5. Заражение куриного эмбриона в амниотическую полость (по Николау и др.)
Рис. 6. Заражение куриного эмбриона в желточный мешок (по Николау и др.)
Первый вариант. Иногда путь заражения осуществляется на горизонтально укрепленном в штативе эмбрионе, при этом зародыш находится внизу, а желток - над ним. Отверстие в скорлупе закрывают каплей расплавленного парафина.
Второй вариант. Эмбрионы помещают в штатив в вертикальном положении. Делают отверстие в скорлупе над центром воздушной камеры и вводят иглу на глубину 3,5-4 см под углом 45° к вертикальной оси в направлении, противоположном месту нахождения зародыша.
Заражение в амниотическую полость. Для этой цели используют эмбрионы 6-10-дневного возраста. Метод используется при культивировании вирусов гриппа, ньюкаслской болезни, ринопневмонии лошадей и др. Есть два способа заражжения (рис. 5).
Закрытый способ. Заражение проводят в затемненном боксе. Яйцо помещают на овоскопе в горизонтальном положении зародышем вверх. Через отверстие в скорлупе над воздушной камерой вводят иглу с затупленным концом по направлению к зародышу. Доказательством того, что игла проникла в амнион, служит движение тела зародыша в направлении передвижения.
Открытый способ. Скорлупу над воздушной камерой срезают так, чтобы образовалось окно диаметром 1,5-2,5 см. Через него пинцетом под контролем глаза снимают подскорлупную оболочку. Затем анатомический (14 см) пинцет с сомкнутыми браншами ведут, продавливая хорионаллантоисную оболочку по направлению к зародышу. Когда пинцет достигнет его, бранши размыкают, захватывают амниотическую оболочку вместе с ХАО и подтягивают к окну. Удерживая левой рукой пинцет с фиксированной в нем оболочкой амниона, вводят вируссодержащий материал (рис. 7). Далее все оболочки опускают, окно закрывают лейкопластырем и эмбрион инкубируют в вертикальном положении.
Заражение в тело зародыша. Для заражения используют эмбрионы 7-12-дневного возраста. Известно два варианта метода.
Первый вариант. Заражают так же, как в амнион закрытым способом, с той лишь разницей, что берут острую иглу и на овоскопе показателем попадания иглы в тело считают подчинение зародыша движениям иглы.
Второй вариант. Заражают так же, как в амнион открытым способом: через окно в скорлупе подтягивают пинцетом тело зародыша. Материал вводят в головной мозг или определенные участки тела. При таких методах заражения бывает значительный процент неспецифической гибели эмбрионов.

Рис. 7. Заражение куриного эмбриона в амнион открытым способом (по Николау и др.)


Рис. 8. Отсасывание аллантоисной жидкости (по Николау)
Рис. 9. Отсасывание амниотической жидкости (по Николау и др.)
Для получения стенки желточного мешка как вируссодержащего материала желток извлекают на чашку Петри, стенку его разрезают ножницами и отполаскивают от содержимого в физиологическом растворе. Тело зародыша извлекают, удерживая его за шею (рис. 10).
При вскрытии куриных эмбрионов ставят бактериологический контроль вируссодержащего материала посевом на МПБ, МПА, МППБ и среду Сабуро. Вируссодержащий материал хранят при минус 25 °С и ниже.
Культивирование с производственными целями на куриных эмбрионах применяется для размножения ряда вирусов (осповакцины, клещевого энцефалита, гриппа, москитной лихорадки и др.). Так, для изготовления гриппозной и оспенной вакцин используют вирусы, размноженные на хорионаллантоисной оболочке, вакцины против москитной лихорадки - в аллантоисной полости, а вирус клещевого энцефалита культивируют в желточном мешке.
Метод размножения вирусов на культурах тканей
Для изготовления живых и инактированных вакцин вирусы размножаются на первичных культурах тканей, а диагностических препаратов также и на перевиваемых культурах.
Для размножения вирусов предложен ряд методов с использованием культур тканей. Такие методы, как Карреля-Берреуза (1910), культивирование кусочков ткани, фиксированных в сгустке плазмы, Меттлендов (1928) - культивирование в переживающих тканях - в настоящее время не используются не только в производстве, но и в исследовательской работе. Эти методы вытеснены культивированием в однослойной культуре клеток.
Работа по культивированию клеток производится в специальных лабораториях при соблюдении высоких требований к стерильности воздуха, посуды, растворов, питательных сред. Используемая посуда должна быть нейтральной, хорошо вымытой и обезжиренной, применяемые реактивы - химически чистыми.

Читайте также:

