Инфекционная активность вакцины это
Обновлено: 23.04.2024
Типы гуморального иммунного ответа при вирусной инфекции. Иммуноглобулин A.
Иммунная система организма на вирусные инфекции или иммунизацию вирусными вакцинами отвечает выработкой антител, обладающих специфичностью к различным вирусным компонентам и принадлежащих к разным классам иммуноглобулинов.
Важнейшая биологическая функция иммуноглобулинов - специфическое связывание с антигеном. Антитела против некоторых эпитопов на поверхности вирионов нейтрализуют инфекционность, они могут также действовать как опсонины, облегчая поглощение и разрушение макрофагами. Кроме того, антитела могут прикрепляться к вирусным антигенам на поверхности инфицированных клеток, вызывая их разрушение вследствие активации классического или альтернативного действия комплемента или с помощью активации Fc-рецепторсвязывающих клеток, таких как NK-клетки, полиморфноядерные лейкоциты и макрофаги (антителозависимая цитотоксичность).
Различают четыре основных класса антител: два мономера IgG и IgE и два полимера IgM и IgA. Все иммуноглобулины имеют подобную структуру, но широко варьируют по аминокислотной последовательности антигенсвязывающего сайта, который определяет их специфичность для данной антигенной детерминанты. N-концевая последовательность L- и Н-цепей образует антигенсвязывающий центр, то есть антидетерминанту. Чем больше антидетерминант на поверхности иммуноглобулина, тем выше его активность.
Авидность характеризует прочность связи антитела с соответствующим антигеном. Афинность - прочность связи между отдельными антидетерминантами и детерминантами.
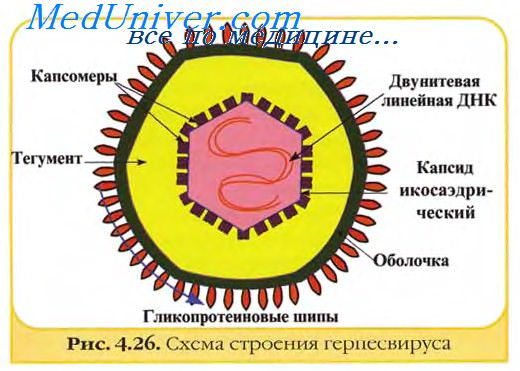
IgG является основным классом антител в крови. Он состоит из двух Н- и L-цепей, каждая из которых содержит постоянные и вариабельные участки. Молекулы IgG содержат два идентичных антигенсвязывающих Fab-фрагмента и Fc-фрагмент, выполняющий эффекторные функции (связывание комплемента, прикрепление к фагоцитам и плацентарному или колостральному трансферу).
В результате системной вирусной инфекции IgG синтезируется в течение длительного периода и является главным фактором защиты от реинфекции. Субклассы IgG отличаются константной областью их V-цепей и, соответственно, биологическими свойствами, такими как фиксация комплемента и прикрепление к фагоцитам.
Первоначально антитела относятся к классу IgM, но соматические рекомбинации (транслокации) затем рождают класс, обусловленный связыванием V-генных сегментов различными постоянными участками Н-цепей. В изменении изотипов (переход изотипов на другой путь) важная роль принадлежит различным цитокинам. Таким образом, через несколько дней IgG , IgA и иногда IgE-антите-ла той же самой специфичности становятся доминантными в иммунном ответе.
Тц-клетки достигают своего пика обычно через неделю после инфекции, а антитела — через 2—3 недели. NK-клетки максимально активируются через два дня, а активность интерферона совпадает с пиком концентрации вируса.
Динамика гуморального иммунного ответа проявляется, в первую очередь, в смене синтеза антител различных классов. В начальной фазе иммунного ответа синтезируется преимущественно IgM с относительно слабым сродством к антигену (авидный класс антител). IgM является пентамером с 10 Fab-фрагментами. Синтез IgM сменяется синтезом IgG, а затем IgA. IgM-антитела находятся в большинстве случаев в плазме крови и лимфе, обладая способностью преципитировать, агглютинировать и лизировать антигены.
Устойчиво высокие титры антител могут отражать также персистенцию вирусной инфекции (например, вирусов герпеса, кори) или повторную стимуляцию вирусным антигеном, однако антитела к некоторым вирусам могут персистировать и без явных признаков заболевания. IgG -антитела содержатся в сыворотке крови в наиболее высокой концентрации (~12г/л), откуда они поступают в тканевую жидкость. В отличие от других иммуноглобулинов, у человека и приматов они способны проникать через плаценту и снабжать плод материнскими антителами. Период полураспада их равен 10-35 дням.
Иммуноглобулин A (IgA) является димером с 4 Fab-фрагментами. Проходя через эпителиальные клетки, IgA приобретает J-фрагмент (секреторный фрагмент), становясь секреторным slgA, который секретируется через эпителий респираторного, кишечного и урогенитального трактов. Секреторный IgA более устойчив к протеазам, чем другие иммуноглобулины, и является основным иммуноглобулином на слизистых поверхностях, в молозиве и молоке многих видов млекопитающих. Поэтому IgA-антитела играют важную роль в защите от инфекции респираторного, кишечного и урогенитального трактов. Иммунизация через слизистые при некоторых инфекциях является более эффективной, чем системное введение вакцины.
Секреторные антитела появляются на 4-7-й день после инфицирования и представлены в основном IgA, IgG и IgM. Они считаются менее специфичными, чем сывороточные. Динамика накопления антител в сыворотке крови и секретах практически одинакова.
В отличие от сывороточного IgA, большая часть которого является мономером, молекула секреторного IgA представляет собой димер. Мономерный IgA синтезируется плазматическими клетками костного мозга, периферических лимфатических узлов, селезенки и других органов. Димерные формы sIgA с соединительной j-цепью синтезируются лимфоидной тканью желудочно-кишечного, респираторного и урогенитального трактов.
Добавочный структурный компонент секреторного IgA, вероятно, функционирует как поверхностный рецептор клеток секреторного эпителия и придает устойчивость sIgA к действию протеаз. Биологическая функция sIgA состоит в основном в местной защите слизистых оболочек от инфекции. Формирование местных секреторных IgA на поверхности слизистых оболочек имеет особое значение для формирования устойчивости организма к вирусам, обычно проникающим через дыхательный, кишечный или урогенитальный эпителий. Для индукции секреторных IgA в кишечнике вирус должен вступить в контакт с лимфоидной тканью кишечника. После формирования местного ответа В-клетки памяти, образующие IgA, мигрируют в другие участки кишечника. Аналогичный механизм индукции IgA функционирует в респираторном тракте.
Система секреторного иммунитета функционирует и регулируется иначе, чем иммунная система в целом. Она может коррелировать с общей иммунной реакцией или быть независимой от нее. Кроме секреторного IgA, существенное значение для иммунитета слизистых оболочек имеют содержащиеся в секретах у человека IgM и IgG. IgM также представляет секреторный иммуноглобулин, однако он не так прочно, как sIgA, связывает секреторный компонент. В пищеварительном тракте IgM играет более важную роль, чем IgG, а в носоглотке - наоборот.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Резюме
Цель исследования. Изучение побочных эффектов и редких поствакцинальных осложнений, а также определение профилактической (количественная оценка активности) и противоэпидемической (реализация свойства вакцины предотвращать развитие эпидемии при тех или иных условиях) эффективности вакцины Инфлювак при массовом ее применении.
Заключение. Вакцина Инфлювак характеризуется высокими показателями профилактической и противоэпидемической защиты, обладает слабой реактогенностью, не вызывает необычных и побочных реакций при массовом применении.
В настоящее время для профилактики гриппа наиболее широкое применение находят инактивированные вакцины, содержащие антигены к трем штаммам вируса гриппа - A/H3N2, A/H1N1 и В.
По технологии изготовления инактивированные вакцины можно разделить на три группы: цельновирионные (обычные), расщепленные (сплит) и субъединичные.
Цельновирионные вакцины состоят из инактивированных цельных вирионов вируса гриппа и содержат, помимо необходимых для иммунизации антигенов, большое количество балласта в виде нуклеокапсида вируса. Расщепленные вакцины производятся из инактивированных расщепленных вирусов гриппа и содержат наряду с поверхностными и внутренние антигены. Субъединичные вакцины, к которым относится Инфлювак, содержат только поверхностные протективные антигены (гемагглютинин и нейраминидазу) и являются препаратами с наиболее высокой степенью очистки от компонентов вируса гриппа.
Целью настоящего исследования являлось изучение побочных эффектов и редких поствакцинальных осложнений, а также определение профилактической (количественная оценка активности) и противоэпидемической (реализация свойства вакцины предотвращать развитие эпидемии при тех или иных условиях) эффективности вакцины Инфлювак при массовом ее применении.
Материал и методы
Исследования проводили с октября по май, т.е. в период предсезонного и сезонного подъема заболеваемости гриппом и острыми респираторными заболеваниями (ОРЗ), в 1999-2000 гг.
Из отобранных для исследования участников были сформированы 3 группы: основная (иммунизированные против гриппа вакциной Инфлювак) и две контрольные, одна из которых вакцинирована против другой инфекции (1-я контрольная группа), вторая по условиям эпидемиологического опыта была оставлена невакцинированной (2-я контрольная группа). Она была образована из 622 студентов V курса, находившихся в тех же условиях, что и участники основной и 1-й контрольной групп, прошедших медицинское освидетельствование и не имевших противопоказаний к проведению вакцинации.
С целью получения статистически значимых показателей эффективности вакцины была определена численность основной и 1-й контрольной групп на основании результатов анализа заболеваемости гриппом и ОРЗ в этом коллективе за 4 последние года и с использованием следующей формулы [1]:
N = n*3,84*k(1+k)*100 / m(1-k) 2
где N - численность группы n - число наблюдаемых групп, m - ожидаемая минимальная заболеваемость, k - предполагаемый минимальный индекс эффективности, который может быть принят как существенный для данной вакцинации.
Из числа отобранных для проведения вакцинации 2532 участников методом рандомизации (единица выборки - подгруппы по 15-20 человек) были сформированы 2 равноценные группы: 1268 вакцинированных против гриппа (основная группа) и 1264 вакцинированных против другой инфекции (1-я контрольная группа). Таким образом, из отобранных для проведения исследования 2532 участников против гриппа были вакцинированы 50%.
Вакцинацию проводили в октябре-ноябре 1999 г. слепым методом (участники исследования не имели информации о том, какой вакциной они иммунизировались). Для этого вакцину Инфлювак и вакцину против другой инфекции, которые внешне не различались, вводили внутримышечно в наружную поверхность верхней трети плеча в объеме 0,5 мл однократно. При этом использовали коммерческие серии вакцины Инфлювак, изготовленные из 3 эпидемических штаммов вирусов гриппа А/Сидней/5/97 (H3N2), А/Пекин/262/95 (H1N1), В/Яманаши/166/98, подобный В/Пекин/184/93. Перед началом исследований все серии вакцины прошли контроль в Государственном научно-исследовательском институте стандартизации и контроля медицинских биологических препаратов им. Л.А. Тарасевича. Для сбора информации о возможных редких и отдаленных побочных реакциях на введение вакцины, а также данных о соматической и инфекционной заболеваемости (в том числе гриппом и ОРЗ) во всех исследуемых группах в течение 8 мес с октября по май было организовано систематическое медицинское наблюдение. С целью подтверждения клинических диагно зов была проведена выборочная серологическая расшифровка заболеваний у больных гриппом и ОРЗ. Для этого по мере обращения у заболевших гриппом или ОРЗ независимо от тяжести заболевания дважды изучали парные сыворотки: первый раз в начале заболевания и повторно - через 14-21 день. Таким образом, за весь период наблюдения двойным слепым методом (ни исследователи, ни сами больные не имели информации о том, к какой группе принадлежит тот или иной участник исследования) собраны парные сыворотки от 132 больных. Каждой паресывороток присваивался индивидуальный шифр для создания режима ослепления при изучении полученного материала в лаборатории. Эти сыворотки были исследованы в реакции торможения гемагглютинации с диагностикумами, содержащими антигены штаммов вируса гриппа A/H3N2, А/H1N1 и В. По результатам изучения сывороток, взятых в динамике, диагноз гриппа подтверждался 4-кратным и более нарастанием титров антител. После получения из лаборатории результатов изучения сывороток и их дешифровки было определено, что серологическая диагностика была выполнена у 52 лиц, вакцинированных против гриппа, и 80 невакцинированных. Кроме того; были собраны и проанализированы результаты оценки клинического течения заболевания гриппом и ОРЗ среди вакцинированных и невакцинированных участников исследования.
Для оценки эффективности вакцины Инфлювак определяли показатели (индекс и коэффициент) профилактической и противоэпидемической защиты (эффективности вакцины) по следующим формулам [1]:
K = b / a и
E = 100*(b-a) / b (%)
где К - индекс эффективности, Е - коэффициент эффективности, а - заболеваемость среди вакцинированных, b - заболеваемость среди невакцинированных.
При определении показателей профилактической эффективности вакцины в соответствии с рекомендациями ВОЗ [2] проводили сравнение показателей заболеваемости в 1-й контрольной и основной группах.
Оценку эффективности вакцинации как противоэпидемического мероприятия (противоэпидемическая эффективность) проводили путем сравнения заболеваемости во 2-й контрольной группе (группа "внешнего" контроля) и в коллективах, где одна половина вакцинирована против гриппа, а другая вакцинации против гриппа не получала (основная и 1-я контрольная группы). В данном случае проводили оценку эффективности иммунизации против гриппа при наличии в коллективе 50% иммунной прослойки. Все собранные количественные данные обрабатывали методом вариационной статистики. Достоверность различий определяли по t-критерию Стьюдента, при этом достоверно значимыми считали различия при р
Результаты и обсуждение
Рисунок. Динамика заболеваемости гриппом у иммунизированных вакциной "Инфлювак" и в контрольных группах (за период наблюдения с декабря 1999 г. по май 2000 г.)
Таким образом, полученные результаты свидетельствуют, что наличие иммунной прослойки в коллективе уменьшает вероятность заболевания гриппом невакцинированных лиц из 1-й контрольной группы.
Таблица 1. Заболеваемость гриппом и острыми респираторными заболеваниями (ОРЗ) в исследуемых группах за период сезонного подъема с ноября 1999 г. по май 2000 г.
| Группа | Число участников | Число заболевших гриппом и ОРЗ | Заболеваемость гриппом на 1000 участников (с учетом серологического подтверждения диагноза) | |
| абс. | на 1000 наблюдений | |||
| Основная (иммунизированные вакциной Инфлювак) | 1268 | 460 | 362,8+/-13,5* | 41,7+/-5,6* |
| 1-я контрольная (невакцинированные против гриппа) | 1264 | 630 | 498,4+/-14,1* | 186,9+/-10,9* |
| Всего (с 50% иммунной прослойкой) | 2532 | 1090 | 430,5+/-9,8* | 114,1+/-6,3* |
| 2-я контрольная ("внешний" контроль) | 622 | 840 | 1350,1 | 506,3+/-20,0 |
Полученные результаты также свидетельствуют, что с учетом серологического подтверждения диагноза отмечается еще более выраженная разница между показателями заболеваемости гриппом в основной группе (иммунизированные вакциной Инфлювак) (41,7 на 1000) по сравнению с 1-й и 2-й контрольными группами (186,3 и 506,3 на 1000 соответственно). Определенные по данным исследования заболеваемости гриппом в 1-й контрольной и в основной группах позволили определить показатели профилактической эффективности вакцины К и Е, которые соответственно равны 4,5 и 77,7%. Вместе с тем обращает на себя внимание, что при расчете показателей профилактической эффективности вакцины К и Е с учетом заболеваемости гриппом во 2-й контрольной группе (506,3 на 1000) и в основной группе (41,7 на 1000) они были выше и соответственно равны 12,1 и 91,8%.
В рекомендациях ВОЗ по организации испытаний профилактических препаратов отмечается, что заболеваемость гриппом в контрольной группе, живущей в одном закрытом учреждении вместе с вакцинированными, может быть меньше обычной за счет уменьшения числа больных, инфицирующих участников контрольной группы, и таким образом повлиять на естественное распространение инфекции [2]. С учетом этого обстоятельства в литературе описаны случаи определения показателей профилактической эффективности при сравнении заболеваемости вакцинированных и лиц из группы "внешнего" контроля, на которую влияние иммунной прослойки по условиям организации эпидемиологического опыта сведено к минимуму [4, 5].
Результаты исследований позволили также провести оценку эффективности иммунизации как противоэпидемического мероприятия при сравнении заболеваемости гриппом в коллективах, в которых вакцинацию не проводили (группа "внешнего", контроля), и в коллективах с 50% иммунной прослойкой за счет иммунизированных вакциной Инфлювак (см. табл. 1). При этом показатели противоэпидемической защиты К и Е в этих коллективах соответственно составили 4,4 и 77,5%.
Результаты анализа полученных материалов показывают, что практически у всех вакцинированных заболевание протекало в легкой форме, в то же время в контрольной группе регистрировали тяжелое течение и заболевания средней тяжести, при этом более чем в 70% случаев они протекали с осложнениями.
Анализ соматической и инфекционной заболеваемости за 7 мес после вакцинации (исключая грипп и ОРЗ) в группах иммунизированных вакциной Инфлювак и невакцинированных против гриппа из этого же коллектива (1-я контрольная группа) не выявил никаких особенностей ни в показателях заболеваемости по нозологическим формам, ни по общей сумме заболеваний в той или иной группе (табл. 2). Во всех случаях разница между соответствующими показателями в данных группах наблюдения оказалась статистически незначимой (р>0,05). Наряду с этим следует отметить, что при систематическом медицинском наблюдении в течение 8 мес за 1268 иммунизированными вакциной Инфлювак ни в одном случае не выявлено необычных, редко встречающихся поствакцинальных реакций.
Таблица 2. Соматическая и инфекционная заболеваемость (исключая грипп и острые респираторные заболевания) в группах вакцинированных и невакцинированных против гриппа с ноября 1999 г. по май 2000 г.
| Заболевания | Заболеваемость на 1000 участников | |
| иммунизированные вакциной Инфлювак (основная группа; n=1268) | невакцинированные против гриппа (1-я контрольная группа; n=1264) | |
| Острые воспалительные заболевания верхних дыхательных путей (кроме гриппа и ОРЗ) | 198,7+/-11,2 | 206,5+/-11,4 |
| Инфекционные | 19,7+/-3,9 | 22,2+/-4,1 |
| Кожные | 57,6+/-6,5 | 49,1+/-6,1 |
| Нервные | 5,5+/-2,1 | 6,3+/-2,2 |
| Сердечно-сосудистые | 6,3+/-2,2 | 5,5+/-2,1 |
| Желудочно-кишечные | 10,3+/-2,8 | 11,1+/-2,9 |
| Прочие | 2,4+/-1,9 | 2,4+/-1,9 |
| Всего | 300,5+/-12,8 | 303,0+/-12,9 |
Таким образом, в результате приведенных испытаний субъединичной гриппозной вакцины Инфлювак фирмы "Солвей Фарма" установлено, что она обладает слабой реактогенностью, не вызывает не обычных и побочных реакций при массовом применении. При этом вакцина Инфлювак характеризуется высокими показателями профилактической и противоэпидемической защиты (индексы и коэффициенты эффективности соответственно равны 4,5 и 77,7% и 4,4 и 77,5%). Следует отметить, что у вакцинированных грипп протекает в легкой форме без осложнений.
Результаты наших исследований подтвердили уже описанную в литературе закономерность, что при гриппозной инфекции наличие 50% иммунной прослойки в коллективе (за счет иммунизации) умень шает вероятность заболевания невакцинированных из этих коллективов по сравнению с невакцинированными лицами из группы так называемого внешнего контроля, на которую влияние иммунной прослойки по условиям эпидемиологического опыта сведено к минимуму. При сравнении уровня заболеваемости гриппом лиц из группы "внешнего" контроля и иммунизированных вакциной Инфлювак в наших исследованиях индекс и коэффициент эффективности были соответственно равны 12,1 и 91,8%.
Выводы
В результате проведенных контролируемых клинических испытаний гриппозной субъединичной вакцины Инфлювак определены параметры ее профилактической эффективности (индекс и коэффициент соответственно равны 4,5 и 77, 5%). При сравнении заболеваемости в группе иммунизированных вакциной Инфлювак и в группе "внешнего" контроля индекс и коэффициент эффективности вакцины имеют тенденцию к росту и соответственно равны 12,1 и 91,8%. Определена противоэпидемическая защита вакцинации при наличии 50% иммунной прослойки в коллективе (индекс и коэффициент соответственно равны 4,4 и 77,5%).
При гриппозной инфекции наличие 50% иммунной прослойки в коллективе (за счет иммунизации) уменьшает вероятность заболевания невакцинированных из этого коллектива.
Вакцина Инфлювак обладает слабой реактогенностью, не вызывает при массовом применении необычных и побочных реакций.
Литература:
1. Бессмертный B.C., Хейфиц Л.Б. Оценка эффективности мероприятий по профилактике инфекционных болезней. М: Медицина; 1963.
2. Поллок Т.М. Испытания профилактических препаратов, применяемых для борьбы с инфекционными болезнями. ВОЗ, Женева 1967.
3. Урбах В.Ю. Статистический анализ в биологических и медицинских исследованиях. М: Медицина; 1975.
4. Ельшина Г.А., Горбунов М.А., Шерварли В.И. и др. Оценка эффективности гриппозной тривалентной профилактической полимерсубъединичной вакцины "Гриппол". Журн микробиол 1998: 3: 40-3.
5. Ельшина Г.А., Горбунов М.А., Бектимиров Т.А. и др. Оценка реактогенности, безвредности и профилактической эффективности тривалентной профилактической полимер-субъединичной вакцины "Гриппол", при введении детям школьного возраста. Журн микробиол 2000; 2: 50-4.
Что такое иммунологическая и эпидемиологическая эффективность вакцинации? Какие показатели используются при оценке эпидемиологической эффективности вакцинации? В каких случаях при оценке эффективности вакцинации используют когортный метод и метод «с
Вакцинация относится к числу мероприятий, требующих значительных материальных затрат, поскольку предусматривает охват прививками широких слоев населения. В связи с этим важно иметь правильное представление об эффективности иммунизации. Эффективность иммунизации оценивается по трем группам критериев:
- показатели документированной привитости (охват прививками),
- показатели иммунологической или клинической эффективности,
- показатели эпидемиологической или полевой эффективности.
Сбор сведений о вакцинированности осуществляется на уровне педиатрического участка по данным журналов профилактических прививок (ф. 064-у), карт профилактических прививок (ф. 063-у), истории развития ребенка (ф. 112-у), сертификата о профилактических прививках (ф. 156-у). Эта информация передается в территориальные центры Госсанэпиднадзора, последние анализируют ее по территориям и переадресуют вышестоящим учреждениям. Оценка привитости проводится на основании изучения величины охвата прививками лиц декретированного возраста в соответствии с действующим календарем профилактических прививок, утвержденным приказом МЗ РФ № 375 от 18.12.1997 г. Нормативными показателями охвата прививками в возрастных группах детей до трех лет следует считать 95%, в старших возрастных группах — 97-98%. Опыт борьбы с оспой показал, что 80-90%-ный охват прививками недостаточен для ликвидации инфекции. Оспу удалось ликвидировать лишь тогда, когда было привито 99% населения. Это обстоятельство важно учитывать при решении задачи ликвидации других инфекций.
Среди болезней, с которыми реально можно бороться средствами активной иммунизации, видное место занимают корь, краснуха и паротит. Вакцинопрофилактика привела к существенному снижению показателей заболеваемости этими инфекциями; среди заболевших уменьшился удельный вес детей прививаемых возрастов, снизились очаговость и пораженность детских дошкольных учреждений. Особенно заметные успехи в этом плане достигнуты в ряде стран за последние два-три десятилетия, что позволило прогнозировать ликвидацию данных заболеваний. В России в последние годы отмечается рост заболеваемости этими инфекциями.
Оценка иммунологической эффективности осуществляется выборочно среди различных групп населения и прицельно в индикаторных группах населения (получающих в соответствии с возрастом прививки), а также в группах риска (детские интернаты, дома ребенка и др.). Основные требования, предъявляемые к иммунологическим исследованиям, сводятся к следующему:
- короткий промежуток времени, в течение которого исследуются все сыворотки;
- стандартность диагностических препаратов, сыворотки и диагностикумов;
- высокая чувствительность иммунологического теста для определения антител [4]. Для этого используется весь арсенал серологических исследований (РНГА, РТГА, ИФА и др.). Выбор теста для оценки иммунологической эффективности вакцины зависит от характера иммунитета при данной инфекции. Например, для столбняка, дифтерии, кори, паротита критерием эффективности вакцины является определение уровня циркулирующих антител, а для туберкулеза, туляремии и бруцеллеза — клеточные реакции, например кожные пробы замедленного типа. К сожалению, для большинства инфекций, в основе которых лежит клеточный иммунитет, защитные уровни клеточных реакций не установлены.
Изучение иммунологической эффективности вакцин проводится путем сопоставления титров специфических антител в сыворотке крови привитых до и в разные сроки после иммунизации, а также путем сравнения этих результатов с данными уровня антител, полученными в те же сроки при обследовании лиц, которым вводили плацебо или препарат сравнения. Плацебо помещают в точно такие же ампулы или флаконы, как и изучаемую вакцину. В ряде случаев целесообразно, исходя из этических соображений, использовать вместо плацебо вакцины, предназначенные для профилактики других инфекционных заболеваний. При этом схема иммунизации, дозировка и место введения препарата должны быть такими же, как и в группе испытуемых.
Иммунологическая активность вакцины может отражать ее профилактическую эффективность в том случае, если известен защитный уровень иммунологических показателей при данной инфекции. Защитный уровень антител устанавливается заранее в опытах с однонаправленным препаратом. Для каждой инфекции определяется свой защитный титр антител: для кори, паротита и гриппа он равен 1:10; для столбняка 1:20; для дифтерии 1:40 по РПГА; для коклюша 0,03 МЕ/мл; гепатита В 0,01 МЕ/мл по иммуноферментному анализу и т. д. При инфекциях, в отношении которых не установлен защитный уровень антител, приходится проводить испытания профилактической эффективности вакцин по показателям заболеваемости данной инфекцией.
Наиболее объективную оценку иммунологической эффективности вакцин можно получить при вакцинации серонегативных к специфическим антигенам людей. Из таких лиц формируют опытную и контрольную группы. Оценку иммуногенности вакцинного препарата осуществляют на основе определения разницы в числе лиц, имеющих антитела в этих двух группах. Коэффициент иммунологической эффективности определяют по следующей формуле:

, где
КЭ — коэффициент иммунологической эффективности;
А — число привитых испытуемым препаратом, у которых исследовали парные сыворотки крови;
Б — то же в контрольной группе лиц;
α — число привитых с возникшим иммунологическим сдвигом;
β — то же в контрольной группе.
Сформировать группы лиц, у которых не определялись бы антитела к широко распространенным возбудителям (грипп, гепатит А и др.), подчас бывает довольно сложно. В таких случаях нередко эффективность препаратов оценивают по нарастанию титров специфических антител до и после вакцинации как в основной, так и в контрольной группе. Иммунологические сдвиги, возникающие при вакцинации, оцениваются также по проценту сероконверсии. Вакцина считается высокоэффективной, если процент сероконверсии составляет 90% и выше. Кроме того, важное значение имеет продолжительность сохранения поствакцинального протективного иммунитета. После введения вакцины против желтой лихорадки она составляет 10-15 лет, брюшнотифозной (вакцины вианвак и Vi тифин) — 3 года, гепатита В — не менее 7-10 лет. Опубликованы результаты исследований о сохранении антител к вирусу краснухи от 9 до 21 года после прививки, причем серонегативность обнаруживалась только у 1% привитых вакциной рудивакс [9].
Для оценки и наблюдения за уровнем популяционного иммунитета проводится плановый серологический (иммунологический) контроль. Он позволяет выявить группы людей, наиболее подверженных риску заболевания, оценить степень защищенности лиц, привитых с нарушением схемы иммунизации или не имеющих документов о вакцинации, дать оценку и составить прогноз изменения эпидемиологической ситуации на конкретной территории. Отбор лиц для обследования в целях изучения иммуноструктуры осуществляется на основе кластерной выборки, рекомендованной ВОЗ. Экстренный серологический контроль проводится в очагах инфекционных заболеваний с целью выявления неиммунных лиц, которые контактировали с источником инфекции и подлежат срочной активной или пассивной иммунизации. Он также показан среди лиц с неясным прививочным анамнезом, при оценке вакцинального процесса у детей из групп риска развития поствакцинальных осложнений и привитых щадящими методами. Исследования иммунологической (клинической) эффективности вакцин могут определять, является ли вакцина иммуногенной и защищает ли она тех, кто привит. В то же время исследования относительной иммуногенности не могут определять, какая из схем вакцинации обеспечивает лучшую защиту, и результаты испытаний клинической эффективности трудно экстраполировать на условия рутинного применения вакцины в общей популяции. Таким образом, хотя исследования иммунологической эффективности вакцин необходимы, они часто не в состоянии помочь правильно оценить преимущества вакцинации.
В условиях плановой вакцинации контролируемые испытания представляются как непрактичными, так и неэтичными. Поэтому применяются обычные эпидемиологические исследования, детально описанные Оренштейном и соавт. [8]. Исследования эпидемиологической (полевой) эффективности прививки прямо отвечают на вопрос, помогает ли прививка людям. Оценка эпидемиологической эффективности предусматривает сбор информации об уровне заболеваемости, проявлениях эпидемического процесса во времени, в пространстве и среди различных групп населения. Кроме того, сопоставляются данные о заболеваемости на территории, где иммунизацию проводили, и там, где ее не проводили, при условии одинакового уровня заболеваемости на этих территориях в течение нескольких предыдущих лет.
В качестве примера можно привести программу всеобъемлющей иммунизации вакциной M-M-R II в Финляндии. Через несколько лет после начала реализации программы заболеваемость корью, краснухой и паротитом уменьшилась более чем на 90%, а к концу 12-летней программы местные случаи кори, паротита и краснухи были ликвидированы. Кроме того, заболеваемость энцефалитами у детей снизилась на треть, и прекратился рост заболеваемости диабетом I типа среди детей 5–9 лет, что также может являться результатом кампании иммунизации [14].
Основными критериями оценки эффекта массовой иммунизации служат показатели не только заболеваемости, но и смертности; изменения в характере очаговости, сезонности и цикличности, возрастной структуре болеющих, а также клиническом течении соответствующей вакцине инфекционной болезни, которые учтены за достаточно длительный период времени до и после проведения прививок. Предусматривается определение индекса эффективности, коэффициента (показателя) защищенности, коэффициента тяжести клинического течения болезни.
Коэффициент защищенности (Е) определяется по формуле:

, где
α — заболеваемость среди лиц, получивших препарат;
β — заболеваемость среди лиц, не получивших препарат.
По показателю защищенности можно определить, какой процент людей из числа получающих вакцинный препарат защищен от заболевания. Показатель защищенности может с известной долей достоверности выводиться из показателя непосредственного риска, определяемого в ходе когортного эпидемиологического исследования.
Индекс эффективности показывает, во сколько раз заболеваемость среди лиц, получивших препарат, ниже заболеваемости среди лиц, его не получивших. Он определяется по формуле.

Индекс эффективности вакцинации равен показателю относительного риска.
Следует также отметить, что вакцинация представляет собой весьма результативное в экономическом плане мероприятие. Согласно данным специалистов Центра по контролю за инфекционными болезнями (США, Атланта), 1 долл., вложенный в вакцинации против кори, дает прибыль, равную 11,9 долл. Прибыль при иммунизации против полиомиелита равна 10,3 долл., паротита - 6,7 долл. Известно, что на 1 долл., вложенный сегодня в вакцинацию против краснухи, приходится 7,7 долл., которые сейчас тратятся на борьбу с этим заболеванием. Экономический эффект удваивается, если используется тривакцина (корь-краснуха-паротит). Иммунопрофилактика коклюша и инфекций, вызываемых гемофильной палочкой, приносит прибыль, соответственно равную 2,1-3,1 и 3,8 долл. На ликвидацию оспы было затрачено 313 млн. долл., величина предотвращенного ущерба ежегодно составляет 1-2 млрд. долл. Ни одна отрасль народного хозяйства не дает такой впечатляющей отдачи. Все затраты на мероприятия, проведенные под эгидой ВОЗ по ликвидации оспы, окупились в течение одного месяца после провозглашения ее ликвидации.
Литература
Вакцины. Виды антигенов вакцин. Классификация вакцин. Виды вакцин. Живые вакцины. Ослабленные ( аттенуированные ) вакцины. Дивергентные вакцины.
Вакцины — иммунобиологические препараты, предназначенные для активной иммунопрофилактики, то есть для создания активной специфической невосприимчивости организма к конкретному возбудителю. Вакцинация признана ВОЗ идеальным методом профилактики инфекционных заболеваний человека. Высокая эффективность, простота, возможность широкого охвата вакцинируемых лиц с целью массового предупреждения заболевания вывели активную иммунопрофилактику в большинстве стран мира в разряд государственных приоритетов. Комплекс мероприятий по вакцинации включает отбор лиц, подлежащих вакцинации, выбор вакцинного препарата и определение схемы его использования, а также (при необходимости) контроль эффективности, купирование возможных патологических реакций и осложнений. В качестве Аг в вакцинных препаратах выступают:
• цельные микробные тела (живые или убитые);
• отдельные Аг микроорганизмов (наиболее часто протективные Аг);
• токсины микроорганизмов;
• искусственно созданные Аг микроорганизмов;
• Аг, полученные методами генной инженерии.
Большинство вакцин разделяют на живые, инактивированные (убитые, неживые), молекулярные (анатоксины) генно инженерные и химические; по наличию полного или неполного набора Аг — на корпускулярные и компонентные, а по способности вырабатывать невосприимчивость к одному или нескольким возбудителям — на моно- и ассоциированные.
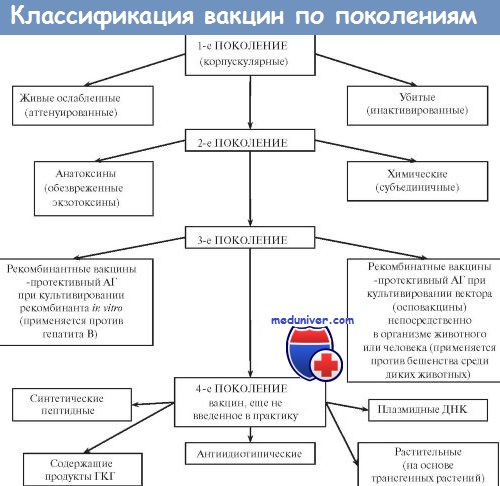
Живые вакцины
Живые вакцины — препараты из аттенуированных (ослабленных) либо генетически изменённых патогенных микроорганизмов, а также близкородственных микробов, способных индуцировать невосприимчивость к патогенному виду (в последнем случае речь идёт о так называемых дивергентных вакцинах). Поскольку все живые вакцины содержат микробные тела, то их относят к группе корпускулярных вакцинных препаратов.
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство живых вакцин— полностью сохранённый набор Аг возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Живые вакцины обладают и рядом недостатков. Наиболее характерный — риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма. Подобные явления более типичны для противовирусных вакцин (например, живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Ослабленные ( аттенуированные ) вакцины
Ослабленные (аттенуированные) вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение вакцинного штамма в организм имитирует инфекционный процесс: микроорганизм размножается, вызывая развитие иммунных реакций. Наиболее известны вакцины для профилактики сибирской язвы, бруцеллёза, Ку-лихорадки, брюшного тифа. Однако большая часть живых вакцин — противовирусные. Наиболее известны вакцина против возбудителя жёлтой лихорадки, противополи-омиелитная вакцина Сэйбина, вакцины против гриппа, кори, краснухи, паротита и аденовирусных инфекций.
Дивергентные вакцины
В качестве вакцинных штаммов используют микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных болезней. Аг таких микроорганизмов индуцируют иммунный ответ, перекрёстно направленный на Аг возбудителя. Наиболее известны и длительно применяются вакцина против натуральной оспы (из вируса коровьей оспы) и БЦЖ для профилактики туберкулёза (из микобактерий бычьего туберкулёза).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

