Искусственный вирус на неврологическую симптоматику
Обновлено: 17.04.2024
Лечение цитомегаловирусной инфекции нервной системы. Вирус простого герпеса и нервная система.
В настоящее время используются два вирусостатических препарата для подавления активной ЦМВИ при СПИДе. Оба препарата относятся к вирусостатинам. Некоторые авторы предлагают комбинированную терапию больных с ЦМВ-поражением ЦНС.
Фоскарнет обладает лучшей способностью к проникновению в ЦСЖ, чем ганцикловир. Кроме действия на ЦМВ, он обладает умеренной антиретровирусной активностью. Начальная доза препарата составляет 90 мг/кг внутривенно и назначается пациентам с нормальной функцией почек в течение 14—21 дня. Затем рекомендован переход на поддерживающую терапию со снижением дозы до 90—120 мг/сут. Введение препарата облегчается при установке постоянного подключичного катетера. Больным, страдающим почечной недостаточностью, назначаются более низкие дозы. Кроме токсического поражения почек, выделяют следующие побочные эффекты фоскарнета: дисфункция желудочно-кишечного тракта, нарушения электролитного баланса, головные боли, парестезии, припадки и токсическая энцефалопатия. Иногда бывает трудно отличить побочные эффекты фоскарнета от проявлений собственно ЦМВ-инфекции.
Ганцикловир также эффективен для лечения ЦМВ-поражения нервной системы у больных СПИДом. Лучше всего лечению данным препаратом поддаются ЦМВ-ПРМ и мультифокальная нейропатия. Начальная доза препарата составляет 5 мг/кг внутривенно в течение 14—21 дня. Затем рекомендован переход на поддерживающую дозу 5 мг/кг/сут. Подавление кроветворной функции, в частности нейтропения, нередко отмечается при лечении ганцикловиром, особенно если одновременно больной получает антиретровирусные средства. Их дозу необходимо снизить. К другим побочным эффектам ганцикловира относятся токсическое поражение печени, желудочно-кишечные расстройства, головные боли, припадки, сонливость, парестезии, токсическая энцефалопатия и токсическое поражение почек. Так же, как и при лечении фоскарнетом, зачастую бывает трудно отличить побочные эффекты препарата от проявлений ЦМВ-инфекции. с. Вирусная резистентность может развиться при длительном лечении ганциковиром или фоскарнетом. При начальной ударной терапии ЦМВ-ретинита или энтерита могут появиться неврологические симптомы. Для их лечения рекомендуется назначение альтернативного средства.
Когда и ганцикловир, и фоскарнет утрачивают эффективность, можно попробовать их комбинацию.
Ожидаемый результат лечения цитомегаловирусной инфекции нервной системы. Проспективных исследований по определению эффективности лечения ЦМВ-поражениий нервной системы при СПИДе не проводилось. Известны только единичные описания улучшения на фоне лечения ЦМВ-ПРМ и мультифокальной нейропатии. Очень мало данных о реакции на лечение ЦМВЭ. Больные, получившие ударную терапию, должны быть переведены на поддерживающий режим, хотя до сих пор неясно, какие дозы препаратов целесообразны. Исследование ЦСЖ дает наиболее надежные критерии активности процесса, поэтому его следует проводить сразу после окончания ударной терапии, а также при прогрессировании неврологических симптомов на фоне поддерживающей терапии. Повторное воспаление и, возможно, неоднократное выявление вирусной ДНК в ЦСЖ методом ПЦР свидетельствует об активной репликации вируса и указывают на резистентность к выбранному режиму лечения.
Вирус простого герпеса и нервная система.
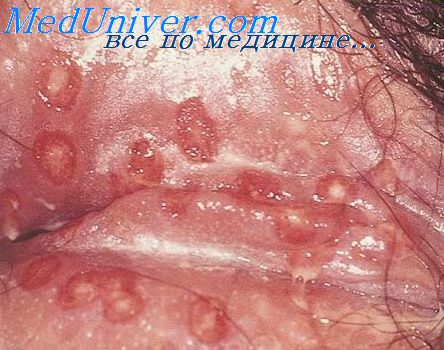
1. Течение инфекции вируса простого герпеса. ВПГ распространен повсеместно общей популяции, и у ВИЧ-инфицированных часто наблюдается инфекция, вызванная ВПГ-2 ректально-генитального типа. Многие случаи ВПГ-2-асептического менингита имеют самоограничивающийся характер, но менингорадикулит, энцефалит или миелит могут давать тяжелые проявления, требующие лечения. У ВИЧ-инфицированных описан также энцефалит, вызванный ВПГ-1, с подострым течением и атипичной клинической картиной, обусловленной глубоким иммунодефицитом.
2. Клиническая картина инфекции вируса простого герпеса. ВПГ-1 вызывает фокальный энцефалит с преимущественным поражением глубоких отделов лобных и височных долей. Клиническими признаками заболевания являются припадки, головные боли, изменения личности и нарушения речи. В течение нескольких дней может развиться спутанность сознания, ступор и кома. У некоторых больных СПИДом не наблюдается такого выраженного прогрессирования. ВПГ-2 вызывает асептический менингит с лихорадкой и головными болями; менингорадикулит с частым вовлечением крестцовых корешков, что служит причиной задержки мочи; менингоэнцефалит. У больных с менингомиелитом отмечается прогрессирующая слабость, спастичность, нарушения чувствительности и атаксия, преимущественно в нижних конечностях, а также нарушение тазовых функций. У больных с ВПГ-2-менингоэнцефалитом наблюдаются спутанность сознания, припадки, головные боли и двигательные нарушения различной степени тяжести. Признаки ВПГ-2-поражения нервной системы могут появиться непосредственно после высыпаний в анально-генитальной области или независимо от них.
3. Диагностика инфекции вируса простого герпеса. Диагноз ВПГ-энцефалита можно предположить при обнаружении ограниченных очагов в нижних отделах лобных или височных долей по данным МРТ-исследования с контрастом. На ЭЭГ регистрируются типичные периодические спайковые разряды. Характерных признаков ВПГ-1 энцефалита другой локализации не существует. В ЦСЖ обычно обнаруживается смешанный плеоцитоз, иногда — эритроциты, чуть сниженный или нормальный уровень глюкозы и повышенное содержание белка. Исследования в культуре редко выявляет наличие вируса. Разработан ПЦР-метод, позволяющий фиксировать вирусную ДНК в ЦСЖ.
4. Лечение инфекции вируса простого герпеса
Ацикловир — вирусостатический препарат, эффективный при герпетических инфекциях. Препарат активизирует тимидинкиназу, которая замедляет репликацию вируса. Ацикловир в дозе 10 мг/кг внутривенно назначают сразу же при подозрении на ВПГ-поражение ЦНС, не дожидаясь результатов диагностических исследований. В подтвержденных случаях лечение рекомендовано продолжать в течение 10—14 дней. После этого иногда назначается поддерживающая терапия повторной аногенитальной инфекции в дозе 200 мг внутрь 5 раз в сутки. К сожалению, появились резистентные штаммы вируса. Таким больным показано лечение фоскарнетом в дозе 60 мг/кг 2 раза в сутки в течение 14-21 дня.
К побочным эффектам ацикловира относятся токсическое поражение почек, печени, желудочно-кишечные расстройства и раздражение в области введения препарата. У больных, страдающих почечной недостаточностью, доза ацикловира должна быть снижена.
Если при лечении у пациента появились головные боли, головокружение и другие серьезные признаки токсического воздействия препарата, включая токсический делирий, спутанность сознания, припадки, необходимо определить уровень препарата в крови и при его высоких показателях откорректировать дозу. Описаны случаи подавления костномозгового кроветворения и артериальная гипотензия при лечении ацикловиром.
5. Ожидаемый результат лечения вируса простого герпеса. Клинические испытания, оценивающие течение ВПГ-энцефалита и других герпетических поражений нервной системы при СПИДе, немногочисленны. У многих пациентов лечение ацикловиром эффективно. У некоторых больных эффект отсутствует, что связано либо с вирусной резистентностью, либо с нарушением функции иммунной системы. Серийные исследования ЦСЖ считаются наиболее надежным методом подтверждения резистентности и должны проводиться после окончания антивирусной терапии, а также в случае прогрессирования неврологических симптомов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Нейроковид – это неофициальное название поражений центральной и периферической нервной системы при COVID-19. Состояние вызвано как прямым повреждающим действием коронавируса, так и опосредованными системными нарушениями работы организма. Патология имеет полиморфные проявления: астенический синдром, психоэмоциональные нарушения, когнитивный дефицит. Тяжелые формы нейроковида характеризуются расстройствами церебрального кровообращения. Диагностика требует проведения нейровизуализации (КТ, МРТ), ЭЭГ, УЗДГ сосудов головы и шеи. Для лечения неврологических последствий COVID-19 используют методы фармакотерапии, физиотерапии, психотерапии, коррекцию образа жизни.
МКБ-10



Общие сведения
По данным зарубежных исследований, с неврологическими последствиями новой коронавирусной инфекции сталкиваются 49% пациентов в США, 50% в Великобритании, 35-45% в Германии. В среднем более трети больных, перенесших COVID-19, предъявляют жалобы, типичные для поражения головного мозга и периферических нервов. Ситуация осложняется тем, что симптоматика накладывается на другие проявления острого периода коронавируса и постковидного синдрома. Неврологические аспекты коронавирусной пандемии требуют дальнейшего изучения и подбора оптимальных схем медицинской помощи, включая длительную реабилитацию.

Причины нейроковида
Поражение нервной системы возникает при любой клинической форме COVID-19, в том числе при бессимптомном или малосимптомном течении. Поскольку повреждение ЦНС и периферических нервных структур не всегда имеет непосредственную связь с коронавирусной болезнью, требуются дальнейшие масштабные исследования и метаанализы. При этом установление точных причинно-следственных связей затруднительно, особенно у пациентов с сопутствующими заболеваниями.
Предрасполагающие факторы
Важный фактор риска позднего нейроковида – длительное и массивное медикаментозное лечение. Применение высоких доз системных кортикостероидов, моноклональных антител и сосудистых препаратов негативно влияет на церебральный кровоток. Ситуация ухудшается при полипрагмазии и у пациентов с коморбидными состояниями, требующими поддерживающей терапии. Прослеживается тенденция к увеличению частоты и тяжести нейроковида среди пожилых больных.
Патогенез
Последние исследования показывают, что SARS-CoV-2 способен преодолевать гематоэнцефалический барьер (ГЭБ). Это реализуется по трем основным механизмам. Во-первых, вирус взаимодействует с рецепторами ангиотензинпревращающего фермента, которые активно экспрессируются на эндотелии церебральных сосудов. Во-вторых, вирусный протеин S напрямую повреждает ГЭБ. В-третьих, возбудитель активизирует сосудистую воспалительную реакцию и нарушает микроциркуляцию.
Инфекция SARS-CoV-2 вызывает прямое повреждение нервных клеток. Вирусный геном встраивается в митохондриальный матрикс нейронов, после чего активизируется репликация возбудителя. В инфицированных клетках развивается окислительный стресс, активизируется приток ионов кальция и нарастает дисфункция митохондрий. Такие изменения результируют некрозом или апоптозом нейронов в разных участках головного мозга.

Симптомы нейроковида
Головная боль – самое распространенное неврологическое проявление коронавирусной инфекции, которое возникает у большинства больных в остром периоде и беспокоит более 13% пациентов во время постковида. Симптом зачастую сопровождается головокружением, мышечными болями, повышенной утомляемостью. Аносмия и дисгевзия возникают у 85-88% людей в начальном периоде болезни, в 10% случаев сохраняются более 6 месяцев после перенесенного COVID-19.
Серьезную проблему представляет астенический синдром при нейроковиде, который проявляется снижением работоспособности, быстрой утомляемостью после незначительных нагрузок, отсутствием бодрости даже после длительного отдыха. Ситуация усугубляется когнитивными нарушениями: ухудшением краткосрочной и долгосрочной памяти, снижением концентрации внимания, расстройствами мышления.
Неврологические осложнения коронавирусной инфекции включают нарушения работы вегетативной нервной системы, контролирующей деятельность внутренних органов. Характерны колебания артериального давления и пульса, особенно при вертикализации и физических нагрузках. Возникают ортостатические и рефлекторные обмороки, несистемное головокружение. Развивается постуральная гипоксемия, которая проявляется одышкой при вставании с постели.
Осложнения
У пожилых людей и пациентов с другими факторами риска возможно развитие цереброваскулярных последствий: ишемического инсульта, тромбоза венозного синуса, кровоизлияния в ткани головного мозга. Риск развития инсульта в остром периоде коронавирусной инфекции варьирует от 2,8% до 8,7%. Смертность при ОНМК в группе пациентов с COVID-19 в 5-6 раз выше, чем в среднем в популяции.
В периоде нейроковида возможен дебют аутоиммунных полирадикулоневропатий (синдромов Гийена-Барре и Миллера-Фишера), лейкоэнцефалопатии, рассеянного склероза. К тяжелым осложнениям относят менингоэнцефалит, острую некротизирующую энцефалопатию. Около 50% людей с гипертермией и снижением сатурации имеют признаки энцефалопатии: атаксию, спутанность сознания, психические симптомы.
Диагностика
Обследование больных с острыми проявлениями нейроковида требует участия невролога, инфекциониста, врачей-реаниматологов. При хронических последствиях COVID-19 пациенты проходят диагностику и терапию в неврологическом отделении. Важную роль играет сбор жалоб, выяснение инфекционного и эпидемиологического анамнеза, статуса вакцинации против коронавирусной инфекции. Полная диагностическая программа включает следующие методы:
- Осмотр у невролога. Оценка неврологического статуса – базовый метод исследования при нейроковиде. При физикальном исследовании определяют уровень сознания, сохранность поверхностной и глубокой чувствительности, состояние моторных и высших психических функций. По показаниям диагностику дополняют консультацией психиатра.
- МРТ головного мозга. На снимках обнаруживаются мультифокальные очаги поражения в белом веществе, признаки точечных кровоизлияний. При острых нарушениях мозгового кровообращения в 80-90% случаев видны участки гиперинтенсивности, которые появляются в первые часы и позволяют быстро провести дифференциальную диагностику.
- Ультразвуковая допплерография. Исследование быстро выявляет нарушения кровотока в экстра- и интракраниальных сосудах, указывает на локализацию и протяженность патологических изменений. УЗДГ также показывает параметры венозного оттока, состояние коллатерального кровообращения, наличие артериовенозных мальформаций.
- ЭЭГ. Исследование электрической активности головного мозга проводится при когнитивных нарушениях, судорожных пароксизмах, инсомнии. По форме и соотношению разных типов волн удается судить о функциональном состоянии нервных структур, определить локализацию и степень патологических изменений.
- Лабораторная диагностика. Анализы клеточного и биохимического состава крови необходимы для оценки общего состояния здоровья. Дополнительно проводится исследование острофазовых показателей, аутоиммунных маркеров. При сохраняющейся одышке требуется анализ газов крови.
Основная задача дифференциальной диагностики – разграничить проявления нейроковида и неврологические проблемы, возникающие по другим причинам. Для этого пациенты проходят полную лабораторную диагностику с ПЦР-исследованием, анализом на антитела классов M и G. Также больным требуется консультация кардиолога, пульмонолога, иммунолога, чтобы исключить прочие проявления постковидного синдрома.

Лечение нейроковида
Терапевтическая программа подбирается с учетом нозологической формы нейроковида, тяжести состояния больного и наличия сопутствующих заболеваний. При критических неврологических осложнениях лечение проводится в реанимационном или неврологическом стационаре. Хронические симптомы требуют длительной амбулаторной терапии с последующей нейрореабилитацией.
Медикаментозное лечение нейроковида включает вазоактивные препараты, нейропротекторы и ноотропы, витаминные комплексы. Для стабилизации психического состояния используются седативные средства, антидепрессанты и легкие транквилизаторы. При ОНМК необходима тромболитическая, антикоагулянтная и антиагрегантная терапия. Манифестация аутоиммунных процессов требует приема стероидных гормонов и иммуносупрессоров.
Для восстановления здоровья большую роль играют немедикаментозные методы: изменение образа жизни, постепенное расширение физической активности, сбалансированное и витаминизированное питание. После улучшения самочувствия рекомендовано санаторно-курортное лечение, талассотерапия, спелеотерапия и бальнеотерапия. Пациентам оказывают помощь на сеансах индивидуальной и групповой психотерапии, применяют методы арт-терапии, музыкотерапии.
Прогноз и профилактика
При проведении комплексной терапевтической программы удается полностью восстановить неврологические функции у большинства пациентов. Однако выздоровление и реабилитация требуют времени: у 20% людей патологические симптомы сохраняются более 5 недель, у 10% – дольше 3 месяцев. Менее благоприятный прогноз при развитии ишемического или геморрагического инсульта при нейроковиде, после чего остаются резидуальные неврологические изменения.
Основу профилактики нейроковида составляют противоэпидемические меры, направленные на борьбу с распространением COVID-19. При отсутствии противопоказаний настоятельно рекомендовано пройти полный курс вакцинации против SARS-CoV-2, что является самой надежной защитой от заражения и развития тяжелых осложнений. Также важны неспецифические меры: физическое дистанцирование, ношение средств индивидуальной защиты, ограничение социальных контактов.
1. Неврологические последствия COVID-19 у пожилых/ А.Ю. Никитина, А.Ш. Чимагомедова, О.С. Левин// Журнал неврологии и психиатрии им С.С. Корсакова. – 2021. – №10.
2. Неврологические нарушение у пациентов с long COVID синдромом и методы клеточной терапии для их коррекции: обзор литературы/ И.С. Долгополов, Г.Л. Менткевич, М.Ю. Рыков, Л.В. Чичановская// Сеченовский вестник. – 2021. – №3.
3. Неврологические аспекты COVID-19. Тактика ведения пациентов неврологом с учетом эпидемиологической ситуации/ Демьяновская Е. Г., Крыжановский С. М., Васильев А. С., Шмырев В. И.// Лечащий врач. – 2021. – №2.
4. Неврологические проявления и осложнения у пациентов с COVID-19/ И.К. Терновых, М.П. Топузова, А.Д. Чайковская, П.Ш. Исабекова, Т.М. Алексеева// Трансляционная медицина. – 2020. – №7.
Особенности вирусной инфекции нервной системы у детей в зависимости от возбудителя
а) Паралитический полиомиелит. С широким распространением вакцинации случаи полиомиелита стали крайне редкими, и повсеместное уничтожение вируса остается приоритетной задачей ВОЗ. Около 90-95% инфекций полиовируса являются субклиническими, 5% проявляются в виде легкой формы заболевания с фебрилитетом и 1-2% в основном дают симптоматику поражения ЦНС либо менингоэнцефалита, либо полиомиелита.
При полиомиелите в патологический процесс вовлекаются клетки передних рогов, двигательные и чувствительные черепные ядра продолговатого мозга, ретикулярная формация, червь мозжечка и в меньшей степени, таламус и III и V слои моторной зоны коры. Нейроны подвергаются дегенеративным изменениям, сопровождающимся вначале полиморфноядерной реакцией, которая позднее становится мононуклеарной.
Клинические проявления возникают после инкубационного периода, который длится 3-35 дней. Первоначальные симптомы включают головную боль, тошноту и лихорадку, а вслед за ними в течение 2-5 дней менингеальные симптомы раздражения и сильную боль в нижней части спины и конечностях. В серьезных случаях паралич появляется в течение первых двух дней.
Обычный спинальный полиомиелит характеризуется асимметричным вялым параличом, затрагивающим ноги, руки и/или туловище с отсутствием сухожильных рефлексов. Задержку мочи при начале заболевания демонстрируют 20-30% пациентов. Бульбарная форма редко бывает изолированной, распространяясь по меньшей мере на шейный отдел спинного мозга в 90% случаев. Могут поражаться все мышцы, иннервируемые черепными нервами. Кроме того, дыхательная недостаточность и гипертензия может быть результатом повреждения стволовой ретикулярной субстанции. Заболевание может сопровождаться энцефалитическими признаками, но они могут также вызываться и дыхательной недостаточностью из-за паралича диафрагмальных и межреберных мышц.
В анализе СМЖ обнаруживают 30-200 клеток/мм3. Изначально преобладают полиморфноядерные клетки, затем через 5-7 дней сменяющиеся лимфоцитарным плеоцитозом. Содержание белка повышается поздно, достигая максимальных значений примерно на 25 день заболевания.
По данным МРТ описано развитие отека спинного мозга с патологическим сигналом от центральной его части (Kibeetal., 1996). До начала клиники вирус может выделяться из кала и ротоглотки первые 19 дней и до трех месяцев после первых клинических проявлений (в среднем пять недель). При типировании вируса определяют один из трех типов полиовируса. Серологический диагноз ставится на основании повышения титра нейтрализующих или комплемент-связывающих антител.
Прогноз паралитического полиомиелита зависит от степени вовлечения. Восстановление поврежденных мышц часто происходит в течение года и более, но если через месяц мышцы все еще остаются парализованными, то обычно окончательно. Прогрессирующая болезнь моторных нейронов (постполиомиелитный синдром), напоминающий амиотрофический склероз, иногда наблюдается у взрослых через 20 и более лет после острого начала заболевания (Dalakas et al., 1986).
Случаи паралитического полиомиелита, связанного с живой вакциной, могут встречаться у пациентов с иммунодефицитом, получивших вакцину или контактировавших с вирусом (Nkowane et al., 1987; Sen et al., 1989; Groom et al., 1994). При этом возможны атипичные проявления. Поскольку редкие случаи полиомиелита могут также возникать у детей без иммунодефицита после живой вакцины (Dussaix et al., 1987), с уменьшением уровня заболеваемости во всем мире, в большинстве развитых стран сейчас используют убитую инъекционную полиовакцину при плановой вакцинации для предупреждения этого осложнения.
Постановка диагноза не представляет трудностей при условии, если не упускать из вида именно это заболевание. Синдром Гийена-Барре отличается от полиомиелита по характеру начала, симметричности распределения слабости и по данным ликвора. Регистрировались редкие случаи паралитического заболевания, связанного с другими вирусами (Kylleman et al., 1993). Вирус Западного Нила вызывал эпидемии заболеваний, напоминающих паралитический полиомиелит.
Случаи интоксикации химикатами или укусов насекомыми также могут имитировать сходную клиническую картину (Gear, 1984).

б) Энтеровирусы. Первоначальная классификация энтеровирусов, до геномного анализа, была основана на цитопатическом эффекте различных культивируемых клеток и инфицированных животных. Были выделены три типа полиовирусов, 24 коксаки-вируса типа А и 6 коксаки-вирусов типа В вирусов и 34 типа ЕСНО-вирусов. Последующие выделенные энтеровирусы обозначались номером, начиная от энтеровируса 68 без дальнейшего подразделения. Позднее геномный анализ последовательности частично подтвердил первоначальную культуральную классификацию.
Эти вирусы внедряются в организм хозяина через желудочно-кишечный тракт, где реплицируются и вызывают виремию, способную привести к инфекции ЦНС. В большинстве случаев отмечается слабый желудочно-кишечный вирусный продром, а в анамнезе присутствуют данные о наличии у членов семьи схожих симптомов. Большая часть случаев протекает в легкой форме с быстрым выздоровлением. Микроорганизмы можно обнаружить с помощью ПЦР или выделить из ликвора, а также из крови, кала и ротоглотки. При экспресс-диагностике ПЦР результаты можно получить через несколько часов. Инфекция встречается в любом возрасте, включая первые недели жизни (Kaplan et al., 1983).
Энтеровирусы Коксаки В1-5 и Коксаки А7, 9 и 25, ЕСНО-вирусы 4,6,9,11,14,16,18,20 и 30, так же как полиовирусы обычно вызывают асептический менингит. Острый эпидемический конъюнктивит, связанный с энтеровирусом 70, может осложняться менингитом, параличом черепных нервов или поражением конечностей, изолированно или совместно. Характерны сильные боли и фасцикуляции (Wadia et al., 1983; Chopra et al., 1986).
Менингит, вызванный вирусом Коксаки группы А, может сопутствовать или предшествовать герпангине, респираторным инфекциям и паротиту. Среди заболеваний группы В могут встречаться плевродиния (болезнь Борнхольма или эпидемическая миалгия) или диарея. Осложнением менингита могут быть миокардит и энцефалит, особенно у детей раннего возраста (Kaplan et al., 1983). Инфекции ЕСНО-вирусов могут вызывать как спорадические случаи, так и эпидемии. Пятнистопапулезная сыпь особенно характерна при инфекциях вирусов ECHO 4, 9 и 16. Иногда сыпь появляется при Коксаки А9 и А23. Также может быть петехиальной.
В литературе сообщалось о последствиях энтеровирусных менингитов (Kaplan et al., 1983). Вероятней всего, они являются результатом развития энцефалита, сопутствующего менингиту. Они особенно характерны при неонатальном энтеровирусном менингите, который также представлен лихорадкой, плохим аппетитом, диареей, гепатомегалией и сыпью (Huang et al., 2003).
Энтеровирусы также могут быть причиной других проявлений заболеваний ЦНС, включая паралич нижних двигательных нейронов (вирус Коксаки А4, 7, 9, В5, вирус ECHO 70); синдром Гийена-Барре и поперечный миелит (Коксаки А9, В1, 4, ECHO 6, 70); церебральную атаксию (Коксаки А9, 4, 7, В3, 4, ECHO 6, 9, 71); периферический неврит (ECHO 9). Энтеровирусы обычно вызывают самопроходящие заболевания, которые, хотя и связаны с заболеваемостью, редко заканчиваются смертельным исходом. Однако в некоторых более уязвимых группах пациентов (например, у младенцев или детей с иммунодефицитом) энтеровирусы могут вызывать угрожающие жизни инфекции.
Плеконарил — антивирусный препарат, который встраивается в капсид пикорнавирусов, включая энтеровирусы, предупреждая прикрепление вирусов к клеточным рецепторам и высвобождение вирусной РНК в клетку. Клинические испытания плеконарила показали некоторую эффективность у пациентов с тяжелой формой заболевания (Rotbart и Webster, 2001); к сожалению, этот лекарственный препарат не выпускался в промышленном масштабе.
в) Вирус эпидемического паротита. Среди неиммунизированного населения свинка выявляется как наиболее частая причина вирусного асептического менингита. Классическая клиническая картина лептоменингита встречается у 0,5-2% пациентов, больных эпидемическим паротитом. Однако плеоцитоз наблюдался только у 56% таких пациентов с паротитом (Russell и Donald, 1958). Паротит в 30-40% случаев может отсутствовать (Levitt et al, 1970), и в таких случаях диагноз можно получить при ПЦР амплификации вирусного генома в СМЖ или серологическими методами. Симптомы менингита появляются с 8 по 20 день после начала паротита. Часто сопровождаются выраженной лихорадкой.
В ликворе наблюдается лимфоцитарный плеоцитоз, нередко значительный, с сотнями клеток/мм 3 . Содержание глюкозы может быть снижено (Wilfert, 1969). Хотя заболевание обычно протекает в легкой форме, плеоцитоз может присутствовать на протяжении нескольких месяцев с длительным сохранением специфических интратекальных олигоклональных IgG (Vandvik et al., 1978a).

г) Вирусы герпеса. Некоторые представители семейства герпесвирусов могут вызывать лимфоцитарный менингит.
• Вирус простого герпеса. ВПГ 2 типа (Nahmias et al., 1982) чаще отвечающий за болезнь, чем 1 тип, который главным образом вызывает энцефалит. Менингит, вызванный ВПГ-2, может быть проявлением первичной инфекции у сексуально активных подростков. Иногда, легкие случаи ВПГ-1 инфекции могут проявляться только в виде раздражения мозговых оболочек (Whitley et al„ 1982а) с выздоровлением пациентов через 7-14 дней.
• Вирус опоясывающего герпеса. Вирус может вызывать асептический менингит, а также более сложное поражение ЦНС, описанное в следующем разделе. Могут встречаться пре-эруптивные неврологические проявления (Tsolia et al., 1995). В этом исследовании, у двоих детей с энцефалитом сопутствующей патологией была атаксия. Другие очаговые неврологические дефициты, кроме атаксии, развились у семи детей: у троих паралич лицевого нерва, у одного сопровождающая гемиплегия, двое имели парез верхних конечностей, у одного был радикулит, перешедший в парез ноги, и у одного ребенка паралич отводящего нерва. У двоих детей наблюдался изолированный менингит. В этой группе только двое детей переживали длительные последствия: у одного наблюдался стойкий паралич руки, у другого паралич отводящего нерва.
Другие синдромы ЦНС, связанные с вирусом ветряной оспы, включают вирусный миозит, радикулопатию, миелит и отсроченный гемипарез после ветряной оспы (Kamholz и Tremblay, 1985; Ichiyama et al., 1990; Rosenfeld et al., 1993; Herrold и Hahn, 1994; Gilden, 2004; Mariotti et al., 2006). Сообщалось также о поражении базальных ганглиев (Silverstein и Brunberg, 1995) и латеральном медуллярном синдроме (Kovacs et al., 1993). Сосудистые явления ишемического характера, часто поражающие крупные мозговые артерии, нередко отмечаются после ветряной оспы (Amlie-Lefond et al., 1995; Tsolia et al., 1995; Lanthier et al., 2005; Losurdo et al., 2006).
Острые артериопатии, приводящие к ишемическим инсультам, могут быть причиной четверти случаев тромбоза мозговых артерий в детском возрасте; в исследовании Guillot et al. (2005) наиболее вероятным этиологическим фактором в 60% случаев определена ветряная оспа (Guillot et al., 2005). Вероятно, при постинфекционных состояниях действует несколько механизмов, а в некоторых случаях важны воспалительные процессы в стенке артерий, так же как повышенная секреция прокоагулянтов, таких как антикардиолипин (Kurugol et al., 2000, 2001).
Кроме того, иммунная реакция хозяина на вирус ветряной оспы включает образование антител, способные на перекрестную реакцию и инактивацию белка S, важного фактора антикоагуляции хозяина. Это может привести к состоянию гиперкоагуляции и развитию молниеносной пурпуры, также как к ишемическому инсульту после Varicella zoster (Josephson et al., 2001).
• Вирус Эпштейна-Барр (ЭБВ). Большинство инфекций ЭБВ в раннем периоде жизни протекает бессимптомно, неврологические осложнения редки; они могут включать в себя асептический менингит, проявления энцефалита и некоторые другие осложнения ЦНС (Hung et al., 2000). Менингит может предвещать некоторые другие неврологические осложнения, такие как инфекционный полиневрит (синдром Гийена-Барре), энцефаломиелит или поражение черепных нервов (Hausler et al., 2002) или паркинсонизм (Hsieh et al., 2002). Примерно у трети пациентов с инфекционным мононуклеозом при исследовании СМЖ обнаруживают >5 клеток/мм 3 и такие показатели могут сохраняться месяцами, часто после полного клинического выздоровления (Pejme, 1964). Полное выздоровление может откладываться на несколько недель и месяцев.
• Вирус герпеса человека (ВГЧ) 6 и 7. ВГЧ-6 инфекция является причиной внезапной экзантемы (exanthema subitum), и в редких случаях вызывает менингоэнцефалит у здоровых прежде детей (Asano et al., 1992; Jones et al., 1994). Хотя большинство первичных инфекций ВПГ-6 (и тесно связанного ВПГ-7) протекают бессимптомно, оба вируса причастны к более 30% фебрильных судорог, встречающихся в первые два года жизни (Hall et al., 1994; Barone et al., 1995; Ward, 2005).
г) Аденовирусные инфекции нервной системы. Выделено множество типов аденовирусов; большинство вызывает легкие инфекции желудочно-кишечного тракта, дыхательной системы или почек и только в редких случаях они являются причиной синдромов поражения ЦНС. Проявления включают асептический менингит, миелит, подострый очаговый энцефалит, Рейе-подобный синдром и преходящую энцефалопатию (Linssen et al., 1991; Straussberg et al., 2001).
д) Парвовирус В19. Большинство инфекций парвовируса В19 имеют бессимптомное течение, но симптоматическая инфекция у детей обычно проявляется в виде лихорадки и сыпи, а у взрослых могут быть артропатии. Также сообщалось о редких случаях ЦНС инфекции с признаками менингоэнцефалита и определением вирусной ДНК в ликворе (Barah et al., 2001, 2003). Иммунный ответ хозяина к парво В19 в ЦНС считается предположительной причиной воспаления с подтверждением повышенного уровня цитокинов в ликворе, так же как специфического HLA-генома хозяина (Kerr et al., 2002).
е) Вирус лимфоцитарного хориоменингита (вирус ЛХМ). Вирус ЛХМ является человеческим зоонозом, вызываемым распространяемым грызунами ареновирусом, поражающим полевых мышей. Вирус передается человеку после контакта с выделениями зараженных мышей, морских свинок и хомяков. Внутриутробная инфекция у человека может привести к поражению плода (Barton и Mets, 2001; Barton et al., 2002), тогда как постнатальное инфицирование обычно протекает бессимптомно или как простудное заболевание, но может встречаться и синдром вовлечения ЦНС (Barton и Hyndman, 2000).
ж) Другие и неопределенные вирусы. Они, вероятно, являются причиной многих случаев заболеваний — в действительности большинства, в которых не могут быть выделены патогенные микроорганизмы. Понятно, что число возможных вирусных агентов велико, и поскольку заболевание обычно протекает в легкой форме, сложные исследования не проводятся.
Аденовирусный энцефалит — это воспаление ткани головного мозга, вызванное возбудителями из семейства Аденовирусов. Риск развития заболевания повышается при нарушенном иммунном статусе, в раннем возрасте, у пациентов после трансплантации. Болезнь проявляется типичными респираторными симптомами аденовирусной инфекции в сочетании с очаговыми неврологическими признаками, головной болью, нарушениями сознания. Диагностика патологии требует инструментальных (МРТ, КТ, ЭЭГ), лабораторных методов исследования (анализ СМЖ, ПЦР, серологические реакции). Лечение в основном патогенетическое — борьба с церебральным отеком, нейропротекция, нейрометаболическая терапия.
МКБ-10
Общие сведения
Аденовирусная инфекция занимает одну треть от всех респираторных вирусных инфекций, особенно часто встречается в детском возрасте от 6 месяцев до 7 лет. Распространена повсеместно, возможны вспышки в организованных коллективах. Доля аденовирусов в инфекционной заболеваемости составляет 10%. Энцефалит относится к редким осложнениям инфекционного процесса, статистические данные по его распространенности отсутствуют. Однако проблема не теряет своей актуальности вследствие риска тяжелых последствий, резидуального неврологического дефицита.

Причины
Заболевание связано с заражением больного ДНК-содержащими вирусами семейства Adenoviridae рода Mastadenovirus. Всего известно 49 патогенных для человека серотипов, которые объединяются в 7 групп по антигенной структуре и факторам патогенности. Манифестные формы болезни чаще всего вызывают вирусы групп В и Е (серотипы 3, 4, 7, 14, 21). Вероятность развития аденовирусной инфекции с переходом в энцефалит возрастает, если присутствуют следующие факторы риска:
- Сезонность. Наибольшее количество заражений приходится на зимне-весенний что обусловлено особенностями патогенеза вирусной инфекции, повышенной восприимчивостью населения.
- Повышенная вирулентность. У некоторых типов аденовирусов выявляются более агрессивные факторы патогенности, из-за чего они чаще приводят к генерализованным формам заболевания.
- Возраст. Аденовирусные энцефалиты характерны для младенцев первого года жизни, у которых иммунная защита еще недостаточно сформирована, а мозговые ткани более склонны к гидрофильности, некротическим процессам.
- Снижение иммунитета. Сюда относят как временное снижение защитных сил (при стрессах, после затяжной болезни), так и первичные, вторичные формы иммунодефицитов.
- Трансплантация. Тяжелую аденовирусную инфекцию относят к одной из причин трансплантационно-ассоциированной смертности у детей после пересадки гемопоэтических стволовых клеток.
Патогенез
Заражение аденовирусами происходит через слизистую органов дыхания воздушно-капельным путем, реже — через эпителий кишечника по фекально-оральному механизму. Сначала развивается местное воспаление в глотке, миндалинах, конъюнктиве, после чего лимфогенным путем вирусы проникают в кровь. Вирусемия продолжается до 10 суток — в это время при сочетании неблагоприятных факторов и высокой патогенности аденовирусов возможно их проникновение в церебральную ткань.
В патогенезе поражения нервной ткани участвуют сами возбудители, оказывающие прямое цитотоксическое влияние, и воспалительные цитокины: гамма-интерферон, фактор некроза опухолей, некоторые типы интерлейкинов. На фоне воспаления отмечаются нарушения микроциркуляции, дисрегуляция сосудистого тонуса, повреждение эндотелия церебральных сосудов. Это провоцирует гипоксию мозга, локальный или диффузный интерстициальный отек.
Для аденовирусного энцефалита характерно поражение ткани мозжечка, на втором месте по частоте вовлечения в процесс — височная доля коры. Интенсивность колеблется от преходящего отека до необратимой дегенерации нервной ткани, что с учетом объема очага повреждения определяет тяжесть состояния, число осложнений. Для новорожденных более типично диффузное распространение воспалительных изменений, склонность к некрозам, образованию мозговых кист.
Симптомы аденовирусного энцефалита
Развитию энцефалита предшествуют специфические для аденовирусной инфекции катаральные проявления. Беспокоят симптомы ринита, фарингита, влажный кашель. При осмотре горла выявляется гиперемия и отечность задней стенки глотки, гиперплазия лимфоидных фолликулов. Типично поражение глаз: слезотечение, светобоязнь, отечность кожи век. Зачастую увеличивается одна или несколько групп периферических лимфатических узлов.
Энцефалит манифестирует с фебрильной лихорадки, сопровождающейся интенсивными головными болями, а у больных детей младшего возраста нередко бывает тошнота, рвота, расстройства стула. Пациенты теряют аппетит, испытывают сильную слабость, сонливость. Менингеальные признаки выражены слабо: небольшая ригидность мышц затылка, повышенная чувствительность к яркому свету и громким звукам, сомнительные симптомы Кернига, Брудзинского.
Очаговые признаки аденовирусного энцефалита зависят от локализации поражения. При распространении воспаления на мозжечок наблюдается неуверенная шатающаяся походка, нарушение координации движений, неспособность контролировать мелкую моторику. Снижается мышечный тонус, возникает тремор при попытке поддержания позы или выполнении целенаправленных движений.
Реже встречаются нарушения речи: нечеткость произношения слов, неправильное построение фраз, затруднение произношения в начале слова или слога. Возможен нистагм — быстрые непроизвольные колебания глазных яблок. Иногда появляются слуховые галлюцинации в виде монотонного шума, невозможность распознавания речи при сохранении способности говорить, вестибулярные нарушения.
Осложнения
Наиболее опасным последствием острого периода энцефалита является отек-набухание головного мозга, который при отсутствии своевременной дегидратации результирует дислокационным синдромом. При вклинении мозга в большое затылочное отверстие существует высокая вероятность смертельного исхода от нарушения витальных функций. Особенно тяжело вирусный процесс протекает у иммунокомпрометированных больных — смертность достигает 70%.
В 30% случаев воспаление распространяется с развитием энцефаломиелита, менингоэнцефалита, энцефаломиелополирадикулоневрита. К другим осложнениям острой стадии относятся полиорганная недостаточность, церебральные кровоизлияния. Отдаленные последствия аденовирусного энцефалита включают нарушения мышечного тонуса, двигательные расстройства, когнитивный дефицит. Изредка после перенесенной болезни формируется гидроцефалия, эпилепсия.
Диагностика
Обследование пациента у невролога начинается со сбора анамнеза, выяснения случаев контакта со страдающими аденовирусной инфекцией. В ходе осмотра обращается внимание на очаговую неврологическую симптоматику, что помогает поставить топический диагноз, а также проводится оценка состояния кожных покровов, работы сердечно-сосудистой и дыхательной системы. Для подтверждения диагноза назначаются специализированные методы исследования:
- МРТ головного мозга. Стандартная визуализация, применение контрастной МР-ангиографии и МР-венографии — самые информативные диагностические методы, которые показывают до 90% очаговых изменений головного мозга при энцефалите. Как альтернатива может производиться КТ головного мозга.
- Нейросонография. УЗИ головного мозга рекомендовано преимущественно до 5-летнего возраста как безопасный и достаточно информативный способ ежедневного мониторинга состояния больного. Для исключения возможных тромботических осложнений проводится дуплексное сканирование мозговых сосудов.
- Дополнительные методы визуализации. При неясном диагнозе и для прогнозирования исходов делают МРТ с функциональными пробами, МР-спектроскопию. Для оценки функционального состояния мозговой коры информативна позитронно-эмиссионная томография.
- Нейрофизиологическое обследование. Соответственно преобладающей клинической симптоматике используются электроэнцефалография, мультимодальные вызванные потенциалы мозга, транскраниальная магнитная стимуляция. Для обнаружения периферических поражений выполняются ЭНМГ, игольчатая миография.
- Исследование ЦСЖ. При диагностической люмбальной пункции определяется смешанный плейоцитоз, который спустя 10-14 дней приобретает лимфоцитарный характер. Уровень белка в пределах возрастной нормы или повышен до 1,5-2 г/л, показатели хлоридов и глюкозы без отклонений.
- Идентификация возбудителя. Для выявления аденовирусов применяется ПЦР крови, цереброспинальной жидкости. Информативны серологические исследования: ИФА на антитела к аденовирусной инфекции, РСК, РТГА, РН. В редких случаях прибегают к выделению вируса на культуре тканей.
Лечение аденовирусного энцефалита
Консервативная терапия
При подозрении на вирусный энцефалит до выяснения этиологического фактора назначается стартовая терапия средствами из группы нуклеотидов и нуклеозидов. После верификации аденовирусной природы заболевания этот препарат отменяют, в качестве этиотропного лечения рекомендованы противовирусные амидные производные D-рибозы.
Основу медицинской помощи при воспалении церебральных тканей составляет комплексная патогенетическая терапия, индивидуально подобранная лечащим врачом. Ее основные направления:
- Дегидратация. При отеке мозга вводят глюкокортикостероиды в возрастных дозах, осмодиуретики в комбинации с салуретиками. Объем инфузионной терапии сокращается до 75% от физиологической потребности.
- Нейропротекция. При крайне тяжелом течении заболевания используется барбитуровая кома для предупреждения распространения поражения на другие отделы головного мозга. С первого дня болезни назначаются энергокорректоры.
- Иммунокоррекция. Для улучшения иммунитета показаны препараты рекомбинантного интерферона, внутривенные иммуноглобулины, в тяжелых случаях проводится плазмаферез.
- Ноотропная терапия. Лекарства применяются для ускорения восстановления неврологических функций, повышения устойчивости церебральной ткани к гипоксии, улучшения обменных процессов в нейронах.
Реабилитация
После купирования острых проявлений аденовирусного энцефалита возможен остаточный неврологический дефицит. Для его коррекции назначается кинезиотерапия, механотерапия, специальные комплексы массажа. При когнитивных нарушениях требуется логопедическая помощь, нейроакустические, дефектологические программы. Диспансерное наблюдение после перенесенного энцефалита продолжается 3-5 лет, включает регулярные инструментальные обследования.
Прогноз и профилактика
Для больных с нормальным иммунным статусом прогноз благоприятный, до 99% случаев заканчиваются выздоровлением, регрессом очаговой неврологической симптоматики. Менее оптимистичен прогноз для детей до года, иммунокомпрометированных пациентов и людей, перенесших трансплантацию. У них более часто возникают генерализованные формы патологии, существует риск полиорганной недостаточности, летального исхода.
Для профилактики заражения аденовирусами необходимо изолировать заболевших, разобщать детей в школах и детских садах на период вспышки инфекции, проводить текущую и заключительную дезинфекцию. При контакте с больными нужно использовать средства индивидуальной защиты. Важную роль играет соблюдение личной гигиены: тщательное мытье рук, обработка их антисептиками при необходимости.
1. Недооцененная инфекция — к вопросу о факторах патогенности аденовирусов человека/ М.Р. Агеева, С.Б. Яцышина// Вопросы вирусология. — 2019. — №2.
2. Вирусный энцефалит: современная тактика ведения пациента/ М.С. Марчук// Украинский медицинский журнал. — 2019. — №2.
3. Федеральные клинические рекомендации по диагностике и лечению вирусных энцефалитов у детей/ Г.П. Иванова, Н.В. Скрипченко. — 2013.
4. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям, больным аденовирусной инфекцией. — 2013.
Читайте также:

