Из за чего папиллома высокого риска
Обновлено: 19.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер
Определение ДНК вируса папилломы человека: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Показание к назначению исследования
Вирусы папилломы человека (ВПЧ) - это группа генетически разнообразных ДНК-содержащих вирусов, относящихся к семейству Papillomaviridae и поражающих эпителий кожных покровов и слизистых оболочек ротовой полости и аногенитальной зоны.
Инфицирование вирусом папилломы человека клинически может проявляться остроконечными кондиломами, папилломами или злокачественной трансформацией клеток. По данным, которые приводит Всемирная организация здравоохранения, 50-80% населения инфицировано ВПЧ, а 5-10% из них имеют клинические проявления заболевания.
Наследственный материал (геном) вируса папилломы человека заключен в белковую оболочку, состоящую из больших (L1) и малых (L2) структурных белков. В зависимости от строения генома L1 были выявлены и описаны различные типы вируса папилломы человека. К настоящему времени выявлено и описано более 200 генотипов вируса папилломы человека, около 45 из них могут инфицировать эпителиальный слой урогенитального тракта.
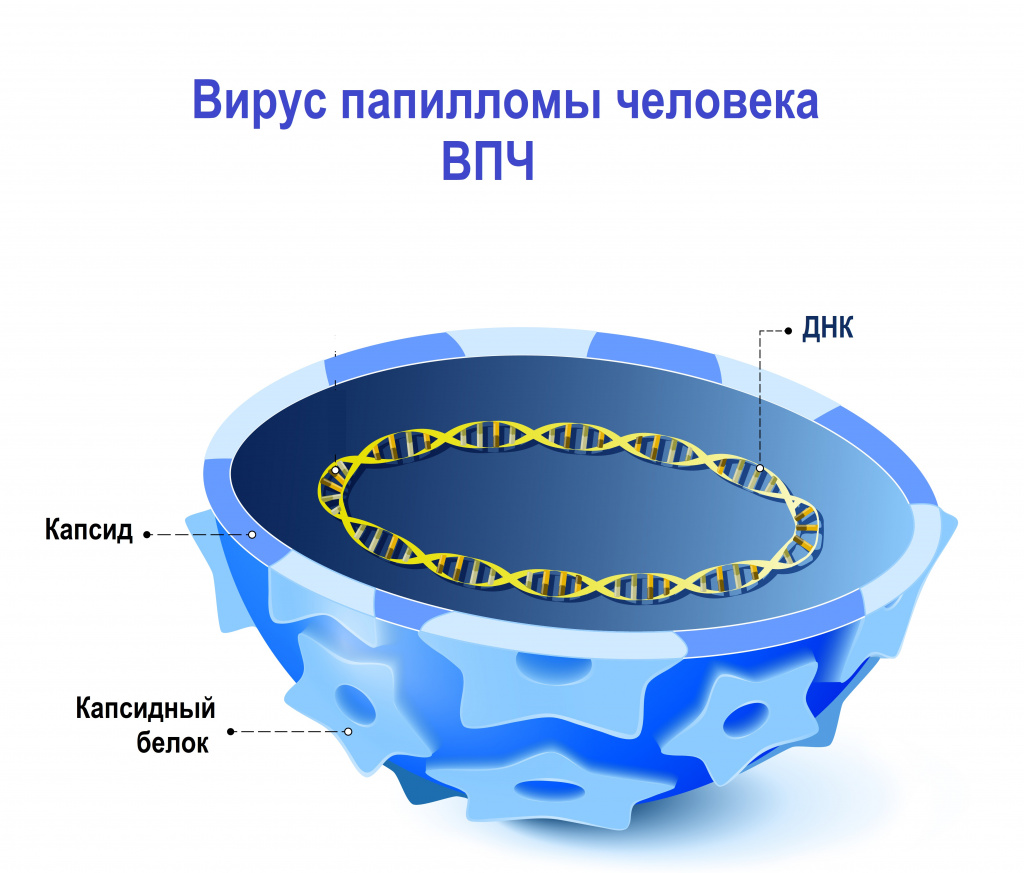
ВПЧ обладает тропностью (свойством поражать определенные органы и/или ткани) к коже и слизистым оболочкам. Источником возбудителя инфекции является больной человек или вирусоноситель.
Основной путь передачи возбудителя - половой (генитально-генитальный, мануально-генитальный, орально-генитальный), однако возможна передача и при соприкосновении (при кожном контакте). Кроме того, ВПЧ может передаваться от матери плоду во время родов.
Риск передачи при однократном половом контакте равен 80% - особенно у девушек, не достигших половой зрелости, из-за особенностей строения эпителия шейки матки в юном возрасте.
Факторы, способствующие инфицированию вирусом папилломы человека и развитию заболевания:
- раннее начало половой жизни;
- частая смена половых партнеров;
- сопутствующая урогенитальная инфекция и нарушение биоценоза влагалища;
- частые роды и аборты;
- иммунодефицитные состояния;
- генетическая предрасположенность и гормональные факторы.
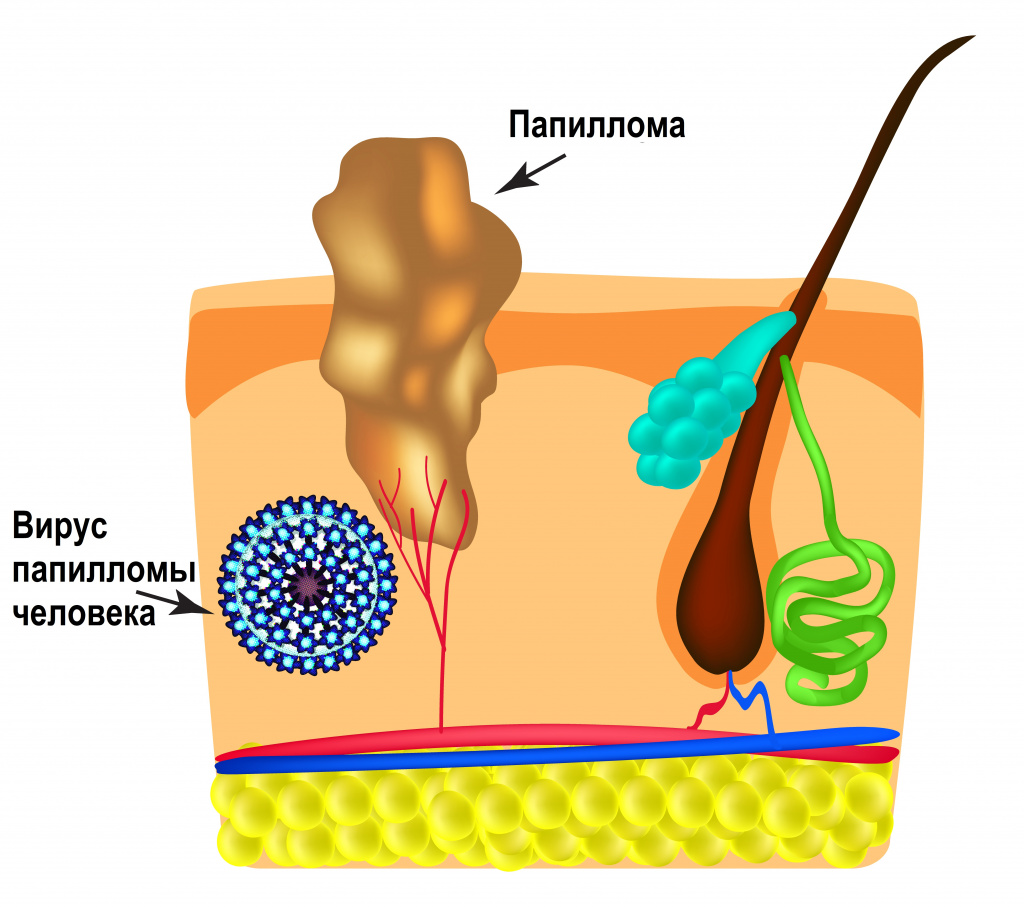
Интервал между инфицированием ВПЧ и инвазивным (проникающим) раком составляет около 10 лет или более.
Инвазивному раку предшествуют предраковые поражения шейки матки, вульвы, влагалища, анального канала, полового члена различной степени тяжести.
Вирус папилломы человека не проникает в кровь, поэтому инфекционный процесс протекает без развития воспалительной реакции.
Выделяют вирусы высокого онкогенного (или канцерогенного) риска (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого онкогенного риска (типы 6, 11, 42, 43, 44).
Типы ВПЧ низкого канцерогенного риска связаны с развитием остроконечных кондилом, папиллом и дисплазиями легкой степени. Типы ВПЧ высокого канцерогенного риска, наряду с остроконечными кондиломами и дисплазиями, также могут вызывать злокачественную трансформацию эпителия, приводя к развитию рака.
Например, высокоонкогенные типы ВПЧ 16 и 18 вызывают в 70% случаев рак шейки матки, в 80% рак вульвы и влагалища, в 92% анальный рак, в 95% рак ротовой полости, в 89% рак ротоглотки, в 63% рак полового члена. Генотипы ВПЧ 6 и 11 обуславливают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза.
Таким образом, дифференцированное определение ДНК вируса папилломы человека назначают в следующих случаях:
- для подтверждения ВПЧ при наличии папилломатозных разрастаний и изменений на слизистых оболочках половых органов;
- для скрининга (обследования лиц, не считающих себя больными) с целью выявления скрыто протекающего заболевания;
- для контроля эффективности проводимой терапии.
- с 21 года до 29 лет - не реже 1 раза в 3 года;
- с 30 до 69 лет - не реже 1 раза в 5 лет.
Высокая сексуальная активность предполагает проведение скрининга с18 лет.
Подготовка к процедуре
Обследование женщин целесообразно проводить в первую половину менструального цикла, но не ранее 5-го дня. Допустимо обследование во второй половине цикла, но не позднее, чем за 5 дней до предполагаемого начала менструации.
Накануне и в день обследования пациентке не рекомендуется спринцевать влагалище. Забор биоматериала не следует осуществлять ранее 24-48 часов после полового контакта, интравагинального УЗИ и кольпоскопии.
Соскоб из уретры проводят до или через 2-3 часа после мочеиспускания.
Мужчинам необходимо исключить половые контакты за 1–2 суток до взятия мазка (соскоба). Нельзя мочиться в течение 1,5-2 часов до процедуры.
Срок исполнения
До 2 рабочих дней, указанный срок не включает день взятия биоматериала.
Что может повлиять на результат
В случае несоблюдения правил подготовки полученный результат может быть некорректным.
Дифференцированное определение ДНК ВПЧ (вируса папилломы человека, Humanpapillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39, 44, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82) + КВМ
Синонимы: Анализ урогенитального соскоба на ВПЧ. HPV DNA, 21 Types, Scrape of Urogenital Epithelial Cells. Краткое описание исследования «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) 21 типа (6, 11, 16, 18, 26, 31, 33, 35, 39.
Исследуемый материал: соскоб эпителиальных клеток урогенитального тракта.
Форма представления результатов: количественный результат по каждому выявляемому показателю.
Единицы измерения: логарифм копий ДНК ВПЧ на 105 эпителиальных клеток (lg копий ДНК/105 эпит. клеток).
До проведения тестов по выявлению ДНК ВПЧ выполняется контроль взятия материала (КВМ). Если в пробе значение КВМ неудовлетворительное (менее 4 lg (10000) копий ДНК человека в пробе), исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т. д.
Расшифровка показателей
Количественный формат теста позволяет выявить вирус, оценить степень риска и возможное наличие предраковых изменений при высокой вирусной нагрузке.
Интерпретация положительного результата
В анализируемом образце биологического материала обнаруженная ДНК, специфичная для вируса папилломы человека исследуемых типов в выявленной концентрации, свидетельствует о наличии возбудителя.
Если абсолютное содержание ВПЧ превышает клинически значимое, напротив обнаруженного штамма вируса указывается его концентрация. Чем выше значение, тем выше риск развития болезней, вызываемых вирусом папилломы человека.
Рост вирусной нагрузки через 3, 6 и 9 мес. после проведенного лечения свидетельствует о возможности рецидива.
- генотипы низкого онкогенного риска: 6, 11, 44;
- генотипы высокого онкогенного риска: 16, 18, 26, 31, 33, 35, 39, 45, 51, 52, 53, 56, 58, 59, 66, 68, 73, 82.
Выявление нескольких генотипов вируса предполагает менее благоприятный прогноз течения заболевания и более высокий риск персистенции.
При обнаружении 16 и 18 генотипов рекомендуется проводить кольпоскопическое обследование, не откладывая.
При выявлении других типов высокого риска назначают цитологическое обследование, а при его положительном результате - кольпоскопию.
Дополнительное обследование при отклонении от нормы
Врач интерпретирует результат анализа с учетом данных о пациенте и болезни, заключений осмотра, цитологического и гистологического исследований.
Гинеколог, уролог или проктолог может назначить дополнительные исследования:
-
цитологическое исследование биоматериала соскобов вульвы и влагалища, кроме шейки матки (окрашивание по Папаниколау, Рар-тест);
В цитологическом методе диагностики для окрашивания биологического материала используют несколько способов окраски. Применение определённого метода окрашивания позволяет решить специфические задачи. Каждый метод окрашивания имеет свои особенности, специфику, например, характер окрашивания ядра, ц.
Что такое внутрипротоковая папиллома молочной железы? Причины возникновения, диагностику и методы лечения разберем в статье доктора Степыко С. Б., маммолога со стажем в 17 лет.
Над статьей доктора Степыко С. Б. работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Внутрипротоковая папиллома молочной железы — это доброкачественная папиллярная опухоль, которая развивается в расширенном протоке молочной железы. Синонимы заболевания — болезнь Шиммельбуша, цистаденопапиллома, кровоточащая молочная железа и болезнь Минца.
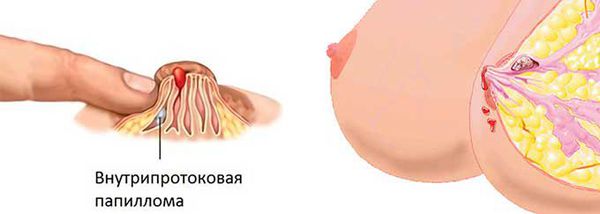
Папиллома может появиться в отдаленных участках протоков, но чаще всего формируется под ареолой, недалеко от соска. Млечный проток при этом расширяется и приобретает форму кисты. Среди остальных доброкачественных опухолей цистоаденома встречается примерно в 1 % случаев [9] .
Новообразования могут диагностироваться в любом возрасте. Их обнаруживают как у подростков, так и у женщин после наступления климакса. Но в зависимости от возраста опухоли отличаются по строению и риску развития злокачественных форм.
Внутрипротоковые папилломы считают одной из форм мастопатии. Грудные железы — это гормонально чувствительный орган, поэтому любые внешние или внутренние влияния на эндокринную систему могут стать провоцирующим фактором. Основные причины развития опухоли:
- дисфункция яичников — нарушения в работе яичников, которое сопровождается сбоем менструального цикла, приводит к нарушению баланса гормонов и преобладающему влиянию эстрогенов;
- гиперпластические заболевания репродуктивных органов (миома, эндометриоз, гиперплазия эндометрия) являются как следствием избытка этрогенов, так и сами участвуют в поддержании патологической секреции гормонов [6] ;
- воспалительные процессы в яичниках — при хроническом инфекционном поражении придатков нарушается гормональная функция, увеличивается риск развития новообразований в грудной железе;
- многократные искусственный аборты — при прерывании беременности нарушается ритмическая секреция гормонов, страдает гипоталамо-гипофизарная система, что приводит к развитию гиперпластических процессов [2] ;
- отсутствие грудного вскармливания, беременностей, завершившихся родами, период лактации менее 1 месяца или больше 1 года — во время кормления происходит окончательное созревание и функциональная перестройка тканей молочной железы, и если у женщины не было достаточной лактации, повышается вероятность развития пролиферативных заболеваний (связанных с избыточным разрастанием тканей);
- синдром поликистозных яичников — при этой патологии в яичниках не созревают яйцеклетки, наблюдается хроническая ановуляция, поэтому организм страдает от дефицита прогестерона.
Внутрипротоковая папиллома может развиваться на фоне диффузной или узловой мастопатии. Гиперплазия стромы в грудных железах ведет к сдавлению протоков, их расширению, а дисгормональное расстройство способствует пролиферации эпителия.
Риск развития эпителиальных новообразований повышается в следующих случаях:
-
, болезни щитовидной железы;
- раннее начало менархе, поздний климакс; или избыточная масса тела;
- неправильное применение гормональной контрацепции [6] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы внутрипротоковой папилломы молочной железы
Цистаденомы небольшого размера могут долгое время не обнаруживаться. Они расположены под ареолой или соском достаточно поверхностно, но связи с соском не имеют, поэтому первые симптомы женщина замечает после сдавления или небольшого повреждения груди. Из соска выделяется небольшое количество капель крови, но болезненные ощущения отсутствуют.
Признаки новообразования можно определить при самообследовании молочных желез. Оптимальный срок для диагностики — первые дни после окончания менструации. В это время грудь не находится под влиянием гормонов, поэтому остается мягкой и эластичной. Если проводить пальпацию во второй фазе цикла, можно принять за новообразование небольшую отёчность [5] .
При осмотре груди может определяться тяжистость (ощущается как натянутые плотные волокна, тяжи ткани). Если папиллома сочетается с узловой формой мастопатии, у пациентки будет пальпироваться очаговое уплотнение. Но в большинстве случаев при самообследовании можно определить кровянистые выделения из соска, а под ареолой — небольшой подвижный узел до 1 см в диаметре. Его сдавление может сопровождаться болью [7] . Иногда уплотнение имеет веретенообразную форму.
В запущенных случаях, когда женщина не проводит ежемесячный осмотр груди, она замечает первые симптомы по красно-коричневым выделениям, которые пачкают бюстгалтер. Иногда на сосках остаются корочки свернувшейся крови [5] .
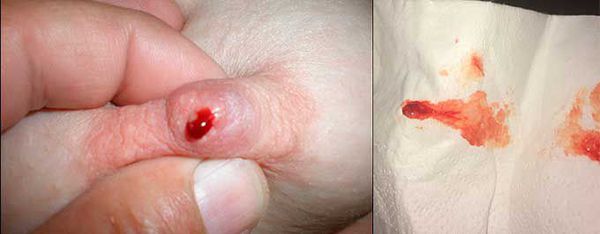
В норме на соске открывается 3-5 протоков груди, но при внутрипротоковой папилломе, расположенной поверхностно, выделения наблюдаются только из одной точки. Если новообразование находится глубоко в тканях, то кровит из нескольких протоков.
Патогенез внутрипротоковой папилломы молочной железы
Механизм развития внутрипротоковой гиперплазии схож с другими гиперпластическими процессам в молочной железе. Этот орган чувствителен к концентрации половых гормонов. Основное влияние на грудь оказывают эстрогены. После начала полового созревания под их влиянием в первую фазу менструального цикла активируются пролиферативные процессы. Они уравновешиваются прогестероном, который повышается после овуляции. У женщин с нарушениями менструального цикла этого не происходит [6] .
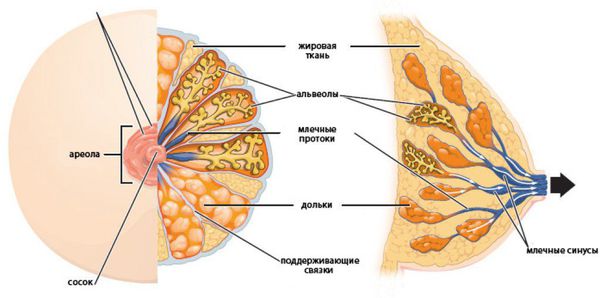
Под нескомпенсированным влиянием эстрогенов в ткани груди происходят следующие процессы:
- активируется деление эпителиальных клеток;
- усиливается выработка факторов роста;
- увеличивается активность фибробластов;
- вырабатываются протоонкогены.
Но не у всех женщин с гормональными нарушениями развивается внутрипротоковая папиллома. Для этого необходимо нарушение иммунных механизмов, снижение апоптоза — запрограммированной гибели клеток. Патологические клетки получают возможность делиться, поэтому в очаге появляются атипичные структуры.
Зависимость от эстрогенов подтверждается иммуногистохимическими анализами. В участках атипической и типичной гиперплазии наблюдается увеличение количества рецепторов к эстрогенам [8] .
Классификация и стадии развития внутрипротоковой папилломы молочной железы
Внутрипротоковые папилломы классифицируют в зависимости от их количества:
- одиночные — одно новообразование, которое часто расположено в конечных отделах протоков, характерно для женщин в период климакса;
- множественные — не имеют строгой локализации, могут обнаруживаться в разных отделах молочной железы, в глубине тканей и поверхностно, характерны для женщин репродуктивного возраста [5] .
Отдельно выделяют юношеский тип внутрипротоковых папиллом, которые формируются в подростковом возрасте.
Существует гистологическая классификация новообразования, согласно которой выделяют два типа папиллом:
- Типичная протоковая гиперплазия — доброкачественная пролиферация эпителия протоков, для которой характерно увеличение количества слоёв клеток, вплоть до полной облитерации просвета.
- Атипичная протоковая гиперплазия — в этом случае происходит увеличение слоёв клеток, которые отличаются цитологической атипией [9] .
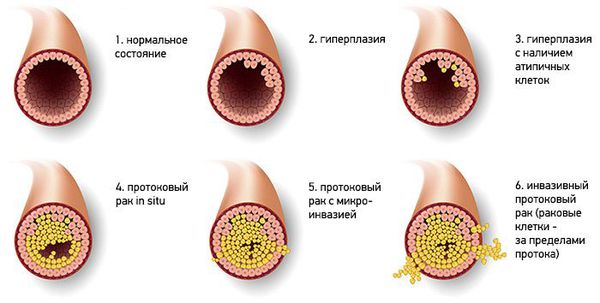
Типичная протоковая гиперплазия может быть нескольких вариантов:
- папиллярная, или слабовыраженная;
- фестончатая (криброзная), имеющая многочисленные выросты, или умеренная;
- солидная, или выраженная.
Типичная гиперплазия представлена гетерогенной клеточной популяцией. Клетки имеют разную форму и размер, ориентированы беспорядочно. Просвет между фестончатыми краями отличается по диаметру и контурам. Исследования показывают, что в новообразовании много рецепторов к эстрогенам.
При атипической протоковой гиперплазии популяция клеток мономорфная. Они одного размера и формы, с округлыми ядрами и имеют чёткие границы. Такой тип называют люминальными атипическими клетками [8] .
При внутрипротоковой папилломе с типичной гиперплазией чаще поражается одна молочная железа. Если у женщины атипическая гиперплазия, то в 50 % случаев поражение будет двусторонним [10] .
Осложнения внутрипротоковой папилломы молочной железы
Основная опасность внутрипротоковой папилломы молочной железы — риск перерождения в злокачественную опухоль. Он зависит от нескольких факторов. У женщин после 45 лет папиллома из-за гормональных особенностей способна перерождаться в рак. Этому способствуют ановуляторные циклы, когда не происходит созревания яйцеклеток и не формируется жёлтое тело, выделяющее прогестерон. В молодом возрасте вероятность озлокачествления ниже.
Если при гистологическом исследовании обнаружена типичная протоковая гиперплазия, риск развития рака в 2 раза выше, чем при других доброкачественных пролиферативных процессах, например, мастопатии [11] . При атипической гиперплазии риски повышаются в 3-5 раз [10] .
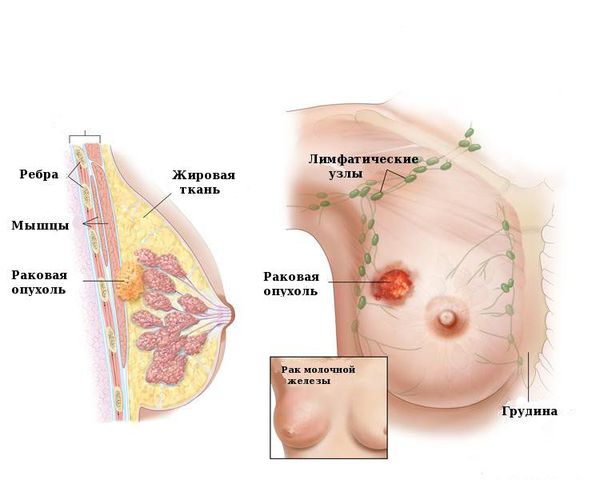
Врач может предположить риски на начальном этапе диагностики. Онконастороженность должна присутствовать при обращении за помощью женщин старше 45-50 лет, у которых папиллома хорошо пальпируется, имеются выраженные выделения из сосков. По данным УЗИ в новообразованиях, склонных к переходу в рак, имеются кальцинаты — плотные структуры с отложением солей кальция. Такие доброкачественные опухоли хорошо заметны при маммографии [5] .
При множественных внутрипротоковых папилломах молочных желез после хирургического удаления часто возникает рецидив [9] .
Диагностика внутрипротоковой папилломы молочной железы
При появлении жалоб женщина должна обратиться на консультацию к маммологу. Первым этапом диагностики является сбор анамнеза и осмотр. Врач фиксирует сопутствующие заболевания и факторы, которые могли спровоцировать развитие внутрипротоковой папилломы, отмечает время появления симптомов.
Осмотр проводится в двух положениях:
- стоя с опущенными руками: маммолог оценивает симметричность груди, наличие локальных изменений, пальпирует грудь;
- лежа с заведенными за голову руками: прощупывается глубокий слой тканей.
Обязательно оценивают выделения из молочной железы. Врач аккуратно надавливает на сосок и берёт отпечаток для цитологического исследования. По его результату можно сделать первые выводы о характере новообразования [7] .
В качестве скринингового метода на начальном этапе диагностики может применяться радиотермометрия и электроимпедансная маммография . При радиотермометрии груди через кожу специальным датчиком измеряется электромагнитное излучение тканей и выстраивается температурный график. Опухоли выглядят более горячими, чем здоровые ткани. Электроимпедансная маммография основана на изучении электропроводности, которая изменяется в опухолевых очагах. Эти способы эффективны для выявления пролиферативных процессов и позволяют отличить внутрипротоковые папилломы и рак молочной железы от фиброаденомы или мастопатии.
Методика основана на том, что при активном клеточном делении, которое происходит при гиперпластических заболеваниях, усиливается кровенаполнение и питание тканей. Это вызывает повышение температуры и электропроводности. При внутрипротоковой папилломе радиотермометрия информативна в 83 % случаев, специфична в 90 %.

Для электроимпедансной маммографии при цистаденоме гипоимпедансные очаги определяются в 70 % случаев, а если этот показатель достигает 100 %, то диагностируют рак [1] .
УЗИ молочной железы проводится для поиска объёмных образований, но при внутрипротоковой папилломе этот метод недостаточно эффективный. Косвенным признаком патологии являются:
- эктазия, или расширение, протоков;
- мягкотканное образование недалеко от соска;
- гипоэхогенный характер образования (на мониторе темнее окружающих тканей);
- четкие контуры опухоли [3] .
У женщин старше 45 лет УЗИ не используется из-за физиологических изменений молочной железы. А маммография также не покажет патологию протоков, если только опухоль не начнёт прорастать в окружающие ткани.
Выявить локализацию процесса помогает дуктография. Это рентгенологический метод диагностики, при котором в млечные протоки вводится контрастное вещество. Она назначается при патологических выделениях из грудных желез, но не во всех случаях. Нет показаний для проведения дуктографии если:
- по цвету выделения молочные, прозрачные, жёлто-зелёные или коричневые;
- нерожавшая женщина принимает препараты, которые влияют на функцию гипофиза;
- пациентка недавно родила или закончила кормить грудью [5] .
Специальная подготовка к дуктографии не требуется. Женщину нужно предупредить, что выдавливать кровь из соска перед процедурой нельзя. Обследование занимает около 30 минут. Специальным инструментом в протоки водится тонкий катетер, по которому нагнетается рентгеноконтрастный раствор. После этого выполняется стандартный снимок, как при маммографии.
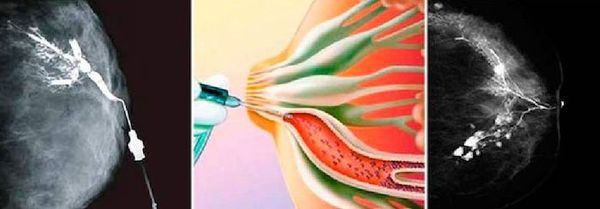
Результат снимка оценивается в тот же день. Обычно внутрипротоковая папиллома не позволяет пройти раствору в дистальные отделы протока, поэтому на снимке появляется дефект наполнения. Дуктография — это безопасный метод диагностики патологии млечных протоков. Он безболезненный, но некоторые пациентки ощущают дискомфорт. По результатам исследования врач получает точное представление о локализации патологического образования, чтобы взять образец тканей для гистологической диагностики [5] .
Подтвердить или опровергнуть злокачественный процесс помогают морфологические методы [reference:4:
- трепан-биопсия — аппаратом со специальной иглой берут фрагмент тканей из патологического очага. Но по некоторым исследованиям, методика недостаточно информативна при внутрипротоковых папилломах, т.к. в этом типе новообразования клетки гетерогенны, а во время забора материала можно захватить только доброкачественный участок. Поэтому есть риск ложного диагноза;
- вакуумная аспирационная биопсия — через толстую иглу берётся фрагмент тканей, который больше, чем при трепан-биопсии. Метод позволяет точно определить доброкачественный и злокачественный процесс [9] .
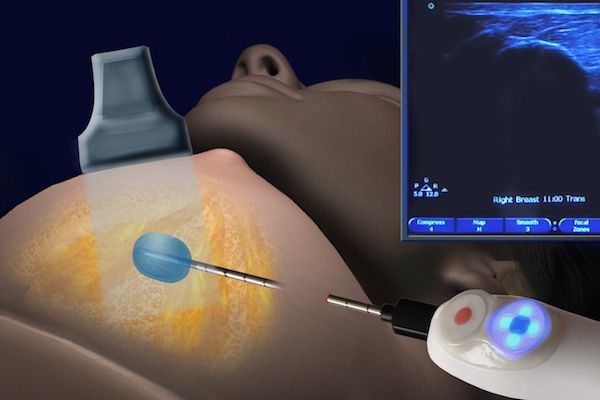
Сравнение результатов гистологии, полученной после вакуумной аспирационной биопсии и изучения тканей, удалённых во время операции, показывает, что диагнозы в большинстве случаев совпадают.
Лечение внутрипротоковой папилломы молочной железы
Консервативная терапия при внутрипротоковой папилломе не применяется. Основной метод лечения — хирургическое удаление, для которого используются разные подходы.
У молодых женщин и подростков с типичной протоковой гипреплазией, которую подтвердили при помощи вакуумной аспирационной биопсии, допускается выжидательная тактика. Но большинство исследователей считают, что папилломы, особенно множественные, нужно удалять [5] .
При атипической протоковой гиперплазии вне зависимости от возраста проводится секторальная резекция молочной железы. Техника операции отличается от той, которая применяется при фиброаденоме. Хирургическое вмешательство проводят под наркозом. Сначала в проток вводят красящее вещество, чтобы точно локализовать новообразование.
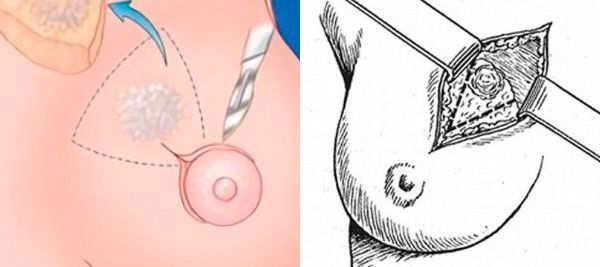
Разрез выполняют по краю ареолы. В ране за соском находят прокрашенный проток, его аккуратно выделяют из окружающих тканей и пересекают. Молочную железу ушивают внутрикожными швами и накладывают стерильную повязку [4] .
Полученные ткани отправляют на гистологическое исследование, чтобы верифицировать тип новообразования. В 15 % случаев послеоперационная диагностика подтверждает, что в очаге не гиперплазия, а инвазивный рак [12] .
Прогноз. Профилактика
Прогноз благоприятный при своевременном обнаружении единичной внутрипротоковой папилломы и её адекватном лечении. Чем младше женщина, тем ниже вероятность, что у неё обнаружится злокачественное новообразование. Но при множественных папилломах существует риск рецидива после секторальной резекции.
Профилактика внутрипротоковой папилломы проводится путем коррекции образа жизни. Защитным действием на молочные железы обладает лактация. Но женщина должна полноценно кормить ребёнка грудью на протяжении не менее 1 месяца. Лактация, которая сохраняется больше года, может иметь негативные последствия [7] .
Гормональные контрацептивы имеют профилактический эффект на молочные железы, но только при их непрерывном использовании на протяжении года и более. Лечение антагонистом эстрогена тамоксифеном и аналогичными препаратами наоборот увеличивает вероятность гиперпластических процессов в грудных железах.
Для профилактики внутрипротоковой папилломы необходимо своевременно диагностировать и лечить гинекологические заболевания. Опасность представляют миома, эндометриоз, кисты яичников, хронические воспалительные процессы [2] .
Рекомендуется избегать искусственных абортов. Они наносят вред гипоталамо-гипофизарной системе, ведут к гормональному сбою и увеличивают риски новообразований молочных желез. Поэтому женщинам, не планирующим беременность, необходимо подбирать эффективный метод контрацепции.
Но главный метод профилактики — регулярное посещение врача и самодиагностика после окончания менструации. Женщинам после удаления внутрипротоковой папилломы груди необходимо 1-2 раза в год приходить на осмотр, чтобы вовремя обнаружить рецидив.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус папилломы человека: причины появления, симптомы, диагностика и способы лечения.
Определение
Вирусы папилломы человека (ВПЧ) — это группа чрезвычайно распространенных и генетически разнородных ДНК-содержащих вирусов, поражающих эпителий кожных покровов и слизистых оболочек. Вирус папилломы человека относится к семейству папилломавирусов. Было выявлено и описано более 190 типов ВПЧ. Каждый тип отличается более чем на 10% от ближайшего родственного штамма. Из их числа более 30 типов ВПЧ могут инфицировать эпителиальный слой урогенитального тракта. В зависимости от онкогенного потенциала выделяют вирусы высокого (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого (типы 6, 11, 42, 43, 44) онкогенного риска.
На долю двух высокоонкогенных типов ВПЧ (16 и 18) приходится до 70% случаев рака шейки матки, 80% рака вульвы и влагалища, 92% анального рака, 95% рака ротовой полости, 89% рака ротоглотки, 63% рака полового члена.
При этом 16-й тип имеет самый высокий канцерогенный потенциал. Генотипы ВПЧ 6 и 11 вызывают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза, который наблюдается в основном у детей младше 5 лет или у лиц 20-30 лет.
Причины появления ВПЧ
Заболевания, вызванные вирусом папилломы человека (ВПЧ), относятся к болезням с латентным началом, хроническим персистирующим течением и проявляются доброкачественными и злокачественными новообразованиями в зоне входных ворот инфекции.
Источником возбудителя инфекции является больной человек или носитель. ВПЧ передается от человека к человеку при оральном, генитальном и анальном половых контактах, а также контактно-бытовым и вертикальным (от матери к ребенку) путями.
Вирус папилломы человека — единственный вирус, который не проникает в кровь, вследствие чего инфекционный процесс протекает без развития воспалительной реакции. В процессе инфицирования вирус папилломы человека поражает незрелые клетки, чаще базального слоя, которые затем становятся постоянным источником инфицирования эпителиальных клеток. Инфицированию способствует наличие микротравм и воспалительных процессов кожи и слизистых оболочек, приводящих к снижению местного иммунитета.
Вирус способен персистировать (хронически присутствовать) в месте проникновения как угодно долго. Инкубационный период заболевания может длиться от нескольких месяцев до нескольких лет. Среднее время между инфицированием ВПЧ и развитием аногенитальных бородавок составляет от 3 месяцев у женщин и до 11 месяцев у мужчин. Инфицирование человека может происходить как одним, так и несколькими типами ВПЧ.
Интервал между инфицированием ВПЧ и прогрессированием до инвазивного рака составляет, как правило, 10 лет или более.
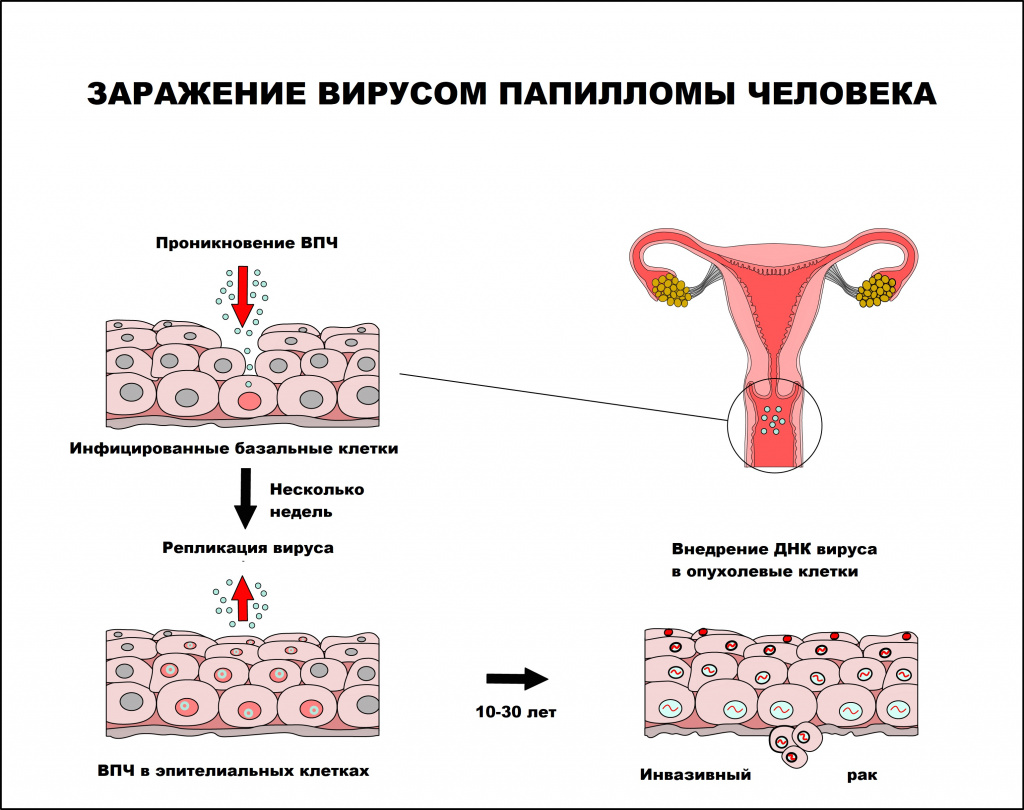
Папилломавирусная инфекция чаще регистрируется у лиц молодого возраста, имеющих большое число половых партнеров. По данным ВОЗ, 50-80% населения инфицировано ВПЧ, но лишь 5-10% инфицированных лиц имеют клинические проявления заболевания.
Классификация заболевания
Общепринятой классификации аногенитальных (венерических) бородавок не существует. Однако выделяют несколько их клинических разновидностей:
- остроконечные кондиломы;
- бородавки в виде папул;
- поражения в виде пятен;
- внутриэпителиальная неоплазия;
- бовеноидный папулез и болезнь Боуэна;
- гигантская кондилома Бушке-Левенштайна (карциномоподобная остроконечная кондилома).
Симптомы ВПЧ
- наличие одиночных или множественных образований в виде папул, папиллом, пятен на кожных покровах и слизистых оболочках половых органов;
- зуд и парестезии (расстройство чувствительности) в области поражения; болезненность во время половых контактов (диспареуния);
- при локализации высыпаний в области уретры наблюдается зуд, жжение, болезненность при мочеиспускании (дизурия); при обширных поражениях в области уретры – затрудненное мочеиспускание;
- болезненные трещины и кровоточивость кожных покровов и слизистых оболочек в местах поражения.
Бородавки в виде папул – папулезные высыпания без пальцеобразных выпячиваний, локализующиеся на кератинизированном эпителии половых органов.
Поражения в виде пятен – серовато-белые, розовато-красные или красновато-коричневые пятна на коже и/или слизистой оболочке половых органов;
Бовеноидный папулез и болезнь Боуэна – папулы и пятна с гладкой или бархатистой поверхностью; цвет элементов в местах поражения слизистой оболочки – бурый или оранжево-красный, а поражений на коже – пепельно-серый или коричневато-черный.
Гигантская кондилома Бушке-Левенштайна – мелкие бородавчатоподобные папилломы, сливающиеся между собой и образующие очаг поражения с широким основанием.
Респираторный папилломатоз – заболевание, при котором папилломы формируются в дыхательных путях, ведущих от носа и полости рта в легкие.
Диагностика ВПЧ
Латентно протекающая инфекция диагностируется только с помощью молекулярно-биологических методов исследования. Субклиническая инфекция диагностируется при молекулярно-биологическом, кольпоскопическом, цитологическом и морфологическом исследовании.
Для улучшения визуализации аногенитальных бородавок может быть проведена проба с 3-5% раствором уксусной кислоты. Тест считается отрицательным, если после обработки уксусной кислотой на поверхности шейки матки нет белых участков. И положительным при выявлении на шейке матки участков белого цвета (ацетобелых участков), отличных от остальной поверхности шейки матки.
Изменения эпителия шейки матки, вызванные ВПЧ, могут быть выявлены цитологическим методом микроскопии слущенных клеток с окраской по Папаниколау (Пап-тест).
Метод окрашивания по Папаниколау - специально разработанный метод, позволяющий с наибольшей степенью достоверности выявить ранние предраковые заболевания шейки матки. Рак шейки матки в структуре злокачественных новообразований репродуктивной системы занимает третье место. До 1992 г. заб.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус папилломы человека: причины появления, симптомы, диагностика и способы лечения.
Определение
Вирусы папилломы человека (ВПЧ) — это группа чрезвычайно распространенных и генетически разнородных ДНК-содержащих вирусов, поражающих эпителий кожных покровов и слизистых оболочек. Вирус папилломы человека относится к семейству папилломавирусов. Было выявлено и описано более 190 типов ВПЧ. Каждый тип отличается более чем на 10% от ближайшего родственного штамма. Из их числа более 30 типов ВПЧ могут инфицировать эпителиальный слой урогенитального тракта. В зависимости от онкогенного потенциала выделяют вирусы высокого (типы 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59) и низкого (типы 6, 11, 42, 43, 44) онкогенного риска.
На долю двух высокоонкогенных типов ВПЧ (16 и 18) приходится до 70% случаев рака шейки матки, 80% рака вульвы и влагалища, 92% анального рака, 95% рака ротовой полости, 89% рака ротоглотки, 63% рака полового члена.
При этом 16-й тип имеет самый высокий канцерогенный потенциал. Генотипы ВПЧ 6 и 11 вызывают практически все виды аногенитальных бородавок и большинство случаев рецидивирующего респираторного папилломатоза, который наблюдается в основном у детей младше 5 лет или у лиц 20-30 лет.
Причины появления ВПЧ
Заболевания, вызванные вирусом папилломы человека (ВПЧ), относятся к болезням с латентным началом, хроническим персистирующим течением и проявляются доброкачественными и злокачественными новообразованиями в зоне входных ворот инфекции.
Источником возбудителя инфекции является больной человек или носитель. ВПЧ передается от человека к человеку при оральном, генитальном и анальном половых контактах, а также контактно-бытовым и вертикальным (от матери к ребенку) путями.
Вирус папилломы человека — единственный вирус, который не проникает в кровь, вследствие чего инфекционный процесс протекает без развития воспалительной реакции. В процессе инфицирования вирус папилломы человека поражает незрелые клетки, чаще базального слоя, которые затем становятся постоянным источником инфицирования эпителиальных клеток. Инфицированию способствует наличие микротравм и воспалительных процессов кожи и слизистых оболочек, приводящих к снижению местного иммунитета.
Вирус способен персистировать (хронически присутствовать) в месте проникновения как угодно долго. Инкубационный период заболевания может длиться от нескольких месяцев до нескольких лет. Среднее время между инфицированием ВПЧ и развитием аногенитальных бородавок составляет от 3 месяцев у женщин и до 11 месяцев у мужчин. Инфицирование человека может происходить как одним, так и несколькими типами ВПЧ.
Интервал между инфицированием ВПЧ и прогрессированием до инвазивного рака составляет, как правило, 10 лет или более.

Папилломавирусная инфекция чаще регистрируется у лиц молодого возраста, имеющих большое число половых партнеров. По данным ВОЗ, 50-80% населения инфицировано ВПЧ, но лишь 5-10% инфицированных лиц имеют клинические проявления заболевания.
Классификация заболевания
Общепринятой классификации аногенитальных (венерических) бородавок не существует. Однако выделяют несколько их клинических разновидностей:
- остроконечные кондиломы;
- бородавки в виде папул;
- поражения в виде пятен;
- внутриэпителиальная неоплазия;
- бовеноидный папулез и болезнь Боуэна;
- гигантская кондилома Бушке-Левенштайна (карциномоподобная остроконечная кондилома).
Симптомы ВПЧ
- наличие одиночных или множественных образований в виде папул, папиллом, пятен на кожных покровах и слизистых оболочках половых органов;
- зуд и парестезии (расстройство чувствительности) в области поражения; болезненность во время половых контактов (диспареуния);
- при локализации высыпаний в области уретры наблюдается зуд, жжение, болезненность при мочеиспускании (дизурия); при обширных поражениях в области уретры – затрудненное мочеиспускание;
- болезненные трещины и кровоточивость кожных покровов и слизистых оболочек в местах поражения.
Бородавки в виде папул – папулезные высыпания без пальцеобразных выпячиваний, локализующиеся на кератинизированном эпителии половых органов.
Поражения в виде пятен – серовато-белые, розовато-красные или красновато-коричневые пятна на коже и/или слизистой оболочке половых органов;
Бовеноидный папулез и болезнь Боуэна – папулы и пятна с гладкой или бархатистой поверхностью; цвет элементов в местах поражения слизистой оболочки – бурый или оранжево-красный, а поражений на коже – пепельно-серый или коричневато-черный.
Гигантская кондилома Бушке-Левенштайна – мелкие бородавчатоподобные папилломы, сливающиеся между собой и образующие очаг поражения с широким основанием.
Респираторный папилломатоз – заболевание, при котором папилломы формируются в дыхательных путях, ведущих от носа и полости рта в легкие.
Диагностика ВПЧ
Латентно протекающая инфекция диагностируется только с помощью молекулярно-биологических методов исследования. Субклиническая инфекция диагностируется при молекулярно-биологическом, кольпоскопическом, цитологическом и морфологическом исследовании.
Для улучшения визуализации аногенитальных бородавок может быть проведена проба с 3-5% раствором уксусной кислоты. Тест считается отрицательным, если после обработки уксусной кислотой на поверхности шейки матки нет белых участков. И положительным при выявлении на шейке матки участков белого цвета (ацетобелых участков), отличных от остальной поверхности шейки матки.
Изменения эпителия шейки матки, вызванные ВПЧ, могут быть выявлены цитологическим методом микроскопии слущенных клеток с окраской по Папаниколау (Пап-тест).
Метод окрашивания по Папаниколау - специально разработанный метод, позволяющий с наибольшей степенью достоверности выявить ранние предраковые заболевания шейки матки. Рак шейки матки в структуре злокачественных новообразований репродуктивной системы занимает третье место. До 1992 г. заб.
Читайте также:

