Как называются вирусы паразитирующие на бактериях
Обновлено: 19.04.2024
Вирусы бактерий. Бактериофаги. Классификация бактериофагов. Морфология бактериофагов. Типы бактериофагов.
Бактериофаги [от бактерии, + греч. phagein, поедать] — группа вирусов, паразитирующих в бактериальных клетках. Вирусы, вызывающие гибель инфицированных бактерий, известны как литические бактериофаги. Размножение и выход дочерних популяций вируса из бактерии сопровождается её гибелью и разрушением (лизисом). Бактериофаги широко распространены в природе — их выделяют из воды, почвы, организмов различных животных и человека. Принципы классификации бактериофагов аналогичны подходам к систематике вирусов вообще.
В основу классификации положены антигенная структура, морфология фагов, спектр действия, химический состав и др. Большинство фагов относится к ДНК-содержащим вирусам с нуклео-капсидом, организованным по принципу смешанной симметрии. По спектру действия выделяют типовые фаги (Т-фаги), лизирующие бактерии отдельных типов внутри вида, моновалентные фаги, лизирующие бактерии одного вида, и поливалентные фаги, лизирующие бактерии нескольких видов. Бактериофаги устойчивы к различным физическим и химическим воздействиям. Большинство из них без вреда переносит высокие температуры (50-70 °С), действие дезинфектаитов (за исключением кислот и формалина), прямой солнечный свет и УФ-облучение в низких дозах. Бактериофаги проявляют иммуногенные свойства, вызывая синтез специфических AT.
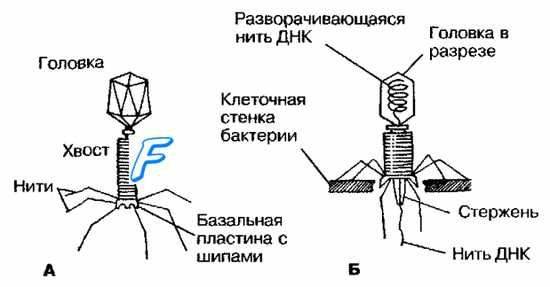
Рис. 5-10. Фаг Т4 кишечной палочки до контакта с бактерией (А) и в момент введения фаговой ДНК (Б).
Морфология бактериофагов. Типы бактериофагов
Строение бактериофагов наиболее полно охарактеризовано на основе изучения Т-фагов кишечной палочки (рис. 5-10). Внешне большинство бактериофагов напоминают сперматозоиды или головастиков, но среди них встречают и другие формы, на основании которых выделяют пять основных типов бактериофагов.
• К типу I бактериофагов относят ДНК-содержащие нитевидные фаги, лизирующие бактерии, содержащие F-плазмиды.
• Фаги типа II представлены головкой и рудиментом хвоста. Геном большинства из них образован молекулой РНК и лишь у фага jc-174 — однонитевой ДНК.
• Бактериофаги типа III имеют короткий хвост (например, Т-фаги 3 и 7).
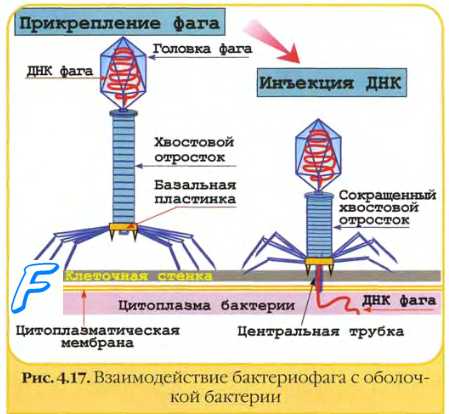
• К типу IV относят фаги с несокращаюшимся хвостом и двухнитевой ДНК (например, Т-фаги 1 и 5).
• Фаги типа V имеют ДНК-геном, сокращающийся чехол хвоста, который заканчивается базаль-ной пластиной (например, Т-фаги 2 или 4).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
БАКТЕРИОФАГИ КАК АЛЬТЕРНАТИВА АНТИБИОТИКАМ В ЛЕЧЕНИИ ИНФЕКЦИЙ
Бактериофаги — вирусы бактерий, естественные микроорганизмы, которые, размножаясь внутри бактериальной клетки, ведут к ее быстрой гибели.
Из истории открытия
Интересный факт: при нанесении бактериофага на влажные слизистые он за 20 минут очищает их от определенного вида бактерий, например от стафилококка. Так быстро не работает ни один антибиотик.
Действие бактериофагов отличается от действия антибиотиков:
- Для определенного вида бактерий существует свой определенный бактериофаг. Но стоит отметить, что не ко всем бактериям есть бактериофаги (это основной недостаток этих препаратов). Для решения вопроса, какую терапию выбрать для лечения инфекции, врач должен сначала взять материал для посева на флору с точным определением вида возбудителя и только после получения анализа на чувствительность микроорганизма к бактериофагам выбрать препарат.
- Бактериофаги не действуют на нормофлору (нормальные бактерии), поэтому лечение бактериофагами экологично и не требует коррекции нормофлоры.
- Бактериофаги не влияют на организм человека, поскольку не способны проникнуть в клетки человека. Поэтому бактериофаги не токсичны и не вызывают побочных эффектов.
- После уничтожения патогена элиминируются (самовыводятся) из организма.
- Бактериофаги просты в применении: большинство их производится в жидком виде. Доступно наружное орошение при местном применении, полоскании, в виде микроклизм при кишечных инфекциях. Но действуют бактериофаги только местно, то есть именно там, где вы их применяете при полоскании, орошении и закапывании. В отличие от антибиотиков, которые при приеме внутрь распределяются по организму и действуют во всех органах и тканях.
- Бактериофаги стимулируют местный иммунитет, так как частицы уничтоженных бактерий побуждают иммунную систему к выработке специфических антител. Из-за этого свойства бактериофаги являются препаратом выбора в лечении бактерионосительства (например, стафилококконосительства) и хронических форм бактериальных инфекций.
- Сочетаются с другими препаратами, в том числе с антибиотиками. Их совместное применение ведет к быстрому выздоровлению от бактериальной инфекции.
- По совокупности описанных свойств бактериофаги применимы как основной препарат для лечения бактериальных инфекций у беременных, детей с рождения и людей пожилого возраста, а также в тех случаях, когда имеется полирезистентность микроорганизма к антибиотикам.
В лаборатории KDL предлагается 2 варианта посевов на флору с определением чувствительности выделенной культуры микроорганизма к препаратам бактериофагов и разным наборам антибиотиков в зависимости от ситуации пациента (выбирает врач), например:
Какие инфекции можно лечить бактериофагами:
- кожные, ожоговые и раневые инфекции;
- инфекции ЛОР органов;
- инфекции урогенитального тракта;
- отдельные инфекции желудочно-кишечного тракта.
Возбудителями этих инфекций могут быть такие бактерии, как золотистый стафилококк, синегнойная палочка, патогенные формы кишечной палочки, сальмонеллы, стрептококки.
В Новосибирском научном центре технологии персонализированного лечения бактериофагами в большой коллекции бактериофагов есть уникальные штаммы, способные бороться с недавно появившимися и уже получившими широкое распространение возбудителями больничных инфекций, такими как грамотрицательные бактерии Acinetobacter baumanii, Stenotrophomonas maltophilia и др.
Последние годы ознаменовались широкими исследованиями бактериофагов из-за нарастающей проблемы антибиотикорезистентности микроорганизмов, которые находят всё новые применения не только в терапии и профилактике, но и в биотехнологиях. Их очевидным практическим результатом должно стать возникновение нового мощного направления персонализированной медицины, а также создание целого спектра технологий в пищевой промышленности, ветеринарии, сельском хозяйстве и в производстве современных материалов. Мы ждем, что второе столетие исследований бактериофагов принесет не меньше открытий, чем первое.
Строение вирусов. Классификация вирусов
Вирусы классифицируют по типу генетического материала, способам репликации, строению и расположению структурных белков (капсидов), а также наличию или отсутствию оболочки.
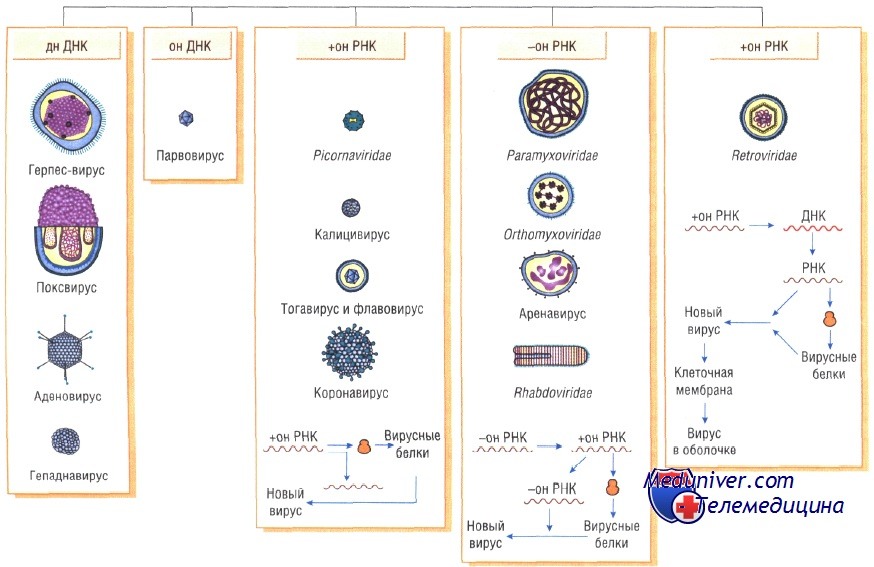
Генетическая структура и способы репликации ДНК-вирусы. Могут быть только двунитевыми и одноните-выми. К. первым относят вирус оспы, герпес-вирусы, аденовирусы, паповавирусы и полиомавирусы. Последние два вируса вызывают развитие доброкачественных (бородавки) и злокачественных (рак шейки матки) опухолей. Вирус гепатита В частично дву- и однонитевой. К однонитевым вирусам относят парвовирусы, вызывающие инфекционную эритему.
Репликация ДНК-вирусов обычно происходит в ядре клеток хозяина и сопровождается продукцией полимераз, воспроизводящих вирусную ДНК. При этом последняя не всегда встраивается в хромосомную ДНК хозяина.
РНК-вирусы. Эти вирусы содержат однонитевую РНК, но различаются по стратегии репродукции, (вирусы, содержащие плюс-однонитевую РНК и минус-однонитевую РНК). У плюс-однонитевых вирусов РНК транслируется в структурные белки и служит матрицей (мРНК) для РНК-зависимой РНК-полимеразы.
В состав минус-однонитевых вирусов входит собственная РНК-зависимая РНК-полимераза, продуцируемая на базе генома вируса мРНК. Последняя в свою очередь может быть матрицей для продукции вирусной (минус-однонитевой) РНК.
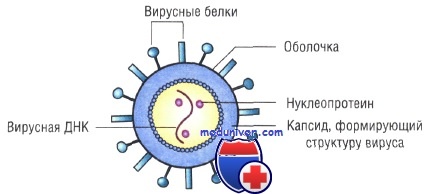
Строение капсидов вирусов. Вирусная нуклеиновая кислота покрыта белковой оболочкой, состоящей из повторяющихся единиц (капсида) с икосаэдрическим (кубическим) или спиральным типами симметрии. Капсиды вирусов с икосаэдрическим типом симметрии имеют практически сферическую форму. Спиральный тип симметрии свойствен РНК-вирусам, капсиды которых окружают нуклеиновую кислоту, располагающуюся в виде спирали.
Капсид состоит из повторяющихся компонентов (капсомеров), количество генов, кодирующих его, снижено, тем самым облегчён процесс сборки вируса.
Оболочка вирусов. В некоторых случаях нуклеиновая кислота и капсидные белки вируса (нуклеокапсид) окружены липидной оболочкой, состоящей из компонентов клетки хозяина или ядерных мембран. Мембрана клетки хозяина изменяется под действием белков, кодируемых вирусом, или гликопротеинов, выступающих в роли рецепторов для других клеток хозяина. Покрытые оболочкой вирусы чувствительны к действию веществ, растворяющих липидную мембрану (например, эфиров).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Бактериофаги под микроскопом / ©Getty images
Сегодня любой старшеклассник имеет хотя бы базовое представление о том, что такое гены, как устроена ДНК, как она копируется и каким образом с нее считывается информация. Можно сказать, что современная молекулярная биология смогла проникнуть в саму суть жизни.
Однако мало кто задумывается над тем, как ученые обо всем этом узнали. Изучать такие процессы на клетках человека и других высокоорганизованных организмов крайне сложно. Тут нужны простые модельные системы. В прошлом столетии ими стали бактериофаги – вирусы, паразитирующие на бактериях.
Невидимые помощники биологов
Случайны ли мутации?
Могут ли мутации в живых клетках возникать случайно, или для этого обязательно нужны ультрафиолетовые лучи, радиация, вирусы, токсины либо иные факторы? Сегодня ответы на эти вопросы входя в школьную программу обучения, когда-то этого не мог сказать ни один из светил науки.
При этом найти ответы было крайне важно, ведь от этого зависело понимание работы генов, наследственности и теории эволюции. Решение было обнаружено в 1943 году (когда даже еще никто не знал, как устроена ДНК!) двумя талантливыми американскими учеными — микробиологом Сальвадором Лурия и биофизиком Максом Дельбрюком. За свое открытие они получили Нобелевскую премию, а помогли им в этом бактериофаги.

Когда Лурия и Дельбрюк впервые попытались проверить эти гипотезы, их ожидало разочарование: мутации в бактериях возникали настолько хаотично, что разобраться в них было совершенно невозможно. Дальше все происходило по сюжету хорошего голливудского фильма. Помогла случайность: однажды Лурия наблюдал, как его коллега выиграл три доллара на игровом автомате и получил приз десятицентовыми монетами. В голове ученого вспыхнула ассоциация, и он понял, что нужно посчитать число колоний с разными мутациями. Мутации, которые возникают чаще, скорее всего, происходят в самых ранних поколениях микроорганизмов (читайте: до встречи с вирусом).
Ученые Сколтеха из лаборатории профессора Северинова исследовали малоизученный тип системы CRISPR-Cas у бактерий, обитающих в условиях чрезвычайно высоких температур. В ходе исследования было устан.
Лурия поделился своей догадкой с Дельбрюком, и тот, чтобы ее проверить, задействовал всю мощь статистики. Гипотеза о том, что мутации возникают только под действием фагов, была опровергнута. Они появляются постоянно, а значит, ошибки при копировании генов могут происходить случайно. Главный двигатель эволюции не останавливается никогда.
Еще в середине позапрошлого столетия чешский монах и биолог Грегор Мендель доказал своими знаменитыми экспериментами с горохом, что живые организмы не наследуют признаки от родителей напрямую. Это происходит по определенным законам через некие субстраты — гены.
Но что есть гены? Ученые быстро поняли, что эти таинственные хранители наследственной информации находятся в хромосомах. Однако, и хромосомы не так просты: в них есть ДНК и белок. Сейчас это кажется удивительным, но до середины прошлого столетия ученые отдавали пальму первенства именно белкам. Таких взглядов придерживался и американский биолог Альфред Херши. Тем не менее он решил перепроверить свои догадки вместе с ботаником Марком Чейзом. Они провели эксперименты с бактериями и фагами, впоследствии ставшие легендарными.

Переносчики ДНК
Ледерберг использовал в своих экспериментах кишечные палочки, а позже его работу продолжил биолог Нортон Зиндер. Он решил проверить, как работает конъюгация в сальмонеллах – возбудителях кишечной инфекции. Зиндер взял два штамма микроорганизмов, неспособных синтезировать некоторые соединения, и выращивал их в среде, бедной питательными веществами, да еще и с пенициллином.
Выжить должны были только самые приспособленные, благодаря новым мутациям. Но фокус, прежде сработавший с кишечными палочками, с сальмонеллами не прошел. Удалось получить лишь один штамм, в котором появились мутанты, способные синтезировать для себя все необходимые вещества.

Так в 1966 году была открыта фаговая трансдукция. Эта суперспособность вирусов делает их отличными переносчиками генетического материала, что весьма полезно в генной инженерии. С помощью фагов в бактерии можно загрузить определенный ген, и они станут производить необходимое соединение.
Косвенно бактериофаги подарили современным ученым простой, быстрый и очень эффективный способ редактирования генов. Без него генная инженерия вряд ли смогла бы достичь таких внушительных успехов. Все началось еще в 1987 году, когда японский ученый Йошизуми Ишино случайно обнаружили в ДНК кишечных палочек странные участки, где находились повторяющиеся последовательности, прерывающиеся уникальными.
Изучать гонку вооружений между бактериями и фагами, конечно, интересно, но для системы CRISPR-Cas нашлось и практическое применение. В 2012 году ученые придумали, как ее использовать для разрезания генов любых организмов в любых местах. Новый способ оказался намного быстрее и эффективнее, чем применявшиеся ранее. Система CRISPR-Cas сейчас используется для создания генетически-модифицированных организмов, производства лекарств, генетической диагностики. Она имеет потенциал и для лечения генетических заболеваний, таких как серповидно-клеточная немия, муковисцидоз.
Читайте также:

