Как победить вирус спида
Обновлено: 12.05.2024
Более 20 лет назад в мире началась эпидемия самого страшного и непонятного вирусного заболевания современности – СПИДа. Его заразность, стремительное распространение и неизлечимость снискали заболеванию славу "чумы ХХ века".
Более 20 лет назад в мире началась эпидемия самого страшного и непонятного вирусного заболевания современности – СПИДа. Его заразность, стремительное распространение и неизлечимость снискали заболеванию славу "чумы ХХ века".
История возникновения
Синдром приобретенного иммунодефицита (СПИД, AIDS по-английски), вызываемый вирусом иммунодефицита человека (ВИЧ), является смертельной болезнью, средств для лечения которой в настоящее время не существует.
Некоторые ученые считают, что вирус ВИЧ был передан от обезьян к человеку примерно в 1926 году. Последние исследования показывают, что человек приобрел этот вирус в Западной Африке. До 1930-х годов вирус никак не проявлял себя. В1959 году в Конго умер мужчина.Позднейшие исследования медиков, проанализировавших его историю болезни, показали, что, возможно, это был первый зафиксированный в мире случай смерти от СПИДа. В 1969 году в США среди проституток были зафиксированы первые случаи болезни, протекавшей с симптомами СПИДа. Тогда медики не обратили на них особого внимания, посчитав редкой формой пневмонии. В 1978 году у гомосексуалистов в США и Швеции, а также среди гетеросексуальных мужчин в Танзании и на Гаити были обнаружены симптомы одного и того же заболевания.
И только в 1981 году Центр по контролю и профилактике болезней (CDC) сообщил о выявлении у молодых гомосексуалистов в Лос-Анджелесе и Нью-Йорке новой болезни. В США было выявлено около 440 носителей вируса ВИЧ. Около 200 из этих людей умерли. Так как большинство больных были гомосексуалистами, новая болезнь получила название "Иммунодефицит, передаваемый гомосексуалистами" (Gay Related Immuno Deficiency – GRID) или "Гомосексуальный рак" (A Gay Cancer).
Иммунный дефицит (снижение иммунитета), от которого страдали заболевшие СПИДом, ранее встречался только как врожденный порок недоношенных новорожденных детей. Врачи установили, что у этих больных снижение иммунитета не было врожденным, но было приобретено в зрелом возрасте.
В 1983 году французским ученым Монтанье была установлена вирусная природа болезни. Он обнаружил в удаленном у больного СПИДом лимфатическом узле вирус, назвав его LAV (lymphadenopathy associated virus).
24 апреля 1984 года директор Института вирусологии человека Мэрилендского университета доктор Роберт Галло объявил о том, что он нашел истинную причину СПИДа. Ему удалось выделить вирус из периферической крови больных СПИДом. Он изолировал ретровирус, получивший название HTLV-III (Human T-lymphotropic virus type III). Эти два вируса оказались идентичными.
В 1985 году было установлено, что ВИЧ передается через жидкие среды тела: кровь, сперму, материнское молоко. В том же году был разработан первый тест на ВИЧ, на основе которого в США и Японии начали проверять на ВИЧ донорскую кровь и ее препараты.
В 1986 году группа Монтанье объявила об открытии нового вируса, который получил название HIV-2 (ВИЧ-2). Сравнительное изучение геномов ВИЧ-1 и ВИЧ-2 показало, что в эволюционном плане ВИЧ-2 далеко отстоит от ВИЧ-1. Авторы высказали предположение, что оба вируса существовали задолго до возникновения современной эпидемии СПИДа. ВИЧ-2 был впервые выделен в 1985 году от больных СПИДом в Гвинее-Бисау и Островах Зеленого Мыса. Исследования показали, что обусловленные ВИЧ-2 и ВИЧ-1 заболевания являются самостоятельными инфекциями, так как имеются различия в особенностях возбудителей, клинике и эпидемиологии.
В 1987 году Всемирная Организация Здравоохранения утвердила название возбудителя СПИД – "вирус иммунодефицита человека" (ВИЧ, или в английской аббревиатуре HIV).
В 1987 году была учреждена Глобальная программа ВОЗ по СПИДу, а Всемирной ассамблеей здравоохранения принята глобальная стратегия борьбы со СПИДом. В этом же году в ряде стран внедряется в лечение больных первый противовирусный препарат – азидотимидин (зидовудин, ретровир).
Необходимо подчеркнуть, что ВИЧ и СПИД не синонимы. СПИД – понятие более широкое и означает дефицит иммунитета. Такое состояние может возникнуть в результате самых различных причин: при хронических истощающих заболеваниях, воздействии лучевой энергии, у детей с дефектами иммунной системы и у больных старческого возраста с инволюцией иммунной защиты, некоторых медикаментозных и гормональных препаратов. В настоящее время название СПИД применяется для обозначения только одной из стадий ВИЧ-инфекции, а именно манифестной ее стадии.
ВИЧ-инфекция - новое инфекционное заболевание, называвшееся до открытия ее возбудителя как синдром приобретенного иммунодефицита (СПИД). ВИЧ-инфекция - прогрессирующее антропонозное инфекционное заболевание, с кровоконтактным механизмом заражения, характеризующееся специфическим поражением иммунной системы с развитием тяжелого иммунодефицита, который проявляется вторичными инфекциями, злокачественными новообразованиями и аутоиммунными процессами.
Источником ВИЧ-инфекции является больной СПИДом человек или бессимптомный вирусоноситель. Основной механизм передачи инфекции – кровоконтактный. Болезнь передается при половых контактах, особенно гомосексуальных; от инфицированной матери к ребенку в период беременности через плаценту, во время родов, при грудном вскармливании от матери к плоду; через бритвенные приборы и другие колюще-режущие предметы, зубные щетки и т. п. Эпидемиологи ВИЧ не допускают существования воздушно-капельного и фекально-орального путей передачи, так как выделение ВИЧ с мокротой, мочой и калом весьма незначительно, а также незначительно и число восприимчивых клеток в желудочно-кишечном тракте и дыхательных путях.
Существует и искусственный путь передачи: при лечебно-диагностических манипуляциях путем проникновения вируса через поврежденную кожу, слизистые оболочки (транс¬фузии крови и ее препаратов, трансплантации органов и тканей, инъекции, операции, эндоскопические процедуры и т. п.), искусственном оплодотворении, при внутривенном введении наркотических веществ, выполнении различного рода татуировок.
В группу риска входят: пассивные гомосексуалисты и проститутки, у которых более вероятны повреждения слизистых оболочек в виде микротрещин. Среди женщин основную группу риска составляют наркоманки, вводящие наркотики внутривенно. Среди больных детей 4/5 составляют дети, матери которых больны СПИДом, инфицированы ВИЧ или принадлежат к известным группам риска. Второе по частоте место занимают дети, которым производили гемотрансфузии, третье – больные гемофилией, медицинский персонал, имеющий профессиональный контакт с кровью и другими биологическими жидкостями ВИЧ-инфицированных пациентов.
Вирус иммунодефицита может существовать в организме человека в течение десяти – двенадцати лет, никак себя не проявляя. А на начальные признаки его проявления многие люди не обращают должного внимания, принимая их за симптомы других, на первый взгляд не опасных заболеваний. Если вовремя не начать процесс лечения, наступает конечная стадия ВИЧ – СПИД. Вирус иммунодефицита может стать базой для развития других болезней, носящих инфекционный характер. Наряду с риском развития СПИДа повышается и риск появления других инфекционных заболеваний.
Симптомы
Лихорадка более 1 месяца, диарея более 1 месяца, необъяснимая потеря массы тела на 10% и более, пневмонии затяжные, рецидивирующие или не поддающиеся стандартной терапии, постоянный кашель более 1 месяца, затяжные, рецидивирующие вирусные, бактериальные, паразитарные болезни, сепсис, увеличение лимфоузлов двух и более групп свыше 1 месяца, подострый энцефалит, слабоумие у ранее здоровых людей.
Последняя стадия – СПИД – протекает в трех клинических формах: онко-СПИД, нейро-СПИД и инфекто-СПИД. Онко-СПИД проявляется саркомой Капоши и лимфомой головного мозга. Нейро-СПИД характеризуется разнообразными поражениями ЦНС и периферических нервов. Что касается инфекто-СПИДа, то он проявляется многочисленными инфекциями.
При переходе ВИЧ в заключающую стадию - СПИД - симптомы заболевания становятся более явными. Человека все чаще и чаще начинают поражать различные заболевания, такие как пневмония, туберкулез легких, вирус герпеса и другие заболевания, получившие название оппортунистические инфекции. Именно они и ведут к самым тяжелым последствиям. В это время вирус иммунодефицита становится тяжелейшим заболеванием. Бывает, что состояние больного настолько тяжелое, что человек даже не в состоянии вставать с постели. Такие люди чаще всего даже не подлежат госпитализации, а находятся дома под присмотром близких им людей.
Диагностика
Основным методом лабораторной диагностики ВИЧ-инфекции является обнаружение антител к вирусу с помощью иммуноферментного анализа.
Лечение
На современном этапе развития медицины лекарства, способного полностью вылечить это заболевание, не существует. Однако, при своевременном начале лечения ВИЧ можно надолго отодвинуть момент перехода вируса иммунодефицита в развитие СПИДа, а следовательно и продлить более-менее нормальную жизнь больному.
Уже разработаны схемы лечения, которые могут существенно замедлить развитие заболевания, а так как инфекция протекает в большинстве случаев длительно, то можно надеяться на создание за это время эффективных лечебных средств.
Исцеление – не то слово, которое часто используется в связи с термином "ВИЧ-инфекция". 35 лет прошло с момента обнаружения вируса и большую часть времени врачи рассматривали полное выздоровление скорее как фантазию, а не возможную перспективу. Всю потому, что ВИЧ не похож ни на один другой вирус. Он уничтожает те самые иммунные клетки, которые предназначены для того, чтобы с ним бороться. Он разрушает иммунную защиту месяцами, а иногда – годами.
На сегодняшний день с заболеванием живут 37 млн человек по всему миру. Однако сегодня ученые больше понимают о том, как вирус "скрывается" в клетках организма и почему наша бдительная иммунная система "не замечает" его.
Национальные институты здравоохранения (NIH) США финансируют усилия по лечению ВИЧ, а фонды – например AmfAR – ищут ресурсы, которые позволят полностью искоренить эпидемию.
"Абсолютно точно, что ВИЧ можно излечить, – говорит Ровена Джонстон, вице-президент и директор по исследованиям AmfAR. – Вопрос на миллиард долларов: "Как это сделать?".
Профессор медицины из Медшколы при Университете Джона Хопкинса Роберт Силичано одним из первых идентифицировал резервуары ВИЧ.
"Проблема в том, что такая форма ВИЧ не видна иммунной системе и на нее не влияют лекарственные препараты", – говорит Силичано. По словам доктора, вирус покидает свою укреплённую башню и идёт на штурм лишь тогда, когда человек перестаёт принимать лекарства.
В одном из докладов, которые представили на конференции по ретровирусам и оппортунистическим инфекциям 2018 года в Бостоне, исследователи обнаружили убедительные доказательства того, что резервуары могут быть активированы и устранены, по крайней мере – у животных. Дэн Барух и его коллеги из Медицинского центра Beth Israel Deaconess и Гарвардской медицинской школы показали, что препарат, который стимулирует иммунную систему и активирует резервуары, в сочетании с мощным антителом может нейтрализовать ВИЧ у инфицированных обезьян на полгода.
"Я думаю, что наши данные повышают вероятность получить препарат для полного вызоровления. Это возможно", – заявил Барух.
Такой метод в научной среде называют shock and kill: он основан на "выталкивании" спящего вируса из резеруаров и последующем уничтожении. Это шаг к избавлению людей от пожизненной зависимости от АРВ-препаратов.
Этот метод еще не был протестирован на людях и вопрос полного выздоровления еще в процессе изучения. Исследователи напоминают, что на сегодняшний день единственным полностью излечившимся от ВИЧ человеком является "берлинский" пациент, которому пересадили костный мозг от донора с особой мутацией, которая не позволяет вирусу иммунодефицита "прикрепляться" к клеткам. Браун прекратил прием АРВ-препаратов после пересадки. Прошло уже больше 10 лет и его тест на ВИЧ остаётся отрицательным.
[Подробнее об излечении Тимоти Рэя Брауна – в материале СПИД.ЦЕНТРа]
Случай Брауна доказывает, что полное выздоровление возможно, но врачи дожны добраться до "каждого закутка" организма, где может прятаться вирус, говорит доктор Стивен Дикс, профессор медицины Калифорнийского университета в Сан-Франциско.
Сейчас некоторые исследователи даже полагают, что возможно полностью реконструировать иммунную систему человека, чтобы она была способна успешно устранить любой вирус. Этим уже пользуются онкологи в борьбе с опухолями: иммунную систему программируют таким образом, что та сама атаковала злокачественные клетки.
"Я настроен оптимистично, поскольку параллели в терапии ВИЧ-инфекции и онкологии настолько тесны, что мы сможем применять товые технологии и в терапии ВИЧ", – говорит Дикс.
Никто из специалистов не ожидает, что ВИЧ будет побежден в следующем году или ближайшие пару лет. Но они более чем уверены, что в будущем мы победим эпидемию.
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
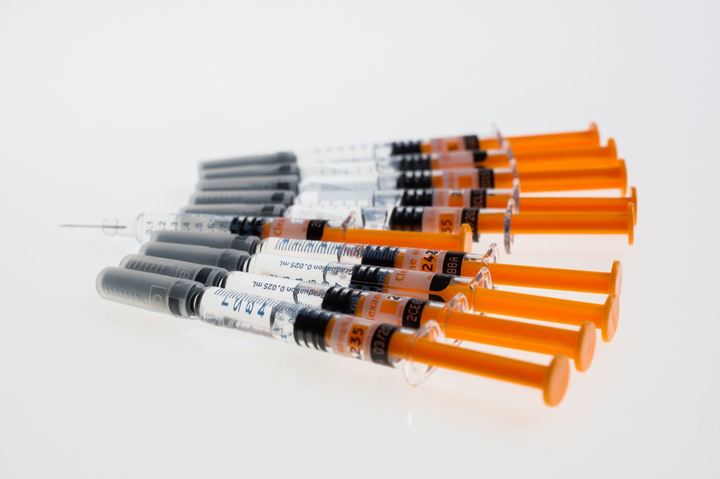
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
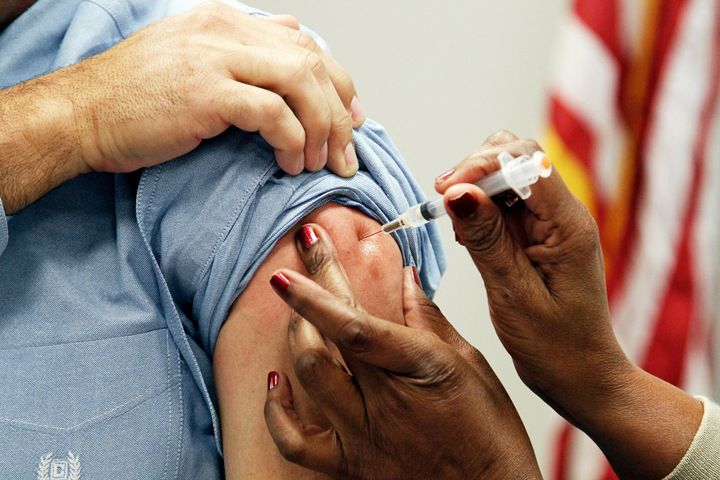
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
Данная схема приема терапии не просто спасала жизни людей, живущих с ВИЧ (при условии доступа к необходимым услугам здравоохранения), она также восстанавливала пораженную вирусом иммунную систему, что позволило людям, принимающим высокоактивную антиретровирусную терапию (АРТ), вести нормальную и здоровую жизнь.
Однако по-прежнему оставались серьезные вызовы, такие как угроза безопасности и труднопереносимые побочные эффекты. Кроме того, необходимо было принимать большое число таблеток в разные часы в течение суток, что создавало проблемы с выполнением условий данных схем. Ситуация со временем улучшилась, и на сегодняшний день большинство ЛЖВ имеют примерно такую же продолжительность жизни, что и люди, живущие без ВИЧ.
Зачем нужно лекарство?
Тем не менее создание лекарства от ВИЧ по-прежнему является труднодостижимой задачей. Даже несмотря на наличие эффективного лечения и профилактики, лекарство от ВИЧ — важная цель. Разумеется, для ЛЖВ изобретение лекарства положит конец в пожизненной необходимости проходить терапию. На сегодняшний день будущее за препаратами долгосрочного действия, однако для 38 миллионов ЛЖВ в мире излечение стало бы идеальной целью. Мировое сообщество смогло бы приблизиться к полному искоренению ВИЧ/СПИДа и снять нагрузку с системы здравоохранения как национального, так и муниципального, и регионального уровней.
В силу этих причин целый ряд государственных деятелей, научные круги, НКО и частный сектор прилагают активные усилия по разработке безопасного и доступного лекарства от ВИЧ. По аналогии с современными схемами антиретровирусной терапии — для полного излечения от ВИЧ могут понадобиться комбинации препаратов и процедур, которые по-разному работают с вирусом. Из-за того что ВИЧ умеет коварно таиться в организме человека, создавая резервуары, не распознаваемые иммунной системой, излечение от ВИЧ может потребовать использование одной из двух основных форм либо их совместное применение (по мнению исследователей, их появление на практике состоится минимум через десятилетие). Эти два подхода носят следующие названия: 1) ремиссия без приема АРТ и 2) полное искоренение вируса.
Неопределяемые без терапии
Большинство подходов, направленных на достижение ремиссии без приема АРТ, включают в себя модификацию иммунной системы с целью установить долгосрочный контроль над вирусом. Исследователи пытаются манипулировать иммунной системой с целью заставить ее распознавать и обезвреживать зараженные ВИЧ клетки или изменять их функционирование, чтобы те лучше справлялись с инфекцией.
Перспективным методом достижения ремиссии без приема АРВТ являются нейтрализующие антитела широкого спектра действия (bNAbs). Эти белки могут предотвратить заражение человеческих клеток практически всеми штаммами ВИЧ и способствовать уничтожению уже инфицированных клеток. Несмотря на то, что такие антитела производятся организмом самостоятельно у некоторых ЛЖВ, обычно их количество слишком мало, чтобы оказать ощутимую пользу, или их выработка производится на слишком позднем сроке после заражения, в результате чего они не способны контролировать быстро размножающийся и мутирующий вирус.
В настоящее время проводятся исследования на животных и людях, принимающих АРТ, с целью определить, способны ли периодические инфузии и инъекции данных антител удерживать ВИЧ в подавленном состоянии после прекращения приема АРТ. Ученые разрабатывают варианты такого вида антител с улучшенными характеристиками, в том числе с большей эффективностью и более длительным пребыванием в организме, а также тестируют лечение комбинациями двух или трех вариантов таких антител.
Полное удаление вируса из организма
Укрепление иммунных клеток для борьбы с ВИЧ. При отсутствии необходимого лечения ВИЧ уничтожает иммунную систему большинства ЛЖВ, со временем приводя к оппортунистическим заболеваниям, связанной с ВИЧ онкологией и к смерти. Тем не менее небольшая доля ЛЖВ не принимает АРТ, при этом их вирус регулярно находится в подавленном состоянии. Каким-то образом их иммунные системы естественным путем защищают организм от вируса и его разрушительного влияния.
С этим также связан феномен людей, которые имели рискованные контакты с ВИЧ-положительными партнерами, но при этом остались не инфицированными — таким образом, их иммунная система защищает их от ВИЧ. Если у исследователей получится воссоздать аналогичный уровень резистентности организма к ВИЧ среди большинства ЛЖВ, то остановка распространения вируса и излечение будут возможными.
Пересадка стволовых клеток. В начале 1990-х ряд исследований показал, что люди с более высокой природной защитой от ВИЧ часто имели мутации в гене, который кодирует белок под названием ССR5 (этот белок возникает на поверхности иммунных клеток человека и используется вирусом для проникновения в клетку с целью дальнейшего инфицирования). Если белок CCR5 не функционирует должным образом или в принципе отсутствует, ВИЧ больше не может поглощать иммунные клетки. Если ученым удастся заблокировать функционирование ССR5 или совсем исключить появление этого белка на поверхности иммунных клеток, у них появится возможность лучше контролировать ВИЧ-инфекцию либо полностью избавить от нее организм.
По предположениям некоторых ученых, если человеку, живущему с ВИЧ, пересадят костный мозг, используя в качестве донора человека с мутацией белка ССR5, его новые клетки смогут восстановить у реципиента иммунную систему, имеющую резистентность к ВИЧ. Однако пересадка костного мозга является сложной и крайне рискованной процедурой, поэтому эту теорию можно протестировать только на тех ЛЖВ, которым жизненно необходима пересадка костного мозга для лечения тяжелой формы рака.
Браун (1996 г. р.) умер в 2020 году после рецидива рака, Кастильехо (родился в Венесуэле в 1980 г.) продолжает жить здоровой жизнью.
Главным вызовом при использовании метода генетического редактирования в клинической практике на данный момент является поиск ответа на вопрос, как доставить редактирующие гены ферменты ко всем клеткам, составляющим резервуар ВИЧ, не подвергая при этом риску безопасность пациента, — для этого необходимо проведение большего количества дополнительных исследований.
Но когда?
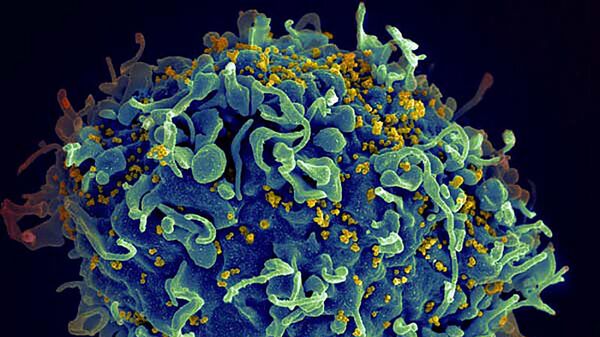
Заражение ВИЧ и многими другими опасными вирусами обычно протекает в два этапа. Сначала вирус активно размножается в организме новой жертвы, что приводит к активации иммунитета и появлению недомогания, похожего по симптомам на грипп. Когда организм начинает бороться с вирусом, инфекция переходит в хроническую стадию, постепенно истощая иммунитет.
Сегодня больные ВИЧ могут прожить десятки лет благодаря приему антиретровирусных препаратов – веществ, подавляющих различные этапы репликации вируса в клетках тела. Так как они часто обладают сильными побочными эффектами, медики часто вынуждены прекращать их прием на несколько недель.

При прекращении их приема ВИЧ "вылезает из окопов" и начинает интенсивно копировать себя, зачастую возвращаясь к начальным масштабам инфекции за три или две недели. В последние годы ученые активно пытаются найти лекарства или антитела, которые помогали бы избежать подобной "контратаки" вируса, или позволяли бы "выгнать" вирус из клеток.
Крайне малое число носителей ВИЧ, примерно 0,3% больных, не нуждается в подобной терапии - их иммунитет по пока неизвестным причинам более эффективно борется с инфекцией и сдерживает ее распространение без помощи лекарств. Многие подобные люди, так называемые "нонпрогрессоры", живут с инфекцией уже более трех десятков лет, не страдая от резкого снижения в уровне CD4-клеток.
Генетики, вирусологи и молекулярные биологи уже много лет изучают их лимфоциты и ДНК в надежде понять, что защищает их иммунитет от истощения, и трансплантировать эти уникальные особенности в организм других больных, которым повезло меньше.
Кауфманн и его коллеги провели одно из самых масштабных исследований такого рода, организовав своеобразную "перепись" среди Т-клеток и прочих иммунных телец, присутствующих в образцах крови у обычных носителей ВИЧ и людей, на которых вирус почти не действует.
Ученых интересовало то, работа каких генов в этих клетках у них отличалась и как эти отличия могли влиять на взаимодействия между вирусом и организмом человека. Дополнительно биологи проанализировали то, как изменилась работа тех же самых генов у больных, проходивших антиретровирусную терапию.
Это позволило им проследить за тем, как лекарства влияли на иммунные клетки, а также тем, было ли их действие похоже на то, что происходит в организме "нонпрогрессоров". Этот анализ раскрыл несколько важных сходств и различий в работе лимфоцитов у всех трех категорий больных.
К примеру, в иммунных тельцах людей, необычно хорошо сопротивлявшихся ВИЧ, а также в немногочисленных выживших лимфоцитах "обычных" больных были активны гены, связанные с работой и ростом трех подтипов Т-клеток –TH-1, TH-17 и TH-22. Они, как отмечают ученые, особенно активно распознавали вирусные частицы и уничтожали их, что, вероятно, помогает "нонпрогрессорам" сдерживать инфекцию.
Что интересно, подобные клетки чаще встречаются не в крови, а в кишечнике человека, где, как сегодня считают исследователи, протекает острая фаза заражения ВИЧ и его фактическое проникновение в организм. Скорее всего, они играют ведущую роль в сдерживании инфекции, так как снижение активности связанных с ними генов или пониженное число этих телец ведет к ускоренному развитию инфекции.
Антиретровирусная терапия, как обнаружили Кауфманн и его коллеги, тоже воздействует на эти участки ДНК, но не так, как это происходит в организме "нонпрогрессоров". Активность части генов вырастает, тогда как другие оказались подавлены, что заметно ослабило способность иммунитета сопротивляться инфекции.
Соответственно, если понять, как "переключить" гены в нужное положение, то можно создать средство, которое не излечит человека от ВИЧ, но переведет инфекцию в такое состояние, что она перестанет прогрессировать. Что для этого надо сделать, ученые планируют выяснить в ближайшее время.
Читайте также:

