Как поднять лейкоциты в крови при вич и гепатите
Обновлено: 12.05.2024
19517 04 Сентября
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
ВИЧ: причины появления, симптомы, диагностика и способы лечения.
Определение
ВИЧ (вирус иммунодефицита человека) – инфекционное хроническое заболевание, передающееся контактным путем, медленно прогрессирующее и характеризующееся поражением иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИДа). СПИД – это финальная стадия ВИЧ-инфекции, когда из-за ослабленной иммунной системы человек становится беззащитным перед любыми инфекциями и некоторыми видами рака. Опасность представляют так называемые оппортунистические инфекции – заболевания, вызываемые условно-патогенной или непатогенной флорой: вирусами, бактериями, грибами, которые у здоровых людей не приводят к серьезным последствиям или протекают легко и излечиваются самостоятельно. При СПИДе они наслаиваются друг на друга, имеют затяжное течение, плохо поддаются терапии и могут стать причиной летального исхода.
Причины появления ВИЧ
Источником инфекции является человек, инфицированный ВИЧ, на любых стадиях заболевания. Вирус передается через кровь, сперму, секрет влагалища, грудное молоко.
Половой путь (незащищенный секс с инфицированным партнером) – доминирующий фактор распространения ВИЧ-инфекции.
Передача ВИЧ от матери ребенку может произойти на любом сроке беременности (через плаценту), во время родов (при прохождении через родовые пути) и грудного вскармливания (при наличии язвочек, трещин на сосках матери и во рту ребенка).
Высокий риск инфицирования существует при внутривенном введении наркотических веществ нестерильными шприцами, при переливании ВИЧ-инфицированной крови и ее препаратов, использовании медицинского и немедицинского инструментария, загрязненного биологическими жидкостями человека, инфицированного ВИЧ. Кроме того, опасность могут представлять органы и ткани доноров, используемые для трансплантации.

Попадая в кровоток, вирус проникает в Т-лимфоциты хелперы, или CD-4 клетки (рановидность лейкоцитов), которые помогают организму бороться с инфекциями. Т-хелперы имеют на поверхности так называемые CD4-рецепторы. ВИЧ связывается с этими рецепторами, проникает в клетку, размножается в ней и в конечном счете уничтожает ее. Со временем вирусная нагрузка увеличивается, а количество Т-хелперов снижается.
При отсутствии лечения через несколько лет из-за значительного снижения числа Т-хелперов появляются связанные со СПИДом состояния и симптомы.
Классификация заболевания
- Стадия инкубации - от момента заражения до появления реакции организма в виде клинических проявлений острой инфекции и/или выработки антител (специфических белков, продуцируемых в ответ на проникновение антигена, в данном случае – вируса).
- Стадия первичных проявлений клинических симптомов:
В дальнейшем продолжается активное размножение вируса и разрушение Т-лимфоцитов, развивается стадия вторичных изменений, для которой характерно прогрессирующее снижение веса, общая слабость, стойкое повышение температуры, озноб, выраженная потливость. Клинические проявления оппортунистических заболеваний обусловливают клиническую картину этой стадии: пациентов беспокоят кашель и одышка, тошнота, рвота, боли в животе, тяжелая диарея, кожные высыпания, сильные головные боли, снижение памяти и внимания и др.
Диагностика ВИЧ
Лабораторные методы исследования:
Скрининг (обследование здоровых людей) на ВИЧ должен быть проведен любому человеку, который считает, что может быть заражен, а также перед любой госпитализацией и операцией, всем беременным женщинам и их половым партнерам.
Обследование целесообразно проходить людям с высоким риском заражения ВИЧ, например, при наличии заболеваний, имеющих одинаковый с ВИЧ-инфекцией механизм передачи (вирусные гепатиты В и С, заболевания, передающиеся половым путем), лицам, имеющим регулярные незащищенные половые контакты, инъекционным наркоманам, детям, рожденным от матерей с ВИЧ-инфекцией, медицинским работникам, напрямую контактирующим с кровью на работе и др.
Существуют экспресс-тесты для скрининга ВИЧ, которые можно делать в домашних условиях. Для определения специфических антител/антигенов к ВИЧ (ВИЧ-1, 2, антиген p24) используют кровь, слюну или мочу. Точность любого экспресс-теста ниже, чем теста, проводимого в лаборатории.
Для стандартного скринингового обследования определяют антитела к ВИЧ 1 и 2 и антиген ВИЧ 1 и 2 (HIV Ag/Ab Combo) в крови с помощью иммуноферментного анализа (ИФА).
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 10 рабочих дней. Синонимы: Анализ крови на антитела к ВИЧ1 и 2 и антиген ВИЧ1 и 2; ВИЧ-1 p24; ВИЧ-1-антиген, p24-антиген; ВИЧ 1 и 2 антитела и антиген p24/25, ВИЧ тест-системы 4-г.
Человечество слишком поздно осознало опасность, которую представляет вирус иммунодефицита человека (ВИЧ).
Вызываемое им заболевание – синдром приобретенного иммунодефицита (СПИД).
Правда, на начало XXI века медики научились эффективно бороться с этой инфекцией.
Никто не станет отрицать, что ведущую роль в этом направлении сыграло совершенствование лабораторных методов выявления инфекции.
А также исследования показателей крови уже зараженных людей.

Виды анализов
По своим характеристикам, ВИЧ относится к категории гемотрансмиссивных инфекций.
Заражение здорового человека происходит при попадании возбудителя в кровеносное русло.
Там вирус связывается с лимфоцитами и другими мишенями, начинает активную репликацию.
Зараженные клетки не сразу, но истощаются и погибают.
За счет этого и возникает иммунодефицит.
Благодаря компенсаторным способностям человеческого организма, инфекция очень долго (до нескольких лет) протекает бессимптомно.
В этом и заключается главная опасность инфекции.
Единственно, что может оказаться информативным в начальных стадиях болезни, это – анализы крови.
В клинической практике они применяются по разным направлениям:
- первичная диагностика – это исследования, которые прямо указывают на наличие или отсутствие ВИЧ-инфекции в организме обследуемого человека
- иммунограмма – направлена на оценку показателей иммунной системы, таких как количество лимфоцитов CD4, которые являются главной мишенью для вирусов
- вирусная нагрузка – помогает оценить степень активности инфекции и эффективность проводимой антиретровирусной терапии
- общий анализ крови (ОАК), который проводится инфицированным людям для общей оценки поражения организма вирусом
- биохимические исследования позволяют оценить функцию основных жизненно важных органов – печени, почек, кроветворной системы и так далее
Сложность в том, что показатели последних двух пунктов меняются в основном на продвинутых стадиях заболевания.
Но если человек вовремя прошел диагностику и узнал о своем статусе, он теперь может держать заболевание под полным контролем.
Достаточно лишь стать на учет в специализированном центре и вовремя сдавать необходимые анализы.
Типичный алгоритм обследования пациента предлагаем рассмотреть в виде следующей таблицы:
Кровь на ВИЧ
Экспресс-метод и ИФА при ситуации, рискованной по заражению или при характерных симптомах (лихорадка, увеличение лимфоузлов, частые простуды, диарея, похудание и так далее)
Повторный анализ
Положительный ответ первого исследования.
Клинический анализ крови
Установление диагноза ВИЧ-инфекции, в дальнейшем – по показаниям
Биохимический анализ крови
Установление диагноза ВИЧ-инфекции, в дальнейшем – по показаниям
Кровь на CD-4 клетки
Установление диагноза ВИЧ-инфекции, сначала двукратно с периодом в 7 дней, в дальнейшем каждые 6-12 месяцев, при ухудшении здоровья – немедленно
Вирусная нагрузка
Установление диагноза ВИЧ-инфекции, перед началом АРТ и дальше – через 3 месяца до получения негативных результатов, в дальнейшем каждые 6 месяцев
Как и любая патология, ВИЧ-инфекция имеет индивидуальные черты у каждого инфицированного человека.
Поэтому предложенная таблица – лишь ориентир.
Точные сроки и перечень необходимых анализов назначаются врачом, который ведет пациента.
Также меняются сроки проведения мониторинговых обследований после того, как пациент начинает прием препаратов антиретровирусной терапии (АРТ).
Показатели общего анализа крови при ВИЧ
На ранних стадиях инфекции, показатели общего анализа крови меняются мало или вообще остаются в переделах нормы.

Внимательный врач может связать некоторые граничные колебания лейкоцитов (формулы белой крови) с эпизодами повторных рецидивных простуд и респираторных инфекций.
В более продвинутых стадиях заболевания, когда компенсаторные возможности организма слабеют, в ОАК возникают такие изменения:
- Анемия. Снижение количества эритроцитов ниже возрастной и половой нормы связывают с повреждением ВИЧ клеток костного мозга и общим истощением организма. Степень анемии коррелирует с активностью ВИЧ-инфекции: малокровие нарастает при прогрессировании заболевания и наоборот, отступает на фоне АРТ-терапии.

- Лейко- и лимфопения являются типичными явлениями для ВИЧ. В общем анализе крови можно обнаружить стойкое снижение количества лейкоцитов (ниже 4*10 в 9 степени) и лимфоцитов (ниже 13%), показатели этих клеток помогают врачам составить предварительный прогноз и разработать меры по защите человека от других инфекций (например – назначить профлечение бисептолом).
- Тромбоцитопения. Падение уровня тромбоцитов ниже нормы (180*10 в 9 степени) весьма характерно для ВИЧ-инфекции, в течение 10 лет, такое явление возникает у 45% инфицированных людей. Вызывают тромбоцитопению два механизма: аутоиммунное повреждение тромбоцитопению и снижение количества их предшественников (мегакариоцитов).
Для пациента очень важно соблюдать сроки, когда врач рекомендует сдавать ОАК.
Это поможет вовремя заметить опасные осложнения ВИЧ-инфекции и предотвратить их.
Кроме того, нельзя забывать о риске развития побочных реакций в ответ на прем препаратов АРТ-терапии.
Показатель СОЭ
Очень важными данными ОАК, является скорость оседания эритроцитов или, сокращенно – СОЭ.
Норма – 4-10 мм в час.
Когда СОЭ ускоряется, это свидетельствует о нарушении белкового баланса крови.

К сожалению, показатель абсолютно неспецифичен: СОЭ возрастает при любой инфекции, травмах, онкологии.
Для пациентов характерно такое сочетание, когда скорость оседания эритроцитов повышена до 30-40-50 мм в час.
А человек чувствует себя более-менее нормально.
Такая картина связана со снижением количества белых кровяных телец.
В частности, тех лимфоцитов, какие синтезируют белки-иммуноглобулины.
Уменьшение количества этих иммунных белков влечет за собой относительное повышение белков-альбуминов, что и отражается в росте СОЭ.
Показатели биохимии крови
Биохимический анализ крови для пациентов очень важен.
С его помощью можно оценить функцию почек и, что более важно – печени.
ВИЧ очень часто соседствует с вирусными гепатитами.

Поэтому показатели трансаминаз помогают вовремя сориентироваться и дообследовать пациента.
Кроме того, контроль за функцией печени и почек позволяет вовремя заметить негативные реакции организма на АРТ-препараты.
Биохимия – важнейший комплекс анализов.
Однако из-за многогранности показателей интерпретировать их должен только специалист.
В этой статье мы просто не сможем осветить все детали таких исследований у пациентов.
ВИЧ-инфекция относится к тяжелым неизлечимым патологиям иммунодефицита человека.
С момента постановки диагноза производится постоянный контроль состояния больного.
Определяется тяжесть течения с помощью лабораторных анализов.
Данные показатели играют решающую роль в назначении антиретровирусной терапии.

Вирусная нагрузка при ВИЧ – это диагностика, позволяющая определить степень тяжести течения патологического процесса.
Показатели определяются с помощью оценки количества частиц вируса, присутствующего в определенном объеме биоматериала инфицированного.
При ВИЧ-инфекции подсчитывается количество копий РНК возбудителя в 1 мл плазмы крови пациента.
Совместно с данным анализом выполняется исследование крови на иммунный статус.
Это позволяет определить состояние иммунной системы (количество CD4).
Характеристика теста на наличие РНК вируса ВИЧ
Показатели вирусной нагрузки (ВН) – это основа мониторинга состояния пациента.
Тест проводится перед началом лечения.
Затем периодически на протяжении всего курса терапии для отслеживания динамики заболевания.
Высокоактивное антиретровирусное лечение – это единственное мероприятие, которое препятствует развитию СПИДа и повышает качество жизни пациента, а также ее продолжительность.
При отсутствии эффекта в результате проводимой медикаментозной терапии и определении высокой ВН лечащий врач корректирует лечебную тактику, при необходимости заменяет препараты.
Вирусная нагрузка определяется преимущественно методом ПЦР, но также используются другие методики исследования.
Количество вируса измеряется числом копий РНК вируса на 1 мл плазмы.
В норме вирусная нагрузка при иммунодефицитном состоянии составляет менее 12 тыс. копий ВИЧ.
Показатели значительно превышающие данные цифры говорят о тяжелом течение болезни и о необходимости коррекции проводимого лечения.
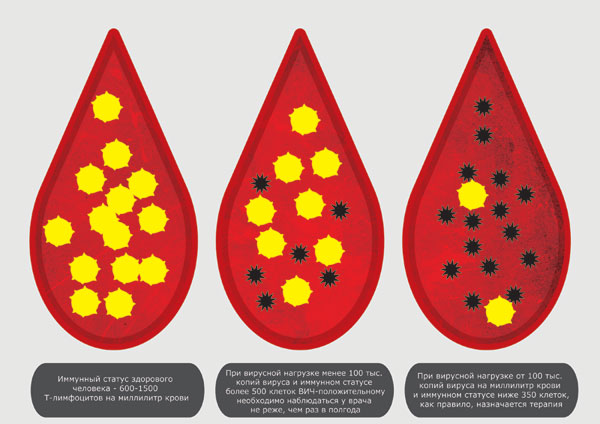
Если высокие показатели наблюдаются без проводимого лечения, врач назначает и расписывает схему терапии в срочном порядке.
Определение состояния иммунной системы при ВИЧ
Вирусная нагрузка выполняется совместно с тестом определения СD4, который при ВИЧ-инфекции является основным показателем количества иммунных клеток в организме.
СD-лимфоциты – это белые клетки крови, которые отвечают за реакцию иммунитета при проникновении в организм инфекционных возбудителей.
В здоровом организме на 1 мл крови определяется более 1000 СD-лимфоцитов.
При инфицировании вирусом иммунного дефицита здоровые клетки, отвечающие за состояние иммунитета, погибают ежедневно в больших объемах.
После чего организм заменяет их на новые.
Со временем вирус иммунодефицита угнетает иммунную систему настолько, что организм не справляется с своевременным возобновлением CD4-лимфоцитов.
Их уровень снижается, иногда до критических показателей.
Снижении количества иммунных клеток до уровня менее 250 – 300 клеток является основным критерием к назначению антиретровирусной терапии.
В противном случае у человека развивается СПИД.
Его опасность заключается в быстром возникновении множественных оппортунистических заболеваний, повышенной вероятности присоединения неинфекционных патологий и раковых процессов.
В результате человек за короткий период времени погибает.
Как правило, процесс снижения иммунных клеток длится не один год (чаще 7-9 лет).
Однако при правильном контролировании состояния больного можно избежать развитие СПИД – конечной стадии течения ВИЧ-инфекции.
Показатели СD4 могут варьироваться в крови, в зависимости от многочисленных факторов.

Это стрессовых ситуаций, менструального цикла у женщин, времени года и суток, присоединении простудных заболеваний.
Поэтому получить максимально точные результаты можно соблюдая некоторые правила.
Диагностика проводится в одно и то же время суток.
Как правило, в утренние часы.
Не выполняется тест при наличии ОРВИ или любых других, даже незначительных простудных состояниях.
Если показатели вирусной нагрузки и СD-лимфоцитов при ВИЧ находятся в пределах нормы, диагностика проводится 1 раз в 3-6 месяцев.
При низком уровне иммунных клеток и повышенном количестве РНК бактериального агента в плазме крови проводится противовирусная терапия.
В данном случае диагностика выполняется намного чаще.
Когда назначается тест на вирусную нагрузку при ВИЧ
Вирусная нагрузка при ВИЧ-инфекции необходима с следующих случаях:
- Подозрение на инфицировании ВИЧ (к примеру, после случайного незащищенного сексуального контакта, переливание донорской крови, рождение ребенка от зараженной матери). Вирусная нагрузка является одним из наиболее ранних диагностических методов, определяющих наличие РНК вируса в крови. Большинство лабораторных исследований проводится не ранее, чем через месяц после предполагаемого инфицирования – это время за которое в крови начинают формироваться антитела к инфекции. Вирусная нагрузка определяется спустя две недели.
- Взятие больного на диспансерное наблюдение.
- У пациентов ВИЧ-инфицированных, перед назначением противовирусной терапии. Забор анализов выполняется 1 раз в 3, 6 месяцев или 1 раз в год, все зависит от получаемых результатов.
- Спустя 4 недели после начала приема антиретровирусных препаратов, для контроля состояния мониторинг проводится 1 раз в 3 месяца.
Какие способы используют для определения вирусной нагрузки при ВИЧ
Для точного вычисления показателей вирусной нагрузки выполняется лабораторное исследование крови.

Иногда РНК возбудителя определяется в других биологических жидкостях, к примеру, в эякуляте или слюне.
Методы вирусной нагрузки:
- ПЦР – диагностика (высокочувствительная методика, используемая в частных клиниках, позволяет распознать болезнь на самых ранних стадиях; наличие вирусного агента определяется уже при наличии 40 копий в 1 мл плазмы крови);
- способ разветвленной ДНК (чаще используется в государственных лабораториях, является наиболее простым, но менее чувствительным по сравнению с ПЦР-диагностикой; определение показателей вирусной нагрузки возможно при больших объемах РНК вируса в плазме);
- метод изотермической амплификации нуклеиновых кислот (NASBA) – высокочувствительное исследование, широко распространено в Европейских странах, на территории РФ практически не используется.
Как правило, на протяжении лечения применяется один и тот же метод диагностики.
Это позволяет сравнивать результаты и быть уверенными в их точности.
Расшифровка результатов теста на вирусную нагрузку при ВИЧ: норма и отклонение
При подозрении на ВИЧ–инфекцию выполнение вирусной нагрузки покажет нулевую реакцию.
Это значит полное отсутствие РНК вирусного агента в организме, другими словами человек является полностью здоровым.
Иногда определение вирусной нагрузки наблюдается не только при ВИЧ, но и на фоне патологических процессов, связанных с болезнями мочевыделительной системы.
В частности, терминальная стадия почечной дисфункции, а также серьезные расстройства эндокринной системы.
Данные патологии провоцируют образование специфических иммуноглобулинов в ответ на инфекции, которые определяются в ходе лабораторной диагностики.
Вирусная нагрузка, выполняемая у женщин в период беременности, может показать наличие антител к ВИЧ-инфекции.
Но в большинстве случаев данные показатели являются ложными и связаны со стрессовым состоянием, в котором пребывает организм при вынашивании плода.
Также с гормональными перестройками.
В данном случае вирусная нагрузка покажет низкие показатели.
Так как несмотря происходящие изменения в организме в период вынашивания плода, при отсутствии инфицирования показатели не могут быть слишком высокими.
Неопределенная вирусная нагрузка при ВИЧ возможна в следующих ситуациях – если лабораторное исследование проводилось до сероконверсии.
То есть периода, когда в плазме крови начинают формироваться первые иммуноглобулины (антитела), определяемые при проведении анализов на ВИЧ-диагностику.
В таких случаях вирусная нагрузка не определяется до первых проявлений болезни.
Нормой при ВИЧ-инфекции считается наличие менее 10 000 – 15 000 клеток вируса на 1 мл крови.
Также следует отметить, данные показатели расшифровки при проведении противовирусного лечения говорят о положительной динамике и высокой эффективности медикаментозной терапии.
Неопределяемая вирусная нагрузка при ВИЧ, после приема противовирусной терапии, не означает полное излечение.
В данном случае отсутствие показателей вирусной нагрузки говорит о неправильно проведенной диагностике.
Либо о значительном снижении РНК вируса в организме больного, до уровня, который достаточно сложно определить.
Вирусная нагрузка 200 000 при ВИЧ считается сильно завышенной.
Такое состояние пациента требует незамедлительного проведения медикаментозного лечения.
Если показатели, превышающую норму при ВИЧ-инфекции, не были своевременно обнаружены, это может привести к развитию СПИД.
И даже к скорому летальному исходу, в результате присоединения других заболеваний.
Вирусная нагрузка свыше 500000 при ВИЧ является показателем развития синдрома приобретенного иммунного дефицита (СПИДа).
Если в результате проведения противовирусной терапии у больного вирусная нагрузка повышается до 700 000 при ВИЧ, это говорит о неэффективности лечения и требуется замена на другие препараты.
Но в большинстве случаев высокие показатели являются основным критерием общего состояния.
Говорят о наличии в организме других, хронических или острых процессов, которые в любой момент могут привести к смерти пациента.
Вирусная нагрузка, определяемая от 20 000 и до 100 000, является опасным состоянием, которое требует постоянного контроля.
При высоких показателях исследования проводимая антиретровирусная терапия позволяет улучшить состояние больного и снизить уровень РНК вируса к норме.
Тест на вирусный контроль и наличие иммунных клеток проводится не реже 1 раза в месяц, иногда чаще.
При этом о необходимости корректирования медикаментозного лечения решает лечащий врач.
Неопределяемая вирусная нагрузка при ВИЧ
Неопределяемые результаты анализа на вирусную нагрузку при ВИЧ чаще говорят о значительном снижении РНК вирусного агента в плазме крови.
До столь мизерного уровня, что даже высокочувствительные методы не в состоянии определить наличие вирусного агента.
Неопределяемая вирусная нагрузка не означает полное излечение от ВИЧ-инфекции и ее исчезновение из всех биологических материалов больного.
Чаще такая реакция наблюдается у пациентов спустя полгода после начала приема антиретровирусных препаратов.

В данном случае снижается вероятность инфицирования своего полового партнера.
Так как в сперме и слюне также снижается количество частиц вируса.
Но пренебрегать правилами безопасности не стоит.
Неопределяемая вирусная нагрузка у беременной женщины является большим преимуществом, так как снижается вероятность заражения плода.
Придерживаясь врачебных рекомендаций относительно образа жизни, режима питания и отдыха, больному удастся поддерживать вирусную нагрузку на неопределяемом или нормальном уровне.
Использование антиретровирусных препаратов поддерживает иммунную систему и предотвращает размножение вирусных агентов.
Адекватная схема терапии позволяет поддерживать нормальное состояние больного.
Предотвращает прогрессирование вирусной инфекции с последующим развитием СПИДа.
Высокая вирусная нагрузка при ВИЧ: используемые препараты
Антиретровирусная терапия – это единственный способ борьбы с прогрессированием вирусной инфекции в организме человека.
Высокая вирусная нагрузка при ВИЧ является основным показателем к назначению необходимых препаратов, среди которых:
- I. НИОТ, НтИОТ, ННИОТ (медикаменты препятствуют дальнейшее размножение РНК вируса внутри клетки).
- II. Ингибиторы протеазы (предотвращает формирование новых копий вируса).
- III. Ингибиторы интегразы (блокируют фермент вирусного агента, предотвращают поражение иммунных клеток).
- VI. Ингибиторы проникновения ВИЧ инфекции в клетку-мишень.
Вирус иммунодефицита серьезное и опасное заболевание, требующее всестороннего контроля состояния пациента.
Доза и курс лечения назначается квалифицированным врачом.
Самолечение в данном случае недопустимо.
Если вам необходимо определить вирусную нагрузку при ВИЧ, обращайтесь к автору этой статьи – венерологу в Москве с многолетним опытом работы.
Лейкопения – это снижение уровня лейкоцитов в периферической крови ниже 4000 в 1 мкл. Причиной данного состояния могут быть инфекционные, воспалительные аутоиммунные заболевания, генетические дефекты иммунной системы и пр. Клинически лейкопения проявляется повышенной восприимчивостью организма к различным инфекциям, однако может протекать абсолютно бессимптомно. Уровень лейкоцитов измеряется при заборе венозной либо капиллярной крови утром натощак. Для коррекции данного лабораторного отклонения проводится лечение основного заболевания.
Классификация
Низкий уровень белых кровяных телец может встречаться у абсолютно здоровых лиц – конституциональная безвредная лейкопения отмечается примерно у 2-5% людей. По происхождению патологические лейкопении разделяют на:
- Наследственные (первичные). Низкое содержание лейкоцитов обусловлено генетически детерминированными нарушениями образования и созревания клеток в красном костном мозге. К ним относятся нейтропения Костмана, наследственная нейтропения аутосомно-доминантного типа и т.д.
- Приобретенные (вторичные). Более распространенный вариант. Лейкопения развивается вследствие действия ионизирующего излучения, неблагоприятного эффекта лекарственных препаратов, биологических агентов (бактерий, вирусов) или факторов иммунной аутоагрессии.
По патогенезу (механизму развития) различают лейкопении, возникшие вследствие:
- Нарушения поступления лейкоцитов в кровь из костного мозга. Развитие лейкопении обусловлено повреждением кроветворных клеток либо неэффективным лейкопоэзом из-за дефектов митоза, созревания лейкоцитов. Наблюдается при длительном приеме цитостатических лекарственных препаратов, действии ионизируюшей радиации, генетических заболеваниях, выраженном дефиците витамина В12, фолиевой кислоты.
- Перераспределения лейкоцитов. Происходит изменение соотношения между циркулирующим и пристеночным пулом белых клеток крови в результате их скопления в расширенных капиллярах органов-депо. Встречается при шоковых состояниях.
- Сокращения времени пребывания в крови. Время присутствия в крови лейкоцитов может уменьшаться из-за их деструкции антителами (при аутоиммунных патологиях), токсическими факторами (при тяжелых инфекциях), чрезмерно активированными макрофагами (при гиперспленизме). Усиленное выведение белых клеток крови может наблюдаться при гнойных процессах – холангите, эндометрите.
В зависимости от типа клеток лейкоцитарного ряда выделяют следующие разновидности лейкопении:
- Нейтропении. Снижение содержания нейтрофилов меньше 47% от общего числа лейкоцитов. Наиболее частый вариант лейкопении. Встречается при вирусных, бактериальных инфекциях, токсическом действии медикаментов. Также возможны наследственные формы нейтропении.
- Лимфопении. Уменьшение уровня лимфоцитов ниже 19%. Характерно для вирусных инфекций, коллагенозов, гранулематозных процессов.
- Эозинопении. Содержание эозинофилов меньше 1%. Наблюдается при избыточной продукции гормонов коры надпочечников (болезнь/синдром Иценко-Кушинга). Эозинопения является индикатором неблагоприятного прогноза при септических процессах.
- Моноцитопения. Показатели моноцитов в лейкоцитарной формуле опускаются ниже 2%. Встречается при острых инфекциях, длительном приеме глюкокортикоидов.
- Агранулоцитоз. Редкое тяжелое жизнеугрожающее состояние, характеризующееся полным или почти полным исчезновением нейтрофилов в крови (ниже 0,75х10^9/л). Наблюдается при приеме миелотоксичных лекарств (цитостатиков, тиреостатиков, некоторых НПВС), действии радиации.

Причины лейкопении
Инфекции
Одна из наиболее распространенных причин лейкопении – вирусные и генерализованные бактериальные инфекции. Патогенез снижения уровня лейкоцитов может быть различным – непосредственное повреждение клеток лимфотропными вирусами (ВИЧ, Варицелла-Зостер, корь), подавление образования в костном мозге, усиленная их потеря с экссудацией.
- Вирусные инфекции. Лейкопения развивается преимущественно за счет снижения содержания лимфоцитов (лимфопения). При инфекционном мононуклеозе, гриппе, вирусных гепатитах лейкоциты снижаются незначительно и быстро возвращаются к норме после выздоровления. При ВИЧ-инфекции уровень лимфоцитов нередко достигает нуля на стадии СПИДа. Даже после лечения значения лейкоцитов могут сохраняться низкими, так как препараты для терапии ВИЧ сами по себе способны вызвать лейкопению.
- Бактериальные инфекции. Лейкопения встречается только при тяжелых генерализованных инфекциях (менингококцемия, риккетсиозы, перитонит). Падение числа лейкоцитов является одним из критериев для диагностирования септического состояния и синдрома системного воспалительного ответа. Наблюдается в основном нейтропения, ее степень коррелирует с тяжестью заболевания. Регресс наступает практически сразу после проведения антибактериальной терапии.
Прием лекарственных препаратов
К развитию лейкопении способен привести широкий спектр лекарственных средств. Известно два основных механизма лекарственно-индуцированной лейкопении: токсическое повреждение костного мозга, ведущее за собой нарушение кроветворения, и образование иммунных комплексов, в результате чего вырабатываются антитела, атакующие собственные лейкоциты макроорганизма.
Лейкопения возникает в среднем на 15 сутки от начала приема лекарства. Степень тяжести может быть самой различной – от незначительного снижения количества белых кровяных клеток до агранулоцитоза. В связи с поражением всех 3-х ростков гемопоэза часто встречается сочетание с анемией и тромбоцитопенией (панцитопения). В большинстве случаев достаточно отмены лекарственного препарата. При развитии агранулоцитоза может потребоваться применение колониестимулирующих факторов. Медикаменты, наиболее часто вызывающие лейкопению:
- Цитостатики: циклофосфамид, хлопамбуцил, метотрексат.
- Тиреостатики: пропилтиоурацил, мерказолил.
- Нестероидные противовоспалительные средства: анальгин, амидопирин.
- Антибактериальные средства: левомицетин, сульфаниламиды.
- Противовоспалительные ЛС: D-Пеницилламин, сульфасалазин.
- Антипсихотические ЛС (нейролептики): аминазин, хлорпромазин.
- Противосудорожные ЛС: карбамазепин, диазепам.
Аутоиммунные воспалительные заболевания
Причиной лейкопении могут быть аутоиммунные заболевания. В этих случаях преимущественно снижаются лимфоциты и нейтрофилы. Существует два основных патогенетических механизма аутоиммунной лейкопении – образование антилейкоцитарных антител и снижение экспрессии на мембранах иммунных клеток специальных белков (CD55, CD59), которые защищают клетки от цитолиза. Лейкопения обычно умеренная, регрессирует во время ремиссии или под влиянием патогенетического лечения. Лейкопенический синдром характерен для следующих патологий:
- Заболевания суставов: ревматоидный артрит, синдром Фелти.
- Диффузные болезни соединительной ткани (коллагенозы): системная красная волчанка, синдром Шегрена.
- Демиелинизирующие заболевания: рассеянный склероз.
- Системные васкулиты: гранулематоз с полиангиитом, неспецифический аортоартериит Такаясу.
- Воспалительные заболевания кишечника (ВЗК): неспецифический язвенный колит, болезнь Крона.
Болезни крови
Механизмов лейкопении при гематологических патологиях несколько – замещение кроветворной ткани злокачественными клетками, фиброзной или жировой тканью, синтез антилейкоцитарных антител, дефицит некоторых химических элементов для гранулоцитопоэза (железа, цианкобаламина, фолиевой кислоты):
- Онкогематологические заболевания. Лейкопенией, вплоть до агранулоцитоза, могут дебютировать острые лейкозы (алейкемическая форма) – такое начало заболевания встречается примерно в 20% случаев. Почти всегда в анализе крови дополнительно выявляются тромбоцитопения и анемия. Лейкопения характерна для лимфогранулематоза (лимфомы Ходжкина). Уровень лейкоцитов нередко остается на низком уровне и после лечения.
- Гемолитические анемии. При аутоиммунных гемолитических анемиях, гемоглобинопатиях, наследственном микросфероцитозе возможна умеренная нейтропения. Примечательно, что падение уровня лейкоцитов происходит вне криза. Период гемолитического криза, напротив, сопровождается небольшим лейкоцитозом.
- Дизэритропоэтические анемии. При апластической анемии, а также длительно протекающей недостаточности витамина В12 и фолиевой кислоты из-за угнетения функционирования всех ростков кроветворения наблюдается панцитопения. Лейкопения при железодефицитной анемии развивается только при крайне выраженном дефиците железа и носит умеренный характер.
Лучевая болезнь
Действие ионизирующей радиации неблагоприятно сказывается на всем организме человека. В первую очередь и сильнее всего страдают органы с высокой скоростью клеточного обновления, к которым относится костный мозг. Под влиянием гамма-лучей, имеющих высокую проникающую способность, гемопоэтические стволовые клетки утрачивают митотическую активность.
Наследственные формы лейкопений
К первичным лейкопениям относятся генетические заболевания, обусловленные мутациями генов, регулирующих созревание или дифференцировку лейкоцитов. Некоторые мутации приводят к изменению структуры лейкоцитарных антигенов, из-за чего они подвергаются аутоиммунному разрушению. В подавляющем большинстве случаев встречаются первичные нейтропении.
Другие наследственные лейкопении часто сопровождаются инфекционными осложнениями, которые зачастую становятся фатальными уже в детском возрасте: болезнь Костмана (генетически детерминированный агранулоцитоз), первичные иммунодефициты (синдром Ди Джорджи, Вискотта-Олдрича), синдром Чедиака-Хегаси. При этих болезнях для восстановления нормальных значений лейкоцитов требуется специфическое лечение.
Другие причины
- Белковое голодание.
- Переливание крови или лейкоцитарной массы.
- Эндокринные расстройства: гипотиреоз, акромегалия, гиперкортицизм.
- Заболевания, протекающие с гиперспленизмом: цирроз печени, малярия, висцеральный лейшманиоз.
- Болезни накопления: болезнь Гоше, болезнь Ниманна-Пика.
Диагностика
Лейкопения выявляется при клиническом исследовании крови. Ввиду многообразия этиологических факторов данного отклонения при его обнаружении следует обратиться к врачу-терапевту для тщательного сбора анамнеза, физикального осмотра, назначения дополнительного обследования:
- Анализы крови. Выполняется подсчет лейкоцитарной формулы, определяется концентрация маркеров воспаления – СОЭ, СРБ, прокальцитонина. Изучается наличие аутоантител (антител к ДНК, цитоплазме нейтрофилов, аЦЦП).
- Выявление инфекционного возбудителя. Методом иммуноферментного анализа идентифицируются антитела к возбудителям (вирусам, бактериям). Для подтверждения ВИЧ-инфекции назначается иммуноблоттинг. Проводится бактериальный посев крови, мокроты, мочи.
- Биопсия. При подозрении на лейкоз выполняется морфологическое исследование костного мозга, при котором обнаруживается гиперплазия гранулоцитарного ростка, большое количество бластных клеток. Для диагностики лимфом проводится аспирационная биопсия увеличенного лимфатического узла, в биоптате выявляется лимфоцитарная гиперклеточность, разрастание коллагена.
- Генетические исследования. Для подтверждения наследственных форм лейкопений необходимо обнаружение мутаций методом полимеразной цепной реакции и цитогенетическими исследованиями.

Коррекция
Конституциональная лейкопения не требует никакого вмешательства. Если причиной развития данного отклонения стал лекарственный препарат, необходима срочная его отмена. При выраженном снижении лейкоцитов или агранулоцитозе прибегают к введению гранулоцитарного колониестимулирующего фактора (Г-КСФ) или инфузии донорских гранулоцитов. Главное условие успешности терапии – лечение основной патологии:
- Элиминация возбудителя. Для лечения гриппа применяется осельтамивир, для борьбы с ВИЧ-инфекцией – антиретровирусные препараты (зидовудин, саквинавир). При бактериальной инфекции назначаются антибиотики.
- Противовоспалительная терапия. Чтобы достигнуть ремиссии аутоиммунных заболеваний, используются глюкокортикостероиды, иммуносупрессанты, производные 5-аминосалициловой кислоты.
- Химиотерапия. При подтверждении онкогематологической патологии назначаются комбинации химиотерапевтических средств – хлорамбуцил, винкристин, этопозид.
- Пересадка костного мозга. В случае неэффективности химиотерапии гемобластозов, а также при тяжелых первичных нейтропениях выполняется трансплантация гемопоэтических стволовых клеток.
Прогноз
Некоторые формы первичных лейкопений характеризуются высоким уровнем смертности (50-90%) среди детей от инфекционных осложнений. При вторичных лейкопениях прогноз в большей степени зависит от основного заболевания. Поэтому при любом уровне снижения лейкоцитов в крови показано тщательное обследование, направленное на выяснение причины и своевременное начало лечения.
1. Патофизиология системы крови. Часть II. Нарушения в системе лейкоцитов/ Николаева О.В., Кучерявченко М.А., Шутова Н.А. и др. – 2016.
4. Синдромная диагностика и базисная фармакология заболеваний внутренних органов. Том 2/ под ред. Г.Б. Федосеева, Ю.Д. Игнатова. – 2004.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

