Как повысить белок в крови при гепатите
Обновлено: 25.04.2024
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
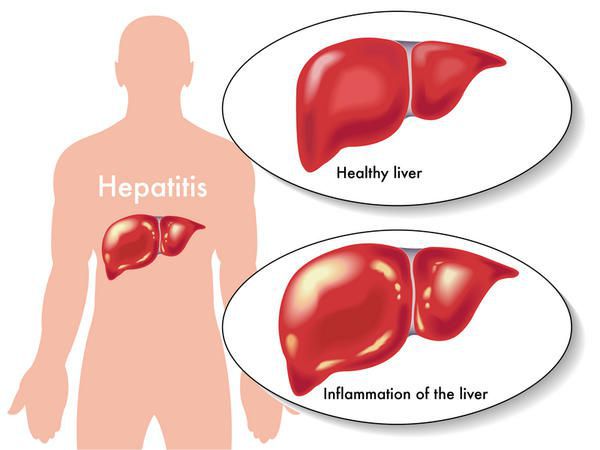
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
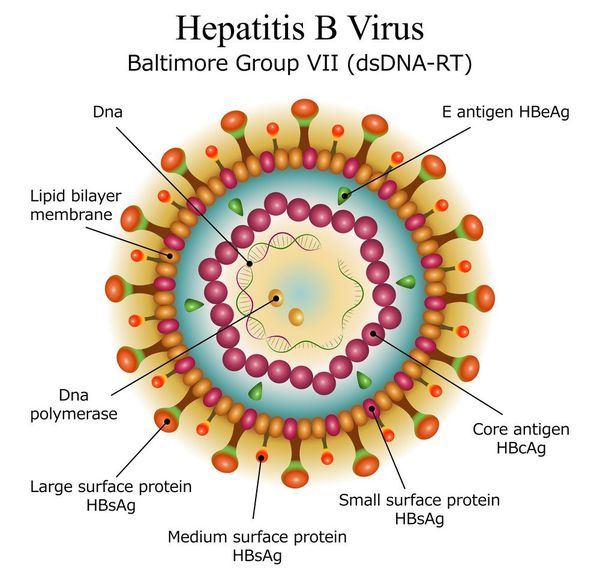
Этиология
вид — вирус гепатита В (частица Дейна)
Развитие вируса гепатита Б происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Эпидемиология
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита Б
Инкубационный период гепатита В длится от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
При первых признаках гепатита B нужно обратиться к доктору.
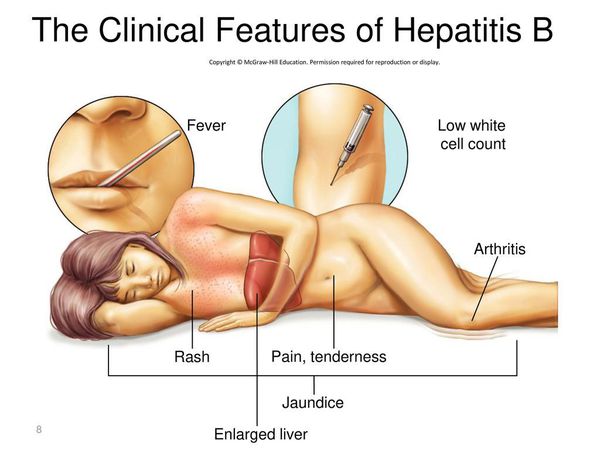
Первые признаки гепатита B
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
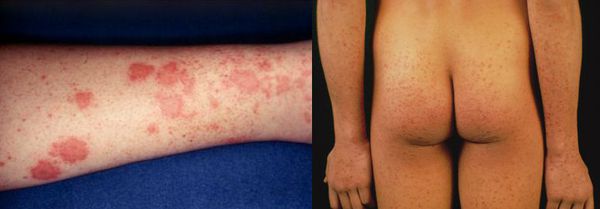
Желтушный период
Этот период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
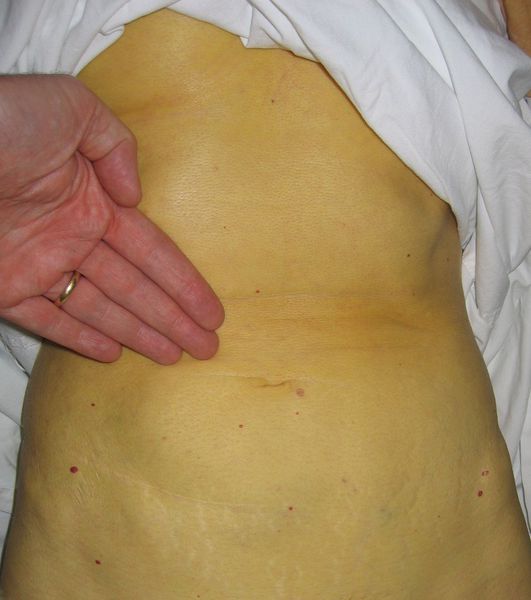
Выздоровление
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия; ;
- лептоспироз;
- ревматоидный артрит.
Гепатит В у беременных
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Патогенез гепатита Б
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
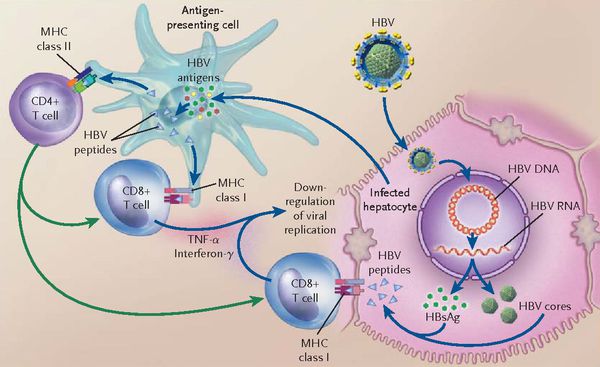
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
Классификация и стадии развития гепатита Б
По цикличности течения:
- острый;
- острый затяжной;
- хронический.
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
Группы риска хронического гепатита B
Хроническим гепатитом чаще страдают дети младше шести лет. При заражении в первый год жизни он развивается в 80–90 % случаев, от года до шести лет — в 30–50 %, у взрослых без сопутствующих заболеваний — менее чем в 5 %. [7]
Осложнения гепатита Б
Чем опасен гепатит Б
Заболевание может привести к острой печёночной недостаточности (синдрому острой печеночной энцефалопатии).
Выделяют четыре стадии болезни:
Диагностика гепатита Б
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- маркеры гепатита В: HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Скрининг при хроническом гепатите
Пациентам с хроническим гепатитом В рекомендуется не реже чем раз в полгода проходить обследование: УЗИ органов брюшной полости, клинический анализ крови, АЛТ, АСТ, тест на альфа-фетопротеин. Скрининг позволяет вовремя заметить обострение болезни и начать специфическую терапию.
Лечение гепатита Б
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений.
Диета и режим при гепатите В
В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
Медикаментозная терапия
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Прогноз. Профилактика
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации против гепатита В в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
Патогенез АГ сложен. Полагают, что это ответ генетически предрасположенного организма на какой-то внешний агент, который является пусковым моментом в развитии аутоиммунных процессов, вызывающих прогрессирующие воспалительно-некротические изменени
 |
Патогенез АГ сложен. Полагают, что это ответ генетически предрасположенного организма на какой-то внешний агент, который является пусковым моментом в развитии аутоиммунных процессов, вызывающих прогрессирующие воспалительно-некротические изменения, приводящие к фиброзу и циррозу печени (ЦП). Генетически детерминированная предрасположенность к этому заболеванию выявлена во многих исследованиях. Доказано, что большая часть больных АГ имеют фенотип по антигенам главного комплекса гистосовместимости HLA-B8, HLA-DR4, DR3 и DR52a. Пусковой агент пока неизвестен, однако есть некоторые данные о роли вирусов гепатита [31, 26], кори [27], Эпштейн-Барр вируса [32], а также интерферона (ИФН) [14] как инициаторов начала АГ.
| Аутоиммунный гепатит (АГ) — хроническое воспалительное заболевание печени невыясненой этиологии, характеризующееся определенными лабораторными, клиническими и гистологическими признаками. Болеют им в основном женщины молодого возраста |
АГ — это прогрессирующее воспаление печени, характеризующееся наличием некрозов в перипортальной, септальной зонах (ступенчатые некрозы) или, более широко, лобулярным гепатитом (ЛГ), гипергаммаглобулинемией и аутоантителами в сыворотке крови [7]. Портальные тракты печени на биоптатах находят расширенными с накоплением в них обширных инфильтратов, имеющих разный клеточный состав: лимфоциты, макрофаги, плазматические клетки. ЛГ — дольковый гепатит, когда некрозы выявляются во второй и третьей зонах ацинусов, а также обнаруживается внутридольковая лимфоидноклеточная инфильтрация, которая выражена значительно больше, чем инфильтрация портальных трактов. ЛГ является частью гистологической картины АГ, если он выявляется одновременно с перипортальным гепатитом. По гистологической картине на АГ может указывать, кроме вышеперечисленного, наличие многоядерных гепатоцитов [2].
Наконец, картина фиброза может присутствовать в той или иной степени даже при умеренной степени активности АГ, а в запущенных случаях, особенно при отсутствии эффективной терапии, формируются мостовидные некрозы и, в конце концов, ЦП.
Хотя гистологическая картина при АГ очень характерна, все-таки она неспецифична. Отличительной чертой АГ является обнаружение в биоптатах преимущественно плазматических клеток, так как выраженная инфильтрация в портальной, перипортальной зоне, вовлечение в процесс долек печени — в равной мере присущи и хроническому вирусному гепатиту (ХВГ).
Одной из основных клинических характеристик АГ является обнаружение аутоантител к клеточным и субклеточным структурам клеток разных органов [22]. Типичным маркером АГ являются антитела к ядрам клеток — ANA. Из других маркеров выявляются антитела к клеткам гладкой мускулатуры (SMA), антитела к микросомам клеток печени и эпителиальных клеток клубочкового аппарата почек (LKM), антитела к растворимому печеночному антигену (SLA), антитела к антигенам (цитокератины 8, 18) мембран гепатоцитов — LMA.
Клинические проявления АГ очень разнообразны [1, 3, 4]. С одной стороны, встречаются бессимптомные формы, когда случайно выявляется повышение АЛТ, АСТ, а с другой — острое начало болезни с тяжелым течением вплоть до развития фульминантного гепатита (ФГ).
Нередко заболевание начинается незаметно с астеновегетативных проявлений, болей в области правого предреберья, незначительной желтухи. Однако у большинства больных АГ начало болезни острое, как при остром вирусном гепатите (ОВГ), и при осмотре пациента врач впервые выявляет признаки хронического гепатита (ХГ) — телеангиоэктазии, пальмарную эритему, увеличение печени и селезенки, а также изменения в анализах крови — гипергаммаглобулинемию, увеличение IgG, снижение содержания общего белка, резкое увеличение СОЭ. Лейкопения и тромбоцитопения наблюдаются у больных на поздних стадиях болезни или при развившихся гиперспленизме и синдроме портальной гипертензии.
Когда АГ впервые проявляется желтухой, как при ОВГ, приходится дифференцировать его от гепатитов А, В, Е и особенно С, при котором антитела в сыворотке крови могут появляться через достаточно продолжительное время после начала болезни. Желтуха у пациентов с АГ может быть разной степени выраженности, часто появляется на поздних стадиях заболевания, бывает непостоянной и усиливается в период обострений. В общем же у большинства больных чаще всего изменяются аминотрансферазы, нежели щелочная фосфотаза (ЩФ) или билирубин.
| Аутоиммунный гепатит был выделен из группы болезней печени и впервые описан как отдельная нозология в начале 50-х годов [33]. В научной литературе существовал под разными названиями. Термин люпоидный гепатит, который часто использовался в нашей стране, ввел в 1956 году Дж. Маккей с соавторами в журнале Lancet, так как при этом заболевании нередко в сыворотке крови больных выявлялись волчаночные клетки. Потом, в последующие годы, люпоидный, или классический, АГ стали называть аутоиммунным активным хроническим гепатитом, но в 1993 году Международная группа по изучению болезней печени предложила термин АГ, а также критерии установления его диагноза [17] |
Для АГ характерно поражение кожи в виде геморрагической сыпи, оставляющей после себя пигментацию. Из других симптомов встречаются волчаночная и узловатая эритемы, очаговая склеродермия, пальмарная эритема и телеангиоэктазии. У всех больных выявляются изменения в эндокринной системе — аменорея, угри, гирсутизм, стрии. Диагностическое значение отдельных симптомов болезни при АГ неодинаково. К наиболее значимым относятся длительная лихорадка и арталгии. В большинстве случаев АГ они присутствуют одновременно, являясь наиболее частыми и постоянно встречающимися жалобами больных [4].
Один из вариантов начала АГ — появление лихорадки с внепеченочными проявлениями, из которых следует назвать аутоиммунный тиреоидит, язвенный колит, гипертиреоидизм, гемолитическая анемия, идеопатическая тромбоцитопения, сахарный диабет, целиакия, полимиозит, фиброзирующий альвеолит, гломерулонефрит и т. д. Желтуха при этом варианте появляется позже [20].
Часто АГ сопровождается бесплодием, однако при возникновении беременности и последующих родах на фоне компенсированного процесса это не влияет на течение АГ и судьбу ребенка даже при постоянном приеме преднизолона (ПР) [30]. Беременность на стадии сформировавшегося ЦП и синдрома портальной гипертензии, которые выявляются у трети больных на момент выявления АГ, нежелательна [3].
В отличие от ХВГ течение АГ у больных непрерывно прогрессирующее, без самопроизвольных ремиссий. Улучшения самочувствия бывают кратковременными, нормализации биохимических процессов не происходит. Прогноз течения АГ хуже у пациентов с острым началом болезни по типу ОВГ, с наличием признаков холестаза, асцитом, повторными эпизодами острой печеночной энцефалопатии (ОПЭ). Как правило, больные, пережившие критический период, имеют лучший прогноз.
Диагноз АГ выставляется на основании соответствия лабораторных и гистологических данных, отсутствия маркеров ВГ, исключения злоупотребления алкоголем и контактов с препаратами крови, гипотоксическими веществами, повышения гамма-глобулинов не менее чем в 1,5 раза выше нормы. Повреждение желчных протоков, отложение меди, гемосидероз, при которых также могут выявляться ЛГ и ступенчатые некрозы, предполагают другую причину ХГ и исключают диагноз АГ. ANA, SMA и LRM-1 должны быть в титрах не менее 1:80 у взрослых и 1:20 у детей (рекомендации Международной группы, 1993).
Дифференциальный диагноз между АГ и другими аутоиммунными заболеваниями, в основном первичным билиарным циррозом (ПБЦ), первичным склерозирующим холангитом (ПСХ), ХВГ основывается на клинических, гистологических и иммунологических параметрах. Однако нередко выявляется так называемый overlap-синдром, когда одновременно у пациентов выявляются признаки АГ и вышеперечисленных хронических заболеваний печени. Далее они будут описываться как варианты АГ [7, 13]. Предполагаемый диагноз АГ в данном случае подразумевает сходство с клиникой АГ (жалобы на слабость, арталгии, миалгии), а биохимический анализ крови отражает преимущественно изменения холестатического порядка, имеет место кожный зуд разной степени выраженности. Пациенты с такими вариантами АГ могут быть обоего пола, любого возраста, но все же чаще это женщины в возрасте до 40 лет и моложе. На гистологии находят перипортальный гепатит с или без ЛГ, часто с поражением желчных протоков, жировой дистрофией гепатоцитов и лимфоидной инфильтацией портальных трактов в виде гранулем [7, 10].
Деление АГ на подтипы практического значения не имеет, однако следует иметь в виду, что подтип 2 АГ может быть связан с гепатитом С либо HCV может индуцировать появление АГ у генетически предрасположенных лиц. Нет данных о различиях гистологической картины при отдельных подтипах АГ
Большинство больных с ПБЦ можно точно отделить от пациентов с АГ с помощью характерных лабораторных и иммунологических данных. Однако при этом варианте наряду с характерными параметрами АГ нередко выявляются гистологические признаки холангита и АМА (антитела к антигенам внутренней поверхности мембраны митохондрий), что очень характерно для ПБЦ. Наиболее важным для подтверждения диагноза ПБЦ является обнаружение АМА подтипа М2 [6]. АМА выявляются у 20-27% больных АГ в разных титрах [19]. Это может отражать диагностические ошибки в определении иммуносерологических маркеров, другие заболевания или одну из стадий ПБЦ. Если у больного повышена щелочная фосфатаза (ЩФ), IgM сыворотки крови и обнаружена АМА — вероятен диагноз ПБЦ. Трех-шестимесячный курс лечения стероидами помогает расшифровать преобладающую патологию — при реакции на лечение можно говорить о превалировании АГ.
Установлено, что у 16% больных АГ выявляется язвенный колит (ЯК), наличие которого характерно для пациентов с ПСХ (от 40 до 60% больных). К тому же при таком сочетании — АГ и признаки ПСХ (наличие ЯК, поражение желчных протоков, слабый ответ на стероиды) — также обнаруживают фенотип HLA-B8, HLADR3, HLA DR4. Поэтому наличие кожного зуда у больных АГ и повышение ЩФ более чем в четыре раза против нормы указывают на необходимость проведения холангиографии (ХГР) и вероятность развития варианта АГ и ПСХ. Поражения желчных протоков несовместимы с диагнозом АГ. Они редки, но когда появляются у больных АГ с сопутствующей патологией кишечника или атипичным повышением ЩФ, можно допустить этот вариант АГ. Окончательный диагноз зависит от результатов ХГР. ХГР выявляет признаки склерозирующего холагнита у 42% больных АГ и ЯК. Но иногда ХГР бывает в норме у 14% больных ПСХ при гистологически подтвержденном диагнозе. Об этом необходимо помнить [24].
АГ считается заболеванием невирусной этиологии, но у 4% больных АГ выявляются антиHCV и еще у 4% — маркеры вируса гепатита В. Больные АГ, имеющие атипичное течение болезни либо плохо отвечающие на терапию стероидами, нередко имеют в сыворотке крови HCV RNA. Любопытно, что 11% больных ХВГ имеют SMA и 28% — ANA. У 62% выявляются аутоантитела к щитовидной железе и ревматоидный фактор. Большая часть этих больных имеют низкие титры SMA и ANA (1:80 и ниже), а пациенты с точным диагнозом АГ — SMA в титрах 1:160 и ANA 1:320. Поэтому больные АГ и с выявляемыми SMA или ANA в титрах ниже 1:320 могут быть отнесены к группе с превалированием вирусного заболевания [11].
Тем не менее пациенты с АГ имеют более выраженную инфильтрацию портальных трактов плазматическими клетками, более выраженные воспалительные изменения в дольках и больше ступенчатых и перисептальных некрозов по сравнению с пациентами ХВГ, особенно ХГС. У больных ХВГ/ХГС наоборот — в портальных трактах преобладает лимфоидноклеточная инфильтрация, чаще выявляется стеатоз и повреждения желчных протоков, особенно при ХГС.
У 13% взрослых больных с признаками АГ не обнаруживаются аутоантитела, а все остальные признаки — иммунологические, биохимические и гистологические, а также возраст и пол соответствуют критериям постановки диагноза АГ. Что важно, эти больные также хорошо реагируют на лечение стероидами [8, 9]. Отмечено, что с течением времени при динамическом наблюдении у некоторых из них появляются соответствующие аутоантитела, характерные для АГ.
Несмотря на разнообразие клинической картины, при АГ основой лечения является назначение преднизолона (ПР). Ответ на данную терапию — один из критериев постановки диагноза АГ. Целесообразность назначения ПР при АГ доказана в многочисленных исследованиях и обусловлена редкими самопроизвольными ремиссиями в течении болезни, высокой смертностью и ухудшением качества жизни [12, 18, 23, 28, 29]. При назначении ПР смертность удается снизить в течение пяти лет с 50 до 20%, а частоту индуцированных ремиссий довести до 80%. У большинства больных ремиссии появляются в течение первых двух лет терапии и почти у всех в последующие четыре года лечения.
Лечение ПР следует назначать всем больным АГ высокой степени активности с фиброзом и циррозом или без. У больных с умеренной степенью активности болезни назначение ПР часто определяется наличием жалоб и симптомов болезни. Больные без симптомов и с умеренной степенью активности процесса по гистологической картине не нуждаются в лечении, но должны тщательно и регулярно наблюдаться для своевременного выявления признаков прогрессирования болезни.
Как правило, начальная доза ПР составляет 20-30 мг/сутки с последующим постепенным снижением ее до поддерживающей — обычно 10 мг/сутки. Из всех схем лечения предпочтителен ежедневный прием однократно утром. Осложнения терапии наблюдаются при дозе более 10 мг/сутки. Нет точных рекомендаций по отмене или снижению дозы иммуносупрессоров, некоторые больные могут долго оставаться в ремиссии после отмены ПР.
Однако было установлено, что у большей части больных в дальнейшем, даже спустя несколько лет после ремиссии, появляются признаки обострения и часто требуется большая доза для ее достижения [15].
Комбинация ПР с азатиоприном (АЗА) может уменьшить побочные эффекты (при этом требуется небольшая доза ПР). Лучше давать 10 мг/сутки ПР с 50 мг/сутки АЗА, чем один ПР, но в большей дозе. Сам АЗА не способен индуцировать ремиссию, но его добавление к ПР поддерживает ее даже в дозе 1 мг/кг/сутки. При неэффективности лечения АЗА назначали 6-меркаптопурин с хорошим эффектом [25]. У 20% больных АГ не удается достигнуть ремиссии — чаще всего у пациентов с признаками ЦП, лиц молодого возраста, при длительном анамнезе болезни до начала терапии ПР и у больных с фенотипом HLA-B8, DR3 [28]. Побочные эффекты при назначении иммунодепрессантов редкие, это в основном диспепсический синдром, сыпи, кушингоидизм, нарушение роста и развития у детей, сахарный диабет и остеопороз у женщин в менопаузе. АЗА может индуцировать миелосупрессию, возникновение катаракты, обладает онкогенным и, возможно, тератогенным эффектами.
Лечение вариантов АГ представляет определенные трудности. Основа терапии, препарат выбора для начала лечения — и здесь ПР. При сочетании АГ и ПБЦ назначают ПР в дозе 20 мг/сутки от трех до шести месяцев, а при отсутствии эффекта — урсодезоксихолевую кислоту (УДХК) или ее коммерческие препараты (урсофальк, урсосан, урсодиол и др.) по 13-15 мг/сутки от трех до шести месяцев.
Тактика лечения больных с вариантом АГ и ПСХ та же, что и при АГ и ПБЦ. Больные АГ и ЯК отвечают на терапию ПР хуже, чем больные с одним АГ (не столь часты ремиссии, чаще и быстрее выявляют прогрессирование к ЦП). Эти пациенты, возможно, должны лечиться УДХК большими дозами (до 15-20 мг/кг/сутки), если признаки холестаза выражены.
При сочетании АГ и ХВГ назначают ПР 20 мг/сутки или 10 мг/сутки ПР и 50 мг/сутки АЗА на три–шесть месяцев, если превалируют признаки АГ. Рекомбинантный ИФН в дозе 3 млн. МЕ/сутки три раза в неделю до 6 месяцев назначают при выявлении признаков ХВГ и маркеров репликации вируса либо неэффективности стероидной терапии [21, 5]. Лечение таких больных представляет собой сложную задачу, так как ПР усиливает вирусную репликацию, а ИФН может усилить иммуноопосредованный печеночно-клеточный некроз, перевести ХВГ в АГ, который до этого мог быть в латентном состоянии, обострить течение болезни с развитием внепеченочных аутоиммунных проявлений, индуцировать выброс антител с неясным клиническим значением. Поэтому лечение состоит в правильном определении преобладания тех или иных клинических синдромов или признаков. В любом случае обострение болезни печени или внезапное появление признаков аутоиммунного заболевания у пациентов с признаками АГ, но с преобладанием вирусного поражения указывает на необходимость прерывания лечения ИФН.
Тактика лечения больных криптогенным ХГ состоит в назначении ПР 10-20 мг/сутки вместе с 50 мг/сутки АЗА до появления ремиссии или максимального эффекта.
Литература

Белки (протеины) — это крупномолекулярные вещества, которые принимают участие в формировании тканей и течении биохимических реакций, а также передают сигналы в организме между клетками. Они входят в состав всех биологических жидкостей, поддерживают осмотическое давление крови и кислотно-основное равновесие (рН)¹. Антитела, которые организм вырабатывает в ответ на повреждение или инфекцию, также являются белковыми образованиями — иммуноглобулинами. Общий белок в крови (T-Prot) входит в перечень стандартных биохимических исследований. Анализ показывает количественное содержание всех протеинов (альбумины, глобулины), которые циркулируют в плазме¹ крови. В этой статье мы расскажем, когда врач может назначить проведение теста и как расшифровать полученные результаты.
Синонимы: Total Protein (TProt, ТР, T-Prot), Serum Total Protein, общий белок сыворотки крови, общий сывороточный белок.
Анализ крови на общий белок
Определение концентрации белков в плазме дает важную информацию об общем состоянии здоровья, функционировании жизненно важных органов и течении патологических процессов. Анализ сдается в рамках биохимического исследования крови, в который также входят холестерин, печеночные пробы, почечные показатели и глюкоза (измеряются в ммоль/л)¹.
Белки крови — особая буферная система, которая поддерживает кислотно-основное равновесие плазмы в оптимальном состоянии — рН 7,37-7,43.² Они также влияют на вязкость и свертываемость крови.
В биохимическом анализе показатель обозначается как общий белок в крови (T-Prot) или Total Protein. Результат лаборатории приводят в граммах на литр (г/л). В развернутом исследовании подсчитывают количество и процентное соотношение разных белковых фракций (протеинограмма)². Для анализа берут кровь из локтевой вены или вены тыльной стороны ладони.
На долю протеинов приходится 6,5-8,5% от всего сухого остатка плазмы (9-10%)¹. Концентрация зависит от скорости их синтеза и разрушения, а также объема распределения в телесных жидкостях и тканях. Показатель может меняться в течение дня, после физической нагрузки и обильного приема пищи.
На анализ пациентов направляет терапевт или врач любой другой специальности, так как общий белок не является специфическим показателем. Нарушения белкового обмена встречаются при любом воспалении, инфекциях, заболеваниях внутренних органов и онкологии. В редких случаях пациенты имеют врожденные нарушения выработки протеинов.
Показания к анализу
Исследование общего белка в крови могут назначить по таким показаниям³:
- общеклинический медицинский осмотр;
- первичный поиск патологии обменных процессов (метаболизма);
- необъяснимая потеря веса;
- отеки конечностей, лица;
- утомляемость и резкая слабость, не соответствующая нагрузке;
- необъяснимая одышка;
- появление жалоб со стороны печени или почек: хроническая усталость, артериальная гипертензия, увеличение живота в объеме за счет внутрибрюшной жидкости, желтуха, бледность кожи, изменение суточного характера мочеиспускания;
- проблемы с питанием, включая расстройства пищевого поведения (анорексия, булимия);
- подозрение на беременность;
- наличие признаков истощения;
- профилактический осмотр для спортсменов, рабочих на тяжелых производствах;
- контроль лечения или хода заболеваний внутренних органов;
- подготовка к любому оперативному вмешательству.
Тестирование на общий белок в крови — первый шаг в диагностике многих заболеваний внутренних органов и обменных нарушений. При отклонении значений больного направляют на уточняющие анализы: определение альбумина или всех белковых фракций (протеинограмма), лейкоцитарная формула, скорость оседания эритроцитов (СОЭ), гематокрит².
Подготовка к анализу
Посещение лаборатории нужно спланировать заранее, так как от качества подготовки зависит информативность лабораторного заключения. Накануне необходимо соблюдать следующие правила³:
- за сутки до исследования отказаться от спиртных напитков, тяжелой физической нагрузки и приостановить прием лекарственных препаратов (после согласования с лечащим врачом);
- за 2-3 дня до проведения теста ограничить употребление жирной пищи, копченостей, солений, кондитерских изделий;
- несколько дней перед манипуляцией не посещать бани, сауны, солярий, а накануне заменить горячую ванну на гигиенический душ;
- в течение 3 часов перед сдачей крови не курить, избегать психоэмоциональных перегрузок;
- за 15 минут до сдачи крови нужно успокоиться и отдохнуть;
- последний прием пищи за 12 часов — накануне вечером в виде легкого ужина;
- утром можно пить только воду (под запретом даже соки и жевательные резинки).

Общий белок в крови — суммарный показатель всех протеинов. Может показывать ложные результаты при неправильной подготовке, обезвоживании, после физической нагрузки. Также не дает информации об изолированном изменении соотношения разных фракций — альбуминов, глобулинов³.
На содержание протеинов также оказывают влияние следующие факторы³:
- фармацевтические средства с половыми гормонами в составе (тестостерон, эстрогены, оральные контрацептивы), фенотиазины;
- высокая физическая активность может временно повысить концентрацию до 10%;
- особенности питания (например, у вегетарианцев, не принимающих специальные пищевые добавки, обнаруживается меньше циркулирующих белков в сыворотке);
- беременность;
- окружающая среда — у людей, которые проживают в теплых странах, больше иммуноглобулинов, чем у жителей холодного климата;
- повреждение внутренних органов приводит к массивной потере белковой части;
- изменение объема циркулирующей крови;
- любое воспаление;
- неправильное хранение реактивов и биологического материала;
- погрешность конкретного метода исследования;
- способ забора материала — длительное наложение жгута перед взятием крови из вены повышает количество белка в сыворотке.

Концентрация белков в плазме непостоянна и быстро меняется в течение дня под воздействием внешних факторов. Она увеличивается на 10-20%, если резко встать после длительного лежания и затем сдать анализ через 30 минут.
Исследование проводят натощак, в утренние часы. Не стоит посещать лабораторию после массажа или физиотерапевтических процедур. Любые воздействия на организм, в том числе рентгенологические, перед анализом должны быть исключены³.
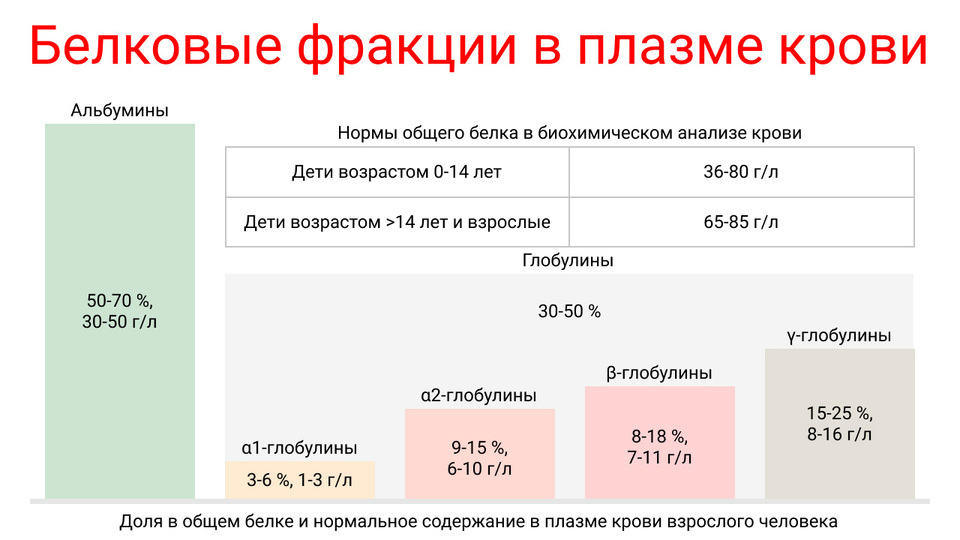
Рисунок 1. Норма общего белка и его фракций. Источник: МедПортал
Нормы белка в крови
Показатели нормы у детей и взрослых отличаются. Нормы (референсные значения) в каждой лаборатории устанавливают свои, что зависит от аппаратного оснащения и методики проведения теста. Поэтому для контроля эффективности назначенной терапии рекомендуют пользоваться услугами одного лечебного или диагностического учреждения.
Женщины и мужчины не имеют значимой клинической разницы в нормах белка крови⁵. Примерно к трехлетнему возрасту количество протеинов в сыворотке у детей и взрослых становится почти одинаковым.
Белки в организме человека вырабатываются и распадаются непрерывно: происходит постоянное их обновление. Кроме гормональных и физических факторов, на этот процесс оказывают влияние характер питания, наследственность, наличие сопутствующих заболеваний.

Нормы могут несущественно отклоняться у здоровых женщин при менструальном кровотечении, в период беременности и кормлении грудью. Снижение общего белка до 55-65 г/л при вынашивании ребенка не считается патологией³.
Альбумин
Общий белок на 50-70% состоит из альбуминов, от которых зависит онкотическое давление плазмы². При их изолированном снижении (гипоальбуминемия) жидкость выходит из сосудистого русла в ткани и полости тела, не возвращаясь обратно. Этот же механизм лежит в основе развития голодных отеков.
Альбумин выполняет транспортную функцию, обеспечивает клетки необходимыми аминокислотами и принимает участие в поддержании постоянства внутренней среды. Нормальное содержание альбумина в плазме взрослого человека — 30-50 г/л.² За сутки клетки печени вырабатывают примерно 12 г этого белка².
Глобулины
Молекулы глобулинов имеют большую молекулярную массу, чем альбумины и хуже растворяются в воде. К ним относятся специфические белки сыворотки, ферменты, гормоны, антитела (иммуноглобулины). Синтезируются в печени и иммунокомпетентных органах.
Общий белок почти на 35-50% состоит из глобулинов. Ниже представлены нормальные значения для основных фракций²:
При изменении соотношения сывороточных белков развивается диспротеинемия. Каждая из фракций имеет свои функции и свойства, поэтому по отклонению их количества можно заподозрить причину нарушений или даже конкретное заболевание.
Выраженность диспротеинемии оценивают с помощью альбумин-глобулинового коэффициента (отношение фракций). У здоровых людей это значение не превышает 2,5-3,5. При циррозе печени или хроническом гепатите показатель снижается до 1-1,5 из-за нарушения выработки альбуминов в печеночных клетках¹.
Причины повышенного белка
Увеличение количества сывороточных белков называют гиперпротеинемией. Она бывает абсолютной (нарушение выработки протеинов из-за повреждения органов) и относительной (связана с изменением объема плазмы).
Возможные причины гиперпротеинемии²:
- тяжелое обезвоживание (профузные поносы и/или рвота, кетоацидоз при сахарном диабете, недостаточное потребление воды, массивное потоотделение);
- обширные ожоги;
- аутоиммунные заболевания, при которых организм начинает вырабатывать большое количество белковых иммуноглобулинов, атакующих собственные органы (ревматизм, системная красная волчанка, саркоидоз);
- лимфома Ходжкина (лимфогранулематоз) — злокачественное поражение лимфоидных тканей;
- опухоли крови и лимфатической системы;
- хронический гепатит в активной фазе;
- цирроз печени на начальных стадиях;
- макроглобулинемия Вальденстрема — опухоль, преимущественно поражающая костный мозг, при которой вырабатывается большое количество моноклонального иммуноглобулина М (IgM);
- перитонит — активное воспаление листков брюшины;
- кишечная непроходимость;
- патология почек в фазе полиурии (избыточного мочеиспускания);
- холера — острое инфекционное заболевание (особо опасное), сопровождающееся поражением тонкой кишки, массивной диареей, рвотой и сильным обезвоживанием организма;
- острые и хронические инфекции.

Тяжелая гиперпротеинемия приводит к нарушению вязкости крови и неправильной ее циркуляции по сосудам. Наиболее опасный исход — синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), при котором тромбозы чередуются с кровотечением.
Причины пониженного белка
Гипопротеинемия — уменьшение концентрации протеинов в крови. Чаще всего связана с непосредственной потерей белков, голоданием или угнетением их синтеза, то есть выработки в органах.
После операции количество белка в крови снижено. Фото: photography33 / Depositphotos
Различают такие причины гипопротеинемии¹:
- ожоговая болезнь;
- длительный перегрев тела (гипертермия), включая лихорадочные состояния;
- сахарный диабет;
- кровотечения;
- тиреотоксикоз — гиперфункция щитовидной железы;
- длительная физическая нагрузка;
- восстановление после операций;
- онкологические заболевания;
- повреждение почек с развитием нефротического синдрома;
- потеря белка при воспалении слизистой оболочки кишечника (энтерит);
- поражение печени с признаками клеточной недостаточности при гепатитах, циррозе, отравлении (токсическими веществами, алкоголем, медицинскими препаратами);
- недостаточное поступление белка с пищей голодание, изнуряющие диеты, строгое вегетарианство);
- нарушение усвоения белковой пищи при панкреатитах (воспаление поджелудочной железы), резекции кишечника (синдром мальабсорбции);
- усиленный распад протеинов вследствие травм, инфекционных заболеваний, синдрома Кушинга;
- воспалительные заболевания кишечника;
- перемещение белков из сосудистого русла в брюшную (асцит) или плевральную полость (плеврит);
- тяжелая сердечная недостаточность;
- неадекватный объем инфузионной терапии через капельницы, в результате чего резко увеличивается циркулирующей крови;
- синдром Пархона (несахарный антидиабет) — нарушение продукции вазопрессина из-за гиперфункции гипоталамо-гипофизарной системы в головном мозге;
- врожденный дефицит гамма-глобулинов или других белковых фракций.
Уменьшение белковой части плазмы может понижать онкотическое давление, вследствие чего развиваются отеки. Жидкость переходит из сосудов в ткани и полости тела. При этом нарушается питание сосудистой стенки и свертываемость крови.

Уровень общего белка менее 40 г/л опасен для жизни³!
К лечению приступают после выяснения причины отклонения от нормы. Медикаментозную терапию подбирает лечащий врач в соответствии с диагнозом, тяжестью состояния больного, сопутствующими заболеваниями.
Как снизить или повысить белок в крови
Лечебные диеты с повышенным или пониженным содержанием протеинов подбирает врач-диетолог в соответствии с диагнозом пациента. При незначительных отклонениях от нормы проблему можно решить самостоятельной коррекцией рациона.
Какие продукты повышают белок в крови
Высокобелковая диета подразумевает употребление 110-120 г белка в сутки⁶. Назначается больным с сахарным диабетом, болезнями почек, тяжелой анемии и при сепсисе.

Продукты животного происхождения (молочные продукты, мясо и рыба) — естественный источник протеинов и незаменимых аминокислот, который усваивается более чем на 90%. Они должны составлять 50% от общего количества белка в суточном рационе взрослого человека, 60% — у детей⁷.
В рацион включают следующие легкоусвояемые источники протеинов:
- нежирная говядина, телятина;
- кролик;
- курица без кожи;
- индейка;
- отварной язык;
- обрезная свинина без жира;
- умеренно жирные сорта рыб, лучше — морской или красной;
- молоко;
- кисломолочные напитки;
- творог;
- сметана;
- твердый сыр;
- яйца (куриные, перепелиные);
- бобовые в виде круп, в составе салатов;
- грибы (при нормальной переносимости);
- киноа;
- семечки, кунжут;
- тофу;
- орехи;
- соевое молоко;
- зеленые овощи.
Какие продукты снижают белок в крови
Когда уровень общего протеина в сыворотке повышен, придерживаются низкобелковой диеты. Потребление белков временно ограничивают до 20-60 г/сут вплоть до нормализации его уровня по результатам контрольного анализа крови. Полностью исключать белки из рациона без консультации врача нельзя.
Низкобелковое питание показано при тяжелом циррозе печени и хронической почечной недостаточности. В качестве компенсации рацион обогащается витаминами и минеральными веществами. Обильное питье естественным образом может понижать белок (ягодные морсы, компоты, чаи). При острой необходимости красное мясо заменяют белым (филе птицы) на фоне большого количества овощей и фруктов.
Заключение
Определение общего белка входит в стандартный биохимический анализ крови. Показатели комплексно оценивает лечащий врач, который направил больного на исследование. Незначительное отклонение от нормы зачастую не требует медикаментозной коррекции, но может подсказать, в каком направлении нужно продолжить диагностический поиск. Тяжелые нарушения белкового обмена всегда сопровождаются проявлениями причинно-значимого заболевания. Лабораторные данные вместе с клинической картиной являются основанием для постановки окончательного диагноза.
Симптомы проблем с печенью
Заподозрить развитие заболеваний печени можно по появлению таких симптомов³:
Виды заболеваний печени
Печень, желчевыводящие пути и желчный пузырь — единый комплекс, работающий сообща. Его называют гепатобилиарной системой. Поражение этой системы встречается при следующих заболеваниях:
- Функциональные: нарушения обмена билирубина (синдром Жильбера), холестаз беременных.
- Диффузные: гепатит — воспаление печеночных клеток (острое или хроническое), которое иногда может трансформироваться в цирроз (необратимое замещение нормальной ткани на рубцовую) при отсутствии своевременного лечения.
- Инфильтративные (с очаговым поражением): гранулематозы (туберкулез, саркоидоз), амилоидоз (нарушение белкового обмена), избыточное накопление жира (алкогольная болезнь печени, сахарный диабет), заболевания крови, гликогенозы.
- Объемные новообразования: кисты, абсцессы, доброкачественные опухоли, рак (гепатоцеллюлярная карцинома), метастазы.
- Печеночно-билиарные: воспаление желчных протоков (холангит), их обструкция при желчнокаменной болезни.
- Сосудистые: тромбоз печеночных вен, венозный застой в печени при тяжелой патологии сердца и легких.

Большинство хронических заболеваний печени в течение многих лет никак не проявляют себя¹. Появление выраженной симптоматики указывает на серьезное повреждение органа, запущенный патологический процесс.
Классификация препаратов для восстановления печени
Гепатопротекторы — это препараты для восстановления печени. Они бывают следующих типов⁴:
- содержащие компоненты растительного происхождения (расторопши, солодки, артишока);
- животного происхождения;
- с эссенциальными фосфолипидами;
- с детоксикационными свойствами;
- препараты желчных кислот;
- лекарства, в составе которых есть другие действующие вещества синтетического происхождения.

Основная масса гепатопротекторов не имеет доказательной базы и применяется только на территории СНГ. Зарубежная медицина не признает вещества, которые в России позиционируются как лучшие препараты для восстановления печени.
Восстановление печени зависит в первую очередь от своевременного устранения повреждающего фактора¹. Поэтому применение гепатопротекторов при лечении заболеваний печени носит вспомогательный характер.
Профилактика заболеваний печени — лучшее, что можно для нее сделать. Следует отказаться от курения и алкоголя, заниматься регулярной физической активностью³. Также не нужно забывать о вакцинации против вирусов гепатита (А,В), инфекции COVID-19.
ТОП препаратов для восстановления печени
В рейтинг препаратов, которые применяют в России для восстановления печени, входят следующие лекарства.
1. Карсил (Легалон, Форливер)
Экстракты расторопши, включая силимарин. Они незначительно стимулируют синтез белков, стабилизируют мембраны печеночных клеток (гепатоцитов), защищая их от повреждения. В инструкцию к применению указано, что препарат обладает антиоксидантными свойствами, усиливает восстановление тканей, тормозит процесс фиброза (замещение нормальной ткани на соединительную — рубцовую)⁴.
Однако механизм действия до конца не изучен, доказательная база сомнительная. В клинической практике эффективность сопоставима с эффектом плацебо.
Противопоказания и особые указания. Таблетки с экстрактами расторопши применяются в качестве вспомогательных лекарств при алкогольных, лекарственных гепатитах. Нельзя использовать их в качестве основного лечения. Умеренно усиливают выброс желчи, что может быть опасно при наличии камней в желчном пузыре.
2. Хофитол
Экстракт листьев артишока. Повышает антитоксические функции печени, стимулирует выработку нормальных ферментов и регенерацию тканей. Имеет выраженное желчегонное действие⁴.
Противопоказания и особые указания. Механизм действия изучен плохо, как и состав таблеток. Использование категорически запрещено при желчнокаменной болезни, острых заболеваниях печени и почек. В высоких дозах может вызывать диарею.
3. Гептрал
Адеметионин. Молекула, которая состоит из аминокислоты метионина и АТФ (источник энергии). В норме присутствует в тканях организма.
Адеметионин — эффективное лекарство для восстановления печени, которое увеличивает концентрацию глутатиона (природный антиоксидант) в клетках. При курсовом использовании способствует быстрому снижению биохимических показателей (АСТ, АЛТ) в крови, оказывает незначительное успокаивающее действие. Часто применяется при алкогольном и токсическом повреждении печени².
Противопоказания и особые указания. Клиническая эффективность остается спорной, поэтому исследования полезных свойств адеметионина продолжаются. Этот препарат не помогает в случае необратимых изменений (фиброз, цирроз).
4. Фосфоглив
Эссенциальные фосфолипиды. В теории восстанавливают мембраны клеток, оказывают антиоксидантный эффект. Но при приеме внутрь биодоступность низкая, то есть препараты могут вообще не попасть в печень.
Противопоказания и особые указания. Нормальная доказательная база отсутствует². Запрещен при беременности и антифосфолипидном синдроме.
5. Урсосан
Урсодезоксихолевая кислота. Улучшает текучесть желчи, предупреждает образование камней в желчном пузыре. Снижает токсичность желчных кислот по отношению к печеночным клеткам, принимает участие в иммунологической защите. Один из немногих гепатопротекторов с доказанной эффективностью⁵.
При длительном приеме может растворить мелкие камни в желчном пузыре. Показан при забросах (рефлюкс) желчи из двенадцатиперстной кишки в желудок, лечении первичного билиарного цирроза (компенсированного).
Противопоказания и особые указания. Ожидаемый побочный эффект от использования в правильно подобранных дозах — жидкий стул. Запрещен при острых воспалительных заболеваниях органов брюшной полости, кальцинированных камнях желчного пузыря, декомпенсации заболеваний печени и почек.
6. Гепа-Мерц
Орнитина аспартат. Связывает избыточный аммиак, который выделяется в большом количестве при тяжелом поражении печени (цирроз). Стимулирует обмен белков, выработку инсулина и соматотропного гормона. Увеличивает устойчивость клеток к действию повреждающих факторов².

Здоровая печень — здоровый мозг
Если уровень аммиака выходит из-под контроля, развивается печеночная энцефалопатия. У человека замедляются мыслительные способности, страдают когнитивные функции и внимание. В тяжелых случаях развивается кома. То есть для исправной работы головного мозга нужна здоровая печень.
Противопоказания и особые указания. Не подходит для лечения детей, женщин в период лактации и больных с тяжелой почечной недостаточностью.
7. Витамины группы В и Е
Универсальные защитники клеточных мембран, оказывают антиоксидантное действие. Рекомендуется поступление не в виде синтетических добавок, а из продуктов питания — растительных масел, свежих овощей, фруктов, орехов, семян².
Противопоказания и особые указания. На синтетические витамины нередко бывают аллергические реакции.
8. Метадоксил
Метадоксин. Усиливает метаболизм, выведение спиртов из организма, уменьшает токсическое воздействие этанола⁴. Используется при комплексном лечении алкогольной болезни печени. Лекарственная форма — таблетки. Дозу и кратность приема устанавливает врач.
Противопоказания и особые указания. Нельзя применять беременным и кормящим женщинам. Возможна индивидуальная непереносимость.

9. Берлитион
Альфа-липоевая (тиоктовая) кислота. Природный антиоксидант, который часто применяют с целью детоксикации при отравлениях. Показан при алкогольной и диабетической полиневропатии.
Противопоказания и особые указания. Усиливает действие сахароснижающих средств, способствует уменьшению концентрации глюкозы в крови. Запрещен женщинам во время беременности и лактации, детям.
10. Реамберин
Меглюмина натрия сукцинат. Дезинтоксикационное средство для внутривенного капельного введения.
Противопоказания и особые указания. Запрещен при беременности, выраженном отечном синдроме, хроническом повреждении почек.
11. Янтарная кислота
Противопоказания и особые указания. Возможны аллергические реакции.
12. Обелива
Обетихолевая кислота. Применяется вместе с урсодезоксихолевой кислотой для лечения неалкогольной жировой болезни печени, первичного билиарного холангита, сахарного диабета. Одобрена Управлением по санитарному надзору США (FDA)⁵.
Противопоказания и особые указания. Запрещен при полной билиарной обструкции.
13. Ацетилцистеин
N-ацетил L-цистеин (NAC). Антидот при отравлении парацетамолом с доказанной эффективностью. Совместно с глюкокортикостероидами может назначаться при других лекарственных гепатитах.
Противопоказания и особые указания. Нельзя использовать в период кровотечения из язвы желудка и двенадцатиперстной кишки, легких, а также детям до 2 лет.
14. Преднизолон (и/или другие глюкокортикостероиды)
Применяется при аутоиммунных и алкогольных гепатитах, лекарственном поражении печени, эозинофилии. Нередко назначается в комбинации с цитостатиками (азатиоприн).
Противопоказания и особые указания. Имеет обширный список противопоказаний — от язвенной болезни до тяжелого сахарного диабета. Лечение проводят под наблюдением врача вплоть до достижения стойкой ремиссии, которую также нередко поддерживают гормонами.
15. Розувастатин (и/или другие статины).
Противопоказания и особые указания. Не подходит для больных с непереносимостью лактозы, детям до 18 лет, беременным, кормящим женщинам, а также при тяжелом нарушении функций печени и почек.

Способность к быстрому самовосстановлению делает печень пригодной для обширной трансплантации. Она сможет полностью регенерировать даже, если останется всего 25% от ее изначальной массы³.
Заключение
Лучшие таблетки для восстановления печени — те, которые врач назначает для устранения основной причины заболевания. К ним относятся противовирусные средства при инфекционных гепатитах (В,С), глюкокортикостероиды при аутоиммунном поражении, антидоты при специфических отравлениях, фармацевтическая терапия алкоголизма. Гепатопротекторы приводят только к симптоматическому улучшению, что является временным решением. Радикально повлиять на работу печени они не смогут.
Читайте также:

