Как происходит внутриутробное заражение герпесом
Обновлено: 24.04.2024
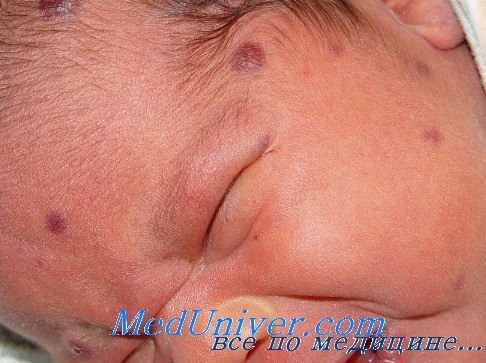
Пример внутриутробной смешанной ЦМВ и герпес инфекции у новорожденного ребенка
Перинатальная вирусная инфекция смешанной этиологии характеризуется выраженной общеинфекционной симптоматикой, гипотрофией, персистирующим течением с обострениями, периодами лихорадки, диспептических явлений, полиорганной патологией, резистентностью к терапии.
В качестве типичного клинического примера Н.И. Михайловская приводит сведения о ребенке Д.
Девочка Д. (дата рождения 26.06.2004 года, история болезни 1969/2004). Клинический диагноз: Перинатальная персистирующая смешанная инфекция — цитомегаловирусная и вируса герпеса 6 типа, фаза репликации (перинатальное поражение ЦНС, гепатит, гипотрофия, анемия, кардиопатия).
Ребенок от 4 беременности, протекавшей гестозом и угрозой прерывания на протяжении всей беременности. Первая беременность закончилась самопрооизволь-ным выкидышем, вторая — срочными родами, третья — медицинским абортом. Девочка родилась в срок с признаками внутриутробной гипотрофии (вес 2550,0, длина 51 см), перинатальной энцефалопатии, с желтухой. С рождения получала лечение у невропатолога. В возрасте 3 месяцев (27.09) вес — 5 100,0, жалоб на ребенка не было. Сделана первая вакцинация АКДС и полиомиелита. Спустя сутки мама стала обращаться к специалистам по поводу выраженного беспокойства, нарушения сна, отказа ребенка от еды, упорного срыгивания, потери веса.
В возрасте 3,5 месяца госпитализирована в Детскую областную больницу, где выявлено повышение активности печеночных ферментов: АЛТ — 240 ед, ACT— 126 ед. Госпитализирована в Центр гепатологии, где у ребенка и у мамы исключена инфекция вирусов гепатитов А, В, С, D, anti-HIV, RW отрицательны. При исследовании в Центре молекулярной диагностики ЦНИИЭ МЗ РФ у ребенка обнаружены anti-CMV IgG в концентрации 93 ME /мл (при допустимой > 10,0). Анемия: НВ — 92 г/л гипохромия, анизоцитоз. УЗИ — гепатомегалия, стенки сосудов печени подчеркнуты, добавочная долька селезенки. НСГ — четвертый желудочек расширен, углублен, глубина передних рогов — 7 мм, умеренная дилятация боковых желудочков головного мозга.
Диагностирована перинатальная цитомегаловирусная инфекция (поражение ЦНС — энцефалопатия с признаками вялотекущего энцефалита, гепатит, анемия). Проведены курсы противовирусной терапии (виферон, ацикловир), ликопида, гепатопротекторов, ак-тиферрина, выполнены назначения невропатолога. При обследовании в возрасте 5,5 месяцев (1.12.04) все функциональные пробы печени в норме. Повторно госпитализирована в возрасте 7 месяцев 8.02.2005 года. Со слов мамы за 3 недели до госпитализации — вакцинация против полиомиелита, после чего внезапное резкое ухудшение состояния, отказ от еды, потеря в весе. При поступлении состояние ребенка средней тяжести за счет интоксикации. Девочка вяла, беспокойна, не интересуется окружающим, крик монотонный, эмоционально не окрашен. Кожа бледна, с сероватым оттенком. Печень на 3—4—3 см выступает из подреберья, плотновата, болезненна, селезенка до 2 см.
Со стороны функциональных проб печени — резкое повышение активности цитолитических ферментов — АЛТ до 9 норм, ACT до 3 норм. Концентрация anti-CMV IgG повысилась до 177!! МЕ/мл. Для уточнения диагноза и тактики лечения девочка госпитализирована в Республиканскую детскую клиническую больницу. При обследовании выявлены маркеры смешанной вирусной внутриутробной инфекции: anti-CMV IgG 168 МЕ/мл, DNA CMV обнаружена в моче и слюне, DNA V. Herpes 6 типа — в крови. Микробиологическое исследование кала: лактозонегативная кишечная палочка (кп) 0, гемолизирующая кп 10* 9, обнаружены золотистый стафилококк, грибы рода Кандида, Клебсиелла, Цитробактер в высоких разведениях.
Допплерография печени и портальной системы — внутрипеченочные желчные протоки с фрагментарно уплотненными стенками. Стенки внутриорганного бассейна равномерно утолщены. УЗИ — Селезенка на верхней границе нормы, подчеркнут рисунок сосудов, почки — ЧЛК с уплотненными стенками. Специалистами РДКБ была назначена терапия: виферон по схеме не менее 6 месяцев, траумель по 1 /2 таблетки 3 раза между едой + хепель по 1 /2 таблетки 3 раза за 30 минут до еды, курсами по 2 месяца с перерывом в 1 месяц, поливалентный бактериофаг 2 курса по 4 дня, по схеме абомин, креон, гомеопатические препараты. Назначения невропатолога включали фенибут. Общее состояние и самочувствие ребенка улучшились, снизилась активности АЛТ и ACT (до 2—3 норм). Однако в возрасте 11 месяцев — вновь беспокойство, нарушение сна, снижение аппетита. За 5 месяцев девочка прибавила в весе лишь 700,0: вес в возрасте 6 месяцев— 7 500,0, в 8 месяцев— 7 300,0, в 9 месяцев — 7 000,0, в 11 месяцев — 8 200,0.
При поступлении в стационар состояние ребенка средней тяжести, явления интоксикации, клинико-лабораторная симптоматика гепатита.
Активность ферментов повысилась до 8 норм, появилась биохимическая симптоматика внутрипеченочного холестаза. Маркеры вирусов гепатитов А, В, С, D отрицательны. В анализах мочи — изостенурия, лейкоциты до 20 в поле зрения. Выписана с улучшением, с тенденцией к нормализации активности ферментов. Однако болезнь приняла хроническое течение, на фоне признаков вторичного иммунодефицитного состояния. Ребенок повторно направлен в РДКБ.
Таким образом, внутриутробная инфекция смешанной вирусной этиологии — цитомегаловирусная и вируса герпеса 6 типа — протекала у ребенка с признаками полиорганной патологии, приняла хроническое течение, осложнилась проявлениями вторичного иммунодефицитного состояния. Фактором, провоцирующим обострение в возрасте трех и шести месяцев, была вакцинация. Детям с признаками перинатальной вирусной инфекции показан медицинский отвод от живых вакцин сроком не менее 2 лет.
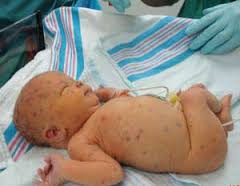
Врожденный герпес – герпетическая инфекция, встречающаяся у новорожденных при антенатальном или интранатальном заражении от инфицированной матери. Характеризуется специфическими кожными проявлениями в виде везикулярной сыпи, которая может также располагаться на слизистых оболочках глаз, рта, внутренних органов. Часто развивается герпетический энцефалит с очаговой симптоматикой и судорогами. Патологические изменения отмечаются в печени, селезенке, легких, почках и других органах. Врожденный герпес диагностируется на основании результатов серологических, гистологических исследований, а также выявления частиц вируса. Лечение – противовирусные препараты, иммуномодуляторы, иммуноглобулины, витаминотерапия.
Общие сведения
Врожденный герпес является одним из множества вариантов герпетической инфекции, к которой также относятся цитомегалия, ветряная оспа, внезапная экзантема детей и другие нозологии. Частота встречаемости заболевания – 1 случай на 2,5-60 тыс. новорожденных. Предположительно, такой разброс статистических данных связан с низкой выявляемостью в развивающихся странах. Врожденный герпес имеет высокую значимость в педиатрии в связи с ростом заболеваемости, а также увеличением случаев рецидивирующего течения. Это обусловлено тем, что вирусом простого герпеса инфицировано практически все население планеты, а сам вирус постоянно претерпевает значительные мутации. Кроме того, низкая специфичность симптомов часто является причиной запоздалой диагностики, что, в свою очередь, представляет опасность для жизни ребенка.

Причины и классификация врожденного герпеса
Возбудитель заболевания – вирус простого герпеса человека. Известно множество типов данного вируса, однако врожденный герпес в 80% случаев вызывается вирусом 2 типа, который также известен как генитальный герпес. Оставшиеся 20% в структуре заболеваемости приходятся на долю вируса простого герпеса 1 типа. Заражение чаще всего происходит интранатально, при прохождении плода по инфицированным родовым путям. Реже врожденный герпес развивается еще в утробе, попадая в организм малыша через плаценту. В этом случае речь идет о наиболее тяжелом течении заболевания, результатом чего обычно является выкидыш или рождение ребенка с разной степенью недоношенности и тяжелыми пороками развития.
Заболевание может протекать в нескольких формах, которые отражают доминирующие клинические проявления. Выделяют 3 формы врожденного герпеса: локализованную, церебральную и генерализованную. Первая из них представлена характерными кожными высыпаниями, и именно этот симптом является ведущим. Церебральная форма, как правило, проявляется менингитом и энцефалитом герпетической природы. Генерализованный врожденный герпес у новорожденных достаточно часто развивается вследствие несовершенства иммунного ответа и сопровождается симптомами со стороны внутренних органов. Мозговые нарушения и кожные элементы также присутствуют.
Симптомы врожденного герпеса
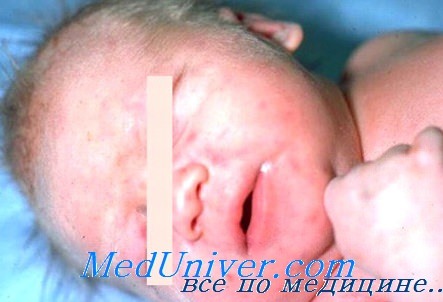
Как уже было сказано выше, симптоматика различается в зависимости от формы заболевания. Чаще всего врожденный герпес дебютирует на 7-14 день жизни. Время появления первых клинических признаков зависит от многих факторов: сроки гестации, срока инфицирования, сопутствующей патологии и т. д. Примерно в половине случаев врожденный герпес проявляется специфической для данной нозологии везикулярной сыпью. Мелкие пузырьки с серозным содержимым могут локализоваться на любой части тела, при этом элементы располагаются группами, образуя скопления и иногда сливаясь. Везикулы окружены кольцом гиперемии и отека, за счет чего они слегка приподнимаются над кожей. Характерно поражение слизистой оболочки глаз в виде кератитов и конъюнктивитов.
Часто содержимое кожных элементов в короткие сроки становится геморрагическим или гнойным. После вскрытия на месте пузырьков остаются эрозии, заживающие путем образования корочки. Общее состояние малыша может ухудшаться незначительно, температура повышается до субфебрильных значений. Исключение составляют случаи так называемого первичного врожденного герпеса, представляющего собой локализованную форму заболевания и проявляющегося обильной сыпью, элементы которой часто сливаются, оставляя после вскрытия обширные эрозии. Температура высокая, высыпания присутствуют не только на коже, но и на слизистых. В отсутствие своевременной терапии генерализация происходит в 50% случаев.
Церебральная форма врожденного герпеса проявляется менингеальной симптоматикой при отсутствии поражения кожи. Иногда везикулярная сыпь возникает позже, спустя примерно неделю после дебюта мозговых нарушений, но элементов сыпи в этом случае всегда немного. На первый план выходят симптомы менингита и энцефалита: нарушения сознания, эпилептиформные, тонические и тонико-клонические судороги. Симптомы неспецифичны, поэтому герпетический энцефалит легко спутать с энцефалитом любой другой природы. Значительная интоксикация ухудшает состояние, однако у новорожденных лихорадка может быть не выражена. Также присутствуют признаки отека мозга, что проявляется стволовыми нарушениями: дисфагией, расстройствами дыхания и пр.
Генерализованная форма врожденного герпеса является самой опасной. Она включает в себя и элементы сыпи, и церебральную симптоматику, описанную выше. Помимо этого, заболевание проявляется поражением внутренних органов: гепатоспленомегалией, пневмонией, специфическими изменениями в почках и надпочечниках. Явления токсикоза выражены в значительной степени. Смертность при генерализованной форме врожденного герпеса составляет более 50%, а по некоторым данным достигает 80-90% случаев, при этом половина выживших детей остаются глубокими инвалидами. Медленный регресс общемозговых и очаговых расстройств и их частая необратимость являются особенностью герпетической инфекции.
Диагностика врожденного герпеса
Выявление заболевания сопряжено для педиатра со значительными трудностями. Во-первых, если отсутствуют кожные проявления, то врожденный герпес можно заподозрить с той же вероятностью, что и многие другие патологии неонатального периода, в частности, внутриутробные инфекции, гипоксическую травму и т. д. Кроме того, часто выявление возбудителя не является доказательством герпетической инфекции, поскольку основная масса населения в мире имела контакт с данным вирусом. Тем не менее, основой диагностики является обнаружение самого вируса или его антигенов в разных средах, например, в содержимом везикул, крови, мазках из носо- и ротоглотки, цереброспинальной жидкости и др.
Метод высокоспецифичен, но занимает много времени. По этой причине проводятся серологические исследования с целью определения специфических антител класса IgM, что является подтверждением острой фазы врожденного герпеса. Подтверждение диагноза возможно также на основании обнаружения антител класса IgG, при этом решающую роль играет не сам факт их наличия, а нарастание титра в динамике не менее чем в 4 раза (при отсутствии нарастания антитела являются материнскими). В диагностике герпетического энцефалита врачи опираются именно на данные серологического исследования. Врожденный герпес также подтверждается, исходя из анамнеза матери и результатов гистологического обследования последа.
Лечение и прогноз врожденного герпеса
Проводится этиотропная терапия заболевания, от сроков ее начала во многом зависит прогноз для жизни и здоровья ребенка. Применяются противовирусные препараты, высокотропные именно к вирусу простого герпеса. Используется парентеральный путь введения. Также назначаются средства наружного действия для лечения везикулярной сыпи. Кроме того, к терапии врожденного герпеса всегда подключаются иммуноглобулины и иммуномодуляторы, проводится курс витаминотерапии. По показаниям осуществляется кислородная поддержка и ИВЛ, вводятся противосудорожные препараты, проводится дегидратация.
Прогноз неблагоприятный. Врожденный герпес часто протекает в генерализованной форме, последствия герпетического энцефалита необратимы. Выжившие дети очень редко не отстают в развитии от сверстников. Большинство из них остаются инвалидами или погибают в период разгара клинических проявлений. Даже если терапия начата своевременно, заболевание может неоднократно рецидивировать с той же симптоматикой. Для профилактики рецидивов возможно использование герпетической вакцины. В настоящее время существует несколько ее видов, но вследствие частых мутаций вируса эффективность вакцинации остается под вопросом.
Внутриутробная герпетическая инфекция. Заражение плода вирусом герпеса
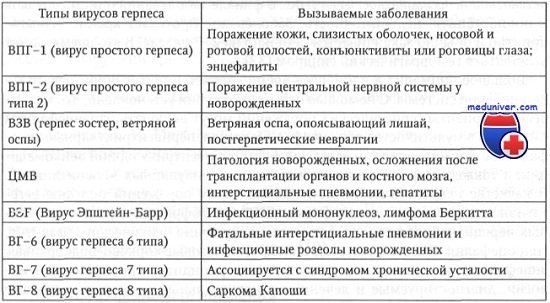
Вероятность перинатальной передачи герпетической, наиболее распространенной и практически неконтролируемой инфекции, очень высока. По данным Т. В. Голосовой, И. К. Никитина, известно более 80 представителей вирусов герпеса, из которых 8 типов патогенны для человека.
В паравертебральных сенсорных ганглиях ВПГ и ЦМВ находятся в латентном состоянии в виде L-prep-частиц. Персистенция вирусов связана с иммунокомпетентностью организма. В ситуациях, сопровождающихся иммуносупрессией, вирусы поражают различные ткани и вызывают разнообразные клинические формы заболевания. Одна из таких ситуаций обусловлена беременностью и взаимоотношением мать — плод.
Вероятно, это обусловлено тем, что вирус простого герпеса содержит детерминанты, подобные одному из фрагментов ФНР. Повышение уровня этих аутоантител в крови новорожденных коррелирует с появлением ЭКГ-признаков, свидетельствующих о снижении активности синусового узла и электрической активности миокарда.
У детей, рожденных женщинами с обострением герпетической инфекции, относительно чаще выявляются нарушения ритма сердца, связанные с угнетением симпатического звена регуляции, а также значительное удлинение интервала QT, что является маркером высокого риска формирования электрической нестабильности миокарда.
По данным Е. М. Малковой с соавторами, у новорожденных (n=62) с обнаруженной ДНК семейства герпесвирусов летальность составила 26,9%, у 7 новорожденных при патолого-анатомическом исследовании обнаружены врожденные пороки развития (гипоплазия легких, ангиоматоз сосудов легкого и генерализованная форма бронхоэктазий).
По результатам анализа у этих детей была выявлена ДНК вируса герпеса человека типа 6, что подтвердило тератогенное действие этого вируса.
Лечение перинатальной герпетической инфекции. К противогерпетическим относят противовирусные (химиопрепараты, интерфероны) и иммунокорригирующие препараты. Рекомендуются для использования в педиатрической практике иммуноглобулин человеческий нормальный, в том числе цитотект внутривенно, иммуноглобулин человеческий нормальный для внутримышечного введения. Однако препараты крови не исключают риск передачи гемотрансмиссивных инфекций. Установлено, что платные и первичные доноры крови являются источниками высокого уровня риска для гемотрансмиссивной передачи ВИЧ-инфекции и гепатитов.
Представляется обоснованным пересмотр показаний к переливанию компонентов и препаратов крови в сторону их сокращения.
Приорететное значение имеет раннее назначение противовирусной терапии. По данным О. Е. Озеровой с соавторами, основной метод диагностики — иммунологический — не всем доступен в связи с трудоемкостью и значительным временем для постановки окончательного диагноза. Поэтому в настоящее время основным диагностическим методом на 1 этапе, помимо клинических методов исследований, является эхография, дающая возможность оценить структуру головного мозга, других органов и установить степень их вовлечения в патологический процесс.
Внутриутробная герпетическая инфекция. Поражения плода герпесом
Внутриутробная герпетическая инфекция характеризуется развитием фетопатии или болезни новорожденных с типичными множественными некрозами в органах. По материалам прозектур г. Ленинграда, за последнее время обнаружено 12 случаев внутриутробной инфекции с типированным возбудителем (Herpes simplex 2-го типа) [Индикова М. Г., Попова Р. Д., 1980].
По данным D. Stowens (1966), автор наблюдал всего 1 случай на 700 аутопсий новорожденных. Этиология обусловлена заражением ДНК-содержащим вирусом Herpes simplex hominis 2-го типа [Krech U., 1972]. Этот тип вируса поражает половые органы женщин, передается половым путем и может персистировать в организме долгие годы. Высыпания везикул у матери наблюдаются в области влагалища и вульвы.
Патегеноз чаще связан с заражением во время родов, допускается возможность восходящей инфекции. Если у матери имеется обострение процесса в последние месяцы беременности, то заражение плода возможно в 40% [Новикова Е. Ч., Полякова Г. П., 1979]. Заболевание протекает очень тяжело, по одним авторам, сочетается с поражениями кожи [Stowens D., 1966], по другим — кожные изменения не характерны, так как они обусловлены вирусом герпеса 1-го типа, а в гениталиях вегетирует вирус герпеса 2-го типа.
Кроме того, бывает незначительная желтуха, лихорадка, на 3—4-е сут наступает смерть.
Печень увеличена, на разрезе пестрая, можно обнаружить мелкие (2—3 мм в диаметре) очажки желтовато-белого цвета, разбросанные в паренхиме, в коре надпочечников — точечные геморрагии.
В мозге в перивентрикулярных, супра- и субталамических отделах едва различимые фокусы размягчения. В легких — очаговая пневмония. Типичны внутриядерные оксифильные включения, окруженные светлым венчиком, хроматин оттеснен к ядерной оболочке.
Включения можно наблюдать только в живых клетках, легче в печени, в невронах мозга они не выявляются. Характерны некрозы коагуляционного типа с глыбчатым распадом в печени, коре надпочечников, в легких, головном мозге.
В печени явления дискомплексации и дистрофии гепатоцитов, по периферии некрозов у новорожденных может быть лейкоцитарная инфильтрация, чаще она отсутствует, описываются в единичных случаях массивные некрозы с регенерацией и образованием псевдо-тубул [Индикова М. Г. и др., 1980]. В легких, кроме очагов некроза, дистрофические изменения в альвеолоцитах и бронхиальном эпителии, перифокальпая пневмония.
В головном мозге очаги некроза особенно массивны. Наличие некрозов в других органах (почках, костном мозге) некоторые связывают не с прямым действием вируса, а с повреждением им эндотелия микроциркуляторного русла.
Внутриутробное заражение вирусом Коксаки В, вирусом сывороточного гепатита, цитомегалии и микоплазмами описаны в соответствующих разделах руководства.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

