Как снизить активность герпеса
Обновлено: 24.04.2024
Для цитирования: Дольникова О.А., Летяева О.И., Зиганшин О.Р. Роль метаболических нарушений в патогенезе рецидивирующего генитального герпеса // Эффективная фармакотерапия. 2020. Т. 16. № 27. С. 28–32.
- Аннотация
- Статья
- Ссылки
- Английский вариант
Рассматриваются особенности патогенеза рецидивирующего генитального герпеса у пациентов с метаболическими нарушениями. Показана роль жировой ткани в развитии хронического воспалительного процесса, иммунологических дисфункций и влияние на противовирусную защиту.
- КЛЮЧЕВЫЕ СЛОВА: генитальный герпес, метаболические нарушения, коморбидность, атеросклероз, переохлаждение, перегревание
Рассматриваются особенности патогенеза рецидивирующего генитального герпеса у пациентов с метаболическими нарушениями. Показана роль жировой ткани в развитии хронического воспалительного процесса, иммунологических дисфункций и влияние на противовирусную защиту.
Генитальный герпес одна из самых распространенных вирусных инфекций человека. По данным Всемирной организации здравоохранения на 2019 г., более 500 млн больны генитальным герпесом [1]. Особое значение имеет тот факт, что в организме может одновременно циркулировать несколько серотипов вируса. Традиционно считалось, что в этиологии генитального герпеса 80% случаев приходится на вирус простого герпеса 2-го типа, 20% – на вирус простого герпеса 1-го типа (ВПГ-1). Однако в одной из работ было показано, что доля первого эпизода аногенитального герпеса, обусловленного ВПГ-1, с течением времени значительно увеличилась среди женщин (с 45 до 61% ) и гетеросексуальных мужчин (с 38 до 41%). ВПГ-1 является ведущей причиной аногенитального герпеса у лиц молодого возраста [2]. Установлено, что ВПГ является одним из важных факторов распространения ВИЧ-инфекции [3]. Огромна роль герпесвирусной инфекции и в развитии патологии плода, а также в снижении показателей имплантации эмбрионов в циклах вспомогательных репродуктивных технологий [4].
Вирус способен проникать через слизистые оболочки уретры, прямой кишки и микротрещины кожи. В эпидемическом отношении очень важен тот факт, что заражение полового партнера возможно даже в отсутствие клинических проявлений. Для вируса простого герпеса характерно длительное рецидивирующее течение, сменяющееся периодами ремиссии [5]. Согласно современным данным, 20% инфицированных вирусом простого герпеса отмечают типичное течение, 60% – атипичное. Речь, в частности, идет о гиперемии и отечности области поражения при отсутствии патологических высыпаний. У 20% больных герпетическая инфекция выявляется только лабораторно [6].
Способность к персистенции и длительному существованию в латентной форме – важное свойство герпесвирусной инфекции [4, 7]. Латентное состояние обусловлено тем, что вирус не экспрессирует на клеточной мембране свои антигены. Латенция проявляется пожизненным сохранением вируса в организме, отсутствием продукции новых вирионов и селективной экспрессии вирусных генов. Под персистенцией понимают способность вируса циклично или непрерывно размножаться в клетках, пополняя пул инфекционных частиц. Это происходит вследствие того, что скомпрометированная иммунная система не распознает персистентное наличие вируса в организме. Механизмы латенции и персистенции изучены недостаточно. В литературе отмечается значимость генотипических особенностей иммунного ответа индивидуума на вирус простого герпеса [6, 7]. Описаны недостаточная активность макрофагов, CD4-лимфоцитов, снижение активности естественных киллеров, цитотоксических лимфоцитов, снижение выработки медиаторов иммунитета и др. [8, 9]. Несмотря на постоянное пополнение данных о механизмах иммунного ответа на герпесвирусную инфекцию, остается много противоречивых суждений о регуляции врожденного и приобретенного иммунитета в условиях хронической вирусной нагрузки. Кроме того, клинические проявления герпесвирусной инфекции во многом обусловлены взаимодействием иммунной системы и свойствами вируса.
В патогенезе рецидивирующего герпеса важная роль принадлежит таким провоцирующим факторам, как переохлаждение и перегревание, различные общие и инфекционные заболевания, ультрафиолетовое облучение, физические и психические стрессы, изменение гормонального статуса.
Длительно протекающая и часто рецидивирующая герпетическая инфекция способствует тяжелым невротическим и депрессивным расстройствам, а также развитию атеросклероза, ишемической болезни сердца, ревматоидного артрита, реактивного артрита [10–13].
Не исключено формирование патологического круга: хроническое рецидивирующее течение герпесвирусной инфекции способствует формированию психических расстройств и соматической патологии, а нарушение липидного обмена и иммунные нарушения – активации вируса простого герпеса. Кроме того, коморбидность нередко сопровождается полипрагмазией, что часто не только приводит к неудачам в терапии, но и становится опасным из-за ятрогении [7, 14, 15].
Проблема коморбидности
Современная патология человека характеризуется сочетанием заболеваний, имеющих мультифакториальный характер и отличающихся системностью поражения. Актуальный в настоящее время персонифицированный подход к терапии пациента требует глубокого понимания патогенеза основного и сопутствующего заболеваний [16–19]. Влияние коморбидной патологии на клинику, диагностику и лечение заболеваний индивидуально и многогранно. Коморбидная патология значительно изменяет клиническую картину и течение основного заболевания, ограничивает и затрудняет лечебно-диагностический процесс.
Одной из широко известных синтропий является метаболический синдром, включающий абдоминальное ожирение, инсулинорезистентность, артериальную гипертензию, атерогенную дислипидемию, гипергликемию. Для метаболического синдрома также характерно хроническое субклиническое воспаление – увеличение показателей С-реактивного белка, провоспалительных цитокинов [20–22].
Роль избыточной массы тела в формировании метаболических и иммунных нарушений
Образ жизни современного общества претерпел значительные изменения: ограничение физических нагрузок, увеличение калорийности пищи, резкий рост стрессовых нагрузок. Как следствие, более 1,9 млрд человек в возрасте 18 лет и старше имеют избыточную массу тела, а 650 млн страдают ожирением [23, 24]. Для мужчин характерен андроидный, абдоминальный тип ожирения. Частое сочетание висцерального ожирения, нарушения углеводного и липидного обмена и артериальной гипертензии позволило объединить их в самостоятельную нозологическую единицу – метаболический синдром. Таким образом была подчеркнута тесная патофизиологическая связь между данными состояниями.
Абдоминальное ожирение сопровождается хроническим воспалением жировой ткани и изменением секреции адипоцитокинов. Хроническое воспаление жировой ткани, индуцированное адипоцитами, рассматривается как одно из звеньев патогенеза ожирения. Кроме того, избыточная масса тела, сопряженная с увеличением синтеза провоспалительных цитокинов жировыми клетками, обусловливает развитие и поддержание субклинического хронического воспаления в тканях. Важная роль в прогрессировании и поддержании воспалительной реакции принадлежит гипоксии адипоцитов [15, 25–28].
Гормональная активность жировой ткани достаточно хорошо изучена. Активированные макрофаги продуцируют широкий спектр провоспалительных цитокинов: фактор некроза опухолей α (ФНО-α), интерлейкины (ИЛ) 1 и 6, свободные жирные кислоты и др.
Фактор некроза опухолей α является многофункциональным провоспалительным цитокином, синтезируемым макрофагами жировой ткани. Одними из важнейших его функций считаются снижение секреции жировыми клетками адипонектина и синтез веществ, стимулирующих активацию воспаления [7, 22]. В низких концентрациях ФНО-α усиливает синтез адгезивных молекул, что способствует привлечению нейтрофилов к месту воспаления, в больших концентрациях – приводит к развитию эндотоксин-индуцированного септического шока. Кроме того, большие концентрации ФНО-α подавляют липопротеиновую липазу жировой ткани, что приводит к уменьшению утилизации жирных кислот. Данный цитокин способствует пролиферации Т- и В-лимфоцитов, активации макрофагов, усиливает продукцию ИЛ-1 и ИЛ-6.
Интерлейкин 1 синтезируется в основном активированными макрофагами. Его роль в иммунном ответе крайне важна, так как именно он создает условия для пролиферации лимфоцитов и формирования клона специфически активированных клеток. Кроме того, ИЛ-1 вызывает продукцию гепатоцитами белков острой фазы, повышает продукцию простагландина Е2 и фосфолипазы А2, усиливает экспрессию адгезивных молекул, повышает продукцию других провоспалительных цитокинов, активирует гранулоциты, фибробласты, кератиноциты, NK-клетки [7, 22].
Интерлейкин 6 относится к провоспалительным цитокинам, формируемым жировой тканью. Он стимулирует синтез фибриногена и С-реактивного белка, являющегося маркером хронического воспаления. Эффекты этого цитокина во многом схожи с действием ИЛ-1. Усиливает завершающую дифференцировку В-клеток и продукцию антител. В комбинации с другими цитокинами усиливает пролиферацию и дифференцировку стволовых клеток, активирует CD4 + - и CD8 + -Т-лимфоциты [11, 15, 28].
При избыточной массе тела также повышается уровень свободных жирных кислот в крови [24]. В условиях переизбытка свободных жирных кислот развивается дислипидемия, характеризующаяся гипертриглицеридемией, повышенным уровнем холестерина липопротеинов низкой плотности (ЛПНП), снижением концентрации холестерина липопротеинов высокой плотности (ЛПВП), увеличением содержания атерогенных малых плотных частиц ЛПНП. В ряде работ показано, что повышенный уровень свободных жирных кислот вызывает в митохондриях макрососудистых эндотелиальных клеток повышенный синтез активных форм кислорода, что приводит к окислению ЛПНП и изменению ЛПВП. Все это провоцирует развитие воспалительного процесса в стенках сосудов, образование холестериновых бляшек [25]. Кроме того, свободные жирные кислоты участвуют в образовании ФНО-α, ИЛ-1, ИЛ-6, формировании митохондриальной дисфункции и окислительного стресса [26].
Жировая ткань секретирует полипептидные провоспалительные гормоны: лептин, адипонектин, резистин и ферменты, регулирующие биосинтез стероидных гормонов. Наиболее значимая роль в регуляции метаболизма жировой тканью принадлежит двум адипокинам: лептину и адипонектину [27]. Лептин оказывает мощное атерогенное, диабетогенное и провоспалительное воздействие. Адипонектин обладает противоположными лептину свойствами [15]. Лептин синтезируется преимущественно адипоцитами и обеспечивает увеличение расхода энергии и снижение массы тела. Полагают, что лептин помимо контроля энергетического статуса и обеспечения физиологических функций может участвовать в развитии воспаления, осуществлять связь между обменными функциями организма и иммунокомпетентностью. Лептин способствует активации и пролиферации лимфоцитов, активирует Т-хелперный ответ, повышает продукцию провоспалительных цитокинов. Провоспалительные медиаторы в свою очередь повышают количество рецепторов лептина в иммунокомпетентных клетках [15, 23, 27].
Гипертрофированные адипоциты синтезируют хемокины, которые обеспечивают приток новых нейтрофилов, макрофагов и лимфоцитов, что стимулирует увеличение гипертрофии адипоцитов и поддерживает воспалительную реакцию. Выявлено, что гипертрофированные адипоциты продуцируют цитокины и, участвуя в активации комплемента, запускают цепь воспалительных процессов. Воспаление приобретает системный характер [10, 20].
Значение репликации вируса и иммунного ответа в рецидиве герпесвирусной инфекции
Герпесвирусные инфекции входят в многочисленную группу инфекционных заболеваний, возбудители которых паразитируют на молекулярно-генетическом уровне. Цикл репликации вируса состоит из нескольких стадий: прикрепление, проникновение внутрь клетки, репликация, экспрессия, сборка вирусных частиц, выход из клетки. Проникновение вируса в клетку сопровождается изменениями вирусной оболочки и клеточной плазмалеммы. Перемещение вирусных частиц через мембрану клетки происходит с помощью клеточных рецепторов, предназначенных для проникновения в клетку жизненно важных веществ (клатрин-, кавеолин-опосредованный эндоцитоз, микропиноцитоз и др.). Необходимо отметить, что для проникновения в клетку и выхода из нее вирусные частицы используют один и тот же механизм [11, 12]. Так, ВПГ для проникновения в клетку использует путь клатрин-опосредованного эндоцитоза. Это позволяет защитить вирусные частицы от воздействия биологически активных веществ цитоплазмы. Анализ литературы свидетельствует, что в процессе слияния вирусной оболочки и плазмалеммы преимущественно участвуют липиды плазмалеммы. Велико значение и состава вирусного суперкапсида. Если в нем преобладают липиды, для входа вируса в клетку трансмембранные участки плазмалеммы не требуются [6, 8]. При завершении слияния вируса и плазмалеммы формируется липидная пора. Особая важность в транспортировке специфических белков придается недавно открытым в биологических мембранах микродоменам, способным легко перемещаться в мозаичном липидном слое мембран. Обнаружено присутствие вирусных гликопротеинов в структуре микродоменов и их взаимодействие с липидными компонентами мембраны клетки. Удаление холестерола ингибировало проникновение вируса [25].
Кроме того, вирусы выработали механизмы для избегания иммунных реакций или торможения их. Один из наиболее изученных механизмов – антигенная изменчивость. Попадая в клетку, вирус либо блокирует энзимы, необходимые для клеточного метаболизма, либо разрушает внеклеточные структуры, высвобождая летальные энзимы.
Для блокировки диссеминации вируса иммунный ответ должен остановить проникновение вирионов в клетки и уничтожить уже инфицированные клетки. Иммунные реакции против вириона чаще всего являются гуморальными, а иммунные реакции, направленные на клетки, инфицированные вирусом, – Т-клеточными. Нейтрализация вируса реализуется за счет активации антител IgG внеклеточной жидкости, IgM крови и IgA на поверхности слизистых оболочек. Кроме того, иммунные комплексы, содержащие вирус, связывают комплемент, что тоже способствует нейтрализации вируса. При распространении вируса от клетки к клетке на первое место выходят клеточные реакции с участием цитотоксических Т-лимфоцитов, которые появляются уже через два-три дня после заражения. Противовирусный иммунитет реализуется преимущественно Т-лимфоцитами и активированными макрофагами [6, 8]. Вырабатываемый интерферон тормозит транскрипцию вирусного генома, что снижает вирусемию.
Нормально функционирующее клеточное звено иммунитета способствует ограничению вирусного заболевания и прекращению формирования инфекционного процесса. Развивается адаптивный иммунный ответ с появлением цитотоксических и хелперных Т-клеток.
Кроме того, для препятствия распространению вирусной инфекции сформирован механизм программируемой клеточной гибели – апоптоз, который не сопровождается выделением цитокинов, медиаторов воспаления, стимулирующих развитие воспалительной реакции. При апоптозе клетка фрагментируется и подвергается фагоцитированию. Процесс апоптоза можно разделить на две основные фазы: формирование апоптотических сигналов и демонтаж клеточных структур [21]. Одним из механизмов реализации апоптоза является экспозиция на поверхности клетки фосфатидилсерина, фосфолипида, который обычно располагается на внутреннем липидном слое ее плазматической мембраны. Окисление активными формами кислорода способствует его перемещению на внешнюю мембрану клетки, что активирует рецептор, запускающий сигнал апоптоза [13, 21].
Вирусы приобрели способность инициировать различные биомеханизмы клеток, включая апоптоз. Вирусы простого герпеса могут либо ингибировать апоптоз, обеспечивая условия для репликации вируса в организме, либо провоцировать смерть клетки для распространения вируса по организму. Для увеличения выживаемости и воспроизводимости в клетке они не только блокируют митохондриальный путь апоптоза, нарушая формирование полноценного иммунного ответа организма, но и способствуют изменению внутриклеточного распределения митохондрий. Вирусы способны концентрировать митохондрии вблизи мест воспроизводства вирионов для максимального использования получаемой энергии. Кроме того, вирусы участвуют в активации программы самоуничтожения иммунокомпетентных клеток, что способствует их сохранению в организме, хронизации инфекционного процесса и носительства [13].
Апоптотический механизм иммуносупрессии рассматривается в патогенезе многих заболеваний, включая вирусные инфекции.
Состояние иммунной системы, иммунологических механизмов, нарушение в системе взаимодействия иммунокомпетентных клеток – важнейшие факторы в развитии и рецидивировании герпесвирусной инфекции.
Проблема коморбидной патологии требует мультидисциплинарного подхода к выбору диагностических и терапевтических методов. Избыточный вес и связанные с ним метаболические нарушения, проявляющиеся в увеличении синтеза провоспалительных цитокинов и поддержании субклинического хронического воспаления в тканях, в сочетании с рецидивирующим генитальным герпесом все чаще являются причиной ошибок при установлении диагноза из-за атипичных и стертых форм заболевания. Анализ литературы позволяет сделать вывод, что патогенез метаболических нарушений на фоне избыточной массы тела и патогенез длительно протекающего хронического инфекционного процесса имеют много общих морфологических и клинических проявлений. Связь между абдоминальным ожирением и рецидивирущей герпесвирусной инфекцией нуждается в дальнейшем изучении.
Именно эти виды герпеса ответственны за появление высыпаний – на коже лица, губах, слизистой оболочке полости рта, а также они являются причиной и генитального герпеса. Нужно отметить, что если раньше вирус герпеса ВПГ-2 – ассоциировался только с развитием генитального герпеса, то сейчас он также вызывает и герпес на лице, губах и слизистой оболочке рта – примерно у 10% пациентов. Герпес типа ВПГ-2 более патогенен (чем ВПГ-1), и у таких пациентов всегда наблюдаются – как более тяжелые клинические проявления, так и более высокая частота рецидивов.
Герпес: фото
Вирус простого герпеса клинически проявляется образованием группы скученных пузырьков, располагающихся на воспаленном основании (коже или слизистой оболочке). Пузырьки сначала заполнены прозрачным содержимым, которое достаточно быстро становится мутным. Если у вас появился герпес – лечение обязательно нужно начать до момента вскрытия герпетических пузырьков. В противном случае не только мазь от герпеса, но и самые лучшие таблетки от герпеса – уже не позволят хоть как-то заметно ускорить заживление.
Как выглядит герпес –
Вирус герпеса (как происходит заражение) –
Изначально дети рождаются с иммунитетом к вирусу герпеса – благодаря антителам, которые достаются каждому ребенку от матери (еще в период беременности). Однако постепенно количество антител уменьшается, и обычно в период от 6 месяцев до 3 лет максимум – у ребенка развивается первичная герпетическая инфекция. Обычно она протекает в виде первичного герпетического гингивостоматита. И в дальнейшем вирус герпеса сохраняется в организме на всю жизнь, периодически обостряясь.
Как передается герпес –
Лучшее средство от герпеса – это безусловно его профилактика, но ниже мы также расскажем и о специальных мазях и таблетках. Вы должны знать, что контактный путь является основным для передачи герпетической инфекции; более редким является воздушно-капельный путь передачи. Контактный путь передачи означает, что заражение вирусом герпеса происходит:
Наиболее заразными являются люди, имеющие клинические проявления герпеса – речь идет о целых или только что вскрывшихся герпетических пузырьках. Имейте в виду, что риск заражения не исчезает после образования корочек, а только чуть-чуть уменьшается. Современные исследования показывают, что заражение герпесом возможно даже от клинически полностью здорового человека.
Важно: у примерно 10% людей – вирус герпеса постоянно определяется в слюне (даже на фоне полного отсутствия у них каких-либо симптомов герпеса).
Из-за чего происходят рецидивы герпеса –
Под воздействием определенных пусковых факторов вирус активируется, вновь продвигается по нервным стволам к поверхностям кожи и/или слизистых оболочек – где и вызывает образование герпетических пузырьков (везикул). Рецидивы могут повторяться 1 или 2 раза в год, но иногда и намного чаще, что в конечном итоге зависит от состояния вашего иммунитета и нервной системы.
Факторы, которые вызывают рецидив герпеса –
- контакт с человеком, имеющим клинические проявления герпеса,
- снижение иммунитета на фоне гриппа или ОРВИ,
- иммунодефицитные состояния,
- переохлаждение, обезвоживание,
- физическая усталость и эмоциональный стресс,
- порезы и царапины кожи, например, после бритья,
- после визита к стоматологу (из-за того, что при длительном широком открывании рта происходит образование трещин в уголках рта),
- после инвазивных косметологических процедур,
- в период менструаций у женщин,
- длительное пребывание на солнце.
Симптомы герпеса –
Лабиальный герпес: фото
В зависимости от объема поражения кожи и тяжести клинических проявлений могут быть назначены либо крем для кожи с противовирусным действием, либо крем в комбинации с таблетированными противовирусными препаратами. Подробный обзор препаратов для лечения вы можете увидеть в конце статьи.
У детей герпетическому стоматиту очень часто сопутствует еще и гингивит. В этом случае (помимо множественных пузырьков и эрозий на каком-то участке слизистой оболочки полости рта) – можно увидеть ярко-красные воспаленные десны.
Общие симптомы герпеса –
первичная герпетическая инфекция может протекать с симптомами, похожими на грипп или ОРВИ (повышенная температура, мышечные боли и даже увеличение подчелюстных лимфатических узлов). Но такие острые симптомы наблюдаются только у 10% от всех заболевших. При повторных вспышках общее состояние организма обычно не нарушается.
Чем лечить герпес у взрослых (лекарства) –
Но, чтобы лечение герпеса было максимально эффективным – вы должны строго соблюдать следующие правила:
Терапия герпеса покажет хорошую эффективность, если она начата не позже 12 часов с момента появления первых герпетических высыпаний. Имейте в виду, что чем позже будет начато лечение – тем меньше будет эффективность даже самых лучших лекарств от герпеса.
Максимальную эффективность покажет терапия, которая начата еще в продромальном периоде (т.е. когда собственно герпетические пузырьки еще не появились, но пациент уже ощущает зуд, жжение или распирание тканей в этой области). Если лечение начинается в этот период, то количество и размер образовавшихся в дальнейшем герпетических пузырьков будет значительно меньшим, и в этом случае полное заживление может быть достигнуто всего за 4-5 дней.
Помните, что если вы начнете лечение позже 48 часов, либо уже после вскрытия герпетических пузырьков – такая терапия заметно не повлияет на скорость выздоровления (заживление очагов). Однако у пациентов с тяжело протекающими и частыми рецидивами – такая терапия может позволить избежать осложнений.
1. Выбираем мазь от герпеса –
Крем Зовиракс: оригинальный препарат ацикловира
Крем или мазь от герпеса с ацикловиром следует наносить на очаг поражения и кожу вокруг него – минимум 5 раз в день (но лучше каждые 2 часа пока вы не спите). Продолжительность терапии обычно составляет 5 дней, но в случае тяжелого герпетического поражения – длительность применения может быть увеличена до 7-10 дней. Нужно отметить, что форма в виде крема более предпочтительна перед мазью, т.к. из мазевой субстанции активные вещества значительно хуже проникают в кожу.
Стоит обращать внимание и на состав, например, эффективной концентрацией ацикловира является именно 5% (хотя в аптеках можно встретить и средства с 3% концентрацией). Кроме того, в составе желательно должны быть пропиленгликоль и/или цетомакрогол, которые увеличивают проникновение молекул ацикловира сквозь поверхностные слои кожи. Это важно, т.к. сам по себе ацикловир достаточно плохо проникает через эпидермис кожи и образующиеся корочки.
Лучшее средство от герпеса с ацикловиром –
На сегодняшний день лучший препарат для наружного применения от герпеса – это крем Зовиракс Дуо-Актив, который содержит комбинацию 5% ацикловира и 1% гидрокортизона. Ацикловир блокирует размножение вируса, а гидрокортизон уменьшает воспаление и отек. При этом, если применение крема начинается еще до появления герпетических пузырьков, то гидрокортизон иногда позволяет вообще предупредить их образование. Но если пузырьки и образуются, то их количество и размер будут меньшим, что уже само по себе позволит заметно ускорить заживление.
Недостатки препаратов на основе ацикловира –
ацикловир является устаревшим препаратом, но в принципе он неплохо работает у большинства пациентов (с некоторыми исключениями). Например, у пациентов с хорошим иммунитетом устойчивость вируса герпеса к ацикловиру встречается – в среднем всего в 3% случаев, что достаточно мало. Однако проблему составляют пациенты с ослабленным иммунитетом + частыми курсами применения ацикловира в прошлом – в таких группах пациентов устойчивость к ацикловиру может наблюдаться уже от 10 до 27% случаев.
Кроме того, молекулы ацикловира имеют очень низкую тропность к вирусу герпеса, что означает, что ацикловир обычно просто не находит какой-то процент вирусных частиц в клетках (к примеру у препаратов на основе пенцикловира/ фамцикловира – тропность в вирусу намного выше). Кроме того, молекулы ацикловира имеют свойство плохо проникать сквозь кожу, а также сквозь образующиеся корочки (к месту размножения вируса). Чтобы хоть как-то уменьшить эту проблему – часть производителей добавляют в состав наружных средств с ацикловиром пропиленгликоль и цетомакрогол.
Альтернативные наружные средства от герпеса –
Выше мы уже сказали, что у пациентов с ослабленным иммунитетом часто развивается устойчивость вируса герпеса к ацикловиру. Что делать таким пациентам? Международные рекомендации в этом случае говорят о необходимости применения курсов фамцикловира в таблетках – это такие препараты как Фавирокс или Фамвир. Таблетированные препараты на основе валацикловира (при подозрении на резистентность к ацикловиру) – применять не имеет смысла, т.к. валацикловир является предшественником ацикловира. Последнее означает, что при наличии устойчивости к ацикловиру – устойчивость будет и к валацикловиру.
Крем Девирс от герпеса –
К сожалению, клинических исследований эффективности местных средств на основе рибавирина – очень мало, и все они, на наш взгляд, имеют достаточно слабую степень доказательности. Знакомясь с исследованиями, мы обратили внимание на то, что этот препарат очень редко применялся в исследованиях в форме монотерапии (обычно его комбинировали – либо с пероральным рибавирином, либо с пероральным ацикловиром), что уже говорит о достаточно слабой эффективности крема. Поэтому наша редакция не может рекомендовать этот препарат для широкого применения – особенно для лечения герпеса губ и небольших поражений на лице. Но препарат вполне может использоваться в составе комплексной терапии, например, при генитальном герпесе.
Выбираем таблетки от герпеса –
Герпес лечение у взрослых: препараты в таблетках
- Ацикловир,
- Валацикловир,
- Фамцикловир.
1. Ацикловир в таблетках по 200 и 400 мг –
Таблетированный ацикловир обладает теми же недостатками, что и кремы: низкая тропность к вирусу (т.е. молекулы ацикловира плохо находят вирусные частицы); у пациентов с плохим иммунитетом + частыми курсами применения ацикловира в прошлом – в 10-27% случаев вирус герпеса может быть устойчив к ацикловиру; плюс низкая биодоступность при пероральном приеме. Плюсы – нет противопоказаний по возрасту, доступная цена, достаточно мало побочных эффектов.
Примеры препаратов с ацикловиром –

Ацикловир в таблетках безусловно работает, особенно если речь идет о пациентах с хорошим иммунитетом и редкими рецидивами герпеса. Если у вас ослабленный иммунитет, если слишком часто принимали ацикловир в прошлом, если вы решили начать принимать препарат более чем 24-48 часов с момента появления герпетических высыпаний – ацикловир не будет особенно эффективен. В этом случае вам лучше сразу начать принимать препарат Фамцикловир, который лучше работает даже при более поздних сроках начала терапии, а также у пациентов с иммунодефицитными состояниями.
Схема применения –
если смотреть официальную инструкцию, то стандартной схемой у взрослых и детей старше 2 лет – является прием ацикловира по 200 мг 5 раз в день (в течение 5 дней). Однократная дозировка 400 мг в официальной инструкции рекомендуется – либо только при тяжелом течении герпетической инфекции, либо у пациентов с ослабленным иммунитетом. Однако, большинство клинических исследований (источник) показывает, что дозировка 200 мг практически не влияет – ни на длительность симптомов, ни на время заживления герпеса.
Исследования показали, что эффективной однократной дозировкой является только 400 мг (соответственно, 5 раз в день, в течение 5 дней). У детей младше 2 лет дозировка уменьшается ровно в 2 раза – от взрослой дозировки. При тяжелом течении герпетической инфекции – прием препарата может быть продлен до 7-10 дней. Кстати, за рубежом, при хроническом рецидивирующем герпесе ацикловир в настоящий момент практически не применяют, отдавая предпочтение валацикловиру и фамцикловиру.
2. Таблетки Валацикловир (Валтрекс) –
Выше мы уже говорили, что таблетированный ацикловир имеет слабую биодоступность, т.е. всего около 10-20% от его количества всасывается в кишечнике, что затрудняет достижение высоких концентраций ацикловира в тканях. Эту проблему решает Валацикловир, имеющий биодоступность уже на уровне 50%. Валацикловир является предшественником ацикловира (т.е. он превращается в ацикловир, уже попав в кровь). Прием таблеток с валацикловиром позволяет создать такую концентрацию ацикловира в тканях, которую возможно достичь традиционным ацикловиром – только путем внутривенных инфузий последнего.
Схема приема –
существует короткая 1-дневная схема лечения. Клинические исследования показали, что прием высоких дозировок препарата в течение 1 дня – было наиболее эффективным для лечения герпеса на губах и коже лица, а также герпетического стоматита. В этом случае схема приема – по 2000 мг 2 раза в день, с интервалом 12 часов (всего 1 день). Но следует учесть, что такая короткая схема будет эффективной – только если лечение начинается не позже 12 часов с момента появления герпетических высыпаний, а также у пациентов с удовлетворительным или хорошим иммунитетом.
Если с момента появления высыпаний прошло больше 12 часов, а также если у вас ослабленный иммунитет – оптимально использовать стандартную схему лечения по 500 мг 2 раза в день, в течение 3-5 дней (при тяжелой форме герпетической инфекции – до 10 дней). При выборе препарата имейте в виду, что при устойчивости вашего вируса герпеса к ацикловиру – прием валацикловира у вас также будет неэффективен.
3. Таблетки Фамцикловир (Фавирокс, Фамвир) –
Преимущество препаратов фамцикловира типа Фавирокса – быстрый противовирусный эффект благодаря максимальной биодоступности (для фамцикловира она составляет около 74%, например, у валацикловира она всего 54%, а у ацикловира только 10-20%). Поэтому упаковки из трех таблеток по 500 мг – достаточно для короткого 1-дневного курса терапии для купирования проявлений герпеса на губе. Подробности о такой схеме применения – читайте ниже.

Схема применения фамцикловира –
существует короткая 1-дневная схема лечения: либо однократно принять 1500 мг, либо по 750 мг 2 раза в день (с 12 часовым интервалом между приемами) – наш опыт говорит о том, что второй вариант все-таки лучше. Такая 1-дневная схема эффективна только при условии, что вы начали прием препарата до 12 часов с момента появления герпетических высыпаний, а также при нормальном состоянии иммунитета у пациента. При ослабленном иммунитете, и/или если лечение начато позже 12 часов с момента появления герпетических высыпаний – нужно использовать стандартную схему применения.
Стандартная схема согласно инструкции – это по 250 мг 2 раза в день, в течение 5 дней (однако при тяжелой форме герпетической инфекции – прием может быть продлен до 7-10 дней). Тут хочется добавить, что многочисленные клинические исследования показывают слабую эффективность такой стандартной схемы – особенно у пациентов с плохим состоянием иммунной системы. Исследования показали, что эффективность терапии значительно возрастает при назначении фамцикловира в более высоких дозировках. У пациентов с хорошим иммунитетом более эффективной будет схема – по 500 мг 2 раза в день (в течение 5 дней). У пациентов с ослабленным иммунитетом – по 500 мг 3 раза в день (в течение 7 дней).
Важно : еще раз обращаем ваше внимание на то, что короткие 1-дневные схемы лечения герпеса у взрослых (герпеса на губах и кожи вокруг рта, на лице) – хорошо работают только при выполнении следующих условий. Во-первых – только если вы начинаете принимать препараты не позже 12 часов с момента появления герпетических высыпаний. Во-вторых – если у вас удовлетворительное или хорошее состояние иммунитета. Если лечение начато позже 12 часов с момента появления высыпаний, а также у пациентов с ослабленным иммунитетом – короткие 1-дневные курсы терапии обычно неэффективны. Тут уже нужна стандартная схема приема.
Важно : если с момента появления первых высыпаний прошло больше 12 часов (и тем более, если больше 24 или 48 часов) – лучше сделать выбор в пользу фамцикловира, т.к. последний лучше работает при более поздних сроках начала терапии герпетической инфекции.
Лечение иммуномодуляторами, профилактика герпеса –
Если у вас высокая частота рецидивов герпеса, либо пусть редкие, но тяжело протекающие вспышки – вам очень важно заняться профилактикой вспышек герпеса. И дело тут не только в том, что тяжелое течение герпетической инфекции и/или ее частые рецидивы – сами по себе свидетельствуют о проблемах с вашим иммунитетом. Дело в том, что вирус герпеса обладает иммуносупрессивным действием на всю систему иммунитета – и на клеточное, и на гуморальное звено иммунитета.
Это означает, что иммунная система под воздействием вируса герпеса – будет продолжать ослабевать, что приведет к дальнейшему увеличению частоты рецидивов и тяжести вспышек. На данный момент существуют следующие направления профилактики вспышек вируса простого герпеса (ВПГ-1, ВПГ-2), но выбирать тот или иной метод – вы должны только после консультации врача. Всем пациентам с частотой вспышек более 6-ти в течение года необходимо сделать анализ на количество специфических антител IgG и IgM к вирусу простого герпеса, а также получить консультацию врача-иммунолога и сделать иммунограмму (в которой оценивается субпопуляционный состав клеток, NK-активность, а также уровни α- и γ-интерферонов).
Важно : прием иммуномодуляторов показан не только для профилактики рецидивов герпетической инфекции – у часто и/или тяжело болеющих герпесом пациентов. Иммуномодуляторы должны использоваться в составе базовой терапии герпетических инфекций (в дополнение к терапии противовирусными препаратами) – у пациентов с ослабленным иммунитетом.
Прививка от герпеса (вакцина Витагерпавак) –
Прививка от герпеса (Вакцина Витагерпавак) –
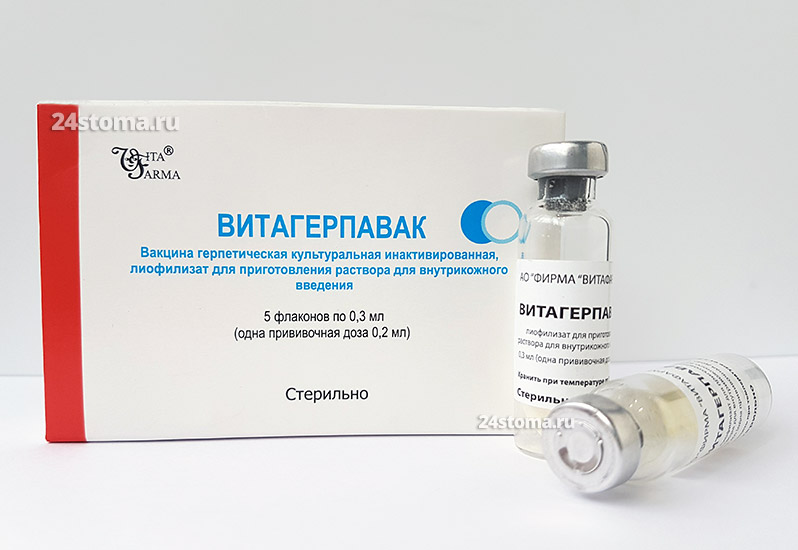
Источники:

Врач — акушер-гинеколог-эндокринолог. Стаж 21+ год. Принимает в Университетской клинике. Стоимость приема 1700 руб.
- Запись опубликована: 20.12.2018
- Reading time: 3 минут чтения
Герпес – инфекционное вирусное заболевание, имеющее хроническое рецидивирующее течение. Возбудителем инфицировано большинство людей. Повсеместное распространение инфекции требует соблюдения мер, исключающих заражение, и проведения своевременного адекватного лечения.
Способы заражения и особенности инфекционного процесса при герпесе
Вирусные частицы способны в течение длительного времени сохраняться на кожных покровах человека и окружающих предметах. Преимущественным путем заражения инфекцией является контактный, второй по значимости – воздушно-капельный.
При проникновении в кожу вирус начинает активно делиться. Развиваются очаги воспаления с болезненными зудящими пузырьками, заполненными прозрачной жидкостью. Из области первичного заражения возбудитель по лимфатическим и кровеносным сосудам распространяется по всему организму.
Активный ответ иммунной системы очищает организм от вируса, а в крови длительное время сохраняются иммуноглобулины M и G, препятствующие развитию рецидивов заболевания. Однако за это время часть вирусных частиц успевает по нервным волокнам проникнуть в клетки нервной системы. Эти возбудители становятся недосягаемыми для иммунитета. Именно они являются причиной рецидивов и бессимптомного носительства инфекции.
Причины, приводящие к обострению герпеса:
- Смена сезонов (сыпь часто появляется весной и осенью), резкая смена климата.
- ОРВИ или другое заболевание, сопровождающееся ослаблением иммунитета.
- Гиповитаминоз, скудное, однообразное питание.
- Чрезмерные эмоциональные и физические нагрузки.
- Переохлаждение.
- Беременность.
Типы вирусов герпеса
Всего в настоящее время у человека выявлено 8 основных типов герпеса:
- Вирус простого герпеса I типа, вызывающий появление характерной сыпи на губах и слизистой рта.
- Вирус простого герпеса II типа, поражающий слизистые оболочки половых органов.
- Вирус ветряной оспы, или вирус герпеса III типа, вызывающий ветрянку и опоясывающий лишай с характерными болями и сыпью по ходу нервов.
- Вирус Эпштейна-Барр, или вирус герпеса IV типа, приводящий к развитию инфекционного мононуклеоза.
- Цитомегаловирус, или вирус герпеса V типа, заражение которым при беременности вызывает рождение детей с тяжелыми врождёнными патологиями.
Оставшиеся три типа до конца не изучены. Есть сведения, что инфицирование ими приводит к развитию синдрома хронической усталости.
Симптомы герпеса
Проявления герпеса можно схематично разделить на местные, общие и связанные с поражением нервной системы.
Герпес губ проявляется сыпью, болью и жжением в месте развития воспалительного процесса. Спустя несколько часов после появления на коже красной каймы губ появляются характерные многокамерные пузырьки, заполненные прозрачной жидкостью.
Сыпь может сохраняться до нескольких суток. Затем пузырьки мутнеют и разрываются, превращаясь в язвочки. Заживление проходит без образования шрамов.
Реже характерная сыпь может появляться на слизистой рта. Такая сыпь редко бывает болезненной и не беспокоит пациента. Бессимптомное протекание способствует распространению инфекции.
Генитальный герпес высыпает на коже и слизистых оболочках половых органов. Появляется характерная сыпь, которая болит и чешется. Пузырьки вскрываются спустя несколько суток с образованием небольших язвочек. После заживления на месте сыпи не остается рубцов.
Характерное течение генитального герпеса наблюдается при первичном заражении герпесом. Рецидивы заболевания могут приводить к появлению неприятных ощущений в области половых органов и интенсивному покраснению слизистых оболочек.
У мужчин воспаляется слизистая головки и крайней плоти, у женщин – половые пути. Поскольку такие симптомы характерны для многих болезней, поставить диагноз без проведения лабораторной диагностики невозможно.
Иногда инфекционный процесс протекает бессимптомно, но при этом больной может заражать половых партнеров.
Генитальный герпес становится причиной формирования врожденных пороков развития у плода и инфицирования ребенка при рождении. Герпетическая инфекция у новорожденного протекает очень тяжело и часто приводит к летальному исходу, несмотря на проводимое лечение.
Опоясывающий лишай проявляется характерными высыпаниями по ходу нервных стволов. На коже высыпают пузырьки, сопровождающиеся воспалением, зудом и болью.
Общие симптомы
За несколько часов или дней до появления сыпи может наблюдаться недомогание, повышение температуры тела, снижение жизненного тонуса, ухудшение самочувствия. Эти симптомы крайне редко отмечаются при герпесе губ. Чаще всего нарушение самочувствия и лихорадка характерны для опоясывающего лишая.
Поражение нервной системы при герпесе
Первичное инфицирование или рецидив герпетической инфекции может привести к воспалению ткани мозга или его оболочек. Ситуация требует скорейшего начала лечения и длительной реабилитации.
Долгосрочный прогноз длительного существования герпеса в нервной ткани неблагоприятен. В 70% случаев при болезни Альцгеймера в ткани мозга выявляется ДНК вируса герпеса. Это значит, что инфекция значительно повышает вероятность развития слабоумия в пожилом возрасте.
Диагностика герпеса
При наличии характерных проявлений герпетической инфекции на коже и слизистых поставить диагноз несложно. А вот определить хронические воспалительные процессы без лабораторной диагностики нельзя. Для постановки диагноза назначают:
- общий и биохимический анализы крови;
- общий анализ мочи;
- урологический или гинекологический мазок для проведения полимеразной цепной реакции (ПЦР), которая выявляет герпес и определяет его тип;
- анализ на иммуноглобулины igm и igg, свидетельствующие об активности инфекционного процесса, адекватности ответа иммунной системы и давности заражения герпесом.
В зависимости от особенностей болезни врач может назначить один или несколько обследований.
Лечение герпеса
Современная медицина может убрать только симптомы болезни. Уничтожить вирус, находящийся в нервной ткани, не представляется возможным. Для лечения обострений и профилактики рецидивов герпеса назначаются:
- противовирусные средства общего и местного действия;
- средства, повышающие иммунитет;
- вакцины.
Из противовирусных средств чаще всего применяются Ацикловир, Фамцикловир, Валацикловир, Тромантадин, Доконазол, Аллокин-альфа. Препараты назначаются внутрь, в инъекциях и местно в виде мазей и кремов.
Наиболее эффективными средствами из числа иммуностимуляторов являются Ликопид, Эпиген-спрей, свечи Виферон.
Профилактика заражения герпесом
- Исключение пользования чужой посудой и полотенцами.
- Использование презерватива при половых сношениях.
- Обработка кожи и слизистых оболочек половых органов после незащищенного полового акта антисептиком мирамистином.
- Проведение вакцинации.
- Изоляция больных ветряной оспой.
В большинстве случаев никакого серьезного вреда для здоровья взрослого человека герпес не несет. Дискомфорт вызывает зуд и боль, которые сопровождают появление сыпи.
Однако воспалительный процесс повреждает целостность кожи и слизистой и делает ее проницаемой для других бактериальных и вирусных инфекционных агентов. В результате может развиться вторичная инфекция.
В статье представлены современные подходы к назначению терапии при острых проявлениях герпесвирусной инфекции, а также к выбору препаратов в целях профилактики ее обострений.
- КЛЮЧЕВЫЕ СЛОВА: герпесвирусная инфекция, этиотропная терапия, супрессивная терапия
В статье представлены современные подходы к назначению терапии при острых проявлениях герпесвирусной инфекции, а также к выбору препаратов в целях профилактики ее обострений.
Герпесвирусные инфекции (ГВИ) широко распространены в мире. В частности, в Европе частота встречаемости достигает 50–80%, в странах Азии – до 90–100% [1]. Свыше 90% населения планеты инфицированы вирусом простого герпеса (ВПГ). До так называемой сексуальной революции прослеживалась четкая зависимость между типом ВПГ и локализацией высыпаний: ВПГ 1-го типа чаще связывали с локализацией в области лица, ВПГ 2-го типа – с генитальной локализацией. В последние годы подобная зависимость утратила актуальность из-за возросшей популярности орогенитальных контактов.
Среди врачей разных специальностей бытует мнение, что только тяжелые формы рецидивирующих ГВИ кожи или слизистых оболочек, инфекционный мононуклеоз, ветряная оспа и опоясывающий герпес требуют применения специфических этиотропных препаратов. Кроме того, часто необоснованно назначают различные иммуномодулирующие препараты в виде монотерапии. Отсутствие этиотропного лечения и наличие сопутствующих заболеваний и состояний, которые расцениваются как провоцирующие факторы, угнетающие иммунный ответ (аутоиммунные заболевания, заболевания желудочно-кишечного тракта и эндокринной системы, острые и хронические воспалительные заболевания органов малого таза, психотравма и хронический стресс, воздействие ультрафиолетового излучения, употребление алкоголя, гормональные циклы, медицинские инвазивные вмешательства, злокачественные новообразования и иммуносупрессивная терапия при их лечении), снижают эффективность терапии, приводят к частым рецидивам заболевания и распространению ГВИ в популяции.
Клинические формы
Клинические формы проявления ГВИ крайне разнообразны. Только при поражении кожи и слизистых оболочек выделяют [2]:
- первичную инфекцию;
- герпетический стоматит (первичный герпес лица и полости рта);
- первичный герпес половых органов;
- первичный герпес другой локализации;
- герпес новорожденных;
- герпетическую экзему Капоши;
- первичный герпес на фоне иммунодефицита;
- рецидивы;
- герпес лица и полости рта;
- герпес половых органов;
- рецидивирующий герпес иной локализации;
- рецидивирующий герпес на фоне иммунодефицита;
- хронический язвенный герпес;
- диссеминированную инфекцию;
- диссеминированное поражение кожи;
- генерализованный герпес (диссеминированное поражение внутренних органов и кожи).
Герпесвирусные инфекции классифицируют по степени тяжести [3]:
- легкое течение (частота рецидивов один-два раза в год, ремиссия не менее шести месяцев);
- среднее (частота рецидивов от трех до пяти раз в год, ремиссия не менее трех месяцев);
- тяжелое (частота рецидивов более шести раз в год, ремиссия от нескольких дней до шести недель);
- бессимптомное.
Диагностика
Диагностика ВПГ представляет большую медико-социальную проблему, поскольку клинические проявления разнообразны и зависят от множества причин: типа вируса, генетической устойчивости человека к ВПГ, тяжести и длительности заболевания, состояния иммунного статуса, механизма инфицирования, вирусной нагрузки, возраста пациента, давности заболевания, наличия сопутствующей патологии.
Алгоритм диагностики ГВИ включает:
- общеклиническое обследование;
- сбор иммунологического, аллергологического, дерматологического и инфекционного анамнеза;
- осмотр дерматолога, аллерголога-иммунолога, офтальмолога, гинеколога, невролога и других профильных специалистов;
- диагностику методом полимеразной цепной реакции (ПЦР) в режиме реального времени (определение ДНК вируса простого герпеса (1-го или 2-го типа) в крови, слюне, моче, содержимом везикул, соскобе со дна эрозии, слизистой уретры, стенок влагалища и цервикального канала, конъюнктивы глаз). Учитывая высокую диагностическую значимость данного метода и зависимость смертности новорожденных от виремии, вызванной ВПГ 1-го и ВПГ 2-го типов, некоторые исследователи рекомендуют использовать ПЦР для лабораторного скрининга на генерализованную герпетическую инфекцию среди детей высокого риска и женщин репродуктивного возраста;
- серологическую диагностику: анализ крови на IgM и IgG к ВПГ методом иммуноферментного анализа (ИФА). Наличие антител свидетельствует об инфицировании, но не всегда позволяет связать клинические проявления инфекции с вирусом герпеса: у части бессимптомных носителей выявляются высокие титры антител, тогда как у ряда пациентов с выраженной симптоматикой титры антител остаются низкими. Использование ИФА целесообразно при исследовании парных сывороток, полученных с интервалом 7–10 дней. Показателем первичной инфекции считается четырехкратное увеличение антител класса IgG к ВПГ;
- цитоморфологические методы (проведение световой микроскопии биоматериала после его окрашивания на предметном стекле);
- иммунофлуоресцентный анализ (используется в основном в научных исследованиях).
В клинической практике для постановки диагноза ВПГ обычно ограничиваются данными анамнеза и клинических проявлений болезни, а также выявлением ДНК ВПГ методом ПЦР в отделяемом из высыпаний, когда диагноз из-за локализации поражений или анамнестических данных вызывает сомнения.
В ряде случаев генитальная локализация ГВИ трудно диагностируется. Только в 20% случаев диагноз верен. 20% пациентов – вирусоносители, которые никогда не имели клинических симптомов или признаков заболевания. Нередко при рецидивах ВПГ генитальной локализации, протекающего в атипичной форме (без выраженных клинических признаков), диагноз кандидоза ошибочен. И наоборот: при заболеваниях, протекающих с язвенными поражениями (сифилисе, болезни Бехчета и др.), ставят диагноз герпеса.
Положительные результаты исследования методом ПЦР подтверждают наличие у пациента генитального герпеса, требующего лечения. Отрицательный результат теста не исключает диагноз, поскольку недостаточное количество материала, его потери при транспортировке в лабораторию и быстрое заживление очага инфекции способны привести к ложноотрицательному результату. В таких ситуациях исследование проводится два-три раза с интервалом две – четыре недели [4].
Полностью элиминировать вирус герпеса из организма не представляется возможным. Поэтому терапия герпетической инфекции направлена на блокаду репродукции вируса.
Противовирусная терапия наиболее эффективна в фазе репликации вируса. При обострении хронической инфекции, вызванной ВПГ, показана противовирусная терапия в комбинации с иммунопрепаратами на фоне патогенетической и симптоматической терапии.
Этиотропная терапия ГВИ считается общепризнанным подходом к лечению острых проявлений инфекции и профилактике ее обострений. Современные этиотропные противогерпетические препараты (ацикловир, валацикловир, фамцикловир) по уровню доказательности относятся к группе A [5]. Молекула валацикловира по сравнению с таковой ацикловира характеризуется более высокой биодоступностью (54%) и длительностью полувыведения (10–20 часов). Это позволяет снизить кратность приема препарата до двух раз в сутки и увеличить приверженность пациентов терапии.
Механизм действия противогерпетических препаратов заключается в угнетении синтеза вирусной ДНК и репликации вирусов за счет конкурентного ингибирования вирусной ДНК-полимеразы.
Последнее время на российском фармацевтическом рынке появляется большое количество препаратов валацикловира. Форма выпуска – таблетки, покрытые пленочной оболочкой, в стандартной дозе 500 мг (валацикловира гидрохлорида гидрат 611,70 мг), а также в дозе 1000 мг (валацикловира гидрохлорида гидрат 1223,40 мг). Клиническую эффективность валацикловира у пациентов с хронической рецидивирующей ГВИ изучали в исследовании [6].
Выделяют два основных способа применения противовирусных химиопрепаратов: эпизодическое назначение (при необходимости, обострениях ГВИ) и пролонгированная терапия. В первом случае препарат назначают коротким курсом 5–10 дней, во втором пациенты принимают препарат ежедневно в течение нескольких месяцев или лет не только для купирования данного рецидива, но и для профилактики последующих обострений [7–9].
Показаниями для назначения супрессивной терапии являются:
- тяжелое течение с частыми обострениями;
- отсутствие продромального периода;
- особые обстоятельства (отпуск, свадьба и т.д.);
- использование иммуносупрессивной терапии;
- наличие психосексуальных расстройств;
- предотвращение риска передачи инфекции.
У пациентов с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные, общеукрепляющие средства). Как правило, таким пациентам показаны длительные курсы противовирусных препаратов (в частности, ацикловир, валацикловир, фамцикловир) [10].
При использовании супрессивной схемы лечения дозы препаратов зависят от клинического течения рецидивов генитального герпеса. Если количество рецидивов не более десяти в год, суточная доза валацикловира составляет 500 мг. При количестве рецидивов свыше десяти в год валацикловир используют в дозе 1000 мг.
В лечении ГВИ легкого и среднетяжелого течения широко используются иммуномодулирующие препараты, интерфероны (ИФН), индукторы интерферона, а также витаминотерапия. При тяжелых формах ГВИ целесообразно внутривенное введение иммуноглобулина.
При тяжелом и длительном течении ВПГ-инфекции в случае курсового использования названных препаратов в качестве монотерапии отмечается недостаточный клинический эффект. При длительном приеме развиваются побочные и нежелательные эффекты. ИФН представляет собой только часть противовирусной защиты иммунной системы и не может заменить другие ее звенья при их несостоятельности. Использование иммунокорректоров без оценки иммунного статуса, индивидуального подбора и контроля их действия бывает малоэффективно или способно приводить к усилению иммунной дисфункции либо гипореактивности ряда звеньев иммунитета вследствие неадекватной стимуляции. Назначение препаратов для местного применения (мази, содержащие ацикловир, Эпиген интим спрей (глицирризиновая кислота) и др.) носит вспомогательный характер, поскольку пузырьковые высыпания на коже лишь одно из проявлений тяжелой ВПГ-инфекции.
Как показывают данные литературы и накопленный нами опыт, вирус герпеса способен реплицировать в других клетках и органах (в орофарингеальной области, лимфоузлах, слизистой прямой кишки и т.д.).
Клинический случай
К врачу аллергологу-иммунологу обратилась пациентка М. 32 лет с жалобами на пузырьковые высыпания на слизистой оболочке красной каймы губ, болезненность в области высыпаний, головную боль, нарушение сна, утомляемость, раздражительность.
Анамнез заболевания. Аналогичные симптомы беспокоят в течение пяти лет. Высыпания локализуются в области носогубного треугольника. Частота рецидивов – от шести до восьми раз в год. В течение полугода обострения ежемесячные. В 2013 и 2015 гг. – два эпизода герпетического кератита (заключение офтальмолога на руках). Неоднократно обращалась к дерматологу по месту жительства – курсы ацикловира 200 мг пять раз в сутки в течение трех – пяти дней с кратковременным эффектом. Кроме того, использовалась местная противовирусная терапия в виде мазей. Настоящее обострение в течение трех дней связывает со стрессом на работе (полгода работает на новом месте, рабочий график ненормированный). Самостоятельно применяла местную терапию без значимого эффекта.
Объективно. Состояние удовлетворительное. Температура тела 36,7 ºС.
На слизистой оболочке красной каймы верхней губы слева сгруппированные пузырьковые высыпания с серозным содержимым, желтоватые корочки, мокнутие.
Лабораторная диагностика. Выявлена ДНК ВПГ 1-го типа методом ПЦР из содержимого везикулы.
Консультация невролога. Астеноневротический синдром. Назначен Атаракс 25 мг по 1/2 таблетки на ночь в течение трех недель. Соблюдение режима труда и отдыха. Во время повторной консультации принято решение об отмене препарата.
Консультация оториноларинголога. Хронический тонзиллит, простая форма, стадия ремиссии. Рекомендован курс промывания лакун миндалин № 10.
Пациентке рекомендована супрессивная терапия препаратом валацикловир 1000 мг один раз в сутки шесть месяцев. Соблюдение указаний невролога, оториноларинголога. Повторная консультация через два с половиной – три месяца.
Пациентка повторно явилась на прием через три месяца. Жалоб не предъявляла. На фоне проводимого лечения рецидивов ГВИ не отмечалось. Со слов больной, стрессовый фон на работе уменьшился, сон нормализовался (отменила Атаракс месяц назад).
Через два месяца после завершения курса супрессивной терапии жалобы отсутствовали. Рецидивов ГВИ не наблюдалось.
Читайте также:

