Какой вирус поражает иммунную систему человека
Обновлено: 18.04.2024
Проведя тщательный анализ этого образца, группа ученых во главе с Майклом Уороби (Michael Worobey) из университета Аризоны показала, что этот мужчина был инфицирован ВИЧ — вирусом, вызывающим синдром приобретенного иммунодефицита.
При жизни ни сам мужчина, ни его лечащие врачи об этом не знали. Формально вирус будет открыт лишь 17 лет спустя.
Извлекая крошечные генетические фрагменты из образца ткани, команда Уороби практически полностью реконструировала геном ВИЧ в том виде, в котором он существовал в те годы. А сама работа ученого помогла пролить свет на возникновение того, что станет причиной одной из самых важных пандемий в истории человечества.
В погоне за образцами
Вирус иммунодефицита человека был выявлен в 1980-х, после того как таинственный новый синдром затронул жителей США, и, как казалось, тогда он появился из ниоткуда. На самом деле эпидемия зародилась за несколько десятилетий до этого, просто на совсем другом континенте. В Африке.
Теперь мы можем с уверенностью утверждать, что по мере распространения геном вируса претерпевал постоянные изменения: сравнивая накопившиеся мутации и оценивая время, за которое они произошли, ученые могут проследить историю эволюции вируса вплоть до самого момента возникновения.
по теме

Общество
Наиболее вероятное место его появления — южный Камерун. А приблизительное время — 1920-е годы. Именно там и тогда вирус от шимпанзе перешел к человеку, перед тем как вскоре перебраться в город, известный в наше время как Киншаса.
В густонаселенном и быстрорастущем регионе с множеством потенциальных реципиентов вирус и обосновался, чтобы затем распространиться по всему миру.
Очевидно, что огромное количество людей тогда было инфицировано ВИЧ еще прежде, чем кто-то узнал о его существовании. Образцы тканей некоторых из погибших сохранились до наших дней: они рутинно собирались для исследований патологоанатомами, обрабатывались химическим фиксатором, располагались на восковых подложках, изучались под микроскопом (скорее всего, безрезультатно), а затем отправлялись в хранилище.
Но поскольку вирус до своего появления на Западе не был идентифицирован, определить заранее, какой именно образец ткани, взятый в то время, может содержать его следы, невозможно. Искать следы вируса в таких условиях — все равно что искать иголку в тысяче стогов сена.
Более того, процесс обработки химическим фиксатором и условия хранения образцов, дошедших до нашего времени, были таковы, что негативно влияли на содержащиеся в них РНК — молекулы, составляющие геном ВИЧ.
Вирус ВИЧ под микроскопом. Компьютерная Модель.
Однако нет ничего странного в том, что за два десятилетия поисков ученым удалось найти лишь два образца со следами вируса, собранных в Киншасе в период до его открытия.
Дэвид Хо (David Ho) из университета Рокфеллера (Rockefeller University) нашел следы вируса в образце крови, взятой в 1959 году; Уороби обнаружил их в кусочке лимфатического узла из 1960 года.
В обоих случаях от молекул РНК в целом сохранилось около одного процента. Но даже этих крошечных кусочков оказалось достаточно, чтобы доказать: именно ВИЧ блуждал по Киншасе за десятилетия до его открытия, а также чтобы наметить основные вехи истории его эволюции.
В то же время, ввиду ненадежности фрагментарных свидетельств, Уороби хотел собрать геном полностью. Целиком.
Его коллеги Софи Грисилс и Том Уоттс (Sophie Gryseels and Tom Watts) для этого разработали более точную технологию извлечения РНК и применили ее к более чем 1600 образцам тканей из Университета Киншасы (University of Kinshasa). И один из них, как оказалось, действительно содержал следы вируса.
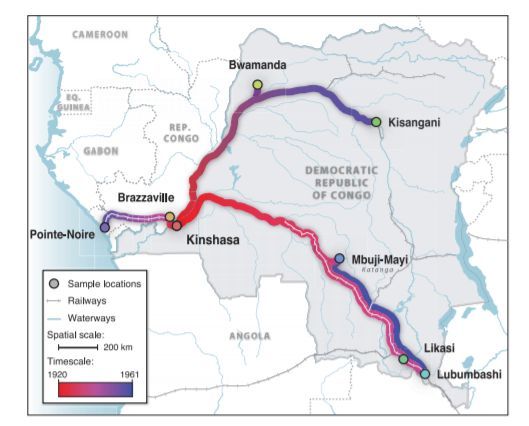
Скрытая эпидемия. Пути распространения ВИЧ в Африке до того, как вирус попал в США.
Место и время
Извлеченные образцы оказались больше всего похожи на подтип С, наиболее распространенный тип ВИЧ в Африке. Тот, что и сейчас доминирует в южной части континента.
На поверку генетический материал, попавший в руки ученых, является лишь малой частью того разнообразия, которое существовало в Киншасе в 1960-е.
А стало быть, из всех подтипов вируса лишь некоторые из тех, что в то время можно было обнаружить в городе, вырвались наружу, дабы стать общемировой проблемой.
История ВИЧ в датах
1930-е
Исследователи полагают, что приблизительно в 1930-х некая форма вируса иммунодефицита обезьян (SIV) перебралась к людям во время разделки или поедания мяса шимпанзе в Демократической Республике Конго. Этот вирус стали называть ВИЧ-1, и это самый распространенный тип вируса на сегодняшний день.
1959
Первый известный случай заболевания СПИДом выявлен при исследовании образцов плазмы крови мужчины, умершего в Демократической Республике Конго в 1959 году.
1960-е
ВИЧ-2, ареал распространения которого ограничен западной частью Африки, перешел к людям от обезьян вида дымчатый мангобей в Гвинее-Бисау в 1960-х.
Генетический анализ вируса, проведенный в 2003 году, говорит, что именно этот тип, вероятно, впервые перебрался в Соединенные Штаты примерно в 1968 году.
1970-е
На протяжении 1970-х вирус, оставаясь незамеченным, продолжает распространяться по США и остальному миру, начинается эпидемия.
1981
Высокая распространенность двух редких заболеваний — саркомы Капоши и пневмонии — отмечена среди молодых гомосексуальных мужчин в Нью-Йорке и Калифорнии в США. Это первый задокументированный случаи СПИДа. К концу года уже 121 человек умер от таинственного заболевания.
1982
Ученые центра по контролю и профилактике заболеваний (Centers for Disease Control and Prevention, CDC) в Атланте, США, предположили, что нарушение работы иммунной системы среди гей-сообщества вызвано инфекционным заболеванием. Они ввели термин Синдром приобретенного иммунодефицита (СПИД) и установили, что помимо геев в группу риска входят потребители инъекционных наркотиков, люди гаитянского происхождения и больные гемофилией. К концу 1982 года СПИД был обнаружен на пяти континентах.
1983
Эпидемия СПИДа бурно развивается в Европе: в первую очередь среди гей-сообщества, а также среди людей, имеющих тесные связи с центральной Африкой.
Начинается расследование случаев СПИДа в Руанде, Заире и других африканских странах.
1984
Используя недавно разработанные техники, в ходе нескольких исследований независимо друг от друга Люк Монтанье (Luc Montagnier) из Института Пастера в Париже (the Pasteur Institute in Paris), Франция, и Роберт Галло (Robert Gallo) из Национального института раковых заболеваний (the National Cancer Institute) в Вашингтоне, округ Колумбия, США, обнаруживают ретровирус, ответственный за развитие заболевания, известного как СПИД. Позднее он будет назван вирусом иммунодефицита человека (ВИЧ).
Случаи заболевания СПИДом все чаще начинают появляться в среде гетеросексуалов.
1985
В Атланте, США, проведена первая конференция, посвященная проблемам СПИДа.
Вслед за прошлогодним открытием вируса на рынке появляется первый метод тестирования на ВИЧ, одобренный Управлением по контролю за продуктами и лекарствами США (US Food and Drug Administration, FDA).
В США начинается тестирование крови в донорских пунктах.
1987
Азидотимидин (AZT), также известный как Зидовудин, первый противовирусный препарат, становится доступным для лечения ВИЧ после клинических испытаний. Препарат работает, блокируя действие обратной транскриптазы фермента ВИЧ, не давая вирусу размножаться в клетках. AZT замедляет развитие СПИДа, отдаляя смерть.
К 1987 году 16908 человек умерли от СПИДа в США. Всего Всемирная организация здравоохранения (ВОЗ) сообщила о 71571 случае заболевания СПИДом, из которых 47022 — в США.
По оценкам Всемирной организации здравоохранения, по всему миру носителями ВИЧ являются от 5 до 10 миллионов человек, ВОЗ запускает глобальную программу по борьбе со СПИДом.
1988
ВОЗ объявила 1 декабря всемирным днем борьбы с ВИЧ/СПИДом.
1991
Красная лента стала международным символом борьбы с ВИЧ/СПИДом.
1992
В США СПИД вышел на первое место среди причин смертности мужчин в возрасте от 24 до 44 лет.
Первые комбинированные лекарственные препараты для лечения ВИЧ появляются на рынке, после того как FDA наряду с AZT одобрило использование Zalcitabine (ddC), который также блокирует обратную транскриптазу.
Комбинированные препараты против ВИЧ оказываются более эффективными, а комплексное лечение замедляет развитие лекарственной резистентности.
1994
Использование AZT для предотвращения передачи ВИЧ от матери ребенку во время беременности рекомендовано в США. Исследование показало, что подобная терапия снижает шанс передачи вируса во время беременности до 8 %, в контрольной группе вероятность передачи составляла 25 %.
Через 12 лет после открытия вируса правительство США впервые запускает кампанию в медиа по пропаганде использования барьерных контрацептивов.
1995
ВОЗ объявила о достижении количеством зараженных миллионной отметки, всего же с начала эпидемии ВИЧ вирусом заразились более 19,5 миллиона человек.
1996
Международная инициатива по вакцинации против СПИДа (IAVI) — некоммерческая организация, базирующаяся в Нью-Йорке, — создана для ускорения поиска вакцины против ВИЧ.
90 % всех заболевших теперь проживают в развивающихся и развитых странах.
1997
Впервые благодаря появлению ВААРТ отмечено резкое падение смертности от СПИДа.
ООН объявляет, что к 2010 году 40 миллионов детей могут потерять одного или обоих родителей из-за СПИДа.
1998
Первые полномасштабные испытания вакцины против ВИЧ начинаются в США.
Две команды исследователей начинают разработку вакцин против штаммов ВИЧ, распространенных в странах Африки к югу от Сахары
В Сан-Франциско обнаружен штамм ВИЧ, устойчивый ко всем лекарственным средствам, подавляющим протеазу, которые в то время существовали на рынке. У некоторых пациентов, использующих для лечения ингибиторы протеазы, встречаются необычные побочные эффекты, такие как рост жировых отложений и проблемы с сердцем.
1999
33 миллиона человек инфицированы ВИЧ, а 14 миллионов умерли от СПИДа по всему миру.
СПИД становится одним из четырех самых массовых убийц современности.
2001
Индийская компания начинает продавать копии дорогих запатентованных лекарств против СПИДа через медицинскую благотворительную организацию в Африке. Этот шаг заставляет некоторые фармацевтические компании снижать цены.
2003
5 миллионов новых случаев СПИДа выявлены на протяжении 2003 года — самое большое количество с начала эпидемии. 3 миллиона человек умерли от СПИДа в этом же году.
2005
Около 40 миллионов человек инфицированы ВИЧ по всему миру.
Высокорезистивный штамм вируса, вызывающий быстрое развитие СПИДа, обнаружен в Нью-Йорке, США.
По оценкам ученых, сам ВИЧ возник где-то между 1896 и 1905 годом. Далеко не все вирусы так молоды. Когда ученые впервые обнаружили следы гепатита B времен Бронзового века, они подсчитали, что вирус менялся в 100 раз медленнее, чем предполагалось до этого. Открытие кардинально изменило предполагаемый период его возникновения. Даже ВИО (вирусы иммунодефицита обезьян), ближайшие родственники ВИЧ, поражающие шимпанзе, эволюционировали с разной скоростью в далеком прошлом и в новейшей истории, что делает оценку времени возникновения очень сложной.
В целом именно благодаря этому факту статистическими методами ученым удалось достаточно точно локализовать время и место начала пандемии. Установить, что с 1920-х годов именно Киншаса, ныне столица Демократической Республики Конго, стала центром первого очага эпидемии ВИЧ, а также положила начало эпидемии 1960-х годов в других частях континента.
Отсюда, из Киншасы, вирус прибыл на Гаити примерно в 1964 году. Причиной тому стало возвращение на родину жителей этого островного государства. До середины 60-х многие жители Гаити работали в только что получившем свою независимость Конго в качестве специалистов. И значительная часть гаитянских работников проживала именно в Киншасе.

Миграция из Гаити в США. Вторая половина 60-х тут наблюдается резкий рост. ВИЧ попадет в США именно в этот период.
Уже с Гаити вирус вместе с мигрантами перебрался на материк — в Соединенные Штаты Америки. Где очень быстро распространился среди гомосексуалов, воспользовавшись относительной уязвимостью перед ВИЧ именно этой группы.
Первые смерти от симптомов, крайне похожих на СПИД, будут зафиксированы здесь (преимущественно среди афроамериканских геев) уже в конце 60-х. Накануне знаменитых Стоунвольских бунтов, органично связанных с борьбой за права черного населения Америки и ставших отправной точкой эмансипации ЛГБТ-движения, завершившегося нынешней либерализаций законодательства относительной однополых браков и партнерств практически во всех западных странах.
Работа Уороби подтвердила эти и некоторые другие тезисы. Не на моделях, а на реальном генетическом материале.
ВИЧ-инфекция — это медленно прогрессирующее инфекционное заболевание, вызываемое вирусом иммунодефицита человека (ВИЧ).
Размножаясь, ВИЧ поражает клетки иммунной системы — так называемые CD4+ Т-лимфоциты. В результате чего количество их постепенно уменьшается.
Что это за клетки?
Они отвечают за уничтожение тех вирусов, которые попали в организм человека и смогли преодолеть гуморальный барьер.
Т-лимфоциты действуют не против возбудителей, циркулирующих в крови, а распознают измененную, то есть зараженную вирусом, клетку и разрушают ее. Клетки CD4 регулируют весь этот процесс, выполняя функцию иммунной памяти.
Именно поэтому против ВИЧ иммунная система не может сработать так, как это было бы с любым другим вирусом.
Стоит сразу отметить, что ВИЧ — вирус нестойкий, он погибает вне среды человеческого организма при высыхании содержащих его жидкостей и практически моментально погибает при температуре выше 56ºС.
ВИЧ содержится во всех биологических жидкостях человеческого организма. Однако достаточное для инфицирования количество ВИЧ может содержаться только в крови, сперме, предэякуляте, вагинальном секрете и грудном молоке.
Слюна, пот и моча не содержат достаточного для инфицирования количества вируса.
Пути инфицирования ВИЧ
Вероятность инфицирования при незащищенном контакте такого типа наиболее велика.
Некоторые другие практики, например оральный секс, могут подразумевать меньшую опасность инфицирования.
Несмотря на то, что в справочниках обычно для орального секса отмечается процент вероятности, отличный от нуля, за всю историю эпидемии пока достоверно не зафиксировано ни одного случая инфицирования таким образом — даже в том случае, если принимающий партнер проглатывает сперму после эякуляции.
Таким образом, получить ВИЧ может каждый независимо от пола, возраста, национальности, сексуальной ориентации, материального достатка или принадлежности к какой-либо социальной группе.
Часто люди могут знать, как необходимо поступать, чтобы избежать инфицирования, однако в силу социальных, культурных или экономических условий, в которых им приходится находиться, они могут воздерживаться от правильных действий.
Что такое СПИД?
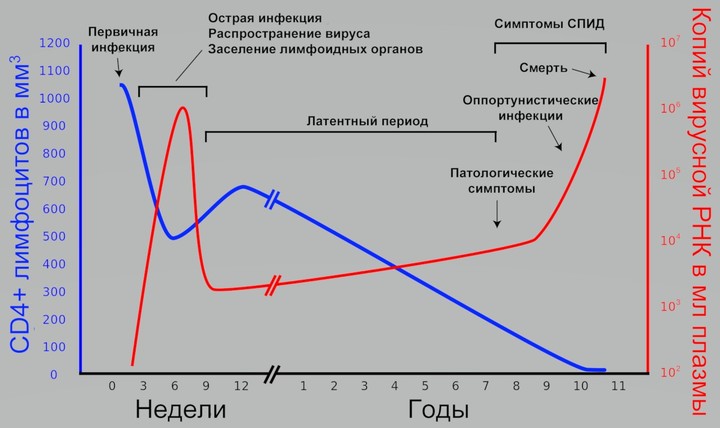
ВИЧ-инфекция течет медленно и почти бессимптомно. В течение многих лет она может никак не тревожить человека.
СПИД — синдром приобретенного иммунодефицита — тяжелое состояние, которое вызывается у человека длительным течением ВИЧ-инфекции.
Считается, что с момента проникновения вируса в организм до достижения стадии СПИДа проходит в среднем 10 лет (от 5 до 15 лет). Но только в том случае, если пациент, получив вирус, не начал лечение.
Антиретровирусная терапия является единственным средством для лечения ВИЧ-инфекции с доказанной эффективностью.
Если антиретровирусная терапия не начата вовремя и количество CD4+ Т-лимфоцитов снизилось ниже критического уровня 200 кл/мкл, у человека появляется вероятность развития СПИДа.
Но СПИДа можно избежать!
Что для этого нужно сделать? Необходимо как можно скорее после обнаружения в организме следов вируса начать так называемую антиретровирусную терапию (сокращенно АРВТ или АРТ).
Антиретровирусная терапия — это комбинация из 3-4 препаратов, которые блокируют размножение ВИЧ на разных этапах. Вследствие ее применения вирус иммунодефицита человека перестает размножаться.
Пока АРТ неспособна элиминировать вирус, то есть полностью вылечить ВИЧ-инфекцию, однако в состоянии не просто продлить жизнь ВИЧ-инфицированного человека, но и повысить ее качество.
Пациенты, которые получают АРТ, не болеют СПИДом!
Предполагаемая продолжительность жизни человека с ВИЧ-инфекцией, получающего АРТ, не отличается от таковой в общей популяции людей. Более того, человек, принимающий препараты АРТ и достигший неопределяемого уровня вирусной нагрузки, безопасен для своего сексуального партнера, даже в том случае, если занимается с ним сексом без презерватива.
Считается, что, если у человека с ВИЧ показатель вирусной нагрузки менее 200 копий, риск передачи отсутствует. Если этот показатель выше — риск безусловно есть. В этом случае ВИЧ-отрицательному партнеру советуется начать доконтактную профилактику (PrEP, ДКП).
Почему важно регулярно проходить тестирование на ВИЧ?
Зная результат обследования, вы избавитесь от неопределенности, связанной с тревожными размышлениями о том, что у вас может быть ВИЧ-инфекция, но вы не знаете об этом.
Плюсы тестирования:
Если результат теста показал, что у вас нет ВИЧ-инфекции, но при этом вы знаете, что ваше поведение связано с риском инфицирования, вы можете узнать, как быть осторожнее, дабы избежать инфицирования в будущем.
Впрочем, о тестировании не стоит забывать даже тем, кто состоит в моногамных отношениях: вы не можете знать наверняка, верен ли ваш партнер. Более того, испытывая чувство вины, он может стыдиться рассказывать вам о тех случайных связях, которые были у него на стороне.
Большинство тестов определяют не сам ВИЧ, а антитела к нему: иммунная система начинает вырабатывать их после того, как вирус попадает в организм. У 97 % людей антитела к ВИЧ выявляют в срок от 3 до 12 недель после инфицирования. В течение этого срока проверку можно проходить как в лабораторных условиях (ИФА-диагностика), так и при помощи домашней тест-системы — по крови или слюне.
Более чувствительные тесты (ИФА четвертого поколения) выявляют антигены, которые являются частью самого вируса и появляются в достаточном для определения количестве, пока антитела еще не появились. Подобные тест-системы показывают результат на сроке в 2—6 недель после инфицирования.
ПЦР-диагностика выявляет не антитела или антигены, а генетический материал вируса. Из-за высокой стоимости и сложности этот метод используется реже других. Он способен показать точный результат в срок от 1 до 4 недель.
Более подробно о том, каким бывает тестирование, вы можете узнать, вернувшись к оглавлению данного раздела.
ВИЧ-положительными называют людей, чей тест на ВИЧ показал положительный результат. То есть вирус в организме этого человека есть.
ВИЧ-отрицательными — людей, чей тест не обнаружил следов вируса в организме.
Знайте: тот факт, что у кого-то из вас обнаружена ВИЧ-инфекция, вовсе не означает, что вы должны отказываться от секса и/или отношений.
Но это значит, что как можно скорее вам нужно начать антиретровирусную терапию. От этого зависит ваше здоровье и здоровье вашего партнера.
Не бойтесь АРВ-терапии: несмотря на то, что в прошлом многие препараты от ВИЧ были весьма токсичны, сегодня они ничуть не опаснее других лекарств. Свои побочные эффекты есть и у них, но всех их можно избежать, если правильно подобрать схему лечения.
Запомните: схема подбирается врачом! Именно он обладает всеми необходимыми знаниями, чтобы определить, какие именно таблетки и по какому графику вам необходимо принимать. Не занимайтесь самолечением!
Если вы столкнулись с побочными эффектами, сообщите об этом вашему лечащему врачу в центре СПИД и попросите его подобрать для вас альтернативную схему терапии.
Как оценивают эффективность АРВТ и от чего она зависит?
Для оценки эффективности и неэффективности лечения используются разные критерии: вирусологические, иммунологические и клинические.
Вирусологическая эффективность — это уменьшение вирусной нагрузки до неопределяемой (менее 20 копий/мкл). Чем быстрее и значительнее упадет вирусная нагрузка, тем дольше терапия будет эффективной. Если через 6 месяцев после начала терапии вирусная нагрузка сохраняется выше порога определения — это вирусологическая неэффективность.
Причинами вирусологической неэффективности лечения могут быть:
низкая приверженность пациента лечению, то есть пропуск приема препаратов; несоблюдение других условий приема лекарств, например, таких как сочетание с пищей, межлекарственные взаимодействия; резистентность вируса к проводимой АРТ.
Иммунологическая эффективность — это увеличение количества CD4+ T- клеток. В разных исследованиях критерием иммунологического ответа служит прирост количества CD4+ T-клеток на 50 в микролитре, на 100 в мкл или на 200 в мкл. Или превышение CD4+ T-клетками порога в 200 кл/мкл или 500 кл/мкл. Под иммунологической неэффективностью подразумевается отсутствие прироста CD4+ T-клеток.
Стадия СПИДа наступает только в том случае, если количество CD4+ ниже 200 кл/мкл.
Клиническая эффективность
Клинический успех лечения оценивается как отсутствие СПИД- индикаторных заболеваний. Уменьшение выраженности общих симптомов.
Клинический успех лечения напрямую связан с вирусологическим и иммунологическим ответом на лечение.
Как рассказать партнеру, с которым я встречаюсь, что у меня ВИЧ?
Многие люди с ВИЧ-инфекцией сталкивались с отказом в отношениях, когда рассказывали о ВИЧ партнерам, с которыми встречались, из-за чего им было тяжело в дальнейшем принимать решение о раскрытии своего статуса.
Рассказать о себе партнеру будет проще, если вы предварительно обсудите это с другими ВИЧ-позитивными людьми или с профессионалом, работающим в этой сфере.
Однако помните, что ваш диагноз касается в первую очередь вас — это ваш личный мир, очень глубокая и интимная часть вас и вашей жизни.
От того, как и при каких обстоятельствах вы это преподнесете, будет зависеть реакция вашего партнера. Лучше всего рассказывать о том, что у вас ВИЧ-инфекция, тогда, когда вы сами приняли свой диагноз, а значит, перестал испытывать чувства вины и стыда, связанные с диагнозом.
Потому что состояние, находясь в котором, мы делимся чем-то сокровенным, отражается на собеседнике.
Теперь меня бросят, и я останусь один?
Нет. Не обязательно. Конечно, такая новость может огорчить и даже напугать вашего любимого человека, но это вовсе не означает, что он обязательно должен вас из-за этого бросить.
В мире много пар, в которых один из партнеров имеет положительный ВИЧ-статус, и эти пары остаются вместе, несмотря на ВИЧ.
Общение и честность являются ключевыми факторами укрепления и успешного развития отношений. Вы оба должны четко говорить о том, как вы чувствуете себя и что вы хотите друг от друга. Вам обоим нужно уметь внимательно слушать и слышать друг друга.
Вместо послесловия
В течение всех последних лет количество людей с ВИЧ в России растет, количество инфицированных от общего их числа равняется примерно одному проценту, то есть с ВИЧ живет практически каждый сотый россиянин. Это очень много.
Значительная часть из них — совсем не представители уязвимых групп, а гетеросексуальные мужчины и женщины, никогда не употреблявшие наркотиков.
Один из ста — совсем немного? Но это закон статистики: тем самым сотым может стать каждый. Вне зависимости от образа жизни, вероисповедания и социального статуса.
Более того, среди российских геев или мужчин, практикующих секс с мужчинами, носителем вируса по разным оценкам является каждый десятый или даже каждый пятый.
Это очень много. Именно поэтому Фонд помощи людям, живущим с ВИЧ, как и многие другие ВИЧ-сервисные организации, регулярно проводит анонимное бесплатное тестирование на ВИЧ.
В любое время пройти абсолютно анонимный тест (для этого не нужны ни прописка, ни паспорт) можно в открытом пространстве фонда СПИД.ЦЕНТР по адресу:
Москва, ул. Нижняя Сыромятническая, д. 11, с.1, офис 313.

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
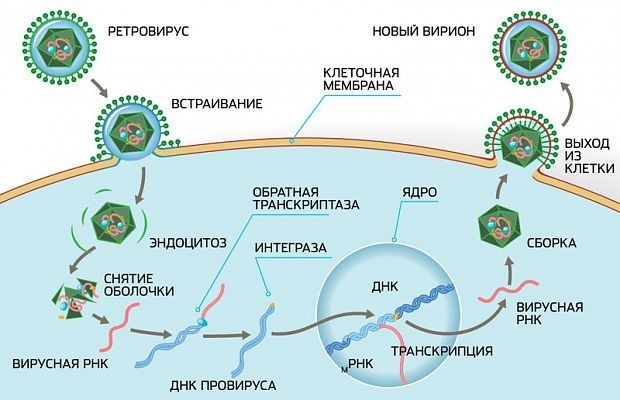
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
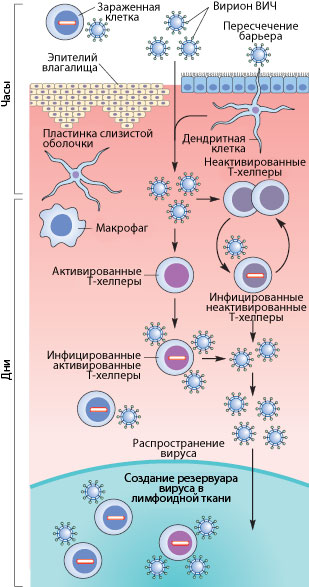
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
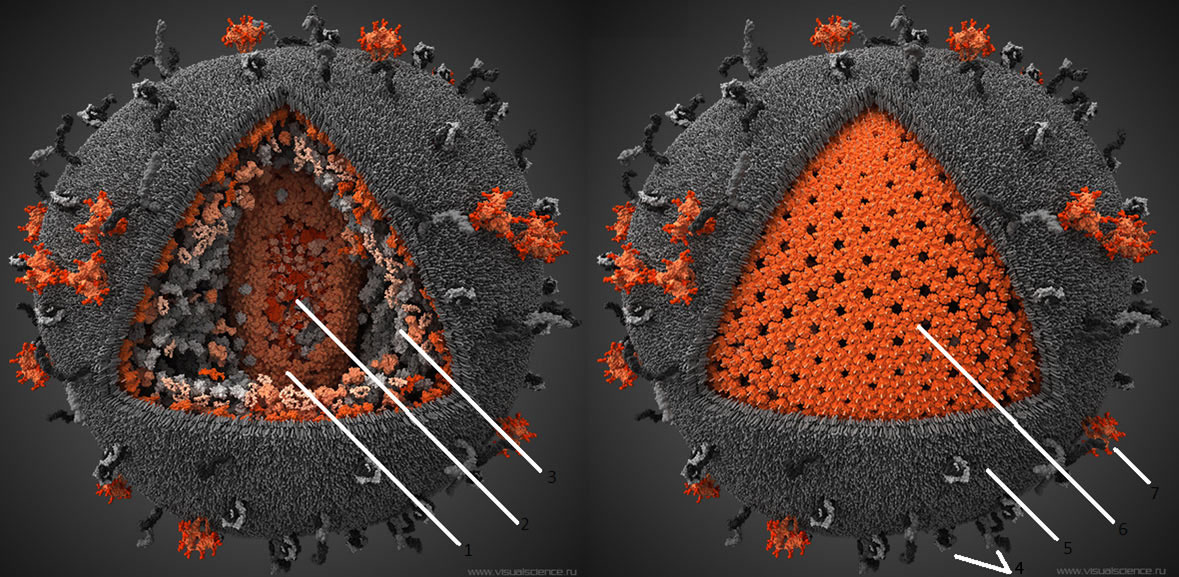
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.
Читайте также:

