Какой вирус уничтожает вич
Обновлено: 22.04.2024
Кандидат биологических наук А. ЛУШНИКОВА. По материалам "Scientific American".
Вирус иммунодефицита человека (ВИЧ) открыли в 1983 году сразу в двух лабораториях: в Институте Пастера во Франции, под руководством Люка Монтанье, и в Национальном институте рака (США), Роберт Галло и его сотрудники. Сейчас уже ни у кого нет сомнений в том, что ВИЧ вызывает страшную болезнь, "чуму ХХ века" - СПИД (это название расшифровывается как "синдром приобретенного иммунодефицита"). Однако за более чем десятилетнюю историю исследований накопилось немало загадок, связанных с развитием этого заболевания. Например, у некоторых зараженных вирусом иммунодефицита людей признаки болезни появляются спустя несколько лет или не появляются вовсе. Оказалось, что существуют люди, устойчивые к СПИДу. Как много таких людей, какими особенностями они обладают, не есть ли это ключ к лечению страшной болезни? На эти вопросы пытается ответить публикуемая статья.
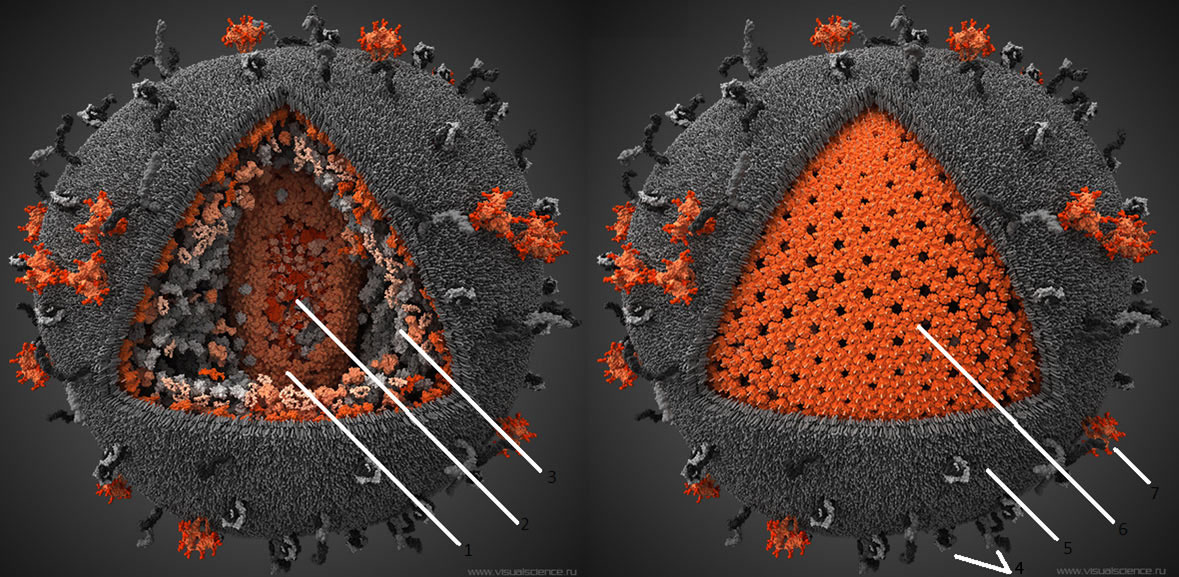
Так устроен вирус иммунодефицита человека. Внутри него находится наследственный материал - две молекулы РНК, на поверхности - белки оболочки.
У человека с обычным иммунитетом клетки-киллеры, несущие на своей поверхности молекулу-рецептор СD8, выделяют гормоноподобные вещества хемокины.
Если человек имеет нормальный ген ССR5, то под контролем этого гена в клетках-мишенях вырабатывается белок, который совместно с другим белком (СD4) служит "посадочной площадкой" для вируса иммунодефицита на поверхности клетки.
Иголка в стоге сена
Генетикам давно известны гены устойчивости к некоторым вирусам у мышей, например к вирусу лейкоза. Но существуют ли подобные гены у человека, и если да, то какова их роль в защите против СПИДа?
Стивен О'Брайн и Михаэль Дин со своими коллегами из Национального института рака США много лет вели поиск таких генов у человека.
В начале 80-х годов американские ученые исследовали множество людей, которые по тем или иным причинам могли заразиться вирусом иммунодефицита. Они проанализировали тысячи образцов крови и обнаружили, казалось бы, необъяснимое явление: у 10-25% обследованных вирус вообще не выявляется, а около 1% носителей ВИЧ - относительно здоровы, признаки СПИДа у них либо отсутствуют, либо выражены очень слабо, а иммунная система в полном порядке. Неужели существует какая-то устойчивость к вирусу у некоторых людей? И если да, то с чем она связана?
Опыты на лабораторных мышах, крысах, морских свинках и кроликах показали, что устойчивость к различным вирусным инфекциям часто определяется целым набором генов. Оказалось, что сходный механизм определяет и устойчивость к вирусу иммунодефицита человека.
Известно, что многие гены ответственны за выработку определенных белков. Часто бывает, что один и тот же ген существует в нескольких измененных вариантах. Такие "многоликие" гены называются полиморфными, а их варианты могут отвечать за выработку различных белков, которые по-разному ведут себя в клетке.
Сравнив восприимчивость к вирусам у мышей, несущих множество разнообразных наборов генов, и у мышей с небольшим числом генных вариантов, ученые пришли к выводу, что чем разнороднее генетически были животные, тем реже они заражались вирусом. В таком случае можно предположить, что в генетически разнообразных человеческих популяциях генные варианты, определяющие устойчивость к ВИЧ, должны встречаться достаточно часто. Анализ заболеваемости СПИДом среди американцев различных национальностей выявил еще одну особенность: более устойчивы американцы европейского происхождения, у африканцев и азиатов устойчивость близка к нулю. Чем объяснить такие различия?
Ответ на этот вопрос предложил в середине 80-х годов американский вирусолог Джей Леви из Калифорнийского университета в Сан-Франциско. Леви и его коллеги пытались выяснить, какие именно клетки в организме поражает вирус. Они обнаружили, что после того, как вирус заражает иммунные клетки, они легко узнаются иммунными клетками другого типа, так называемыми Т-киллерами (убийцами). Киллеры разрушают зараженные вирусом клетки, препятствуя дальнейшему размножению вируса. Клетки-убийцы несут на своей поверхности особую молекулу - рецептор CD8. Она, как принимающая антенна, "узнает" сигналы от клеток, зараженных вирусом, и клетки-убийцы уничтожают их. Если из крови удалить все клетки, несущие молекулу CD8, то вскоре в организме обнаруживаются многочисленные вирусные частицы, происходит быстрое размножение вируса и разрушение лимфоцитов. Не в этом ли ключ к разгадке?
В 1995 году группа американских ученых под руководством Р. Галло обнаружила вещества, которые вырабатываются в клетках-киллерах, несущих молекулы CD8, и подавляют размножение ВИЧ. Защитные вещества оказались гормоноподобными молекулами, называемыми хемокинами. Это небольшие белки, которые прикрепляются к молекулам-рецепторам на поверхности иммунных клеток, когда клетки направляются к месту воспаления или заражения. Оставалось найти "ворота", сквозь которые проникают в иммунные клетки вирусные частицы, то есть понять, с какими именно рецепторами взаимодействуют хемокины.
Ахиллесова пята иммунных клеток
Вскоре после открытия хемокинов Эдвард Бергер, биохимик из Национального института аллергических и инфекционных болезней в Бетезде, США, обнаружил в иммунных клетках, в первую очередь поражаемых вирусом (их называют клетки-мишени), сложный по строению белок. Этот белок как бы пронизывает мембраны клеток и содействует "посадке" и слиянию вирусных частиц с оболочкой иммунных клеток. Бергер назвал этот белок "фузин", от английского слова fusion - слияние. Оказалось, что фузин родствен белкам-рецепторам хемокинов. Не служит ли этот белок "входными воротами" иммунных клеток, через которые вирус проникает внутрь? В таком случае взаимодействие с фузином какого-нибудь другого вещества закроет доступ вирусным частицам в клетку: представьте, что в скважину замка вставляется ключ, и вирусная "лазейка" исчезает. Казалось бы, все встало на свои места, и взаимосвязь хемокины - фузин - ВИЧ уже не вызывала сомнений. Но верна ли эта схема для всех типов клеток, зараженных вирусом?
Пока молекулярные биологи распутывали сложный клубок событий, происходящих на поверхности клеток, генетики продолжали поиск генов устойчивости к вирусу иммунодефицита у людей. Американские исследователи из Национального института рака получили культуры клеток крови и различных тканей от сотен пациентов, зараженных ВИЧ. Из этих клеток выделили ДНК для поиска генов устойчивости.
Чтобы понять, насколько сложна эта задача, достаточно вспомнить, что в хромосомах человека содержится около 100 тысяч различных генов. Проверка хотя бы сотой доли этих генов потребовала бы нескольких лет напряженной работы. Круг генов-кандидатов заметно сузился, когда ученые сосредоточили свое внимание на клетках, которые прежде всего поражает вирус, - так называемых клетках-мишенях.
Уравнение со многими неизвестными
Одна из особенностей вируса иммунодефицита заключается в том, что его гены внедряются в наследственное вещество зараженной клетки и "затаиваются" там на время. Пока эта клетка растет и размножается, вирусные гены воспроизводятся вместе с собственными генами клетки. Затем они попадают в дочерние клетки и заражают их.
Из множества людей с высоким риском заражения ВИЧ отобрали зараженных вирусом и тех, кто не стал носителем ВИЧ, несмотря на постоянные контакты с больными. Среди зараженных выделили группы относительно здоровых и людей с быстро развивающимися признаками СПИДа, которые страдали сопутствующими заболеваниями: пневмонией, раком кожи и другими. Ученые изучили разные варианты взаимодействия вируса с организмом человека. Различный исход этого взаимодействия, по-видимому, зависел от набора генов у обследованных людей.
Выяснилось, что люди, устойчивые к СПИДу, имеют мутантные, измененные гены рецептора хемокинов - молекулы, к которой прикрепляется вирус, чтобы проникнуть в иммунную клетку. У них контакт иммунной клетки с вирусом невозможен, поскольку нет "принимающего устройства".
В это же время бельгийские ученые Михаэль Симпсон и Марк Парментье выделили ген другого рецептора. Им оказался белок, который также служит рецептором для связывания ВИЧ на поверхности иммунных клеток. Только взаимодействие этих двух молекул-рецепторов на поверхности иммунной клетки создает "посадочную площадку" для вируса.
Итак, основными "виновниками" заражения клеток вирусом иммунодефицита служат молекулы-рецепторы, названные CCR5 и CD4. Возник вопрос: что происходит с этими рецепторами при устойчивости к ВИЧ?
В июле 1996 года американская исследовательница Мэри Керингтон из Института рака сообщила, что нормальный ген рецептора ССR5 обнаруживается лишь у 1/5 обследованных ею пациентов. Дальнейший поиск вариантов этого гена среди двух тысяч больных дал удивительные результаты. Оказалось, что у 3% людей, не заразившихся вирусом, несмотря на контакты с больными, ген рецептора ССR5 измененный, мутантный. Например, при обследовании двух нью-йоркских гомосексуалистов - здоровых, несмотря на контакты с зараженными, выяснилось, что в их клетках образуется мутантный белок CCR5, не способный взаимодействовать с вирусными частицами. Подобные генетические варианты были найдены лишь у американцев европейского происхождения или у выходцев из западной Азии, у американцев же африканского и восточноазиатского происхождения не нашли "защитных" генов.
Оказалось также, что устойчивость некоторых пациентов к инфекции лишь временная, если они получили "спасительную" мутацию только от одного из своих родителей. Через несколько лет после заражения количество иммунных клеток в крови таких пациентов снижалось в 5 раз, и на этом фоне развивались сопутствующие СПИДу осложнения. Таким образом, неуязвимыми для ВИЧ были только носители сразу двух мутантных генов.
Но у обладателей одного мутантного гена признаки СПИДа все же развивались медленнее, чем у носителей двух нормальных генов, и такие больные лучше поддавались лечению.
Продолжение следует
Не так давно исследователи обнаружили разновидности чрезвычайно агрессивных вирусов. Людей, зараженных такими вирусами, не спасает даже присутствие двух мутантных генов, обеспечивающих устойчивость к ВИЧ.
Это заставляет продолжать поиск генов устойчивости к ВИЧ. Недавно американские исследователи О'Брайн и М. Дин с коллегами обнаружили ген, который, присутствуя у людей лишь в одной копии, задерживает развитие СПИДа на 2-3 года и более. Значит ли это, что появилось новое оружие в борьбе с вирусом, вызывающим СПИД? Скорее всего, ученые приоткрыли еще одну завесу над загадками ВИЧ, и это поможет медикам в поисках средств лечения "чумы ХХ века". В многочисленных популяциях американцев афро-азиатского происхождения мутантные гены так и не найдены, но тем не менее есть небольшие группы здоровых людей, контактировавших с зараженными. Это говорит о существовании других генов защиты иммунной системы от страшной инфекции. Пока можно лишь предполагать, что в различных популяциях человека сложились свои системы генетической защиты. По-видимому, и для других инфекционных заболеваний, включая вирусный гепатит, также имеются гены устойчивости к вирусам-возбудителям. Теперь уже никто из генетиков не сомневается в существовании таких генов для вируса иммунодефицита. Исследования последних лет дали надежду найти решение такой, казалось бы, неразрешимой проблемы, как борьба со СПИДом. Кто станет победителем в противоборстве ВИЧ - человек, покажет будущее.
Наука - здравоохранению
КАК ЛЕЧИТЬ СПИД. ПОИСК СТРАТЕГИИ
Результаты исследований последних лет заставили задуматься не только ученых и практических врачей, занимающихся проблемами СПИДа, но и фармацевтов. Раньше основное внимание уделялось комбинированному лечению инфекции, направленному против вируса. Применялись препараты, препятствующие размножению вируса в клетке: невипарин и атевирдин. Это так называемая группа ингибиторов обратной транскриптазы ВИЧ, которые не дают наследственному материалу вируса внедряться в ДНК иммунных клеток. Их сочетают с аналогами нуклеозидов типа зидовудина, диданозина и ставудина, которые облегчают течение болезни. Однако эти средства токсичны и обладают побочными действиями на организм, поэтому их нельзя считать оптимальными. Им на смену все чаще приходят более совершенные средства воздействия на ВИЧ.
В последнее время появилась возможность препятствовать "посадке" вирусных частиц на поверхность клеток. Известно, что этот процесс происходит за счет связывания вирусного белка gр120 с клеточными рецепторами. Искусственное блокирование мест связывания ВИЧ с помощью хемокинов должно защищать клетки от вторжения ВИЧ. Для этого нужно разработать специальные препараты-блокаторы.
Другой путь - получение антител, которые будут связываться с рецепторами ССR5, создающими "посадочную площадку". Такие антитела будут препятствовать взаимодействию этих рецепторов с вирусом, не давая доступа ВИЧ в клетки. Кроме того, можно вводить в организм фрагменты молекул ССR5. В ответ на это иммунная система начнет вырабатывать антитела к данному белку, которые также перекроют доступ к нему вирусных частиц.
Наиболее дорогостоящий способ обезопасить вирусные частицы - ввести в иммунные клетки новые мутантные гены. В результате сборка рецептора для "посадки" вируса на поверхности "оперированных" клеток прекратится, и вирусные частицы не смогут заразить такие клетки. Подобная защищающая терапия, по-видимому, наиболее перспективна при лечении больных СПИДом, хотя и весьма дорого стоит.
При лечении сопровождающих СПИД раковых заболеваний врачи чаще всего прибегают к высоким дозам химических препаратов и к облучению опухолей, что нарушает кроветворение и требует пересадки больным здорового костного мозга. А что, если в качестве донорских кроветворных клеток пересадить больному костный мозг, взятый от людей, генетически устойчивых к инфекции ВИЧ? Можно предположить, что после такой пересадки распространение вируса в организме пациента будет остановлено: ведь донорские клетки устойчивы к инфекции, поскольку не имеют рецепторов, позволяющих вирусу проникнуть через клеточную мембрану. Однако эту привлекательную идею вряд ли удастся воплотить в практику полностью. Дело в том, что иммунологические различия между пациентом и донором, как правило, приводят к отторжению пересаженной ткани, а иногда и к более серьезным последствиям, когда донорские клетки атакуют чужеродные для них клетки реципиента, вызывая их массовую гибель.
Т-киллеры - иммунные клетки, которые уничтожают зараженные вирусом клетки.
Рецепторы клеток - особые молекулы на поверхности, которые служат "опознавательным знаком" для вирусных частиц и других клеток.
Ген рецептора - ген, ответственный за выработку соответствующего белка.
Хемокины - гормоноподобные вещества на поверхности иммунных клеток, которые подавляют размножение вируса в организме.
Культура клеток - клетки, развивающиеся вне организма, в питательной среде пробирки.
Мутантные гены - измененные гены, не способные контролировать выработку нужного белка.
Клетки-мишени - иммунные клетки, которые в первую очередь поражает вирус.
Цифры и факты
- Сегодня в мире 29 миллионов зараженных вирусом иммунодефицита. 1,5 миллиона человек уже умерли от вызванного этим заражением СПИДа.
- Самый неблагополучный по СПИДу регион - Африка. В Европе лидируют Испания, Италия, Франция, Германия. С 1997 года к этим странам присоединилась Россия. На территории бывшего СССР зараженность ВИЧ распределяется так: 70% - Украина, 18,2% - Россия, 5,4% - Беларусь, 1,9% - Молдова, 1,3% - Казахстан, остальные - менее 0,5%.
- В России и странах ближнего зарубежья существует более 80 центров по профилактике и борьбе со СПИДом.
Читайте в любое время
У человека с обычным иммунитетом клетки-киллеры, несущие на своей поверхности молекулу-рецептор СD8, выделяют гормоноподобные вещества хемокины. Хемокины взаимодействуют с другими иммунными клетками-мишенями, которые в первую очередь заражает вирус иммунодефицита. Хемокины связываются с белком фузином на поверхности клеток-мишеней и тем самым закрывают доступ в клетку вирусным частицам. Те же клетки, которые вирус все-таки заразил, уничтожаются киллерами. Если клеток-киллеров с молекулой СD8 у человека не очень много, он все же заражается вирусом.
Если человек имеет нормальный ген ССR5, то под контролем этого гена в клетках-мишенях вырабатывается белок, который совместно с другим белком (СD4) служит "посадочной площадкой" для вируса иммунодефицита на поверхности клетки. Если же ген ССR5 мутантный, то взаимодействия с вирусом не происходит, и, несмотря на контакт с вирусом, человек остается здоровым.

Обзор
Автор
Редакторы
Обратите внимание!
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Эволюция и происхождение вирусов
В 2007 году сотрудники биологического факультета МГУ Л. Нефедова и А. Ким описали, как мог появиться один из видов вирусов — ретровирусы. Они провели сравнительный анализ геномов дрозофилы D. melanogaster и ее эндосимбионта (микроорганизма, живущего внутри дрозофилы) — бактерии Wolbachia pipientis. Полученные данные показали, что эндогенные ретровирусы группы gypsy могли произойти от мобильных элементов генома — ретротранспозонов. Причиной этому стало появление у ретротранспозонов одного нового гена — env, — который и превратил их в вирусы. Этот ген позволяет вирусам передаваться горизонтально, от клетки к клетке и от носителя к носителю, чего ретротранспозоны делать не могли. Именно так, как показал анализ, ретровирус gypsy передался из генома дрозофилы ее симбионту — вольбахии [7]. Это открытие упомянуто здесь не случайно. Оно нам понадобится для того, чтобы понять, чем вызваны трудности борьбы с вирусами.
Из давних письменных источников, оставленных историком Фукидидом и знахарем Галеном, нам известно о первых вирусных эпидемиях, возникших в Древней Греции в 430 году до н.э. и в Риме в 166 году. Часть вирусологов предполагает, что в Риме могла произойти первая зафиксированная в источниках эпидемия оспы. Тогда от неизвестного смертоносного вируса по всей Римской империи погибло несколько миллионов человек [8]. И с того времени европейский континент уже регулярно подвергался опустошающим нашествиям всевозможных эпидемий — в первую очередь, чумы, холеры и натуральной оспы. Эпидемии внезапно приходили одна за другой вместе с перемещавшимися на дальние расстояния людьми и опустошали целые города. И так же внезапно прекращались, ничем не проявляя себя сотни лет.
Вирус натуральной оспы стал первым инфекционным носителем, который представлял действительную угрозу для человечества и от которого погибало большое количество людей. Свирепствовавшая в средние века оспа буквально выкашивала целые города, оставляя после себя огромные кладбища погибших. В 2007 году в журнале Национальной академии наук США (PNAS) вышла работа группы американских ученых — И. Дэймона и его коллег, — которым на основе геномного анализа удалось установить предположительное время возникновения вируса натуральной оспы: более 16 тысяч лет назад. Интересно, что в этой же статье ученые недоумевают по поводу своего открытия: как так случилось, что, несмотря на древний возраст вируса, эпидемии оспы не упоминаются в Библии, а также в книгах древних римлян и греков [9]?
Строение вирусов и иммунный ответ организма

Рисунок 1. Первооткрыватель вирусов Д.И. Ивановский (1864–1920) (слева) и английский врач Эдвард Дженнер (справа).

Почти все известные науке вирусы имеют свою специфическую мишень в живом организме — определенный рецептор на поверхности клетки, к которому и прикрепляется вирус. Этот вирусный механизм и предопределяет, какие именно клетки пострадают от инфекции. К примеру, вирус полиомиелита может прикрепляться лишь к нейронам и потому поражает именно их, в то время как вирусы гепатита поражают только клетки печени. Некоторые вирусы — например, вирус гриппа А-типа и риновирус — прикрепляются к рецепторам гликофорин А и ICAM-1, которые характерны для нескольких видов клеток. Вирус иммунодефицита избирает в качестве мишеней целый ряд клеток: в первую очередь, клетки иммунной системы (Т-хелперы, макрофаги), а также эозинофилы, тимоциты, дендритные клетки, астроциты и другие, несущие на своей мембране специфический рецептор СD-4 и CXCR4-корецептор [13–15].

Одновременно с этим в организме реализуется еще один, молекулярный, защитный механизм: пораженные вирусом клетки начинают производить специальные белки — интерфероны, — о которых многие слышали в связи с гриппозной инфекцией. Существует три основных вида интерферонов. Синтез интерферона-альфа (ИФ-α) стимулируют лейкоциты. Он участвует в борьбе с вирусами и обладает противоопухолевым действием. Интерферон-бета (ИФ-β) производят клетки соединительной ткани, фибробласты. Он обладает таким же действием, как и ИФ-α, только с уклоном в противоопухолевый эффект. Интерферон-гамма (ИФ-γ) синтезируют Т-клетки (Т-хелперы и (СD8+) Т-лимфоциты), что придает ему свойства иммуномодулятора, усиливающего или ослабляющего иммунитет. Как именно интерфероны борются с вирусами? Они могут, в частности, блокировать работу чужеродных нуклеиновых кислот, не давая вирусу возможности реплицироваться (размножаться).

Причины поражений в борьбе с ВИЧ
Тем не менее нельзя сказать, что ничего не делается в борьбе с ВИЧ и нет никаких подвижек в этом вопросе. Сегодня уже определены перспективные направления в исследованиях, главные из которых: использование антисмысловых молекул (антисмысловых РНК), РНК-интерференция, аптамерная и химерная технологии [12]. Но пока эти антивирусные методы — дело научных институтов, а не широкой клинической практики*. И потому более миллиона человек, по официальным данным ВОЗ, погибают ежегодно от причин, связанных с ВИЧ и СПИДом.

Подобный вирусный механизм характерен не только для ВИЧ. Он описан и при инфицировании некоторыми другими опасными вирусами: такими, как вирусы Денге и Эбола. Но при ВИЧ антителозависимое усиление инфекции сопровождается еще несколькими факторами, делая его опасным и почти неуязвимым. Так, в 1991 году американские клеточные биологи из Мэриленда (Дж. Гудсмит с коллегами), изучая иммунный ответ на ВИЧ-вакцину, обнаружили так называемый феномен антигенного импринтинга [23]. Он был описан еще в далеком 1953 году при изучении вируса гриппа. Оказалось, что иммунная система запоминает самый первый вариант вируса ВИЧ и вырабатывает к нему специфические антитела. Когда вирус видоизменяется в результате точечных мутаций, а это происходит часто и быстро, иммунная система почему-то не реагирует на эти изменения, продолжая производить антитела к самому первому варианту вируса. Именно этот феномен, как считает ряд ученых, стоит препятствием перед созданием эффективной вакцины против ВИЧ.

Открытие биологов из МГУ — Нефёдовой и Кима, — о котором упоминалось в самом начале, также говорит в пользу этой, эволюционной, версии.

Сегодня не только ВИЧ представляет опасность для человечества, хотя он, конечно, самый главный наш вирусный враг. Так сложилось, что СМИ уделяют внимание, в основном, молниеносным инфекциям, вроде атипичной пневмонии или МЕRS, которыми быстро заражается сравнительно большое количество людей (и немало гибнет). Из-за этого в тени остаются медленно текущие инфекции, которые сегодня гораздо опаснее и коварнее коронавирусов* и даже вируса Эбола. К примеру, мало кто знает о мировой эпидемии гепатита С, вирус которого был открыт в 1989 году**. А ведь по всему миру сейчас насчитывается 150 млн человек — носителей вируса гепатита С! И, по данным ВОЗ, каждый год от этой инфекции умирает 350-500 тысяч человек [33]. Для сравнения — от лихорадки Эбола в 2014-2015 гг. (на состояние по июнь 2015 г.) погибли 11 184 человека [34].
* — Коронавирусы — РНК-содержащие вирусы, поверхность которых покрыта булавовидными отростками, придающими им форму короны. Коронавирусы поражают альвеолярный эпителий (выстилку легочных альвеол), повышая проницаемость клеток, что приводит к нарушению водно-электролитного баланса и развитию пневмонии.

Рисунок 8. Электронная микрофотография воссозданного вируса H1N1, вызвавшего эпидемию в 1918 г. Рисунок с сайта phil.cdc.gov.
Почему же вдруг сложилась такая ситуация, что буквально каждый год появляются новые, всё более опасные формы вирусов? По мнению ученых, главные причины — это сомкнутость популяции, когда происходит тесный контакт людей при их большом количестве, и снижение иммунитета вследствие загрязнения среды обитания и стрессов. Научный и технический прогресс создал такие возможности и средства передвижения, что носитель опасной инфекции уже через несколько суток может добраться с одного континента на другой, преодолев тысячи километров.

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
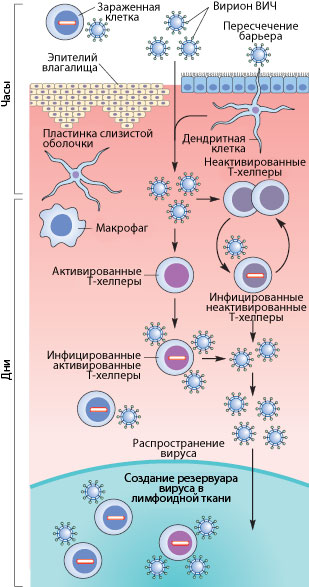
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
Иммунные клетки со спящим ВИЧ можно уничтожить с помощью других вирусов.
Вирус иммунодефицита трудно изгнать из организма не только потому, что он чрезвычайно изменчив и может уйти как от иммунной атаки, так и от лекарств. Проблема в том, что он способен оставаться в спящем виде, встроившись в геном клетки и никак себя не проявляя. Современные методы терапии позволяют снизить уровень активного вируса до ничтожных показателей, несмотря на всю его изменчивость. Но после курса лечения вирус, спящий в хромосомах клеток, может проснуться и начать размножаться.
Сейчас активно ищут способ добраться именно до неактивного вируса. В первую очередь на ум тут приходят какие-нибудь ДНК-редактирующие инструменты, которые проникали бы в иммунную клетку и вырезали из ее ДНК гены ВИЧ. Иной путь предлагают исследователи из больницы Оттавы: их идея состоит в том, чтобы просто уничтожать клетки, в которых поселился опасный постоялец. Но чем их уничтожать и как отличить лимфоциты с вирусом от лимфоцитов без вируса?
Джонатан Эйнджел (Jonathan B. Angel) и его коллеги некоторое время назад обнаружили, что в клетках со спящим вирусом плохо работает система интерфероновой противовирусной защиты. Когда вирус проникает в клетку, она начинает активно синтезировать белок интерферон, который чувствуют соседние клетки и начинают после этого готовиться к вирусной атаке. Кроме того, интерферон посылает соответствующие сигналы иммунной системе; наконец, интерферон действует на саму зараженную клетку так, чтобы она быстрее погибла и не дала бы вирусу размножаться и распространяться дальше.
Но, как мы сказали, у лимфоцитов с ВИЧ, даже если ВИЧ в них неактивен, интерфероновая защита ослаблена. В этом они похожи на некоторые разновидности рака. Против таких раковых клеток порой используют особые вирусы, которые называются онколитическими: за счет того, что система противовирусной защиты в них работает плохо, вирусы свободно в них размножаются и убивают большое количество своих злокачественных хозяев. Но если в ВИЧ-инфицированных клетках тоже не работают интерфероновая система, может, онколитические вирусы сработают и на них?
В статье в Journal of Infectious Diseases говорится, что так оно и есть. В экспериментах использовали вирус Мараба, или MG1, который действительно поражал и разрушал лимфоциты с ВИЧ, а здоровые клетки не трогал (очевидно, потому, что здоровые клетки деятельность онколитического вируса сами быстро пресекали). Вирус работал не только в клеточной культуре – когда его добавляли в кровь, взятую у ВИЧ-инфицированных, то уровень ДНК вируса иммунодефицита в образцах заметно падала.
В ближайшем будущем авторы работы как раз собираются это выяснить в опытах с животными – заодно удастся увидеть, как онколитический вирус сработает против ВИЧ не в культуре клеток и не в образце крови, а в настоящем организме.

Борьба с вирусом иммунодефицита человека (ВИЧ) не прекращается, и пока он остается нерешенной проблемой человечества. Современные методы лечения продлевают жизнь инфицированных людей практически до продолжительности жизни здоровых, но при этом они лишь подавляют репликацию вируса, не позволяя добиться полного излечения. Некоторая доля зараженных ВИЧ клеток не погибает и становится латентным (скрытым) резервуаром вируса. Ученые из США разработали специальные антитела, направляющие цитотоксичные Т-клетки на атаку латентных ВИЧ-клеток. Перспективы прямого применения этого подхода не очевидны, но полученные результаты могут оказаться важным шагом на пути разработки средств и методов полного излечения от СПИДа.
По данным Всемирной организации здравоохранения, на конец 2014 года с момента определения вируса иммунодефицита человека в 1981 году в мире заразились ВИЧ-инфекцией более 70 миллионов человек. Из них более 35 миллионов умерли, почти 37 миллионов живут инфицированными. Из-за широкого распространения и относительно быстрого роста числа зараженных ВИЧ присвоен статус пандемии (см. Epidemiology of HIV/AIDS). Особенно широко ВИЧ распространен на юге Африки (в некоторых странах этого региона, например в ЮАР и Ботсване, заражено больше 20% населения). В России, по данным на начало 2016 года, зафиксировано около миллиона ВИЧ-инфицированных, но по статистике только около половины больных знает о том, что они заражены ВИЧ, так что реальная картина может оказаться гораздо хуже.
ВИЧ заражает клетки иммунной системы и перестраивает их функции под свои потребности. В результате иммунная система подавляется и развивается синдром приобретенного иммунного дефицита (СПИД). Организм больного теряет возможность защищаться от инфекций и опухолей. Без лечения человек, зараженный ВИЧ, погибает в течение 9–11 лет от так называемых оппортунистических заболеваний, с которыми здоровый организм обычно успешно справляется.
ВИЧ во внешней среде нестабилен и передается только через кровь или биологические жидкости. Заражение происходит через поврежденные кожу и слизистые оболочки или при медицинских процедурах. В цикле репродукции ВИЧ вирусная РНК с помощью вирусной обратной транскиптазы превращается в ДНК и включается в геном клетки (рис. 2). Затем она транскрибируется в РНК, которая направляет синтез вирус-специфических белков, обеспечивающих размножение вируса и формирующих вирусную частицу, которая затем отпочковывается от клетки.

На разработку вакцин против ВИЧ были брошены значительные силы и средства, но об окончательной победе остается только мечтать. Причины неудач — в удивительной способности вируса изменять иммунологические свойства и таким образом уклоняться от действия антител, индуцированных вакциной.
Впрочем, в последние годы достигнут значительный прогресс в поддержании качества жизни больных СПИДом. Применение высокоэффективной комбинированной терапии, направленной против вирусных обратной транскриптазы и протеазы, при условии своевременного диагноза заражения позволяет продлить жизнь инфицированных людей практически до продолжительности жизни здоровых. Но некоторая доля клеток, зараженных ВИЧ (примерно одна из миллиона), не погибает и остается латентным резервуаром вируса, в котором ДНК ВИЧ интегрирована в геном, — и если противовирусную терапию прекратить, резервуар может активироваться и болезнь возобновится. Поэтому терапию приходится продолжать на протяжении всей жизни зараженного человека. Но противовирусная терапия стоит весьма дорого и может быть сопряжена с нежелательными побочными эффектами. Поэтому разработка подходов для ликвидации ВИЧ-резервуаров весьма актуальна и с медицинской, и с экономической точки зрения.
Недавно два коллектива исследователей, независимо друг от друга, практически одновременно опубликовали статьи, в которых описали оригинальный подход для ликвидации латентных ВИЧ-клеток. Обе статьи подготовлены научными коллективами из США. В обсуждаемых работах сделана попытка подойти к решению этой проблемы с помощью биспецифических антител (bi-specific antibodies).
Разработку биспецифических антител можно считать одним из наиболее важных достижений последнего времени в иммунологии и медицине, особенно в лечении онкологических заболеваний. Такой подход к лечению стали изучать в середине 80-х годов ХХ века, и довольно быстро исследования in vitro показали, что у него большой потенциал. В отличие от обычных природных антител (рис. 3), биспецифические антитела представляют собой искусственные белковые конструкции состоящие из фрагментов двух различных антител (рис. 4) и поэтому связывающиеся с двумя различными антигенами. Наиболее часто и успешно они используются для лечения рака. В этих случаях они чаще всего устроены так, что связывают цитотоксические Т-клетки (T-киллеры) иммунной системы (по их поверхностному антигену CD3) с раковыми клетками-мишенями, подлежащими уничтожению (по их поверхностному антигену).





Рис. 6. А, B — схема строения искусственно сконструированных биспецифических антител к антигену CD3 цитотоксических Т-клеток и поверхностному антигену ВИЧ; вариабельный домен из тяжелой белковой цепи (VH) соединен с вариабельным доменом из легкой цепи (VL). C — схема атаки клеток, зараженных ВИЧ. Изображение из обсуждаемой статьи J. Sung et al.
Авторы обеих работ полагают, что созданные ими биспецифические антитела потенциально могут стать эффективным иммунотерапевтическим средством для истребления латентных резервуаров ВИЧ. И научное сообщество, и общество в целом должны приветствовать и поддерживать исследования, направленные на полное излечение от ВИЧ. Но в данном случае перспективы клинического применения описанного подхода пока не вполне очевидны, необходимы дополнительные детальные исследования. Описанные исследования проводились in vitro, и неизвестно, в какой мере достигнутые эффекты будут иметь место в организме. Известно, что иммунотерапия с помощью чужеродных антител вызывает в организме иммунный ответ, направленный против этих антител. И такой побочный эффект действительно наблюдался группой A. Pegu et al. в опытах на обезьянах.
Агент, который бы индуцировал продукцию антигенов ВИЧ в латентно зараженных клетках, не повреждая при этом здоровые клетки, пока неизвестен. Более того, латентные резервуары ВИЧ могут находиться, например, в центральной нервной системе, куда проникновение белковых молекул затруднено из-за наличия гематоэнцефалического барьера. В общем, до применения полученных результатов пока очень далеко, и необходимо провести еще много исследований. Тем не менее, обсуждаемые работы представляются важным шагом на пути разработки средств и методов полного избавления от ВИЧ.
Источники:
1) Julia A. M. Sung et al. Dual-Affinity Re-Targeting proteins direct T cell-mediated cytolysis of latently HIV-infected cells // The Journal of Clinical Investigations. 2015. V. 125. P. 4077–4090.
2) Amarendra Pegu et al. Activation and lysis of human CD4 cells latently infected with HIV-1 // Nature Communications. 2015. V. 6. Article number: 8447.
3) Douglas D. Richman. HIV: Cure by killing // Nature. 2015. V. 528. P. 198–199. (Популярный синопсис к обсуждаемым статьям.)
Вячеслав Калинин
Снеер 17.02.2016 12:32 Ответить
ВИЧ/СПИД - РЕАЛЬНОСТЬ ИЛИ ВЫМЫСЕЛ?
Борьба со СПИДом идёт во всём мире уже более 30 лет. Однако, есть и такое мнение, что вируса иммунодефицита человека не существует в природе, и поэтому вся эта борьба совершенно бессмысленна.
Это альтернативное мнение разделяют тысячи людей по всему миру, включая известных учёных, врачей, журналистов, а также тех, кто лично столкнулся с этой проблемой, получив диагноз ВИЧ-инфекция, или этот диагноз был поставлен их близким.
Большинству людей практически ничего не известно об этом альтернативном мнении. И когда им предлагают, а зачастую можно сказать навязывают пройти обследование на ВИЧ-инфекцию, они делают это, совершенно не зная о том, какие последствия может вызвать это обследование. Причём эти последствия могут оказаться весьма и весьма неприятными, и даже трагическими.
Противники официальной теории ВИЧ/СПИДа считают, что тестирование на ВИЧ необходимо немедленно прекратить, а также прекратить назначение ВИЧ-позитивным пациентам так называемой антиретровирусной терапии против ВИЧ. По их мнению, эта практика, основанная на ложной ВИЧ/СПИД-теории, не несёт населению ничего, кроме геноцида.
Чтобы каждый человек смог самостоятельно разобраться в этой проблеме, и сделать для себя свои собственные выводы, и решить, стоит ли ему когда-либо тестироваться на ВИЧ-инфекцию или принимать лекарственные препараты против ВИЧ, стоит ознакомиться с этим альтернативным мнением. Ниже по ссылкам Вы можете найти 6 книг, 6 статей и 6 фильмов, достаточно подробно раскрывающих это мнение.
Если ранее Вы были абсолютно уверены в истинности официальной ВИЧ/СПИД-теории, то Вам стоит обратить внимание на эти материалы, чтобы избежать возможных негативных последствий, связанных с тестированием на ВИЧ или приёмом антиретровирусной терапии.
protopop " />
Снеер 17.02.2016 15:40 Ответить
Grecko " />
Снеер 19.02.2016 22:04 Ответить
Докажите делом, сходите в центр ВИЧ-профилактики, введите себе пару кубиков инфицированной крови и ни в коем случае не начинайте антиретровирсную терапию. Если это всё "миф" и "заговор", то Вам ничего не грозит, кроме всемирного признания и Нобелевки за опровержение вирусной теории ВИЧ/СПИД. Как, слабО?
aa 19.02.2016 01:04 Ответить
Может не совсем по теме - но так, задумался. Мы все знаем, что человек не может жить без кожи. Не только человек, но всякий зверь, даже гидра имеет свою примитивную кожу. Если объяснения появления мембраны у клетки еще как -то есть, например, пропусканием ультразвука
через раствор - подобие "липосом". Но то далекое и очень далекое подобие реальной клеточной мембраны. А как же быть с многоклеточными? Неужели, появление "кожи" объясняется только через начальный "симбиоз"? Конечно, мы то знаем, что мир был сотворен Богом. Но иногда интересно немного пофантазировать и конечно, теория эволюции является подходящей.
Gli4i " />
aa 20.02.2016 18:21 Ответить
aa 19.02.2016 01:10 Ответить
Хотя, в наше время, наверно, даже школьнику ясно, что если человек говорит, что все появилось случайно, а сам не сможет "создать" даже блошиной лапки - то тот человек просто умничает, либо шутит.
Grecko 19.02.2016 22:02 Ответить
Но если ВИЧ постоянно мутирует, то а) в организме с большой вероятностью одновременно будут сосуществовать несколько генетически различных линий вируса, и как результат б) данные антитела либо не будут действовать вообще, либо будут быстро "выдыхаться" в силу "генетического убегания" вируса. По-моему, это гораздо более серьёзный барьер для их перспективы, чем гематоэнцефалический.
Читайте также:

