Каков процент выздоровления при гепатите с
Обновлено: 18.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Определение
Хронический гепатит В – хроническое заболевание печени, продолжающееся более 6 месяцев, в основе которого лежит инфицирование и поражение печени вирусом гепатита В (HBV), проявляющееся воспалительными, некротическими и фибротическими изменениями печеночной ткани различной степени тяжести.
Острый гепатит В – острое инфекционное заболевание, вызываемое вирусом гепатита В (HBV). Характеризуется острым поражением печени и интоксикацией (с желтухой (35%) или без нее (65%)) и протекает с выраженным многообразием клинических проявлений и исходов: от выздоровления (около 90% пациентов) до развития хронического гепатита В, цирроза печени и гепатоцеллюлярной карциномы (печеночно-клеточного рака).
Гепатит B относится к заболеваниям, представляющим потенциальную угрозу для жизни, и является одной из основных проблем здравоохранения во всем мире.
Причины появления вирусного гепатита В
Заболевание имеет преимущественно парентеральный механизм передачи, то есть возбудитель попадает непосредственно в кровь: например, во время переливания крови, инвазивных исследований, оперативных вмешательств, гемодиализа и т.д.
В последние годы врачи констатируют увеличение полового пути передачи вируса. У 25% пациентов не удается установить источник заражения.
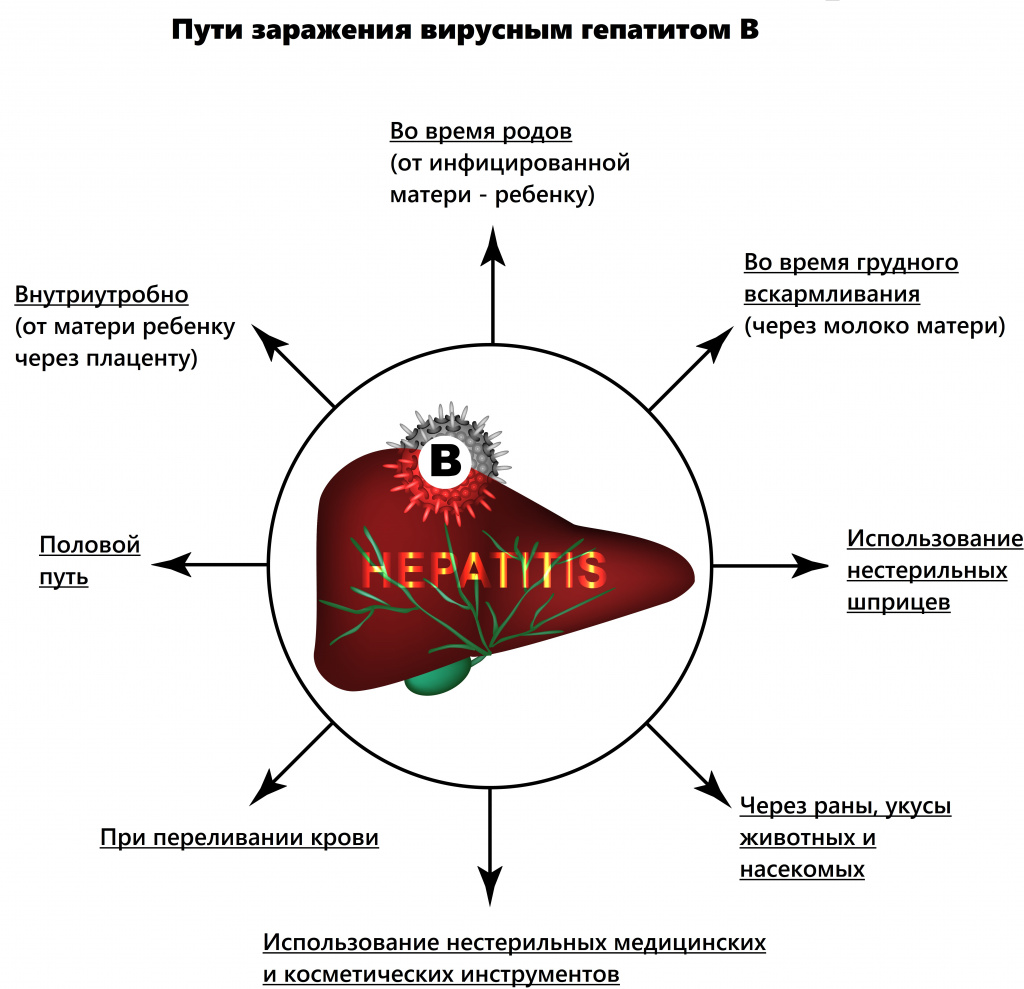
В группу риска входят гомосексуалисты, медицинские работники, члены семьи носителя HBV, пациенты с хроническими заболеваниями кожи. При развитии острого гепатита В в первом и втором триместрах беременности вероятность заражения плода небольшая, в третьем триместре инфицирование почти закономерно (вертикальный путь заражения).
Возбудитель заболевания - вирус из семейства гепаднавирусов, содержащий ДНК. Структура вируса:
- ядерный антиген (НВсАg);
- антиген инфекционности (НВеАg);
- поверхностный антиген (HBsAg);
- поверхностные белки для связывания с рецепторами гепатоцита (preS1-Ag и preS2-Ag);
- Х-антиген (НВхАg), регуляторный белок, усиливающий синтез вирусных белков.
Есть предположение, что именно он ответственен за канцерогенез и развитие гепатоцеллюлярной карциномы;
- вирусный гепатит В легкой степени;
- вирусный гепатит В средней степени тяжести;
- вирусный гепатит В тяжелый.
- острый (молниеносный) гепатит;
- хронический гепатит.
Инкубационный период
Продолжительность периода составляет в среднем от 30 до 180 дней. В течение этого времени пациент может предъявлять жалобы на головную боль, тошноту, хроническую усталость, ухудшение памяти и снижение аппетита. В некоторых случаях наблюдается вечернее незначительное повышение температуры тела.
Для этого периода развития заболевания характерны появление рвоты, изжоги, отрыжки, вздутие живота, боли в суставах и в мышцах, температура тела может повышаться до 38,00С.
Наблюдаются кожный зуд, желтуха, кровоизлияния на коже и кровоточивость десен, потемнение мочи и обесцвечивание кала, увеличивается печень, нарушается сон, пациент испытывает сильные головные боли, снижается артериальное давление, учащается сердцебиение, наблюдаются отеки ног.
При переходе гепатита в хроническую форму симптоматические проявления уменьшаются и наступает период ремиссии. Однако каждое новое обострение вирусного гепатита В протекает тяжелее предыдущего, что связано с разрушением ткани печени, которое постепенно приводит к развитию цирроза и печеночной недостаточности.
Переход гепатита В в цирроз
Для этой стадии характерно расстройство психики, наблюдаются кровотечения в области пищевода, желудка и прямой кишки, развивается асцит (в брюшной полости присутствует свободная жидкость), кожа становится бледной, печень уменьшается и становится плотной.
Диагностика
Лабораторные методы исследования – это первый этап диагностики заболевания.
В общем анализе крови может наблюдаться повышение лейкоцитов (более 9-11*109/л), сдвиг лейкоцитарной формулы влево и увеличение СОЭ (скорости оседания эритроцитов) более 30-40 мм/ч.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной. От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек. Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и первичный рак печени.
Эпидемиология
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5 до 2%. Существуют регионы, для которых характерна более высокая распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в изолированных поселениях в Японии. В России наблюдается рост заболеваемости гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году). Источниками заражения вирусным гепатитом C служат больные острыми и хроническими формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Основным путем инфицирования HCV является парентеральный. Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во время кардиохирургических операций, развивался острый вирусный гепатит C, у 60% из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик (5-8%). Возможна передача HCV от матерей с острой или хронической формой инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не удается.
Вирус гепатита С
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
Патогенез
Считают, что вирус оказывает прямое цитопатическое действие и вызывает иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
- возможностью внепеченочной репликации вируса, включая иммунокомпетентные клетки (клетки, предшественники гемопоэза, лимфоциты и моноциты периферической крови, миофибробласты);
- гетерогенностью генотипов и частыми мутациями генома вируса;
- индукцией каскада иммунопатологических реакций;
- активизацией процессов перекисного окисления липидов в печени.
В течении хронической HCV-инфекции может происходить нейтрализация мажорного варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV представляют собой движущуюся мишень, которую ограничивает иммунная система хозяина. Появление нового мажорного квазивида сопровождается повышением виремии и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый мажорный вариант заменяется. Такой процесс приводит к периодической волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС) и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные антигенные пептиды, представленные HLA-комплексом II класса на поверхностной мембране антиген-презентирующих клеток. В зависимости от типа цитокинового профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом, Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов, у которых болезнь перешла в хроническую стадию, в острой фазе вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2 цитокиновой продукции может играть важную роль в иммунопатогенезе хронической ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит является следствием повышенного уровня IL10, предполагаемого отрицательного регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса при хронической инфекции и, кроме того, может вызывать повреждение печени. Известно, что CTL способны быстро опознавать и направленно лизировать клетки, несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение свободных радикалов из митохондриальных электронно-транспортных путей и модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой эволюционно-отобранный механизм, с помощью которого вирус препятствует преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных клеточных культур прямая цитопатичность вируса гепатита С не может быть исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не удается элиминировать вирус. До сих пор нет ясного представления о том, почему это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями, обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию. В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти 20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов позволяет вирусу активно воздействовать на иммунную систему. Длительная ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская лимфома и появление органоспецифических и неспецифических аутоантител. Таким образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное заболевание.
Диагностика
Лабораторная диагностика гепатита С основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться разрешенными МЗ РФ к применению диагностическими препаратами отечественного или зарубежного производства в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время используют тест-системы третьего поколения ELISA-3. Подтверждающим методом является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом является слабость. Целенаправленный опрос больных часто помогает выявить такие факторы риска, как переливание крови, внутривенное введение наркотиков, хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью больных, активность сывороточных трансаминаз редко превышает верхнюю границу нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных трасаминаз не отражает степени изменений в печени: она может быть нормальной, несмотря на значительные морфологические изменения. Концентрация РНК ВГС в сыворотке имеет существенное значение для определения контагиозности и для мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая 105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше 40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и выполняют УЗИ печени.
Естественное течение и прогноз
Инфицирование ВГС приводит к развитию острого гепатита С, протекающего в манифестной (желтушной) или чаще в латентной (безжелтушной) формах, которые развиваются в соотношении 1:6. Около 17-25% больных острым гепатитом С выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С. Большинство больных с биохимическими и иммунологическими признаками хронического гепатита имеют слабовыраженную или умеренную степень воспалительно-некротического поражения печени и минимально выраженный фиброз. Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет развивается фиброз печени и может наступить смерть от цирроза печени и его осложнений. У 30-40% больных с циррозом печени высок риск заболевания раком печени.
Считается, что не более чем у 30% больных ВГС с минимальной морфологической активностью через 20 лет возможно развитие цирроза печени. Таким образом, больные, у которых при гистологическом исследовании биоптата печени выявляется наличие минимального воспаления и минимального фиброза, нуждаются в динамическом наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное разрешение хронической HCV-инфекции маловероятно.
Клиническая картина
У большинства больных с хроническим гепатитом С заболевание протекает бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии. Физикальный осмотр пациента помогает установить диагноз зачастую только на стадии цирроза печени.
Внепеченочные проявления HCV-инфекции
Ассоциация хронического гепатита С с различными внепеченочными проявлениями — хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые иммунные механизмы включают:
- моно- или поликлональную пролиферацию лимфоцитов;
- образование аутоантител;
- отложение иммунных комплексов;
- секрецию цитокинов.
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о триггерной роли вируса в инициации аутоиммунных процессов у генетически предрасположенного индивидуума.
Заболевания, ассоциированные с HCV-инфекцией
Ассоциированные с продукцией или отложением иммуноглобулинов:
- Криоглобулинемия
- Лейкоцитокластерный васкулит
- Мембранозно-пролиферативный гломерулонефрит
- В-клеточная лимфома
- Плазмоцитома
- MALTома
- Тиреоидит
- Синдром Шегрена
- Гемолитическая анемия
- Тромбоцитопения
- Красный плоский лишай
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1 (до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическое исследование печени
Гистологическая картина не является патогномоничной, при этом достаточно часто выявляются характерные изменения. Отличительная особенность ее — лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как изолированными, так и частью воспалительных изменений портальных трактов. По клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того, выявляются следующие характерные изменения: негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы (обнаруживаются редко), пролиферация и активация сателлитных клеток печени, пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше, чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
Лечение
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в каждом конкретном случае. Больные, у которых гистологическая активность минимальна, должны находиться под динамическим наблюдением, так как они имеют хороший жизненный прогноз без лечения и очень низкий риск развития цирроза печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при хронической HCV-инфекции:
- Возраст моложе 45 лет
- Женский пол
- Отсутствие ожирения
- Срок инфицирования менее 5 лет
- Отсутствие коинфекции HBV
- Отсутствие иммунодепрессии
- Отсутствие алкоголизма
- Умеренное повышение АЛТ
- Отсутствие цирроза
- Низкое содержание железа в печени
- Низкий уровень HCV RNA в сыворотке
- Генотип 2 или 3
- Однородность популяции вируса
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без результатов гистологического исследования противовирусное лечение проводить не рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, — это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется, лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это комбинация ИФa и рибавирина.
- в течение 6 месяцев - при генотипах 2 и 3;
- в течение 6 месяцев - при генотипе 1 и низком уровне виремии;
- в течение 12 месяцев - при генотипе 1 и высоком уровне виремии.
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы тела.
В последние годы для повышения эффективности интерферона применяют пегилирование, которое заключается в присоединении к молекуле интерферона полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный период полураспада. Предварительные данные свидетельствуют о большей эффективности такого лечения по сравнению с терапией интерфероном альфа.
Другие противовирусные препараты в лечении хронического гепатита С
Имеются данные, свидетельствующие о положительном действии таких препаратов, как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
Вирусный гепатит С является одной из главных причин хронических заболеваний печени. Первичная диагностика гепатита С осуществляется путем определения антител к белкам вируса гепатита С (ВГС) в сыворотках с использованием широко представленных на рынке тест-систем для иммуноферментного анализа (ИФА). Положительные результаты, полученные при скрининге сывороток, несут информацию о самом факте инфицирования, однако серологические методы не позволяют разграничить разрешившуюся острую инфекцию от хронического заболевания, а также оценить эффективность антивирусной терапии. В связи с этим для установления диагноза и характеристики активности хронического гепатита наряду с комплексным клиническим обследованием пациентов проводятся вирусологические исследования, направленные на определение прямых маркеров ВГС - РНК и вирусспецифических белков.
Патогенез гепатита С остается во многом неясным. До сих пор не существует однозначного ответа на вопрос, как присутствие вируса в организме влияет на развитие заболевания. Во многом это обусловлено тем, что исследователи этой проблемы получают противоречивые результаты. В этом обзоре мы постарались коротко изложить существующие в настоящее время опубликованные данные и результаты собственных исследований, касающиеся связи между присутствием РНК и белков ВГС в организме больных и активностью хронического гепатита С.
Для изучения распределения РНК вируса гепатита С в различных органах и тканях инфицированного организма применяют методы полимеразной цепной реакции с этапом обратной транскрипции (ОТ-ПЦР), гибридизации in situ, ПЦР in situ. Вирусные белки выявляют либо с помощью поликлональных сывороток, либо с помощью моноклональных антител.
Для оценки влияния вирусной нагрузки на активность хронического гепатита С, которая может варьировать от минимальных гистологических изменений в печени до случаев цирроза и гепатокарциномы, используют различные варианты количественного и полуколичественного методов ОТПЦР. Активность патологического процесса в печени оценивают по уровню активности фермента аланинаминотрансферазы (АЛТ), индексу гистологической активности (ИГА). Стадию заболевания характеризуют, используя гистологический индекс склероза (ГИС). Гистологический диагноз (ИГА и ГИС) ставится на основании морфологического изучения биопсийного материала печени и выражается в баллах в соответствии с международной классификацией (DesmetV.J. et al., 1994).
По данным ряда исследователей, репликация вируса возрастает по мере прогрессирования болезни (Cho S.W. et al., 1996), и более высокий уровень виремии коррелирует с более серьезным повреждением печени (Gretch D. et al., 1994). При исследовании парафиновых срезов печени Dries V. с соавт. (1999) отмечали более частое выявление РНК В ГС в печени пациентов с высоким уровнем воспалительной активности по сравнению со случаями, при которых повреждения печени были минимальны. По мнению авторов, это связано с тем, что вирусная нагрузка клеток печени может определять воспалительно-некротическую реакцию (Dries V. et al., 1999). По данным Jamal M.M. с соавт. (1999), у пациентов с постоянно нормальным уровнем АЛТ наблюдается значительно более низкий уровень РНК ВГС в печени, чем у больных с повышенным уровнем АЛТ. Adinolfi L.E. с соавт. (1998) указывают, что у пациентов с циррозом печени уровень РНК в печени превышает таковой у пациентов с низким уровнем ИГА (1-4). Наиболее высокий уровень РНК ВГС в печени наблюдается у больных с ИГА>8 (Adinolfi L.E.etal., 1998).
В противоположность этому большинство исследователей сходятся на том, что прямая связь между количеством РНК ВГС в организме (как в печени, так и в периферической крови) и степенью активности патологического процесса отсутствует (BallardiniG.etal., 1997, McGuinnesP.H. et al., 1996, Negro F. et al., 1998, 1999, Rodriguez-Inigo E.et al., 1999, Sugano M. et al., 1995). Поданным этих авторов, присутствие вируса в организме и уровень вирусной РНК не коррелируют со значениями ИГА, ГИС или АЛТ. Есть данные об уменьшении уровня вирусной РНК в печени при прогрессировании хронического гепатита С (Di MartinoetaL, 1997).
Результаты, полученные в нашей лаборатории, согласуются с последней концепцией: при исследовании материалов (ткани печени, сыворотки и лимфоцитов периферической крови) от 75 пациентов с хроническим гепатитом С не было обнаружено достоверных отличий между частотой выявления РНК ВГС у больных с различной активностью заболевания (Лакина Е.И. и др., 2000). При проведении нами количественного анализа уровня РНК ВГС в сыворотке крови больных ХГС (Amplicor Monitor Test, v.2.0., "Roche Diagnostics") также не выявлено значимой корреляции между показателями ИГА, ГИС, АЛТ и уровнем виремии.
В настоящее время в литературе активно обсуждается вопрос о роли лимфоцитов в развитии ВГС-инфекции. Результаты выявления РНК ВГС в мононуклеарах периферической крови больных гепатитом С, полученные разными исследователями, варьируют в широких пределах. Так, по данным одних авторов, РНК ВГС в мононуклеарах периферической крови встречается у 24% больных (Young K.S. et al., 1993), по данным других - у всех (100%) обследованных (MellorG. et al., 1998, OkumuraA. et al., 1998). Согласно нашим данным, РНК ВГС в лимфоцитах периферической крови выявляется в 64% случаев. Связи между наличием ВГС в лимфоцитах и активностью гепатита С не обнаружено.
Zignego A.L. с соавт. (1995) показали, что РНК вируса чаще встречается в клетках крови пациентов с более серьезными повреждениями печени. Для объяснения существования этой связи авторы предположили, что активная инфекция различных субпопуляций клеток, вовлеченных в иммунный ответ хозяина, может нарушать их функцию, приводя к персистенции ВГС и развитию хронических повреждений печени. Частое обнаружение РНК ВГС в периферических мононуклеарах больных с хроническими повреждениями печени может объясняться тем, что при длительной ВГС-инфекции клеток печени происходит увеличение пула инфицированных лимфоидных клеток путем передачи от клетки к клетке (Zignego et al., 1995). Показано, что инфицированные лимфоидные клетки могут быть причиной заражения здоровой печени, пересаженной в организм ВГС-инфицированного пациента (Feray С. et al., 1992). Внепеченочный резервуар инфекции может также служить источником реактивации болезни после прекращения интерферонотерапии (Gil В. et al., 1993).
При изучении вопроса о том, насколько уровень вируса в сыворотке отражает его количество в печени, данные исследователей расходятся. Тогда как одни авторы выявляют корреляцию между присутствием геномной РНК в печени и уровнем виремии (De Moliner L. et al., 1998, Mc Guinnes P.H. et al., 1996, Negro F. et al., 1999), другие (Ballardini G. et al., 1997) подобную связь отрицают. Martin с соавт. (1998) указывают на существование корреляции между количеством РНК ВГС в печени и в сыворотке крови, но не в периферических мононуклеарах. В работе Sugano M. с соавт. (1995) сообщается о положительной корреляции между уровнем РНК ВГС в печени и сыворотке крови до лечения интерфероном. После интерферонотерапии корреляция между количеством РНК в печени и в сыворотке не была обнаружена. Подсчет инфицированных клеток в печени после проведения гибридизации in situ показал, что число клеток, содержащих РНК ВГС, может колебаться от 4,8% до 87,6% у разных больных, и уровень виремии прямо зависит от числа инфицированных клеток в печени (Gosalvez J. et al., 1998, Lau G.K.K. et al., 1994, Rodriguez-Inigo E. et al., 1999). При сопоставлении частоты выявления РНК ВГС в печени и в сыворотке крови нами были получены результаты, согласно которым примерно в трети случаев возникает ситуация, когда при наличии вируса в печени РНК ВГС в сыворотке не выявляется: частота выявления РНК ВГС в печени составляет 86%, в сыворотке крови -51%. Эти результаты согласуются с данными других авторов (Haydon G.H. et al.„ 1998, Seidi S. et al., 1999). Например, в работе Haydon G.H. с соавт. (1998) геномная РНК ВГС выявлена в клетках печени 10 из 12 пациентов, негативных по этому показателю в сыворотке.
Жизненный цикл ВГС включает образование репликативных (минус-) цепей РНК, которые служат матрицей для образования геномных молекул. Частота выявления репликативной формы РНК ВГС по данным одних исследователей составляет 35% случаев (Gastaldi M. et al., 1995), тогда как по данным других до 100% (Okabe M. et al., 1997, Sansonno D. et al., 1997, Chang M. et al., 2000). Существенное расхождение данных может объясняться трудностями, возникающими при определении минус-РНК, так как количество негативных цепей РНК на один (lanford R.E. et al., 1995) - три (Mellor J. et al., 1998) порядка ниже, чем +РНК. Это объясняется тем, что одна молекула -РНК может служить матрицей для синтеза нескольких геномных молекул.
Среди исследователей нет единого мнения о том, насколько репликация вируса связана с процессами повреждения печени и выходом вирусных частиц в периферическую кровь (De Moliner L. et al., 1998. Negro F. et al., 1999). По данным Negro F. с соавт. (1998, 1999), использовавших полуколичественный метод PCR, нет строгой связи между вирусной репликацией и уровнем виремии. Согласно полученным нами данным, репликация вируса в печени сопровождается большей частотой выявления РНК ВГС в сыворотке крови, однако достоверной корреляции между этими параметрами не обнаружено. Несоответствие между количеством выявленных геномной и репликативной форм РНК ВГС в печени и уровнем виремии может быть следствием ряда причин: 1 - элиминации вируса из сыворотки с помощью специфических антител; 2 - поступления ВГС в периферическую кровь не только из печени, но и из других органов и тканей; 3 - нарушения процесса высвобождения вируса из клеток печени под действием лекарственных средств или других факторов (Negro F. et al., 1998). Опыты, проведенные в нашей лаборатории, не выявили достоверной корреляции между частотой встречаемости минус-РНК ВГС в печени и степенью поражения печеночной ткани (Лакина Е.И. и др., 2000). Это согласуется с предположением, что вирус может реплицироваться, не вызывая серьезных повреждений в ткани печени (Negro F. et al., 1998). Однако есть данные о возможном участии вирусной репликации в развитии цитопатического эффекта (Chang M. et al., 2000, Tsutsumi M. et al., 1994). С помощью метода гибридизации in situ показано, что клетки, содержащие репликативную форму РНК вируса, локализованы преимущественно в очагах поражения печени (Tsutsumi M. et al., 1994). Обнаружена достоверная корреляция между количеством гепатоцитов, содержащих репликативную форму РНК ВГС, и степенью воспаления печени. Следует отметить, что для геномной РНК ВГС авторы такой связи не выявили (Chang M. et al., 2000).
Согласно мнению большинства исследователей, хотя печень и является главным органом, где происходит вирусная репликация, ВГС может реплицироваться в периферических мононуклеарах, лимфатических узлах, поджелудочной железе, в меньшей степени - в костном мозге, селезенке, щитовидной железе и надпочечниках (Lerat Н. et al., 1996, Okumura A. et al., 1998, Gowans E.J., 2000, Grovatto M. et al., 2000, Radkoowski M. et al., 2000).
Наряду с определением РНК, перспективным методом изучения активности вирусной репродукции является выявление вирусных белков непосредственно в тканях с помощью иммуногистохимических методов (ИГХ). В качестве иммунных реагентов для детекции антигенов ВГС используются как моноклональные антитела (Ballardini G. et al., 1995, Gonzalez-Peralta R.P. et al., 1994, Noun-Aria K.T et al., 1995, Sansonno D. et al., 1995, Nayak N.C., SatharS.A., 1999), так и поликлональные антисыворотки, полученные от экспериментально иммунизированных животных (Gonzalez-Peralta R.P. et al., 1994, Tsutsumi M. et al., 1994) или больных хроническим гепатитом С людей (Ballardini G. et al., 1995, Nouri-Aria K.T. et al., 1995).
Большой интерес представляет вопрос о связи экспрессии вирусных белков с активностью патологических процессов в печени. Согласно большинству исследований, число гепатоцитов, содержащих вирусные антигены, не коррелирует ни со степенью гистологических изменений в печени, ни с показателями биохимической активности (Gonzalez-Peralta R.P. et al., 1994, Nayak N.C., Sathar S.A., 1999, Gowans E.J., 2000). С другой стороны, Hiramatsu N. с соавт. (1992) показали, что экспрессия антигенов ВГС в печени возрастала с увеличением степени поражения органа. Sansonno D., Damacco F. (1993), изучая печень больных острым гепатитом С, обнаружили топографическую связь между очагами воспаления и некроза с одной стороны и гепатоцитами, экспрессирующими антигены ВГС, - с другой. Однако при переходе болезни в хроническое состояние эта связь не обнаруживалась.
Мы изучали распределение антигенов нуклеокапсида, неструктурных белков NS3, NS4A и NS4B с помощью полученных нами МКА в клетках печени больных хроническим гепатитом С на криостатных срезах печени. Были использованы биопсийные материалы от больных с различной активностью гепатита С и на разных стадиях заболевания. Параллельно ткань печени анализировали методом RT-PCR на наличие геномной и репликативной цепей РНК ВГС. В целом, антигены ВГС обнаружены в печени 33 из 34 (97%) пациентов, имеющих геномную РНК в ткани печени. Уровень детекции белка нуклеокапсида составлял 53%, NS3 - 76%, NS4 - 81%. Репликативная форма РНК ВГС значительно чаще ассоциировалась с выявлением соrе-белка. При этом доля антиген-позитивных гепатоцитов варьировала в широких пределах от 1 до 90% у разных пациентов, составляя в среднем около 32%. У больных с ХГС обнаружены качественные и количественные различия в соотношении структурных и неструктурных белков ВГС в клетках печени. В целом, все исследованные белки накапливались в печени пациентов с более тяжелыми формами ХГС (Абдулмеджидова АГ. и др., 2000). Между антиген-содержащими клетками и очагами воспаления и некроза ткани печени топографической связи выявлено не было, что подтверждает ранее полученные данные (Sansonno D., Damacco F., 1993). Эти результаты свидетельствуют в пользу гипотезы об отсутствии прямого цитопатического действия ВГС.
Анализ внутриклеточной локализации вирусных белков методом ИГХ показал, что специфическое окрашивание наблюдается только в цитоплазме гепатоцитов, что согласуется с большинством опубликованных работ (Ballardini G. et al., 1997, Blight К. et al., 1994, Brody R.I. et al., 1998, Gonzalez-Peralta et al., 1994, 1995, Nouri-Aria K.T. et al., 1995, Sansonno D. et al., 1995 (a,b), 1997).
Большой интерес представляет использование моноклональных антител для выявления белка нуклеокапсида ВГС в сыворотках крови больных гепатитом С и доноров (Onto E. et al., 1996, Jolivet-Reynaud С. et al., 1998, Masalova O.V. et al., 1998). Подобные исследования наталкиваются на две основные трудности: низкая концентрация вируса и блокирование антигенов ВГС антителами в составе иммунных комплексов (Onto E. et al., 1996, Shiratori Y. et al., 1997). В нашей лаборатории разработан метод для количественного определения соге-белка, входящего в состав циркулирующих в плазме "свободных" вирионов и иммунных комплексов. При исследовании плазм от 80 антиВГС-позитивных доноров оказалось, что вирусная РНК выявляется только в половине образцов. В 94,4% РНК-позитивных плазм выявлен и белок нуклеокапсида ВГС. Концентрация белка core в разных образцах варьировала в широких пределах и составляла 5-850 пг/мл (Масалова О.В. и др., 2000). В сыворотках пациентов с ХГС (n=71) белок нуклеокапсида был обнаружен у 74% больных. Концентрация соге-белка не коррелировала с тяжестью заболевания Показано, что циркуляция ВГС в виде иммунных комплексов ассоциирована с более продвинутой стадией ХГС (согласно значениям ГИС) (Masalova O.V. et al., 2000). Тест-системы для ИФА на основе моноклональных антител, позволяющие определять белок нуклеокапсида не только на качественном, но и на количественном уровне, являются более простым и дешевым, чем ПЦР, методом выявления ВГС. Их внедрение в практику здравоохранения может существенно обогатить возможности современной диагностики и контроля за течением гепатита С.
Таким образом, несмотря на десятилетнее изучение вопроса о связи между присутствием вируса гепатита С в организме и прогрессированием хронического гепатита, многое по-прежнему остается неясным. Данные о роли вирусного генома и вирусных белков в патогенезе инфекции противоречивы. Необходимы дальнейшие исследования по комплексному анализу обоих компонентов иммунного распознавания: вируса (РНК, структурных и неструктурных белков) и иммунной системы хозяина (антител к ВГС, Т-клеток, цитокинов и иммунных комплексов). Эти знания необходимы для разработки эффективных средств профилактики и специфических препаратов для лечения гепатита С, что позволит контролировать это широко распространенное тяжелое заболевание человека.
* Работа поддержана РФФИ, проект № 01-04-48890
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

