Китай африканская чума свиней вакцина
Обновлено: 18.04.2024
На фоне эпидемии коронавируса мир забыл про другой вирус, который распространяется со зловещей быстротой. Африканская чума свиней (АЧС) охватила сегодня многие страны, включая Россию. Наши ученые заявляют, что отечественная вакцина от АЧС должна появиться к концу 2021 года - раньше, чем в других странах.
Ирина Мишина
Африканская чума свиней поразила сегодня многие страны ЕС, Китай, США. В Россию этот вирус пришел в 2007 году. Похоже, сейчас начался новый всплеск этого заболевания. Сразу оговоримся: для человека вирус АЧС опасности не представляет, он поражает животных и наносит серьезный урон сельскому хозяйству. Африканская чума свиней – вирусное заболевание, которое поражает все поголовье свиней. На сегодня этот вирус не поддается лечению. Единственный выход - полное уничтожение зараженных животных на пораженной вирусом территории.
Сейчас, судя по всему, началась новая волна. Так, об очаге АЧС сообщает комитет ветеринарии при правительстве Калужской области. Заболевание выявили в Перемышльском районе области. Трупы животных сожгли, на месте провели санитарные работы. 1 сентября результаты исследования подтвердили наличие у погибших животных вирус АЧС. Ранее очаги африканской чумы были выявлены в Барятинском, Спас-Деменском и Мосальском районах.
В Польше в 2020 году вирус африканской чумы свиней поразил множество крестьянских хозяйств. Ожидается, что их число будет расти. Большинство из них — подсобные хозяйства, но риск заражения промышленных ферм растет. По официальным данным, большинство зараженных хозяйств находится в Восточной Польше, остальные — в провинциях, граничащих с Германией.
Первые вспышки африканской чумы появились в 1921 году в Кении. Затем, в середине 20 века, вирус АЧС начал поражать европейские страны: Португалию, Испанию, Францию, Италию… До России вирус добрался в 2007 году. Вакцину – единственный способ преодолеть АЧС - пытаются изобрести давно во многих странах, но, к сожалению, пока это ни у кого не получилось.
В социальных сетях описывают случаи истребления животных в мелких фермерских хозяйствах в случае их отказа входить в крупные агрохолдинги.
Действительно, в социальных сетях можно найти немало жутковатых историй на эту тему. Рассказы фермеров не могут оставить равнодушными.
директор Федерального исследовательского центра вирусологии и микробиологии Денис Колбасов считает разработку вакцины против АЧС проблемой не только научной, но и социально-экономической.
Основной центр разработки российской вакцины против АЧС находится во Владимирской области. Про находящийся там Исследовательский центр вирусологии и микробиологии рассказывают разное. Некоторые даже вспоминают советские времена, когда этот институт производил что-то вроде бактериологического оружия… Так или иначе, сейчас там занимаются сложными вакцинами.
Как водится, с объявлением о создании вакцины у нас как всегда поторопились. Но есть шанс, что в данном случае, на основе серьезных исследований, проведенных по всем международным стандартам, действительно будет сделано важное открытие, которое спасет и сотни фермерских хозяйств, и тысячи животных во всем мире.
О существенном прогрессе в разработке эффективной вакцины против африканской чумы свиней в начале этой недели сообщила команда исследователей из Харбинского ветеринарного научно-исследовательского института (Китай). По данным информационного агентства Xinhua, это первый шаг в разработке эффективных и безопасных вакцин против этой болезни.
Бу Чжигао, директор Харбинского ветеринарного научно-исследовательского института CAAS, заявил, что перед Китаем стоит большая задача контроля над распространением африканской чумы свиней. Необходимо срочно разработать более мощные средства, такие как вакцина, для предотвращения распространения заболевания.
"Прорыв в раскрытии тонкой структуры вируса является важным и фундаментальным исследованием, которое даст подсказки для изучения основных механизмов заражения, патогенности и иммунологии африканской чумы свиней, а также разработки вакцины", - сказал он.
Ученые работали четыре месяца, чтобы собрать более 100 ТВ высококачественных данных, что позволило команде осуществить значительный прорыв в выявлении структуры и характера вируса.
"Африканская чума свиней, история эпидемии которой составляет почти 100 лет, является сложной глобальной проблемой. Вирус имеет стабильную структуру и может выживать месяцами при нормальных температурах, представляет большую задачу для профилактики и контроля. Ученые имели ограниченные знания о вирусе. Мы надеемся сделать шаг к лучшему пониманию заболевания ", - пояснил Ван Сянси, один из членов команды.
Однако, пока вакцина поступит в продажу, могут пройти годы исследований и испытаний.
Африканская чума свиней, впервые описанная в Кении в 1921 году, является очень заразным вирусным заболеванием свиней со смертностью, которая приближается к 100%. За последнее десятилетие болезнь распространилась во многих странах . В течение 2018 и 2019 из-за АЧС было уничтожено более 30000000 свиней. Пандемия африканской чумы свиней вызвала экономические потери для производителей свиней во всем мире в размере 2 млрд долларов.
Фернандо Родригез, директор CReSA, рассказывает, на какой стадии находится разработка вакцины против АЧС.


Fernando Rodríguez
Почему у нас все еще нет вакцины против АЧС?
Об АЧС не вспоминали достаточно долго, особенно, учитывая тот факт, что на территории Субсахарской Африки этот вирус оставался эндемичным с момента первого своего появления, увеличивая уровень нищеты и недоедания в затронутых им регионах. Даже когда это заболевание прописалось в Европе, число исследовательских групп, заинтересовавшихся этой темой, никогда не превышало одной дюжины, при этом, Испания и Португалия были теми странами, в которых таких исследователей было большинство. Поэтому, нет ничего странного в том, что за те 60+ лет, что мы знаем о существовании вируса, было опубликовано всего 1 454 об АЧС в общем, или 167 статей об АЧС и вакцинах.

Вирус АЧС сам по себе, как и его эпидемиологический цикл, является комплексным, у него есть более чем восприимчивый реципиент: свиньи и дикие кабаны в Европе. При этом, ситуация в Африке еще сложнее, поскольку там существуют два естественных резервуара: аргасовые клещи и африканские кабаны-бородавочники.
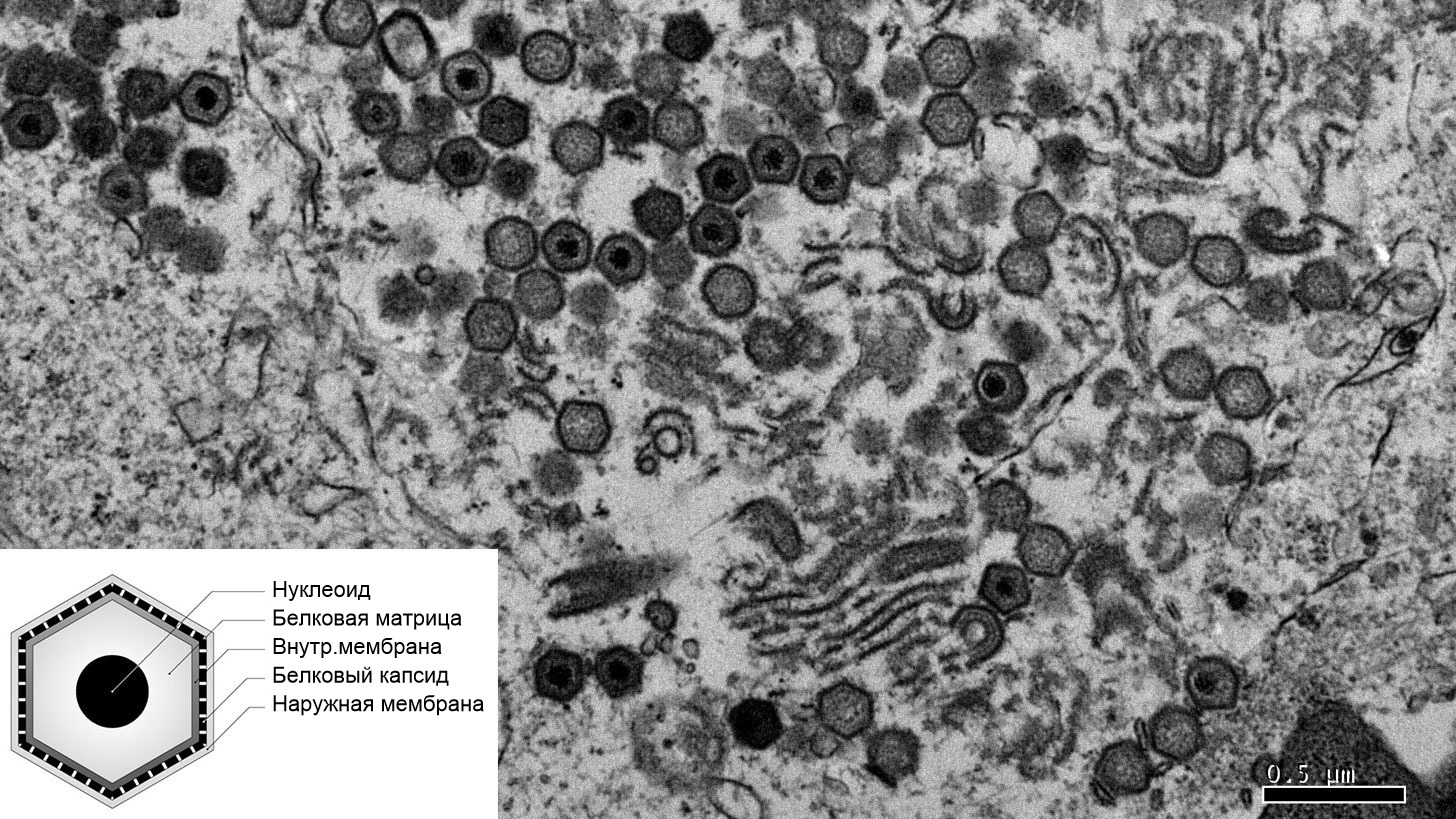
Изображение клетки, зараженной вирусом АЧС, на электронном микроскопе.
Тем не менее, и это абсолютно личная оценка, если что и осложнило ситуацию еще больше, так это наша исторически сложившаяся неспособность исследовать данную проблему основательным и скоординированным образом, при том, что к тому времени (начало 2000 г.г.) лучшие лаборатории были закрыты, поскольку существовало мнение, что этот вирус уже не представляет никакой угрозы. А теперь мы должны спешить.
На какой стадии находятся текущие исследования, направленные на разработку вакцины против АЧС? С какой нормативной базой вы работаете? Когда станет возможно получить вакцину против вируса АЧС?
Несмотря на все то, что пишут в последнее время, в поисках вакцины против АЧС сделаны огромные шаги вперед, и мы ближе, чем когда-либо к тому, чтобы объявить о хороших новостях. Что же касается типа вакцины, можно, в общих чертах, сказать:
- Классические инактивированные вакцины против вируса АЧС (АЧСв) не работают, по крайней мере, таким образом, как это планировалось – скорее всего, по причине их неспособности продуцировать цитотоксичные Т-клетки, требуемые для элиминации зараженных клеток.
- Живые аттенюированные вакцины, полученные как классическими методами, так и путем генетических манипуляций, дают фантастический уровень защиты, как минимум – от материнского вируса. На сегодняшний день считается, что данная стратегия находится ближе всех к рынку и почти все исследовательские группы, как показывает недавно составленный экспертами в данной области отчет Европейской Комиссии, очень на нее надеются. Это будет нелегко, поскольку созданные к настоящему моменту прототипы, в том числе разработанные в лаборатории USDA на Плам-Айленде, а также те, что были получены в сотрудничестве между Молекулярно-биологическим Центром Северо Очоа и CreSA-IRTA, в самом ближайшем будущем должны быть усовершенствованы, особенно в плане их безопасности и технической возможности ДИВЖ (которая позволяет отличить вакцинированных животных от заразившихся естественным путем). Консорциум, который был создан USDA-ARS и CReSA-IRTA, гарантирует оптимизацию прототипов. Интерес, проявленный деловыми кругами, а также финансирование, открытое ЕС позволяют с оптимизмом относиться к возможности выхода аттенюированной вакцины на рынок через 5-10 лет, обязательно при этом учитывая, что данные временные рамки предложены оптимистом-ученым, слабо разбирающимся в корпоративном маркетинге.
- Вакцины аттенюированные vs субъединичные. Тот же самый отчет Еврокомиссии призывает нас вести работу над вакцинами будущего, основанных на субъединицах. Сложность строения вируса, состоящего из более, чем 200 различных белков, а также трудность их введения в живой организм (in vivo) таким образом, чтобы они были оптимально представлены иммунной системе, подсказывают нам быть более консервативными в отношении периодов коммерциализации. Несмотря на их огромные преимущества в плане безопасности и возможности ДИВЖ (DIVA), мы должны учитывать проявляемую ими до настоящего времени невысокую действенность против смертоносных штаммов АЧСв. Нам следует продолжать работать плечом к плечу по обоим направлениям, идентифицируя и защищающий вирус антигены, и иммунологические механизмы, отвечающие за эту защиту. Короче говоря, требуется больше инвестиций на проведение базовых исследований.
Исходя из имеющейся информации, какой ожидается уровень эффективности вакцины?
Всегда непросто экстраполировать лабораторные результаты на полевые условия. Единственное, что мы можем сказать сегодня – это то, что имеющиеся в наших лабораториях прототипы вакцин защищают 100% свиней от ЭКСПЕРИМЕНТАЛЬНОГО ЗАРАЖЕНИЯ грузинским штаммом, толкуя защиту как способность животного избежать гибели (контрольные животные гибнут в течение 10 дней). И это правда, что некоторые животные демонстрируют, в течение непродолжительного периода, сниженное количество вируса, обнаруженного в крови и носовых секрециях, по сравнению с контрольными.
Какими целевыми характеристиками должна эта вакцина обладать ?
Критическое значение имеют уровень безопасности и возможность ДИВЖ. Мы не можем игнорировать тот факт, что это живая вакцина, поэтому ее использование должно производиться при наличии жестких гарантий безопасности. Использование вакцин на основе субъединиц будет намного более простым и менее рестриктивным.
Хотя введение путем инъекций будет, скорее всего, более благосклонно воспринято индустрией, нам не следует забывать и о составах для перорального применения (для использования, например, в приманках для диких кабанов), аналогично тому, как это происходит с проходящими проверку вакцинами против туберкулеза или классической чумы свиней.
Учитывая, какой удар болезнь нанесла за последние годы, достаточно ли ресурсов выделяется в мире на проведения исследований?
Возможно, в наши дни этой проблеме уделяется гораздо больше внимания и для борьбы с ней выделяется больше денег, однако, это не имеет никакого значения, если все не будет продолжаться.
Критика не только в адрес властей, которые зачастую не воспринимают болезнь достаточно серьезно, но также и в адрес исследователей, потому что мы иногда воспринимаем такие обстоятельства как возможность поохотиться на финансирование, не отдавая себя работе полностью в существующих сложнейших условиях. Ограниченность мировых ресурсов, в общих словах, должна заставить нас переосмыслить, каким образом использовать эти ресурсы наиболее рационально. Я пользуюсь представившейся возможностью публично поблагодарить за фонды, инвестированные испанским правительством в наше направление исследований, начиная с 2004 г., а также за их веру в эти исследования еще до того, как вирус АЧС вновь стал угрожать нашей экономике. Это позволило компаниям, вроде Boehringer Ingelheim (сначала), а теперь уже и другим, заинтересоваться нашим прогрессом. Мы считаем это большой удачей.
Комментарии к статье
Китайские ученые разработали экспериментальную вакцину, которая сможет защитить животных от смертельного вируса, который вызывает африканскую чуму свиней. Вирусологи предупреждают, что предстоит еще провести клинические испытания вакцины и наладить массовое ее производство.

Фото: Александр Петросян, Коммерсантъ / купить фото
Фото: Александр Петросян, Коммерсантъ / купить фото
Африканская чума свиней — вирусное заболевание, прокатившееся по Китаю и едва не уничтожившее популяцию домашних свиней в стране. За последние 18 месяцев, по данным местного министерства сельского хозяйства, численность свиней в Китае, составлявшая свыше 440 млн особей, сократилась более чем на 40%. Вспышка началась в августе 2018 года в Шэньяне, на северо-востоке Китая. Ветеринарным властям долго не удавалось поставить заслон на пути инфекции. Сейчас ситуация находится под контролем.
Африканская чума свиней — заболевание очень заразное, вирус вызывает тяжелый и в основном смертельный для свиней геморрагический синдром. Единственным способом остановить распространение эпизоотии до сих пор в мире считается поголовное уничтожение свиней в очаге инфекции.
Харбинские исследователи продвинулись в своей работе дальше всех в мире, констатирует вирусолог Даниэль Рок, сотрудник Университета Иллинойса: они достигли очевидных успехов и в безопасности препарата, и в тестировании.
Команда Бу начала работу над вакциной, выделив вирус африканской чумы свиней из селезенки зараженной свиньи. Штамм, который распространялся по Китаю, оказался генетически почти идентичен штамму, который был обнаружен в Грузии в 2007 году и разошелся по Восточной Европе, а уже потом достиг Китая. Исследователи решили сделать вакцину на основе живого, но ослабленного вируса. Этот подход уже показал эффективность при работе над вакцинами от классической чумы свиней и парвовируса свиней. Бу и его команда выключили несколько генов из генома нескольких штаммов вируса африканской чумы свиней и получили данные, что именно эти части генома ответственны за тяжелое протекание болезни. Опыт на семинедельных поросятах показал, что штаммы с выключенными генами надежно защищают от вируса.
А затем выяснилось, что свиньи, вакцинированные высокой дозой ослабленного штамма, при воздействии дикого вируса проявляли только слабые симптомы или не проявляли их вовсе.
Так что если вдруг вирусу африканской чумы свиней вздумается перекинуться на человека, то оружие для победы над заразой у врачей будет.

Африканская чума свиней (АЧС) — вирусная, контагиозная, септическая болезнь свиней, характеризующаяся лихорадкой, признаками токсикоза, геморрагическим диатезом и высокой летальностью. При острой, наиболее распространенной форме инфекции, 100% животных погибают в течение 5-10 суток. Поскольку вакцины против АЧС не разработаны, то для ликвидации и предупреждения распространения болезни во всем мире применяются стемпинг аут и жесткие карантинные мероприятия.
Патологоанатомические изменения при АЧС

Предыстория
На рубеже 60-х годов прошлого столетия, когда в мире были разработаны вакцины против полиомиелита, бешенства, кори, перспективы создания вакцин против вирусных болезней человека и животных представлялись весьма радужными. Поэтому, когда в 1957 и 1960 гг. АЧС впервые была занесена из Африки на Пиренейский полуостров, специалисты Португалии и Испании, получив аттенуированные, т.е. ослабленные в лабораторных условиях, штаммы, с согласия правительств вакцинировали около 600 тыс. свиней. Через несколько месяцев количество неблагополучных пунктов в обеих странах увеличилось в три-шесть раз, погибло до 50% привитого поголовья, у выживших свиней отмечали проявление клинических признаков болезни в поствакцинальный и отдаленный периоды. Негативные результаты широкомасштабного применения живых вакцин и последующие лабораторные исследования привели к формированию устойчивой позиции, что средства специфической профилактики АЧС на основе аттенуированных штаммов разработать невозможно, а ликвидацию болезни следует проводить посредством строгих ветеринарно-санитарных мероприятий, включающих тотальный убой свиней в очаге и угрожаемой зоне.

Опасен ли АЧС для людей
Первые попытки разработать вакцину
В 1960-х годах в связи с опасностью непреднамеренного или преднамеренного заноса вируса АЧС на территорию бывшего СССР было принято решение создать средства для временной защиты от болезни, чтобы обеспечить, как минимум, плановый убой свиней и переработку мясной продукции в комплексах, где содержали до 120-240 тыс. голов свиней. Специально для этого в г. Покров Владимирской области был построен ВНИИ ветеринарной вирусологии и микробиологии (сейчас — ГНУ ВНИИВВиМ Россельхозакадемии); институтским ученым помогли создать и научно-исследовательскую лабораторию в Народной республике Конго. Руководил проектом по "африканке" профессор Никифор Иванович Митин.
Параллельно с исследованиями по созданию средств специфической защиты от болезни накапливались данные о сероиммунотиповом плюралитете вируса АЧС. Первыми эту тему подняли британские и испанские ученые, но затем их интерес к этому направлению угас, а вот наши ученые по результатам реакции задержки гемадсорбции в культуре клеток и иммунологической пробы на свиньях создали сероиммунотиповую классификацию. Более ста хранившихся в институте изолятов и штаммов вируса АЧС со всего мира были разделены на девять сероиммунотипов. Для каждого из них надо было разрабатывать свои средства для временной защиты свиней.
.jpg)
Экономический ущерб от АЧС
В результате многократного пассирования, применения классических и весьма экзотических методов селекции в первичных и перевиваемых культурах клеток были получены аттенуированные штаммы (т.н. вакцинные) первых пяти сероиммунотипов. Они были безвредны для свиней в десятикратной прививочной дозе и на 14-е сутки обеспечивали формирование защиты продолжительностью не менее 4 месяцев. Все вакцинные штаммы соответствовали и другим требованиям: не передавались контактно при совместном содержании с интактными животным, не ревертировали в пяти последовательных пассажах на свиньях, были слабореактогенными. В зависимости от способов и целей применения были разработаны различные формы экспериментальных вакцин: нативные, концентрированные, лиофилизированные и эмульгированные. Предполагалось, что применять вакцины против АЧС в промышленных свинокомплексах закрытого типа можно будет только по специальному разрешению Главного управления ветеринарии МСХ СССР. Однако крупномасштабные эксперименты и лабораторные исследования с иммунологически ослабленными животными, включая супоросных свиноматок, подтвердили вероятность повторения негативного опыта испанских и португальских ученых. В результате сочли, что разработанные живые вакцины вряд ли будут когда-либо востребованы.

АЧС в России
Современное состояние исследований
Неудачи в создании живых, инактивированных, субъединичных вакцин стимулировали исследования свойств вируса, иммунологических механизмов защиты при АЧС, поиск протективных белков.
Профессор В.В. Макаров на основании обобщения полученных во ВНИИВВиМ экспериментальных данных сформулировал иммунологическую концепцию, согласно которой: 1) нейтрализация вируса АЧС антителами невозможна ввиду того, что вирус проникает в клетки-мишени (моноциты, макрофаги) путем фагоцитоза независимо от специфических рецепторов, а образование комплекса "вирион + антитело", наоборот, усиливает фагоцитоз по типу опсонизации; 2) ограничение репродукции вируса АЧС в организме свиньи происходит посредством противоклеточных эффекторных механизмов иммунитета, при этом критическую протективную роль выполняют цитотоксические Т-лимфоциты, которые, как правило, не индуцируются инактивированными и субъединичными вакцинами. Доказано, что важен и антителозависимый цитолиз нормальными киллерами.
Исходя из локализации в оболочке вирионов и плазматической мембране зараженных клеток, из сотни вирусных белков определены четыре-пять потенциально протективных. По логике, решающую роль в индукции защиты при АЧС должен играть белок, обладающий свойством серотиповой специфичности, который феноменологически обнаруживает себя в реакции задержки гемадсорбции. В 1990-х годах нами был идентифицирован серотипоспецифический гликопротеин, а испанскими исследователями — ген, кодирующий синтез вирусного CD-подобного белка, который отвечает за гемадсорбцию. Так разными путями был найден один и тот же критически важный для формирования противовирусной защиты белок.
В ведущих вирусологических центрах мира сейчас исследуют защитные свойства рекомбинантных конструкций, кодирующих синтез потенциально протективных белков. Молодые ученые нашего института совместно с американскими коллегами проводят интереснейшие и обнадеживающие исследования с геном CD-подобного белка "вакцинных" штаммов вируса АЧС. Министерство образования и науки Российской Федерации в рамках МЦП ЕврАзЭС "Инновационные биотехнологии" финансирует выполняемые нами научно-исследовательские работы по созданию тест-системы для серодиагностики АЧС методом иммуноблоттинга на основе рекомбинантных иммунодоминантных белков. Полученные рекомбинантные конструкции будут полезны и в исследованиях по созданию кандидатных генно-инженерных вакцин.

Что такое стемпинг аут
Один из важнейших элементов современной политики контроля эпизоотических инфекций, буквально "подворный убой", stamping out-- в переводе с английского — ?тушить, затаптывать огонь, искоренять, подавлять, истреблять?. Процедура заключается в убое всех больных и подозреваемых в заражении (экспозированных) животных, утилизации, уничтожении их трупов (сжигании, захоронении), очистке и деконтаминации хозяйства. Ключевыми моментами процедуры стемпинг аут в современном понимании являются:
- обозначение зараженной территории;
- интенсивный надзор за болезнью с целью выявления зараженной территории и территории, где содержались опасно контактировавшие животные, или местности внутри этих зон;
- установление карантина и ограничение передвижения животных;
- немедленный убой всех восприимчивых животных, находящихся либо в зараженных и смежных помещениях, либо на всей зараженной территории; надежная утилизация туш животных и другого потенциально инфекционного материала;
- чистка и дезинфекция зараженных мест содержания животных;
- освобождение этих помещений от восприимчивых животных на необходимое время.
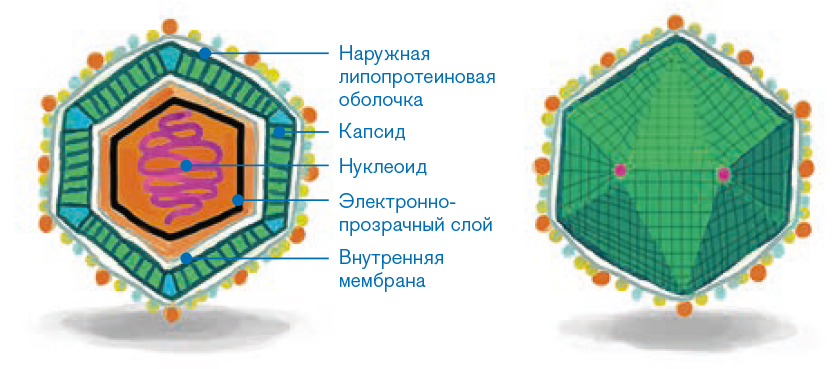
Вирус АЧС классифицирован в отдельное семейство Asfarviridae. Крупные частицы вируса АЧС размером около 200 нанометров имеют сложное строение и округлую или икосаэдрическую форму.
В их архитектуре выявляются несколько слоев: внешняя оболочка, происходящая из клеточной мембраны и приобретаемая в процессе выхода из клетки почкованием, и внутренняя мембрана, окружающая икосаэдральный капсид, в центре которого расположена сердцевина из слоя фибриллярных компонентов и нуклеоида.
Вирус чрезвычайно устойчив к факторам различной природы, его выживаемость в объектах среды и продуктах свиного происхождения необычно высока. Вне организма в физиологических средах или сыворотке крови вирус сохраняется 6 лет при ?50°С, 18 месяцев в крови и сыворотке при комнатной температуре, до 1 месяца при +37°С. В полевых условиях он устойчив к гниению, длительно сохраняется в различных выделениях больных свиней: крови и тканях, истечениях, сгустках и т.п. Внутри организма больных свиней общая инфекционность туши превышает 1013 инфекционных единиц вируса; 96% ее аккумулируется в костном мозге.
Основной фактор непредсказуемого заноса АЧС в благополучные страны — сохраняемость вируса в пищевых продуктах.
Краткая история АЧС
АЧС установлена более ста лет назад английским ученым Р. Монтгомери (R.E. Montgomery). Естественная история АЧС может быть разделена на четыре периода.
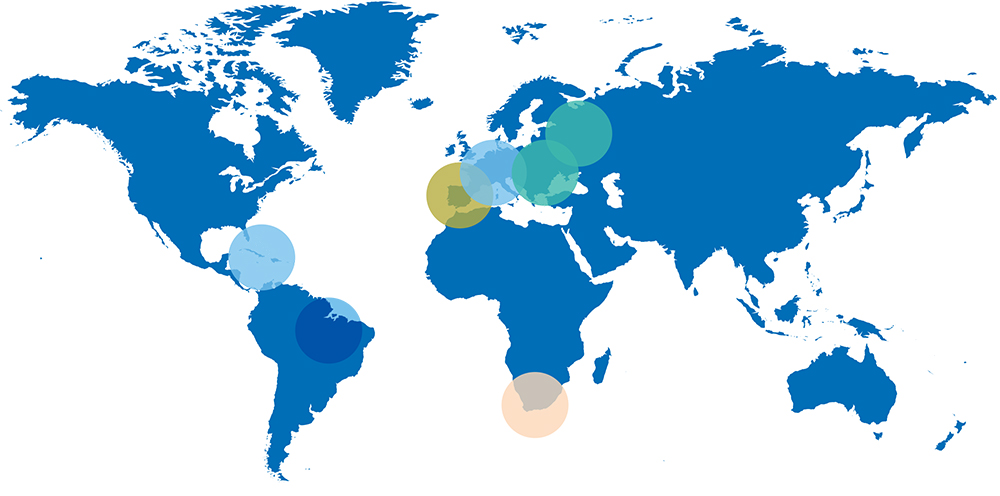
Распространение только в пределах традиционного южноафриканского нозоареала в природноочаговой форме с трансмиссивной передачей инфекции и редкими случаями острой летальной АЧС при заражении завезенных из Европы домашних свиней.
Возникновение, распространение среди домашних свиней и кабанов в Испании и Португалии, становление самостоятельного антропургического цикла и эндемии с рядом спорадических вспышек в других странах Южной Европы.
Занос АЧС в Грузию, широкое распространение в юго-восточном регионе Евразии (Армения, Азербайджан, Абхазия, Нагорный Карабах, Россия, Иран, Украина, Латвия, Литва, Эстония, Белоруссия, Польша), становление эндемии на юге и в центре европейской части РФ.
текст Алексей Середа, доктор биологических наук, ведущий научный сотрудник ВНИИ ветеринарной вирусологии и микробиологии Российской академии сельскохозяйственных наук
иллюстрация Галя Панченко
Читайте также:

