Куда могут пустить вирусы
Обновлено: 16.04.2024
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
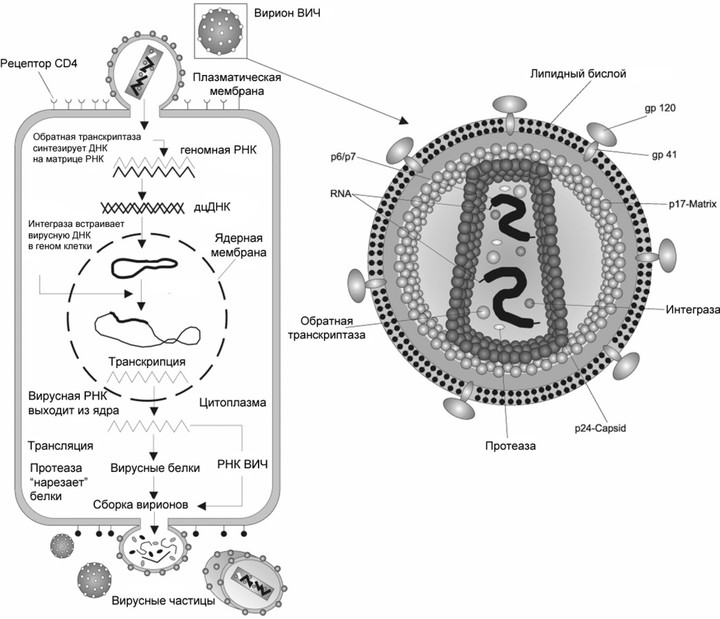
Жизненный цикл вируса, на примере вируса иммунодефицита
Как с ними бороться?
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
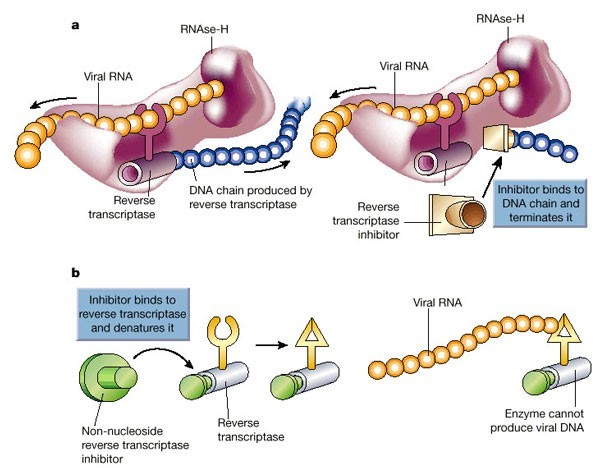
Механизм дейсвтия ингибиторов обратной транскриптазы
3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
4. Созревание
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.
Преступность постепенно уходит в интернет – такой вывод можно сделать из августовского доклада Генпрокуратуры РФ. Если общее число преступлений в стране за последний год выросло на 1,9%, то в Сети злоумышленники стали активнее на 46,8%.
Компьютерные вирусы появились одновременно с самими компьютерами. На роль первого зловреда претендует Elk Cloner, созданный в 1981 году 15 летним американским школьником Ричардом Скрентой. То был невинный розыгрыш: программа попадала на магнитную дискету, и при считывании с нее информации на дисплей ПК выводился стишок-дразнилка.
Попав на устройство, вирус может проделать один из нескольких трюков – в зависимости от того, как злоумышленник решил заработать на жертве. Первый вариант – показать как можно больше рекламы, получив доход от рекламодателей. За это отвечают adware-вирусы, запускающие рекламу почти при каждом действии пользователя, – тот ни в состоянии ни определить источник спама, ни избавиться от него. Неприятно, но еще не худший вариант.
Второй вариант – украсть пользовательские данные с целью продажи в Darknet. Так работают вирусы-трекеры, фиксирующие активность пользователя в браузере – вплоть до списка контактов, паролей, местонахождения. Банковские трояны отслеживают финансовые операции и крадут номера банковских карт.
Четвертый способ монетизации вируса – захват вычислительных ресурсов компьютера. Например, для запуска DDoS-атак на организации: такие атаки требуют много ресурсов, поэтому злоумышленник захватывает сотни устройств, формируя из них зараженную сеть – ботнет.
Одна из главных задач ботнетов в последние годы – скрытая добыча криптовалюты (криптоджекинг), также ресурсоемкая и требующая слаженной работы множества девайсов. В 2017 году, когда биткоин дорожал с каждым месяцем, количество атак с целью криптоджекинга показало феноменальный рост: +8500% за год (данные Symantec). В прошлом году биткоин стабилизировался, что немного успокоило и хакеров. И все же по итогам года криптомайнеры, по данным Check Point, стали самым распространенным типом вирусов (37% атак), обогнав и банковские трояны (13%), и шифровальщиков (4%). Сейчас топ 3 самых распространенных вирусов в России также составляют криптомайнеры: Cryptoloot, XMRig и Jsecoin (в июне атаковали 11%, 9% и 7% организаций соответственно; данные Check Point).
Вообще, развитие криптовалют привело к всплеску киберпреступности по многим направлениям. Сюда входит и хищение криптокошельков, и организация мошеннических ICO, и использование криптовалют в качестве анонимного способа получить от жертвы выкуп. В общем, что скорее принесет миру эта технология – пользу или вред, еще предстоит разобраться.
От киберугроз сегодня не скроешься, ведь даже для смартфонов, которые мы повсюду носим с собой, создаются миллионы вредоносных программ
Троян, который всегда с тобой
Отдельный класс кибератак заточен под мобильные устройства. Их тоже становится все больше: в 2012 м насчитывалось 214 тыс. известных вредоносов, в 2014 м – 1,55 млн, в 2018 м – свыше 4 млн (данные GData). Самый распространенный механизм проникновения – тот же фишинг, только вместо зараженных сайтов носителем вируса выступают фальшивые приложения (fake applications). Они маскируются под обычный софт, вплоть до полного копирования интерфейса и функций.
Дети – самая уязвимая категория пользователей
Впрочем, вредоносы хранятся и в официальном Android-маркете, хотя их доля составляет менее 1% от общего количества программ. Как выяснили специалисты Сиднейского университета, проанализировав более миллиона приложений из GooglePlay, около двух тысяч оказались поддельными. Топ 3 мобильных вирусов на сегодняшний день по версии Check Point – Lotoor, Triada и Ztorg – также разработаны под ОС Android.
Bildagentur-online / Vostock Photo
Малый бизнес под ударом
О важности киберпрививок
Прежде всего Ильин советует обзавестись на устройстве новой версией антивируса и следить за его обновлениями. Звучит банально, но на практике исполняется не всегда. Более того, проблема своевременного обновления ПО касается не только антивирусов. Согласно исследованию Avast’s PC Trends Report 2019, более половины программ, установленных на компьютерах по всему миру, не имеют критических обновлений.
А многие пользователи отказываются переходить на новые версии Windows, не желая привыкать к интерфейсу. Скоро им придется принимать трудное решение: в январе 2020 го Microsoft перестанет выпускать обновления безопасности для популярной Windows 7.
Если заражение все-таки произошло, нельзя соглашаться на условия злоумышленника – например, перечислять выкуп за разблокировку устройства. Ведь сам вирус останется в системе, а значит, киберзлодей может повторить тот же трюк. Лучше сделать снимок экрана и обратиться к специалистам: поскольку проблема массовая, с ней научились разбираться. Идеальный вариант – иметь на внешнем винчестере резервную копию важных данных. Тогда шифровальщики нипочем: достаточно отформатировать зараженный компьютер, установить новую ОС, и как будто ничего не было.
А вот сохранность персональных данных, увы, несколькими простыми шагами не обеспечить.
Рынок кибербезопасности растет как вширь, по объемам выручки, так и вглубь, по степени сложности защитных инструментов. Но идеальный антивирус пока не появился и вряд ли когда-либо будет изобретен
Не думай об угрозах свысока
По мнению специалистов, виртуальное пространство постепенно удастся превратить из Шервудского леса в культурный городской парк, вот только до этого момента придется набить еще немало шишек. Возможно, наведение порядка ускорится благодаря активности национальных регуляторов, обращающих все более пристальное внимание на сферу киберпреступности.
Топ 3 самых активных мобильных вирусов
Lotoor – вирус, использующий уязвимости в ОС Android для получения root-доступа к устройству.
AndroidBauts – вирус, засоряющий смартфон агрессивным рекламным спамом и собирающий данные о местоположении.
Piom – рекламное ПО, отслеживающее активность пользователя в браузере и показывающее таргетированные объявления.
Источник: Check Point Global Threat Index, июль 2019 года.
Топ 10 самых активных вирусов для ПК
XMRig – программа для майнинга криптовалюты Монеро, впервые обнаруженная в мае 2017 года.
Jsecoin – вирус для криптоджекинга, встраиваемый в веб-сайты. Добыча криптовалюты начинается прямо в браузере.
Dorkbot – червь, запускающий удаленное исполнение кода и загрузку на компьютер рекламного ПО.
Emotet – троян, поражающий банковские приложения. Распространяется в виде ссылок в письмах, использует различные техники, чтобы остаться незамеченным для антивируса.
Nanocore – многофункциональный троян, делающий снимки экрана, захватывающий контроль над ПК и веб-камерой, а также добывающий криптовалюту.
Agentesla – вирус, крадущий пароли. Перехватывает ввод с клавиатуры, делает снимки экрана, собирает пользовательскую информацию в браузере.
Trickbot – мощный банковский троян, регулярно совершенствуемый для обхода антивирусных систем.
Formbook – вирус, крадущий пароли, делающий скриншоты, перехватывающий ввод с клавиатуры. Может устанавливать на ПК другие вирусы.
С начала пандемии Всемирная организация здравоохранения подчеркивала, что COVID-19 распространяется в основном через очень тесный личный контакт. Согласно этой логике больной человек выдыхает через рот и нос содержащие вирус тяжелые капли, которые оседают на землю прежде, чем успевают пролететь больше двух метров.
Раньше организация придерживалась мнения, что существует низкая вероятность так называемой воздушно-пылевой передачи вируса за пределами больниц, где при проведении некоторых процедур выделяются супермелкие частицы, которые остаются в воздухе дольше, чем крупные капли, выделяемые при дыхании.

Носить маску в ограниченных замкнутых пространствах — все еще хорошая идея!
Начнем с первого вопроса.
Крупные капли и мелкие капли: в чем разница?
Это достаточно простой, пусть и отчасти устаревший, взгляд на механизм распространения респираторных заболеваний. Процесс начинается с того, что, когда вы выдыхаете, чихаете или кашляете, в воздух выделяются облако газа и капли жидкости.
Если капли относительно крупные, они тяжелые и, как дождь, падают на землю, прежде чем начать испаряться. Другие капли мельче и становятся еще меньше из-за испарения. Эти более мелкие капли могут оставаться в подвешенном состоянии дольше, иногда до нескольких часов, перемещаясь с потоками воздуха.
Важно: если капля достаточно маленькая, жидкость из нее испарится раньше, чем она успеет достигнуть земли, так что, если в этой капле содержатся, например, микробы, они становятся достаточно легкими, чтобы перемещаться в потоках воздуха, как пыль (отсюда и название).
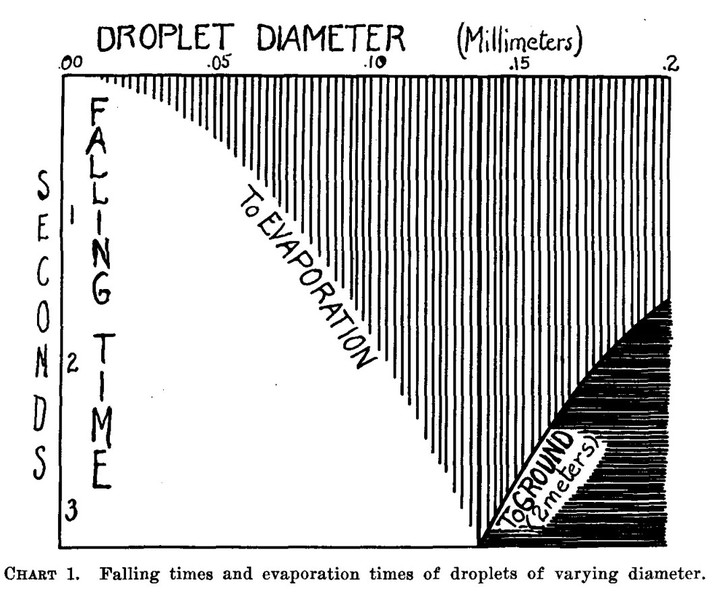
Таблица, составленная Уэллсом в 1934 году, которая показывает, как различаются по размерам капли и аэрозоли. American Journal of Epidemiology
Почему это важно для нас? Один из первых вопросов, на который стремились ответить эпидемиологи при изучении COVID-19, был вопрос, распространяется ли вирус в виде пыли, которая перемещается по воздуху, или крупных капель, которые оседают?
Если мы имеем дело с мелкой пылью, нужно бить тревогу. Значит, типологически это болезнь, передаваемая воздушно-пылевым, а не капельным путем. То есть она относится к тому же типу, что и корь, ветряная оспа, туберкулез, а стало быть, является высокозаразной. Один человек, заболевший корью, может инфицировать в среднем 12—18 других.
Крупные капли — тоже повод для тревоги. Но меньшей. В основном крупными каплями передаются такие заболевания, как грипп, коклюш, обычные ОРВИ и коронавирусы. При таких заболеваниях люди заражаются только при тесном контакте с заболевшим, потому что большие капли быстро падают на землю (на расстоянии около двух метров). Такие капли могут оседать на поверхностях, так что в свою очередь могут стать источником заражения. К счастью, в случае с COVID-19 все постепенно приходят к общему мнению, что вероятность заболеть от прикосновения к загрязненной поверхности крайне мала.

Фото, снятое в лаборатории Лидии Буруйба, показывает все капли, которые выпускаются в воздух при чихании. JAMA
Воздушная опасность
Выходит, что разделение на капельную и воздушно-пылевую передачу, предложенное Уэллсом, хоть и используется до сих пор, устарело.
Это значит, что найденный вирус или не был способен заразить, или присутствовал в слишком маленьких количествах, чтобы вызвать заболевание. И действительно, результаты лабораторных исследований нельзя с высокой точностью обобщить для условий реального мира, в котором вирус распространяется и заражает людей. А одно то, что вирус далеко перемещается в каплях, еще не значит, что он может заражать людей на больших расстояниях.
Один из первых вопросов при изучении COVID-19, был вопрос, распространяется ли вирус в виде пыли, которая перемещается по воздуху, или крупных капель, которые оседают?
Вне тела вирус может быстро разрушаться. Концентрация тоже имеет значение. Воздействия небольшого количества частиц вируса может быть недостаточно, чтобы вызвать заболевание. И тут стоит обратиться ко второму нашему вопросу. Отслеживание контактов показывает, что воздушно-пылевая передача коронавируса может происходить в ограниченных замкнутых пространствах. Как именно?
Так, по их данным, передача COVID-19 чаще всего происходит из-за вдыхания капель на расстоянии в пределах двух метров от зараженного человека, но существуют случаи и условия, в которых SARS-CoV-2 может проявлять себя отчасти как воздушно-пылевой, а не капельный вирус.

Опасная близость
Так, терапевт и эксперт-вирусолог из Сент-Эндрюсского университета Мюге Чевик (Muge Cevik) отмечает, что в домашних условиях зараженный человек может быть изолирован в комнате и не передавать вирус другим жильцам. В ее систематическом обзоре для журнала Lancet, в котором анализировались исследования как SARS-CoV-2, так и других подобных ему вирусов, отмечается, что опасность заражения значительно снижается, если люди держатся всего в одном метре друг от друга. Из этого можно предположить, что высокий риск заразиться COVID- 19 присутствует в первую очередь через крупные капли, которые быстро оседают на землю.
Но в то же время учеными были зафиксированы случаи, когда много людей собиралось в замкнутом пространстве (например, в церкви), пело или кричало, в результате чего инфицированными оказались сразу все участники мероприятия, в том числе находившиеся достаточно далеко от носителя. Все это больше похоже на передачу воздушно-пылевым путем.
Печально известная репетиция хора в штате Вашингтон — обернувшаяся крупной вспышкой — пример, в котором заражение, возможно, произошло именно так. Опасной эту встречу сделало совпадение многих факторов риска: пение (в процессе которого зараженный человек выпускает в воздух жизнеспособные частицы вируса), время, проведенное участниками вместе (репетиция длилась два с половиной часа), и взаимодействие между членами хора в замкнутом пространстве (они не только все вместе репетировали, но и делились на группки поменьше, чтобы выпить чаю с печеньем).
Другое исследование, проведенное в Китае, изучило вспышку заражения после обряда в буддийском храме. Как выяснилось, почти всеми инфицированными оказались пассажиры одного из автобусов, привезших людей на церемонию. В нем ехал только один больной человек, но заразились 24 из 67 пассажиров, что также можно расценивать как свидетельство воздушно-пылевой передачи вируса.

Почему молчат врачи?
Существует целый комплекс предельно конкретных инструкций для обращения с высокозаразными воздушно-пылевыми инфекциями в больничных условиях. Например, пациента с опасной воздушно-пылевой инфекцией чаще всего необходимо поместить в палату, давление воздуха в которой ниже, чем во всех других помещениях в здании. Так вирус, содержащийся в воздухе палаты, не сможет покинуть ее пределов (ведь воздух движется из области с более высоким давлением в область с более низким).
При капельной передаче медицинские работники могут проявлять чуть меньше мер предосторожности. Например, носить обычные медицинские маски в процессе стандартных процедур и сохранять респираторы с высокой степенью фильтрации (количество которых бывает ограничено) для самых опасных процедур и случаев.
Среди факторов риска: пение, время, проведенное участниками вместе и взаимодействие между членами хора в замкнутом пространстве.
При таком рассмотрении становится понятно, почему ВОЗ испытывает сомнения по поводу маркировки COVID-19 как воздушно-пылевой инфекцией. Она не распространяется по воздуху так, как корь. Она не настолько заразна. Отслеживание контактов постоянно показывает, что COVID-19 с наибольшей вероятностью передается между людьми в тесном физическом контакте. Воздушно-пылевой обозначает явление, требующее очень много ресурсов, и звучит очень пугающее для больниц и людей, работающих в них. И COVID-19 не подходит под это определение.
Как использовать всю эту информацию?
В целом информация о том, что COVID-19 может передаваться по воздуху, на самом деле, никак не должна влиять на то, как мы защищаемся от него сами и защищаем окружающих. Двухметровая дистанция между людьми — по-прежнему хороший способ предотвратить передачу вируса через крупные капли. Ношение масок может, кроме того, предотвратить выделение и крупных, и мелких капель. А стало быть, обезопасить не только носителя маски, но и людей, окружающих его.
Время тоже имеет значение: чем больше времени мы проводим в закрытых плохо вентилируемых помещениях с другими людьми, тем выше риск получить инфицирующую дозу вируса.

Кроме того, в помещении многое зависит от его вентиляции. В замкнутом пространстве, воздух в котором постоянно обновляется притоком кислорода извне, риск заражения ниже, чем в комнате с застоявшимся воздухом. Американское общество инженеров систем отопления, охлаждения и кондиционирования уже опубликовало подробные руководства по тому, как добиться улучшения вентиляции в зданиях во время пандемии.
Мы же должны задумываться о том, чем занимаемся вместе с другими людьми. При крике, пении и других похожих действиях выделяется больше капель (всех размеров), чем если сидеть молча.
Одна из наших собеседниц, доктор Моравская, надеется: привлечение внимания к воздушно-пылевой передаче COVID-19 приведет к тому, что общество будет проявлять больше интереса к инженерным решениям для закрытых помещений, которые помогут задержать распространение пандемии.
Одни вирусы способны интегрироваться в геном клетки-мишени и таким образом оставаться во всех дочерних клетках, которые будут в будущем получены после ее деления. К таким вирусам относятся гаммаретровирусы и лентивирусы. Другие делать этого не умеют (например, адено- и аденоассоциированные вирусы). Но для производства белков и репликации (размножения) все они используют клетку и ее синтетический аппарат.
Как это работает?
Для того чтобы вирус мог проникнуть в клетку, белки его оболочки должны связаться с мембранными белками клетки-мишени. Важно отметить, что проникает вирус только в те клетки, которые могут в дальнейшем помочь его репликации. Вирус ВИЧ живет в клетках иммунной системы, вирус гепатита С — в клетках печени. Есть особые вирусы, которые поражают только растения или даже только бактерии.
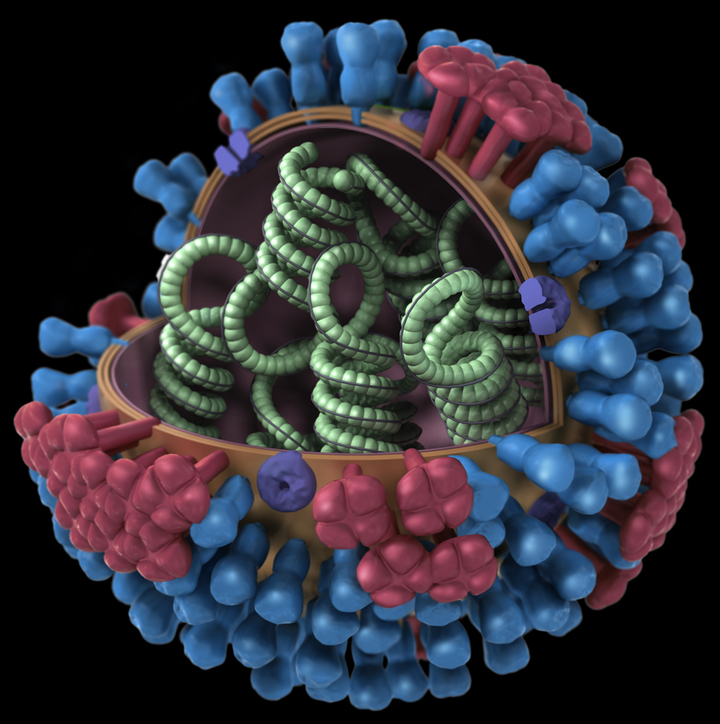
Строение вируса гриппа. Под оболочкой вириома - генетический материал вируса, необходимый для его воспроизводства в клетке.
Содержащие неактивный вирус и оставшиеся в живых клетки иногда сохраняют возможность нормального функционирования. В этом случае клетки могут быть заражены, но вирус проявит себя спустя длительный период времени. Так устроен герпес.
В зависимости от того, каким типом нуклеиновой кислоты представлен генетический материал, выделяют ДНК-содержащие вирусы и РНК-содержащие вирусы. И тут стоит остановиться на классификации.
Типы вирусов. Коротко о главном
Современная типология вирусов содержит 7 классов и была предложена Дэвидом Балтимором еще в 1971 году. С тех пор, впрочем, она была уточнена и расширена, в том числе советскими учеными. И выглядит в настоящее время таким образом:
Вирусы, содержащие двухцепочечную ДНК
Описание
Для репликации вирусу необходимо попасть в ядро клетки-мишени и воспользоваться ее ДНК-полимеразой. Иногда вирус вызывает незапланированное деление самое клетки, то есть становится онкогенным. Эти вирусы хорошо изучены.
Пример: Вирус герпеса, адено- и папилломавирусы
Вирусы, содержащие одноцепочечную ДНК
Описание
Попадая в ядро клетки, вирусы образуют двухцепочечную ДНК, после чего реплицируются так же, как вирусы класса I.
Пример: Парво- и цирковирусы
Вирусы, в которых РНК способна к репликации (редупликации)
Описание
Вирусы этого класса могут размножаться в цитоплазме клетки, им не нужна молекула ДНК. Каждый ген, находящийся в РНК вируса, кодирует только один вирусный белок.
Пример: Бирна- и реовирусы
Вирусы, содержащие одноцепочечную (+) РНК
Описание
Из геномной (+) РНК на рибосомах хозяина создаются вирусные белки. В одном фрагменте РНК могут быть закодированы разные белки, что увеличивает сложность вируса без удлинения генов.
Пример: Пикорнавирусы (полиомиелит, гепатит А) и коронавирусы
Вирусы, содержащие одноцепочечную (–) РНК
Описание
(–) РНК этих вирусов предварительно должна быть транскрибирована в (+) РНК вирусными РНК-полимеразами, после чего может начаться синтез вирусных белков. Вирусы этого класса делятся еще на две группы, в зависимости от их генома и места его репликации (цитоплазма или ядро).
Пример: Филовирусы, аренавирусы (геморрагическая лихорадка Ласса), ортомиксовирусы (вирусы гриппа) и так далее.
Вирусы, содержащие одноцепочечную (+) РНК, реплицирующиеся через стадию ДНК
Описание
Такие вирусы используют фермент обратную транскриптазу для превращения (+) РНК в ДНК, которая встраивается в геном хозяина ферментом интегразой. Дальнейшая репликация происходит при помощи полимераз клетки хозяина.
Пример: Ретровирусы (в том числе ВИЧ)
Вирусы, содержащие двухцепочечную ДНК, реплицирующиеся через стадию одноцепочечной РНК
Описание
Молекула ДНК замкнута в кольцо и является матрицей для синтеза мРНК и дополнительных молекул РНК, которые используются при репликации вирусного генома обратными транскриптазами.
Пример: Колимовирусы (вызывают инфекции растений) и гепаднавирусы (например, гепатит В)
Вакцинация и лечение
Как правило, организмы умеют бороться с паразитирующими на них вирусами. На примере млекопитающих и человека мы обычно говорим о главном инструменте — врожденном иммунитете.
Впрочем, наиболее эффективен этот вид защиты в отношении бактериальных инфекций и не может обеспечить продолжительную и надежную защиту, особенно от инфекций вирусных.
Именно поэтому огромное значение имеет приобретенный иммунитет, в результате которого клетки иммунной системы обучаются вырабатывать специфические к вирусу антитела, способные уничтожать как саму вирусную частицу, так и зараженные ею клетки.
Еще одна врожденная система борьбы с вирусными инфекциями — внутриклеточная. Как правило, клетка способна распознать чужеродную РНК в своей цитоплазме, куда ее сперва и доставляют многие вирусы, и имеет специальные комплексы для ее деградации. Но часть вирусов научились обходить и эту ловушку. К примеру, ротавирусы, которые даже внутри клетки сохраняют капсид с геномной РНК.
Миссия: уничтожить
Основная сложность в лечении вирусных заболеваний заключается в том, что они используют естественные функции клеток-мишеней для своего размножения, поэтому ученым зачастую оказывается не так-то просто придумать препарат, который будет токсичен для вируса и безопасен для самой клетки. Если такой безопасности достичь не удастся, лекарство будет иметь слишком много побочных эффектов, повреждающих сам организм, что окажется нецелесообразно для использования.

Сравнение жизненных циклов ВИЧ и вируса гриппа. Если первый использует обратную транскрипцию и живет в клетках иммунной стистемы, вирион второго, проникая в эпительные клетки дыхательных путей целиком - а именно там он и обитает - распадается уже внутри клетки, а репликация вирусной РНК происходит в ядре с помощью вирусных полимераз PA, PB1 и PB2 путем комплементарного копирования.
По принципу действия противовирусные препараты подразделяются на две группы: стимулирующие иммунную систему атаковать вирусы (например, за счет индукции синтеза белков-интерферонов) и атакующие вирусы напрямую. Препараты второй группы различаются по этапу жизненного цикла вируса, на котором они активны: это препараты, препятствующие проникновению вируса в клетку, препятствующие размножению вируса внутри клетки и препятствующие выходу копий вируса из клетки.
Еще один класс противовирусных препаратов блокирует ферменты, необходимые для создания и модификаций белков вируса. Такие лекарства называют протеазными ингибиторами.
Вместо заключения: а могут ли вирусы приносить пользу?
Безусловно, да. Несмотря на то, что вирусы ассоциируются у большинства людей с однозначным вредом, они могут приносить и пользу — если речь идет о так называемых вирусных векторах и терапевтических подходах на их основе.
Исследователи давно научились помещать в белковую оболочку вируса интересующие их нуклеиновые кислоты, чтобы доставлять нужный ген в клетки, а также убирать те гены, которые делают вирус опасным для организма.
Это позволило сделать возможной генную терапию, помогающую бороться с заболеваниями, вызванными известными генетическими мутациями. Создание вирусных векторов — достаточно непростая задача, к тому же ограниченная свойствами самих вирусных частиц: количеством помещающейся генетической информации, местом ее вставки, стабильностью. Кроме того, вирусный вектор, используемый в медицине, не должен вызывать иммунного ответа или критично влиять на жизнедеятельность клетки. Тем не менее эти сложности решаются, поэтому уже одобрен ряд вполне успешных и безопасных генных терапий. А в качестве основы для вирусных векторов чаще всего используются ретро-, ленти-, адено- и аденоассоциированные вирусы.
Читайте также:

