Лимфаденит герпес у детей
Обновлено: 24.04.2024
Инфекции вируса простого герпеса у детей
Вирус простого герпеса - распространенная причина возникновения патологических очагов в полости рта у детей до 3 лет и у школьников. Первичный герпетический гингивостоматит начинается с распространенных везикул и пустул в периоральной области, а также везикул и эрозий в полости рта. Десны становятся отечными, красными, рыхлыми и легко кровоточат. Эпителиальные клеточные массы и экссудат образуют пленку на поверхности слизистой оболочки.
Высыпания обычно сопровождаются лихорадкой, раздражительностью и увеличением шейных лимфоузлов. Очаги могут также распространяться на лицо и верхнюю часть туловища. У детей грудного и младшего детского возраста они нередко появляются на кистях вследствие аутоинокуляции. Выраженность симптомов в течение 7-10 дней постепенно уменьшается, в течение этого периода необходимо обследовать пациентов с целью контроля обезвоживания.
Герпетический гингивостоматит следует дифференцировать с энтеровирусными инфекциями, при которых обычно развиваются везикулы, изъязвления и петехии на твердом нёбе, но без поражения десен. Хотя афты могут быть очень болезненными, эти очаги, как правило, изолированные, без диффузного воспаления, которое ассоциируется с герпесом.
Первичные инфекции простого герпеса могут поражать любые участки кожи и слизистых оболочек, что обычно происходит вследствие прямой инокуляции ранее травмированных участков. Очаги состоят из герпетиформных или сгруппированных красных папул, из которых через 24-48 ч развиваются везикулы и, нередко, пустулы. В течение следующих 5-7 дней везикулы вскрываются и покрываются корочкой. Десквамация и заживление занимают 10-14 дней.

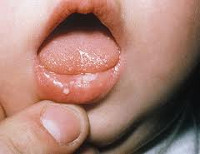
Герпетический гингивостоматит:
а - у этого 6-летнего мальчика развились распространенные везикулы в периоральной области и эрозии на слизистой оболочке при первом эпизоде простого герпеса
б - 19-летний юноша испытывал сильную боль вследствие распространенных везикул и эрозий на слизистой десен и щек во время пика первичной инфекции простого герпеса.
Первичная герпетическая инфекция на дистальном участке пальца кисти называется герпетическим панарицием. Как и в случае герпетического гингивостоматита, первичные инфекции на других участках сопровождаются болезненной локальной аденопатией и гриппоподобными симптомами.
У детей большинство инфекций вызывается ВПГ-1, в то время как ВПГ-2 обычно обнаруживают при генитальных инфекциях у подростков и взрослых. Однако ВПГ-2 можно обнаружить не только на участках гениталий, а ВПГ-1 может переноситься изо рта на руки и на гениталии. Хотя возможность полового контакта необходимо учитывать у любого ребенка с генитальным герпесом, чаще всего источник заболевания, вероятно, не венерический.
Везикулы обычно локализуются только в области промежности и кожи гениталий и быстро изъязвляются. Эритема и отек могут приводить к тяжелой дизурии и задержке мочеиспускания.
У детей с иммунодефицитом или у пациентов с некоторыми кожными заболеваниями, такими как атопический дерматит, себорейный дерматит и иммунологические пузырные заболевания, инфекция простого герпеса может распространиться на всю кожную поверхность (герпетическая экзема Капоши), а также в легкие, внутренние органы и ЦНС. ВПГ может также вызвать сепсис и/или менингит с тяжелыми неврологическими осложнениями или угрожающими жизни пациентов отделения для выхаживания новорожденных.
Ранняя диагностика и противовирусная терапия могут уменьшить тяжесть заболевания и смертность в этой клинической ситуации.

Первичная инфекция простого герпеса:
а - многокамерный пузырь наблюдался на пальце этого ребенка с герпетическим панарицием
б - у 4-летнего мальчика герпетический панариций развился вследствие аутоинокуляции от очагов в полости рта. Очаги в полости рта и на пальце разрешились без терапии через 2 нед
в - у здоровой 3-летней девочки развились сгруппированные однородные везикулы и пустулы на 4-м пальце ступни в сочетании с болезненной эритемой, отеком и стерильным лимфангиитом на тыльной стороне стопы
После первоначального эпизода вируса простого герпеса (ВПГ) переходит в латентное состояние. Ряд эндогенных и экзогенных факторов может вызывать реактивацию вируса, в том числе стрептококковая инфекция горла, инфекции верхних дыхательных путей, солнечный ожог и хирургическая операция. Очаги обычно возникают вблизи места первичных высыпаний, слизистые оболочки, как правило, не поражаются, системные симптомы отсутствуют, и высыпания заживают меньше чем за неделю.
Хотя рецидивы непредсказуемы, со временем периоды между эпизодами увеличиваются даже у тех лиц, у которых вначале они были частыми.
Клиническое подозрение на простой герпес можно быстро подтвердить тестом Тцанка в отделении реанимации или у постели больного. Лабораторный анализ на вирусную культуру дает положительный результат через 12-36 ч. В некоторых центрах в качестве быстрых и надежных методов подтверждения диагноза применяются ПЦР и иммунофлуоресцентное окрашивание содержимого пузыря на предметном стекле. Мазок по Тцанку берут, удалив покрышку пузыря скальпелем или ножницами, путем соскоба в основании пузыря, чтобы получить влажную и мутную клеточную массу. Полученный материал размазывают по предметному стеклу скальпелем, подсушивают 95% этанолом и окрашивают по Гимзе или Райту.

Инфекция простого герпеса:
а - сгруппированные пустулы появились на задней поверхности бедра у подростка с инфекцией рецидивирующего ВПГ-2.
б - высыпания рецидивирующего простого герпеса вокруг глаз у 11-летнего мальчика.
Роговица не была поражена, везикулы покрылись корочкой менее чем через неделю.
в - у 16-летней сексуально активной девушки развились болезненные везикулы в области гениталий, которые разрешились после 10 дней приема ацикловира перорально.
Диагностическим признаком при вирусном происхождении пузыря является многоядерная гигантская клетка, которая представляет собой слияние эпидермальных клеток с наслоениями многих ядер, поэтому такая клетка намного больше, чем другие воспалительные клетки. К сожалению, в тесте Тцанка невозможно дифференцировать ВПГ и ветряную оспу, поэтому, если этого требует клиническая ситуация, необходим культуральный анализ. Если риск вирусной инфекции высокий и задержка с началом лечения может стать катастрофической для пациента, особенно при иммунодефиците, следует начать противовирусную терапию, даже если результат теста Тцанка отрицательный, пока диагноз не будет подтвержден более чувствительными и специфическими методами.
В целом, при герпетических инфекциях проводится симптоматическая терапия с применением прохладных компрессов, лубрикантов и системных анальгетиков. Местные противовирусные препараты малоэффективны при терапии неосложненных инфекций у иммунокомпетентных индивидуумов. Состояние детей с иммунодефицитом в случае первичных или рецидивирующих инфекций простого герпеса и пациентов с тяжелым первичным герпетическим гингивостоматитом или генитальным герпесом обычно быстро улучшается при парентеральном введении ацикловира (5 мг/кг массы тела каждые 8 часов).
Некоторым пациентам, особенно детям старшего возраста без поражения слизистой полости рта, можно назначить ацикловир перорально. Некоторые из назначаемых внутрь препаратов, в частности валацикловира гидрохлорид и фамцикловир, обеспечивают достаточные уровни лекарства в крови. Хотя они еще не разрешены для применения у детей, необходимо следить за изменениями в инструкции по применению, поскольку эти медикаменты могут стать безопасной и эффективной альтернативой парентеральному введению ацикловира для детей с серьезными герпетическими инфекциями. В случае рецидивирующего заболевания прием внутрь ацикловира при продромальных признаках болезненности кожи перед появлением пузырей может уменьшить длительность эпизода заболевания.
Отдельным детям с частыми, множественными, распространенными рецидивирующими высыпаниями может потребоваться длительная супрессивная терапия. Недавние исследования показали, что длительная профилактическая терапия детей грудного возраста после неонатальной инфекции ВПГ может уменьшить риск неврологических осложнений.

Образование пузырей при дистальном дактилите на большом и указательном пальцах правой кисти у 5-летней девочки.
Культуральный анализ материала из горла и большого пальца кисти показал наличие бета-гемолитических стрептококков группы А.
Инфекция быстро прореагировала на пероральный прием амоксициллина.
Инфекцию вируса простого герпеса (ВПГ) обычно дифференцируют с другими пузырьковыми высыпаниями по типично сгруппированным элементам, клиническому течению, положительному результату теста Тцанка и культуральному анализу, а также по характерным результатам биопсии кожи. Импетиго может имитировать герпес, однако пузыри обычно довольно крупные, с корочкой в центре и распространяются по периферии, а окрашивание по Граму выявляет грамположительные кокки.
Пузырный дистальный дактилит, вызванный b-гемолитическими стрептококками группы А или St. aureus, можно ошибочно принять за герпетический панариций. При стафилококковой или стрептококковой инфекции очаги на кончике пальца обычно сливаются и образуют один или несколько пузырей диаметром 5-10 мм, а окрашивание по Граму и культуральный анализ показывают наличие бактериального возбудителя. В отличие от импетиго на других участках, пузыри на пальцах напряженные, поскольку роговой, или наружный, слой эпидермиса на акральных участках толстый. Иногда высыпания простого герпеса могут иметь дерматомное распределение. В этой ситуации необходим анализ на вирусную культуру, чтобы исключить опоясывающий лишай.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Герпетический стоматит у детей – острое воспалительное поражение слизистой оболочки полости рта, вызываемое вирусом простого герпеса. Герпетический стоматит у детей проявляется лихорадкой, лимфаденитом, слюнотечением, тошнотой, везикулярными высыпаниями, эрозиями и афтами в ротовой полости, потерей аппетита. Диагноз герпетического стоматита у детей ставят по данным анамнеза, клинической картины, цитологического исследования, РИФ, ПЦР, ИФА. Лечение герпетического стоматита у детей включает противовирусную, десенсибилизирующую, иммунокорригирующую терапию, местную обработку полости рта, физиопроцедуры.
Общие сведения
Герпетический стоматит у детей – герпес-вирусная инфекция, протекающая с преимущественным поражением слизистой полости рта и явлениями общей интоксикации. В педиатрии и детской стоматологии герпетический стоматит занимает первое место среди воспалительных заболеваний полости рта у детей, составляя почти 80% случаев. Герпетический стоматит рассматривается как проявление первого контакта организма ребенка с вирусом простого герпеса I типа. Наиболее часто герпетический стоматит встречается у детей от 1 до 3 лет, что связано с их возрастно-морфологическими особенностями, снижением уровня трансплацентарных антител и незрелостью клеточного и специфического иммунитета. Герпетический стоматит может наблюдаться и у детей первого года жизни, с первых месяцев находящихся на искусственном вскармливании.
Выделяют два типа герпетического стоматита у детей: первичный острый и хронический рецидивирующий. Дети, переболевшие острым герпетическим стоматитом, становятся бессимптомными вирусоносителями или страдают хроническим типом инфекции. Герпетический стоматит у детей может сопровождаться поражением нервной системы и внутренних органов, угнетением иммунных реакций, поэтому требует серьезного внимания со стороны педиатров, детских стоматологов, детских иммунологов, детских неврологов и других специалистов.

Причины герпетического стоматита у детей
ВПГ I типа – ДНК-содержащий вирус, относящийся к семейству Herpesviridae и клинически проявляющийся высыпаниями на коже лица и слизистой оболочке ротовой полости. Попадая в организм ребенка, ВПГ активно размножается в эпителиальных клетках и окружающих лимфатических узлах (чаще всего, подчелюстных), проникает в кровяное русло (первичная вирусемия), а оттуда в различные органы (печень, селезенку и др.) с последующим размножением и вторичной вирусемией. На следующем этапе наблюдается поражение кожи и слизистых губ, полости рта и зева с развитием у детей симптомов герпетического стоматита. Герпесная инфекция способна переходить в латентную форму с пожизненной персистенцией вируса в нервных ганглиях.
Источником возбудителя являются дети, больные острым герпетическим стоматитом, взрослые с рецидивирующим герпесом губ и вирусоносители. Герпетический стоматит очень заразен: ВПГ I типа может передаваться здоровым детям контактно-бытовым (через поцелуи, игрушки, предметы обихода) и воздушно-капельным путем (при кашле и чихании), возможна вертикальная передача от матери к плоду (при рецидиве герпеса с вирусемией у беременной).
Рецидивы хронического герпетического стоматита у детей возникают на фоне подавления иммунитета под действием провоцирующих факторов: переохлаждения, перегревания, длительной инсоляции, эмоционального стресса, авитаминоза, приема больших доз антибиотиков, перенесенных ОРВИ. Чаще всего герпетический стоматит у детей наблюдается в весенне-осенний период.
Симптомы герпетического стоматита у детей
В зависимости от клинических симптомов герпетический стоматит у ребенка может протекать в легкой, среднетяжелой и тяжелой формах; в его развитии выделяют инкубационный, продромальный периоды, разгар болезни (катаральный, период высыпаний), период угасания и клинического выздоровления. Среди детей чаще встречаются легкие и среднетяжелые формы герпетического стоматита.
Латентный период герпетического стоматита у детей составляет от 2 до 14 дней. В продромальном периоде ребенок становится беспокойным, капризничает, плачет, отказывается от пищи, плохо спит. Отмечаются слюнотечение, тошнота, рвота, увеличение и болезненность подчелюстных и шейных лимфоузлов.
Образование везикул продолжается в течение 2-4 дней и сопровождается сильной болезненностью. Одновременно можно наблюдать высыпания на разных стадиях развития. Афты и эрозии постепенно очищаются и затягиваются без рубцевания. Для герпетического стоматита у детей характерно волнообразное течение: появление высыпаний с лихорадкой завершается коротким стабильным периодом, затем начинается новая волна высыпаний с очередным скачком температуры.
При сниженном иммунитете и присоединении вторичной бактериальной инфекции возникают гнойничковые поражения слизистой и кожи. Острый герпетический стоматит у детей в зависимости от тяжести течения и эффективности лечения может продолжаться от 7 до 14 дней. Опасное течение острая герпесвирусная инфекция может приобретать в первые месяцы жизни ребенка в связи с генерализацией поражения, риском развития септического состояния, поражения внутренних органов, серозных оболочек мозга.
Диагностика герпетического стоматита у детей
Диагноз герпетического стоматита у детей ставится на основании клинической картины, анамнеза, результатов цитологического, вирусологического и серологического исследований.
Для идентификации вируса может использоваться сыворотка крови, слюна, мазки, смывы или соскобы со слизистой ротовой полости. Установить возбудителя герпетического стоматита у детей можно методом иммунофлюоресценции (РИФ) и ПЦР. Серологическую идентификацию титра вирусных антител проводят с помощью ИФА и РСК.
Герпетический стоматит у детей необходимо дифференцировать от других видов стоматита (аллергического, медикаментозного, грибкового), герпетической ангины, специфических инфекций (кори, скарлатины, ветряной оспы, дифтерии), многоформной эксудативной эритемы.
Лечение герпетического стоматита у детей
При неосложненном течении герпетического стоматита лечение амбулаторное, в осложненных случаях и у детей первых трех лет жизни может потребоваться госпитализация. Детям с герпетическим стоматитом показаны постельный режим, обильное питье, протертая, теплая, нераздражающая пища, пользование отдельной посудой и предметами гигиены.
Комплексное лечение герпетического стоматита у детей (общее и местное) подбирают в зависимости от периода заболевания и степени выраженности симптомов. При лихорадке и болезненности назначают парацетамол, ибупрофен; для снятия отека - антигистаминные препараты (мебгидролин, клемастин, хифенадин). Системная этиотропная терапия (ацикловир, интерферон) более эффективна в начальном периоде. С целью иммунокоррекции назначаются лизоцим, экстракты тимуса, инъекции гамма-глобулина.
Местное лечение герпетического стоматита у детей проводится детским стоматологом и детским пародонтологом. Осуществляется ежедневная обработка слизистой оболочки полости рта антисептиками, анестетиками, отварами трав, смазывание противовирусными препаратами. При среднетяжелой форме герпетического стоматита у детей для очищения поверхности слизистой от некротических масс используются растворы протеолитических ферментов (трипсина, химотрипсина).
В период эпителизации эрозий применяют кератопластические средства (витамины A, Е, масло шиповника и облепихи). Физиолечение при герпетическом стоматите у детей назначают с первых дней заболевания (УФО, инфракрасное облучение). При рецидивирующем герпетическом стоматите у детей показаны курсы общеукрепляющих средств (витаминов C, В12, рыбьего жира), высококалорийная диета.
Прогноз и профилактика герпетического стоматита у детей
Герпетический стоматит у детей в большинстве случаев заканчивается клиническим выздоровлением через 10-14 дней. В тяжелых случаях существует риск осложнений в виде герпетического кератоконъюнктивита, герпетического энцефалита, генерализации инфекции.
Предотвратить контакт детей с герпесвирусной инфекцией невозможно, т.к. носительство ВПГ среди взрослого населения составляет 90 %. Профилактика герпетического стоматита может включать изоляцию больного ребенка от здоровых детей, ограничение контактов со взрослыми в активной фазе инфекции, соблюдение правил личной гигиены, закаливание, занятия физкультурой.
Лимфаденит у детей – это воспалительная реакция лимфатических узлов в ответ на локальные или общие патологические процессы в организме. Серозный лимфаденит у детей протекает с увеличением, уплотнением, болезненностью лимфоузлов; гнойный лимфаденит сопровождается местными (гиперемией, отеком) и общими симптомами (резким ухудшением самочувствия, лихорадкой). Диагноз лимфаденита у детей устанавливается на основании клинического осмотра, общего анализа крови, УЗИ и пункции лимфоузлов. В лечении лимфаденита у детей применяется консервативная тактика (антибактериальная, десенсибилизирующая, дезинтоксикационная терапия, местные аппликации, УВЧ) или хирургическое вскрытие и дренирование гнойного очага с обязательной ликвидацией первичного источника инфекции.
МКБ-10
Общие сведения
Лимфаденит у детей – инфекционный или неинфекционный воспалительный процесс в периферических органах лимфатической системы – лимфоузлах. Лимфадениту принадлежит одно из ведущих мест по частоте встречаемости в педиатрической практике, что обусловлено морфофункциональной незрелостью лимфатической системы ребенка. Чаще всего лимфаденит наблюдается у детей в возрасте от 1 до 6 лет и имеет более бурное течение, чем у взрослых. Лимфаденит у детей развивается вторично, осложняя течение основных инфекционно-воспалительных заболеваний, поэтому увеличение лимфатических узлов у ребенка может обнаруживаться различными детскими специалистами: врачом-педиатром, детским отоларингологом, детским стоматологом, детским хирургом, детским иммунологом, детским ревматологом и др.

Причины
Рост и развитие лимфоидных образований у детей продолжается до 6-10 лет; этот период связан с повышенной восприимчивостью к различным инфекционным агентам и недостаточной барьерно-фильтрационной функцией. Лимфоузлы, как элементы иммунной защиты, вовлекаются во все патологические процессы, протекающие в организме: распознавая и захватывая чужеродные частицы (бактерии, токсины, продукты распада тканей), они препятствуют их распространению из местного очага и попаданию в кровь.
Лимфаденит у детей чаще всего имеет неспецифический генез, его основными возбудителями являются гноеродные микроорганизмы, в первую очередь, стафилококки и стрептококки. При лимфадените у детей обычно имеется первичный очаг острого или хронического гнойного воспаления, из которого инфекция попадает в лимфоузлы с током лимфы, крови или контактным путем.
Более 70% случаев лимфаденита у детей связано с воспалительными процессами ЛОР-органов - тонзиллитом, синуситом, отитом. Лимфаденит у детей часто сопутствует инфекциям кожи и слизистых оболочек: фурункулам, пиодермии, гнойным ранам, экземе, стоматиту. Лимфаденит может осложнять течение различных бактериальных и вирусных инфекций у детей - скарлатины, дифтерии, ОРВИ, гриппа, паротита, ветряной оспы, кори. Наибольшее количество лимфаденитов у детей отмечается в осенне-зимний период вследствие увеличения числа инфекционных и обострения хронических заболеваний.
Лимфаденит у детей старше 6-7 лет может быть связан с воспалительными заболеваниями зубо-челюстной системы (пульпитом, периодонтитом, остеомиелитом). При этом нарастание симптомов лимфаденита у детей может происходить после затухания патологического процесса в первичном очаге. Причиной специфического лимфаденита у детей являются инфекционные заболевания с типичным для них поражением лимфатических узлов - туберкулез, инфекционный мононуклеоз, бруцеллез, актиномикоз, сифилис и др.
В некоторых случаях лимфаденит у детей может быть связан с заболеваниями крови (острыми и хроническими лейкозами), опухолями лимфоидной ткани (лимфосаркомой, лимфогрануломатозом), а также травматическим повреждением самих лимфоузлов. Лимфаденит обычно наблюдается у детей с лимфатико-гипопластическим диатезом, часто болеющих ОРВИ, имеющих в анамнезе сопутствующие герпесвирусные инфекции (ЦМВ, вирус Эпштейна-Барра) и хронические заболевания ЖКТ.
Классификация
В зависимости от типа возбудителя выделяют неспецифический и специфический лимфаденит у детей, который может иметь острое (до 2-х недель), подострое (от 2-х до 4-х недель) или хроническое (более месяца) течение. По характеру воспалительных изменений лимфатических желез у детей различают серозные (инфильтрационные), гнойные, некротические (с расплавлением узлов) лимфадениты и аденофлегмоны.
По очагу поражения лимфадениты у детей разделяют на регионарные (шейные, подчелюстные, подмышечные, паховые и т. д.) и генерализованные; по этиологическому фактору - одонтогенные (связанные с патологией зубо-челюстной системы) и неодонтогенные.
Симптомы
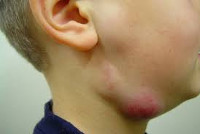
Как правило, при лимфадените у детей поражаются лимфоузлы в области лица и шеи (наиболее часто - подчелюстные и шейные с одной или обеих сторон, реже - околоушные, щечные, затылочные, заушные), в отдельных случаях – подмышечные, паховые.
Серозная стадия острого неспецифического лимфаденита у детей (1-3 сутки заболевания) проявляется болезненными, заметно увеличенными в размерах и плотно-эластичными на ощупь регионарными лимфоузлами, без потери их подвижности и развития местной кожной реакции. Общее состояние ребенка не нарушено, температура колеблется от нормальных до субфебрильных значений.
Переход острого лимфаденита в гнойную стадию (3-6 сутки заболевания) протекает с ярко выраженными местными признаками и резким ухудшением самочувствия детей. Наблюдаются признаки интоксикации: озноб, высокая температура (до 40ºС), головная боль, сильная слабость, отсутствие аппетита и нарушение сна. В области пораженных лимфоузлов возникают интенсивные тянущие или стреляющие боли, явления периаденита, местная гиперемия и отек кожи. Возможно развитие аденофлегмоны с появлением очагов флюктуации и выходом гнойного воспаления за пределы лимфоузла. Аденофлегмоны челюстно-лицевой области могут осложниться тромбозом кавернозного синуса, медиастинитом, сепсисом.
Хроническая форма лимфаденита у детей может развиться первично, если возбудителями являются слабовирулентные микроорганизмы, или стать продолжением острой формы заболевания. При хроническом течении вне обострения лимфоузлы увеличены, ограничены в подвижности, достаточно плотные, но безболезненные; самочувствие ребенка не нарушено; нагноение развивается редко. При наличии у ребенка очага хронической инфекции, длительно поддерживающего вялотекущий лимфаденит, лимфоузлы постепенно разрушаются и замещаются грануляционной тканью.
Туберкулезный лимфаденит у детей имеет продолжительное течение, ограничивается обычно шейной группой лимфоузлов, собранных в плотный, безболезненный, значительный пакет, похожий на ошейник. Туберкулезный лимфаденит у детей может осложняться казеозным распадом, образованием свищевых ходов, рубцовыми изменениями кожи.
Диагностика
Диагностика лимфаденита у детей включает тщательный физикальный осмотр, оценку клинической картины и анамнеза заболевания, исследование клинического анализа крови, УЗИ лимфатических узлов и ряд дополнительных дифференциально-диагностических исследований. Выявление лимфаденита у детей может потребовать обследования у врачей различных специальностей: педиатра, инфекциониста, детского отоларинголога, гематолога, хирурга, фтизиатра.
В ходе диагностики необходимо установить этиологию лимфаденита у детей, выявить первичный очаг гнойного воспаления. Вспомогательными методами выявления туберкулезного лимфаденита у детей служат туберкулиновые пробы, рентгенография грудной клетки, диагностическая пункция и бактериологический посев материала. При подозрении на онкологический процесс выполняется биопсия лимфатических узлов с цитологическим и гистологическим исследованием ткани.
Дифференциальная диагностика лимфаденитов различной локализации у детей проводится с опухолями слюнных желез, метастазами злокачественных новообразований, флегмоной, ущемленной паховой грыжей, остеомиелитом, системными заболеваниями (саркоидоз, лейкоз), диффузными заболеваниями соединительной ткани (ювенильный ревматоидный артрит, системная красная волчанка, дерматомиозит).
Лечение лимфаденита у детей
Лечение лимфаденита у детей определяется стадией, типом заболевания, степенью интоксикации и направлено на купирование инфекционно-воспалительных процессов в лимфоузлах и устранение первичного очага инфекции.
При остром серозном и хроническом неспецифическом лимфадените у детей применяют консервативную терапию, включающую антибиотики (цефалоспорины, полусинтетические пенициллины, макролиды), десенсибилизирующие средства, местное лечение (сухое тепло, компрессы с мазью Вишневского, УВЧ). Показаны общеукрепляющие препараты – кальция глюконат, аскорутин, витамины, иммуностимуляторы.
При отсутствии эффекта терапии или переходе лимфаденита в гнойную стадию, ребенка госпитализируют и проводят экстренное вскрытие, дренирование и санацию гнойного очага. В случае некротического лимфаденита у детей выполняют тщательный кюретаж полости, при необходимости производят удаление лимфоузла. В послеоперационном периоде показана комплексная противовоспалительная и дезинтоксикационная терапия. Лечение специфического туберкулезного лимфаденита у детей проводят в специализированных лечебных учреждениях.
Прогноз и профилактика
Прогноз лимфаденита у детей при своевременном адекватном лечении – благоприятный, при длительном хроническом течении возможно замещение лимфоидной ткани на соединительную; иногда в области пораженных лимфоузлов развивается нарушение лимфооттока (лимфостаз).
Предупреждение лимфаденита у детей заключается в устранении источников хронической инфекции, своевременном лечении зубов, травматических и гнойных поражений кожи и слизистых оболочек, повышении общей и местной сопротивляемости организма.
1. Лечение острых лимфаденитов шеи в детской хирургической практике: Автореферат диссертации/ Джабарова Е.В. - 2012.
2. Оптимизация диагностики и лечения лимфаденита лица и шеи у детей: Автореферат диссертации/ Анохина И.В. - 2013.
3. Лимфадениты, лимфангоиты, лимфоаденопатии челюстно-лицевой области: учеб.-метод. пособие/ Н.Н. Черченко. – 2007.

2. Трухан Д.И. Лимфаденопатия неясного генеза // Справочник поликлинического врача. 2018. № 3. С. 16-24.
3. Савенкова М.С., Вашура Л.В., Абдулаев А.К., Анджель А.Е., Балакирева Г.М., Румянцева И.Г., Кузнецова Е.С. Значение герпесвирусных инфекций у детей // Педиатрия. Журнал им. Г.Н. Сперанского. 2015. Т. 95. № 2. С. 134-141.
4. Динова Е.А., Щербина А.Ю., Румянцев А.Г. Дифференциальная диагностика лимфоаденопатий в практике врача // Трудный ребенок. 2007. Т. 5. № 2. С. 15-16.
5. Нагорная Н.В., Бордюгова Е.В., Вильчевская Е.В., Дудчак А.П., Марченко Е.Н. Лимфоаденопатия у детей // Здоровье ребенка. 2013. Т. 49. № 6. С. 166-172.
6. Маркелова Е.В., Кныш С.В., Невежкина Т.А., Байбарина Е.В. Альфа-герпесвирусы: современный взгляд на структуру // Тихоокеанский медицинский журнал. 2018. № 4 (74). С. 5-9. DOI: 10.17238/PmJ1609-1175.2018.4.5–9.
7. Инфекционные болезни: национальное руководство / Под ред. Н.Д. Ющука, Ю.Я. Венгерова. М.: ГЭОТАР-Медиа, 2009. С. 262-269, 752-800.
8. Неверов В.А., Демиденко Т.П., Васильев В.В. Герпесвирусные инфекции, вызываемые лимфотропными вирусами. Часть III // Российский семейный врач. 2018. Т. 22. № 1. С. 5-11. DOI: 10.17816/RFD201815-11.
9. Неверов В.А., Демиденко Т.П., Васильев В.В. Герпесвирусные инфекции, вызываемые лимфотропными вирусами. Часть IV // Российский семейный врач. 2018. Т. 22. № 2. С. 5-13. DOI: 10.17816/RFD201825-13.
10. Неверов В.А., Демиденко Т.П., Васильев В.В. Герпесвирусные инфекции, вызываемые лимфотропными вирусами. Часть V // Российский семейный врач. 2018. Т. 22. № 3. С. 5-13. DOI: 10.17816/RFD201835-13.
13. Долгих Т.И., Соколова Т.Ф., Турок Н.Е., Носкова Ф.В. Клинико-лабораторные параллели герпесвирусных инфекций, сопряженных с лимфоаденопатиями у детей // Педиатрия. Журнал им. Г.Н. Сперанского. 2011. Т. 90. № 4. С. 70-72.
Лимфаденопатия является одним из симптомов многих заболеваний, различных как по клинической картине, так и по методам диагностики и лечения [1]. Одна из основных функций лимфатических узлов - барьерная, снижена у детей раннего возраста, что объясняет генерализацию инфекции в данной возрастной группе. В большинстве случаев причиной увеличения лимфатических узлов различной локализации у детей и подростков являются процессы, не связанные ни с гематологическими, ни с онкологическими заболеваниями, причиной гипертрофии лимфоидной ткани является инфекционный процесс 3. Чаще всего на детский возраст приходится инфицирование герпесвирусами, в особенности вирусом Эпштейна-Барр [4].
По данным ВОЗ, герпесвирусная инфекция занимает второе место после гриппа и ОРВИ в структуре заболеваемости вирусными инфекциями [5]. Известно, что большинство жителей нашей планеты в разные периоды жизни инфицируются хотя бы одним, а чаще несколькими типами вирусов, относящимися к семейству герпесвирусов (ГВ). У половины из них заболевание протекает с рецидивирующим течением. Особенностью герпесвирусной инфекции является сохранность вируса в организме в течение всей жизни и развитие транзиторных нарушений иммунной регуляции, обусловленных недостаточностью различных звеньев иммунной системы [2; 4; 5].
α-Герпесвирусы характеризуются быстрой репликацией вируса и цитопатическим действием на культуры инфицированных клеток. Репродукция α-герпесвирусов протекает в различных типах клеток, вирусы могут сохраняться в латентной форме, преимущественно в нервных ганглиях [6; 7].
β-Герпесвирусы видоспецифичны, поражают различные виды клеток, которые при этом увеличиваются в размерах (цитомегалия), могут вызывать иммуносупрессивные состояния. Инфекция может принимать генерализованную или латентную форму; в культуре клеток легко возникает персистентная инфекция [7].
Клинические формы заболеваний, вызываемых герпесвирусами [3; 11]
Вирус простого герпеса 1-го типа
Вирус простого герпеса 2-го типа
Варицелла зостер вирус
Вирус герпеса человека 6 типа
Вирус герпеса человека 7 типа
Экзантема у детей
Нейроинфекция при СПИДе
Цитомегалия у больных после трансплантации органов
Системные болезни после трансплантации
Вирус герпеса человека 8 типа
Энцефалит у новорожденных
Из всех известных герпесвирусов, по данным литературы, наиболее часто у детей с лимфаденопатией встречаются: вирус Эпштейна-Барр (ВЭБ), цитомегаловирус (ЦМВ), вирус простого герпеса человека 1-го и 2-го типов, вирус герпеса человека 6-го типа [12].
Таким образом, представляет определенный научный интерес изучение вклада герпесвирусных инфекций как этиологического фактора в развитие синдрома лимфаденопатии для проведения эффективной терапии [13].
Цель исследования: выявить особенности клинико-лабораторных параметров и инфекционной нагрузки у детей и подростков с лимфаденопатией инфекционной этиологии.
Материал и методы исследования
Все пациенты с лимфаденопатией инфекционной этиологии были разделены на 2 группы: первую группу составили дети раннего и дошкольного возраста (с 1 года 7 месяцев до 6 лет) – 58 человек, вторую группу - дети школьного возраста (с 7 лет и старше) – 60 человек. Всем детям было проведено серологическое исследование сыворотки крови методом иммуноферментного анализа (ИФА): определены специфические антитела класса IgM, IgG к следующим возбудителям: цитомегаловирусу, вирусу Эпштейна-Барр, вирусу простого герпеса 1 и 2 типов, вирусу герпеса 6 типа.
Проведена оценка анамнеза (особенности течения пре-, пери- и постнатального периодов, генеалогического анамнеза), клинических (характеристика лимфатических узлов, наличие увеличения и/или других изменений паренхиматозных органов - печени и/или селезёнки (по результатам УЗИ), выраженность симптомов интоксикации) и лабораторных параметров (особенности гемограммы).
Лейкоцитозом у детей старше 1 года считали уровень лейкоцитов выше 10*109/л. Оценка лейкоцитарной формулы проведена в относительных величинах: эозинофилией - уровень эозинофилов более 4%, нейтрофилезом - у детей 1-4 лет считали увеличение нейтрофилов более 50%, 5 лет и старше – выше 60%. За нормальное содержание моноцитов принимали 4-12%. Лимфоцитозом считали для детей 1-4 года – относительное количество лимфоцитов выше 60%; 5 лет и старше – выше 50% Ускоренным считался уровень СОЭ выше 10 мм/ч.
Все расчеты выполнены в операционной системе Windows XP с использованием пакета Microsoft Office XP. Исследования проведены на сертифицированном оборудовании: гематологический анализатор Syswex KX-21N, Япония (клинический анализ крови); автоматический анализатор для ИФА EVOLIS BIO-RAD, Франция (иммуноферментный анализ); аппарат Hitachi HI VISION Avius, Япония (ультразвуковое исследование).
Результаты исследования и их обсуждение
У преимущественного большинства детей, вошедших в исследование, определены специфические IgG к герпесвирусам, лишь у 16 человек (13,6%) - IgM. У детей раннего и дошкольного возраста (1 группа) чаще встречались антитела к цитомегаловирусу – 43 человека (74,1%), на втором месте по частоте встречаемости - к вирусу Эпштейна-Барр – 37 человек (63,8%). Реже встречались антитела к вирусу герпеса 1-го и 2-го типов – у 22 человек (37,9%) и вирусу герпеса 6-го типа – у 18 детей (31%).
Во второй группе (школьников) преобладали антитела к вирусу Эпштейна-Барр – 55 человек (91,7%), реже – к цитомегаловирусу – у 46 человек (76,7%), к вирусу герпеса 1-го и 2-го типов - у 29 человек (48,3%), к вирусу герпеса 6-го типа – у 10 детей (16,7%).
По данным анамнеза, более половины детей раннего и дошкольного возраста были отнесены в группу часто болеющих (частота заболеваемости в год 5 и более раз) - 60,3%, в отличие от школьников, среди которых часто болеющими были 41,7% человек.
У значительного числа детей и подростков отмечена гепато- и/или спленомегалия (по результатам УЗИ). При этом у детей раннего/дошкольного возраста данные изменения встречались чаще, чем у школьников (58,6% и 48,3% соответственно) (рис. 1).

Рис. 1. Частота встречаемости гепатолиенального синдрома
Выраженность интоксикационного синдрома имеет незначительные возрастные различия. Практически у половины пациентов первой группы (дети раннего возраста и дошкольники) (41,3%) определялись симптомы интоксикации: в 10,3% - субфебрильная температура, у 31% детей – другие симптомы интоксикации, такие как снижение аппетита, слабость, вялость, утомляемость, головная боль. Во второй группе (школьников) наблюдалась такая же ситуация: 48,3% человек имели симптомы интоксикации: субфебрилитет и другие (18,3% и 30% соответственно) (рис. 2).

Рис. 2. Частота встречаемости интоксикационного синдрома
По данным клинического обследования, больше чем у половины детей раннего/дошкольного возраста встречалось увеличение тонзиллярных (55,2%) лимфоузлов, практически у половины – подчелюстных (44,8%), реже - переднешейных (27,6%) и заднешейных (25,9%) лимфатических узлов. Тогда как больше чем у половины школьников (56,7%) наблюдалось увеличение подчелюстных, реже – переднешейных (45%), заднешейных (41,7%) и тонзиллярных (35%) лимфатических узлов.
У детей раннего/дошкольного возрастов очень редко встречалось увеличение затылочных, заушных и подбородочных лимфоузлов (1,7%). В данной группе пациентов не наблюдалось увеличения надключичных и подключичных лимфоузлов. В то время как у школьников отмечено увеличение подбородочных (3,3%), подключичных (3,3%) и надключичных (1,7%) лимфоузлов, увеличения заушных лимфатических узлов не наблюдалось.
По данным гемограммы, у равного количества детей обеих групп встречался лейкоцитоз и увеличение СОЭ (24,1%). Лимфоцитоз определялся в 44,8% и в 55% у детей первой и второй групп соответственно.
У детей раннего и дошкольного возраста (1 группа) моноцитопения отмечена у 29,3% детей, эозинофилия - 25,9%. Нейтрофилез наблюдался у 9 детей (15,5%), наличие мононуклеаров – у 5 детей (8,6%).
В группе школьников (2 группа) - в равной степени отмечены эозинофилия и моноцитопения (по 20%). Наличие мононуклеаров определено у 3 человек (5%). Значительно реже наблюдался нейтрофилез (3,3%) и лейкоцитоз (1,7%).
Таким образом, подтверждена важная роль вирусов семейства Herpesviridae в развитии лимфаденопатий у детей и подростков. Лидирующая роль в развитии лимфаденопатии принадлежит вирусам Эпштейна-Барр, цитомегаловирусу. Меньшее значение имеют вирусы простого герпеса 1 и 2 типов и вирус герпеса 6 типа. Отмечена высокая частота вирусных ассоциаций у детей и подростков с лимфоаденопатией - 74,6% (88 детей из 118). Наиболее часто у детей раннего и дошкольного возрастов с лимфаденопатией определялись антитела к цитомегаловирусу, тогда как у детей 7 лет и старше - к вирусу Эпштейна-Барр. Наряду с лимфаденопатией, у детей, вошедших в исследование, с большой частотой наблюдалась гепатомегалия, особенно у детей дошкольного и школьного возраста группы. У школьников чаще по сравнению с детьми раннего и дошкольного возраста выявлен длительный субфебрилитет. В гемограмме детей и подростков с лимфаденопатией в половине случаев отмечен лимфоцитоз, в 25% - ускорение СОЭ, в 20% - эозинофилия.
В связи с вышеизложенным в лечении детей и подростков с лимфаденопатией эффективным является определение вирусной нагрузки с последующей соответствующей терапией. Выявление причины гепатоспленомегалии и её возможная коррекция является важной составляющей комплексной индивидуализированной терапии и профилактики. Необходим постоянный клинико-лабораторный мониторинг состояния здоровья детей данной группы. При неэффективности комплексного лечения, включающего противовирусную направленную терапию, ребёнок должен быть проконсультирован онко-гематологом с целью уточнения диагноза.
Причины увеличения лимфоузлов у детей. Какую инфекцию предполагать?
Лимфатические узлы - это периферические органы иммунной системы. Они представляют собой биологические фильтры, которые задерживают чужеродные агенты, попавшие в организм, пытаются их обезвредить и участвуют в выработке иммунного ответа. Поэтому увеличение лимфоузлов в большинстве случаев говорит о наличии инфекции в организме, присутствии бактерий и вирусов. Ощупывать их нужно мягкими круговыми движениями, указательным, средним и безымянным пальцами. Нужно оценивать при этом следующие характеристики: болезненность, размеры, плотность, подвижность, изменения кожи над узлом. Они могут быть безболезненными, или ребенок может испытывать боль при касании, это обычно связано с размером узла. Чем он больше, тем сильнее растягивается покрывающая его капсула, и оказывается давление на рецепторы кожи. Размеры часто зависят от силы иммунного ответа и воспалительного процесса, протекающего в узле. Консистенция может быть тестообразной, лимфоузлы бывают очень твердыми или мягкими, эластичными. Кожа над узелком меняется обычно при гнойных процессах.
Эти периферические органы иммунитета могут увеличиваться местно. В таком случае речь идет об увеличении одного или двух узелков, находящихся недалеко от места воспаления. Например, увеличенные миндалины при ангине. Однако увеличение лимфоузлов может быть системным, во всем организме, в том числе и вокруг внутренних органов, например, около легких или селезенки. Разумеется, прощупать многие из внутренних узлов невозможно, тогда на помощь приходят рентгенография, УЗИ, компьютерная томография.
У детей увеличение лимфоузлов не всегда является патологией. Например, в норме у них прощупываются шейные, подмышечные, паховые узлы, в два года могут несколько увеличиваться миндалины во рту. Все это связано с перестройками в детской иммунной системе, когда большое количество клеток иммунитета мигрируют в узлы для своего дальнейшего развития.
При разных инфекциях характер измененных лимфатических узлов бывает специфическим, и это является ценным диагностическим признаком. Задача родителей сводится к регулярной проверке лимфатических узелков ребенка, ощупыванию и определению их характера, а также своевременному обращению к специалисту с подозрением на ту или иную инфекционную болезнь. Кстати, часто увеличенные узлы сочетаются с определенным типом лихорадки и многими другими симптомами, позволяющими врачу определить заболевание почти наверняка.
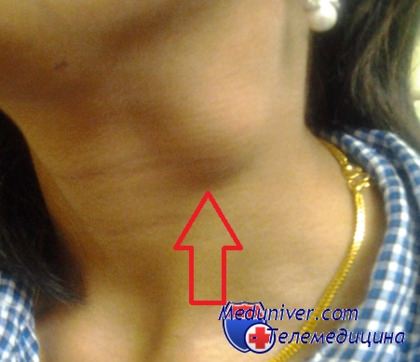
Инфекционный мононуклеоз вызывается вирусом, и хотя это заболевание встречается далеко не так часто, как обычная простуда, болеют им преимущественно дети младшего возраста. При этом заболевании увеличение ламфоузлов - один из основных признаков. В размерах меняются чаще всего парные шейные узлы, расположенные симметрично. При повороте головы в сторону они особенно четко видны. Иногда увеличиваются затылочные, к ним могут присоединяться также подмышечные и паховые узелки.
В норме узлы, которые прощупываются, похожи на просяное зернышко, то есть они довольна маленькие (до 50 мм), при этом подвижны, как говорят врачи "не спаяны с окружающими тканями". При мононуклеозе они могут увеличиваться до размеров горошины или даже куриного яйца. При касании они лишь слегка болезненны, сохраняют подвижность, на ощупь плотноваты, а кожа над ними выглядит обычно. В некотрых случаях шея видимо утолщается, за счет воспаления клетчатки вокруг лимфоузлов, так называемая "бычья шея". Иногда спустя 2-4 недели лимфоузлы несколько уменьшаются, но в целом остаются увеличенными длительное время: от нескольких месяцев до года.
Краснуха также характеризуется увеличением лимфатических узлов. В этом случае увеличение узлов системное, особенно сильно меняются в размерах затылочные и задние ушные лимофузлы. Они становятся плотными, и при их ощупывании ребенок испытывает боль. При этом повышается температура, затем на лице появляется сыпь, которая со временем "спускается" на туловище и конечности.
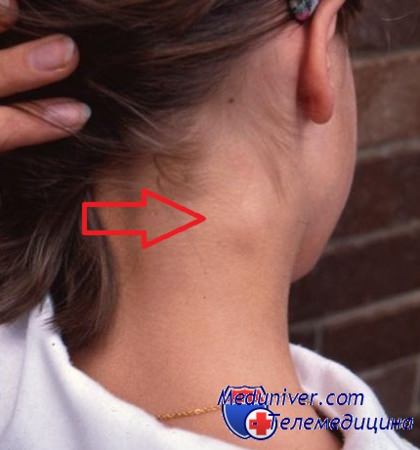
При инфекционных заболеваниях дыхательных путей степень увеличения узлов зависит от того, насколько выражен и длителен воспалительный процесс. При этом практически всегда увеличиваются миндалины, несильно увеличиваются шейные, затылочные лимфоузлы, они болезненны при ощупывании, немного уплотнены, и кожа над ними не изменена. При трахеитах, бронхитах, пневмониях могут быть увеличены внутригрудные лимфоузлы, прощупать их невозможно. Многое здесь зависит от самого возбудителя инфекции, в некоторых случаях увеличение лимфатических узлов может быть и системным.
Туберкулез чаще всего характеризуется системным увеличением лимфоузлов. Таким образом, увеличиваются узлы, располагающиеся в грудной полости, в основном, в месте перехода бронха в легкое. Иногда происходит увеличение лимфатических узлов, прилежащих к трахее или бронхам. Увидеть их можно на рентгеновском снимке или компьютерной томограмме. Одновременно в размерах постепенно увеличиваются шейные лимфоузлы, чаще с одной стороны или последовательно, напоминая нитку бус. Они становятся все более плотными, и менее подвижными, болезненными по мере того, как растягивается капсула в процессе увеличения. Со временем кожа нам ними может изменяться: краснеть, изъязвляться. Узел размягчается, палец при легком надавливании на него как бы проваливается. Затем образуется небольшое отверстие - свищ, по которому оттекает гной. Инфекция в лимфатические узлы попадает уже вторично, из очага в легких.
Лимфоузлы при бруцеллезе, как и при инфекционном мононуклеозе, долгое время остаются увеличенными. Родителей при этом должен насторожить тот факт, что накануне ребенок употреблял недостаточно термически обработанное мясо скота или сырое молоко, именно так и передается возбудитель этой инфекции. Лимфоузлы при бруцеллезе увеличиваются системно, при этом можно сказать, что размер узлов зависит от количества бактерий, находящихся и размножающихся в них.
Заражение туляремией возможно несколькими путями. Например, при употреблении мяса больного животного. При укусе насекомых или контакте с животными (зайцами, мышами и т.д.) в месте внедрения возбудителя образуется язвочка, и увеличиваются близлежащие лимфатические узлы, возможно и системное их увеличение. Все это часто сочетается с лихорадкой, воспалением слизистой оболочки горла и конъюнктивы глаз.
Родителям важно понимать, что лимфатическая система распространена по всему организму, и в лимфу сбрасываются яды, токсины и возбудители инфекции из всех органов и тканей. За каждый участок организма отвечают свои группы лимфатических узлов. К примеру, заболевания зубов могут вызвать увеличение подбородочных, подчелюстных узлов. Заболевания дыхательных путей приводят к увеличению шейных, затылочных, околоушных лимфоузлов. Если инфекция локализовалась в руке или ноге, то увеличиваются чаще локтевые или подколенные узлы соответственно. Поэтому возбудителя чаще всего приходится искать рядом с воспалившимся узлом. Вторым важным моментом является то, что лимфатические узлы, увеличенные из-за инфекции, чаще всего мягкие на ощупь и подвижные. А вот как будто бы каменный узел, плотно спаянный с окружающими тканями может быть тревожным признаком развития опухоли. Узел, который остается увеличенным более двух недель, однозначно требует похода к врачу и сдачи дополнительных анализов.
Читайте также:

