Литический цикл развития вирусов
Обновлено: 24.04.2024
Литический цикл – модель развития бактериофага, включающая три этапа: заражение бактериальной клетки, воспроизведение фага, лизис клетки-хозяина. Бактериофаги развиваются по двум вариантам: литический цикл и лизогенный цикл. Характерно что, умеренные фаги и вирулентные фаги на начальных этапах взаимодействия с бактериальной клеткой проходят одни и те же стадии. Умеренные фаги могут формировать профаги и кроме литического цикла, проходить через лизогенный цикл развития. Вирулентные бактериофаги способны развиваться только по литической модели, включающей в себя пять стадий.
Содержание:
Адсорбция бактериофага
Первая стадия развития по литическому пути – адсорбция фага на фагоспецифических рецепторах бактериальной клетки. Этот процесс происходит посредством специфических рецепторов, располагающихся на кончике нити, хвостика или шипа фага.
На клеточной стенке бактерии присутствуют фагоспецифические рецепторы, которые фаг способен распознавать. Для одних бактериофагов такие рецепторы находятся в липопротеидном слое клеточной стенки, для других – в липосахаридном слое, для третьих – на пилях или жгутиках.
Базальная пластинка с шипами (статья Бактериофаги) прикрепляется к стенке бактериальной клетки. В месте контакта с помощью фермента лизоцима, содержащегося в шипах и базальной пластинке, вызывается лизис клеточной стенки. Параллельно ионы кальция активируют АТФ-азу, содержащуюся в белках чехла, что приводит к его сокращению в два раза. В результате, внутренний стержень прокалывает клеточную стенку и цитоплазматическую мембрану на разрушенном участке.
Отмечается, что адсорбция фага является пусковым моментом его жизненного цикла и отличается специфичностью. Это дает возможность использовать бактериофаги для идентификации бактерий.
Инъекция нуклеиновой кислоты
Вторая стадия развития по литическому пути – инъекция нуклеиновой кислоты бактериофага в клетку-хозяина. Около 10% фаговой нуклеиновой кислоты активно впрыскивается при сокращении чехла хвоста. Остальная часть генетического материала втягивается в цитоплазму бактериальной клетки благодаря транскрипции и работе трансляционного аппарата. Белки капсида, чехла и стержня остаются снаружи клеточной стенки и внутрь клетки не попадают.
Репликация нуклеиновых кислот
Третья стадия развития бактериофага по литическому пути – совместная репликация нуклеиновой кислоты бактериофага и бактериальной клетки.
Нуклеиновая кислота бактериофага направляет синтез ферментов, используя белоксинтезирующий аппарат бактерии. Затем каким-либо способом инактивируются
ДНК и РНК хозяина, и впоследствии ферменты фага окончательно расщепляют ее. После этого РНК фага полностью подчиняет клеточный аппарат синтеза белка.
Репликация геномной ДНК или РНК бактериофага не отличается от общего механизма репликации. Степень зависимости нуклеиновой кислоты фага от хромосомы клетки определено набором генов у фага. Крупные фаги производят репликацию не зависимо от бактериальных генов, средние – частично нуждаются в их помощи. Мелкие – почти полностью зависимы от хромосомных генов клетки-хозяина.
После начала репликации синтезируются поздние вирусные информационные РНК, что приводит к образованию второго набора вирус-специфических белков, в том числе и субъединиц вирусного капсида.
Морфогенез фагов
Четвертая стадия развития бактериофага по литическому пути – морфогинез фагов. Этот процесс представляет собой сборку вновь синтезированных вирионов (заключение нуклеиновой кислоты в белковую оболочку).
Морфогенез мелких фагов протекает по типу самосборки. У крупных – морфогинез требует активности десятков генов и происходит при участии нескольких самостоятельных линий. Так для фага Т4 этот процесс требует активности более 40 генов и протекает при участии трех линий. На одной, при участии 20 генов, идет сборка хвоста. На второй, при участии 16 генов – головка фага. На третьей, при участии 5 генов – сборка ворсин. Соединение хвоста и головки участия генов не требует, но не происходит до тех пор пока головка и отросток не будут смонтированы полностью. Ворсины присоединяются к хвосту только после его полного соединения с головкой.
Последовательность и согласованность всех процессов внутриклеточного размножения обеспечивается благодаря строгому генетическому контролю со стороны нуклеиновой кислоты фага.
Лизис клетки
Пятая и заключительная стадия развития бактериофага по литическому пути – лизис клетки. Клетка лопается под воздействием лизоцима и высвобождает от 200 до 1000 новых фаговых частиц, способных инфицировать другие бактерии.
Выход вновь синтезированных фагов из клетки может происходить несколькими способами:
- путем почкования (характерно для фага М13 – единственного, не вызывающего гибель клетки при выходе из нее);
- путем лизиса клетки изнутри – осуществляется ферментом лизоцим и вызывает гибель клетки.
Лизоцим синтезируется, как поздний вирус-специфический белок и воздействует на пептидогликановый слой стенки клетки бактерии. Это приводит к разрыву стенки и выходу синтезированных фагов.
Лизис бактерии может происходить и извне, как следствие адсорбции большого количества фагов на одной и той же клетке. При этом не наблюдается размножение фагов. Это объясняется тем, что обычно после внедрения одного фагового генома в клетку, у нее возникает состояние иммунитета к суперинфекции данным фагом и проникновение других фаговых геномов становится невозможным.
(c) Справочник AgroXXI

Литический цикл – модель развития бактериофага, включающая три этапа: заражение бактериальной клетки, воспроизведение фага, лизис клетки-хозяина [3] .
Бактериофаги развиваются по двум вариантам: литический цикл и лизогенный цикл. Характерно что, умеренные фаги и вирулентные фаги на начальных этапах взаимодействия с бактериальной клеткой проходят одни и те же стадии. Умеренные фаги могут формировать профаги и кроме литического цикла, проходить через лизогенный цикл развития. Вирулентные бактериофаги способны развиваться только по литической модели, включающей в себя пять стадий [4] .
Содержание:
Адсорбция бактериофага
Первая стадия развития по литическому пути – адсорбция фага на фагоспецифических рецепторах бактериальной клетки. Этот процесс происходит посредством специфических рецепторов, располагающихся на кончике нити, хвостика или шипа фага [1] .
На клеточной стенке бактерии присутствуют фагоспецифические рецепторы, которые фаг способен распознавать. Для одних бактериофагов такие рецепторы находятся в липопротеидном слое клеточной стенки, для других – в липосахаридном слое, для третьих – на пилях или жгутиках [1] .
Базальная пластинка с шипами (статья "Бактериофаг") прикрепляется к стенке бактериальной клетки. В месте контакта с помощью фермента лизоцима, содержащегося в шипах и базальной пластинке, вызывается лизис клеточной стенки. Параллельно ионы кальция активируют АТФ-азу, содержащуюся в белках чехла, что приводит к его сокращению в два раза. В результате, внутренний стержень прокалывает клеточную стенку и цитоплазматическую мембрану на разрушенном участке [1] .
Отмечается, что адсорбция фага является пусковым моментом его жизненного цикла и отличается специфичностью. Это дает возможность использовать бактериофаги для идентификации бактерий [3] .

Адсорбция бактериофага на клеточной стенке бактерии

Инъекция нуклеиновой кислоты
Вторая стадия развития по литическому пути – инъекция нуклеиновой кислоты бактериофага в клетку-хозяина. Около 10% фаговой нуклеиновой кислоты активно впрыскивается при сокращении чехла хвоста. Остальная часть генетического материала втягивается в цитоплазму бактериальной клетки благодаря транскрипции и работе трансляционного аппарата. Белки капсида, чехла и стержня остаются снаружи клеточной стенки и внутрь клетки не попадают [1] .

Введение нуклеиновой кислоты (НК) фага в бактериальную клетку

1. Схема введения НК фага в бактериальную клетку.
2. Пустые фаговые капсиды и отростки на поверхности инфицированной клетки (микрография) [2]
Репликация нуклеиновых кислот
Третья стадия развития бактериофага по литическому пути – совместная репликация нуклеиновой кислоты бактериофага и бактериальной клетки [1] .
Нуклеиновая кислота бактериофага направляет синтез ферментов, используя белоксинтезирующий аппарат бактерии. Затем каким-либо способом инактивируются ДНК и РНК хозяина, и впоследствии ферменты фага окончательно расщепляют ее. После этого РНК фага полностью подчиняет клеточный аппарат синтеза белка [1] .
Репликация геномной ДНК или РНК бактериофага не отличается от общего механизма репликации. Степень зависимости нуклеиновой кислоты фага от хромосомы клетки определено набором генов у фага. Крупные фаги производят репликацию не зависимо от бактериальных генов, средние – частично нуждаются в их помощи. Мелкие – почти полностью зависимы от хромосомных генов клетки-хозяина. После начала репликации синтезируются поздние вирусные информационные РНК, что приводит к образованию второго набора вирус-специфических белков, в том числе и субъединиц вирусного капсида [1] .

Схема сборки фаговых частиц

Морфогенез фагов
Четвертая стадия развития бактериофага по литическому пути – морфогинез фагов. Этот процесс представляет собой сборку вновь синтезированных вирионов (заключение нуклеиновой кислоты в белковую оболочку) [1] .
Морфогенез мелких фагов протекает по типу самосборки. У крупных – морфогинез требует активности десятков генов и происходит при участии нескольких самостоятельных линий. Так для фага Т4 этот процесс требует активности более 40 генов и протекает при участии трех линий. На одной, при участии 20 генов, идет сборка хвоста. На второй, при участии 16 генов – головка фага. На третьей, при участии 5 генов – сборка ворсин. Соединение хвоста и головки участия генов не требует, но не происходит до тех пор пока головка и отросток не будут смонтированы полностью. Ворсины присоединяются к хвосту только после его полного соединения с головкой [1] .
Последовательность и согласованность всех процессов внутриклеточного размножения обеспечивается благодаря строгому генетическому контролю со стороны нуклеиновой кислоты фага [3] .

Выход вирионов фага из бактериальной клетки

Лизис клетки
Пятая и заключительная стадия развития бактериофага по литическому пути – лизис клетки. Клетка лопается под воздействием лизоцима и высвобождает от 200 до 1000 новых фаговых частиц, способных инфицировать другие бактерии [1] .
Выход вновь синтезированных фагов из клетки может происходить несколькими способами:
- путем почкования (характерно для фага М13 – единственного, не вызывающего гибель клетки при выходе из нее);
- путем лизиса клетки изнутри – осуществляется ферментом лизоцим и вызывает гибель клетки [1] .
Лизоцим синтезируется, как поздний вирус-специфический белок и воздействует на пептидогликановый слой стенки клетки бактерии. Это приводит к разрыву стенки и выходу синтезированных фагов [1] .
Лизис бактерии может происходить и извне, как следствие адсорбции большого количества фагов на одной и той же клетке. При этом не наблюдается размножение фагов. Это объясняется тем, что обычно после внедрения одного фагового генома в клетку, у нее возникает состояние иммунитета к суперинфекции данным фагом и проникновение других фаговых геномов становится невозможным [3] .
Оставьте свой отзыв:
Отзывы:
Составитель: Григоровская П.И.
Последнее обновление: 11.05.21 16:54
Статья составлена с использованием следующих материалов:
Иконникова Н.В. Бактериофаги – вирусы бактерий: учеб. пособие, Минск: ИВЦ Минфина, 2017. – 41 c
Литусов Н.В. Бактериофаги. Иллюстрированное учебное пособие. – Екатеринбург: Изд-во УГМА, 2012. - 38 с.
Лысак В.В. Микробиология : учеб. пособие / В. В. Лысак. – Минск: БГУ, 2007 – 430 с

Лизогенный цикл – модель развития умеренных бактериофагов. Отличается от литического цикла тем, что после проникновения в цитоплазму геном фага не уничтожает геном бактерии, а встраивается в него, образуя профаг. Клетки бактерий, содержащие профаг, не лизируются, а продолжают делиться, передавая профаг по наследству [3] .
Бактериофаги способны развиваться по двум моделям: лизогенный цикл и литический цикл. Начальные стадии обоих путей взаимодействия фагов с бактериальной клеткой сходны [2] [1] .
Начальные стадии взаимодействия с клеткой
Как указывалось ранее, начальные стадии взаимодействия умеренных фагов с клетками бактерий такие же, как и у вирулентных. В начале умеренный бактериофаг проходит через первые две стадии литического цикла:
- адсорбция фага на фагоспецифических рецепторах бактериальной клетки;
- инъекция нуклеиновой кислоты бактериофага в клетку-хозяина [1] .
В дальнейшем умеренный профаг может, как включится в литический цикл, так и образовать профаг, то есть развиваться по лизогенному циклу [3] .

Взаимодействие умеренных и вирулентных бактериофагов с клеткой

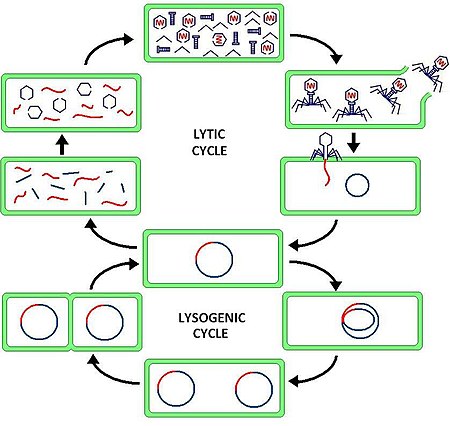
1. Адсорбция фага на клетке; 2. Интеграция фаговой ДНК в хромосому бактерии; 3. Репликация фаговой ДНК вместе с бактериальной; 4. Деление клетки; 5. Репликация фаговой ДНК и синтез фаговых белков; 6. Образование капсидов; 7. Упаковка ДНК в капсиды; 8. Созревание фаговых частиц; 9. Лизис клетки и выход фаговых частиц [3] .
Развитие умеренных фагов по лизогенному пути
Данная кольцевая молекула обычно не приступает к транскрипции, а встраивается в бактериальную хромосому. Встраивание ДНК фага λ в бактериальную хромосому осуществляется в одном и том же месте. Этот процесс называется сайт-специфической рекомбинацией. За интеграцию ДНК фага отвечает фермент лямбда-интеграза. Этот фермент распознает две разные последовательности: одну в хромосомной ДНК, другую в ДНК фага, с последующим разрывом молекул ДНК и их дальшейшим перекрестным воссоединением [3] .
После внедрения ДНК бактериофага λ в бактериальную клетку выбор между двумя путями развития зависит от скорости накопления регуляторных белков. Если преобладает белок Cro, то начинают развиваться события литического цикла. При проявлении функции репрессорного белка cI, литический цикл не осуществляется, поскольку cI связывается с ДНК фага λ в особых участках и препятствует транскрипции фаговых генов [3] .
При выборе лизогенного пути процесс завершается тем, что ДНК фага λ реплицируется с клеточной ДНК и функционирует с ней как единая структура. Все дочерние клетки такой бактерии (лизогенная бактерия) при делении получают копию фаговой ДНК (профаг) в составе хромосомы [3] .
Устойчивость лизогенного цикла
Лизогенный цикл поддерживается благодаря постоянному образованию белка репрессора сІ. Однако это состояние довольно неустойчиво. В любой момент могут проявиться антирепрессорные функции белка Cro и произойти переключение на окончательные стадии литического пути: Сначала совместную репликацию нуклеиновой кислоты бактериофага и бактериальной клетки. Затем морфогинез бактериофага. И окончание цикла развития – лизис клетки [2] [3] .
Экспериментально установлено, что в популяции лизогенных бактерий в одной из 102–105 клеток наблюдается спонтанная индукция профага и запускается литический путь, что приводит к лизису бактериальных клеток [3] .
Эффективность лизогенного цикла зависит как от состояния бактерии-хозяина, так и от воздействия физических и химических факторов. Индукторами перехода от лизогенного цикла к литическому и обратно могут являться: ультрафиолетовое излучение, митомицин C, алкирующие агенты, иногда изменение температуры [3] .
Литический цикл ( / л ɪ т ɪ к / LIT -ik ) является одним из двух циклов вирусной репродукции ( со ссылки на бактериальные вирусы или бактериофаг ), другая являющееся лизогенной цикл . Литический цикл приводит к разрушению инфицированной клетки и ее мембраны. Бактериофаги, которые используют только литический цикл, называются вирулентными фагами (в отличие от фагов умеренного климата ).
В литическом цикле вирусная ДНК существует как отдельная свободно плавающая молекула внутри бактериальной клетки и реплицируется отдельно от бактериальной ДНК-хозяина, тогда как в лизогенном цикле вирусная ДНК находится внутри ДНК-хозяина. Это ключевое различие между литическим и лизогенным (бактерио) фаговыми циклами. Однако в обоих случаях вирус / фаг реплицируется с использованием механизма ДНК хозяина.
Содержание
- Прикрепление - фаг прикрепляется к поверхности клетки-хозяина, чтобы ввести свою ДНК в клетку.
- Проникновение - фаг вводит свою ДНК в клетку-хозяин, проникая через клеточную мембрану.
- Транскрипция - ДНК клетки-хозяина разрушается, и метаболизм клетки направлен на инициирование биосинтеза фага.
- Биосинтез - ДНК фага реплицируется внутри клетки, синтезируя новую ДНК фага и белки.
- Созревание - реплицированный материал собирается в полностью сформированные вирусные фаги (каждый из которых состоит из головы, хвоста и хвостовых волокон).
- Лизис - новообразованные фаги высвобождаются из инфицированной клетки (которая сама уничтожается в процессе) для поиска новых клеток-хозяев для заражения.
Чтобы заразить клетку-хозяина, вирус должен сначала ввести в клетку свою собственную нуклеиновую кислоту через плазматическую мембрану и (если присутствует) клеточную стенку. Вирус делает это либо путем присоединения к рецептору на поверхности клетки, либо с помощью простой механической силы. Связывание происходит из-за электростатических взаимодействий и зависит от pH и присутствия ионов. Затем вирус выпускает свой генетический материал (одно- или двухцепочечную РНК или ДНК ) в клетку. У некоторых вирусов этот генетический материал является кольцевым и имитирует бактериальную плазмиду . На этом этапе клетка заражается и также может стать мишенью для иммунной системы. В основном этому способствуют рецепторы на поверхности клетки.
На этапах транскрипции и биосинтеза вирус захватывает механизмы репликации и трансляции клетки, используя их для создания большего количества вирусов. Нуклеиновая кислота вируса использует метаболический аппарат клетки-хозяина для производства большого количества вирусных компонентов.
В случае ДНК-вирусов ДНК транскрибируется в молекулы информационной РНК (мРНК), которые затем используются для управления рибосомами клетки. Один из первых транслируемых полипептидов разрушает ДНК хозяина. В ретровирусах (которые вводят цепь РНК) уникальный фермент, называемый обратной транскриптазой, транскрибирует вирусную РНК в ДНК, которая затем снова транскрибируется в РНК. Как только вирусная ДНК берет на себя управление, она побуждает механизм клетки-хозяина синтезировать вирусную ДНК, белок и начинает размножаться.
Биосинтез (например, Т4 ) регулируется в трех фазах продукции мРНК, за которыми следует фаза продукции белка. [1]
Ранняя фаза Ферменты модифицируют процесс транскрипции хозяина с помощью РНК-полимеразы . Среди других модификаций вирус Т4 изменяет сигма-фактор хозяина, продуцируя антисигма-фактор, так что промоторы хозяина больше не распознаются, но теперь распознают средние белки Т4. Для синтеза белка субпоследовательность Шайна-Далгарно GAGG доминирует над ранней трансляцией генов. [2] Средняя фаза Нуклеиновая кислота вируса (ДНК или РНК в зависимости от типа вируса). Поздняя фаза Структурные белки, в том числе для головы и хвоста.
Примерно через 25 минут после первоначального заражения образуется около 200 новых вирионов (вирусных телец). После созревания и накопления достаточного количества вирионов используются специализированные вирусные белки для растворения клеточной стенки. Клетка разрывается (то есть подвергается лизису ) из-за высокого внутреннего осмотического давления (давления воды), которое больше не может сдерживаться клеточной стенкой. Это высвобождает вирионы потомства в окружающую среду, где они могут инфицировать другие клетки, и начинается еще один литический цикл. Фаг, вызывающий лизис хозяина, называется литическим или вирулентным фагом. [3]
В геноме фага есть три класса генов, которые регулируют возникновение литического или лизогенного цикла. Первый класс - это гены непосредственного раннего развития, второй - гены отсроченного раннего периода, а третий - гены позднего периода. Следующее относится к хорошо изученному умеренному фагу лямбда E. coli.
- Непосредственные ранние гены: Эти гены экспрессируются промоторы , признаваемого хозяин РНК - полимераза, и включают в себя CRO , CII и N . CII представляет собой фактор транскрипции, который стимулирует экспрессию основного лизогенного репрессорного гена, cI , тогда как Cro является репрессором для экспрессии cI . На решение о лизисе-лизогении в основном влияет конкуренция между Cro и CII, что приводит к определению того, выработан ли достаточный репрессор CI. Если это так, CI репрессирует ранние промоторы, и инфекция шунтируется по лизогенному пути. N - это фактор, препятствующий терминации, который необходим для транскрипции отложенных ранних генов.
- Задержанные ранние гены: к ним относятся гены репликации O и P, а также Q , который кодирует антитерминатор, ответственный за транскрипцию всех поздних генов.
- Поздние гены:
Q-опосредованное включение поздней транскрипции начинается примерно через 6-8 минут после инфицирования, если выбран литический путь. Более 25 генов экспрессируются с одного позднего промотора, что приводит к четырем параллельным путям биосинтеза. Три пути служат для производства трех компонентов вириона: наполненной ДНК головы, хвоста и боковых волокон хвоста. Вирионы самостоятельно собираются из этих компонентов, причем первый вирион появляется примерно через 20 минут после заражения. Четвертый путь - лизис. В лямбда-5 в лизисе участвуют белки: холин и антихолин из гена S , эндолизин из гена R и белки спанина из генов Rz и Rz1. . В лямбда дикого типа лизис происходит примерно через 50 мин, высвобождая примерно 100 завершенных вирионов. Время лизиса определяется белками холина и антихолина, причем последний ингибирует первый. В общем, белок холин накапливается в цитоплазматической мембране до тех пор, пока внезапно не образуются отверстия микронного размера, которые запускают лизис. Эндолизин R попадает в периплазму, где атакует пептидогликан. Белки спанина Rz и Rz1 накапливаются в цитоплазматической и внешней мембранах, соответственно, и образуют комплекс, охватывающий периплазму через сеть пептидогликана. Когда эндолизин разрушает пептидогликан, комплексы спанина высвобождаются и вызывают разрушение внешней мембраны.Разрушение пептидогликана эндолизином и разрушение внешней мембраны комплексом спанина оба необходимы для лизиса при лямбда-инфекциях.
Ингибирование лизиса : Т4-подобные фаги имеют два гена, rI и rIII , которые ингибируют холин Т4, если инфицированная клетка подвергается суперинфекции другим Т4 (или близкородственным) вирионом. Повторная суперинфекция может привести к тому, что инфекция Т4 продолжится без лизиса в течение нескольких часов, что приведет к накоплению вирионов до уровней, в 10 раз превышающих нормальные. [4]
Литический цикл ( / л ɪ т ɪ к / LIT -ik ) является одним из двух циклов вирусной репродукции ( со ссылки на бактериальные вирусы или бактериофаг ), другая являющееся лизогенной цикл . Литический цикл приводит к разрушению инфицированной клетки и ее мембраны. Бактериофаги, которые используют только литический цикл, называются вирулентными фагами (в отличие от фагов умеренного климата ).
В литическом цикле вирусная ДНК существует как отдельная свободно плавающая молекула внутри бактериальной клетки и реплицируется отдельно от бактериальной ДНК-хозяина, тогда как в лизогенном цикле вирусная ДНК находится внутри ДНК-хозяина. Это ключевое различие между литическим и лизогенным (бактерио) фаговыми циклами. Однако в обоих случаях вирус / фаг реплицируется с использованием механизма ДНК хозяина.
- Прикрепление - фаг прикрепляется к поверхности клетки-хозяина, чтобы ввести свою ДНК в клетку.
- Проникновение - фаг вводит свою ДНК в клетку-хозяин, проникая через клеточную мембрану.
- Транскрипция - ДНК клетки-хозяина разрушается, и метаболизм клетки направлен на инициирование биосинтеза фага.
- Биосинтез - ДНК фага реплицируется внутри клетки, синтезируя новую ДНК фага и белки.
- Созревание - реплицированный материал собирается в полностью сформированные вирусные фаги (каждый из которых состоит из головы, хвоста и хвостовых волокон).
- Лизис - новообразованные фаги высвобождаются из инфицированной клетки (которая сама уничтожается в процессе), чтобы найти новые клетки-хозяева для заражения.
Привязанность и проникновение
Чтобы заразить клетку-хозяин, вирус должен сначала ввести в клетку свою собственную нуклеиновую кислоту через плазматическую мембрану и (если присутствует) клеточную стенку. Вирус делает это либо путем прикрепления к рецептору на поверхности клетки, либо с помощью простой механической силы. Связывание происходит из-за электростатических взаимодействий и зависит от pH и присутствия ионов. Затем вирус высвобождает свой генетический материал (одно- или двухцепочечную РНК или ДНК ) в клетку. У некоторых вирусов этот генетический материал является кольцевым и имитирует бактериальную плазмиду . На этом этапе клетка заражается и также может стать мишенью для иммунной системы. В основном этому способствуют рецепторы на поверхности клетки.
Транскрипция и биосинтез
На этапах транскрипции и биосинтеза вирус захватывает механизмы репликации и трансляции клетки, используя их для создания большего количества вирусов. Нуклеиновая кислота вируса использует метаболический аппарат клетки-хозяина для производства большого количества вирусных компонентов.
В случае ДНК-вирусов ДНК транскрибируется в молекулы информационной РНК (мРНК), которые затем используются для управления рибосомами клетки. Один из первых транслируемых полипептидов разрушает ДНК хозяина. В ретровирусах (которые вводят цепь РНК) уникальный фермент, называемый обратной транскриптазой, транскрибирует вирусную РНК в ДНК, которая затем снова транскрибируется в РНК. Как только вирусная ДНК берет на себя управление, она побуждает механизм клетки-хозяина синтезировать вирусную ДНК, белок и начинает размножаться.
Биосинтез (например, Т4 ) регулируется в трех фазах продукции мРНК, за которыми следует фаза продукции белка. [1]
Ранняя фаза Ферменты изменяют процесс транскрипции хозяина с помощью РНК-полимеразы . Среди других модификаций вирус Т4 изменяет сигма-фактор хозяина, производя антисигма-фактор, так что промоторы хозяина больше не распознаются, но теперь распознают средние белки Т4. Для синтеза белка субпоследовательность Шайна-Далгарно GAGG доминирует над ранней трансляцией генов. [2] Средняя фаза Нуклеиновая кислота вируса (ДНК или РНК в зависимости от типа вируса). Поздняя фаза Структурные белки, в том числе для головы и хвоста.
Созревание и лизис
Примерно через 25 минут после первоначального заражения образуется около 200 новых вирионов (вирусных телец). После созревания и накопления достаточного количества вирионов используются специализированные вирусные белки для растворения клеточной стенки. Клетка разрывается (т.е. подвергается лизису ) из-за высокого внутреннего осмотического давления (давления воды), которое больше не может сдерживаться клеточной стенкой. Это высвобождает вирионы потомства в окружающую среду, где они могут инфицировать другие клетки, и начинается еще один литический цикл. Фаг, вызывающий лизис хозяина, называется литическим или вирулентным фагом. [3]
В геноме фага есть три класса генов, которые регулируют возникновение литического или лизогенного цикла. Первый класс - это гены непосредственного раннего развития, второй - гены отсроченного раннего периода, а третий - гены позднего периода. Следующее относится к хорошо изученному умеренному фагу лямбда E. coli.
- Непосредственные ранние гены: Эти гены экспрессируются промоторы , признаваемого хозяин РНК - полимераза, и включают в себя CRO , CII и N . CII представляет собой фактор транскрипции, который стимулирует экспрессию основного лизогенного репрессорного гена, cI , тогда как Cro является репрессором для экспрессии cI . Решение о лизисе-лизогении в основном зависит от конкуренции между Cro и CII, что приводит к определению того, выработан ли достаточный репрессор CI. Если это так, CI репрессирует ранние промоторы, и инфекция шунтируется по лизогенному пути. N - фактор, препятствующий терминации, который необходим для транскрипции отложенных ранних генов.
- Отсроченные ранние гены: они включают гены репликации O и P, а также Q , который кодирует антитерминатор, ответственный за транскрипцию всех поздних генов.
- Поздние гены:
Q-опосредованное включение поздней транскрипции начинается примерно через 6-8 мин после инфицирования, если выбран литический путь. Более 25 генов экспрессируются с одного позднего промотора, что приводит к четырем параллельным путям биосинтеза. Три пути служат для производства трех компонентов вириона: наполненной ДНК головы, хвоста и боковых волокон хвоста. Вирионы самостоятельно собираются из этих компонентов, причем первый вирион появляется примерно через 20 минут после заражения. Четвертый путь - лизис. В лямбда-5 в лизисе участвуют белки: холин и антихолин из гена S , эндолизин из гена R и белки спанина из генов Rz и Rz1 . В лямбда дикого типа лизис происходит примерно через 50 минут, высвобождая примерно 100 завершенных вирионов. Время лизиса определяется белками холина и антихолина, причем последний ингибирует первый. В общем, белок холин накапливается в цитоплазматической мембране до тех пор, пока внезапно не образуются отверстия микронного размера, которые запускают лизис. Эндолизин R попадает в периплазму, где атакует пептидогликан. Белки спанина Rz и Rz1 накапливаются в цитоплазматической и внешней мембранах, соответственно, и образуют комплекс, охватывающий периплазму через сеть пептидогликана. Когда эндолизин разрушает пептидогликан, комплексы спанина высвобождаются и вызывают разрушение внешней мембраны. Разрушение пептидогликана эндолизином и разрушение внешней мембраны комплексом спанина оба необходимы для лизиса при лямбда-инфекциях.
Ингибирование лизиса : Т4-подобные фаги имеют два гена, rI и rIII , которые ингибируют холин Т4, если инфицированная клетка подвергается суперинфекции другим Т4 (или близкородственным) вирионом. Повторная суперинфекция может привести к тому, что инфекция Т4 продолжится без лизиса в течение нескольких часов, что приведет к накоплению вирионов до уровней, в 10 раз превышающих нормальные. [4]
Читайте также: