Менактра вакцина менингококковая полисахаридная серогрупп a c y и w-135
Обновлено: 22.04.2024
Раствор для внутримышечного введения
Вакцина Менактра® представляет собой раствор очищенных капсульных полисахаридов Neisseria meningitidis групп A, C, Y и W-135, индивидуально конъюгированных с белком-носителем (очищенным анатоксином Corynebacterium diphtheriae).
Состав
Одна доза (0,5 мл) содержит:
Действующие вещества:
Моновалентные менингококковые конъюгаты (полисахарид + белок-носитель):
Полисахарид серогруппы A - 4 мкг
Полисахарид серогруппы С - 4 мкг
Полисахарид серогруппы Y - 4 мкг
Полисахарид серогруппы W-135 - 4 мкг
Дифтерийный анатоксин ~ 48 мкг
Вспомогательные вещества:
Натрия хлорид 4,35 мг, натрия гидрофосфат 0,348 мг, натрия дигидрофосфата моногидрат 0,352 мг, вода для инъекций - до 0,5 мл.
Описание
Бесцветный прозрачный или слегка мутноватый раствор.
Фармакотерапевтическая группа
Код ATX
Фармакологические свойства
Возбудителем менингококковой инфекции, включая менингит и септицемию, является бактерия N. meningitidis; выделяют ряд серогрупп возбудителя. Введение вакцины Менактра® индуцирует выработку специфических антител, обладающих бактерицидной активностью в отношении капсулярных полисахаридов серогрупп возбудителя менингококковой инфекции, входящих в состав вакцины (А, С, Y и W-135).
Иммунологическая эффективность
Клинические исследования по изучению эффективности не проводились, поскольку выработка сывороточных бактерицидных антител (СБА) считается показателем эффективности менингококковых вакцин.
Иммунологические свойства вакцины Менактра ® изучали в 3 клинических исследованиях у детей в возрасте 9-18 мес, в 4 клинических исследованиях у детей в возрасте 2-10 лет и в 6 клинических исследованиях у лиц в возрасте 11-55 лет. Иммуногенность оценивали по уровню функциональных антител, определяемого с помощью анализа СБА.
Первичный иммунологический профиль вакцины изучали в рамках клинических исследований у участников в возрасте 2-10 лет. Иммунный ответ оценивали спустя 28 дней после введения вакцины Менактра ® (в сравнении с исходным уровнем антител до вакцинации). У участников исследования наблюдали значительное повышение средних геометрических титров СБА. У 86-100 % участников при исходно неопределяемых значениях титра СБА (<1:8) была отмечена сероконверсия по антигенам всех серогрупп возбудителя, определяемая как 4-х кратное (или более) увеличение титров антител спустя 28 дней после вакцинации в сравнении с титром антител до вакцинации.
Способность вакцины Менактра® вызывать развитие иммунологической памяти после первичной вакцинации подтверждена данными клинических исследований у детей и у взрослых.
Результаты 3 клинических исследований, проведенных у детей в возрасте 9-18 мес с однократным или двукратным введением вакцины Менактра ® отдельно или одновременно с другими педиатрическими вакцинами (пневмококковой конъюгированной вакциной (ПКВ) или вакциной для профилактики кори, паротита, краснухи и ветряной оспы (КПКВ)), подтвердили, что у большинства участников в группах с двукратным введением вакцины Менактра®, при ее применении отдельно или одновременно с другими педиатрическими вакцинами, наблюдалось увеличение титра СБА ≥1:8 ко всем серогруппам вакцины. У ≥91 % и ≥86 % участников в группе с отдельным двукратным введением вакцины Менактра ® наблюдалось увеличение титра СБА ≥1:8 к серогруппам А, С, Y и к серогруппе W-135, соответственно. После введения второй дозы вакцины Менактра® одновременно с ПКВ или с КПКВ (или КПКВ + вакцина для профилактики инфекций, вызываемых Haemophilus influenzae тип b), у большинства участников исследования наблюдалось нарастание титра СБА ≥1:8 (у >90 % участников исследования к серогруппам А, С и Y, у >81 % участников к серогруппе W-135). Значения средних геометрических титров СБА после вакцинации ко всем четырем серогруппам менингококков, входящим в состав вакцины, были высокими.
Кинетика иммунного ответа: отсутствуют данные о кинетике первоначального ответа на введение вакцины Менактра ® , однако, как и в случае других полисахаридных и конъюгированных вакцин, иммунная защита обычно формируется через 7-10 дней после вакцинации.
Продолжительность защиты: способность вакцины Менактра® индуцировать формирование иммунной памяти после первичной вакцинации была доказана в ходе клинических исследований. В одном из исследований было продемонстрировано, что персистенция бактерицидных антител в крови через 3 года после однократного введения вакцины Менактра® была выше по сравнению с группой привитых, получивших однократную иммунизацию неконъюгированной 4-х валентной полисахаридной менингококковой вакциной против серогрупп A, C, Y и W-135. В группе привитых вакциной Менактра® наблюдались более высокая концентрация СБА, а также более высокая доля лиц, имевших специфические высокоавидные антитела, что говорит о формировании иммунной памяти.
Показания к применению
Профилактика инвазивной менингококковой инфекции, вызываемой N. meningitidis серогрупп A, C, Y и W-135, у лиц в возрасте от 9 мес до 55 лет.
Противопоказания
- Известная гиперчувствительность с системными проявлениями к любому компоненту вакцины, включая дифтерийный анатоксин, или на предыдущее введение других вакцин, включающих те же компоненты.
- Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии).
Применение при беременности и в период грудного вскармливания
Исследования на животных не выявили отрицательного действия вакцины Менактра® на течение беременности и эмбриофетальное развитие, процесс родов и постнатальное развитие. В связи с тем, что исследований вакцинации беременных женщин не проводилось, а пострегистрационный опыт ее применения у беременных женщин ограничен, введение вакцины беременным женщинам рекомендуется только в случае крайней необходимости, как например, во время вспышки менингококковой инфекции, перед поездкой в эндемичный район, и только после оценки соотношения пользы и риска вакцинации.
В настоящее время неизвестно, способны ли действующие вещества, входящие в состав вакцины, проникать в грудное молоко. Однако ранее было показано, что антитела к полисахаридам обнаруживаются у молодых мышей, находившихся на грудном вскармливании.
В исследованиях у мышей не было продемонстрировано неблагоприятное влияние на постнатальное развитие потомства, получавшего с материнским молоком антитела, выработка которых была индуцирована введением вакцины Менактра ® . В то же время эффекты у детей первого года жизни, матери которых были иммунизированы вакциной Менактра® в период грудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины необходимо оценить риски и пользу данной иммунизации.
Способ применения и дозы
Вакцинация проводится одной дозой 0,5 мл.
Вакцину следует вводить внутримышечно, принимая во внимание возраст прививаемого: детям в возрасте от 9 до 12 мес - в передне-боковую область бедра; детям от 12 мес и старше и взрослым - в дельтовидную мышцу плеча.
Не вводить вакцину внутрисосудисто. Перед введением необходимо убедиться, что игла не попала в кровеносный сосуд.
У детей в возрасте от 9 до 23 мес курс вакцинации вакциной Менактра® состоит из 2 инъекций по одной дозе вакцины (0,5 мл) с интервалом не менее 3 мес.
У лиц в возрасте от 2 до 55 лет вакцинация проводится однократно дозой 0,5 мл.
При сохраняющемся риске менингококковой инфекции однократная ревакцинация может быть проведена в соответствии с национальными рекомендациями, если с момента введения предыдущей дозы прошло не менее 4 лет.
Побочное действие
Характер и частота выявленных в исследованиях побочных эффектов различались в зависимости от возраста прививаемых.
В ходе клинических исследований у детей в возрасте от 9 до 18 мес, в течение 7 дней после вакцинации, наиболее часто отмечались чувствительность в месте инъекции и болезненность. В ходе клинических исследований у детей в возрасте от 2 до 10 лет наиболее часто отмечались болезненность и покраснение в месте инъекции, раздражительность, диарея, сонливость, анорексия; у подростков в возрасте от 11 до 18 лет и у взрослых лиц от 18 до 55 лет наиболее часто отмечались болезненность в месте инъекции, головная боль и повышенная утомляемость.
Частота развития приведенных ниже побочных эффектов классифицирована согласно рекомендациям Всемирной организации здравоохранения (ВОЗ) и включает следующие категории:
Со стороны обмена веществ и питания
Очень часто: потеря аппетита
Со стороны нервной системы
Очень часто: сонливость
Со стороны желудочно-кишечного тракта
Очень часто или часто: рвота
Общие расстройства и нарушения в месте введения
Очень часто: болезненность, эритема в месте инъекции, отек в месте инъекции, раздражительность, аномальный плач, лихорадка
Со стороны обмена веществ и питания
Очень часто или часто: снижение аппетита
Со стороны нервной системы
Очень часто или часто: сонливость
Со стороны желудочно-кишечного тракта
Очень часто: диарея
Часто: рвота
Со стороны кожи и подкожных тканей
Часто: сыпь, крапивница
Со стороны скелетно-мышечной и соединительной ткани
Часто: артралгия
Общие расстройства и нарушения в месте введения
Очень часто: болезненность и уплотнение в месте инъекции
Очень часто или часто: раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка
Со стороны обмена веществ и питания
Очень часто или часто: снижение аппетита
Со стороны нервной системы
Очень часто: головная боль
Со стороны желудочно-кишечного тракта
Очень часто или часто: диарея
Часто: рвота
Со стороны кожи и подкожных тканей
Часто: сыпь
Со стороны скелетно-мышечной и соединительной ткани
Очень часто: артралгия
Общие расстройства и нарушения в месте введения
Очень часто: боль, уплотнение, покраснение и отек в месте инъекции, повышенная утомляемость, общее недомогание
Часто: озноб, лихорадка
Ревакцинация
У подростков и взрослых серьезные нежелательные явления встречались в 1,3 % случаев после ревакцинации вакциной Менактра®.
В пострегистрационный период дополнительно получена информация о следующих нежелательных явлениях после введения препарата (в настоящее время частота развития данных явлений и их причинно-следственная связь с применением вакцины Менактра® не может быть определена):
Со стороны крови и лимфатической системы
Лимфоаденопатия
Со стороны иммунной системы
Реакции гиперчувствительности, такие как анафилактический шок, анафилактоидные реакции, стридорозное дыхание, затруднение при дыхании, отек верхних дыхательных путей, крапивница, покраснение кожи, кожный зуд, снижение артериального давления.
Со стороны нервной системы
Синдром Гийена-Барре (СГБ), парестезии, потеря сознания (обусловленная нарушениями регуляции со стороны вегетативной нервной системы), головокружение, судороги, паралич лицевого нерва, острый рассеянный энцефаломиелит, поперечный миелит.
Со стороны скелетно-мышечной и соединительной ткани
Миалгия
Общие расстройства и нарушения в месте введения
Обширная реакция в месте введения, проявляющаяся выраженным отеком конечности, может сопровождаться покраснением, чувством жара в месте инъекции, повышенной чувствительностью, или болезненностью в месте инъекции.
Пострегистрационное исследование безопасности
Риск СГБ после введения вакцины Менактра® оценивался в рамках ретроспективного когортного исследования (США). По результатам медицинского обследования 1 431 906 пациентов, получивших вакцину Менактра®, сообщалось о 72 случаях СГБ. Во всех случаях вакцина Менактра® была введена пациентам не ранее 42 дней до начала развития симптомов. Еще 129 случаев СГБ не подтверждены или были исключены из анализа из-за отсутствия или недостаточности медицинской информации. На основании результатов анализа был оценен дополнительный риск СГБ, который варьировался от 0 до 5 дополнительных случаев СГБ на 1 000 000 привитых в течение 6 недель после вакцинации.
Передозировка
О случаях передозировки не сообщалось.
Взаимодействие с другими лекарственными средствами
В клинических исследованиях у детей в возрасте от 4 до 6 лет включительно вакцину Менактра ® применяли совместно с вакциной для профилактики дифтерии, столбняка, коклюша (бесклеточной). В клинических исследованиях у детей младше 2 лет вакцину Менактра ® применяли совместно с одной или несколькими из следующих вакцин во время введения второй дозы в возрасте 12 месяцев: пневмококковой 7-ми валентной конъюгированной вакциной (ПКВ7), вакциной для профилактики кори, паротита, краснухи (с компонентом против ветряной оспы или без него), вакциной для профилактики ветряной оспы, вакциной для профилактики вирусного гепатита А или вакциной для профилактики инфекции, вызываемой Haemophilus influenzae тип b.
При совместном применении вакцины Менактра ® и вакцины против дифтерии, столбняка и коклюша (бесклеточной) у детей в возрасте от 4 до 6 лет включительно предпочтительно вводить одновременно обе указанные вакцины, или следует вводить вакцину Менактра ® перед применением вакцины против дифтерии, столбняка и коклюша (бесклеточной). Снижение иммунного ответа на вакцину Менактра ® было продемонстрировано при ее введении через месяц после введения вакцины против дифтерии, столбняка и коклюша (бесклеточной). Отсутствуют данные по оценке иммунного ответа на введение вакцины Менактра® после введения вакцины против дифтерии, столбняка и коклюша (бесклеточной) у детей до 4 лет или на введение вакцины Менактра® лицам младше 11 лет после введения других вакцин, содержащих дифтерийный анатоксин.
Титры пневмококковых антител против некоторых серотипов, содержащихся в ПКВ7, были снижены после одновременного введения вакцины Менактра® и вакцины ПКВ7.
БЦЖ вакцина не должна применяться одновременно с вакциной Менактра®.
Вводить вакцины необходимо всегда в разные участки тела, используя отдельные шприцы для каждой из них.
Особые указания
Вакцинация особенно показана следующим группам с высоким риском заболевания менингококковой инфекцией:
- лицам, которые имели непосредственный контакт с пациентами, инфицированными менингококками серогрупп A, C, Y или W-135 (в семье или в учреждениях закрытого типа);
- лицам с дефицитом пропердина и компонентов комплемента;
- лицам с функциональной или анатомической аспленией;
- туристам и лицам, выезжающим в гиперэндемичные по менингококковой инфекции зоны, такие как страны Африки, расположенные к югу от Сахары;
- сотрудникам исследовательских, промышленных и клинических лабораторий, регулярно подвергающимся воздействию N. meningitidis, находящейся в растворах, способных образовывать аэрозоль;
- студентам различных вузов, и, особенно, проживающим в общежитиях или в гостиницах квартирного типа;
- призывникам и новобранцам.
Запрещено вводить вакцину Менактра® подкожно или внутрикожно, поскольку данные о безопасности и эффективности вакцины при подкожном и внутрикожном введении отсутствуют.
Запрещается смешивать вакцину Менактра® в одном шприце с другими вакцинами или препаратами.
Применение вакцины у лиц с тромбоцитопенией или нарушениями свертываемости крови не изучалось. Как и в случае других вакцин, вводимых внутримышечно, следует оценить соотношение пользы и риска применения вакцины у лиц с повышенным риском развития кровотечения при внутримышечной инъекции.
Риск развития синдрома Гийена-Барре (СГБ) после введения вакцины Менактра® оценивался в рамках пострегистрационного ретроспективного когортного исследования. Описаны случаи развития СГБ, характеризовавшиеся наличием связи по времени с введением вакцины Менактра®. Лица, которым ранее был установлен диагноз СГБ, могут составлять группу повышенного риска развития данного состояния после введения вакцины Менактра®. Решение об использовании вакцины Менактра® в данной ситуации должно приниматься после оценки потенциальных пользы и рисков.
Вакцина не предназначена для профилактики менингитов, вызванных другими микроорганизмами, или для профилактики инвазивной менингококковой инфекции, вызванной менингококками серогруппы В.
Хотя после введения вакцины Менактра® может наблюдаться гуморальный иммунный ответ к дифтерийному анатоксину, данная вакцина не может считаться иммунизирующим агентом против дифтерии. Не рекомендуется изменять график вакцинации стандартными вакцинами против дифтерии в связи с введением вакцины Менактра®.
У лиц с нарушенным иммунным статусом, а также на фоне иммуносупрессивной терапии, может наблюдаться сниженный иммунный ответ на введение вакцины Менактра ® .
Как при любой вакцинации, защитный иммунитет может вырабатываться не у всех 100 % привитых.
Перед применением вакцины медицинский работник или лечащий врач должен информировать пациента, его родителей, опекунов или других ответственных взрослых лиц о возможных пользе и риске для пациента, связанных с введением вакцины.
Перед введением вакцины следует принять необходимые меры предосторожности, направленные на профилактику тяжелых побочных реакций, а именно: изучить прививочный анамнез пациента, выяснить наличие противопоказаний к иммунизации и провести оценку текущего состояния здоровья пациента.
Введение вакцины проводится под контролем медицинского работника, а в кабинете, где проводят вакцинацию, должны быть доступны необходимые средства противошоковой терапии (например, растворы эпинефрина гидрохлорида (1:1000) и глюкокортикостероидов для инъекций).
После введения вакцины Менактра ® отмечались случаи обморока. Необходимо предусмотреть меры для предотвращения травм, связанных с падением в обморок, а также возможность оказания медицинской помощи в случае обморока.
Влияние на способность управлять транспортными средствами, механизмами
Исследований по изучению влияния вакцины на способность к управлению автомобилем и другими механизмами не проводилось.
Форма выпуска
Срок годности
2 года.
Не использовать по истечении срока годности, указанного на упаковке.
Датой окончания срока годности является последнее число месяца, указанного на упаковке.
Условия хранения
При температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Препарат, подвергшийся замораживанию, использованию не подлежит.
Условия транспортирования
При температуре от 2 до 8 °С. Не замораживать.
Условия отпуска
Отпускают по рецепту.
Производитель
Санофи Пастер Инк., США
Sanofi Pasteur Inc.,
Discovery Drive, Swiftwater, Pennsylvania, 18370, USA
Владелец регистрационного удостоверения
Санофи Пастер Инк., США
Sanofi Pasteur Inc.,
Discovery Drive, Swiftwater, Pennsylvania, 18370, USA
Организация, уполномоченная владельцем РУ на принятие претензий от потребителя
Менактра - цена, наличие в аптеках
Указана цена, по которой можно купить Менактра в Москве. Точную цену в Вашем городе Вы получите после перехода в службу онлайн заказа лекарств:
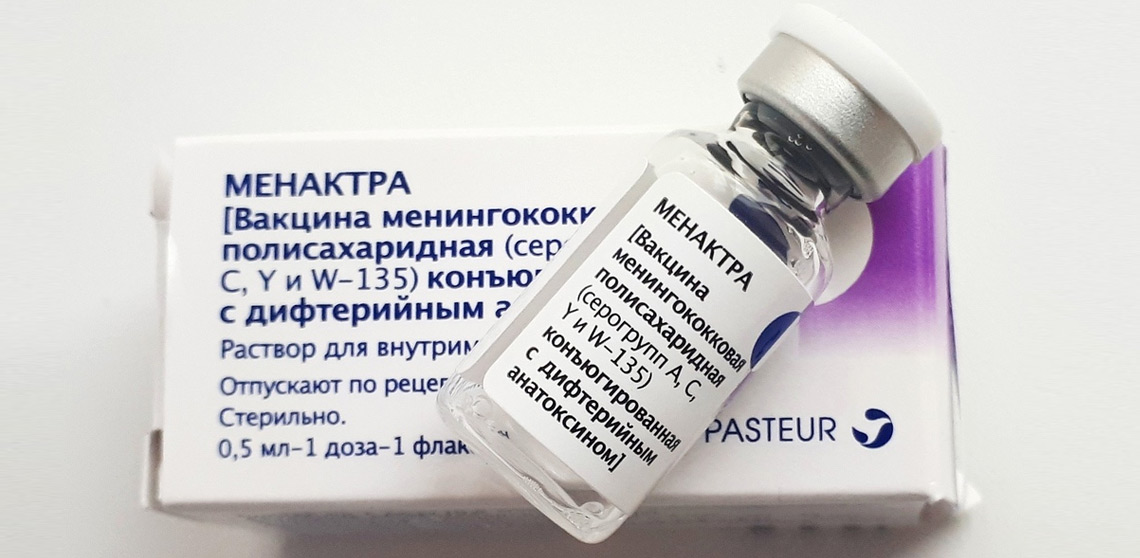
Стоимость прививки Менактра в Москве составляет 7500 руб. В цену включён осмотр врача перед вакцинацией.
Похожие вакцины (аналоги Менактра):
Вакцина менингококковая полисахаридная (серогрупп А, С, Y и W-135), конъюгированная с дифтерийным анатоксином.
Лекарственная форма: раствор для внутримышечного введения.
Вакцина Менактра представляет собой раствор очищенных капсульных полисахаридов Neisseria meningitidis групп А, С, Y и W-135, индивидуально конъюгированных с белком-носителем (дифтерийным анатоксином).
В качестве вспомогательных веществ присутствуют: натрия хлорид, натрия гидрофосфат, натрия дигидрофофата моногидрат, вода для инъекций.
Описание
Иммунологические свойства
Применение вакцины Менактра вызывает выработку специфических антител против капсульных полисахаридов Neisseria meningitidis групп А, С, Y и W-135, обладающих бактерицидной активностью.
Иммунологическая эффективность
Выработка сывороточных бактерицидных антител считается показателем эффективности менингококковых вакцин.
Кинетика иммунного ответа: иммунная защита может наблюдаться через 7-10 дней после вакцинации.
Продолжительность защиты: способность вакцины Менактра индуцировать формирование иммунной памяти после первичной вакцинации была доказана в ходе клинических исследований. В одном из исследований было продемонстрировано, что персистенция бактерицидных антител в крови через 3 года после однократного введения вакцины Менактра была выше по сравнению с группой привитых, получивших однократную иммунизацию 4-валетной полисахаридной менингококковой вакциной против серогрупп А, С, Y и W-135. В группе привитых вакциной Менактра наблюдались более высокая концентрация сывороточных бактерицидных антител, а также более высокая доля лиц, имевших специфические высокоавидные антитела, что говорит о формировании иммунной памяти.
Показания к применению
Профилактика инвазивной менингококковой инфекции, вызываемой Neisseria meningitidis серогрупп А, С, Y и W-135 у лиц в возрасте от 9 мес до 55 лет.
Противопоказания
- Известная гиперчувствительность с системными проявлениями к любому компоненту вакцины, включая дифтерийный анатоксин, или на предыдущее введение других вакцин, включающих те же компоненты.
- Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления и в период ремиссии).
Применение при беременности и в период грудного вскармливания
Исследования на животных не выявили отрицательного действия вакцины Менактра на течение беременности и фето-эмбрионльного развития плода, процесс родов и постнатальное развитие. В связи с тем, что исследований вакцины у беременных женщин не проводилось, а постмаркетинговый опыт ее применения ограничен, введение вакцины беременным женщинам рекомендуется только в случае крайней необходимости, как например, во время вспышки менингококковой инфекции, перед поездкой в эндемичный район, и только после оценки соотношения пользы и риска вакцинации.
В настоящее время неизвестно, способны ли активные вещества, входящие в состав вакцины, проникать в грудное молоко. Однако ранее было показано, что антитела к полисахаридам обнаруживаются у молодых мышей, находившихся на грудном вскармливании.
В исследованиях на мышах не было продемонстрировано неблагоприятного влияния на постнатальное развитие потомства, получавшего материнские антитела с молоком и выработка которых была индуцирована введением вакцины Менактра. В то же время, эффекты у детей первого года жизни, матери которых были иммунизированы вакциной Менактра в период грудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины, необходимо оценить риски и пользу данной иммунизации.
Способ введения и дозы
Вакцинация проводится одной дозой 0,5 мл.
Вакцину следует вводить внутримышечно, принимая во внимание возраст и массу прививаемого: детям в возрасте от 9 до 12 мес – в передне-боковую область бедра; детям в возрасте от 12 мес и старше – в дельтовидную мышцу плеча.
Не вводить вакцину внутривенно или подкожно.
У детей в возрасте от 9 до 23 мес, курс вакцинации вакциной Менактра состоит из 2 инъекций по одной дозе вакцины (0,5 мл) с интервалом не менее 3 мес.
У лиц в возрасте от 2 до 55 лет вакцинация проводится однократно в дозе 0,5 мл.
В случае неблагополучной эпидемической ситуации по менингококковой инфекции рекомендуется проводить однократную ревакцинацию в возрасте от 15 до 55 лет, при условии, что с момента предыдущей вакцинации прошло не менее 4 лет.
Побочное действие
- Очень часто: ≥ 10%
- Часто: ≥ 1 и ˂ 10%
- Нечасто: ≥ 0,1 и ˂ 1%
- Редко: ≥ 0,01 и ˂ 0,1%
- Очень редко: ˂ 0,01%
- Частота неизвестна: не может быть определена согласно имеющимся данным.
Дети в возрасте от 9 до 18 мес
Со стороны обмена веществ и питания
Со стороны нервной системы
Со стороны желудочно-кишечного тракта
Общие расстройства и нарушения в месте введения
Очень часто: болезненность, эритема в месте инъекции, отек в месте инъекции, раздражительность, аномальный плач, лихорадка.
Дети в возрасте от 2 до 10 лет
Со стороны обмена веществ и питания
Со стороны нервной системы
Со стороны желудочно-кишечного тракта
Со стороны кожи и подкожных тканей
Со стороны скелетно-мышечной и соединительной ткани
Общие расстройства и нарушения в месте введения
Очень часто: болезненность и уплотнение в месте инъекции.
Очень часто или часто: раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка.
Лица в возрасте 11-55 лет
Со стороны обмена веществ и питания
Со стороны нервной системы
Со стороны желудочно-кишечного тракта
Со стороны кожи и подкожных тканей
Со стороны скелетно-мышечной и соединительной ткани
Общие расстройства и нарушения в месте введения
Очень часто: боль, уплотнение, покраснение и отек в месте инъекции, повышенная утомляемость, общее недомогание.
Часто: озноб, лихорадка.
Взаимодействие с другими лекарственными средствами
- лицам, которые имели непосредственный контакт с пациентами, инфицированными менингококками серогрупп А, С, Yи W-135 (в семье или учреждениях закрытого типа);
- лицам с дефицитом пропердина и компонентов комплемента;
- лицам с функциональной или анатомической аспленией;
- туристам и лицам, выезжающим в гиперэндемичные по менингококковой инфекции зоны, такие как страны Африки, расположенные к югу от Сахары;
- сотрудникам исследовательских, промышленных и клинических лабораторий, регулярно подвергающимся воздействию Neisseria meningitidis, находящейся расворах, способных образовывать аэрозоль;
- студентам различных вузов, и, особенно, проживающих в общежитиях или в гостиницах квартирного типа;
- призывникам и новобранцам.
Влияние на способность к вождению автотранспорта и управлению механизмами
Исследований по изучению влияния вакцины на способность к вождению автотранспорта и управлению механизмами не проводилось.
Условия хранения
Производитель
Составить индивидуальный график вакцинации или получить грамотную консультацию специалиста теперь можно не выходя из дома, потому что мы заботимся о Вас, снижая количество контактов и экономя Ваше время!
А еще мы отвечаем на интересующие вас вопросы в специальном разделе! Чаще всего это вопросы индивидуального характера в отношении вакцинации, иммунитета и тому подобного.
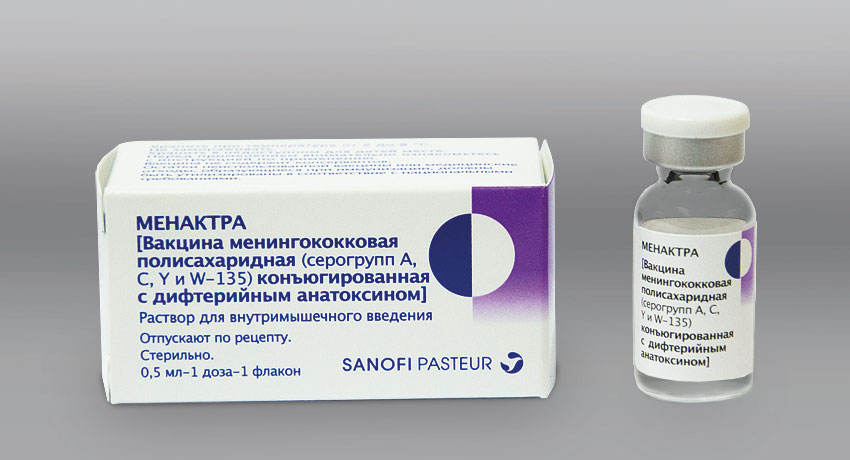
р-р д/в/м введения 1 доза: флакон 0,5 мл - 1 или 5 шт.
Форма выпуска, состав и упаковка
Раствор для в/м введения бесцветный, прозрачный или слегка мутноватый.
1 доза (0.5 мл)
моновалентные менингококковые конъюгаты полисахаридов Neisseria meningitidis серогруппы A*
моновалентные менингококковые конъюгаты полисахаридов Neisseria meningitidis серогруппы C*
моновалентные менингококковые конъюгаты полисахаридов Neisseria meningitidis серогруппы Y*
моновалентные менингококковые конъюгаты полисахаридов Neisseria meningitidis серогруппы W-135*
*каждый полисахарид конъюгирован с дифтерийным анатоксином. Содержание белка дифтерийного анатоксина в прививочной дозе составляет около 48 мкг.
Вспомогательные вещества: натрия хлорид - 4.35 мг, натрия гидрофосфат - 0.348 мг, натрия дигидрофосфата моногидрат - 0.352 мг, вода д/и - до 0.5 мл.
1 доза (0.5 мл) - флаконы стеклянные (1) - пачки картонные.
1 доза (0.5 мл) - флаконы стеклянные (5) - пачки картонные.
Клинико-фармакологическая группа: Вакцина для профилактики заболеваний, вызванных менингококками
Фармако-терапевтическая группа: МИБП-вакцина
Фармакологическое действие
Вакцина Менактра представляет собой раствор очищенных капсульных полисахаридов Neisseria meningitidis групп A, C, Y и W-135, индивидуально конъюгированных с белком-носителем (очищенным анатоксином Corynebacterium diphtheriae).
Возбудителем менингококковой инфекции, включая менингит и септицемию, является бактерия N. meningitidis, выделен ряд серотипов возбудителя. Применение вакцины Менактра вызывает выработку специфических антител против капсулярных полисахаридов серогрупп возбудителя менингококковой инфекции, входящих в вакцину (А, С, Y и W-135), которые обладают бактерицидной активностью.
Клинические исследования по изучению эффективности не проводились, поскольку выработка сывороточных бактерицидных антител (СБА) считается показателем эффективности менингококковых вакцин.
Иммунологические свойства вакцины Менактра изучали в 3 клинических исследованиях у детей в возрасте 9-18 мес, в 4 клинических исследованиях у детей в возрасте 2-10 лет и в 6 клинических исследованиях в группе лиц в возрасте 11-55 лет. Иммуногенность оценивали по уровню этих функциональных антител, определяемых с помощью бактерицидного анализа сыворотки с применением комплемента крольчат (БАС).
Первичный иммунологический профиль изучали в рамках клинических исследований на участниках от 2 до 10 лет. Иммунный ответ оценивали непосредственно перед однократным введением вакцины Менактра и спустя 28 дней. У участников исследования наблюдали значительное повышение среднего геометрического титров (СГТ) бактерицидных антител. Во всех серогруппах у 86-100% участников при исходно неопределяемых значениях титров СБА (<1:8) была отмечена сероконверсия, определяемая как 4-кратное (или более) увеличение титров антител спустя 28 дней после вакцинации
Способность вакцины Менактра вызывать развитие иммунологической памяти после первичной вакцинации документирована данными клинических исследований как у детей, так и у взрослых.
Результаты 3 клинических исследований, проведенных у детей от 9 до 18 мес с однократным или двукратным введением вакцины Менактра отдельно или одновременно с другими педиатрическими вакцинами (пневмококковой конъюгированной вакциной (ПКВ) или вакциной для профилактики кори, паротита, краснухи и ветряной оспы (КПКВ)), подтвердили, что у большинства участников в группах с двукратным введением вакцины Менактра, отдельно или одновременно с другими педиатрическими вакцинами, наблюдалось увеличение доли лиц с титром СБА ≥1:8 ко всем серогруппам вакцины. У 91% и 86% участников в группе с отдельным двукратным введением вакцины Менактра наблюдалось увеличение титра СБА ≥1:8 к серогруппам А, С, Y, и к серогруппе W-135 соответственно. Когда вторая доза вакцины Менактра была введена одновременно с ПКВ или с КПКВ (или КПКВ + вакцина для профилактики инфекций, вызываемых Haemophilus influenzae), у большинства участников исследования наблюдалось нарастание титра СБА ≥1:8 (у >90% участников исследования к серогруппам А, С и Y, и у >81% участников к серогруппе W-135). Значения СГТ СБА оказались выше исходных ко всем четырем серогруппам менингококков, включенных в вакцину.
Кинетика иммунного ответа: отсутствуют данные о кинетике первоначального ответа на введение вакцины Менактра, однако, как и в случае других полисахаридных и конъюгированпых вакцин, иммунная защита может наблюдаться через 7-10 дней после вакцинации.
Продолжительность защиты: способность вакцины Менактра индуцировать формирование иммунной памяти после первичной вакцинации была доказана в ходе клинических исследований. В одном из исследований было продемонстрировано, что персистенция бактерицидных антител в крови через 3 года после однократного введения вакцины Менактра была выше по сравнению с группой привитых, получивших однократную иммунизацию 4-валентной полисахаридной мснингококковой вакциной против серогрупп А, С, Y и W-135. В группе привитых вакциной Менактра наблюдались более высокая концентрация сывороточных бактерицидных антител, а также более высокая доля лиц. имевших специфические высокоавидные антитела, что говорит о формировании иммунной памяти.
Показания препарата Менактра
- профилактика инвазивной менингококковой инфекции, вызываемой N. meningitidis серогрупп А, С, Y и W-135 у лиц в возрасте от 9 месяцев до 55 лет.
Режим дозирования
Вакцинация проводится однократно в дозе 0,5 мл.
Вакцину следует вводить внутремышечно, принимая во внимание возраст и массу прививаемого: детям в возрасте от 9 до 12 мес - в передне-боковую область бедра; детям в возрасте от 12 мес и старше - в дельтовидную мышцу плеча.
У детей в возрасте от 9 до 23 мес курс вакцинации вакциной Менактра состоит из 2 инъекций по 1 дозе вакцины (0.5 мл) с интервалом не менее 3 мес.
У лиц в возрасте от 2 до 55 лет вакцинация проводится однократно в дозе 0.5 мл.
Меры предосторожности при примененеии
Перед введением вакцины необходимо принять необходимые меры предосторожности, направленные на профилактику тяжелых побочных реакций, которые включают изучение прививочного анамнеза пациента, выяснение наличия противопоказаний к иммунизации и оценку текущего состояния здоровья пациента.
Введение вакцины проводится под контролем медицинского работника, а в кабинете, где проводят вакцинацию, должен быть доступны необходимые средства противошоковой терапии (например, растворы эпинефрина гидрохлорида (1:1000) и глюкокортикостероидов для инъекции).
После введения вакцины Менактра отмечались случаи обморока. Необходимо предусмотреть меры для предотвращения травм, связанных с падением в обморок, а также медицинскую помощь в связи с обмороком.
Побочное действие
Характер и частота выявленных в исследованиях побочных эффектов различались в зависимости от возраста прививаемых. В ходе клинических исследований у детей в возрасте от 9 до 18 мес в течение 7 дней после вакцинации наиболее часто отмечались чувствительность в месте инъекции и болезненность; у детей в возрасте от 2 до 10 лет наиболее часто отмечались болезненность и покраснение в месте инъекции, раздражительность, диарея, сонливость, анорексия; у подростков в возрасте от 11 до 18 лет и у взрослых лиц от 18 до 55 лет наиболее часто отмечались болезненность в месте инъекции, головная боль и повышенная утомляемость. Частота развития приведенных ниже побочных эффектов классифицирована согласно рекомендациям Всемирной организации здравоохранения (ВОЗ) и включает следующие категории: очень часто: ≥ 10 %; часто: ≥ 1 % и < 10%; нечасто: ≥ 0,1 % и < 1 %; редко: ≥ 0,01 % и < 0,1 %; очень редко: < 0,01%; частота неизвестна: не может быть определена согласно имеющимся данным.
Дети в возрасте от 9 до 18 мес
Со стороны нервной системы: очень часто - сонливость.
Со стороны пищеварительной системы: очень часто - потеря аппетита; очень часто или часто - рвота.
Общие расстройства и нарушения в месте введения: очень часто - болезненность, эритема в месте инъекции, отек в месте инъекции, раздражительность, аномальный плач, лихорадка.
Со стороны обмена веществ и питания
Очень часто или часто: снижение аппетита
Со стороны нервной системы
Очень часто или часто: сонливость
Очень часто: диарея
Со стороны кожи и подкожных тканей
Часто: сыпь, крапивница
Со стороны скелетно-мышечной и соединительной ткани
Общие расстройства и нарушения в месте введения
Очень часто: болезненность и уплотнение в месте инъекции
Очень часто или часто: раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка
Лица в возрасте 11-55 лет
Со стороны обмена веществ и питания
Очень часто или часто: снижение аппетита
Со стороны нервной системы
Очень часто: головная боль
Очень часто или часто: диарея
Со стороны кожи и подкожных тканей
Со стороны скелетно-мышечной и соединительной ткани
Очень часто: артралгия
Общие расстройства и нарушения в месте введения
Очень часто: боль, уплотнение, покраснение и отек в месте инъекции, повышенная утомляемость, общее недомогание
Часто: озноб, лихорадка
В постмаркстинговый период дополнительно получена информация о следующих нежелательных явлениях после введения препарата (в настоящее время частота развития данных явлений и их причинно-следственная связь с применением вакцины Менактра не может быть определена):
Со стороны иммунной системы
Реакции гиперчувствительности, такие как анафилактический шок, анафилактоидные реакции, стридорозное дыхание, затруднение при дыхании, отек верхних дыхательных путей, крапивница, покраснение кожи, кожный зуд. снижение артериального давления.
Со стороны нервной системы
Синдром Гийена-Барре (СГБ). парестезии, потеря сознания (обусловленная нарушениями регуляции со стороны вегетативной нервной системы), головокружение, судороги, паралич лицевого нерва, острый рассеянный энцефаломиелит, поперечный миелит.
Со стороны скелетно-мышечной и соединительной ткани
Противопоказания к применению
известная гиперчувствительность с системными проявлениями к любому компоненту вакцины, включая дифтерийный анатоксин, или на предыдущее введение других вакцин, включающих те же компоненты;
острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии).
Применение при беременности и кормлении грудью
Исследования на животных не выявили отрицательного действия вакцины Менактра на течение беременности и фето-эмбрионального развития плода, процесс родов и постнатальное развитие. В связи с тем, что исследований вакцины у беременных женщин не проводилось, а постмаркетинговый опыт ее применения ограничен, введение вакцины беременным женщинам рекомендуется только в случае крайней необходимости, как например, во время вспышки менингококковой инфекции, перед поездкой в эндемичный район, и только после оценки соотношения пользы и риска вакцинации. В настоящее время неизвестно, способны ли активные вещества, входящие в состав вакцины, проникать в грудное молоко. Однако ранее было показано, что антитела к полисахаридам обнаруживаются у молодых мышей, находившихся на грудном вскармливании.
В исследованиях на мышах не было продемонстрировано неблагоприятного влияния на постнатальное развитие потомства, получавшего материнские антитела с молоком и выработка которых была индуцирована введением вакцины Менактра. В то же время, эффекты у детей первого года жизни, матери которых были иммунизированы вакциной Менактра в период грудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины, необходимо оценить риски и пользу данной иммунизации.
Применение у детей
Вакцинации подлежат дети достигшие 9-иесячного возраста.
Особые указания
Вакцинация особенно показана следующим группам с высоким риском заболевания менингококковой инфекцией:
лицам, которые имели непосредственный контакт с пациентами, инфицированными менингококками серогрупп А, С, Y или W-135 (в семье или в учреждениях закрытого типа);
лицам с дефицитом пропердина и компонентов комплемента;
лицам с функциональной или анатомической аспленией;
туристам и лицам, выезжающим в гиперэндемичные по менингококковой инфекции зоны, такие как страны Африки, расположенные к югу от Сахары;
сотрудникам исследовательских, промышленных и клинических лабораторий, регулярно подвергающиеся воздействию N. meningitidis, находящейся в растворах, способных образовывать аэрозоль;
студентам различных вузов, и, особенно, проживающих в общежитиях или в гостиницах квартирного типа;
призывникам и новобранцам.
Запрещено вводить вакцину Менактра внутривенно, подкожно или внутрикожно, поскольку данные о безопасности и эффективности вакцины при подкожном, внутривенном и внутрикожном введении отсутствуют.
Запрещается смешивать вакцину Менактра в одном шприце с другими вакцинами или препаратами.
Применение вакцины у лиц с тромбоцитопенией или нарушениями свертываемости крови не изучалось. Как и в случае других вакцин, вводимых внутримышечно, следует оценить соотношение пользы и риска применения вакцины у лиц с повышенным риском развития кровотечения при внутримышечной инъекции.
Риск развития синдрома Гийена-Барре (СГБ) после вакцинации Менактрой оценивался в рамках постмаркетингового ретроспективного когортного исследования. Описаны случаи развития СГБ, характеризовавшиеся наличием связи по времени с введением вакцины Менактра. Лица, которым ранее был установлен диагноз СГБ, могут составлять группу повышенного риска развития данного состояния после введения вакцины Менактра. Решение об использовании вакцины Менактра в данной ситуации должно приниматься после оценки потенциальных пользы и рисков.
Вакцина не предназначена для профилактики менингитов, вызванных другими микроорганизмами или для профилактики инвазивной менингококковой инфекции, вызванной менингококками серогруппы В.
У лиц с нарушенным иммунным статусом, а также на фоне иммуносупрсссивной терапии, может наблюдаться сниженный иммунный ответ на введение вакцины Менактра.
Как при любой вакцинации, защитный иммунитет может вырабатываться не у всех 100% привитых.
Перед применением вакцины медицинский работник или лечащий врач должен информировать пациента, его родителей, опекунов или других ответственных взрослых лиц о возможной пользе и риске для пациента, связанных
с введением вакцины.
Влияние на способность к вождению автотранспорта и управлению механизмами
Исследований по изучению влияния вакцины на способность к управлению автомобилем и другими механизмами не проводилось.
Передозировка
Нет достоверных данных.
Лекарственное взаимодействие
У детей в возрасте до 2 лет вакцину Менактра применяли совместно с одной или несколькими из следующих вакцин: пневмококковой конъюгированной вакциной (ПКВ), вакциной для профилактики кори, паротита, краснухи, вакциной для профилактики ветряной оспы или вакциной для профилактики вирусного гепатита А.
Отсутствуют данные для оценки безопасности и иммуногенности вакцины Менактра при совместном применении в возрасте 18 мес с АКДС-содержащими вакцинами.
Титры пневмококковых антител против некоторых серотипов, содержащихся в 7-валентной пневмококковой конъюгированной вакцине (ПКВ7), были снижены после одновременного введения вакцины Менактра и вакцины ПКВ7.
Вакцину БЦЖ не следует применяться одновременно с вакциной Менактра.
Вводить вакцины необходимо всегда в разные участки тела, используя отдельные шприцы для каждой из них.
Условия и сроки хранения
При температуре от 2 до 8°С. Не замораживать. Хранить в недоступном для детей месте. Препарат, подвергшийся замораживанию, использованию не подлежит. Срок годности - 2 года.
Менактра (Menaktra) - вакцина менингококковая полисахаридная (серогрупп А, С, Y и W-135), конъюгированная с дифтерийным анатоксином
Регистрационный номер: ЛП-002636
Торговое название: Менактра
Группировочное название: вакцина для профилактики менингококковых инфекций
Лекарственная форма: раствор для внутримышечного введения
Страна-производитель: Sanofi Pasteur, США
Предварительное обследование: не требуется
Стоимость вакцины: 7000 руб.(дополнительно оплачивается осмотр перед вакцинацией)
Применяется: Для взрослых и детей
Условия отпуска из аптек: по рецепту

Оставьте заявку на вакцинацию.
Наш менеджер согласует удобное для вас время приема.
ОПИСАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Внешний вид: Бесцветный прозрачный или слегка мутноватый раствор.
Фармакотерапевтическая группа: МИБП-вакцина.
Код АТХ: J07AH08.
Вакцина Менактра (Menaktra) представляет собой раствор очищенных капсульных полисахаридов Neisseria meningitidis групп А, С, Y и W-135 индивидульно конъюгированных с белком-носителем (очищенным анатоксином Carynebacterium diphtheriae).
Иммунологические свойства
Возбудителем менингококковой инфекции, включая менингит и септицемию, является бактерия N. meningitidis,. выделен ряд серотипов возбудителя. Применение вакцины Менактра вызывает выработку специфических антител против капсулярных полисахаридов серо групп возбудителя менингококковой инфекции, входящих в вакцину С, С, Y и W-1З5) , которые обладают бактерицидной активностью.
Иммунологическая эффективность
Клинические исследования по изучению эффективности не проводились, поскольку выработка сывороточных бактерицидных антител (СБА) считается показателем эффективности менингококковых вакцин.
Иммунологические свойства вакцины Менактра изучали в 3 клинических исследованиях у детей в возрасте 9-18 мес, в 4 клинических исследованиях у детей в возрасте 2-10 лет и в 6 клинических исследованиях в группе лиц в возрасте 11-55 лет. Иммуногенность оценивали по уровню этих функциональных антител, определяемых с помощью бактерицидного анализа сыворотки с применением комплемента крольчат (БАС).
Первичный иммунологический профиль изучали в рамках клинических исследований на участниках от 2 до 10 лет. Иммунный ответ оценивали непосредственно перед однократным введением вакцины Менактра и спустя 28 дней. у участников исследования наблюдали значительное повышение среднего геометрического титров (СГТ) бактерицидных антител. Во всех серо группах у 86-100 участников при исходно неопределяемых значениях титров СБА «1: 8) была отмечена сероконверсия , определяемая как 4-кратное (или более) увеличение титров антител спустя 28 дней после вакцинации.
СОСТАВ
Одна доза (0,5мл) содержит:
Активные вещества:
- Полисахарид серогруппы А* - 4мкг;
- Полисахарид серогруппы С* - 4 мкг;
- Полисахарид серогруппы Y* - 4 мкг;
- Полисахарид серогруппы W-135* - 4 мкг.
* - каждый полисахарид конъюгирован с дифтерийным анатоксином. Содержание белка дифтерийного анатоксина в прививочной дозе составляет около 48мкг.
Вспомогательные вещества:
- Натрия хлорид 4, З5 мг;
- Натрия гидрофосфат 0, З48 мг;
- Натрия дигидрофосфата моногидрат 0,З52 мг;
- Вода для инъекций - до 0,5 мл.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
Способность вакцины Менактра вызывать развитие иммунологической памяти после первичной вакцинации документирована данными клинических исследований как у детей, так и у взрослых.
Результаты З клинических исследований, проведенных у детей от 9 до 18 мес с однократным или двукратным введением вакцины Менактра отдельно или одновременно с другими педиатрическими вакцинами (пневмококковой конъюгированной вакциной СПКВ) или вакциной для профилактики кори, паротита, краснухи и ветряной оспы (КПКВ)), подтвердили, что у большинства участников в группах с двукратным введением вакцины Менактра, отдельно или одновременно с другими педиатрическими вакцинами, наблюдалось увеличение доли лиц с титром СБА ~1:8 ко всем серогруппам вакцины. У 91% и 86% участников в группе с отдельным двукратным введением вакцины Менактра наблюдалось увеличение титра СБА>1:8 к серогруппам А, С, Y, и к серо группе W-1З5, соответственно. Когда вторая доза вакцины Менактра была введена одновременно с ПКВ или с КПКВ (или КПКВ + вакцина для профилактики инфекций, вызываемых Наеmорhilus influenzae), у большинства участников исследования наблюдалось нарастание титра СБА ~1:8 (у > 90 участников исследования к серогруппам А, С и Y, и у > 81% участников к серогруппе W-1З5). Значения СГТ СБА оказались выше исходных ко всем четырем серо группам менингококков, включенных в вакцину.
Кинетика иммунного ответа:
отсутствуют данные о кинетике первоначального ответа на введение вакцины Менактра, однако, как и в случае других полисахаридных и конъюгированных вакцин, иммунная защита может наблюдаться через 7-10 дней после вакцинации.
Продолжительность защиты
Способность вакцины Менактра индуцировать формирование иммунной памяти после первичной вакцинации была доказана в ходе клинических исследований. В одном из исследований было продемонстрировано, что персистенция бактерицидных антител в крови через З года после однократного введения вакцины Менактра было выше по сравнению с группой привитых , получивших однократную иммунизацию 4-валентной полисахаридной менингококковой вакциной против серогрупп А, С, Y и W-1З5. В группе привитых вакциной Менактра наблюдались более высокая концентрация сывороточных бактерицидных антител, а также более высокая доля лиц, имевших специфические высокоавидные антитела, что говорит о формировании иммунной памяти.
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Профилактика инвазивной менингококковой инфекции, вызываемой N.meningitidis серогрупп А, С, Y и W-1З5 у лиц в возрасте от 9 мес до 55 лет.
Оссобенное показано группам
Вакцинация особенно показана следующим группам с высоким риском заболевания менингококковой инфекцией:
- Люди, которые имели непосредственный контакт с пациентами, инфицированными менингококками серогрупп А, С, Y или W-135 (в семье или в учреждениях закрытого типа);
- Людям с дефицитом пропердина и компонентов комплемента; лицам с функциональной или анатомической аспленией;
- Туристам и людям, выезжающим в гиперэндемичные по менин ГО кокковой инфекции зоны, такие как страны Африки, расположенные к югу от Сахары;
- Сотрудникам исследовательских, промышленных и клинических лабораторий, регулярно подвергающиеся воздействию N. meningitidis, находящейся в растворах, способных образовывать аэрозоль;
- Cтудентам различных вузов, и, особенно, проживающих в общежитиях или в гостиницах квартирного типа;
- Призывникам и новобранцам.
ПРОТИВОПОКАЗАНИЯ
- Известная гиперчувствительность с системными проявлениями к любому компоненту вакцины, включая дифтерийный анатоксин, или на предыдущее введение других вакцин, включающих те же компоненты;
- Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (в этих случаях вакцинацию проводят после выздоровления или в стадии ремиссии).
СПОСОБ ПРИМЕНЕНИЯ И ДОЗИРОВКА
Вакцинация проводится одной дозой 0,5 мл.
Вакцину следует вводить внутримышечно, принимая во внимание возраст и массу прививаемого: детям в возрасте от 9 до 12 мес - в передне-боковую область бедра; детям в возрасте от 12 мес и старше - в дельтовидную мышцу плеча.
у детей в возрасте от 9 до 2З мес, курс вакцинации вакциной Менактра состоит из 2 инъекций по одной дозе вакцины (0,5 мл) с интервалом не менее З мес.
у лиц в возрасте от 2 до 55 лет вакцинация проводится однократно в дозе 0,5 мл.
Применение при беременности и в период грудного вскармливания
Исследования на животных не выявили отрицательного действия вакцины Менактра на течение беременности и фето-эмбрионального развития плода, процесс родов и постнатальное развитие. В связи с тем, что исследований вакцины у беременных женщин не проводилось, а постмаркетинговый опыт ее применения ограничен, введение вакцины беременным женщинам рекомендуется только в случае крайней необходимости, как например, во время вспышки менингококковой инфекции, перед поездкой в эндемичный район, и только после оценки соотношения пользы и риска вакцинации.
В настоящее время неизвестно, способны ли активные вещества, входящие в состав вакцины, проникать в грудное молоко. Однако ранее было показано, что антитела к полисахаридам обнаруживаются у молодых мышей, находившихся на грудном вскармливании.
В исследованиях на мышах не было продемонстрировано неблагоприятного влияния на постнатальное развитие потомства, получавшего материнские антитела с молоком и выработка которых было индуцировано введением вакцины Менактра. В то же время, эффекты у детей первого года жизни, матери которых мыши иммунизированы вакциной Менактра в период т рудного вскармливания, не исследовались. Перед принятием решения об иммунизации кормящей женщины, необходимо оценить риски и пользу данной иммунизации.
Меры предосторожности при применении
Перед введением вакцины необходимо принять необходимые меры предосторожности, направленные на профилактику тяжелых побочных реакций, которые включают изучение прививочного анамнеза пациента, выяснение наличия противопоказаний к иммунизации и оценку текущего состояния здоровья пациента.
Введение вакцины проводится под контролем медицинского работника, а в кабинете, где проводят вакцинацию, должны быть доступны необходимые средства противошоковой терапии (например, растворы эпинефрина гидрохлорида (1:1000) и глюкокортикостероидов для инъекций).
После введения вакцины Менактра отмечались случаи обморока. Необходимо предусмотреть меры для предотвращения травм, связанных с падением в обморок, а также медицинскую помощь в связи с обмороком.
ПОБОЧНЫЕ ДЕЙСТВИЯ
Характер и частота выявленных в исследованиях побочных эффектов различались в зависимости от возраста прививаемых.
Побочные реации у детей от 9 до 18 мес
- Потеря аппетита;
- Сонливость;
- Рвота;
- Диарея;
- Сыпь;
- Крапивница;
- Артралгия;
- Болезненность и уплотнение в месте инъекции;
- Раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка.
Побочные реакции у детей от 2 до 10 лет
- Снижение аппетита;
- Сонливость;
- Диарея;
- Рвота;
- Сыпь, крапивница;
- Артралгия;
- Болезненность и уплотнение в месте инъекции;
- Раздражительность, покраснение в месте инъекции, отек в месте инъекции, лихорадка.
Побочные реакции у подростков от 11 до 18 лет и взрослых от 18 лет
- Снижение аппетита;
- Головная боль;
- Диарея;
- Рвота;
- Сыпь;
- Артралгия;
- Боль, уплотнение, покраснение и отек в месте инъекции, повышенная утомляемость, общее недомогание;
- Озноб, лихорадка.
ПЕРЕДОЗИРОВКА
Нет достоверных данных.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
У детей младше 2 лет вакцину Менактра применяли совместно с одной или несколькими из следующих вакцин: пневмококковой конъюгированной вакциной (ПКВ), вакциной для профилактики кори, паротита, краснухи, вакциной для профилактики ветряной оспы или вакциной для профилактики вирусного гепатита А.
Отсутствуют данные для оценки безопасности и иммуногенности вакцины Менактра при совместном применении в возрасте 18 мес с АКДС- содержащими вакцинами.
Титры пневмококковых антител против некоторых серотипов содержащихся в 7-валентной пневмококковой конъюгированной вакцине (ПКВ7) были снижены после одновременного введения вакцины Менактра и вакцины ПКВ7.
БЦЖ вакцина не должна применяться одновременно с вакциной Менактра. Вводить вакцины необходимо всегда в разные участки тела, используя отдельные шприцы для каждой из них.
ОСОБЫЕ УКАЗАНИЯ
Запрещено вводить вакцину Менактра внутривенно, подкожно или внутрикожно, поскольку данные о безопасности и эффективности вакцины при подкожном, внутривенном и внутрикожном введении отсутствуют.
Запрещается смешивать вакцину Менактра в одном шприце с другими вакцинами или препаратами.
Применение вакцины у лиц с тромбоцитопенией или нарушениями свертываемости крови не изучалось . Как и в случае других вакцин, вводимых внутримышечно, следует оценить соотношение пользы и риска применения вакцины у лиц с повышенным риском развития кровотечения при внутримышечной инъекции.
Риск развития синдрома Гийена-Барре (СГБ) после вакцинации Менактрой оценивался в рамках постмаркетингового ретроспективного когортного исследования. Описаны случаи развития СГБ, характеризовавшиеся наличием связи по времени с введением вакцины Менактра. Лица, которым ранее был установлен диагноз СГБ, могут составлять группу повышенного риска развития данного состояния после введения вакцины Менактра. Решение об использовании вакцины Менактра в данной ситуации должно приниматься после оценки потенциальных пользы и рисков.
Вакцина не предназначена для профилактики менингитов, вызванных другими микроорганизмами или для профилактики инвазивной менингококковой инфекции, вызванной менингококками серогруппы В у лиц с нарушенным иммунным статусом, а также на фоне иммуносупрессивной терапии, может наблюдаться сниженный иммунный ответ на введение вакцины Менактра.
Как при любой вакцинации, защитный иммунитет может вырабатываться не у всех 100 привитых.
Перед применением вакцины медицинский работник или лечащий врач должен информировать пациента, его родителей, опекунов или других ответственных взрослых лиц о возможной пользе и риске для пациента, связанных с введением вакцины.
ВЛИЯНИЕ НА СПОСОБНОСТЬ К ВОЖДЕНИЮ АВТОТРАНСПОРТА И УПРАВЛЕНИЮ МЕХАНИЗМАМИ
Исследований по изучению влияния вакцины на способность к управлению автомобилем и другими механизмами не проводилось.
ФОРМА ВЫПУСКА
Внешний вид: Раствор для внутримышечного введения 0,5 мл/доза.
По 1 или 5 флаконов вместе с инструкцией по медицинскому применению в пачке картонной.
УСЛОВИЯ ХРАНЕНИЯ
При температуре от 2 до 8 С·. Не замораживать. Хранить в недоступном для детей месте.
Препарат, подвергшийся замораживанию, использованию не подлежит.
СРОК ГОДНОСТИ
Срок годности - 2 года.. Не использовать по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА
Препарат отпускается по рецепту .
ПРОИЗВОДИТЕЛЬ
Санофи Пастер Инк., США
Sапоfi. Pasteur Inc.,
Discovery Dri.ve, Swiftwater, Pennsylvania, 18370, USA
ПРЕТЕНЗИИ
Обо всех случаях необычных прививочных реаций и при выявлении рекламаций на качество препарата следует сообщать по адресу:
Федеральная служба по надзору в сфере здравоохранения (Росздравнадзор):
Записаться на прием, получить консультацию

Оставьте заявку на вакцинацию.
Наш менеджер согласует удобное для вас время приема.
Читайте также:

