Метаболическая терапия при гепатите
Обновлено: 17.04.2024
Успешное лечение острого токсического гепатита у пациента со стеатозом печени и метаболическим синдромом
Русских А.В.
ГБОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ, Москва
Сочетание “алкогольного” анамнеза со стеатозом печени, по данным разных авторов, может встречаться в 50 % случаев. Строго разделить острый алкогольный гепатит (ОАГ) и неалкогольный стеатогепатит (НАСГ) удается не всегда, т. к. в клинической практике эти состояния часто сочетаются. Данный клинический пример иллюстрирует “перекрест” двух заболеваний печени, которые могут взаимоотягощать течение двух патологических процессов – ОАГ и НАСГ. Для комплексного лечения ОАГ и НАСГ в настоящее время может использоваться хорошо изученная и безопасная комбинация орнитина, адеметионина, пентоксифиллина, метформина, урсодеоксихолиевой и тиоктовой кислот (Тиогамма). С учетом участия тиоктовой кислоты в антиоксидантной защите можно считать обоснованным назначение Тиогаммы всем больным с признаками метаболического синдрома и токсическим поражением печени.
Несмотря на значительный прогресс в изучении патогенеза заболеваний печени алкогольной этиологии, остается много нерешенных вопросов, поэтому в настоящее время все больше внимания уделяется патологическим процессам, отягощающим течение токсического гепатита и являющимся фоновыми заболеваниями. К таким состояниям в первую очередь следует отнести метаболический синдром (МС) с главенствующей ролью инсулинорезистентности и стеатоз печени.
Строго разделить острый алкогольный гепатит (ОАГ) и неалкогольный стеатогепатит (НАСГ) удается не всегда, и в клинической практике эти состояния часто сочетаются, взаимоотягощая друг друга. При этом разговор о “безопасной” дозе алкоголя не всегда можно использовать как универсальный под-
ход к каждой клинической ситуации.
НАСГ – это дисметаболический процесс, который характеризуется инфильтрацией и жировой дистрофией гепатоцитов, воспалительными изменениями с последующими цитолизом и фиброзом. На первом этапе болезни архитектоника печени остается сохранной. Однако доказано, что без правильного лечения и при употреблении алкоголя НАСГ может прогрессировать в цирроз печени и привести к печеночно-клеточной недостаточности. Развитие дистрофических, воспалительно-некротических и фибротических изменений в печени в такой ситуации связано с нарушением процессов перекисного окисления липидов вследствие инсулинорезистентности, с одной стороны, и с токсическими эффектами ацетальдегида, с другой.
Сочетание “алкогольного” анамнеза со стеатозом печени, по данным разных авторов, может встречаться в 50 % случаев. При этом в каждом конкретной ситуации целесообразно выявление преобладающего этиологического фактора [1, 2].
ОАГ – это процесс, вызванный основным метаболитом этанола – ацетальдегидом, образующимся в гепатоцитах под воздействием алкогольдегидрогеназы и цитохрома Р450 2Е1 из молекул С2Н5ОН и заканчивающийся повреждением гепатоцитов. Примерно в половине случаев этот процесс сочетается с МС [2, 7].
Варианты ОАГ
1. Латентный (безжелтушный) вариант встречается в 30 % случаев и характеризуется в основном лабораторными изменениями при минимальной клинике. Пациенты с указанным вариантом поражения печени при правильном лечении имеют благоприятный исход болезни.
2. Желтушный вариант ОАГ встречается наиболее часто (до 50 %). У пациентов отмечаются выраженная клиническая картина – слабость, желтуха, боль в правом подреберье, асцит, диспепсические явления. Часто наблюдаются субфебрилитет, повышение билирубина до 5–7 норм.
3. Холестатический вариант наблюдается в 15 % случаев и сопровождается желтухой, обесцвечиванием кала, потемнением мочи, выраженным зудом, характерно повышение билирубина до 20 норм. В половине случаев данный вариант заканчивается летально.
4. Фульминантный ОАГ встречается в 5 % случаев и отличается быстрым прогрессированием желтухи, энцефалопатии и печеночноклеточной недостаточности. Лабораторные изменения представлены лейкоцитозом, достигающим 20–40 тыс. в 1 мкл, повышением СОЭ до 40–50 мм/ч, анемией с макро-
цитозом. Билирубин повышается преимущественно за счет прямой фракции, достигая высоких
показателей. Активность трансаминаз возрастает многократно, при этом соотношение АСТ/АЛТ
больше 2, повышается активность γ-глутаматтранспептидазы (ГГТП), щелочной фосфатазы. Нарастают
биохимические признаки печеночной недостаточности: снижение протромбинового индекса, уровней альбумина и холинэстеразы. К летальному исходу (до 95 %) приводят печеночная кома и кровотечение из варикозно расширенных вен пищевода.
Исход ОАГ зависит от варианта течения и фонового хронического поражения печени, а также от своевременной диагностики и правильного лечения [2]. Главными терапевтическими принципами лечения ОАГ являются отказ от приема алкоголя, богатая белками и достаточно калорийная диета (30 ккал/кг массы тела), дезинтоксикационная терапия, орнитин, адеметионин, пентоксифиллин и урсодеоксихолевая кислота (УДХК).
УДХК обладает противовоспалительным и антиооксидантным эффектами, способствует регенераторным процессам [9]. Пентоксифилин подавляет синтез фактора некроза опухоли α, предотвращая развитие гепаторенального синдрома, снижает смертность на 40 % [2]. Адеметионин – обладает детоксикационным, регенерирующим, антиоксидантным эффектами, действует как метаболический субстрат важнейших биохимических реакций в организме. Он восстанавливает структуру и свойства клеточных мембран, повышая выживаемость, отодвигает сроки трансплантации печени при тяжелых формах ОАГ [1, 2, 7].
Данные мета-анализа 10 исследований указывают на достоверное повышение выживаемости больных тяжелым ОАГ при использовании глюкокортикостероидов. Стандартный курс составляет 40 мг преднизолона или 32 мг метилпреднизолона перорально в сутки с обязательным назначением ингибиторов протонной помпы [2].
МС включает нарушение всех видов обмена: углеводного, белкового, липидного, и проявляется нарушением толерантности к углеводам различной степени, инсулинорезистентностью, гиперурикемией и подагрой, ожирением с явлениями стеатоза печени или НАСГ; в некоторых случаях МС включает не все вышеперечисленные признаки. У больных МС, протекающим с минимальными проявлениями, практически в 100 % случаев выявляется стеатоз печении, а у 25–30 % пациентов имеет место НАСГ [2, 3].
Варианты НАСГ
Клинически НАСГ характеризуется мало- и бессимптомным течением. Наиболее часто при НАСГ больные отмечают неопределенный дискомфорт, проявления диспепсического синдрома. Незначительное увеличение размеров печени характерно для большинства пациентов; признаки
портальной гипертензии, печеночной недостаточности выявляются редко – не более чем у 8–10 % больных. Биохимическое исследование крови обнаруживает умеренное повышение уровней АЛТ и АСТ (1,5–3,0 нормы) в сочетании с незначительным повыением уровней ГГТП и щелочной фосфатазы (до 1,5–2,0 норм) [3, 10].
Несмотря на определенные достижения в области терапии МС, лечение таких больных остается сложной задачей. Принципы лечения НАСГ включают перестройку пищевых поведенческих реакций. Рациональное снижение массы тела на 1500 г в неделю способствует уменьшению жировой инфильтрации гепатоцитов. Медикаментозная коррекция МС инсулинсенсетайзерами, например метформином, снижает у больных НАСГ уровень гипергликемии и повышает чувствительность
к инсулину, уменьшает активность печеночных ферментов, выраженность жировой дистрофии, воспалительных изменений и фиброза в печени [6, 7]. Как важное направление может рассматриваться применение препаратов с антиоксидантной активностью (тиоктовой кислоты и УДХК) [3–5], которое может быть вполне оправданно с точки зрения патогенеза НАСГ. В настоящее время проводится исследование по применению вышеуказанных препаратов больными с хроническими
вирусными гепатитами для коррекции инсунорезистентности (при НАСГ и/или токсическим поражение печени) перед проведением противовирусной терапии. Из положительных эффектов тиоктовой кислоты обращаем внимание на следующие: препарат способствует снижению концентрации глюкозы в крови и увеличению гликогена в печени, а также преодолению инсулинорезистентности. Участвует в регулировании липидного и углеводного обмена, стимулирует обмен холестерина. Улучшает функцию печени, снижает повреждающее влияние на нее эндогенных и экзогенных токсинов, в т. ч. алкоголя. Благотворно воздействует на репаративные процессы: уменьшает проявления висцеральной микроангиопатии в тканях, в т. ч. в гепатоцитах, улучшает печеночную функцию. Препараты тиоктовой кислоты и УДХК также способствуют снижению синтеза провоспалительных цитокинов, уменьшают абсорбцию холестерина в подвздошной кишке, снижая синтез холестерина в печени.
Клинический пример
Пациент Р. 64 лет, физик, обратился в поликлинику с жалобами на слабость, потливость, повышение артериального давления (АД) до 170/100 мм рт. ст., сухость во рту, боли в правом подреберье, увеличение живота, склонность к жидкому стулу.
печеночных трансаминаз: АСТ, ГГТП –норма, АЛТ – 1,5 нормы. Уровень глюкозы натощак – 7,0 ммоль/л; от дальнейшего обследования и лечения в тот период отказался. Ухудшение состояния отметил неделю назад, когда появились слабость, сухость во рту, увеличился живот (в течение 10 дней
ежедневно после стресса употреблял крепкие спиртные напитки до 200 мл). Обратился в поликлинику, при амбулаторном обследовании выявлено: АСТ 1749 ЕД (43 нормы), АЛТ 607 ЕД (15 норм), ГГТП 441ЕД (8 норм), глюкоза натощак – 8,8 ммоль/л, мочевая кислота – 554 ммоль/л. Пациенту была предложена госпитализация в стационар дневного пребывания.
При осмотре в стационаре: общее состояние удовлетворительное, обращает на себя внимание повышенная масса тела до 110 кг (индекс массы тела – 32 кг/м2), гиперемия кожных покровов. Над легкими прослушивается везикулярное дыхание, хрипов нет. Частота дыханий – 18 в минуту. Тоны
сердца звучные, ритм правильный. АД –160 /90 мм рт. ст. Пульс – 80 в минуту. Живот при пальпации мягкий, увеличен за счет подкожножировой клетчатки, безболезненный, печень + 5 см (размеры по Курлову – 15–12–10 см). Перкуторно жидкость в брюшной полости не определяется.
Больному в стационаре проведен комплексный клинико-лабораторный мониторинг: общий анализ крови – гемоглобин 162 г/л, эритроциты 5,4 × 1012/л, лейкоциты 9,3 × 109/л, тромбоциты 169 тыс., СОЭ 40 мм/ч. Биохимический анализ: глюкоза 9,8 ммоль/л, билирубин общий 45,6 мкмоль/л, мочевина 4,2 ммоль/л, креатинин 89 мкмоль/л, мочевая кислота 521 мкмоль/л, железо 31,4 ммоль/л, АСТ 1843 ЕД (45 – норм), АЛТ 720 ЕД (18 норм), ГГТП 524 ЕД (9,5 норм), щелочная фосфатаза 192 ЕД (9,5 – норм),
холестерин 6,4 ммоль/л. Наличие гепатотропных вирусов не подтверждено. По данным ультразвукового исследования брюшной полости размеры печени увеличены: правая доля – 167 × 90, левая 78 × 65 мм, портальная вена – до 13 мм, селезеночная вена – до 11 мм, размеры селезенки – 15 × 10 см. Желчный пузырь не увеличен, толщина стенки – 2,5 мм, конкрементов нет. Поджелудочная железа несколько увеличена, гиперэхогенна, главный панкреатический проток не расширен. Жидкость в брюшной полости не определяется.
С учетом данных, полученных при сборе жалоб, анамнеза, а также результатов осмотра и лабораторных данных поставлен диагноз “острый токсический гепатит высокой степени активности, протекающий на фоне стеатоза печени в рамках метаболического синдрома”.
В условиях дневного стационара проведено следующее лечение: физиологический раствор 0,9 % – 500 мл + адеметионин 10,0 мл внутривенно капельно № 10, Тиогамма 600 мг внутривенно капельно № 10, метформин (Метфогамма) 1000 мг на ночь, орнитин 5 г 2 раза в сутки. На фоне проведенного лечения через 10 дней состояние значительно улучшилось, выписан в удовлетворительном состоянии со следующими биохимическими показателями: АСТ 51 ЕД, АЛТ 95 ЕД, ГГТП 159 ЕД, щелочная
фосфатаза 83 ЕД. Рекомендован полный отказ от алкоголя. С учетом сохраняющегося синдрома холестаза также рекомендован прием УДХК 500 мг вечером в течение 3 месяцев, орнитин 5 г 2 раза в
сутки в течение 3 месяцев, Тиогамма 600 мг утром в течение 2 месяцев, метформин (Метфогамма) 1000 мг на ночь постоянно. Контроль биохимических показателей 1 раз в 3 месяца.
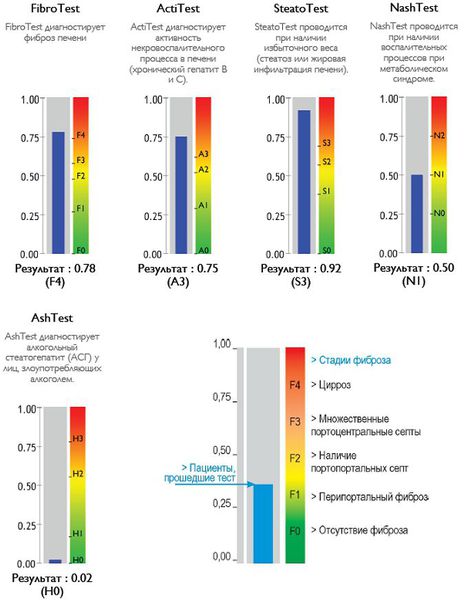
Через месяц после полного восстановления функции печени пациенту предложена реабилитация по МС (питание до 1200 ккал/сут, ежедневные аэробные нагрузки, например ходьба или плавание в бассейне). В тот период проведен ФиброТест, который применяется для оценки стадии фиброза при алкогольном и неалкогольном стеатозе. Применять данный тест при активном воспалительном процессе в печени не рекомендовано.
Приводим результаты данного исследования: диагностика фиброза Fibro 1–2, НешТест NASH-2 свидетельствует о выраженном неалкогольном стеатозе, АшТест ASH-0 – об отсутствии или наличии минимального алкогольного стеатоза. Данные результаты полностью соответствуют предшествующей диагностической концепции.
Анализируя этот клинический пример, обращаем внимание на следующее: у пациента несомненно имеет место “метаболический орнамент”, скорее всего связанный с генетической предрасположенностью и неправильным образом жизни (гиподинамия, избыточное питание, отсутствие физических нагрузок), подтвержденный лабораторно. Для коррекции инсулинорезистентности, лежащий в основе МС, назначены метформин (Метфогамма) и тиоктовая кислота (Тиогамма). С другой стороны, четкое указание на употребление гепатотоксической дозы алкоголя перед ухудшением состояния позволило с учетом лабораторных данных поставить диагноз острого токсического гепатита, латентного (безжелтушного) течения. Для коррекции этого процесса назначен орнитин и адеметионин, а затем УДХК.
Таким образом, данный клинический пример иллюстрирует “перекрест” двух заболеваний печени, которые могут взаимоотягощать течение патологического процесса – НАСГ и ОАГ. Своевременная диагностика, правильное, патогенетически обоснованное лечение в сочетании с полным отказом от алкоголя в короткие сроки привели к купированию ОАГ и полной нормализации лабораторных показателей.
Литература
1. Яковенко Э.П., Григорьев П.Я., Агафонова Н.А. и др. Метаболические заболевания печени: проблемы терапии // Фарматека 2003. № 10.
2. Практическая гепатология / Под ред. Н.А. Мухина. М., 2005.
3. Mendez-Sanchez N, Arrese M, Zamora-Valdes D, Uribe M, et al. Current concepts in pathogenesis of nonalcoholic fatty liver disease. Liver Int 2007;27(4):423–33.
4. Arivazhagan P, Panneerselvam C. Effect of DL –alpha-lipoic acid on tissue nucleic acid contents in aged rats. Pharmacol Res 2000;42(3):223-6.
5. Roberts E. A. Pediatric nonalcoholic fatty liver disease (NAFLD): A “growing” problem? J Hepatol 2007;46(6):1133–42.
6. Konrad T, Vicini P, Kusterer K, et al. Alpha-Lipoic acid treatment decreases serum lactate and pyruvate concentrations and improves glucose effectiveness in lean and obese patients with type 2 diabetes. Diabetes Care 1999;22(2):280–87.
7. Tilg H, Kaser A. Management of acute alcoholic hepatitis. In: Prevention and Intervention in Liver Disease. IASL–EASL Postgraduate Course. Madrid, 2002:28–37.
8. Lazaridis KN, Gores GJ, Lindor KD. Ursodeoxycholic acid mechanisms of action and clinical use in hepatobiliary disorders. J Hepatol 2001;35:134–46.
9. Brunt EM. Nonalcoholic steatohepatiatis. Semin Liver Dis 2004;24:3–20.
Об авторах / Для корреспонденции
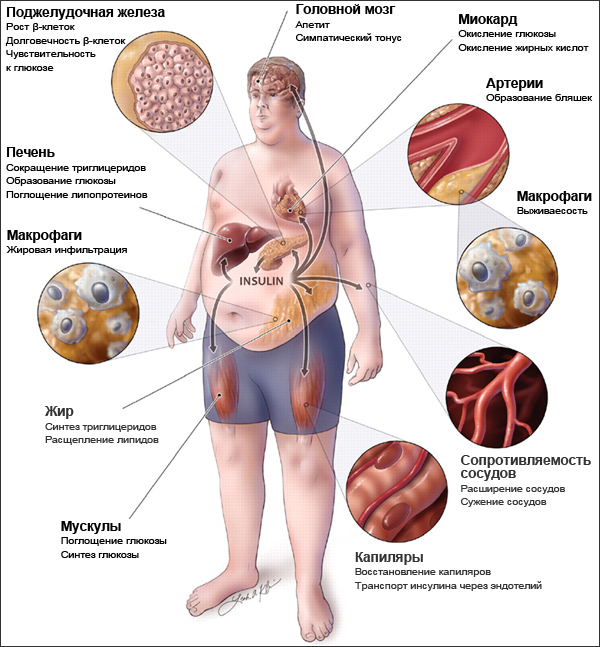
Метаболический синдром развивается у 40 % людей в основном пенсионного возраста и у всех, кто ведет малоподвижный образ жизни и неправильно питается. Распространенность метаболического синдрома продолжает расти.
В основе метаболического синдрома и его проявлений лежит инсулинрезистентность. Резистентность (устойчивость) к инсулину заключается в том, что для поддержания нормального метаболизма требуется большее количество инсулина.
Отмечено, что инсулинрезистентность часто встречается у больных с хроническим вирусным гепатитом С (ХГС), что свидетельствует о тесной связи этих двух состояний. Поскольку ХГС больны более 170 млн. человек, сочетание инфекции с инсулинрезистентностью представляет серьезную проблему мирового здравоохранения.
С резистентностью к инсулину связано также развитие у больных ХГС стеатоза – жирового перерождения печени, которое почти в 2 раза чаще, чем в среднем у населения. Стеатоз связан также с повышением индекса массы тела (ИМТ), сахарным диабетом 2 типа, возрастом старше 40 лет, гепатитом С, вызванным вирусом С генотипа 3 и фиброзом.
Генотип вируса 3 оказывает прямое стеатогенное действие, у пациентов с другими генотипами вируса основную роль в формировании стеатоза играет инсулинрезистентность.
Независимо от того, что развивается первым, резистентность к инсулину является основным фактором риска тяжелого фиброза печени и рассматривается как важный прогностический фактор формирования цирроза печени.
Резистентность к инсулину играет основную роль в формировании сахарного диабета 2 типа, поэтому не удивительно, что среди больных гепатитом С он встречается в 2 раза чаще.
Резистентность к инсулину ухудшает результаты лечения ХГС. Для оценки инсулинрезистентности используют индекс HOMA-IR. При значении этого индекса больше 4 эффективность лечения (частота устойчивого вирусологического ответа – УВО) снижалась на 40 %. У пациентов с индексом HOMA-IR меньше 2 ранний вирусологический ответ определялся у всех пациентов.
Жировой гепатоз также значительно ухудшает прогнозы на выздоровление.
Поскольку на успех противовирусной терапии значительно влияют степень ожирения, резистентность к инсулину и стеатоз печени, следует оценивать эти факторы при назначении терапии. Если они присутствуют, то для достижения наилучшего терапевтического эффекта требуется коррекция резистентности к инсулину и лечение стеатоза.
Симптомы метаболического синдрома
Нарушения, объединенные рамками метаболического синдрома, длительное время протекают бессимптомно. Наиболее ранними проявлениями метаболического синдрома являются дислипидемия и повышение артериального давления. Часто не все компоненты метаболического синдрома встречаются одновременно:
- абдоминально-висцеральное ожирение (окружность талии более 102 см у мужчин и более 88 см у женщин);
- инсулинорезистентность при высоком уровне инсулина;
- дислипидемия (сочетание гипертриглицеридемии — больше 1,7, низкого уровня ХЛ ЛВП и повышения фракции мелких ХЛ ЛНП;
- артериальная гипертензия (артериальное давление выше 130/85 мм рт. ст.);
- ранний атеросклероз и ишемическая болезнь сердца.
Возможные жалобы на повышенную утомляемость, апатию, одышку, повышенный аппетит, жажду, учащенное мочеиспускание, головную боль, сухость кожи, потливость.
Лечение метаболического синдрома
Лечение назначают в зависимости от степени обменных нарушений и тех заболеваний, которые выявлены у пациента. Лечение направлено на коррекцию углеводного обмена, снижение массы тела, купирование артериальной гипертонии и симптомов сахарного диабета.
Немедикаментозное лечение метаболического синдрома
Первым этапом лечения метаболического синдрома является изменения стиля жизни, в первую очередь правильное питание и повышение физической нагрузки. Первым шагом и его обязательным звеном должно быть снижение таким образом массы абдоминально-висцерального жира, который играет ключевую роль в развитии и прогрессировании метаболического синдрома.
Снижение общей массы тела на 10-15% от исходной сопровождается уменьшением висцеральной жировой ткани, т. е. жира, расположенного не в подкожном слое, а вокруг внутренних органов. Это, как правило, ведет к повышению чувствительности тканей к инсулину, улучшению показателей липидного и углеводного обмена, нормализации повышенного артериального давления.
Снижение массы тела должно быть постепенным. Быстрый и резкий сброс массы тела на 10-20 кг приводит к снижению гормона лептина и к возникновению труднопреодолимого чувства голода, и в результате к возврату лишних килограммов, иногда даже в большем количестве, чем до терапии.
Потеря массы тела снижает содержание свободных жирных кислот в печени, что приводит к снижению инсулинрезистентности, повышает внепеченочную чувствительность к инсулину, уменьшает воспаление в жировой ткани.
Медикаментозное лечение метаболического синдрома
Дополнительным лечением метаболического синдрома является назначение урсодезоксихолевой кислоты и витамина Е, которые оказывают антиоксидантное действие и улучшают результаты лечения ХГС.
Препараты, повышающие чувствительность к инсулину (тиазолидиндиолы и метформин) снижают резистентность к инсулину и уменьшают выраженность фиброза и степени жирового гепатоза у больных гепатитом С.
Все это улучшает результаты терапии противовирусными препаратами.
Поэтому обследование пациентов, готовящихся к противовирусной терапии, в особенности с генотипом 3, обязательно должно включать анализ на инсулинрезистенстность (индекс HOMA-IR), оценку степени метаболического синдрома и всех его компонентов с обязательной последующей коррекцией желательно до начала терапии.
Тактика лечения пациентов с ожирением и метаболическим синдромом при гепатите С
При выявлении у пациентов с HCV сопутствующего поражения печени в результате метаболического синдрома (неалкогольная жировая болезнь печени - стеатоз) необходимо провести дополнительное обследование на показатели обменных и гормональных нарушений, характерных для этого заболевания.
Рекомендуется для оценки степени поражения печени использовать исследование крови – Фибромакс, которое дает возможность оценить отдельно степень поражения печени вирусом и отдельно метаболическим синдромом.
Тактика лечения зависит от степени поражения печени в целом, и отдельно каждым повреждающим фактором. Лечение противовирусными препаратами может быть назначено сразу, а дальнейшее лечение метаболического синдрома после получения УВО.
Если степень поражения печени вирусом значительно меньше, чем метаболическим синдромом, возможно начинать противовирусную терапию после лечения метаболического синдрома.
В случаях наличия сопутствующих заболеваний печени необходимо ставить целью лечения не только получение УВО, но и сохранение и восстановление печени, пострадавшей от других патологических факторов.
Диагностическим тестом при гепатите С служит определение антител к вирусу методом ИФА (анти-HCV). Если антитела к HCV обнаружены, необходимо определять РНК HCV чувствительным методом молекулярной диагностики.
В случае положительного результата на антитела и отрицательного результата определения РНК-HCV необходимо выполнять повторные исследования для подтверждения выздоровления.
Цель лечения вирусного гепатита С
Цель лечения – полное удаление вируса и предупреждение заболеваний печени и внепеченочных заболеваний, включая воспалительно-дегенеративные поражения, фиброз, цирроз, рак печени и тяжелые внепеченочные проявления.
Контрольный показатель эффективности лечения
Устойчивый вирусологический ответ (УВО) – отсутствие вируса (определяемой РНК-HCV) через 12 и 24 недели после окончания лечения. Исследование необходимо проводить чувствительным методом молекулярной диагностики с нижним порогом определения 15 МЕ/мл и менее.
Результаты исследований с долгосрочным наблюдением показали, что УВО соответствует окончательному излечению от гепатита в 99% случаев.
У пациентов с циррозом и выраженным фиброзом исследования РНК-HCV следует продолжать и после получения УВО.
Обследование перед началом терапии (подробнее. )
Исключение других причин поражения печени
Прежде всего необходимо исключить другие факторы, влияющие на течение заболевания: наличие гепатотропных вирусов – гепатита В, ВИЧ, алкоголизма, аутоиммунного заболевания печени, поражение печени генетическими и метаболическими заболеваниями: гемахроматоз, сахарный диабет или ожирение, токсическое поражение печени и другие.
Оценка степени поражения печени.
Поскольку от стадии фиброза зависит вероятность выздоровления, прежде всего, необходимо выявление цирроза или выраженного фиброза. В настоящее время убедительно показана возможность оценки степени фиброза не инвазивными методами:
эластометрия / эластография (на аппарате фиброскан),
фибромакс и фибротест (по показателям крови)
Наиболее информативным является совместное определение степени фиброза (по крови и на аппарате фиброскан), что полностью заменяет биопсию.
Пациентам с циррозом необходимо исключать гепатоцеллюлярную карциному (первичный рак печени), а также осложнение цирроза – выраженную портальную гипертензию с расширением вен пищевода и желудка. С этой целью важно до начала терапии провести ЭГДС (гастроскопию).
Для оценки состояния печени проводится биохимическое обследование крови с определением структурных (АЛТ, АСТ, ГГТ) и функциональных показателей (альбумин, общий белок, белковые фракции, фракции липидов), а также общий клинический анализ крови.
Определение характеристик вируса.
Для назначения противовирусной терапии необходимо определить вирусную нагрузку и генотип вируса.
Количественное определение вируса должно проводиться чувствительным методом.
Генотипы устанавливаются методами, позволяющими достоверно определить подтип вируса (например, 1а и 1в), так как они влияют на выбор терапии.
Определение генетических характеристик пациента.
Определение генотипа интерлейкина 28В не потеряло своего прогностического значения.
Противопоказания для применения препаратов прямого противовирусного действия.
Абсолютных противопоказаний к применению препаратов прямого противовирусного действия нет.
Следует соблюдать меры предосторожности при лечении препаратом софосбувир пациентов с заболеваниями почек и сердца.
Пациентам с декомпенсированным циррозом класса В и С противопоказана комбинация препаратов Викейра Пак.
Продолжается исследование безопасности препарата симепревир для пациентов с декомпенсированным циррозом.
Показания к лечению: кого следует лечить?
Все пациенты с компенсированным и декомпенсированным хроническим гепатитом С являются кандидатами на лечение, если они не имеют противопоказаний.
Не имеет значения, получали они ранее терапию или нет.
Приоритет в лечении определяется стадией фиброза. В первую очередь следует назначать терапию пациентам с фиброзом F3-F4 по шкале METAVIR.
Пациентам с декомпенсированным циррозом (класс В и С по шкале Чайлд-Пью) лечение должно быть назначено незамедлительно. Желательно проводить его в условиях отделения трансплантологии.
К группе высокого приоритета относятся также пациенты, коинфецированные ВИЧ и гепатитом В, а также с клинически значимыми внепеченочными проявлениями, такими как васкулит, сопровождающийся криоглобулинемией.
Пациентам с умеренным фиброзом F2 назначение лечения оправдано, однако при необходимости оно может быть отложено (например, по материальным соображениям).
Время начала терапии у пациентов без проявлений или с легким течением заболевания (F0-1) и без внепеченочных симптомов определяется индивидуально.
Препараты прямого противовирусного действия, доступные в Европе.
СОФОСБУВИР – следует принимать в дозе 400 мг (1 таблетка) один раз в сутки.
Софосбувир выводится в основном (80%) почками с мочой, поэтому назначение его требует осторожности у пациентов с заболеваниями почек.
Возможны межлекарственные взаимодействия с многими препаратами, поэтому следует внимательно относиться к сопутствующим заболеваниям и корректировать прием препаратов, назначенных для лечения этих заболеваний.
ЛЕДИПАСВИР – доступен в комбинации с софосбувиром (400 мг софосбувира и 90 мг ледипасвира). Доза для приема – 1 таблетка в день независимо от приема пищи.
Так как ледипасвир может взаимодействовать с другими лекарственными препаратами, следует соблюдать меры предосторожности, с частым контролем функции почек. Кроме того, важно учитывать прием пациентом статинов и препаратов в схеме антиретровирусной терапии.
СИМЕПРЕВИР – следует принимать 1 капсулу 150 мг 1 раз в сутки. Пациентам, принимающим симепревир, противопоказаны некоторые препараты, в том числе антиретровирусные.
ДАКЛАТАСВИР – 1 таблетка 60 мг 1 раз в сутки. Многочисленные лекарственные взаимодействия даклатасвира требуют внимательного отношения при его назначении и соответственно контроля при его применении.
ВИКЕЙРА ПАК – комплексный препарат, включающий 4 действующих вещества (ритонавир, усиливающий действие паритапревира, омбитасвир и дасабувир).
Рекомендуемая дозировка 1 раз в сутки во время еды 2 таблетки ритонавира/паритапревира/омнитасвира, а также дасабувир 2 раза в сутки. При назначении следует учитывать многочисленные лекарственные взаимодействия и класс цирроза.
Варианты лечения различных групп пациентов.
Для лечения хронического гепатита С противовирусными препаратами прямого действия существует несколько различных схем, эффективность и безопасность которых проверена во многих клинических испытаниях.
Выбор комбинаций лекарственных средств осуществляется врачом и зависит от генотипа и подтипа вируса, тяжести заболевания печени, результатов предшествующей терапии.
Длительность терапии зависит от степени поражения печени и наличия компенсированного или декомпенсированного цирроза. Стандартный курс терапии – 12 недель, при циррозе может быть увеличен до 24 недель.
Возможно назначение дополнительно к схеме лечения препарата рибавирин у пациентов с циррозом и с отрицательными прогностическими факторами ответа на лечение, например, при содержании тромбоцитов менее 75х10^3/мкл.
Для лечения пациентов с генотипом 1 (1а и 1в) существует 4 рекомендованные схемы препаратов прямого противовирусного действия:
Для лечения пациентов с генотипом 2 существует только одна безинтерфероновая схема: софосбувир+даклатасвир в течение 12 недель.
Пациентов с циррозом, ранее уже получавших или не получавших терапию, следует лечить также 12 недель.
Для лечение пациентов, инфицированных HCV генотипа 3, пока существует только одна схема безинтерфероновой терапии: софосбувир +даклатасвир. Ледипасвир в отношении HCV генотипа 3 значительно менее эффективен, чем даклатасвир, поэтому схемы с применением ледипасвира для этого генотипа не рекомендованы.
Пациентам с HCV генотипа 3 с циррозом, получавшим или не получавшим ранее терапию, следует назначать эту схему лечения с добавлением рибавирина и длительностью курса 24 недели.
Контроль лечения
В процессе лечения необходимо контролировать эффективность и безопасность (побочные нежелательные эффекты).
Контроль эффективности лечения основан на регулярном определении уровня РНК HCV с использованием чувствительных количественных методов.
РНК HCV следует определять до начала терапии, через 2 недели, а затем через 4, 8 и 12 недель, а также через 12 и 24 недели после окончания курса лечения.
Прекращение терапии вследствие ее бесперспективности при лечении препаратами прямого противовирусного действия правилами НЕ предусмотрено.
Контроль безопасности лечения
Схемы лечения препаратами прямого противовирусного действия хорошо переносятся. Случаи выраженных нежелательных явлений, требующих отмены препаратов, отмечены редко.
Однако, во время терапии необходимо контролировать проявления токсичности других препаратов, применяемых для лечения сопутствующих заболеваний, а также проявления лекарственных взаимодействий. При лечении схемами, содержащими софосбувир, необходимо контролировать состояние почек.
Наиболее часто отмечаются утомляемость и головная боль.
Лечение следует безотлагательно прекратить при обострении гепатита (АЛТ выше нормы в 10 раз).
Тактика лечения пациентов с ожирением и метаболическим синдромом
При выявлении у пациентов с HCV сопутствующего поражения печени в результате метаболического синдрома (неалкогольная жировая болезнь печени - стеатоз) необходимо провести дополнительное обследование на показатели обменных и гормональных нарушений, характерных для этого заболевания.
Рекомендуется для оценки степени поражения печени использовать исследование крови – Фибромакс, которое дает возможность оценить отдельно степень поражения печени вирусом и отдельно метаболическим синдромом.
Тактика лечения зависит от степени поражения печени в целом, и отдельно каждым повреждающим фактором. Лечение противовирусными препаратами может быть назначено сразу, а дальнейшее лечение метаболического синдрома после получения УВО.
Если степень поражения печени вирусом значительно меньше, чем метаболическим синдромом, возможно начинать противовирусную терапию после лечения метаболического синдрома.
В случаях наличия сопутствующих заболеваний печени необходимо ставить целью лечения не только получение УВО, но и сохранение и восстановление печени, пострадавшей от других патологических факторов.
С целью совершенствования терапии хронического вирусного гепатита С проведена оценка влияния препарата ремаксол на биохимические показатели, параметры эндотоксикоза, перекисное окисление липидов и антиоксидантную систему при ХГС.
Использование препарата ремаксол, обладающего гепатопротективным, антигипоксическим, антиоксидантным и цитопротективным эффектами в составе комплексной патогенетической терапии больных ХГС значительно улучшает биохимические показатели, уменьшая выраженность цитолитического и холестатического синдромов.
Применение ремаксола влияет на состояние процессов липопероксидации, уменьшая их активность, повышает потенциал антиоксидантной системы и снижает проявления эндотоксикоза.
Ключевые слова: хронический гепатит С, терапия, ремаксол.
Центральным звеном в генезе патоморфологических изменений в печеночной паренхиме при хроническом гепатите С (ХГС) является цитолиз гепатоцитов, инициирующий процесс некробиоза печеночных клеток и формирования синдрома эндогенной интоксикации [4, 5, 6]. Универсальным механизмом повреждения и гибели гепатоцитов является чрезмерная пероксидация мембранных структур, обусловленная выработкой свободных радикалов и, в первую очередь, активных форм кислорода [4].
Широкое участие свободнорадикальных процессов в патогенезе вирусных гепатитов ставит вопрос о необходимости коррекции нарушений фармакологическими средствами. В этих условиях для поддержания гомеостаза патогенетически обоснованным является введение лекарственных препаратов, способных тем или иным способом предотвращать избыточный синтез активных метаболитов кислорода, снижать чрезмерную интенсивность реакций перекисного окисления липидов (ПОЛ), а также способствовать повышению содержания или активности эндогенных антиоксидантов [1, 5]. Данными свойствами в полной мере обладают препараты, созданные на основе янтарной кислоты [2].
Целью работы была оценка эффектов комбинированного препарата ремаксол у больных ХГС в отношении параметров цитолиза, эндотоксикоза и липопероксидации.
Материалы и методы
Обследовано в динамике 80 больных с ХГС минимальной и умеренной активности, наивных в отношении противовирусной терапии. Диагноз ХГС устанавливался на основании обнаружения у пациентов антител к вирусу гепатита С (анти-HCV, ИФА) и детекции HCV-RNA методом ПЦР с определением генотипа вируса и вирусной нагрузки. Степень активности заболевания констатировалась по данным ультразвукового сканирования печени, выраженности и регулярности цитолитического синдрома, длительности заболевания, а также данным ряда других лабораторно-инструментальных методов.
В исследование включались больные ХГС, наивные в отношении противовирусной терапии, подписавшие информированное согласие, в возрасте 20-50 лет; при отсутствии тяжелых сопутствующих заболеваний внутренних органов, включая цирроз печени; уровне общего белка выше 65 г/л; альбуминов - больше 46 г/л; активности аланинаминотрансферазы (АлАТ) в пределах 100-300 ед/л (N 11-40 ед/л); концентрации щелочной фосфатазы (ЩФ) более 250 ед/л (N 117-140 ед/л); активности гаммаглютаматтранспептидазы (ГГТП) выше 100 ед/л (N 7-50 ед/л). Критерии исключения: отказ больного от участия в исследовании; цирроз печени; нарушение больным протокола исследования; беременность, период лактации; некомплаентность; ВИЧ-инфекция; онкологические заболевания; тяжелая соматическая патология в стадии суб- и декомпенсации; выявление у больных, получавших лечение нежелательных побочных реакций на препарат.
Рутинное биохимическое обследование подразумевало оценку параметров АлАТ, АсАТ, лактатдегидрогеназы (ЛДГ), ЩФ, ГГТП, фракций билирубина и др. на анализаторе HITACHI - 911. Показатели средних молекул (СрМ) исследовали методом Габриэлян Н.И. и Липатовой В.И. (1984), диеновых конъюгатов (ДК) - методом Гавриловой В.Б. и Мишкорудной М.И. (1983); малонового диальдегида (МДА) - методом Гончаренко М.С. и Латиновой А.М. (1985), активности супероксиддисмутазы (СОД) - по методике Fried R. (1975), активности каталазы - методом Дубининой Е.Е. с соавт. (1988), витамин Е - методом Черняускене Р.Ч. с соавт., (1984).
Больные подразделялись на 2 группы: в 1-й группе (49 человек) пациенты получали внутривенные инфузии ремаксола (400,0 мл) на протяжении 12 дней, во 2-ой группе (31 человек) - "активное плацебо" (400,0 мл) на протяжении 12 дней. Терапия ремаксолом проводилась до начала противовирусной терапии ХГС. Дизайн исследования: двойное слепое плацебо-контролируемое. Рандомизация исследования осуществлялась методом случайной выборки при включении больного в исследование. После окончания проведения метаболической терапии всем пациентам была назначена стандартная комбинированная противовирусная терапия, в соответствии с консенсусом по лечению ХГС [6]. Существенных различий по степени активности и этиологии гепатита (таблицы 1, 2), параметрами лабораторного обследования (таблицы 3, 4) до начала лечения между группами не было.
Таблица 1
Частота встречаемости различных генотипов вируса гепатита С в группах с различными методами терапии.
| Группы / Генотип | 1 группа (ремаксол) n=49 | 2 группа (плацебо) n=31 |
| 1b | 28,6% | 28,1% |
| 2а | 4,1% | 3,2% |
| 3а | 59,2% | 58,6% |
| 1b и 2a | 2,0% | 3,2% |
| Нетипируемый | 6,1% | 6,9% |
Таблица 2.
Степень активности ХГС в группах с различными методами терапии.
| Группы / Степень активности | 1 группа (ремаксол) n=49 | 2 группа (плацебо) n=31 |
| Минимальная | 14,7% | 15,6% |
| Умеренная | 85,3% | 84,4% |
Таблица 3
Динамика изменения биохимических показателей крови у больных ХГС в группах с различными методами терапии (M±m).
| Группы / Показатели | 1 группа (ремаксол) n=49 | 2 группа (плацебо) n=31 | ||
| 0 день | 13 день | 0 день | 13 день | |
| АлАТ, ед/л | 178,1±9,6* | 64,5±6,0** | 169,3±13,0 | 134,7±21,9 |
| АсАТ, ед/л | 147,2 ± 9,0* | 50,3 ± 4,7** | 141,2±13,8 | 109,8±22,7 |
| Общий билирубин, мкмоль/л | 26,6±1,3* | 15,1±0,4 | 25,5±1,5 | 21,8±4,3 |
| Прямой билирубин, мкмоль/л | 6,9±0,6* | 1,8±0,2** | 6,6 ± 0,6 | 5,8±2,3 |
| ЩФ, ед/л | 289,6±3,6* | 138,6±4,2** | 286,1±9,6* | 181,9±7,7 |
| ГГТП, ед/л | 231,5±6,0* | 64,2±4,5** | 233,8±11,2* | 132,6±11,9 |
| ЛДГ, ед/л | 581,2±9,3* | 390,5±11,5** | 574,1±27,5* | 507,5±26,1 |
Таблица 4
Показатели эндотоксикоза и липопероксидации у больных ХГС в группах с различными методами терапии (М±m).
| Группы / Показатели | Здоровые (n=15) | 1 группа (ремаксол) n=49 | 2 группа (контроль) n= 31 | ||
| 0 день | 13 день | 0 день | 13 день | ||
| Средние молекулы, опт. ед. | 0,26±0,01 | 0,62±0,01* | 0,35±0,01** | 0,61±0,02 | 0,50±0,03 |
| Диеновые конъюгаты, усл. ед. | 5,98±0,21 | 8,79±0,17* | 6,81±0,22** | 8,77±0,21 | 7,86±0,21 |
| Малоновый диальдегид, нмоль/мл | 2,82±0,12 | 6,23±0,08* | 3,37±0,16** | 6,24±0,13 | 5,23±0,14 |
| Активность супероксиддисмутазы, усл. ед. | 310,54±20,48 | 181,5±16,9* | 235,3±7,8** | 180,6±10,5 | 199,6±6,8 |
| Активность каталазы, МЕ?10 4 /мл | 5,89±0,31 | 2,93±0,26* | 4,06±0,12** | 2,88±0,23 | 3,43±0,14 |
| Вит. Е, усл. ед. | 5,39±0,23 | 2,12±0,25* | 3,89±0,12** | 2,13±0,18 | 2,56±0,09 |
Ремаксол является гепатопротектором, обладающим антигипоксическим, антиоксидантным, цитопротективным эффектами, которые опосредуются биологическими эффектами его активных компонентов: янтарной кислоты, рибоксина, никотинамида, метионина, натрия, калия, магния хлорида [2, 3].
Результаты и обсуждение.
При оценке выраженности цитолитических процессов до начала лечения у большинства больных ХГС регистрировалась умеренно выраженная активность с уровнем трансфераз от 3 до 7 норм и средние показатели составили в 1-й группе АлАТ - 178,1 ± 9,6 ед/л, АсАТ - 147,2 ± 9,0 ед/л, ЛДГ - 581,2 ± 9,3 ед/л, во 2-й группе 169,3 ± 13,0 , 141,2 ± 13,8 и 574,1 ± 27,5 - соответственно (таблица 3). Анализ полученных результатов после завершения курса терапии выявил существенное (p<0,05) снижение уровня АлАТ в основной (1-й) группе до 64,5 ± 6,0 ед/л, при этом различия со 2-й группой (134,7 ± 21,9) на 13-14 день были достоверными. По показателям АсАТ и ЛДГ прослеживалась аналогичная тенденция (таблица 3).
При оценке нарушений пигментного обмена до начала терапии у всех пациентов было отмечено повышение обеих фракций билирубина: в 1-й группе общий билирубин достигал значения 26,6 ± 1,3 мкмоль/л, прямой билирубин - 6,9 ± 0,6 мкмоль/л, во 2-й группе общий билирубин составил 25,5 ± 1,5 мкмоль/л, прямой билирубин - 6,6 ± 0,6 мкмоль/л. После проведенной терапии (таблица 3) у группы пациентов, получавших ремаксол, показатели обеих фракций билирубина нормализовались (15,1±0,4 и 1,8±0,2 мкмоль/л соответственно), тогда как в группе, получавшей плацебо, отмечалась лишь тенденция к снижению показателей билирубина (общий билирубин снизился до 21,8 ± 4,3 мкмоль/л, прямой -до 5,8 ± 2,3 мкмоль/л).
Кроме гипербилирубинемии оценивались такие показатели холестаза как ГГТП и ЩФ. В обеих группах пациентов до начала лечения отмечалось повышение уровня ГГТП: до 231,5±6,0 ед/л в 1-й группе и 233,8 ±11,2 ед/л - во 2-й. После окончания инфузионной терапии в 1-й группе (ремаксол) показатели ГГТП снизились в 3,6 раза, достигнув практически нормальных значений (64,2±4,5 ед/л), тогда как во 2-й группе (плацебо) они снизились лишь в 1,7 раза (до 132,6±11,9 ед/л). Уровень ЩФ и в 1-й и во 2-й группах значительно превышал нормальные показатели (289,6±3,6 и 286,1±9,6 ед/л соответственно). По окончании терапии у пациентов 1-й группы (ремаксол) данный показатель нормализовался, достигнув значения 138,6± ,2, тогда как во 2-й группе лишь наметилась тенденция к его снижению (181,9±7,7).
При исследовании процессов эндотоксикоза при ХГС было установлено значительное увеличение параметров СрМ: в 1-й группе до 0,62±0,01 опт. ед., во 2-й - до 0,61±0,02, на 13-14 день после проведенного лечения показатели снизились до 0,35±0,01 опт. ед в 1-й группе против 0,50±0,03 - во 2-й со статистически достоверными различиями между группами (таблица 4).
Отражали процессы эндогенной интоксикации при ХГС также повышенные уровени ДК, МДА: в 1-й группе показатель ДК составил 8,79±0,17 усл.ед., МДА - 6,23±0,08 нмоль/мл, во 2-й группе - 8,77±0,21, 6,24±0,13 соответственно (таблица 4). После проведенной инфузионной терапии в 1-й группе (ремаксол) отмечалось более выраженное уменьшение активности процессов липопероксидации (значение ДК составило 6,81±0,22 усл. ед., МДА - 3,37±0,16 нмоль/мл) по сравнению со 2-й группой (показатели достигли 7,86±0,21., 5,23±0,14 соответственно).
При оценке активности антиоксидантного статуса (АОС) до начала терапии в обеих группах отмечалось его угнетение, что проявлялось в снижении показателей активности СОД до 181,5±16,9 усл. ед. в 1-й группе и 180,6±10,5 - во 2-й, каталазы до 2,93±0,26 МЕх10 4 /мл и 2,88±0,23, витамина Е до 2,12±0,25 усл. ед. и 2,13±0,18 соответственно по сравнению с показателями здоровых людей (таблица 4). После окончания терапии в 1-й группе (ремаксол) отмечалась более выраженная положительная динамика параметров АОС: активность СОД увеличилась до 235,3±7,8 усл. ед. против 199,6±6,8 усл. ед. во 2-й группе, активность каталазы - до 4,06±0,12 МЕх10 4 /мл против 3,43±0,14 во 2-й группе и витамин Е до 3,89±0,12 усл. ед. против 2,56±0,09 усл.ед. во 2-й группе.
Таким образом, комплексная терапия больных ХГС с использованием курса инфузий ремаксола позволяет осуществлять последующее противовирусное лечение на исходно более благоприятном уровне метаболических процессов в организме и менее выраженной эндогенной интоксикации
Выводы
Использование комбинированного метаболического препарата ремаксол в комплексной терапии больных ХГС позволяет редуцировать процессы цитолиза гепатоцитов, уменьшить выраженность биохимических проявлений синдрома холестаза, нормализовать параметры пигментного обмена, снизить явления эндогенной интоксикации.
Система липопероксидации у больных ХГС на фоне использования метаболических средств, составляющих основу препарат ремаксол, демонстрирует существенное снижение окислительных процессов наряду с восстановлением ферментативного и неферментативного антиоксидантного потенциала крови, что свидетельствует о патогенетической направленности лечебных эффектов данного лекарственного средства.
1. Александрова Л.Н. Оценка гепатопротективной активности метаболической композиции на основе янтарной кислоты // Новые технологии в диагностике и лечении инфекционных болезней: VII Российский съезд инфекционистов.- Н.Новгород, 25-27 октября 2006.-С.239.
2. Ивницкий Ю. Ю. и др. Янтарная кислота в системе метаболической коррекции функционального состояния и резистентности организма. СПб., 1998. С. 82.
3. Кожока Т.Г. Лекарственные средства в фармакотерапии патологии клетки.- М.,-2007.-136с.
4. Новицкий Г.К. Актуальные вопросы инфекционной патологии / Г.К. Новицкий // Иркутск.- 1993.- №1.- С. 102-103.
5. Подымова С.Д. Болезни печени: Руководство для врачей. -3-е изд., перераб. и доп. - М.: Медицина, 1998. - 704 с.
6. Weigand K., Stremmel W., Encke J. Лечение HCV-инфекции // Клиническая гепатология - 2008 4(1) - С. .22-30.
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
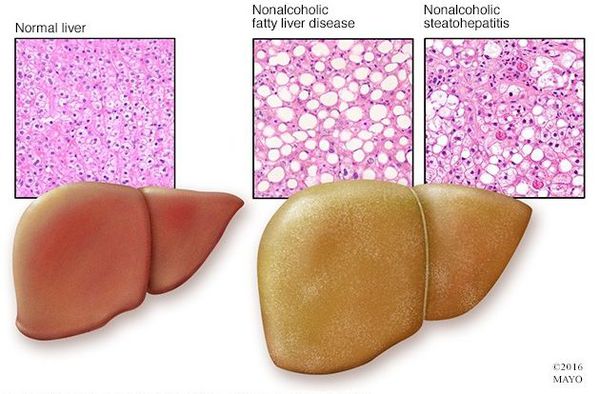
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
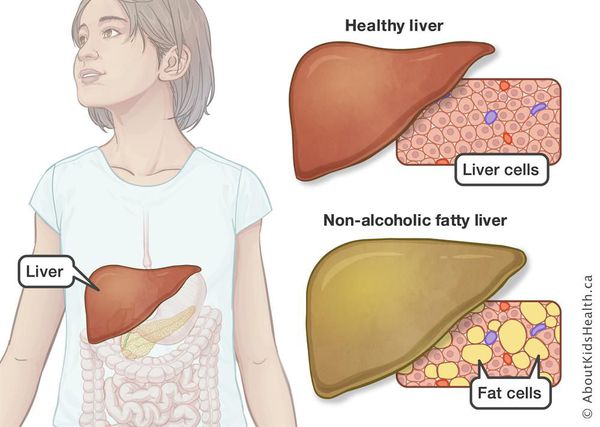
Все эти изменения неуклонно приводят к:
- разрушению клеток печени (неалкогольный стеатогепатит);
- накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
- изменению биохимического состава крови;
- развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
- в конечном итоге, циррозу.
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются: [11]
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ): ИМТ = вес (кг) : (рост (м)) 2 . Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3. Этот результат говорит об ожирении I степени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
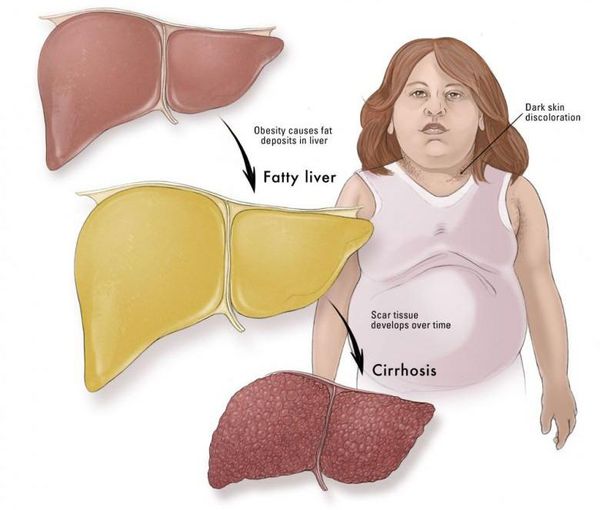
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности. [7]
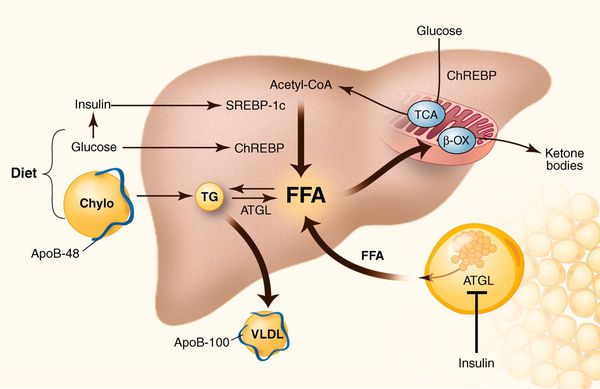
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу [9] , а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.
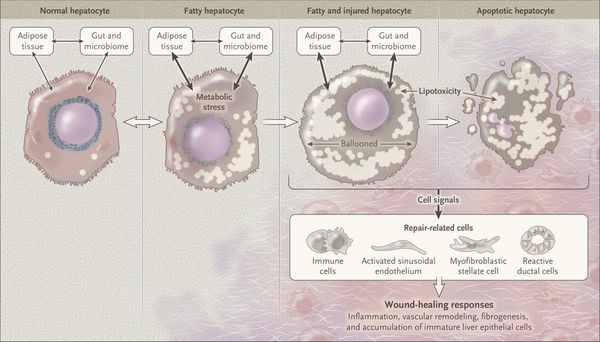
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
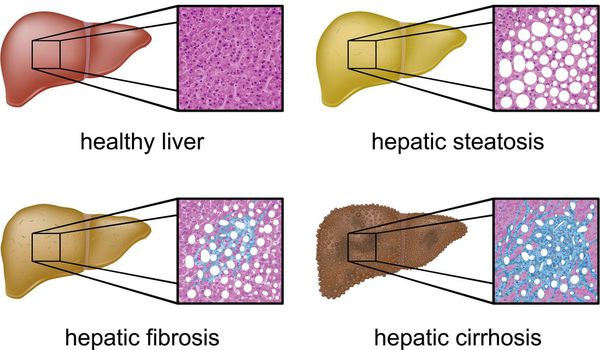
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
- I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
- II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
- III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
- S1 (до 33% жировой инфильтрации);
- S2 ( 33-60% жировой инфильтрации)
- S3 (более 60% жировой инфильтрации)
- F1,F2, F3, цирроз.
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
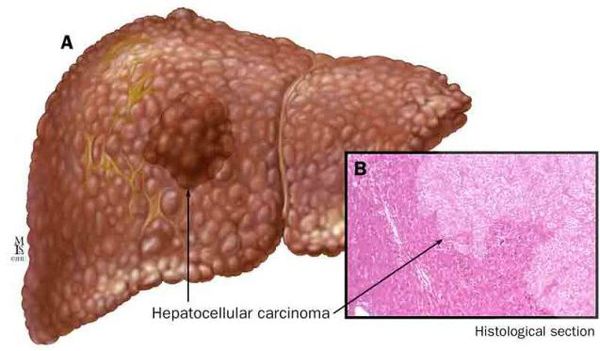
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ [4] , МСКТ, МРТ и эластометрии (FibroScan), при необходимости исследуется морфологическое состояние — биопсия печени. [3]
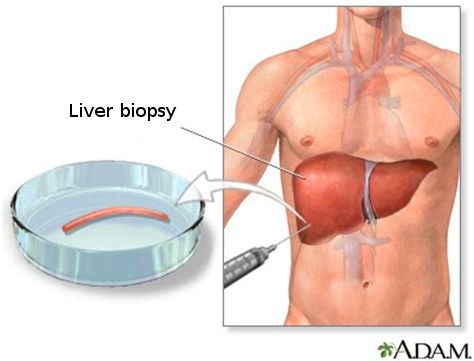
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
- коррекция углеводного, жирового (липидного) обмена веществ;
- нормализация процессов окисления в клетке;
- влияние на основные факторы риска;
- снижение массы тела;
- улучшение структуры печени на обратимых стадиях.
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
- инфузионная терапия с пролонгацией приёма препаратов внутрь, подбор диеты и физической активности;
- сдача контрольных анализов и оценка результатов.
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Читайте также:

