Миалгия при гепатите с
Обновлено: 12.05.2024
Описаны два случая аутоиммунного гепатита. В первом случае наличие симметричных артритов, высокого ревматоидного фактора послужило основанием для ошибочного диагноза ревматоидного артрита (РА). Гепатомегалия, повышение уровней аминотрансфераз и острофазовых показателей расценивались как системные проявления РА. Морфологическое исследование биоптата печени позволили верифицировать аутоиммунный гепатит. Во втором случае полиморфизм клинических проявлений привел к ошибочной диагностике смешанного заболевания соединительной ткани. Смерть больной наступила от кровотечения из варикозно расширенных вен пищевода. На аутопсии печени выявлена картина микро- и макронодуллярного цирроза печени.
Ключевые слова: аутоиммунный гепатит, ревматоидный артрит, смешанное заболевание соединительной ткани
Хронические диффузные заболевания печени (ХДЗП) любой этиологии часто сопровождаются внепеченочными (системными) проявлениями. Системные проявления иногда возникают задолго до клинически выраженного поражения печени, в то время как печеночные признаки впервые выявляются на стадии цирроза печени. ХДЗП в течение нескольких лет могут протекать под маской различных аутоиммунных заболеваний. Наибольшее разнообразие системных проявлений характерно для хронического аутоиммунного гепатита (ХАГ). В клинической практике ревматолога нередко встречаются "ревматологические" синдромы ХДЗП. Обсуждая эту проблему, считаем интересным привести следующие клинические наблюдения:
1. У больной К., 54 лет, в 44 года появились рецидивирующие нестойкие артриты мелких суставов кистей с ускорением СОЭ до 47 мм в час. На протяжении нескольких лет отмечались полинейропатии, слабость. Больная наблюдалась эндокринологом с диагнозом аутоиммунный тиреоидит. В дальнейшем развилась картина ревматоидоподобного артрита с выраженными экссудативными проявлениями со стороны мелких суставов кистей, коленных и голеностопных суставов. Полиартрит сопровождался лихорадкой до 38°С и кожным васкулитом с геморрагической петехиальной сыпью на голенях, эритематозными высыпаниями на туловище, ревматоидными узелками в затылочной области головы, а также увеличением печени (+ 4 см) и селезенки (+ 2 см). При лабораторном исследовании: СОЭ 62 мм в час, умеренная анемия (эритроциты 3,4х10 12 , гемоглобин 109 г/л), РФ 1:80 в реакции Ваалер-Роузе. Белковые фракции: общий белок 101,0 г/л, альбумины 15,2 г/л, глобулины 85,8 г/л (гамма-глобулины 56,5 г/л). В анализах мочи - изолированная протеинурия 0,066-0,165 г/л.
Увеличение печени и селезенки было расценено как гепатолиенальный синдром у больной с ревматоидным артритом (РА). Через месяц от начала лечения (нестероидными противовоспалительными и глюкокортикостероидными препаратами) полиартрит и васкулит купированы, сохранялись незначительные артралгии. В последующие годы наблюдалось несколько эпизодов лихорадки до 39°С по 7-10 дней, один из них сопровождался пневмонитом, прогрессировало похудание (потеря веса составила 25 кг), появился умеренный синдром Рейно, ксеростомия. Лабораторные данные: СОЭ до 56 мм в час, гипоальбуминемия до 14,9 г/л, гиперглобулинемия 79,5 г/л, гипер-гамма-глобулинемия 56,9 г/л, снижение протромбинового индекса до 50%. Трансаминазы: АлАТ 91,2, АсАТ 58,3 ед (N 40); билирубин 8,1 мкм/л, прямой - отр., непрямой - 8,1 мкм/л; щелочная фосфатаза 0,95-2,35, тимоловая проба 17,4-43,3 ед, HBsAg отр. Отмечалась высокая иммунологическая активность заболевания: ЦИК 440-542 ед.; РФ 1:640, положительный LE-тест.
Появление признаков печеночной недостаточности явилось основанием для детального обследования печени и верификации диагноза РА, тем более, что за 4 года признаки эрозивного артрита не прогрессировали. На ультразвуковом исследовании выявлено увеличение печени и селезенки, структура печени диффузно неоднородна; диаметр воротной вены 15 мм, селезеночной 8 мм. На сканограмме печени размеры ее увеличены, контуры неровные, накопление радионуклида неравномерное, в селезенке - резко повышено. При лапароскопическом исследовании: печень значительно увеличена, правая доля достигает уровня пупка, фиброз капсулы, селезенка занимает все левое подреберье. Париетальная брюшина с усиленным сосудистым рисунком. Проведенная биопсия печени выявила картину хронического аутоиммунного гепатита с начальными признаками цирроза. Гистологическое исследование: множество ступенчатых некрозов, обилие лимфоплазмоцитарных инфильтратов с преобладанием плазматических клеток, образующих на отдельных участках розетки. В портальных трактах сформированные лимфоидные фолликулы, макрофаги и фибробласты с развитием соединительной ткани, врастающей на отдельных участках в дольки, начало формирования "ложных долек".
Таким образом, ХАГ диагностирован у больной через 10 лет с момента появления первых признаков болезни. Длительное время заболевание печени протекало под маской различных ревматологических синдромов. Стало очевидным, что многочисленные системные проявления в виде ревматоидоподобного артрита, васкулита, полинейропатии, лихорадки, пневмонита, нефрита, тиреоидита, синдромов Рейно и Шегрена были аутоиммунными проявлениями хронического гепатита.
Клиническая картина указывала на системное заболевание соединительной ткани (СЗСТ), однако полиморфизм признаков не укладывался в рамки одной нозологической формы: отмечался нефрит с нефротическим синдромом и почечной недостаточностью, резко положительный LE-тест, "волчаночная" эритема, имелись проявления полимиозита, кожного и дигитального ангиита, явления склеродермо-подобного поражения кожи. Это явилось основанием для постановки диагноза смешанного заболевания соединительной ткани с признаками СКВ, ССД и дерматомиозита.
На проведение интенсивной терапии, включающей: 3 плазмафереза, 2 пульс-терапии (ПТ) метипредом в дозе 1000 и 750 мг, и пероральный прием преднизолона 60 мг/сут. больная отреагировала положительно: через 4 недели исчезли отеки, темная окраска кожи, кожный васкулит, прошли явления полимиозита и плевропневмонии, купирована лихорадка, нормализовалась СОЭ. На фоне удовлетворительного состояния у больной развился тубуло-интерстициальный компонент нефрита с полиурией (диурез 3-4,5 л в сутки) и полидипсией, депрессией удельного веса мочи (1001-1010). На фоне лечения преднизолоном через 2 недели диурез и удельный вес мочи восстановились, исчезла протеинурия. Больная была переведена на амбулаторное лечение. Через 3 месяца она прекратила прием преднизолона. Через год больная поступила в ревматологическое отделение с выраженной кахексией и гипотрофией мышц, иктеричностью кожи, асцитом, расширенной венозной сетью на коже живота и передней грудной стенке, увеличением печени (печень плотная, с острым краем выступала на 2 см ниже края реберной дуги). При обследовании: гемоглобин 101 г/л, эритроциты 2,8х10 12 ; билирубин 64,8 мкм/л, прямой - 35,1, непрямой - 29,7; АсАТ 0,85, АлАТ 0,40 мккат/л (N 0,06-0,14). HBsAg отр.; холестерин 6,6 ммоль/л, b-липопротеина 28 ед; белковые фракции: альбумины 12,8 г/л, глобулины 87,2 г/л, гамма-глобулины 59,5 г/л; протромбиновое время 50%; креатинин крови 0,15 ммоль/л. Анализ мочи без патологии.
При данной госпитализации не вызывало никаких сомнений наличие у больной цирроза печени с явлениями портальной гипертензии. Проведенная лапароскопия подтвердила данный диагноз: в брюшной полости определялась жидкость с желтовато-зеленым оттенком, печень у края реберной дуги серо-бурого цвета, поверхность неровная, множественные белесоватые образования от 0,5 до 1,0 см в диаметре. Глиссонова капсула с фиброзом по краю, спаечный процесс между диафрагмальной поверхностью печени и париетальной брюшиной. Серозный покров желудка, кишечника, большого сальника, париетальной брюшины с выраженным сосудистым рисунком.
Через полгода наступила смерть от кровотечения из варикозно-расширенных вен пищевода. Морфологические изменения печени на аутопсии соответствовали микро- и макронодуллярному циррозу печени умеренной степени активности: в печени наличие мелких и крупных "ложных долек", узлов-регенератов, выраженная диффузная крупнокапельная жировая дистрофия гепатоцитов, в портальных трактах лимфоцитарная инфильтрация с умеренной плазматизацией и формированием фолликулов, диффузная нейтрофильная инфильтрация. Имелось интенсивное разрастание грубо-волокнистой соединительной ткани со значительным утолщением серозных листков (брюшины в верхнем этаже брюшной полости, плевры и перикарда) с формированием множественных спаек.
Как выяснилось позже, больная более 10 лет страдала алкоголизмом, который привел к развитию алкогольного (мелкоузлового) цирроза печени, осложненного варикозным расширением вен пищевода и желудка, кровотечением и острой постгеморрагической анемией, явившейся непосредственной причиной смерти. Наличие на вскрытии смешанного микро-макронодуллярного цирроза печени с характерными морфологическими проявлениями указывает на аутоиммунный фактор в механизме повреждения печени.
Особенностью случая является поздняя диагностика ХДЗП, клинические проявления которого при первой госпитализации были вытеснены яркими внепеченочными аутоиммунными проявлениями, протекающими под маской ревматологических синдромов, что послужило основанием для постановки первичного диагноза СЗСТ.
ЛИТЕРАТУРА.
1. Апросина З.Г. Хронический активный гепатит как системное заболевание. М., Медицина, 1981.
2. Радченко В.Г., Шабров Л.В., Нечаев В.В. Аутоиммунный гепатит. Хр. заболевания печени. - С-Петербург, 2000, 66-68.
3. Подымова С.Д. Хр. аутоиммунный гепатит. Болезни печени. М., Медицина, 1993, 229-240.
4. Уэндс Дж. P., Кофф P.С., Иссельбахер К. Дж. Хр. гепатит. Вн. болезни под редакцией Е. Браунвальда и др., книга 7, 237-243.
5. Апросина З.Г. Аутоиммуиный гепатит. Рос. журн. гастроэнтерологии. 1998, VIII, 47-55.
6. Апросина З.Г. Аутоиммунный гепатит. Информационный бюллетень. 1998, 3-4 (4), 12-20.
Summary
Two case of autoimmune hepatitis are described. In the 1st case the presence of symmetrical arthritis, high rheumatoid factor led to erroneous diagnosis of rheumatoid arthritis (RA). Hepatomegalia, increasing of aminotransferase levels and acute phase indices were interpreted as systemic manifestations of RA. Morphologic studies of hepatic bioptates allowed us to verificate autoimmunic hepatitis. In the 2nd case polymorphism of clinical manifestations led to diagnosis of diffuse connective tissue disease. Lethal outcome in this patient was due to intestinal hemorrhage from varicose dilated essophageal veins. During autopsy of the liver the picture of micro- and macronodular hepatic cirrhosis was revealed.
Key words: autoimmunic hepatitis, rheumatoid arthritis, diffuse disease of connective tissue
Изучение хронических вирусных поражений печени выявило широкий спектр внепеченочных проявлений хронического гепатита В (ХГВ), а впоследствии, при открытии вируса гепатита С, и хронического гепатита С (ХГС). В России ведущая роль в изучении системности поражения при вирусных заболеваниях печени принадлежит исследованиям, проведенным в клинике им. Е.М.Тареева: изучение хронического активного гепатита как системного заболевания (Апросина З.Г., 1974, 1981 гг.), внепеченочных поражений при ХГС (Игнатова Т.М., 2000 г., Русских А.В., 2004 г., Милованова С.Ю., 2005 г., Карпов С.Ю., 2005 г.); при ХГВ (Ильянкова А.А., 2001 г., Абдурахманов Д.Т., 2003 г., Ибрагимова М.М., 2004 г., Крель П.Е., 1995 г., Тэгай С.В., 2003 г., Русских А.В., 2004 г.), поражения системы крови (Гусейнова Л.А., 1981 г.), легких (Дроздова А.С., 1989 г.), почек (Потапова А.В., 1989 г., Косминкова Е.Н., 1992 г.), синдрома Шегрена (Лопаткина Т.Н., 1980 г., Чернецова О.В., 2004 г.), системных васкулитов при вирусных гепатитах (Семенкова Е.Н., 1994).
В развитии внепеченочных поражений основное значение имеют иммунные реакции, возникающие в ответ на репликацию вирусов гепатита В или С в печени, в тканях лимфоидного и нелимфоидного происхождения. Предположения о наличии внепеченочных сайтов репликации вирусов гепатита В и С возникли в связи с наблюдением случаев быстро развивающегося острого гепатита у пациентов с вирусным циррозом печени после пересадки здоровой донорской печени. Инфицирование донорского органа у больных после ортотопической трансплантации печени объяснялось внепеченочной локализацией вирусов [1]. Помимо иммунных нарушений в возникновении системных поражений имеет значение прямое цитопатическое действие вирусов гепатита. Нередко внепеченочные поражения (ВПП) являются единственным проявлением вирусной инфекции и могут определять прогноз и тактику лечения заболевания.
Особенности хронического гепатита В с внепеченочными проявления гепатита
Внепеченочные проявления гепатита встречаются у 10-20% больных хроническим гепатитом В и включают широкий спектр поражений различных органов и систем [2]. Поражения кожи, наблюдаемые при острых и хронических болезнях печени, обусловленных HBV, весьма вариабельны и включают макулярные, макулопапулярные, папуловезикулярные высыпания, рецидивирующую крапивницу, петехии, пурпуру, узловатую эритему, скарлатиноподобную сыпь, гангренозную пиодермию, витилиго, гиперпигментацию и изъязвления в области нижних конечностей, аллергический капиллярит, пурпуру Шенлейна-Геноха 5.
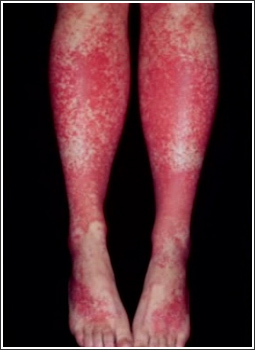
Смешанная криоглобулинемия (СКГ) встречается среди больных ХГВ в 3-17% случаев, может проявляться кожной пурпурой, артритами и/или артралгиями, поражением почек, синдромом Рейно [5, 6, 8, 9]. Поражение почек при ХГВ протекает в трех формах – хронический гломерулонефрит (ХГН), тубулоинтерстициальный нефрит (ТИН), в рамках васкулита при узелковом полиартериите, ассоциированном с HBVинфекцией 16. Частота поражения почек при ХГВ составляет 14%, в том числе ХГН – 12,6%, ТИН – 1,4% [11]. В клубочках выявляются депозиты различных антигенов HBV, включая HBsAg, HBeAg, HBcAg; у части больных в ткани почки была обнаружена HBV ДНК [13]. ИК могут активировать комплемент и вызывать поражение клубочков путем формирования мембраноатакующих комплексов и дальнейшего каскада реакций, таких как индукция протеаз, оксидативное повреждение и разрушение цитоскелета нефрона [14]. Узелковый полиартериит (УП) является системным васкулитом с поражением средних и мелких артерий. Циркулирующие ИК, содержащие вирусные белки, вовлекаются в патогенез УП, ассоциированного с HBV инфекцией [15]. По данным Е.Н. Семенковой, инфицирование вирусом гепатита В выявляется в 56,9% случаев УП. [16] Отмечено, что почти все случаи HBV-ассоциированного УП связаны с инфекцией вируса гепатита В дикого типа, характеризующейся HBe-антигенемией и высокой репликацией HBV. Предположительно повреждение почек происходят в результате отложения вирусных HBeAg-HBeAb ИК [15]. В целом, хроническая HBV-инфекция демонстрирует широкий спектр внепеченочных поражений, в генезе которых имеют значение как иммунокомплексные реакции, так и реакции гиперчувствительности замедленного типа.
Рис.1. Пурпура на коже нижних конечностей у больного хроническим гепатитом С
Внепеченочные проявления гепатита В могут длительно маскировать поражение печени, являясь ведущими клиническими проявления гепатита болезни и нередко определяющими прогноз заболевания. Однако, с введением программ массовой вакцинации против вируса гепатита В инфицированность населения начала снижаться. А после открытия в 1989 году вируса гепатита С все большее значение стало придаваться изучению обширного спектра поражений при этой инфекции.
Особенности хронического гепатита С с внепеченочными проявления гепатита
Согласно различным исследованиям, от 40 до 74% пациентов, инфицированных вирусом гепатита С, могут иметь хотя бы одно внепеченочное проявление (ВПП) за время течения болезни [17, 18, 19]. Более того, ВПП могут являться первым признаком HCV инфекции в отсутствии у ряда больных признаков поражения печени. Основной особенностью ХГС является частое развитие внепеченочных поражений преимущественно иммунокомплексного генеза, в первую очередь обусловленных смешанной криоглобулинемией (СКГ), выявляемой у 19-56% больных [18, 20, 21]. Только небольшая группа больных ХГС с СКГ (менее 15%) имеет симптомное течение – криоглобулинемический синдром [21, 22].
Распространенность смешанной криоглобулинемии увеличивается с длительностью HCV-инфекции в организме и продолжительностью заболевания и чаще наблюдается у женщин на 2-м-3-м десятилетии болезни. В некоторых исследованиях показано, что длительность HCV инфекции у больных ХГС со СКГ почти в 2 раза выше, чем у пациентов без СКГ, у 40% больных со СКГ выявляют признаки цирроза печени [20]. В настоящее время установлено, что вирус гепатита С имеет высокий тропизм к мононуклеарам периферической крови, которые могут служить его резервуаром и местом репликации. Вирус гепатита С связывается с лигандом CD81 на поверхности В-лимфоцитов через Е2-белок, что приводит к активации этих лимфоцитов. На первом этапе продуцируются только поликлональные криоглобулины, затем доминирующий клон В-клеток начинает продуцировать моноклональные иммуноглобулины. Смешанная криоглобулинемия является причиной системного васкулита с поражением сосудов мелкого и среднего калибра с возможным вовлечением в патологический процесс различных органов и систем [18, 23, 24]. Известно, что при ХГС васкулиты могут быть обусловлены не только СКГ, но и (со значительно меньшей частотой) – иммунными комплексами, не обладающими свойствами преципитировать на холоде, то есть не содержащими IgM РФ [18, 25, 26]. Поражение кожи чаще всего (95% случаев) представлено кожным васкулитом от пурпуры (лейкоцитокластический васкулит) и петехий на нижних конечностях (рис. 1) до выраженных некротических язв. Биопсия кожи в местах повреждений выявляет иммунокомплексный васкулит мелких сосудов с мононуклеарной инфильтрацией. HCV-антитела выявляются в кожных повреждениях в 40% случаев [19]. Пурпура у больных ХГС без СКГ характеризуется меньшей распространенностью и отсутствием язвенно-некротических изменений кожи по сравнению с больным со СКГ [27]. Синдром Рейно при ХГС часто является ранним клиническим проявлением КГ-синдрома, как правило, протекает без дигитальных некрозов. Однако, при высоком криокрите частота дигитальных некрозов увеличивается [10, 27]. Поражение мышц. Миалгии часто наблюдаются при ХГС, особенно в рамках КГ-синдрома в сочетании с артралгиями, кожным васкулитом.
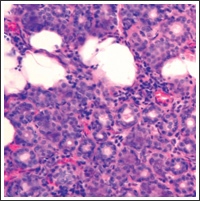
Рис. 2. Очаговая лимфоцитарная инфильтрация слюнной железы, характерная для синдрома Шегрена
По данным клиники им. Е.М.Тареева частота поражения легких была выше у больных без СКГ (11,3%), чем с КГ (6,3%). В группе пациентов без КГ поражение легких характеризовалось развитием фиброзирующего альвеолита, у больных с КГ наблюдалась картина легочного васкулита [27]. Поражение сердца. Имеются наблюдения миокардита хронического течения на фоне HCV-инфекции. Поражение миокарда, ассоциированное с HCV-инфекцией, может быть обусловлено: прямым (вирусным) воздействием на миокард; непрямым (иммунологическим) механизмом поражения и апоптозом клеток, обусловленным внутренними и внешними сигналами [34]. Имеются данные о прямом повреждающем действии на миокард core-белка вируса. Иммуноопосредованный путь повреждения миокарда осуществляется при участии В-клеток, Т-клеток и макрофагов. Обнаружение (+) и (-)-цепей HCV РНК в ткани миокарда у больных миокардитом, дилатационной миокардиопатией и (+)-цепи HCV РНК в миокарде больных гипертрофической кардиомиопатией, сочетающихся с HCV-инфекцией, позволяют обсуждать возможность репликации HCV в ткани миокарда. Обсуждается также роль реакций клеточного иммунитета на тканевые антигены вируса и индуцированные им аутоантигены, роль иммунных комплексов в патогенезе поражения миокарда. Кроме того, не исключается роль цитокинов (продуцируемых активированными вирусом иммуноцитами), которые через механизм повышения продукции оксида азота вызывают отрицательный инотропизм и повреждение сердечной мышцы [35].
Поражение суставов. Артралгии и/или артриты встречаются у 21-74% больных ХГС [19, 24]. Артриты при хронической HCV-инфекции могут рассматриваться как часть аутоиммунного процесса (например, в связи с криоглобулинемией) или как независимый процесс. Описано два вида поражения суставов: полиартрит мелких суставов, подобный ревматоидному артриту, который встречается очень редко и имеет мягкое течение; и неэрозивный олигоартрит с вовлечением средних и крупных суставов, часто интермиттирующего течения, как правило, связанный с криоглобулинемией. Ревматоидный фактор в сыворотке крови выявляется в 50-80% случаев. Антитела к циклическому цитруллиновому пептиду (АЦЦП) обнаруживаются менее, чем у 6% больных с HCV-ассоциированным артритом, что можно использовать для дифференциального диагноза ревматоидного артрита и поражения суставов в рамках HCV-инфекции [19]. Синдром Шегрена (СШ). У больных ХГС с высокой частотой (14-77%) выявляются морфологические признаки лимфоцитарного сиалоаденита и поражение слезных желез (у 26-50%).
Морфологические изменения малых слюнных желез характеризовались небольшой воспалительной инфильтрацией (рис. 2) и распространенным фиброзом ацинарной ткани [36, 37]. Клинически ксерофтальмия и ксеростомия имеют субклиническое течение у 73,8% больных, клинически очевидный СШ отмечается у больных ХГС с КГ [37]. Синдром Шегрена у больных является фактором риска развития злокачественной В-клеточной лимфомы, особенно при сочетании со СКГ [38]. Поражение щитовидной железы. Прямая связь между HCV-инфекцией и заболеванием щитовидной железы до конца не установлена, однако, поражение щитовидной железы (особенно гипотиреоз) чаще встречается среди больных ХГС, чем в общей популяции. У 13% больных, инфицированных HCV, выявляется гипотиреоз и у 25% обнаруживаются антитиреоидные антитела. В 30% случаев поражение щитовидной железы выявляется в ходе ПВТ. В связи с этим остается открытым вопрос, является ли нарушение функции щитовидной железы вирус-индуцированным или нежелательным эффектом противовирусной терапии. ПВТ, возможно, вызывает развитие нарушения функции щитовидной железы de novo или вызывает обострение уже существующего субклинического поражения щитовидной железы [39, 40].
Как и при ХГВ, внепеченочные проявления гепатита ХГС создают определенные трудности в дифференциальном диагнозе ХГС, определяя у части больных неблагоприятный прогноз криоглобулинемического васкулита, поражения почек, В-клеточной лимфомы. Особенности лечения хронических гепатитов В и С с системными проявления гепатита. Адекватный подход к лечению хронических вирусных гепатитов с внепеченочными проявлениями гепатита включает в себя две независимые, но тесно связанные цели. Первая – эрадикация вируса или снижение вирусной нагрузки с помощью этиотропной противовирусной терапии. Вторая – патогенетическое лечение аутоиммунных нарушений с использованием иммуносупрессивной терапии и/или плазмафереза с целью контроля образования иммунных комплексов. По мнению большинства исследователей, для лечения хронической HBV-инфекции оптимальна комбинированная терапия: использование препаратов, различающихся по механизму действия, – сочетание ИФН-? с аналогами нуклеоз(т)идов, сочетание нескольких аналогов нуклеоз(т)идов. Преимуществом интерферона-? является более низкая частота рецидивов после отмены препарата, а аналогов нуклеоз(т)идов – отсутствие нежелательных эффектов, в том числе иммуностимулирующего действия, что обусловливает его применение у больных с внепеченочными проявлениями гепатита и декомпенсированным циррозом печени. В ряде случаев при наличии миокардита, тубулоинтерстициального нефрита, полимиозита оправдано применение иммуносупрессивной терапии, несмотря на усиление репликации вируса гепатита В под влиянием стероидов [6,43-46]. Лечение ХГС со СКГ направлено на подавление вирусной репликации и угнетение В-клеточной пролиферации. Эрадикация HCV при противовирусной терапии приводит к исчезновению СКГ и регрессу клинических проявлений, но часть больных ХГС не отвечает на ПВТ, у ряда пациентов отмечаются выраженные нежелательные эффекты лечения. Применение кортикостероидов при хроническом вирусном гепатите с аутоиммунными нарушениями может приводить к увеличению вирусной нагрузки. В то же время, известно, что интерферонотерапия может вызывать ухудшение таких внепеченочных проявлений HCV-инфекции, как периферическая нейропатия, миокардит, тубуло-интерстициальный нефрит, полимиозит. Недавно было предложено использовать ритуксимаб (химерные моноклональные антитела к CD20) в качестве анти-В-клеточной терапии у больных ХГС с криоглобулинемией, не отвечающих на ПВТ [47, 48]. Его действие связано с быстрым, но обратимым, угнетением CD20+ В-клеток в периферической крови [49, 50]. Ряд исследований свидетельствуют об эффекте ритуксимаба у больных ХГС с периферической нейропатией и комбинации ритуксимаба и плазмафереза у больных ХГС с криоглобулинемическим васкулитом [47, 51], а также эффективность ритуксимаба и ПВТ у больных ХГС с КГ-гломерулонефритом и сосудистой пурпурой [23, 52]. Таким образом, лечение больных хроническими вирусными гепатитами с внепеченочными проявления гепатита не разработано, представляет серьезные проблемы и нуждается в дальнейшем изучении и выработке тактики.
Что такое гепатит А (болезнь Боткина)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вирусный гепатит А (Hepatitis A viruses, HAV) — острое инфекционное заболевание, вызываемое вирусом гепатита А, клинически характеризующееся синдромом общей инфекционной интоксикации, синдромом нарушения пигментного обмена, синдромами энтерита, холестаза, увеличением печени и в некоторых случая селезёнки, сопровождающееся нарушением функции печени, преимущественно доброкачественного течения.
Этиология
семейство — пикорнавирусы (Picornaviridae)
вид — вирус гепатита А (HAV)
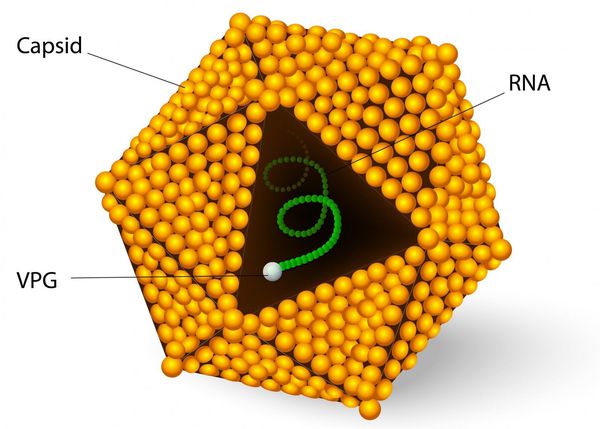
Во внешней среде очень устойчив: при температуре окружающей среды около 4°C сохраняется несколько месяцев, при 2°C — несколько лет, при замораживании очень длительно, при комнатной температуре — несколько недель. В растворе хлорсодержащих средств (0,5-1 мг/л) гибнет в течение часа, при 2,0-2,5 мг/л — в течение 15 минут, ультрафиолетовое облучение приводит к гибели в течение минуты, при кипячении сохраняется до 5 минут. В кислой среде желудка не погибает.
Наиболее значимым маркером вирусного гепатита А являются антитела класса М (анти-HAV IgM), которые образуются в начальный период заболевания и выявляются до 5 месяцев. Появление анти-HAV IgG (маркера перенесённой ранее инфекции) начинается с 3-4 недели заболевания. Антиген вируса выявляется в каловых массах за 7-10 дней до начала манифестных (явно выраженных) проявлений болезни. [1] [2] [4]
Эпидемиология
Заражение гепатитом А происходит при контакте с источником инфекции — живым человеком (больной различными формами заболевания и вирусоноситель). Больные с типичными формами являются главным источником распространения вируса (от конца скрытого и всего желтушного периодов).
Ежегодно в мире регистрируется примерно 1,5 млн случаев заболевания (количество субклинических и бессимптомных форм сложно даже представить). Смертность по миру в 2016 г., по данным ВОЗ, составила 7134 человек [10] .
Условно существует территориальное распределение по уровням инфицирования населения: высокий, средний и низкий.
Районы с высоким уровнем инфицирования это преимущественно Юго-Восточная Азия, Средняя Азия, Африка, Центральная Америка (плохие санитарные условия и низкий доход) — большинство населения к периоду взросления уже переболели и имеют иммунитет, вспышки болезни встречаются редко.
Районы со средним уровнем инфицирования — страны с переходной экономикой, развивающиеся, имеющие различия в санитарно-гигиенических условиях на территории одного региона, например Россия (большая часть населения к периоду взросления не болела и не имеет иммунитета к вирусу, возможны большие вспышки болезни).
Районы с низким уровнем инфицирования — развитые страны с высоким уровнем дохода и хорошими санитарно-гигиеническими условиями, например США, Канада, Европа, Австралия. Большинство людей не имеет иммунитета и не болела, вспышки случаются редко и чаще среди групп риска [7] .
В окружающую среду вирус выделяется преимущественно с фекалиями.
Механизм передачи: фекально-оральный (пути — водный, контактно-бытовой, пищевой), парентеральный (редко при переливании крови), половой (орально-анальный контакт).
Восприимчивость населения высокая.
Факторы риска заражения:
- высокая скученность населения;
- несоблюдение правил личной гигиены и правил хранения, обработки и приготовления продуктов питания;
- неудовлетворительное состояние объектов водоснабжения;
- бытовой очаг заболевания.
Кто находится в группе риска
- путешественники (особенно в страны жаркого климата и с плохими социальными условиями);
- гомосексуалисты;
- люди, употребляющие наркотики (любые), алкоголики;
- медработники (непривитые и не болевшие);
- бездомные;
- люди, имеющие постоянные контакты (в силу профессии или иных причин) с мигрантами из неблагополучных по гепатиту А регионов.
Характерна осенне-весенняя сезонность, повышенная привязанность к жарким южным регионам.
Иммунитет после перенесённого заболевания стойкий, пожизненный, то есть повторно заболеть нельзя [1] [3] [4] [7] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы гепатита А
Заболевание начинается постепенно. Инкубационный период гепатита А протекает 7-50 дней.
Синдромы вирусного гепатита А:
- общей инфекционной интоксикации;
- нарушения пигментного обмена (желтуха);
- энтерита (воспаление слизистой тонкой кишки);
- холестаза (уменьшение количества желчи, поступающей в двенадцатиперстную кишку);
- гепатолиенальный (увеличение печени и селезёнки);
- отёчный;
- нарушения функции печени.
Типичное течение болезни — это желтушная форма болезни средней степени тяжести (устаревшее название — желтуха или болезнь Боткина).
Начальный период болезни (преджелтушный) имеет продолжительность от 2 до 15 дней и может протекать по нескольким вариантам:
При осмотре обнаруживается увеличение печени и, в меньшей степени, селезёнки, чувствительность края печени, повышение ЧСС (пульса), носовые кровотечения. В конце периода моча темнее, а кал становится светлее.
Следующий период (желтушный) длительностью около 7-15 дней характеризуется снижением выраженности симптомов предшествующего периода (то есть с появлением желтухи самочувствие улучшается). Усиливается желтушное окрашивание склер, кожных покровов и слизистой оболочки ротоглотки. Моча приобретает цвет тёмного пива, кал белеет. Присутствует общая слабость, недомогание, плохой аппетит, чувство тяжести и переполненности в правом подреберье, больной расчёсывает себя из-за зуда кожи (лихенификация), появляются петехии (мелкие кровоизлияния) на коже.
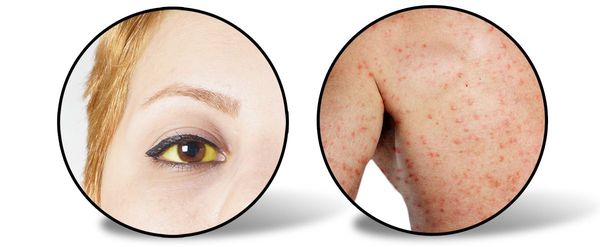
При врачебном исследовании выявляется увеличение печени и селезёнки, явственно положителен симптом Ортнера (болезненность при поколачивании ребром ладони по правой рёберной дуге), гипотония (может быть и нормотония), токсическая брадикардия (снижение ЧСС), появляются периферические отёки, возможны боли в суставах (артралгии).
Далее при благоприятном течении заболевания (которое наблюдается в большинстве случаев) происходит регресс клинической симптоматики, осветление мочи и потемнение кала, более медленное спадение желтушности кожи, склер и слизистых оболочек.
Под нетипичным течением болезни подразумеваются лёгкие безжелтушные формы гепатита А (отсутствие симптомов или лёгкая слабость без желтухи, тяжесть в правом подреберье), фульминантные формы.
Факторы, увеличивающие риск тяжёлого течения гепатита А:
Последствия для беременных
У беременных гепатит А протекает в целом несколько тяжелее, чем у небеременных. Примерно в 36 % случаев возможно развитие слабости родовой деятельности, преждевременные роды (31-37 неделя) и послеродовые кровотечения. Вирус не проникает через плаценту, то есть какого-то специфического действия на плод не оказывает. В грудном молоке вирус не содержится [1] [2] [4] [7] .
Патогенез гепатита А
Воротами для проникновения вируса является слизистая оболочка органов желудочно-кишечного тракта, где происходит его первичное размножение в эндотелиальной выстилке тонкого кишечника и мезентериальных лимфоузлах.
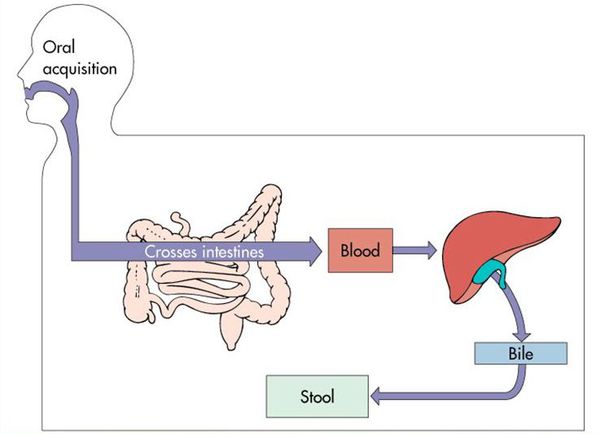
Далее происходит гематогенное распространение вирусных частиц и проникновение их в печень, где они локализуются в ретикулогистиоцитарных клетках Купфера и гепатоцитах. В результате этого происходит повреждение клеток:
- проникновение вируса в клетку;
- захват лизосомой;
- разрушение белковой оболочки вируса;
- сборка белков по программе вирусной РНК;
- встраивание этих белков в цитолемму клетки;
- образование патологических пор в оболочке клетки;
- поступление внутрь клетки ионов натрия и воды;
- баллонная дистрофия (разрушение ультраструктур клетки и образование крупных вакуолей) с последующим некрозом (его объём, как правило, ограничен);
- гибель клетки и лимфоцитарная иммунная реакция, приводящая к основному объёму поражения.
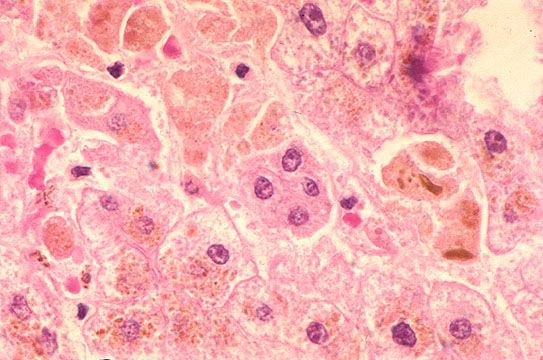
В дальнейшем вирус попадает в желчь, с ней он проникает в кишечник и выводится в окружающую среду с фекалиями. Вследствие компетентных реакций иммунной защиты размножение вируса заканчивается, и он покидает организм больного. [2] [3] [4]
Классификация и стадии развития гепатита А
По степени разнообразия проявлений выделяют две формы гепатита А:
- клинически выраженная (желтушная, безжелтушная, стёртая);
- субклиническая (инаппарантная).
По длительности течения также выделяют две формы гепатита А:
- острая циклическая (до трёх месяцев);
- острая затяжная (более трёх месяцев).
Степени тяжести гепатита А:
- лёгкая;
- среднетяжёлая;
- тяжёлая;
- фульминатная (молниеносная).
Согласно МКБ-10 (Международной классификации болезней десятого пересмотра), заболевание подразделяют на три вида:
- В15. Острый гепатит А;
- В15.0. Гепатит А с печёночной комой;
- В15.9. Гепатит А без печёночной комы. [2][4]
Осложнения гепатита А
Заболевание может привести к следующим осложнениям:
- печёночная кома (дисфункция центральной нервной системы, связанная с тяжёлым поражением печени — встречается крайне редко);
- холецистохолангит (выраженные боли в правом подреберье, нарастание желтухи и зуда кожи);
- гемолитико-уремический синдром, преимущественно у детей (гемолитическая анемия, тромбоцитопения, острая почечная недостаточность);
- развитие аутоиммунного гепатита I типа.
Гепатит А не приводит к формированию хронических форм, однако из-за выраженного воспалительного процесса возможно появление длительных резидуальных (остаточных) явлений:
- дискинезия (нарушение моторики) желчевыводящих путей;
- постгепатитная гепатомегалия (увеличение размеров печени из-за разрастания соединительной ткани);
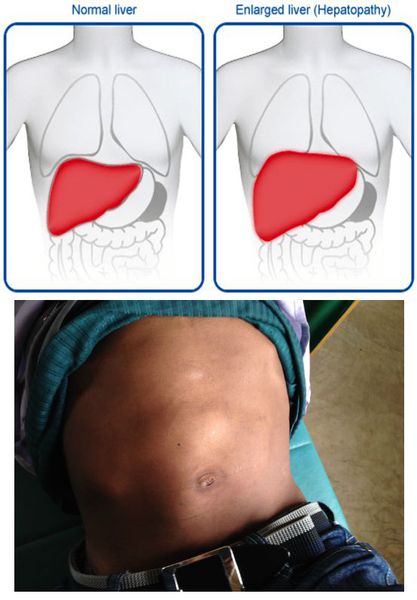
- постгепатитный синдром (повышенная утомляемость, аснено-невротические проявления, тошнота, дискомфорт в правом подреберье). [1][5]
Диагностика гепатита А
Методы лабораторной диагностики:
- Клинический анализ крови — нормоцитоз или лейкопения, лимфо- и моноцитоз, нейтропения, СОЭ в норме или снижена.
- Биохимический анализ крови — повышение общего билирубина и в большей степени его связанной фракции (реакция Эрлиха), повышение аланинаминотрансферазы и аспартатаминотрансферазы, снижение протромбинового индекса, повышение тимоловой пробы (снижение альбуминов и повышение гамма-глобулинов), повышение гамма-глутамилтранспептидазы, щелочной фосфатазы и другие показатели.
- Биохимический анализ мочи — появление уробилина и желчных пигментов за счёт прямого билирубина. Ранее, особенно в вооруженных силах, для выявления больных на начальной стадии практиковалось использование пробы Разина: утром производится опускание индикаторной полоски в мочу (при наличии уробилина она меняет цвет), и военнослужащий с подозрением на заболевание госпитализировался для углублённого обследования. Тест на уробилин становится положительным в самом начале заболевания — в конце инкубационного периода из-за болезни печёночной клетки.
- Серологические тесты — выявления анти-HAV IgM и анти-HAV IgG методом ИФА (иммуноферментного анализа) в различные периоды заболевания и HAV RNA с помощью ПЦР-диагностики (полимеразной цепной реакции) в острый период.
- Ультразвуковое исследование органов брюшной полости — увеличение печени и иногда селезёнки, реактивные изменения структуры печёночной ткани, лимфаденопатия ворот печени.
Обследование лиц, бывших в контакте с больным
Лица, контактирующие с больным вирусным гепатитом А, подлежат осмотру врачом-инфекционистом с последующим наблюдением до 35 дней со дня разобщения с больным. Наблюдение включает термометрию, осмотр кожных покровов, определение размеров печени и селезёнки, а также лабораторное обследование (АЛТ, общий билирубин, антитела классов М и G к вирусу гепатита А вначале и через три недели от первичного обследования).
Дифференциальная диагностика проводится со следующими основными заболеваниями:
- в начальный период: ;
- гастрит, гастроэнтероколит;
- полиартрит;
- энтеровирусная инфекция;
- в желтушный период: ;
- псевдотуберкулёз; ;
- желтухи другой этиологии (гемолитическая болезнь, токсические поражения, опухоли ЖКТ и другие заболевания);
- гепатиты другой этиологии (вирусные гепатиты В, С, Д, Е и другие, аутоиммунные гепатиты, болезнь Вильсона — Коновалова и т.п.) [1][2][3][4][9] .
Лечение гепатита А
Этиотропная терапия (направленная на устранение причины заболевания) не разработана.
Медикаменты
В зависимости от степени тяжести и конкретных проявлений назначается инфузионная терапия с глюкозо-солевыми растворами, обогащёнными витаминами. Показано назначение сорбентов, препаратов повышения энергетических ресурсов, при необходимости назначаются гепатопротекторы, в тяжёлых случаях — гормональные препараты, препараты крови, гипербарическая оксигенация и плазмаферез.
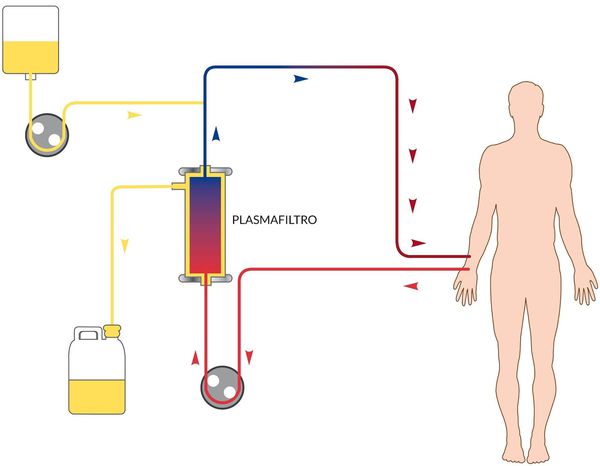
Нужна ли госпитализация
В случае лёгких форм гепатита А лечение может проводиться на дому (при наличии условий). Госпитализация потребуется, начиная со среднетяжёлых форм, лицам групп риска по тяжёлому течению, пациентам с осложнёнными формами, беременным и детям. Каких-либо особенностей при дальнейшем лечении вирусного гепатита А у детей нет.
Режим постельный или полупостельный. При гепатите А нарушаются процессы образования энергии в митохондриях, поэтому предпочтителен длительный отдых.
Лечение в стационаре и выписка
Лечение гепатита А проходит в инфекционном отделении больницы. Выписка пациентов происходит после появления стойкой и выраженной тенденции к клиническому улучшению, а также улучшения лабораторных показателей.
Критерии выписки больных:
- стойкая и выраженная тенденция к клиническому улучшению (отсутствие интоксикации, уменьшение размеров печени, регресс желтухи);
- стабильное улучшение лабораторных показателей (нормализация уровня билирубина, значительное снижение уровня АЛТ и АСТ).
При неосложнённых формах реконвалесценты (выздоравливающие больные) подлежат наблюдению в течении трёх месяцев с осмотром и обследованием не реже одного раза в месяц. [2] [3] [6]
Физиотерапия
В фазе реконвалесценции, особенно при затяжных формах болезни, возможно применение физиотерапевтических методов лечения:
- грязевых аппликаций на область правого подреберья;
- акупунктуры;
- массажа проекции области печени, желчного пузыря, желчевыводящих протоков.
Диета
Показана диета № 5 по Певзнеру — механически и химически щадящая, употребление повышенного количества жидкости и витаминов, запрет алкоголя. Исключается острое, жареное, копчёное, ограничивается кислое и соль. Все блюда готовятся на пару, тушатся, отвариваются и подаются только в тёплом виде.
Прогноз. Профилактика
Прогноз заболевания, как правило, благоприятный. Пациенты выздоравливают спустя 1-3 месяца после выписки из стационара. В редких случаях заболевание приобретает затяжной характер.
Критерии излеченности:
- отсутствие интоксикации;
- полная нормализация уровня билирубина, АЛТ и АСТ;
- нормализация размеров печени и селезёнки;
- появление в крови антител к вирусу гепатита А класса G (Anti-HAV-IgG).
Неспецифические мероприятия, позволяющие снизить количество случаев инфицирования:
- обеспечение условий и факторов потребления безопасной питьевой воды (водоснабжение);
- обеспечение и контроль за соблюдением утилизации сточных вод (канализационное хозяйство);
- контроль за качеством обследования персонала, связанного с пищевой промышленностью;
- контроль и соблюдение технологии хранения, приготовления и транспортировки пищевых продуктов и воды.
К личным профилактическим мерам относится тщательное мытьё рук после посещения туалета, смены подгузников, а также перед приготовлением или приёмом пищи.
Вакцинация
Специфическим профилактическим мероприятием является проведение иммунизации против гепатита А: практически у 100% привитых двукратно людей вырабатывается стойкий иммунитет, предотвращающий развитие заболевания. Вакцинация — это самый лучший способ предотвратить заражение.
HCV-инфекция представляется в настоящее время одной из актуальных проблем общественного здравоохранения в связи с ее распространенностью в популяции, высокой частотой формирования цирроза печени и гепатоцеллюлярной карциномы, развитием внепеченочных проявлений, определяющих трудности диагностики заболевания и его лечения. Вирус гепатита С является причиной 20% всех случаев острого гепатита, а хроническая HCV-инфекция ответственна за развитие 70% случаев хронического гепатита, 40% всех наблюдений терминального цирроза печени, 60% гепатоцеллюлярной карциномы и в 30% является причиной направления пациента на трансплантацию печени.
Отличительной особенностью вируса гепатита С является его значительная изменчивость с образованием множества одновременно существующих, иммунологически различающихся антигенных вариантов, обладающих значительными возможностями адаптации и способностью избегать иммунную систему хозяина.
В патогенезе поражения органов при HCV-инфекции обсуждаются прямой цитопатический эффект вируса и вызванные им иммунологические реакции, обуславливающие повреждение печени и других органов и тканей: репликация вируса вне печени - в тканях лимфоидного и нелимфоидного происхождения. Размножение вируса в иммуно-компетентных клетках (лимфоцитах) приводит к нарушению их иммунологической функции.
Для диагностики HCV-инфекции используются иммуноферментный метод (ELISA) и рекомбинантный иммуноблоттинг (RIBA) 1, 2, 3-го поколений, а также полимеразная цепная реакция - PCR.
Основным методом диагностики хронического гепатита С является морфологическое исследование печени, позволяющее уточнить стадию (наличие цирроза) и активность процесса, не всегда коррелирующую с уровнем трансаминаз и гаммаглобулинов сыворотки крови. Применение методов молекулярной биологии, исследование HCV РНК в ткани печени и других органов позволяют приблизиться к пониманию патогенеза острой и хронической HCV-инфекции.
Персистирование HCV дает широкий спектр клинико-морфологических вариантов: от стойких признаков активного заболевания и продолжающегося повреждения печени с развитием в дальнейшем клиники многосистемного страдания до состояния клинического выздоровления (от острой инфекции) с очень низким уровнем вирусной репликации и непрогрессирующим характером гистологических изменений.
Особенности течения хронического гепатита С определяются, наряду с уровнем виремии, генотипом вируса, дополнительными факторами, повреждающими печень: наличием двойной, тройной вирусной инфекции (HBV, HDV, вирусы герпесгруппы), злоупотреблением алкоголем, приемом ряда лекарств, вызывающих повреждение печени. Особый интерес представляют варианты хронического гепатита С с нормальным уровнем аланиновой и аспарагиновой аминотрансфераз в сыворотке крови. При данной форме гепатита не выявляется корреляция с уровнем виремии и генотипом HCV, в гистологической картине преобладают минимальная или умеренная активность процесса, дискутабельным остается вопрос о лечении подобных вариантов поражения печени.
У 40-45% больных наряду с печеночными проявлениями наблюдаются разнообразные внепеченочные проявления (табл.), нередко выходящие на первый план в клинической картине и в ряде случаев определяющие прогноз заболевания.
Таблица. Внепеченочные проявления хронической HCV-инфекции (1)
| Эндокринные | Гипертиреоз Гипотиреоз Тиреоидит Хашимото Сахарный диабет |
| Гематологические | Смешанная криоглобулинемия Идиопатическая тромбоцитопения Неходжкинская В-лимфома* Макроглобулинемия Вальденстрема Апластическая анемия |
| Поражение слюнных желез и глаз | Лимфоцитарный сиалоаденит* Язвы роговицы Mooren Увеит |
| Кожные | Кожный некротизирующий васкулит* Поздняя кожная порфирия Красный плоский лишай Мультиформная эритема* Узловатая эритема* Малакоплакия Крапивница* |
| Нейромышечные и суставные | Миопатический синдром* Периферическая полинейропатия* Синдром Гийена-Барре Артриты, артралгии* |
| Почечные | Гломерулонефрит* |
| Аутоиммунные и другие | Узелковый периартериит Интерстициальный легочный фиброз* Легочный васкулит* Гипертрофическая кардиомиопатия CRST-синдром Антифосфолипидный синдром Аутоиммунный гепатит 1 и 2 типа Синдром Бехчета Дерматомиозит |
Статистический анализ позволяет считать доказанной связь с хронической HCV-инфекцией таких внепеченочных проявлений, как смешанная криоглобулинемия, мембранопролиферативный гломерулонефрит, поздняя кожная порфирия, аутоиммунный тиреоидит. Предположительной считается связь HCV-инфекции с идиопатической тромбоцитопенией, красным плоским лишаем, язвами роговицы Mooren, синдромом Шегрена (лимфоцитарным сиалоаденитом) и В-клеточной лимфомой. В отношении других внепеченочных проявлений нет доказательств их тесной взаимосвязи с HCV-инфекцией, однако необходимы дальнейшие исследования, которые позволят, по-видимому, дополнить представленный перечень.
Из внепеченочных проявлений ХГС смешанная криоглобулинемия обнаруживается наиболее часто, особенно у женщин среднего и пожилого возраста с длительно текущей инфекцией (в среднем в течение 10,7 лет), при наличии цирроза печени. В зависимости от диагностических методов криоглобулинемия выявляется у 42-96% больных. У 10-42% больных имеются клинические проявления криоглобулинемии: слабость, артралгии, пурпура, периферическая полинейропатия, синдром Рейно, артериальная гипертония, поражение почек. В составе криопреципитатов выявляют HCV РНК и lgG anti-HCV к структурным и неструктурным белкам HCV (core, E2/NS1, NS3, NS4, NS5), lgM anti-HCV к core-белку; С3-фракцию комплемента. Концентрация HCV РНК в криопреципитатах в 103-105 раз выше, чем в сыворотке. HCV РНК при криоглобулинемии выявляется также в костном мозге, мононуклеарах периферической крови, кератиноцитах, эпителии протоков и эндотелиоцитах. Ряд больных с клиническими признаками криоглобулинемии имеют минимальные гистологические признаки поражения печени. Роль HCV-инфекции в развитии криоглобулинемии подтверждается исчезновением клинических проявлений криоглобулинемии в результате противовирусной терапии интерфероном альфа.
Идиопатическая тромбоцитопения, возможно, обусловлена HCV-инфекцией в большей части случаев, чем считалось ранее.
Сиалоаденит встречается у 14-57% больных ХГС, однако в большинстве случаев типичная картина синдрома Шегрена (клинические, гистологические признаки, серологические маркеры) отсутствует.
Разнообразные поражения кожи описаны в сочетании с ХГС, из них кожный некротизирующий васкулит с папулезными или петехиальными высыпаниями, обусловленный отложением криоглобулинов, наиболее четко ассоциирован с HCV-инфекцией. Несмотря на то, что HCV РНК выявляется в коже и кератиноцитах, в патогенезе некротизирующего васкулита рассматривается больше роль криоглобулинемии, чем репликации вируса в стенке сосудов.
Нейромышечные и суставные внепеченочные проявления хронической HCV-инфекции разнообразны и в большинстве случаев обусловлены криоглобулинемией. Мышечная слабость, миопатический синдром, миалгии, единичные наблюдения миастении упоминаются в связи с ХГС. В дебюте ОВГС описан синдром Гийена-Барре, но чаще хроническая HCV-инфекция сочетается с периферической полинейропатией в рамках криоглобулинемии.
Системность поражения, наблюдаемая при HCV-инфекции, отражает генерализованный характер гепатита С с вовлечением в патологический процесс многих органов и тканей, что затрудняет своевременную диагностику и лечение хронического гепатита.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Гепатит С: причины появления, классификация, симптомы, диагностика и способы лечения.
Определение
Гепатит С – это вирусное инфекционное заболевание, которое вызывает воспаление печени, зачастую приводя к ее серьезным повреждениям. Вирус гепатита С распространяется через зараженную кровь.
До недавнего времени лечение гепатита С требовало еженедельных инъекций и приема пероральных препаратов, которые многие люди, инфицированные вирусом, не могли использовать из-за других проблем со здоровьем или серьезных побочных эффектов.
Сегодня ситуация изменилась – разработаны лекарства нового поколения, и с их помощью хронический гепатит С поддается терапии.
Тем не менее около половины людей с гепатитом С не подозревают о том, что инфицированы, поскольку часто болезнь протекает бессимптомно.
Поэтому скрининг гепатита С необходимо проходить регулярно, особенно при наличии факторов риска заражения.
Причины появления гепатита С
Заболевание обычно распространяется, когда кровь человека, зараженного вирусом гепатита С, попадает в организм незараженного. Особенно часто это происходит в среде наркоманов.
В группе риска находятся люди, которым часто переливают кровь, и длительное время находящиеся на гемодиализе.
Заражению подвержены новорожденные дети, если их мать больна гепатитом С.
Кроме того, существуют редкие, но все же возможные ситуации инфицирования вирусом:
- Совместное использование предметов личной гигиены, которые могли соприкасаться с кровью больного человека (бритвы, ножницы или зубные щетки).
- Половой контакт с человеком, зараженным вирусом гепатита С.
- Татуировки или пирсинг, выполненные в ненадлежащих санитарных условиях.
Вирус гепатита С не передается при совместном использовании столовых приборов, кормлении грудью, объятиях, поцелуях, при держании за руку, кашле или чихании, через укусы насекомых. Также он не распространяется через еду или воду.
- Острый гепатит С – это ранняя стадия, когда гепатит длится менее шести месяцев.
- Хронический гепатит С – это долгосрочный тип, когда заболевание длится больше шести месяцев.
- Минимальная активность (печеночные трансаминазы (АЛТ и АСТ) в биохимическом анализе крови повышены не более, чем на 3 нормы)).
- Умеренная активность (3–10 норм печеночных трансаминаз).
- Высокая активность (> 10 норм).
В течение первых 6 месяцев от начала заболевания человек может даже не подозревать, что болен, ощущая лишь необъяснимую усталость, плохой аппетит, тяжесть в правом подреберье, регулярную головную боль и головокружение.
В этот же период может меняться цвет кала (от светлого вплоть до белого) и мочи (от темно-желтой до коричневой). Некоторые пациенты говорят, что у них болят суставы.
По мере прогрессирования заболевания к первоначальным симптомам присоединяются спонтанные кровотечения (носовые, маточные, кровотечения из десен), желтушность кожных покровов, склонность к образованию гематом, зуд, накопление свободной жидкости в брюшной полости (асцит), отеки ног. Кроме того, пациенты начинают терять вес, снижается память, появляются проблемы со зрением, на коже формируются сосудистые звездочки.
У мужчин может отмечаться гинекомастия (увеличение грудных желез), снижение либидо, уменьшение размера яичек.
Симптомы острого гепатита С включают желтуху, усталость, тошноту, жар и мышечные боли. Они появляются через 1-3 месяца после инфицирования вирусом и продолжаются от двух недель до трех месяцев.
Диагностика гепатита С
Диагноз ставится на основании жалоб больного и анамнеза. При подозрении на вирусный гепатит С врач обязательно выясняет, были ли в течение жизни переливания крови, хирургические манипуляции, не употреблял ли пациент инъекционные наркотики, делал ли татуировки и пирсинг, имели ли место незащищенные половые контакты.
Для уточнения диагноза могут понадобиться следующие обследования:
-
Клинический анализ крови с развернутой лейкоцитарной формулой.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Читайте также:

