Микст инфекция при гепатите с
Обновлено: 15.04.2024
Острый вирусный гепатит В (ВГВ) – вирусная антропонозная инфекционная болезнь с преимущественным парентеральным и вертикальным механизмами передачи возбудителя; характеризуется циклически протекающим паренхиматозным гепатитом с возможной хронизацией.
Острый вирусный гепатит D (гепатит дельта, гепатит B с дельта-агентом) – вирусный гепатит с парентеральным механизмом передачи возбудителя, вызываемый дефектным вирусом, репликация которого возможна только при наличии в организме HBsAg, протекающий в виде ко- и суперинфекции.
Острый вирусный гепатит C (ВГС) – антропонозная инфекционная болезнь с парентеральным механизмом передачи возбудителя, характеризуемая лѐгким или субклиническим течением острого периода болезни, частым формированием хронического гепатита C, возможным развитием цирроза печени и гепато-целлюлярной карциномы.
Пользователи протокола: инфекционисты, терапевты, врачи общей практики, гастроэнтерологи, акушер-гинекологи, хирурги, невропатологи, врачи/фельдшеры скорой медицинской помощи, анестезиологи-реаниматологи, организаторы здравоохранения.
Класс I – польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным.
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
Классификация
Осложнения: острая и подострая дистрофия печени с развитием печѐночной энцефалопатии и печѐночной комы.
- Иннапарантная – нет клиники, нормальные показатели АЛТ, в крови специфические маркеры вирусных гепатитов.
- Субклиническая – нет клиники, в крови специфические маркеры вирусных гепатитов, в сочетании с изменениями в биохимических пробах печени.
- Типичная желтушная циклическая – желтуха с цитолитическим синдромом с четким разграничением 3-х периодов болезни, специфические маркеры вирусных гепатитов.
- Типичная желтушная с холестатическим компонентом – желтуха более интенсивная, высокая билирубинемия, незначительная трансаминаземия, имеется тенденция к повышению ЩФ, в крови специфические маркеры вирусных гепатитов. Более продолжителен желтушный период.
- Атипичная холестатическая – наблюдается редко, у больных пожилого возраста. Желтуха интенсивная с выраженным зудом кожи. Гипербилирубинемия, гиперхолестеринемия, повышение ЩФ и ГГТП. Тенденция к ускорению СОЭ и субфебрилитет в желтушном периоде, в крови специфические маркеры вирусных гепатитов.
- Атипичная безжелтушная – клинические симптомы, идентичные преджелтушному периоду, полное отсутствие желтухи, гепатомегалия. Специфические маркеры вирусных гепатитов в сочетании с повышенным уровнем АЛТ.
- Острая циклическая – в течение 1-1,5 месяцев прекращается репликация вируса, он элиминируется из организма и наступает полная санация (для ГА, ГЕ – типичная форма; ГВ, ГС и ГД – один из вариантов).
- Острая прогредиентная – фаза активной репликации вируса сохраняется 1,5-3 месяца. Завершение инфекции: либо санация, либо трансформация в хроническое течение (ГВ, ГС и ГД).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне (исследования, необходимые для всех пациентов с ОВГ): не проводятся.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
- Биохимический профиль: АЛТ, АСТ, общий билирубин и фракции, тимоловая проба, общий белок, альбумин, холестерин, щелочная фосфатаза, ГГТП.
- серологические маркеры ВГ: (anti-HAV-IgM, anti-НЕV-IgМ, HBsAg (качественный тест), antiHBsAb, HBeAg, anti HBeAb, anti-HBc – IgM, total, anti-HCV-IgM, total, anti-HDV-IgM, total;
- биохимический профиль: (липопротеиды, триглицериды, белковые фракции, глюкоза, калий, натрий, хлориды, амилаза, остаточный азот, мочевина, креатинин);
- коагулограмма: ПВ, общий фибриноген, время рекальцификации плазмы, этаноловый тест, время свертывания крови;
- ПЦР: определение HBV-ДНК (качественный тест), при наличии anti-HDV и при тяжелых формах ОГВ – определение HDV-РНК (качественный тест), определение HCV- РНК (качественный тест);
Выделены три варианта клинического течения хронического микст-гепатита C+B: типичный, холестатический и микст-гепатит с внепеченочными проявлениями. При типичном варианте доминируют симптомы преимущественного поражения печени – гепатомегалия, болевой и цитолитический синдромы при отсутствии выраженного холестаза и признаков внепеченочного поражения. Холестатический вариант характеризуется выраженным внутрипеченочным холестазом в сочетании с гипербилирубинемией и симптомами поражения печени – гепатомегалией и цитолитическим синдромом. При внепеченочном варианте микст-гепатита C+B доминируют симптомы внепеченочного поражения

1. Абдурахманов Д.Т. Латентная HBV-инфекция в патогенезе хронических заболеваний печени // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 2002. - № 6. - С. 31-37.
2. Бацких С.Н. Латентная HBV-инфекция: Безобидный лабораторный феномен или серьезная клиническая проблема? // Гепатол. форум. - 2010. - № 3. - С. 2-8.
3. Естественное течение сочетанных вирусных гепатитов В и С / В.В. Горбаков, А.И. Хазанов, Н.П. Блохина и др. // Клин. микробиол. - 2001. - Т. 3. - № 3. - С. 209-214.
4. Маевская М.В. Клинические особенности тяжелых форм алкогольной болезни печени. Роль вирусов гепатита В и С // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 2006. - № 2. - С. 25-38.
5. Непомнящих Д.Л. Ультраструктурный анализ биоптатов печени при хронических гепатитах и гепатопатиях // Бюл. экспер. биол. - 1994. - Т. 118, № 9. - С. 306-310.
6. Непомнящих Д.Л., Айдагулова С.В., Непомня- щих Г.И. Биопсия печени: Патоморфогенез хронического гепатита и цирроза. - М.: Изд-во РАМН, 2006. - 368 с.
7. EASL Clinical Practice Guidelines: Management of chronic hepatitis B // J. Hepatol. - 2009. - Vol. 50. - P. 227-242.
8. Lock A.S., McMahon B.J. Chronic hepatitis B: update 2009 // Hepatology. - 2009. - Vol. 50. - P. 661-669.
9. Matsuoka S., Nirei K., Tamura A. et al. Influence of occult hepatitis B virus coinfection on the incidence of fibrosis and hepatocellular carcinoma in chronic hepatitis C // Intervirology. - 2008. - Vol. 51. - P. 352-361.
10. Seed C.R., Kiely P., Keller A.J. Residual risk of transfusion transmitted human immunodeficiency virus, hepatitis B virus, hepatitis C virus and human T lymphotrophic virus // Intern. Med. J. - 2005. - Vol. 35. - P. 592-598.
Хронический микст-гепатит С+В предсталяет собой серьезную проблему в связи с разнообразной, но более тяжелой по сравнению с моногепатитами С и В, клинической картиной и неоднозначностью в подходах к терапии [1-4, 7, 8, 10]. Так, относительно хронического гепатита С, при хронической микст-инфекции HCV+HBV, реже наблюдается минимальная степень активности (18 % против 33 %) и чаще - умеренная (44% против 27 %), что в целом характеризует течение хронического микст-гепатита С+В как более тяжелое. Распределение пациентов с гепатитом С+В по стадии заболеваний, или по выраженности фиброза, имеет тот же профиль, что и при гепатите С, c явным преобладанием случаев со слабовыраженным портальным фиброзом (70 %), тем не менее, при микст-гепатите чаще отмечается конечная стадия заболевания - цирроз печени [6, 9].
Цель исследования - на основе анализа клинических синдромов, биохимических тестов и результатов патоморфологического исследования биопсии печени пациентов с хроническим микст-гепатитом С+В выделить различные патоморфогенетические варианты инфекционно-вирусного процесса.
Материал и методы исследования
Исследовано 112 пациентов в возрасте от 16 до 69 лет с маркерами хронических гепатитов С и В, преобладали мужчины (74 пациента). Изучали эпидемиологический анамнез, клиническую картину, результаты клинико-биохимического, серологического, молекулярно-биологического и патоморфологического исследований. Анализировали анамнез, пути возможного заражения вирусами гепатита С и В: парентеральное употребление наркотических веществ, гемотрансфузии, хирургические вмешательства. Выявляли токсические факторы: алкоголь, лекарственную гиперпрогмазию, профессиональные вредности, учитывали наличие патологии желудочно-кишечного тракта и паразитарной инвазии.
Диагноз хронического микст-гепатита С+В верифицирован на основании данных эпидемиологического анамнеза, клинико-инструментальных данных, результатов биохимического, иммуносерологического анализа, ПЦР-диагностики и изучения биопсии печени, что позволило идентифицировать маркеры HCV- и HBV-инфекции, установить степень активности и стадию заболевания. Исследования выполнены с информированного согласия пациентов и в соответствии с этическими нормами Хельсинкской Декларации (2000).
Результаты исследования и их обсуждение
Анализ эпидемиологического анамнеза выявил факторы риска заражения вирусами гепатитов С и В: переливание крови и ее компонентов, донорство, парентеральное введение лекарственных препаратов, наркоманию с парентеральным введением наркотических веществ, инвазивные методы исследования и лечения, профессиональный контакт с кровью. Перенесенный острый вирусный гепатит в анамнезе имел место у 34 % пациентов. Среди факторов дополнительного гепатотоксического воздействия - лекарственная гиперпрогмазия (33 %), злоупотребление алкоголем (18 %), сочетанное употребление этанола и наркотических веществ (4 %). У 41 % пациентов имелась патология желудочно-кишечного тракта, у 24 % - патология других органов и систем.
В соответствии с особенностями клинического течения заболевания и результатами комплексного клинико-патоморфологического исследования пациентов выделено три варианта хронического микст-гепатита С+В: типичный (с преобладанием типичных симптомов поражения печени) - 61 % случаев, холестатический - 25 % и вариант с выраженными внепеченочными проявлениями - 14 % пациентов.
Спектр серологических маркеров вирусных гепатитов В и С при всех клинических вариантах не имел существенных различий, во всех наблюдениях регистрировались суммарные HCVAb, в большинстве случаев - антитела к NS-антигенам HCV и набор антигенов и антител HBV, при этом отличительной особенностью серологического спектра холестатического варианта было более редкое выявление HBsAg и более частое обнаружение HВeAg. По данным ПЦР-диагностики, в целом среди всех пациентов доминировала репликация HCV (68 % случаев) по сравнению с репликацией HBV - 52 % случаев.
В клинической характеристике для пациентов с типичным вариантом хронического гепатита С+В наиболее частые проявления заболевания - гепатомегалия, астеновегетативный и болевой абдоминальный синдромы (табл. 1), более редкие - диспепсия (1/3 пациентов), субиктеричность склер, спленомегалия и печеночная энцефалопатия - менее трети пациентов; в единичных случаях наблюдали геморрагический синдром. Выраженные симптомы холестаза и внепеченочных поражений отсутствовали.
Таблица 1. Сравнительная характеристика основных клинических синдромов при хроническом микст-гепатите C+B ( %)
Степень выраженности цитолиза в большинстве случаев соответствовала минимальной и слабовыраженной степени активности (67 % пациентов), других значимых изменений биохимических показателей не выявлено (табл. 2). Изменения основных показателей периферической крови и системы гемостаза (незначительное удлинение протромбинового времени) определялись в единичных случаях.
Особенностью клинической картины холестатического варианта было сочетание синдрома холестаза с гепатомегалией и желтухой (92 % наблюдений), более частые, в сравнении с типичным вариантом, спленомегалия, симптомы печеночной энцефалопатии и астеновегетативные проявления. Кроме того, цитолитический синдром был более выраженным и в большинстве случаев сочетался с повышением уровня маркеров холестаза.
Таблица 2. Сравнительная характеристика биохимических показателей крови при хроническом микст-гепатите C+B
Щелочная фосфатаза (ЩФ)
Для внепеченочного варианта наиболее характерны сочетания астеновегетативного синдрома и симптомов внепеченочного поражения (100 %), а также гепато-, спленомегалия и холестаз - по 71 % пациентов. Кроме того, у 50 % пациентов отмечены отклонения в системе гемостаза - удлинение протромбинового времени и снижение протромбинового индекса. Изменения показателей периферической крови (анемия и тромбоцитопения) носили более выраженный характер в сравнении другими вариантами.
При патоморфологическом исследовании биоптатов печени пациентов с различными вариантами клинического течения хронического микст-гепатита С+В выявлен достаточно выраженный полиморфизм. Липидная инфильтрация была ведущей формой дистрофии гепатоцитов, особенно при типичном варианте и наличии внепеченочных симптомов (85 и 81 % случаев соответственно). Диффузный интрацеллюлярный холестаз и ацидофильная дегенерация достигали наибольшей выраженности при холестатическом варианте. Клеточно-инволютивная дистрофия гепатоцитов, особенно диффузная, доминировала при манифестации внепеченочных симптомов. Перстневидная трансформация ядер гепатоцитов (структурный маркер HBcAg) отмечена в 87 % биоптатов при наличии внепеченочных симптомов, в 71 % - при типичном варианте и в 57 % - при холестатическом варианте. Альтеративная компонента (наличие очагов некробиоза, телец Каунсильмена и постнекротических гранулем) играла более заметную роль при холестатическом варианте хронического микст-гепатита С+В.
Клеточная инфильтрация портальной стромы имела, как правило, мононуклеарный характер с распространением в паренхиму; особенно активный лимфодиапедез отмечен при холестатическом варианте. Фиброзные изменения печени в наибольшей степени выражены при холестатическом и внепеченочном вариантах. Эпителий желчных протоков подвергался альтерации и компенсаторной пролиферации при типичном и холестатическом вариантах (81 и 78 % соответственно).
Таким образом, внутрипеченочный холестаз обусловливал более тяжелое поражение печени при хроническом микст-гепатите C+B. Клинически это проявлялось выраженными симптомами поражения печени и тенденцией к прогрессированию заболевания по сравнению с типичным вариантом.
При электронно-микроскопическом исследовании биоптатов печени при трех клинических вариантах хронического микст-гепатита выявлены стереотипные изменения ультраструктуры гепатоцитов, отражающие комплекс альтеративных и компенсаторных перестроек. Во всех случаях в перипортальных гепатоцитах обнаружены специфичные для гепатита В перстневидные ядра с лизированной нуклеолеммой.
Варьирование электронной плотности цитоплазматического матрикса, содержания гликогена, различная степень альтерации и редукции мембранных органелл, а также полиморфизм липидных капель и резидуальных телец обусловливали значительную гетерогенность гепатоцитов. В большинстве случаев редуцированы и повреждены митохондрии - с резко уменьшенным количеством крист и просветленным матриксом. В части гепатоцитов на фоне опустошенности цитоплазмы перинуклеарная зона сохраняла биосинтетический комплекс - регенераторный потенциал в виде элементов гранулярной цитоплазматической сети и митохондрий. Для токсических воздействий характерна гиперплазия элементов гладкой цитоплазматической сети и крупновезикулярная липидная инфильтрация. В целом, деструкция цитоплазматических органелл гепатоцитов соответствовала степени активности инфекционного процесса, достигая наибольшей выраженности при высоких показателях цитолиза, чаще ассоциируясь с синдромом холестаза.
Типичный вариант характеризовался значительной гетерогенностью популяции паренхиматозных клеток, обусловленной полиморфизмом внутриклеточной организации. Холестатический вариант определяли множественные компоненты желчи и вторичные фагосомы с накоплением осмиофильных гранул липофусцина и резидуальных телец, расположенные не только вблизи билиарных полюсов, но и диффузно в цитоплазме клеток, а также в просветах синусоидов. Клинический вариант с внепеченочными проявлениями отличала наибольшая выраженность клеточно-инволютивной дистрофии гепатоцитов [5], что ограничивало репликацию вирусов в паренхиматозных клетках печени с вероятным инфицированием и репликацией в других органах, в частности в почках (что установлено с помощью ПЦР-диагностики в 8 биоптатах почки), обусловливая манифестацию внепеченочных синдромов.
Холестатический вариант микст-гепатита отличался выраженным внутрипеченочным холестазом, сочетающимся с гепатомегалией и желтухой (по 92 %), гипербилирубинемией (75 %), спленомегалией (67 %) и более выраженным цитолитическим синдромом по сравнению с типичным вариантом. Сочетание гипербилирубинемии с повышением показателей холестаза и цитолиза установлено в 58 % случаев. При хроническом микст-гепатите C+B с внепеченочными проявлениями присутствовали те же клинические синдромы, что и для типичного и холестатического вариантов, при ведущей роли синдромов внепеченочной патологии.
Структурные изменения печени при типичном варианте хронической микст-инфекции HCV+HBV отличались дистрофией гепатоцитов с минимальной альтеративной компонентой и наименьшей степенью клеточной инфильтрации и фиброза. Патогномоничными признаками холестатического варианта были интрагепатоцеллюлярный холестаз, обусловливающий гибель гепатоцитов, и значительная клеточная инфильтрация. При внепеченочном варианте доминировала клеточно-инволютивная дистрофия.
Выделены три варианта клинического течения хронического микст-гепатита C+B: типичный, холестатический и микст-гепатит с ведущей ролью внепеченочных проявлений. При типичном варианте доминируют симптомы преимущественного поражения печени - гепатомегалия, болевой и цитолитический синдромы при отсутствии выраженного холестаза и признаков внепеченочного поражения. Холестатический вариант характеризуется выраженным внутрипеченочным холестазом при наличии симптомов поражения печени - гепатомегалия, цитолитический синдром, гипербилирубинемия. При внепеченочном варианте доминируют симптомы внепеченочного поражения.
Холестатический вариант микст-гепатита С+В характеризуется наиболее значительной альтеративной компонентой (наличие очагов некробиоза и некроза, апоптотических телец Каунсильмена, постнекротических гранулем) и фиброзных изменений печени, что позволяет рассматривать этот вариант как наиболее неблагоприятный в плане развития цирроза печени.
Выделение трех вариантов клинического течения хронического микст-гепатита C+B с комплексной оценкой каждого из вариантов, дополненное описанием морфологической картины, имеет большое практическое значение для выбора тактики терапии.
Селятицкая В.Г., д.б.н., профессор, зав. лабораторией эндокринологии и зам. директора по научной работе Научного центра клинической и экспериментальной медицины СО РАМН, г. Новосибирск;
Поляков Л.М., д.м.н., профессор, зав. лабораторией медицинской технологии и зам. директора по научной работе НИИ биохимии СО РАМН, г. Новосибирск.
Государственная медицинская академия, Нижний Новгород
Особенности микст-гепатита В+С острого и хронического течения (клинико-серологические параллели)
Ведущие позиции в структуре сывороточных гепатитов на сегодняшний день занимает микст-гепатит В+С. Частота обнаружения сочетанного поражения печени этими вирусами достигает 45% [1, 2].
Целью работы явилось изучение характеристики течения и особенностей инфекционного процесса при смешанной HBV/HCV-инфекции острого и хронического течения.
Материалы и методы.
Диагноз верифицирован обнаружением специфических маркеров HBV (HbsAg, HbeAg/анти-Hbe, анти-HB core IgM, анти-HB core сум) и HCV (анти-HCV core IgM, анти-HCV core IgG, анти-HCVNS-4). Арбитражным методом в постановке диагноза явилось обнаружение HBV ДНК и HCV РНК методом ПЦР. Обследование больных проводилось в динамике для оценки отдаленных исходов болезни.
Результаты и обсуждение.
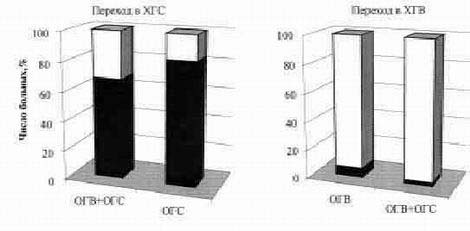 |
| — хронизация; — выздоровление |
| Рис. 1. Частота хронизации при остром микст-гепатите В+С сранительно с ОГВ и ОГС |
| — HBsAg(+); — HBsAg(-) —HbeAg(+); — HbeAg(-) — ДНК(+); — ДНК(-) — РНК(+); — РНК(-) |
| Рис. 2. Сравнительная частота выявления маркеров HBV и HCV в разных группах больных (по данным первичного обследования) |
| Рис. 3. Частота обнаружения HBV ДНК и HCV РНК при остром микст-гепатите В+С |
Жданов Ю.Е., Соринсон С.Н., Малышева Е.Б. и др. Некоторые особенности течения вирусных гепатитов В и С у лиц, употребляющих наркотические вещества. В кн.: Инфектология. Достижения и перспективы. Тез. докл. юбил. науч. конф., посвященной 100-летию первой кафедры инф. болезней в России. СПб; 1996.
Шахгильдян И.В. Современная эпидемиологическая характеристика гепатитов В и С в Российской Федерации. Информац бюл 1999; 3(7).
Фролов А.В. Прогредиентное затяжное течение острого гепатита В. Диагностика, прогнозирование, возможности терапии. Автореф. дис. … канд. мед. наук. СПб; 1991.
Шерлок Ш., Дули Дж. Заболевания печени и желчных путей. Практич. рук. Пер. с англ. Под ред. З.Г.Апросиной, Н.А.Мухина. М: ГЭОТАР-Медицина; 1999.
Tsai J.F., Jeng J.F., Ho M.S. et al. Independent and additive effect modification of hepatitis C and B viruses infection of the development of chronic hepatitis. J Hepatol 1996; 24: 17—21.
Mathurin P., Poynard T., Moussali J. et al. HBV replication in patients with HCV and HBV dual infections. In: IX Triennial international symposium on viral hepatitis & liver disease. Abstract Volum. Rome; 1996.
"Медикум"
новый научно-практический медицинский журнал, который будет издаваться на 2-х языках: русском и английском, в трех формах выпуска: печатная, интернет-версия, CD-версия.
Хронический вирусный гепатит – воспаление ткани печени, сохраняющееся в течение длительного (более 6-ти месяцев) периода времени.
Код протокола: Н-T-026 "Хронический вирусный гепатит"
Для стационаров терапевтического профиля
- Другие уточненные хронические вирусные гепатиты В18.8
- Другие неуточненные хронические вирусные гепатиты В18.9
Классификация
- хронический вирусный гепатит В (ХВГВ): HbeAg-позитивный и HBeAg-негативный (с мутацией pre-cor зоны); HbsAg-негативный (с мутацией по гену S);
- хронический вирусный гепатит С (ХВГС): 1b / 1а / 2 / 3 / 4 генотип; с высокой или низкой вирусной нагрузкой;
- хронический вирусный гепатит, не классифицируемый другим образом.
- иммунной толерантности (для вирусного гепатита В).
4. По стадии:
*Степени активности хронического гепатита определяют по выраженности некроза паренхимы и воспалительной клеточной инфильтрации применением полуколичественного (рангового) анализа, оценивая выраженность гистологических признаков в баллах (индекс Knodell, шкала METAVIR).
**Оценка индекса гистологической активности
| Компоненты индекса | Пределы баллов |
| 1. Перипортальные некрозы с мостовидными некрозами или без них | 0-10 |
| 2. Внутридольковая дегенерация и фокальные некрозы | 0-4 |
| 3. Портальное воспаление | 0-4 |
| 4. Фиброз | 0-4 |
Факторы и группы риска
В группу риска входят:
- наркоманы;
- лица с беспорядочными половыми связями;
- пациенты отделений гемодиализа;
- больные, нуждающиеся в повторных трансфузиях крови или ее компонентов;
- медицинские работники;
- члены семьи носителя вирусов.
Наиболее значимые пути заражения, по которым происходит массивная передача возбудителя, - переливание крови и ее продуктов (70% случаев посттрансфузионного гепатита), инъекции и другие инвазивные вмешательства, гемодиализ, трансплантация органов, татуаж. Роль полового, вертикального и перинатального путей заражения более существенна для ХВГВ. В 40% случаев не удается установить путь передачи возбудителя. Основной путь передачи HCV - парентеральный: трансфузии, трансплантации органов от инфицированных доноров, внутривенное введение наркотиков.
Диагностика
Жалобы и анамнез
ХВГВ чаще протекает с явлениями астеновегетативного синдрома, пациентов беспокоят слабость, утомляемость, бессонница или гриппоподобный синдром, мышечные и суставные боли, тошнота. Менее характерны боли в эпигастральной области, диарея, кожная сыпь, желтуха.
У большинства пациентов с ХГС даже на фоне высоких уровней сывороточных трансаминаз заболевание зачастую протекает бессимптомно либо с явлениями астеновегетативного синдрома. Реже отмечается тошнота, потеря аппетита, кожный зуд, артралгии и миалгии.
ХВГД является исходом суперинфекции вирусом гепатита Д у пациентов с ХВГВ и имеет, по сравнению с ХВГВ и ХВГС более выраженные клинические проявления.
При физикальном обследовании основным объективным симптомом является гепатомегалия, повышение плотности печени. При высокой активности процесса, а также формировании цирроза печени возможны спленомегалия, иногда – лимфаденопатия, наличие печеночных знаков (пальмарная и подошвенная эритема, сосудистые звездочки, гиперпигментация).
- эндоскопическое исследование, контрастное исследование пищевода с барием (варикозное расширение вен пищевода);
- ультразвуковое исследование гепатобилиарной системы (гепатомегалия, спленомегалия, изменение структуры печени);
Формирование и прогрессирование портальной гипертензии: спонтанного бактериального перитонита, портосистемной энцефалопатии, гепаторенального синдрома, гепатопульмонального синдрома, вторичного гиперспленизма с цитопенией (аплазия костного мозга), коагулопатия (потребления), ДВС-синдром.
- общий анализ крови;
- общий анализ мочи;
- копрограмма;
- биохимические пробы печени (АЛТ, АСТ, щелочная фосфатаза, ГГТП или ГГТ, билирубин, белки сыворотки крови, коагулограмма или протромбиновое время, креатинин или мочевина);
- серологические маркеры (HBsAg, HBeAg, анти-HBc, HBe IgG, анти-HBc IgM, анти HBe IgG, DNA HBV, анти-HCV total, RNA HCV, анти-HDV, RNA HDV);
Лабораторная диагностика
Изменения общего анализа крови малохарактерны и чаще наблюдаются в качестве побочных эффектов противовирусной терапии.
Биохимические изменения крови включают:
- синдром цитолиза (повышение активности АЛТ, АСТ, альдолазы, ЛДГ,4,5-орнитинкарбамилтрансферазы);
- синдром холестаза (повышение активности/содержания ЩФ, 5-нуклеотидазы, ГГТП, билирубина (прямой фракции), желчных кислот, холестерина, b-ЛП, фосфолипидов);
- синдром печеночно-клеточной недостаточности (снижение содержания альбуминов, холинестеразы, протромбина, проконвертина, задержка выделения бромсульфалеина);
- синдром иммунного воспаления (повышение содержания g-глобулинов, IgA, IgM, IgG, увеличение тимоловой пробы, снижение сулемовой пробы, наличие аутоантител: антинуклеарных (ANA), антигладкомышечных (ASMA), к микросомам печени и почек 1 типа (LKM-1), к растворимому антигену печени (SLA));
- синдром шунтирования (повышение содержания аммиака, фенолов, свободных аминокислот).
- анти-HDV, RNA HDV.
Дифференциальный диагноз
1. Болезни печени и ее сосудов: аутоиммунный гепатит, латентный цирроз печени, эхинококкоз печени, рак печени, доброкачественные опухоли печени, непаразитарные кисты печени, туберкулезный гранулематоз, туберкулома печени, болезнь Бадда-Киари.
3. Болезни сердечно-сосудистой системы: констриктивный перикардит, недостаточность кровообращения II и III степени ("застойная печень").
Лечение
- щадящий режим (избегать физических перегрузок, перегреваний, переохлаждений);
- диета №5;
- обязательное исключение любых алкогольсодержащих напитков.
В лечении хронического вирусного гепатита ведущую роль играет противовирусная терапия с использованием интерферонов и аналогов нуклеозидов/нуклеотидов. Учитываются активность процесса, клинико-биохимические и гистологические изменения печени.
- гистологические признаки активности.
- анемия или невозможность переносимости анемии.
- отсутствие ИФН-терапии в анамнезе.
- большая давность заболевания (свыше 10 лет);
- рецидив.
Факторы пациента:
Для лечения ХВГВ используются пегилированные интерфероны в монотерапии и аналоги нуклеотидов/нуклеозидов.
Стандартная доза пегилированного интерферона α2а составляет 180 мкг 1 раз в неделю, пегилированного интерферона α2b - 1,5 мкг/кг 1 раз в неделю. Стандартная длительность терапии – 24 недели, однако в настоящее время она пересматривается в сторону увеличения до 48 и даже 96 недель.
В качестве альтернативы, а также при наличии противопоказаний к интерферонотерапии используют аналоги нуклеотидов/нуклеозидов (ламивудин 100 мг/сутки или адефовир 10 мг/сут. или энтекавир 0,5 мг/сут.). Лечение у HBe-позитивных пациентов длится до достижения сероконверсии (появление anti-HBe) и исчезновения DNA HBV, у HBe-негативных пациентов - до исчезновения DNA HBV на протяжении не менее 24 недель. При отсутствии сероконверсии и отрицательной качественной ПЦР эффективность терапии оценивают по снижению вирусной нагрузки (не более 104), а длительность терапии в этих случаях может быть неопределенно долгой.
На фоне лечения аналогами нуклеотидов/нуклеозидов возможно возникновение резистентности (чаще к ламивудину) в виде ухудшения течения заболевания, подъема АЛТ, увеличения вирусной нагрузки. В этих случаях дальнейшее лечение ламивудином комбинируют с адефовиром.
При ХВГС используют комбинированную противовирусную терапию интерферонами и рибавирином. Продолжительность лечения при 1,4,5 и 6 генотипах составляет 48 недель, а при генотипах 2 и 3 – 24 недели. Стандартная доза пегилированного интерферона α2а составляет 180 мкг 1 раз в неделю, пегилированного интерферона α2b - 1,5 мкг/кг 1 раз в неделю. Доза рибавирина при лечении пациентов с генотипами 1,4,5 и 6 составляет 1200 мг в сутки, с генотипами 2 и 3 - 1000 мг в сутки.
При ХВГД используют стандартные дозы пегилированных интерферонов. Рекомендуемая длительность лечения - от 48 до 96 недель.
В случаях сопутствующего холестаза у пациентов с хроническими вирусными гепатитами доказана эффективность урсодезоксихолевой кислоты (500-1000 мг/сутки). При возникновении серьезных побочных эффектов терапии, не поддающихся коррекции (лейкопения менее 1,8, тромбоцитопения менее 80, анемия тяжелой степени, глубокая депрессия, аутоиммунные заболевания), рассматривают вопрос об отмене терапии. У пациентов с ХВГС терапию отменяют также при отсутствии вирусологического ответа после 12 недель лечения.
Диспансеризация проводится поликлиническим терапевтом, гатроэнтерологом, инфекционистом. Осмотры с определением биохимических показателей активности воспаления, маркеров вирусной репликации и других тестов проводятся не реже 1 раза в полгода, а при проведении ПВТ – 1 раз в месяц.
Через 6 месяцев после окончания курса лечения исследуют уровень АЛТ, HCV RNA и HBV DNA. Если уровень АЛТ нормален, HCV RNA и HBV DNA отрицателен, то эффект расценивают как стойкий положительный.
В противном случае дальнейшую тактику ведения пациента выбирают индивидуально. У больных на стадии вирусного цирроза печени каждые 6 месяцев проводят исследование α-фетопротеина и УЗИ.
3. Рибавирин 200 мг
Перечень дополнительных медикаментов:
5. Лактулоза 200,0
- ответ на момент окончания лечения – эффективность лечения оценивают непосредственно на момент завершения его курса;
- стойкий ответ – сохранение нормального уровня АЛТ и отрицательные результаты HCV RNA и HBV DNA через 6 месяцев после завершения курса лечения.
Госпитализация
Госпитализация при необходимости коррекции печеночной дисфункции, уточнения активности процесса, подбора противовирусной терапии и ее коррекции при возникновении нежелательных явлений – в гастроэнтерологические или терапевтические стационары.
Профилактика
Проводится с помощью рекомбинантной HBV-вакцины, которая вводится трехкратно (0-1-6 месяцев).
Иммунизации подлежат:
- наркоманы, проститутки, гомосексуалисты (обеспечить полную иммунизацию данной категории невозможно, но при всяком удобном случае им нужно предлагать вакцинацию).
Поддерживающие дозы вакцины следует вводить каждые 5-10 лет.
Заключается во введении двух доз гипериммунного HBV-иммунноглобулина (500 МЕ внутримышечно с интервалом в 1 месяц).
Категории лиц, подлежащие данному виду иммунизации:
- ранее не иммунизированный медицинский персонал, получивший травмы кожных покровов при оказании помощи пациентам, инфицированным вирусом гепатита В. Иммуноглобулин следует вводить в течение первых 7 суток с последующим проведением активной иммунизации. Если пациент является HBV- негативным, необходимо провести активную иммунизацию и проанализировать действия персонала для предупреждения повторных травм;
- новорожденные от HBV-позитивных матерей. В первые 12 ч. с момента рождения в разные участки тела вводят 200 МЕ иммуноглобулина и 0,5 мл (10 мкг) рекомбинантной вакцины. Вторую и третью дозы вакцины вводят через 1 и 6 месяцев.
Информация
Источники и литература
Информация
Нерсесов А.В. д.м.н., профессор, кафедра внутренних болезней, факультет усовершенствования врачей, КазГМА
Петрова Н.П., доцент кафедры инфекционных болезней Алматинского государственного института усовершенствования врачей
Хронический гепатит С – заболевание печени, вызванное вирусом гепатита С, длительностью 6 и более месяцев. В 10 – 40% случаев хронический гепатит С прогрессирует до цирроза печени, а в 5% случаев до гепатоцеллюлярной карциномы (чаще у пациентов с циррозом или выраженным фиброзом).
Пользователи протокола: гастроэнтерологи, инфекционисты, терапевты, врачи общей практики, а также врачи смежных специальностей, осуществляющие ведение и лечение пациентов с гепатитом С на разных стадиях заболевания.
Методология: Протокол разработан на основе Клинических руководств ведущих международных сообществ (EASL, AASLD, CASL, SASL, FASL, EACS, РОПИП) и адаптирован с учетом используемых на территории Казахстана методов диагностики и лечения. Классификация рекомендаций, использованная в данном протоколе, представлена в Таблице 1.
Таблица 1. Классификация рекомендаций
Классификация
Клиническая классификация
Общепринятой классификации ХГС не существует. При постановке диагноза необходимо указывать вирусологический статус (генотип и вирусную нагрузку), активность (биохимическую и/или гистологическую), а также стадию заболевания (по данным непрямой эластографии или морфологического исследования).
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
(+) исследования необходимые для пациентов с ЦП
Хронический гепатит С протекает бессимптомно или малосимптомно и может сопровождаться такими неспецифичными симптомами как:
• Депрессия (оценивается у всех пациентов с использованием шкалы Бека)
• сахарный диабет 2 типа
При сборе анамнеза следует учитывать указания на гемотрансфузии, трансплантацию органов и тканей, небезопасные инвазивные (немедицинские) манипуляции, принадлежность в группам риска (потребители наркотиков, лица с беспорядочными половыми связями, пациенты, находящиеся на хроническом гемодиализе, пациенты с онкогематологическими заболеваниями, лица, живущие с ВИЧ и другими парентеральными инфекциями, сексуальные партнеры лиц с ВГС, медицинские работники, дети, рожденные от HCV-инфицированных матерей, лица с измененными функциональными пробами печени). Лицам с указанными факторами риска необходим профилактический скрининг на наличие ВГС (anti-HCV).
При физикальном обследовании на начальной стадии ХГС патологии не выявляется, за исключением незначительной гепатомегалии. По мере прогрессирования заболевания может отмечаться увеличение и уплотнение печени. Спленомегалия и другие стигмы хронического заболевания печени могут проявляться на более поздних стадиях.
Вирусный гепатит С преимущественно протекает бессимптомно. При переходе хронического гепатита С в цирроз в 6,4% случаев отмечаются симптомы, обусловленные дисфункцией печени и портальной гипертензией:
В ряде случаев ВГС выявляется у пациентов с ГЦК, которая, как правило, протекает бессимптомно, кроме случаев запущенной стадии, когда опухоль достигает значительных размеров, вызывая ухудшение функции печени (желтуха, асцит, печеночная энцефалопатия), боли в верхнем правом квадранте, астенизацию и потерю веса.
ОАК с подсчетом тромбоцитов. Могут быть выявлены анемия (в результате гиперспленизма, кровотечений из ВРВ), лейкопения, тромбоцитопения (в результате гиперспленизма и прямого миелодепрессивного влияния ВГС), ускорение СОЭ (при инфекционных осложнениях).
Биохимический профиль включает определение показателей АЛТ, АСТ, ГГТП, альбумина, билирубина, щелочной фосфатазы, МНО или ПВ, а также рутинных (глюкозы, креатинина, холестерина) и некоторых специфических показателей, таких как, гамма-глобулины, IgG (скрининг аутоиммунного гепатита), сывороточное железо и ферритин (скрининг гемохроматоза и вторичной перегрузки железом), церулоплазмин (скрининг болезни Вильсона-Коновалова), АФП (скрининг ГЦК). Активность АЛТ и АСТ может быть минимальной ( < ВГН), слабовыраженной (< 5 ВГН), умеренной (5-10 ВГН), выраженной (>10 ВГН) и не всегда коррелирует с гистологической активностью. Уровень билирубина при ХГС, как правило, нормальный. Его увеличение может наблюдаться при остром гепатите или свидетельствовать об ухудшении деятельности печени на поздней стадии заболевания, что также сопровождается снижением уровня альбумина и увеличением МНО или ПВ. Показатели щелочной фосфатазы и ГГТП могут увеличиваться при остром гепатите и оставаться на уровне нормы при хроническом гепатите.
В план клинического лабораторного обследования включаются также ОАМ, копрограмма.
- anti-HCV, маркеры других парентеральных инфекций таких как ВГВ (HBsAg, HBeAg, anti-HBs, anti-HBe, anti-HBc total/IgM), ВГD (anti-HDV у носителей HBsAg), ВИЧ (anti-HIV), а также (при подозрении на острый гепатит) ВГА (anti-HAV) и ВГЕ (anti-HEV)
Качественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа.
• В случае подозрения на острый ВГС или у иммуносупрессивных пациентов необходимо определение HCV RNA (рекомендация А1)
• Если тест на anti-HCV положительный, необходимо определить HCV RNA, чувствительным молекулярным методом (рекомендация А1)
• Пациенты с положительным тестом anti-HCV и отрицательным молекулярным тестом на HCV RNA должны быть протестированы на HCV RNA через 3 месяца для подтверждения элиминации вируса (рекомендация А1).
− ИФА (+) в 50% в момент острых проявлений, поэтому ПЦР при подозрении на ОГС проводится во всех, в том числе, ИФА (–) случаях
Количественное определение HCV RNA с помощью высокочувствительной ПЦР в режиме реального времени с нижним лимитом определения 15 МЕ/мл на автоматических анализаторах закрытого типа, а также определение генотипа ВГС.
В настоящий момент известно 6 различных типов вируса, которые обозначаются цифрами от 1 до 6. Также существует подтипы, обозначаемые буквами (например, подтип 1а и 1b). На территории РК преимущественно распространенны генотипы 1b, 2 и 3.
Функциональные пробы щитовидной железы (ТТГ)
Тест на беременность
Определение полиморфизма гена интерлейкина – 28В. Результат анализа полиморфизма в гене ИЛ28В полезен в прогнозе эффективности лечения и принятии решения о выборе режима терапии у пациентов с ВГС 1 генотипа. 1
Инструментальные исследования
Радиологическое исследование
Радиологическое исследование печени (в первую очередь УЗИ) позволяет идентифицировать признаки стеатоза, выраженного фиброза и перехода в цирроз печени (закругление контуров печени, неравномерность поверхности и крупнозернистость паренхимы печени), признаки портальной гипертензии и тромбоза (увеличение диаметра, кавернозная трансформация, наличие тромбов воротной и селезеночной вен, асцит, спленомегалия), а также наличие объемных образований (ГЦК). Могут использоваться и другие визуализирующие технологии (КТ, МРТ).
Эндоскопическое исследование
При прогрессировании хронического гепатита С в цирроз диагностика портальной гипертензии может, помимо прочих методов, осуществляться путем эндоскопического обследования, позволяющего выявить варикозное расширение вен (пищевода и желудка) и портальную гастропатию.
Оценка тяжести заболевания печени должна проводиться до ПВТ. Выявление пациентов с циррозом печени имеет особое значение, так как эффективность ПВТ обратно пропорциональна стадии фиброза. Отсутствие выраженного фиброза имеет значение при принятии решения о времени начала ПВТ. Пациенты с явными клиническими признаками цирроза не нуждаются в биопсии печени для оценки стадии фиброза. Пациенты с признаками цирроза печени должны быть обследованы на ГЦК. Выраженный фиброз может быть у пациентов с нормальной активностью АЛТ, поэтому оценка степени тяжести заболевания должна проводиться независимо от показателей АЛТ. Пункционная биопсия остается эталонным методом оценки стадии фиброза печени. Риск тяжелых осложнений при биопсии очень низок (от 1/4000 до 1/10000). У пациентов с нарушением свертываемости крови можно использовать трансюгулярную биопсию печени с одновременной оценкой давления в портальной вене. При ХГС альтернативные, неинвазивные методы (непрямая эластография и биомаркеры) могут быть использованы вместо биопсии. Непрямая эластография может быть использована для оценки стадии фиброза печени у пациентов с ХГС, но необходимо учитывать факторы, которые могут повлиять на достоверность результатов, например выраженная активность заболевания, ожирение. Оба метода (непрямая эластография и биомаркеры) точны при оценке цирроза и нулевого фиброза, но менее точны при промежуточных стадиях фиброза. Комбинирование биомаркеров и непрямой эластографии повышает точность оценки стадии фиброза и уменьшает необходимость в проведении ункционной биопсии. В случае противоречивых результатов биомаркеров и непрямой эластографии, можно использовать пункционную биопсию печени. Гистологическая оценка также необходима при смешанной этиологии (например, ВГС с ВГВ, метаболическим синдромом, алкоголизмом или аутоиммунными заболеваниями).
Пункционная биопсия печени (ПБП) – относительно безопасный метод оценки морфологических изменений печени у пациентов с ХГС. ПБП позволяет оценить выраженность фибротического процесса и некровоспалительных изменений. Результаты ПБП легко интерпретируются и поддаются полуколичественной оценке. ПБП проводится в динамике с целью оценки прогрессирования поражения печени при ХГС. ПБП – единственный доступный метод, позволяющий оценить вклад сопутствующих заболеваний (стеатогепатит, гемохроматоз, аутоиммунный гепатит и т.д.) в патологическом процессе и их влияние на течение и эффективность лечения ХГС. Необходимо помнить, что ПБП имеет ряд ограничений. В частности, имеет значение опыт врача, проводящего пункцию, и морфолога, оценивающего морфологические изменения; малый объем образцов ткани печени; инвазивность и дискомфорт для пациентов; риск развития осложнений. ПБП требует строгого выполнения правил ее выполнения в условиях специализированных отделений и наличия квалифицированных морфологов.
2. Всем пациентам перед выполнением биопсии печени должно быть выполнено УЗИ ОБП. Данное исследование позволяет выявить анатомический вариант строения печени и наличие очаговых образований в ее паренхиме, что может потребовать проведения прицельной биопсии под визуальным контролем.
3. В течение недели перед проведением пункции необходимо определить количество тромбоцитов и протромбиновое время (ПВ), либо протромбиновый индекс (ПИ)
• Если количество тромбоцитов ≥90 000 /мм3, то манипуляцию можно выполнять рутинным способом (чрескожная биопсия печени)
• Если ПВ удлинено менее чем на 3 сек. в сравнении с контрольным значением (предоставляется лабораторией, в которой выполняется исследование образца крови), ПИ не менее 70%, тромбиновое время (ТВ) и активированное частичное тромбопластиновое время (АЧТВ) не превышают 1,5 нормы, биопсию можно проводить чрескожным доступом
• Во всех других случаях решение о выполнении биопсии печени принимается на индивидуальной основе путем оценки пользы и риска от планируемой манипуляции. В случае строгой необходимости в проведении биопсии печени у пациентов с гипокоагуляцией или низким количеством тромбоцитов в некоторых случаях может быть оправдана заместительная терапия
4. Перед биопсией необходимо подписать у пациента информированное согласие, в котором доступно описана методика манипуляции и возможные осложнения.
5. Во время выполнения биопсии врач и пациент должны быть в постоянном контакте. Больной четко и своевременно должен выполнять команды врача. При повышенной возбудимости пациента и отсутствии признаков печеночной недостаточности возможно назначение седативных препаратов.
6. Выбор иглы для биопсии целесообразно осуществлять с учетом личного опыта оператора. В повседневной практике удобны в применении иглы Менгини и иглы типа Tru-cut.
7. Врачи, личный опыт которых не превышает 20 манипуляций, выполняют биопсию в присутствии и под контролем более опытного доктора в условиях специализированного гепатологического центра.
9. Активное наблюдение пациентов в течение 8 часов и первой ночи после манипуляции должно проводиться в условиях медицинской организации. Оценка результатов ПБП проводится с применением полуколичественных шкал описания степени некро-воспалительных изменений и стадии фиброза ткани печени (см. Таблицы 3 и 4).
Таблица 3. Морфологическая диагностика степени некровоспалительной активности гепатита
*Для определения стадии заболевания печени чаще применяется шкала METAVIR
К преимуществам метода относятся:
• Неинвазивность
• Воспроизводимость
• Больший чем при биопсии оцениваемый объем ткани печени (в 100-200 раз больше)
• Быстрота и удобство применения (обследование занимает в среднем 5 мин)
• Немедленный результат
• Оценка эффективности терапии
• Возможность обследования детей
• Высокой биохимической активности (АЛТ/АСТ выше верхнего лимита нормы в 3 и более раз)
• Не менее 60% успешных измерений.
Таблица 5. Интерпретация результатов непрямой эластографии
Читайте также:

