Могут ли болеть кости при герпесе
Обновлено: 19.04.2024
Штамм вируса герпеса 6 типа (ВГЧ-6 или HHV-6) был открыт еще в 1986 году. В 2012 году произошло сенсационное открытие: оказывается, вирус герпеса 6 типа у взрослых может никак себя не проявлять, но при этом может вызывать болезненное состояние
Откуда он берется?
По разным данным около 80% людей инфицированы вирусом герпеса 6 типа. Чаше всего встреча с инфекцией происходит в раннем детстве — в возрасте с 6 месяцев до 2 лет. Это связано с утратой ребенком материнского иммунитета и высокой распространенностью вируса. Первая встреча может протекать в форме розеолы — резкого повышения температуры, после чего через 3-4 дня появляется сыпь. Это единственное специфическое проявление у детей, по которым можно заподозрить ВГЧ-6.
Увы, попав в организм, любой вирус герпеса его не покинет. У большинства людей иммунная система достаточно успешно подавляет развитие вирус герпеса 6 типа. Продолжая жить в организме, но ни на что не влияет. Но так происходит не у всех.
Вечно без сил
Часто возникают нарушения сна, депрессия, раздражительность, трудности с концентрацией внимания, ухудшение памяти и интеллекта. Иногда пропадает аппетит, человек резко худеет или толстеет, возникают проблемы в желудке, кишечнике, мочевыделительной системе. Более того, могут появиться симптомы аллергии или чувствительность к яркому свету, алкоголю, лекарствам и т.п.
Как узнать?
На этапе постановке диагноза или для его уточнения врачи назначают лабораторный тест Антитела к вирусу герпеса VI типа (Herpes simplex virus VI), IgG. Его можно сдать и самостоятельно, если вас беспокоит сниженная работоспособность, а по итогам обратиться к врачу. Для него достаточно сдать кровь в лаборатории через 3 часа после приема пищи или утром натощак.
Спровоцировать ВГЧ-6 к активности может любое снижение иммунитета. Чаще всего его запускают стресс, грипп, обострение хронической инфекции. Зачастую люди связывают устало-депрессивное состояние с последствием заболевания или стресса, а на самом деле они стали триггером для активации вируса. Активный вирус живет и размножается за счет лимфоцитов — главных клеток иммунной системы. Поэтому и возникают симптомы инфекции и поражения нервной системы, которая тесно связана с иммунной. При активации вируса HHV6 его можно обнаружить методом ПЦР в соскобе из ротоглотки или в моче. Если есть высыпания на коже и повышение температуры, то можно выявить вирус герпеса 6 типа в крови.
Кому пригодится?
Врачи выделяют несколько групп пациентов, которым необходимо исследование Антитела к вирусу герпеса VI типа (Herpes simplex virus VI), IgG или выявление вирусов группы герпеса в мазке из ротоглотке Это те люди, которых беспокоят:
- проблемы с памятью, невозможность сосредоточиться на деле;
- беспричинные боль и першение в горле;
- болезненность лимфоузлов на шее и под ушами по непонятной причине;
- боли в мышцах, не связанные с физической нагрузкой;
- боли в суставах, не имеющие объективных причин (травма, остеохондроз и т.п.);
- головные боли, которых раньше не бывало;
- проблемы со сном;
- слабость и истощение после физической нагрузки, явно не соответствующие затратам сил;
- частые простудные заболевания
- ощущение лихорадки или озноба при нормальной температуре
Как лечить?
Несмотря на все это, вирус герпеса 6 типа — не приговор. С ним вполне можно жить, как только ваш иммунитет сможет взять его под контроль. Как ни удивительно, большую помощь в этом может оказать здоровый образ жизни. Обязательно надо наладить сон: у тех, кто спит менее 6 часов в сутки, риск проявлений СХУ выше в несколько десятков раз.
На сервисе СпросиВрача доступна консультация ревматолога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте! Есть результаты анализов в итоге? АЦЦП, РФ, СРБ, СОЭ? Суставы опухают? Расхаживаетесь дольше 30 минут утром?
Марина, здравствуйте! По вопросу ревматоидному артриту практически ничего нет. Есть анализ антинуклеарные антитела- везде написано не обнаружены , и ревмафактор тоже в норме
Марина, суставы болят в плечах. А ногах только нижняя косточка по бокам отекшие с ощущением множества маленьких шариков на ощупь

Да, при движении мне намного лучше. Стоит только присесть или прилечь хоть на пол часа, моментально все болит и ломит

Марина, Обезболивающее не пью, не знаю что поможет. Иногда не выдерживаю и мажу Найз гель, помогает, но все равно чувствую те места где болит.

Если с печенью и желудком все прилично, можно и внутрь принимать. Тот-же найз 100мг, например при сильных болях, не больше 200мг в сутки.
Желудок слабый, поверхностный гастрит. А печень сейчас перегружена валацикловиром, в комплексе пью легалон. Поэтому опасаюсь большого приема таблеток

Если это аутоиммунное заболевание, то заглушить его могут только иммунодепрессанты, возможно вместе с гормонами. Препараты серьёзные, как вы понимаете, поэтому назначаются только после внятного диагноза. Никакое ревмо заболевание не развиваются так быстро, что счёт идёт на дни. Так что вы можете спокойно обследоваться. Если будут сильные боли, можно уколоть мелоксикам 15мг внутримышечно, это самый щадящий вариант.
Изучена распространенность и этиологическая структура активной герпесвирусной инфекции у детей с различными формами и вариантами ювенильного артрита, сопоставлены форма и вариант ювенильного артрита у пациентов с активностью герпесвирусной инфекции и без
The article describes the prevalence and etiological structure of the active herpes virus infection in children with different forms and variants of juvenile arthritis, the form and variant peculiarities of juvenile arthritis in patients with active herpes infection, and without it were compared.
В последние десятилетия изучение роли инфекционных (вирусно-бактериальных ассоциаций) и наследственных факторов в развитии хронических воспалительных заболеваний суставов у детей сохраняет свою актуальность. Согласно современным представлениям ювенильный артрит (ЮА) рассматривается как обобщающее понятие, объединяющее гетерогенную группу хронических заболеваний суставов, имеющих различный этиопатогенез и иммуногенетическое происхождение, различную нозологическую принадлежность и неоднозначный прогноз. В группу ЮА можно отнести ювенильный ревматоидный артрит (ювенильный идиопатический артрит (ЮИА)) и ювенильный спондилоартрит (ЮСА), а также ювенильный хронический артрит, который представлен хроническим течением реактивного артрита [1, 2]. Среди ЮА наиболее значимым является ЮИА, приводящий к ранней инвалидизации в детском возрасте [3–5]. ЮИА так же, как ювенильные артриты в целом, представляет гетерогенную группу, в которой выделяют различные формы и варианты течения. Традиционно принято выделение системных и преимущественно суставных форм [3].
ЮА относятся к мультифакториальным заболеваниям, в развитии которых имеют место не только экзогенные (инфекционные и средовые), но и наследственные факторы, в том числе иммуногенетические [3, 5–7]. Развитие и прогрессирование ЮИА определяется сочетанием генетически детерминированных и вторичных дефектов иммунорегуляторных механизмов, приводящих к быстрой трансформации физиологической острой воспалительной реакции в хроническое прогрессирующее воспаление. Однако механизмы становления аутоиммунного патогенеза ЮИА довольно сложны и, несмотря на многочисленные исследования, до конца не раскрыты [6–8]. Влияние вирусной инфекции, в том числе герпесвирусной, в качестве триггерного фактора развития ЮА очевидно, в то время как этиологическая роль только предполагается. Во многом нерешенным остается вопрос об уровне взаимосвязи инфекционных и генетических факторов в развитии и течении ювенильного артрита. По мнению ряда авторов, не исключается возможность инициации инфекционным агентом артрита, особенно у генетически предрасположенного больного [9–11]. В литературе имеются данные о том, что герпесвирусные инфекции у детей с ЮИА не только утяжеляют его течение, но и могут участвовать в реализации патогенетических иммунокомплексных процессов [8, 12].
У детей спектр клинических проявлений герпесвирусной инфекции (ГВИ) весьма разнообразен: он зависит от локализации патологического процесса, его распространенности, состояния иммунной системы больного и антигенного типа вируса [13–15]. По данным литературы у детей с ЮИА выделяется два варианта инфицирования вирусами и бактериями: в начале заболевания и спустя несколько месяцев и лет от его дебюта. Во всех случаях как носительства, так и острой герпесвирусной инфекции ЮИА протекает в виде более тяжелых клинических форм [8, 9], и вирусно-бактериальное инфицирование у детей с ЮИА является прогностически неблагоприятным признаком, указывающим на большую тяжесть болезни с возможностью возникновения необратимых процессов с нарушением функции суставов, развитием висцеритов и васкулитов [3, 8].
Кроме того, использование иммуносупрессивной терапии, а в последние десятилетия генно-инженерных биологических препаратов, мишенью которых являются узловые патогенетические звенья воспалительного процесса (ФНО-α, интерлейкины-1, 6 и т. д.), способствует не только подавлению аутоиммунных реакций, но и создает условия для реактивации латентных вирусных инфекций [16–21].
Поэтому вопрос о роли герпесвирусной инфекции как о причинном агенте, усугубляющем дефект иммунорегуляторных систем и обуславливающем развитие иммунных нарушений, лежащих в основе ЮИА, является актуальным.
Целью настоящего исследования было изучить распространенность активной герпесвирусной инфекции (ГВИ) у больных с различными формами и вариантами ЮА.
Пациенты и методы исследования
В исследование были включены 163 ребенка с воспалительными заболеваниями суставов, наблюдавшиеся в детском ревматологическом отделении на клинической базе (УДКБ № 1) кафедры детских болезней лечебного факультета ФГБОУ ВО Первый МГМУ им. И. М. Сеченова.
При формировании групп больных по нозологическим формам и вариантам течения использовались Берлинские диагностические критерии (Берлин, 1996 г.) реактивного артрита, классификационные критерии ЮСА Гармиш-Партенкирхен (1987 г.) и критерии диагностики ЮИА (1997 г.) Американской коллегии ревматологов (American College of Rheumatology, ACR). Согласно этой классификации и в соответствии с поставленными задачами нами выделялась системная и преимущественно суставная форма ЮИА.
Всем пациентам проводилось комплексное клинико-лабораторное и инструментальное обследование, принятое в детской ревматологии, которое включало оценку жалоб, анамнеза, данных физикального осмотра (выраженность суставного синдрома и внесуставных проявлений), стандартные лабораторные исследования (клинические, биохимические и иммунологические анализы крови, общий анализ мочи), а также инструментальные методы. С целью исключения поражения глаз все больные были осмотрены окулистом, по показаниям — другими специалистами.
У всех обследованных детей методом сплошного скринингового исследования крови осуществлялась идентификация ДНК вирусов герпеса 1-го, 2-го, 3-го, 4-го, 5-го и 6-го типов с помощью качественной ПЦР.
Результаты исследования и их обсуждение
Всего в исследование вошло 163 пациента. С системным ЮИА было 34 ребенка, с суставной формой — 87, с ЮСА — 17, с хроническим реактивным артритом (ХРеА) — 25. Во всех группах, за исключением ЮСА, преобладали девочки — их в 1,4 раза больше мальчиков. Как известно, ЮСА развивается преимущественно у мальчиков подросткового возраста, о чем свидетельствует и средний возраст в этой группе, который составил 14,88 ± 0,6 года в сравнении с другими вариантами ЮА, где средний возраст соответствовал 8–10 годам (табл. 1). Средний возраст дебюта заболевания был наименьшим в группе с суставной формой ЮИА — 3,77 ± 0,3 года, набольшим в группе ЮСА — 9,7 ± 0,59. Средняя продолжительность заболевания в целом по группам составила 5 лет, за исключением ХРеА, где средняя продолжительность заболевания составила 2,98 ± 0,66 года.
В целом ГВИ была выявлена у 81 пациента с ЮА (49,7%). С системным ЮИА — 21 ребенок (62%), что достоверно выше, чем при суставном ЮИА — 39 (45%, р ≤ 0,05).
Частота ГВИ в зависимости от пола и возраста
В группе пациентов с активной ГВИ, как и группе без ГВИ, соотношение девочек и мальчиков было примерно одинаково и составило 1,4:1 (р ≤ 0,005). То есть группы сопоставимы по половому составу.
Анализ распределения по возрасту пациентов с ГВИ и без ГВИ показал, что среди детей с маркерами активной ГВИ достоверно преобладает возрастная группа от 1 года до 6 лет — 65% (р ≤ 0,001), а пациенты без ГВИ в основном 7–11 лет — 67% (р ≤ 0,001). Число пациентов в возрасте 12–17 лет в обеих группах было примерно одинаково — 49% и 51% (р > 0,05) (рис. 1).
Структура герпесвирусной инфекции у пациентов с ЮА
Частота выявления моно- и микст-ГВИ у пациентов с ЮА (n = 81) представлена на рис. 2.
У обследованных детей с различными формами и вариантами ЮА был проведен анализ структуры положительных маркеров активной ГВИ. Моноинфекция (положительный маркер активной ГВИ к одному вирусу герпеса) диагностирована в 47% (53 ребенка), микст-инфекция (положительные маркеры двух и более активных ГВИ) — у 53% (60 детей).
При анализе структуры положительных маркеров ГВИ (табл. 2) достоверно чаще выявлялись положительные маркеры активной инфекции ВПГ 1-го типа — 34 ребенка (30%), по сравнению с положительными маркерами активной ВЗВ-инфекции — 17 детей (15%, р ≤ 0,05). Положительные маркеры активной ВГЧ 6-го типа и ВЭБ-инфекции — у 31 ребенка (27,5%, р > 0,05) соответственно. Положительных маркеров активной ЦМВ-инфекции не было выявлено ни у одного пациента с ЮА, что согласуется с данными зарубежной литературы [19].
У больных с положительными маркерами ГВИ ВЗВ достоверно чаще встречается в виде моноинфекции — 59% (р ≤ 0,05), а ВГЧ 6-го типа достоверно чаще встречался в виде микст-инфекции — 65% (р ≤ 0,001). Положительные маркеры ВПГ 1-го типа и ВЭБ были выявлены примерно в одинаковом проценте случаев — как в виде моноинфекции, так и в составе микст-инфекции (рис. 3).
Анализ положительных маркеров активной ГВИ при различных формах и вариантах ЮА показал (табл. 3), что при суставной форме ЮИА достоверно чаще выявляются положительные маркеры ВПГ 1-го типа и ВГЧ 6-го типа — 33%, по сравнению с ВЗВ — 10% (р ≤ 0,001). У пациентов с ХРеА достоверно чаще выявляются положительные маркеры ВЭБ и ВГЧ 6-го типа — 35%, по сравнению с ВПГ 1-го типа и ВЗВ — 12% (р ≤ 0,001) и 18% (р ≤ 0,005) соответственно. При системной форме ЮИА и ЮСА достоверных различий по частоте встречаемости положительных маркеров ГВИ не получено: ВПГ 1-го типа, ВЭБ, ВГЧ 6-го типа, ВЗВ определяются примерно с одинаковой частотой (рис. 4). Это, вероятно, связано с более высокой вирусной и антигенной нагрузкой: пациенты с системной формой ЮИА получают агрессивную иммуносупрессивную терапию, что увеличивает риск активации латентных и коморбидных инфекций, в том числе ГВИ. Обращает внимание, что при ЮСА положительных маркеров ВГЧ 6-го типа не обнаружено ни у одного пациента. Больные с ЮСА — преимущественно в возрасте 14–15 лет, а инфекция ВГЧ 6-го типа характерна для детей раннего возраста — к пяти годам жизни различными видами герпеса инфицируются до 90% детей [14].
При анализе моно-ГВИ у пациентов с различными формами и вариантами ЮА (табл. 4) выявлено, что при ЮИА (как при суставной, так и при системной форме особенно) преобладает моноинфекция ВЭБ — 27% и 38%. При системной форме ЮИА достоверно реже выявляется моноинфекция ВГЧ 6-го типа — 8% (р ≤ 0,001). У пациентов с суставной формой ЮИА, помимо моноинфекции ВЭБ, преобладает моноинфекция ВПГ 1-го типа и ВГЧ 6-го типа — 35% и 30% соответственно по сравнению с ВЗВ — 8% (р ≤ 0,001). При ЮСА преобладает моноинфекция ВПГ 1-го типа — 58% по сравнению с ВЭБ — 13% (р ≤ 0,001) и ВЗВ — 29% (р ≤ 0,005). Как было показано ранее, маркеры ВГЧ 6-го типа у больных с ЮСА не выявлялись ни у одного ребенка. У больных с ХРеА, напротив, с одинаковой частотой определялись ВПГ 1-го типа, ВЗВ, ВГЧ 6-го типа — 29% по сравнению с ВЭБ — 13% (р ≤ 0,05) (рис. 5).
В общей структуре микст-инфекции у пациентов с ЮА преобладают сочетания ВГЧ 6-го типа + ВЭБ и ВГЧ 6-го типа + ВПГ 1-го типа — в 32% и 25% соответственно, реже встречаются сочетания ВПГ 1-го типа + ВЭБ и ВПГ-1-го типа + ВЗВ — 11% (рис. 6).
Анализ микст-ГВИ у пациентов с различными формами и вариантами ЮА выявил, что микст-инфекция у больных с системным ЮИА составляла 24%, при этом преобладала микст-инфекция ВПГ 1-го типа + ВГЧ 6-го типа, при суставной форме микст-инфекция выявлялась в 15% случаев и была представлена преимущественно сочетаниями: ВПГ 1-го типа + ВГЧ 6-го типа и ВЭБ + ВГЧ 6-го типа. При ЮСА микст-инфекция встречалась реже, чем при других вариантах ЮА, и составляла 12% — в виде сочетания ВЭБ + ВЗВ. При ХРеА микст-инфекция выявлялась в 20%, преобладало сочетание ВЭБ + ВЧГ 6-го типа (рис. 7). Это в целом отражает тенденцию, выявленную при анализе общей структуры положительных маркеров ГВИ: при суставной форме ЮИА достоверно чаще выявляются положительные маркеры ВПГ 1-го типа, при ХРеА — ВГЧ 6-го типа.
Обнаруженные в настоящем исследовании различия в частоте и структуре ГВИ при разных формах и вариантах ЮА требуют дальнейшего анализа с целью оценки влияния ГВИ на клиническое течение ЮА и обсуждением возможной этиопатогенетической роли ГВИ в развитии ЮА.
Выводы
- У больных с различными формами и вариантами ЮА активная ГВИ выявлялась в 49,7%. Среди положительных маркеров ГВИ у детей с ЮА наиболее часто встречаются ВПГ 1-го типа, а реже других — ВЗВ. Активная ЦМВ-инфекция не была диагностирована ни у одного пациента с ЮА.
- При системном варианте ЮИА ГВИ выявляются чаще, чем при других вариантах и формах ЮА, и составляют 62%. Преобладает активная инфекция ВПГ 1-го типа и ВЭБ, чаще встречается микст-герпесвирусная инфекция.
- При суставной форме ИЮА ГВИ выявляется несколько реже, чем при других формах ЮА, — 45% и представлена ВПГ 1-го типа, ВГЧ 6-го типа и ВЭБ (выявляются с одинаковой частотой), в то время как ВЗВ встречается достоверно реже.
- ЮСА характеризуется высокой частотой выявления ГВИ — 53%. Преимущественно за счет ВПГ 1-го типа и ВЗВ. Особенностью ЮСА является отсутствие маркеров ВГЧ 6-го типа.
- При ХРеА частота выявления ГВИ составляет 48%. В структуре ГВИ преобладает ВЭБ и ВГЧ 6-го типа — как в виде моно-, так и в форме микст-инфекции.
Литература
- Cassidy J. T., Petty R. E., Laxer R. M., Lindsley C. B. Textbook of pediatric rheumatology. 6 th ed. Philadelphia: Saunders Elsevier, 2010. 794 р.
- Cellucci T., Guzman J., Petty R. E., Batthish M., Benseler S. M., Ellsworth J. E., Houghton K. M., LeBLANC C. M., Huber A. M., Luca N., Schmeling H., Shiff N. J., Soon G. S., Tse S. M. Management of Juvenile Idiopathic Arthritis 2015: A Position Statement from the Pediatric Committee of the Canadian Rheumatology Association // J Rheumatol. 2016; 43 (10): 1773–1776.
- Жолобова Е. С., Шахбазян И. Е., Улыбина О. В. Афонина Е. Ю. Ювенильный ревматоидный (идиопатический) артрит. В кн.: Геппе Н. А., Подчерняева Н. С., Лыскина Г. А. (ред.). Ювенильный ревматоидный артрит. Рук-во по детской ревматологии. М.: ГЭОТАР-Медиа, 2011. С. 162–245.
- Баранов А. А., Алексеева Е. И., Бзарова Т. М. Протокол ведения пациентов с ювенильным артритом // Вопросы современной педиатрии. 2013; 12 (1): 37–56.
- Ravelli A. Handbook of Juvenile Idiopathic Arthritis. Switzerland, Adis (Springer International Publishing). 2016; 115–124.
- Donn R., De Leonibus., Meyer S., Stevens A. Network analysis and juvenile idiopathic arthritis (JIA): a new horizon for understanding of disease pathogenesis and therapeutic target identification // Pediatr Rheumatol Online J. 2016; 14 (1): 40. DOI: 10.1186/s12969–016–0078–4.
- Кравченко Н. П., Олейник Е. К. Механизмы нарушения иммунологической толерантности // Труды карельского научного центра РАН, 2015; (12): 3–22. DOI: 10. 17076/eb230.
- Соболева Н. Г. Ювенильный ревматоидный артрит у детей Краснодарского края (особенности этиопатогенеза, оптимизация лечебной тактики). Автореф. дис. … д.м.н. Краснодар, 2009.
- Ball R. J., Avenell A., Aucott L., Hanlon P., Vickers M. A. Systematic review and meta-analysis of the sero-epidemiological association between Epstein-Barr virus and rheumatoid arthritis // Arthritis Research & Therapy. 2015; 17: 274. DOI: 10.1186/s13075–015–0755–6.
- Halenius A., Hengel H. Human cytomegalovirus and autoimmune disease // Biomed Res Int. 2014; 2014: 472978. DOI: 10.1155/2014/472978. Epub 2014 Apr 29.
- Draborg A. H., Duus K., Houen G. Epstein-Barr virus in systemic autoimmune diseases // Clin Dev Immunol. 2013; 2013: 535738. DOI: 10.1155/2013/535738. Epub 2013 Aug 24.
- Бочанцев С. В., Потрохова Е. А., Соботюк Н. В., Устян Л. А., Пертельс Т. Г. Диагностика вирусной инфекции Эпштейна–Барр при системной красной волчанке и ревматоидном артрите // Российский педиатрический журнал. 2014; 17 (5): 42–48.
- Исаков В. А., Архипова В. И., Исаков Д. В. Герпесвирусные инфекции человека. СПб: СпецЛит, 2013. С. 51–198.
- Боковой А. Г. Герпесвирусные инфекции у детей: диагностика, клиника и лечение. Роль в формировании контингента часто болеющих детей. Учебное пособие. М.: МАКС Пресс, 2008. 144 с.
- James S. H., Kimberlin D. W. Neonatal Herpes Simplex Virus Infection // Infect Dis Clin North Am. 2015; 29 (3): 391–400. DOI: 10.1016/j.idc.2015.05.001. Epub 2015 Jul 4.
- Davies H. D., Byington C. L., Maldonado Y. A., Barnett E. D., Edwards K. M., Lynfield R., Munoz-Rivas F. M., Nolt D. L., Nyquist A. C., Rathore M. H., Sawyer M. H., Steinbach W. J., Tan T. Q., Zaoutis T. E. Infectious Complications With the Use of Biologic Response Modifiers in Infants and Children // Pediatrics. 2016; 138 (2): e20161209. DOI: 10.1542/peds.2016–1209. Epub 2016 Jul 18.
- Nicolai R., Cortis E., Ravà L., Bracaglia C., Pardeo M., Insalaco A., Buonuomo P. S., Tozzi A. E., De Benedetti F. Herpes Virus Infections During Treatment With Etanercept in Juvenile Idiopathic Arthritis // J Pediatric Infect Dis Soc. 2016; 5 (1): 76–79. DOI: 10.1093/jpids/piu078. Epub 2014 Jul 31.
- Comar M., Delbue S., Lepore L., Martelossi S., Radillo O., Ronfani L., D’Agaro P., Ferrante P. Latent viral infections in young patients with inflammatory diseases treated with biological agents: prevalence of JC virus genotype 2 // J Med Virol. 2013; 85 (4): 716–722. DOI: 10.1002/jmv.23525. Epub 2013 Jan 30.
- Kawada J., Iwata N., Kitagawa Y., Kimura H., Ito Y. Prospective monitoring of Epstein-Barr virus and other herpesviruses in patients with juvenile idiopathic arthritis treated with methotrexate and tocilizumab // Mod Rheumatol. 2012; 22 (4): 565–70. DOI: 10.1007/s10165–011–0552–2. Epub 2011 Nov 5.
- Zhang N., Wilkinson S., Riaz M., Ostor A. J., Nisar M. K. Does methotrexate increase the risk of varicella or herpes zoster infection in patients patients with juvenile rheumatoid arthritis? A systematic literature review // Clin Exp Rheumatol. 2012; 30 (6): 962–71. Epub 2012 Dec 17.
- Che H., Lukas C., Combe B. Risk of herpes/herpes zoster during antitumor necrosis factor therapy in patients with rheumatoid arthritis. Systematic rewiew and meta-analysis // Joint Bone Spine. 2014; 81 (3): 215–221. DOI: 10.1016/j.jbspin.2013.07.009. Epub 2013 Aug 7.
Е. Ю. Солдатова* , 1
Е. С. Жолобова**, доктор медицинских наук, профессор
Е. В. Мелёхина*, кандидат медицинских наук
А. В. Горелов**, доктор медицинских наук, профессор, член-корреспондент РАН
* ФГУН ЦНИИЭ Роспотребнадзора, Москва
** ФГБОУ ВО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Постгерпетическая невралгия (ПГН) — это осложнение опоясывающего герпеса, вызванного тем же вирусом, что и ветряная оспа (лат. herpes zoster virus). При этом заболевании поражаются кожа и нервные волокна, что проявляется сильной жгучей болью уже после заживления герпетических пузырей.
Риск возникновения постгерпетической невралгии увеличивается с возрастом; чаще всего этому заболеванию подвержены люди старше 60-ти лет. Данное состояние возникает примерно у 10–20% пациентов, перенесших опоясывающий герпес . Его вылечить нельзя, но лечение постгерпетической невралгии может облегчить симптомы и снять боль. Больше чем у половины пациентов боли проходят сами по себе спустя некоторое время.
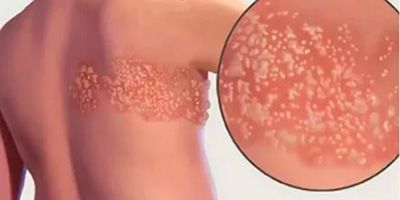
Симптомы постгерпетической невралгии, как правило, ограничиваются той областью кожи, где впервые возникли высыпания — чаще всего они опоясывают туловище или появляются сбоку, впрочем заболевание может поражать и лицо.
Болевые ощущения могут длиться в течение 3-х месяцев и дольше после заживления герпетических пузырьков. Пациенты описывают её, как жгучую, острую, пронзающую или глубокую, она возникает даже при малейшем прикосновении к коже в поражённой области, в том числе и от лёгкого прикосновения одежды (аллодиния). Гораздо реже больные чувствуют зуд и онемение.
Причины постгерпетической невралгии
После того как человек перенёс ветряную оспу, вирус остаётся в организме на всю жизнь. С возрастом иммунная система ослабевает (в частности — от приёма лекарств или химиотерапии) и вирус может активизироваться, в результате чего возникает опоясывающий лишай.
Повреждение нервных окончаний при высыпаниях приводит к возникновению постгерпетической невралгии. Будучи повреждёнными, нервные волокна не могут посылать сигнал от кожи к мозгу так, как они это делают в норме. Вместо этого, ими передаются усиленные сигналы, а пациент чувствует мучительную боль, которая может длиться месяцами или даже годами.
Факторы риска
Если у вас появились признаки опоясывающего лишая, то риск возникновения постгерпетической невралгии значительно усиливается при следующих условиях:
- возраст старше 50-ти лет;
- ярко выраженные симптомы опоясывающего лишая, имеются обильные высыпания и интенсивная боль;
- наличие сопутствующих заболеваний, в том числе сахарного диабета;
- наличие высыпаний на лице.
Осложнения
При длительном течении заболевания, особенно если оно сопровождается очень сильным болевым синдромом, у пациентов часто возникают следующие осложнения:
- депрессия;
- усталость;
- нарушения сна;
- потеря аппетита;
- сложности с концентрацией внимания.
Наши врачи
Методики лечения
На вопрос о том, как лечить постгерпетическую невралгию невозможно дать однозначный ответ, поскольку не существует универсального лечения данного заболевания, которое бы подходило всем больным. Как правило, требуется кропотливый подбор лекарственных препаратов и методик (а иногда — и их сочетание) для того, чтобы облегчить боль пациента.
Лидокаиновые пластыри
Это пластыри, содержащие местное обезболивающее средство — лидокаин. Их следует наклеивать на поражённый участок кожи. За счёт постоянного равномерного выделения анестетика, такие пластыри приносят временное облегчение, снижая болевые ощущения и давая передышку.
Пластыри с высоким содержанием капсаицина
Это современный метод обезболивания при постегрпетической невралгии, который заключается в следующем: содержащееся в пластыре вещество является производным жгучего перца, который блокирует болевые рецепторы кожи. Аппликация такого пластыря может проводиться только врачом. Процедура занимает 2 часа, но хороший обезболивающий эффект от неё пролонгирован и может сохраняться до 3-х месяцев. Если возникнет необходимость, процедуру повторяют.
Медикаментозная терапия
Медикаментозная терапия предусматривает использование следующих групп препаратов:
Эпидуральное введение анестетиков и стероидных гормонов
Эпидуральная блокада позвоночника предусматривает введение препаратов в эпидуральное пространство, что приводит к утрате чувствительности в области воздействия. Это значит, что данная процедура предусматривает введение действующего вещества непосредственно в источник боли. Достижение лечебного эффекта в данном случае возможно за счёт следующих факторов:
- обезболивающие свойства препарата;
- максимально возможная концентрация в поражённой области;
- рефлекторное действие на всех уровнях нервной системы.
Радиочастотная деструкция нервов
Радиочастотная деструкция нервов обеспечивает стойкий обезболивающий эффект, который сохраняется до года и более. Это малоинвазивная нехирургическая процедура, которая позволяет значительно облегчить боль в тех случаях, когда другие способы
Лечение постгерпетической невралгии в ЦЭЛТ
Если у вас или ваших близких присутствует данная патология мы рекомендуем обратится в Клинику Боли ЦЭЛТ. Наши специалисты по лечению боли (алгологи) владеют всеми перечисленными методиками и смогут подобрать наиболее эффективную для каждого пациента.
Важно, что при некоторых из них пациент получает практически мгновенный устойчивый эффект обезболивания, который длится продолжительное время.
Читайте также:

