Может герпес вызвать воспаление суставов
Обновлено: 25.04.2024
Рассмотрены первичные и вторичные системные васкулиты у детей, клинические проявления, частота встречаемости, подходы к лечению. Приведен клинический пример.
Primary and secondary systemic vasculitis in children were considered, as well as clinical manifestations, frequency and approaches to treatment. A clinical case was given.
Ангиит или васкулит у детей — первичное или вторичное воспаление стенок кровеносных сосудов.
Первичные системные васкулиты — группа заболеваний, характеризующихся поражением стенки сосудов различного калибра (от микроциркуляторного русла до аорты и ее ветвей) по типу очагового воспаления и некроза с последующим вовлечением в патологический процесс органов и тканей в зоне сосудистого повреждения.
Вторичные васкулиты развиваются при инфекционных, аутоиммунных, ревматических, онкогематологических и других заболеваниях [1, 2].
Этиология большинства первичных васкулитов неизвестна. Полагают, что их возникновению у ребенка могут способствовать частые острые инфекционные болезни, очаги хронической инфекции, лекарственная аллергия, наследственная предрасположенность к сосудистым или ревматическим заболеваниям. Бактериальные или вирусные инфекции (стрептококковая, герпесвирусная, парвовирусная, гепатит В или С), с одной стороны, аллергия или отягощенный аллергологический анамнез. с другой стороны, по мнению специалистов, служат двумя равновеликими факторами, формирующими фон для гиперсенсибилизации организма или выступающими как триггерные, провоцирующие факторы.
В настоящее время установлено, что вирусная инфекция Эпштейна–Барр (ЭБВ) и инфекция герпеса человека 6-го типа ассоциированы с целым рядом аутоиммунных заболеваний (классические ревматические болезни, васкулиты, неспецифический язвенный колит и др.). Известно, что вирус герпеса человека 6-го типа у детей при первичном инфицировании и при его реактивации вызывает инфекционную эритему с симптомами васкулита, который наблюдается в 3 раза чаще, чем при ЭБВ и цитомегаловирусной инфекции (ЦМВ) [3–5].
Эти вирусы могут вызывать хронические манифестные и стертые формы заболевания, протекающие по типу хронического мононуклеоза. При этом развитие аутоиммунного заболевания может манифестировать через большой промежуток времени после инфицирования.
Герпетическая инфекция гистологически манифестирует отложением фибрина в микрососудах, при этом меняется поверхностная конформация эндотелия; на инфицированном эндотелии в 2–3 раза повышается уровень выработки тромбина, уменьшается тканевая экспрессия тромбомодулина и активация белка С (G. M. Vercelotti, 1990).
Изменения в области поврежденного участка сосуда разнообразны — от ишемии до кровоизлияния, некроза, инфаркта. Степень сосудистых расстройств зависит от калибра пораженных артерий и состояния коллатерального кровообращения [2].
Большое значение в развитии васкулитов имеют формирование, циркуляция и осаждение на стенках сосудов иммунных комплексов, антинейтрофильных цитоплазматических антител, иммунное пролиферативно-деструктивное воспаление стенки артерий различного калибра, повреждение эндотелия сосудов, повышение сосудистой проницаемости, гиперкоагуляция с нарушением кровотока, ишемия в зоне повреждения сосудов.
В начальный период васкулитов наблюдают общие проявления неспецифического воспалительного синдрома: субфебрильная или фебрильная лихорадка, артралгии, похудание, симптомы периферических и висцеральных сосудистых расстройств, умеренная анемия, лейкоцитоз в периферической крови, увеличение СОЭ, признаки гиперкоагуляции, диспротеинемия, повышение уровня С-реактивного белка, IgA, циркулирующих иммунных комплексов и криоглобулинов [2].
Своеобразие клинических проявлений обусловлено локализацией васкулита, калибром пораженных сосудов, распространенностью патологического процесса, особенностями морфологических изменений (преобладание деструктивных или пролиферативных процессов), степенью расстройств гемодинамики и ишемии органов и тканей.
Доказан сосудистый генез массивных кровоизлияний и некрозов при герпесвирусных энцефалитах. Ярким свидетельством морфологических изменений сосудов, которые удается прижизненно визуализировать при этих инфекциях, являются данные зарубежных и отечественных исследователей, указывающие на развитие коронарита после острой и чаще на фоне хронически текущей ЭБВ-инфекции, а также системного васкулита (синдрома Кавасаки). Коронарные повреждения обнаружены у 55% детей, перенесших ЭБВ-инфекционный мононуклеоз c длительностью лихорадки свыше 5 дней.
Известно, что при герпесвирусной инфекции имеет важное значение способность вирусов к цитопатическому эффекту, проявляющих тропизм к кровеносным сосудам. Поражение сосудов при ЭБВ регистрируется в 7–30%, а при ЦМВ — у 8% [4, 6–8].
Вирус герпеса человека 6-го типа у детей при первичном инфицировании и при его реактивации вызывает инфекционную эритему с симптомами васкулита, который наблюдается в 3 раза чаще, чем при ЭБВ- и ЦМВ-инфекции.
В течение нескольких лет авторами изучалась частота встречаемости и клинических проявлений синдрома васкулита у детей при различных вариантах течения герпесвирусных инфекций. Исследования проводились у 202 больных в возрасте от одного года до 14 лет, из них — 160 детей с инфекционным мононуклеозом (ИМ) и 42 — с синдромом васкулита без признаков инфаркта миокарда, находившихся в соматических и инфекционных отделениях Морозовской городской детской клинической больницы г. Москвы.
Кроме того, при УЗДГ-исследовании оценивалось состояние комплекса интима-медиа и состояния сосудов головы и шейной области у 20 детей в возрасте от 6 мес до 14 лет с активно персистирующими герпесвирусными инфекциями (ЭБВ, ЦМВ и ВГЧ 6-го типа без признаков ИМ) в условиях многопрофильной клиники Vessel Clinic.
В клинико-лабораторном мониторинге наблюдения за больными проводились исследования:
- общих анализов периферической крови, мочи, биохимии крови, коагулограммы;
- бактериологические исследования микробиоценоза ротоглотки, кишечника, паразитарных инфекций, гельминтов;
- серологические исследования осуществлялись методами: реакция иммунофлуоресценции (РИФ) на респираторные вирусы и РИФ с моноклональными антителами к белкам ЦМВ pp 65, рр 72;
- непрямая реакция иммунофлуоресценции (НРИФ) на антигены герпесвирусов в клетках крови и иммуноферментный анализ (ИФА) на герпесвирусы 1-го, 2-го, 4-го, 5-го и 6-го типов; микоплазмы, хламидии, парвовирус 19-го типа и др.;
- полимеразная цепная реакция (ПЦР) на ДНК ЭБВ, ЦМВ, ВПГ 1-го типа, ВПГ 2-го типа; ВГЧ 6-го типа в крови, слюне и моче.
Проявления васкулита имели место при всех этиологических вариантах ИМ в виде пятнисто-папулезной или пятнисто-папулезной с геморрагическим компонентом сыпи, которая чаще расценивалась как токсико-аллергическая у больных, получавших антибиотики аминопенициллинового ряда и реже у не получавших подобных препаратов (рис. 1, 2).
Проявления васкулита в виде геморрагической сыпи, по типу кожной пурпуры, с признаками тромбоваскулита отмечались у большинства больных, страдающих герпесвирусной активно персистирующей инфекцией без признаков инфекционного мононуклеоза, при этом сыпь не имела характерной для геморрагического васкулита (по типу Шенлейна–Геноха) локализации, элементы которой появлялись на различных участках кожи: в области груди, живота, спины, подмышечной впадины, голенях, которые распространялись на фоне лихорадки, а затем стихали. В местах сыпи у некоторых больных появлялась пигментация.
При дуплексном сканировании сосудов головы и шеи при активно персистирующих герпесвирусных инфекциях выявлялись ЭХО-признаки затруднения венозного оттока или ангиоспазма артерий Виллизиева круга, при явном уплотнении комплекса интима-медиа (КИМ) сосудов, что косвенно указывало на эндотелиальную дисфункцию, развившуюся, вероятнее всего, в результате длительного цитопатического воздействия на сосудистый эндотелий непосредственно активно персистирующих герпесвирусов.
.jpg)
В качестве клинического примера представлена история болезни ребенка Елизаветы С., 2 г. 11 мес (28.10.2010 г. рождения).
Состояние при поступлении тяжелое. Температура тела — 37,2? С. Кожные покровы бледные, на коже нижних конечностей пятнисто-папулезная сыпь с геморрагическим пропитыванием, элементы разных размеров, склонные к слиянию на стопах, несколько элементов на верхних конечностях, в области локтей.
Ангионевротические отеки левой стопы, правой кисти, движения в правом голеностопном суставе затруднены.
Зев гиперемирован, миндалины — налетов нет. Передне- и заднешейные, подчелюстные лимфоузлы до 2 см, безболезненные, не спаянные с окружающими тканями.
По остальным органам без видимой патологии.
УЗИ органов брюшной полости, почек, селезенки от 24.10.2013: ЭХО-признаки умеренной гепатомегалии, мезаденита.
По другим органам без выраженных структурных изменений и патологических включений.
Осмотр ЛОР-врача от 24.10.2013 — диагноз: левосторонний острый средний катаральный отит.
Результаты анализов крови представлены в таблицах 1–3.
За время пребывания в отделении отмечалось три волны высыпаний с крупными геморрагическими сливными элементами в бедренных и подколенных областях обеих конечностей и ангионевротическими отеками (рис. 3).
Клинический диагноз: геморрагический васкулит, смешанная форма (кожно-суставной синдром), протекающий на фоне реактивации смешанной персистирующей герпесвирусной инфекции ЭБВ, ВГЧ 6-го типа и бактериальной инфекции.
.jpg)
Рекомендовано включить в лечение глюкокортикоиды и Виферон по 1 млн в суппозиториях.
- Режим боксовый.
- Стол 15.
- Цефтриаксон 550 мл 2 раза в день в/в капельно 25.10.2013–30.10.2013 г.
- Супрастин 0,3 2 раза в день на физрастворе в/в.
- Бифидумбактерин 5 доз 3 раза в день в рот.
- Преднизолон 25 мг в/в в 10:00 с 25.10.2013–28.10.2013 г.
- Преднизолон 3 раза в день, в рот после завтрака — 10 мг, после обеда — 7,5 мг, после ужина — 5 мг с 31.10.2013 г.
- Гепарин 0,3 подкожно 6:00, 14:00, 22:00 с 25.10.2013–11.2013 г.
- Курантил 25 мг в таблетках 3 раза в день в рот с 25.10.2013–11.2013 г.
- Орошение зева Мирамистином 3 раза в день.
- Туалет носа физраствором 3 раза в день.
- Нафтизин 0,05% 1 капля 3 раза в день в нос.
- Отипакс 3 капли 3 раза в день в левое ухо.
- Мукалтин 1 таблетка 3 раза в день в рот.
- Свечи Виферон 500 000 1 раз в день ректально.
- Лосек 5 мг 2 раза в день, в рот за 30 мин до еды, на ночь с 31.10.2013–11.2013 г.
- Инфузионная терапия.
Состояние ребенка при выписке удовлетворительное. Не лихорадит. Катаральные явления купированы. Кожа чистая. Зев рыхлый. В легких дыхание пуэрильное, хрипов нет. Тоны сердца умеренной громкости, ритмичные. Живот мягкий, безболезненный. Стул и диурез в норме. Менингеальных знаков нет. Ребенок выписан домой с улучшением под наблюдение участкового педиатра.
Таким образом, в практической деятельности врача педиатра инфекциониста, семейного врача необходимо определять маркеры активной репликации герпетических вирусов 4-го, 5-го и 6-го типов не только у больных с типичными клиническими проявлениями инфекционного мононуклеоза, у длительно лихорадящих, часто болеющих; у детей с лимфаденопатиями, но и с синдромом васкулита с целью уточнения триггерных факторов его развития, а также предупреждения часто неоправданного и длительного назначения антибиотиков при ИМ и обоснования адекватной противовирусной терапии.
Лечение назначают с учетом нозологического диагноза, фазы болезни и ее клинических особенностей.
Выбор методов лечения васкулита предполагает воздействие на возможную причину и основные механизмы развития болезни. Воздействие на триггерный инфекционный агент, подавление иммунного воспаления путем назначения препаратов противовоспалительного и иммунодепрессивного действия: глюкокортикоидов (преднизолон, метилпреднизолон), цитостатиков (циклофосфамид, метотрексат).
Удаление антигенов и циркулирующих иммунных комплексов с использованием внутривенного введения антител, плазмафереза синхронно с пульс-терапией глюкокортикоидами и/или цитостатиками. Коррекция гемостаза: назначение антикоагулянтов, антиагрегантов. Симптоматическая терапия.
Эффект лечения оценивают по динамике клинических синдромов и лабораторных показателей. Лечение в острую фазу заболевания проводят в стационаре, затем продолжают амбулаторно при обязательном диспансерном наблюдении и контроле.
Литература
- Лыскина Г. А. Системные васкулиты. В кн.: Детская ревматология. Руководство для врачей / Под ред. А. А. Баранова, Л. К. Баженовой. М.: Медицина, 2002. С. 221–270.
- Vanhoutte P. M., Mombouli J. V. Vascular endothelium: vasoactive mediators // Prog. Cardiovasc. Dis. 1996. V. 39. Р. 229–238.
- Yamashita S., Murakami C., Izumi Y. Severe chronic active Epstein- Barr virus infection accompanied by virus-associated hemophagocytic syndrome, cerebellar ataxia and encephalitis // Psychiatry Clin. Neurosci. 1998. Aug; 52 (4): 449–452.
- Kragsbjerg P. Chronic active mononucleosis // Scand. J. Infect. Dis. 1997. 29 (5): 517–518.
- Okano M. Epstein-Barr virus infecion and its role in the expanding spectrum of human diseases // Acta Paediatr. 1998. Jan; 87 (1): 11–18.
- Толстикова Т. В., Брегель Л. В., Киклевич В. Т., Субботин В. М. Коронариты у детей // Сиб. мед. журн. 2009. № 2. С. 67–69.
- Nakagawa A., Ito M., Iwaki T. et al. Chronic active Epstein-Barr virus infection with giant coronary aneurysms // Am. J. Clin. Pathol. 1996. Vol. 105. N6. P. 733–736.
- Егорова О. Н., Балабанова Р. М., Чувиров Г. Н. Значение антител к герпетическим вирусам, определяемых у больных с ревматическими заболеваниями // Терапевтический архив. 1998. № 70 (5). С. 41–45.
Ф. С. Харламова* , 1 , доктор медицинских наук, профессор
Н. Ю. Егорова*, кандидат медицинских наук
О. В. Шамшева*, доктор медицинских наук, профессор
Н. Л. Вальтц**
А. В. Денисова***
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
*** Многопрофильная клиника Vessel Clinic, Москва
Человек постоянно контактирует с окружающей средой, а значит и с населяющими ее микроорганизмами, многие из которых являются патогенными, способными вызвать воспалительный процесс. Инфекционный артрит развивается при попадании инфекции в сустав. Предупредить тяжелые осложнения этого заболевания может только своевременное обращение за медицинской помощью.
Общие сведения о заболевании
Инфекционный артрит – это воспаление сустава, вызванное местной или общей инфекцией. Симптомы болезни и ее течение во многом зависят от вызвавшей инфекционный процесс инфекции.
Коды инфекционных артритов по МКБ-10:
- стафилококковый - M00.0;
- пневмококковый - M00.1;
- стрептококковые - M00.2;
- вызванные другими уточненными бактериальными возбудителями - M00.8;
- пиогенный неуточненный - M00.9;
- туберкулезный – М01.1;
- гонококковый - M01.3;
- вирусный – М01.5.
Заболевание очень распространено и может стать причиной стойкого нарушения суставной функции. Четверть пациентов, обращающихся по поводу заболеваний суставов, страдают инфекционными артритами.
Причины инфекционного артрита
Причиной заболевания является инфекция – гнойная инфекция из расположенных рядом очагов (флегмон, абсцессов) или занесенная с током крови при холециститах тонзиллитах, а также общие инфекционные заболевания. При попадании инфекционных возбудителей в сустав иммунная система начинает с ними бороться, вызывая воспалительный процесс, течение которого напрямую связано с особенностями инфекционного возбудителя.
Воспаление может быть:
- неспецифическим – то есть, иметь общие симптомы, характерные для воспалительных процессов; вызываются такие процессы гноеродной патогенной и условно-патогенной микрофлорой – стафилококками, стрептококками, синегнойной и кишечной палочками и др.; вызываемые ими воспалительные процессы носят обычно острый гнойный характер и протекают остро, особенно, у детей;
- специфическим – при таком воспалении развиваются, как общие симптомы, характерные для всех артритов, так и симптомы, свойственные данной инфекции; к таким инфекциям относят туберкулезный, бруцеллезный, гонорейный, вирусный, грибковый, паразитарный воспалительные процессы.
Инфекционные артриты имеют два механизма развития:
- бактериально-метастатический – воспаление начинается из-за присутствия в суставе инфекции;
- токсико-аллергический – воспаление развивается за счет общей интоксикации и неадекватного иммунного ответа на внедрение в организм инфекции;
- смешанный – действуют оба механизма.
Факторы, предрасполагающие к развитию инфекционного артрита: вредные привычки, поднятие тяжестей, наличие лишней массы тела, сахарного диабета. Гнойные поражения суставов особенно часто развиваются у женщин, страдающих ревматоидным артритом.
Симптомы инфекционного атрита
Инфекционный артрит обычно начинается и протекает остро, иногда подостро. Но при некоторых специфических инфекциях он имеет незаметное начало и длительное течение.
Начало болезни и первые симптомы
При остром начале основными симптомами инфекционного артрита являются: выраженная лихорадка, озноб, летучие мышечно-суставные боли в сочетании с резкой болезненностью в пораженном суставе, отеком и гиперемией кожи над ним. Практически всегда остро протекает инфекционный артрит у детей.
Подострое течение имеет не такое заметное начало, температура тела нормальная или субфебрильная. Отек, гиперемия и боль в суставах умеренные.
Самым опасным является скрытое, незаметное течение, характерное для туберкулезного артрита. Характерны неопределенные боли в суставах, похрустывание, снижение двигательной активности. Болезнь протекает на фоне туберкулеза, небольшое повышение температуры также может не привлечь внимания, поэтому туберкулезный артрит редко выявляется на ранних стадиях.
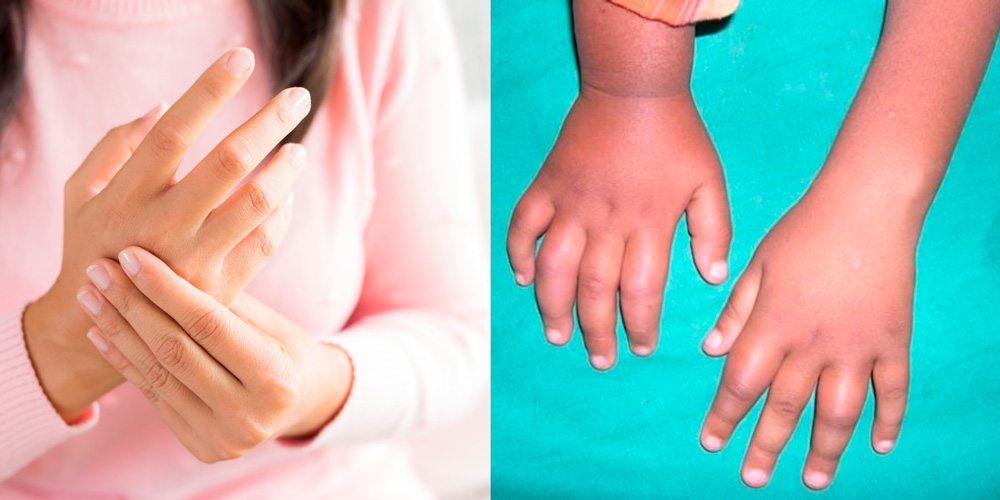
Боли и и отеки характерны для начальной стадии инфекционного токсико-аллергического артрита у детей и взрослых
Явные симптомы
Острый гнойный артрит развиваются очень быстро, состояние ухудшается с каждым днем, беспокоит лихорадка, отечность, гиперемия и боль нарастают. Не исключено, что больному потребуется хирургическая помощь.
При более медленном течении симптомы инфекционного артрита развиваются постепенно, появляется общее недомогание, слабость, суставные боли становятся постоянными, усиливаясь при движении. Постепенно нарушается функция конечностей: появляются трудности в их сгибании или разгибании.
Когда необходимо обращаться за медицинской помощью
К врачу нужно обращаться при появлении следующих симптомов:
- постоянных или регулярно повторяющихся болях в суставах;
- появлении лихорадки, недомогания в сочетании с болями в суставах;
- отека, гиперемии кожи над суставом в сочетании с лихорадкой у пациентов, уже страдающих хроническим артритом – возможно, к имеющемуся хроническому воспалению присоединилась инфекция;
- появление суставных болей при туберкулезе легких, гонорее, бруцеллезе и др. инфекционных заболеваниях.
Опасности
Заболевание часто протекает тяжело, с осложнениями.
Стадии заболевания
Течение болезни связано с ее клинической формой, поэтому стадии развития патологического процесса могут иметь значительные различия. Рассмотрим стадии развития острого гнойного артрита, разработанные НИИ им. Вишневского:
- Начальная – гнойный процесс без деструкции внутрисуставных тканей:
- А. - без поражения околосуставных тканей;
- В. – с развитием гнойных процессов в прилегающих тканях.
- Развернутая – гнойный артрит с деструкцией внутрисуставных тканей:
- А. - без поражения околосуставных тканей;
- В. – с гнойным поражением окружающих мягких тканей.
- Запущенная – с поражением костной и хрящевой ткани:
- А. - без поражения окружающих тканей;
- В. – с гнойным поражением данных тканей;
- С. – с выходом гноя на поверхность тела (свищами).
- Завершающая:
- при отсутствии адекватного лечения – деструкция, неподвижность сустава, инвалидизация;
- при правильном лечении – полное или частичное восстановление функции конечности.
Возможные осложнения
Инфекционный артрит может давать ранние и поздние осложнения. К ранним осложнениям относятся в основном осложнения гнойного артрита:
- нагноение околосуставных тканей;
- генерализация инфекции, сепсис.
Отдаленные последствия – это утрата функции конечности разной степени: от легкой до полной неподвижности.
Классификация
Происхождение и симптомы инфекционного артрита разных клинических форм имеют, как сходство, так и отличие. Рассмотрим наиболее распространенные формы.
Острый гнойный
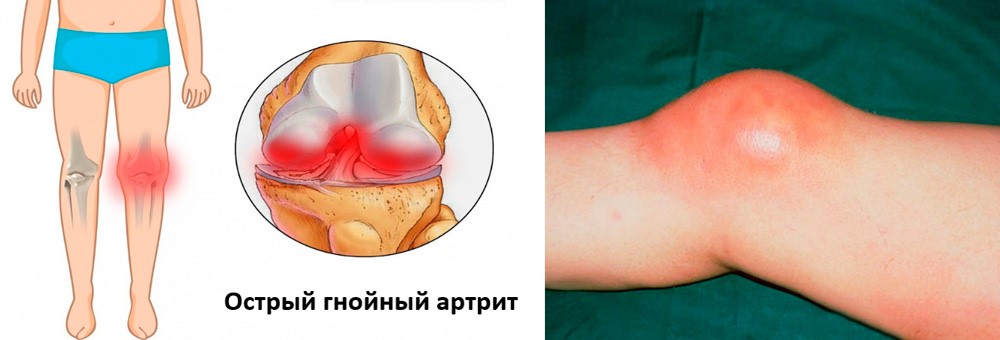
Острый гнойный артрит коленного сустава
Данная форма заболевания развивается при попадании в сустав гноеродной инфекции (синегнойной палочки, стафилококков, стрептококков и др.). Заражение может быть первичным при ранениях и вторичным – при переходе инфекции из окружающих тканей или отдаленных очагов инфекции. К группе риска относятся лица, страдающие ревматоидным артритом, особенно, женщины.
Начинается заболевание остро и протекает тяжело. Появляется лихорадка, головная боль, озноб. Пораженный сустав отекает, кожа над ним краснеет. Боль настолько сильная, что больной не может пошевелить конечностью и старается придать ей положение, вызывающее наименьшую болезненность.
Без оказания своевременной помощи суставные поверхности быстро разрушаются с ограничением подвижности конечности. При назначении адекватного лечения наступает полное выздоровление.
Септический
Развивается на фоне уже существующего сепсиса – генерализованного инфекционного процесса. Инфекция попадает в суставную полость гематогенным путем - с током крови. Заболевание может протекать в виде:
- бактериально-метастатической формы с симптомами острого гнойного артрита – состояние пациента может быть крайне тяжелым; прогноз заболевания зависит от своевременного лечения;
- токсико-аллергической формы – течение не всегда имеет острый характер, часто протекает подостро с множественным поражением суставов мигрирующего (чередующегося) характера; процесс носит негнойный характер и заканчивается выздоровлением на фоне излечения сепсиса.
Туберкулезный
Артрит в данном случае также протекает в виде бактериально-метастатической и токсико-аллергической форм. В первом случае поражаются в основном позвоночник и крупные суставы конечностей, а заболевание носит название костно-суставного туберкулеза. Протекает изначально хронически с нарастающими болями при движении, общим недомоганием. Основные изменения видны на рентгене в виде поражения суставной костной ткани от появления пятна с утратой костью кальция до разрушения кости. При отсутствии лечения приводит к инвалидности.
Токсико-аллергическая форма впервые описанная Понсе в начале 20-го века, протекает очень похоже на ревматоидный артрит с хроническим началом и поражением мелких суставов кисти и стоп. Возможна также их деструкция и инвалидизация. Поражение крупных суставов иногда протекает без последствий и проходит на фоне противотуберкулезной терапии.
Хондропротекторы что это как выбрать, насколько они эффективны
Боль в суставах в состоянии покоя
Гонорейный
Поражение суставов гонококковой инфекцией может иметь бактериально-метастатическую и токсико-аллергическую формы. В обоих случаях поражаются крупные суставы, чаще всего один коленный (голеностопный, лучезапястный). Протекает болезнь остро, с высокой температурой, интоксикацией и сильнейшими суставными болями. Колено отекает, краснеет, до него невозможно дотронуться из-за болей.
При проведении своевременного лечения болезнь имеет благоприятный исход. Если же не лечить, быстро наступает полная неподвижность конечности.
Боррелиозный
Боррелиоз или болезнь Лайма – это инфекция, вызываемая спиралевидными бактериями – спирохетами боррелиями. Передается она клещами и протекает в виде последовательной смены стадий:
- Через 1-2 недели после укуса клеща появляются повышение температуры тела, интоксикация, скованность мышц и появление на теле в месте укуса клеща покраснения - эритемы, окруженной концентрическими кольцами, распространяющейся на большие участки тела. При своевременном назначении антибактериальной терапии заболевание может закончиться на этой стадии.
- Развивается через 1 – 3 месяца после начала заболевания и проявляется в виде поражений нервной системы (менингитов, невритов с острыми болями) и сердца (сердечных блокад, миокардитов и др.).
- Поражение суставов начинается через полгода (иногда через 2 года) после начала заболевания у генетически предрасположенных людей и протекает в виде сильных суставных болей, доброкачественного рецидивирующего воспалительного процесса, протекающего по типу инфекционно-аллергического артрита с асимметричным поражением 1 – 2 суставов (чаще всего коленного) и заканчивающегося через несколько лет выздоровлением у большинства больных. Но у некоторых пациентов заболевание может переходить в хроническую форму с постепенным нарушением функции конечностей.
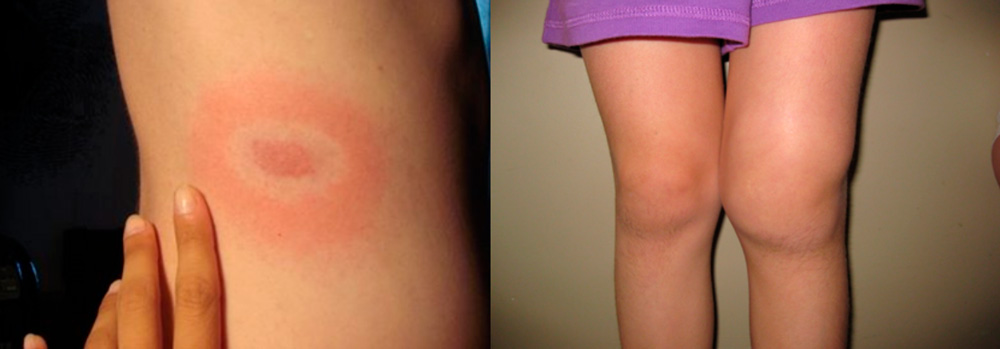
Начальная стадия боррелиоза – мигрирующая эритема и 3 стадия - хронический артрит колена
Вирусный
Развивается на фоне различных вирусных заболеваний:
- Парвовирусная инфекция, вызванная парвовирусом B19 – заболевание протекает с интоксикацией, лихорадкой, кожными проявлениями в виде красных пятен, возвышающихся над кожей папул и точечных подкожных кровоизлияний. Одновременно происходит симметричное поражение суставов. Могут вовлекаться мелкие суставчики кисти, лучезапястные, локтевые, коленные, голеностопные суставы. Симптомы похожи на ревматоидные поражения, но протекают от 3 месяцев до года и имеют благоприятный исход.
- Краснуха – артрит развивается чаще у взрослых женщин на фоне уже имеющихся симптомов краснухи или перед их появлением. У детей такие поражения встречаются редко. Околосуставные ткани отекают, краснеют, появляются сильные боли, нарушающие суставную функцию. Поражение асимметричное с вовлечением мелких суставов кисти, лучезапястных, коленных, локтевых суставов. Артрит продолжается две-три недели, после чего наступает полное выздоровление.
- Вирусные гепатиты В и С – артриты развиваются достаточно часто, но имеют доброкачественное течение и заканчиваются полным выздоровлением. Поражаются мелкие суставы кисти, локтевые, голеностопные и реже другие суставы. Воспаление в суставах обычно начинается до появления желтухи и заканчивается в период ее разгара.
Грибковый
Чаще всего грибковые поражения суставов развиваются при актиномикозе, но встречаются и при другой грибковой инфекции. Патогенные грибки попадают в суставную полость из расположенного рядом костного очага поражения или из отдаленных очагов (кариозные зубы) с током крови. Течение хроническое, с рецидивами и возможным присоединением бактериальной инфекции. Очень часто возникают свищи – ходы, по которым гной из сустава выделяется на поверхность кожи. При отсутствии адекватного лечения приводит к постепенной утрате суставной функции.
Паразитарный
Причиной артрита обычно является эхинококкоз, поражающий костную ткань позвонков, костей таза и длинных костей конечностей. В суставах обычно развивается токсико-аллергический воспалительный процесс. Часто вовлекаются суставы позвоночника, тазобедренные, коленные и локтевые суставы. Течение доброкачественное, но сопровождается сильными суставными болями. Выздоровление наступает при назначении полноценного лечения эхинококкоза.
Инфекционно-аллергический артрит
Инфекционно-аллергический артрит возникает, когда есть аллергия, на фоне которой развивается при неблагоприятных условиях воспалительный процесс в суставах. Заболевание протекает в бурной форме, сопровождается высокой температурой и сильными болевыми признаками. В области поражения наблюдается покраснение, отечность, припухлость. На разных участках кожи – кольцеобразная аллергическая сыпь. Лечением инфекционно-аллергического артрита занимаются ревматолог и аллерголог.
Локализация инфекционного артрита
При инфекционном поражении суставов локализация патологического процесса зависит от особенностей инфекции и ее клинической формы. При острых гнойных артритах – это в основном крупные суставы – коленный, голеностопный, локтевой. Мелкие суставы кисти и стопы поражаются при токсико-аллергической форме туберкулезного и некоторых вирусных артритах.
Асимметричное поражение одного-двух крупных суставов характерно для боррелиоза, чаще всего при этой инфекции в процесс вовлекаются коленные суставы.
Острый артрит – что это такое
Это воспалительный процесс в суставной полости, протекающий с ярко выраженными симптомами. Если воспаление развивается в одном суставе, то носит название моноартрита, в двух - трех – олигоартрита, при множественном поражении - полиартрита.
Заболевание может развиваться в любом возрасте у мужчин и женщин. Отдельные его виды чаще поражают женщин (ревматоидный артрит) или мужчин (реактивный артрит). Код по Международной классификации болезней 10-го пересмотра (МКБ10) М13.9 (другие неуточненные артриты).
Большинство острых артритов заканчиваются полным выздоровлением. Но некоторые виды после окончания острого периода переходят в хроническую форму и продолжают медленно прогрессировать с разрушением хрящевой ткани. Любой нелеченый артрит также может принять хроническое течение с чередованием обострений и ремиссий и постепенной утратой суставной функции.
Причины острого артрита
Причины развития данной патологии могут быть разными:
- Травма. При закрытой травме поврежденные клетки реагируют выделением провоспалительных (поддерживающих воспаление) веществ. Это приводит в развитию асептического (без инфицирования) серозного (негнойного) воспаления сустава. Чаще всего травмируется колено.
- Проникновение в суставную полость инфекционных возбудителей. Инфекция может попадать в сустав при открытых травмах, из расположенных рядом гнойников или из отдаленных очагов инфекции. Все инфекционные возбудители делятся на:
- неспецифические – в основном это представители условно-патогенной микрофлоры, обитающие на соприкасающихся с внешней средой поверхностях тела – коже и слизистых; при определенных условиях они становятся патогенными (золотистый стафилококк, стрептококк, пневмококк и др.); эти возбудители могут вызывать, как серозные, так и гнойные острые артриты;
- специфические – сустав инфицируется при какой-то общей инфекции – бруцеллезе, туберкулезе, гонорее и др.
- Инфекционно-аллергические процессы – с развитием аллергической реакции на инфекцию или на токсические продукты, выделяемые инфекционными возбудителями (реактивный артрит).
- Аутоаллергии. Заболевание начинается после попадания в организм инфекции, развития на нее аллергии, после чего потом происходит сбой в работе иммунной системы и развитие аллергии на собственные суставные ткани (ревматоидный артрит).
- На фоне общего заболевания - острый артрит развивается на фоне псориатического, подагрического.
Предрасполагающие факторы, способствующие развитию заболевания: профессиональная деятельность, связанная с тяжелыми физическими перегрузками или частыми травмами (спортсмены, грузчики), переохлаждения, малоподвижный образ жизни в сочетании с лишней массой тела. Для инфекционно-аллергических и аутоаллергических артритов основным предрасполагающим фактором является отягощенная наследственность (аналогичные заболевания у близких родственников).
Симптомы острого артрита
Острый артрит имеет характерные симптомы, поэтому его трудно с чем-то спутать.
Первые признаки
Начальные симптомы острого артрита: повышение температуры тела, недомогание, слабость, головная боль. При серозном воспалении эти симптомы могут быть выражены незначительно, при гнойном – ярко. Кожа над пораженной областью отекает, краснеет, становится горячей на ощупь. Болевой сидром выражен, особенно, если процесс гнойный. Ограничение подвижности из-за боли. При поражении височно-нижнечелюстного сустава появляются боли в нижней челюсти и нарушение жевания.
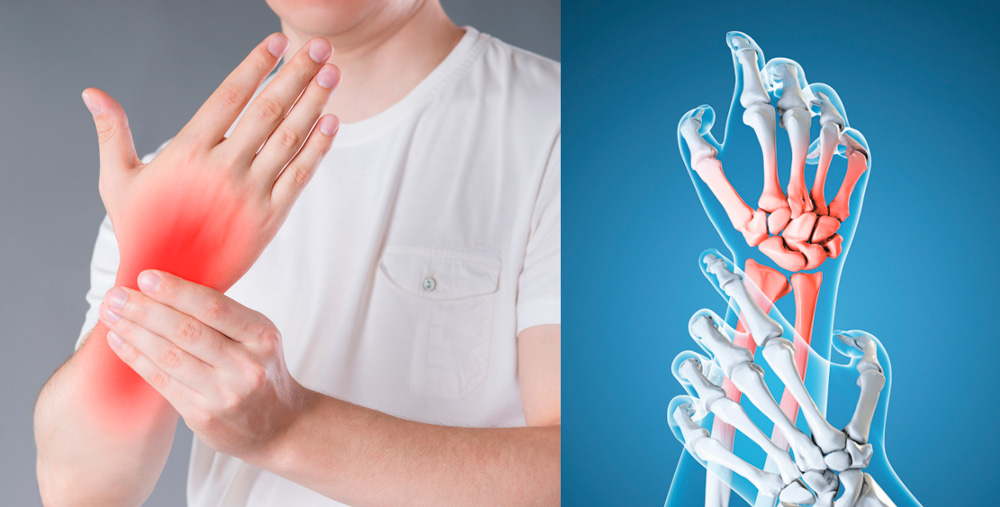
Боли в суставах и покраснения кожного покрова - основные симптомы острого артрита
Явные симптомы
Все симптомы нарастают, больной сустав неподвижен из-за боли. Нарастает отечность и покраснение околосуставных тканей. При скоплении в суставной полости большого объема воспалительной жидкости (экссудата) у проводящего обследование врача появляется ощущение движения жидкости под пальцами (флюктуации). При отсутствии медицинской помощи появляется риск развития серьезных осложнений.
Опасные симптомы
За медицинской помощью следует обращаться, если появились следующие симптомы:
- лихорадка в сочетании с отеком, покраснением и болезненностью сустава;
- боль, припухлость и покраснение в одном или нескольких суставах;
- появление вышеперечисленных симптомов через несколько дней после травмы или резкое внезапное обострение всех симптомов, которые ранее были значительно менее выражены;
- сильная суставная боль в суставе, препятствующая сгибанию и разгибанию конечности;
- боли в нижней челюсти и нарушение процесса жевания.
Чем опасно заболевание
Асептический воспалительный процесс может пройти самостоятельно, но, если присоединится инфекция, возможно тяжелое течение заболевания с многочисленными осложнениями и деформацией сустава.
Стадии острого артрита
Стадии острого серозного неосложненного артрита:
- Начальная – воспаление и отек синовиальной оболочки, скопление в суставной полости серозного содержимого. Кожа над суставом отекает, краснеет, появляется боль (от умеренной до сильной);
- Развернутая – нарастание всех признаков воспаления без значительного разрушения тканей сустава. Но на клеточном уровне разрушения имеются. Боли нарастают, конечность сгибается с трудом;
- Восстановительная - постепенное стихание острого воспаления и риск разрастания внутри сустава соединительной ткани, что приведет к нарушению суставной функции. Поэтому очень важно правильное проведение реабилитации.
Стадии острого гнойного артрита:
- Начальная – в суставной полости появляется гной, пока еще не разрушающий сустав. Симптомы: высокая температура, отечность и болезненность, больно пошевелить конечностью. На рентгенографии выявляется расширение суставной щели из-за нарастающего объема гноя. Прилегающие ткани могут быть не изменены, но иногда вокруг сустава образуются гнойники, при этом состояние больного резко ухудшается.
- Развернутая – разрушаются мягкие ткани внутри сустава: синовиальная оболочка, связки, сухожилия мышц. Конечность неподвижна из-за сильнейших болей. Эта стадия может протекать, как с поражением, так и без поражения околосуставных тканей.
- Деструктивная – разрушается хрящевое покрытие сустава и расположенная под ним кость. На рентгенограмме просматривается очаговое разрушение хряща и кости, сужение суставной щели. Деструкция может протекать без проникновения гноя в окружающие ткани, с образованием абсцессов и флегмон, а также с прорывом гноя на поверхность тела и образованием свищей.
- Конечная – при своевременно начатом лечении можно остановить гнойный воспалительный процесс на любой стадии. В зависимости от того, насколько далеко зашло разрушение сустава, возможно полное выздоровление или частичное нарушение функции сустава.
Функция в значительной степени может быть восстановлена при проведении реабилитационных мероприятий. При отсутствии лечения развивается полная неподвижность сустава (анкилоз).
Возможные осложнения
Любые артриты опасны. А гнойный артрит – это еще и риск для жизни больного. При отсутствии адекватное лечения возможны следующие осложнения:
- развитие стойких нарушений суставной функции с его неподвижностью и инвалидизацией;
- переход острого воспаления в хроническое с обострениями артрита и постепенным разрушением суставных тканей;
- тяжелые гнойные местные (абсцессы, флегмоны) и общие (сепсис) осложнения с угрозой жизни больного.
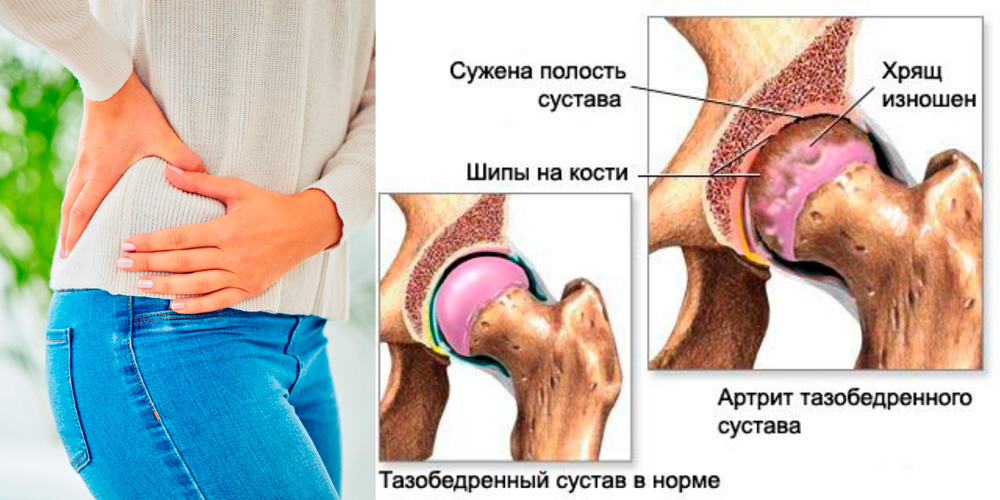
Распространенное осложнение острого артрита - нарушение суставной функции
Первая помощь больному при осложнении
- принять обезболивающее (Анальгин, Пенталгин, Найз – если повышена температура, то эти лекарства подействуют и как жаропонижающее) и успокоительное (настой валерианы или пустырника, Валокордин);
- нанести на больной сустав любую обезболивающую мазь или гель - Диклофенак, Пенталгин и др.
- вызвать врача на дом; если очень высокая температура, то лучше вызвать скорую помощь;
- лечь и принять положение, максимально уменьшающее боль.
При подозрении на гнойный артрит врач направит вас в хирургическое отделение больницы. Не отказывайтесь от госпитализации – на кону может стоять не только ваше здоровье, но и жизнь.
Клинические формы острого артрита
Хондропротекторы что это как выбрать, насколько они эффективны
Боль в суставах в состоянии покоя
Каждый вид артрита имеет как общие с остальными видами клинические симптомы, так и собственные отличительные особенности.
Травматический острый артрит
Даже при небольших травмах и перегрузках нарушается работа клеток синовиальной оболочки сустава, в ответ они вырабатывают активные действующие вещества (простагландины, цитокины), поддерживающие воспаление. Чаще всего при закрытых травмах артрит имеет асептический характер и проявляется в виде небольшой припухлости и болезненности сустава. Но в суставную полость может попасть инфекция. Это происходит при открытых ранах или с током крови из отдаленных очагов инфекции, например, из ЛОР-органов (тонзиллиты, гаймориты), кариозных зубов и др., что становится причиной развития острого неспецифического артрита, в том числе гнойного.
Асептическое воспаление может пройти самостоятельно без последствий, но иногда при этом все же остаются изменения, приводящие к нарушению функции сустава. Поэтому заболевание необходимо лечить под контролем врача с последующим проведением реабилитации.
Острый гнойный артрит (неспецифический)
Присоединение неспецифической (патогенной и условно-патогенной - постоянно обитающей на поверхности тела человека) инфекции к любому виду артрита проявляется ухудшением общего состояния. Артрит может иметь серозный или гнойный характер. При серозном (негнойном) слегка повышается температура тела, усиливается покраснение и отек околосуставных тканей. При назначении антибактериальной терапии заболевание заканчивается полным выздоровлением. Если не лечить, то в результате процесс может переходить в гнойный.
Гнойный артрит – это тяжелое общее заболевание, сопровождающееся высокой лихорадкой, ознобом, головной болью, недомоганием. Одновременно появляется покраснение и отечность тканей над суставом с сильной болью и невозможностью движения в конечности.
Заболевание требует экстренной госпитализации в хирургическое отделение больницы с последующей длительной реабилитацией в амбулаторных условиях.
Острый инфекционный артрит (специфический)
Инфекционные специфические артриты протекают по-разному, в зависимости от вызвавшего его возбудителя. Так, гонорейный артрит протекает остро, с лихорадкой, покраснением и отеком сустава. Остро протекают вирусные артриты (при парвовирусной инфекции, хронических гепатитах, краснухе), но клиническое течение их доброкачественное, заканчивающееся, как правило, благоприятным исходом.
Острый подагрический артрит
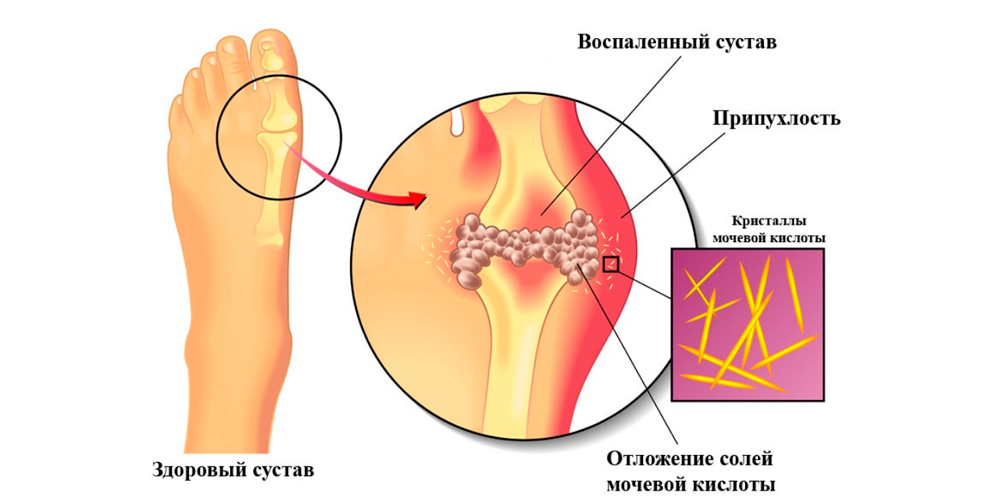
Острый подагрический артрит стопы
Причиной подагры является повышенное содержание солей мочевой кислоты в крови и скопление ее кристаллов в суставных и околосуставных тканях, вызывающее раздражение и воспаление. Приступы подагры всегда протекают остро. Внезапно появляется сильнейшая боль в одном или нескольких суставах. Над пораженным суставом появляются резкий отек и выраженное покраснение тканей. Боли очень сильные, но через некоторое время все проходит без каких-либо последствий. Повторный приступ может появиться через несколько месяцев или даже лет.
После первого же приступа острого подагрического артрита необходимо обратиться к врачу (лучше сразу к ревматологу), провести обследование и придерживаться всех рекомендаций специалиста, иначе со временем нарушаются суставные функции.
Острый реактивный артрит
Этот вид артрита развивается через 1 – 1,5 месяца после перенесенной мочеполовой, кишечной или ЛОР-инфекции. Воспаление имеет серозный (негнойный) характер с асимметричным поражением нескольких суставов, в том числе, коленного и нижней челюсти. Имеется склонность к рецидивированию и появлению хронических болей. Поэтому очень важно вовремя выявить и пролечить инфекцию, а также провести реабилитационные мероприятия.
Острый ревматоидный артрит
Заболевание обычно протекает хронически и начинается постепенно. Но иногда встречаются и острые воспалительные процессы с резким отеком и покраснением пораженных тканей, сильными болями и нарушением движений. И если при медленном незаметном начале чаще поражаются мелкие суставы кисти и стопы, то при остром артрите обычно происходит симметричное поражение одного – двух крупных суставов.
Острый ревматоидный артрит – это негнойный процесс, но боли могут быть очень сильными. В дальнейшем присоединяется поражение мелких суставчиков и процесс протекает с характерными для заболевания проявлениями, может часто обостряться. Чем раньше больной обращается за медицинской помощью, тем больше у него шансов на сохранение функции суставов.
Острый ревматический артрит
Поражение суставов при ревматизме может возникнуть через 1 – 2 недели после перенесенной инфекции (обычно стрептококковой). Клинически ревматический артрит проявляется небольшим повышением температуры, недомоганием, слабостью, покраснением и отечностью в нескольких симметричных суставах. Боли могут иметь летучий характер. Через некоторое время все эти симптомы полностью исчезают, может оставаться лишь незначительная болезненность в суставах. Но это вовсе не значит, что наступило выздоровление: второй этап – поражения сердца, они гораздо более тяжелые.
Ревматический артрит очень опасен именно осложнениями со стороны сердца, поэтому требует немедленной медицинской помощи, длительного лечения и соблюдения рекомендаций врача.
Изучена распространенность и этиологическая структура активной герпесвирусной инфекции у детей с различными формами и вариантами ювенильного артрита, сопоставлены форма и вариант ювенильного артрита у пациентов с активностью герпесвирусной инфекции и без
The article describes the prevalence and etiological structure of the active herpes virus infection in children with different forms and variants of juvenile arthritis, the form and variant peculiarities of juvenile arthritis in patients with active herpes infection, and without it were compared.
В последние десятилетия изучение роли инфекционных (вирусно-бактериальных ассоциаций) и наследственных факторов в развитии хронических воспалительных заболеваний суставов у детей сохраняет свою актуальность. Согласно современным представлениям ювенильный артрит (ЮА) рассматривается как обобщающее понятие, объединяющее гетерогенную группу хронических заболеваний суставов, имеющих различный этиопатогенез и иммуногенетическое происхождение, различную нозологическую принадлежность и неоднозначный прогноз. В группу ЮА можно отнести ювенильный ревматоидный артрит (ювенильный идиопатический артрит (ЮИА)) и ювенильный спондилоартрит (ЮСА), а также ювенильный хронический артрит, который представлен хроническим течением реактивного артрита [1, 2]. Среди ЮА наиболее значимым является ЮИА, приводящий к ранней инвалидизации в детском возрасте [3–5]. ЮИА так же, как ювенильные артриты в целом, представляет гетерогенную группу, в которой выделяют различные формы и варианты течения. Традиционно принято выделение системных и преимущественно суставных форм [3].
ЮА относятся к мультифакториальным заболеваниям, в развитии которых имеют место не только экзогенные (инфекционные и средовые), но и наследственные факторы, в том числе иммуногенетические [3, 5–7]. Развитие и прогрессирование ЮИА определяется сочетанием генетически детерминированных и вторичных дефектов иммунорегуляторных механизмов, приводящих к быстрой трансформации физиологической острой воспалительной реакции в хроническое прогрессирующее воспаление. Однако механизмы становления аутоиммунного патогенеза ЮИА довольно сложны и, несмотря на многочисленные исследования, до конца не раскрыты [6–8]. Влияние вирусной инфекции, в том числе герпесвирусной, в качестве триггерного фактора развития ЮА очевидно, в то время как этиологическая роль только предполагается. Во многом нерешенным остается вопрос об уровне взаимосвязи инфекционных и генетических факторов в развитии и течении ювенильного артрита. По мнению ряда авторов, не исключается возможность инициации инфекционным агентом артрита, особенно у генетически предрасположенного больного [9–11]. В литературе имеются данные о том, что герпесвирусные инфекции у детей с ЮИА не только утяжеляют его течение, но и могут участвовать в реализации патогенетических иммунокомплексных процессов [8, 12].
У детей спектр клинических проявлений герпесвирусной инфекции (ГВИ) весьма разнообразен: он зависит от локализации патологического процесса, его распространенности, состояния иммунной системы больного и антигенного типа вируса [13–15]. По данным литературы у детей с ЮИА выделяется два варианта инфицирования вирусами и бактериями: в начале заболевания и спустя несколько месяцев и лет от его дебюта. Во всех случаях как носительства, так и острой герпесвирусной инфекции ЮИА протекает в виде более тяжелых клинических форм [8, 9], и вирусно-бактериальное инфицирование у детей с ЮИА является прогностически неблагоприятным признаком, указывающим на большую тяжесть болезни с возможностью возникновения необратимых процессов с нарушением функции суставов, развитием висцеритов и васкулитов [3, 8].
Кроме того, использование иммуносупрессивной терапии, а в последние десятилетия генно-инженерных биологических препаратов, мишенью которых являются узловые патогенетические звенья воспалительного процесса (ФНО-α, интерлейкины-1, 6 и т. д.), способствует не только подавлению аутоиммунных реакций, но и создает условия для реактивации латентных вирусных инфекций [16–21].
Поэтому вопрос о роли герпесвирусной инфекции как о причинном агенте, усугубляющем дефект иммунорегуляторных систем и обуславливающем развитие иммунных нарушений, лежащих в основе ЮИА, является актуальным.
Целью настоящего исследования было изучить распространенность активной герпесвирусной инфекции (ГВИ) у больных с различными формами и вариантами ЮА.
Пациенты и методы исследования
В исследование были включены 163 ребенка с воспалительными заболеваниями суставов, наблюдавшиеся в детском ревматологическом отделении на клинической базе (УДКБ № 1) кафедры детских болезней лечебного факультета ФГБОУ ВО Первый МГМУ им. И. М. Сеченова.
При формировании групп больных по нозологическим формам и вариантам течения использовались Берлинские диагностические критерии (Берлин, 1996 г.) реактивного артрита, классификационные критерии ЮСА Гармиш-Партенкирхен (1987 г.) и критерии диагностики ЮИА (1997 г.) Американской коллегии ревматологов (American College of Rheumatology, ACR). Согласно этой классификации и в соответствии с поставленными задачами нами выделялась системная и преимущественно суставная форма ЮИА.
Всем пациентам проводилось комплексное клинико-лабораторное и инструментальное обследование, принятое в детской ревматологии, которое включало оценку жалоб, анамнеза, данных физикального осмотра (выраженность суставного синдрома и внесуставных проявлений), стандартные лабораторные исследования (клинические, биохимические и иммунологические анализы крови, общий анализ мочи), а также инструментальные методы. С целью исключения поражения глаз все больные были осмотрены окулистом, по показаниям — другими специалистами.
У всех обследованных детей методом сплошного скринингового исследования крови осуществлялась идентификация ДНК вирусов герпеса 1-го, 2-го, 3-го, 4-го, 5-го и 6-го типов с помощью качественной ПЦР.
Результаты исследования и их обсуждение
Всего в исследование вошло 163 пациента. С системным ЮИА было 34 ребенка, с суставной формой — 87, с ЮСА — 17, с хроническим реактивным артритом (ХРеА) — 25. Во всех группах, за исключением ЮСА, преобладали девочки — их в 1,4 раза больше мальчиков. Как известно, ЮСА развивается преимущественно у мальчиков подросткового возраста, о чем свидетельствует и средний возраст в этой группе, который составил 14,88 ± 0,6 года в сравнении с другими вариантами ЮА, где средний возраст соответствовал 8–10 годам (табл. 1). Средний возраст дебюта заболевания был наименьшим в группе с суставной формой ЮИА — 3,77 ± 0,3 года, набольшим в группе ЮСА — 9,7 ± 0,59. Средняя продолжительность заболевания в целом по группам составила 5 лет, за исключением ХРеА, где средняя продолжительность заболевания составила 2,98 ± 0,66 года.
В целом ГВИ была выявлена у 81 пациента с ЮА (49,7%). С системным ЮИА — 21 ребенок (62%), что достоверно выше, чем при суставном ЮИА — 39 (45%, р ≤ 0,05).
Частота ГВИ в зависимости от пола и возраста
В группе пациентов с активной ГВИ, как и группе без ГВИ, соотношение девочек и мальчиков было примерно одинаково и составило 1,4:1 (р ≤ 0,005). То есть группы сопоставимы по половому составу.
Анализ распределения по возрасту пациентов с ГВИ и без ГВИ показал, что среди детей с маркерами активной ГВИ достоверно преобладает возрастная группа от 1 года до 6 лет — 65% (р ≤ 0,001), а пациенты без ГВИ в основном 7–11 лет — 67% (р ≤ 0,001). Число пациентов в возрасте 12–17 лет в обеих группах было примерно одинаково — 49% и 51% (р > 0,05) (рис. 1).
Структура герпесвирусной инфекции у пациентов с ЮА
Частота выявления моно- и микст-ГВИ у пациентов с ЮА (n = 81) представлена на рис. 2.
У обследованных детей с различными формами и вариантами ЮА был проведен анализ структуры положительных маркеров активной ГВИ. Моноинфекция (положительный маркер активной ГВИ к одному вирусу герпеса) диагностирована в 47% (53 ребенка), микст-инфекция (положительные маркеры двух и более активных ГВИ) — у 53% (60 детей).
При анализе структуры положительных маркеров ГВИ (табл. 2) достоверно чаще выявлялись положительные маркеры активной инфекции ВПГ 1-го типа — 34 ребенка (30%), по сравнению с положительными маркерами активной ВЗВ-инфекции — 17 детей (15%, р ≤ 0,05). Положительные маркеры активной ВГЧ 6-го типа и ВЭБ-инфекции — у 31 ребенка (27,5%, р > 0,05) соответственно. Положительных маркеров активной ЦМВ-инфекции не было выявлено ни у одного пациента с ЮА, что согласуется с данными зарубежной литературы [19].
У больных с положительными маркерами ГВИ ВЗВ достоверно чаще встречается в виде моноинфекции — 59% (р ≤ 0,05), а ВГЧ 6-го типа достоверно чаще встречался в виде микст-инфекции — 65% (р ≤ 0,001). Положительные маркеры ВПГ 1-го типа и ВЭБ были выявлены примерно в одинаковом проценте случаев — как в виде моноинфекции, так и в составе микст-инфекции (рис. 3).
Анализ положительных маркеров активной ГВИ при различных формах и вариантах ЮА показал (табл. 3), что при суставной форме ЮИА достоверно чаще выявляются положительные маркеры ВПГ 1-го типа и ВГЧ 6-го типа — 33%, по сравнению с ВЗВ — 10% (р ≤ 0,001). У пациентов с ХРеА достоверно чаще выявляются положительные маркеры ВЭБ и ВГЧ 6-го типа — 35%, по сравнению с ВПГ 1-го типа и ВЗВ — 12% (р ≤ 0,001) и 18% (р ≤ 0,005) соответственно. При системной форме ЮИА и ЮСА достоверных различий по частоте встречаемости положительных маркеров ГВИ не получено: ВПГ 1-го типа, ВЭБ, ВГЧ 6-го типа, ВЗВ определяются примерно с одинаковой частотой (рис. 4). Это, вероятно, связано с более высокой вирусной и антигенной нагрузкой: пациенты с системной формой ЮИА получают агрессивную иммуносупрессивную терапию, что увеличивает риск активации латентных и коморбидных инфекций, в том числе ГВИ. Обращает внимание, что при ЮСА положительных маркеров ВГЧ 6-го типа не обнаружено ни у одного пациента. Больные с ЮСА — преимущественно в возрасте 14–15 лет, а инфекция ВГЧ 6-го типа характерна для детей раннего возраста — к пяти годам жизни различными видами герпеса инфицируются до 90% детей [14].
При анализе моно-ГВИ у пациентов с различными формами и вариантами ЮА (табл. 4) выявлено, что при ЮИА (как при суставной, так и при системной форме особенно) преобладает моноинфекция ВЭБ — 27% и 38%. При системной форме ЮИА достоверно реже выявляется моноинфекция ВГЧ 6-го типа — 8% (р ≤ 0,001). У пациентов с суставной формой ЮИА, помимо моноинфекции ВЭБ, преобладает моноинфекция ВПГ 1-го типа и ВГЧ 6-го типа — 35% и 30% соответственно по сравнению с ВЗВ — 8% (р ≤ 0,001). При ЮСА преобладает моноинфекция ВПГ 1-го типа — 58% по сравнению с ВЭБ — 13% (р ≤ 0,001) и ВЗВ — 29% (р ≤ 0,005). Как было показано ранее, маркеры ВГЧ 6-го типа у больных с ЮСА не выявлялись ни у одного ребенка. У больных с ХРеА, напротив, с одинаковой частотой определялись ВПГ 1-го типа, ВЗВ, ВГЧ 6-го типа — 29% по сравнению с ВЭБ — 13% (р ≤ 0,05) (рис. 5).
В общей структуре микст-инфекции у пациентов с ЮА преобладают сочетания ВГЧ 6-го типа + ВЭБ и ВГЧ 6-го типа + ВПГ 1-го типа — в 32% и 25% соответственно, реже встречаются сочетания ВПГ 1-го типа + ВЭБ и ВПГ-1-го типа + ВЗВ — 11% (рис. 6).
Анализ микст-ГВИ у пациентов с различными формами и вариантами ЮА выявил, что микст-инфекция у больных с системным ЮИА составляла 24%, при этом преобладала микст-инфекция ВПГ 1-го типа + ВГЧ 6-го типа, при суставной форме микст-инфекция выявлялась в 15% случаев и была представлена преимущественно сочетаниями: ВПГ 1-го типа + ВГЧ 6-го типа и ВЭБ + ВГЧ 6-го типа. При ЮСА микст-инфекция встречалась реже, чем при других вариантах ЮА, и составляла 12% — в виде сочетания ВЭБ + ВЗВ. При ХРеА микст-инфекция выявлялась в 20%, преобладало сочетание ВЭБ + ВЧГ 6-го типа (рис. 7). Это в целом отражает тенденцию, выявленную при анализе общей структуры положительных маркеров ГВИ: при суставной форме ЮИА достоверно чаще выявляются положительные маркеры ВПГ 1-го типа, при ХРеА — ВГЧ 6-го типа.
Обнаруженные в настоящем исследовании различия в частоте и структуре ГВИ при разных формах и вариантах ЮА требуют дальнейшего анализа с целью оценки влияния ГВИ на клиническое течение ЮА и обсуждением возможной этиопатогенетической роли ГВИ в развитии ЮА.
Выводы
- У больных с различными формами и вариантами ЮА активная ГВИ выявлялась в 49,7%. Среди положительных маркеров ГВИ у детей с ЮА наиболее часто встречаются ВПГ 1-го типа, а реже других — ВЗВ. Активная ЦМВ-инфекция не была диагностирована ни у одного пациента с ЮА.
- При системном варианте ЮИА ГВИ выявляются чаще, чем при других вариантах и формах ЮА, и составляют 62%. Преобладает активная инфекция ВПГ 1-го типа и ВЭБ, чаще встречается микст-герпесвирусная инфекция.
- При суставной форме ИЮА ГВИ выявляется несколько реже, чем при других формах ЮА, — 45% и представлена ВПГ 1-го типа, ВГЧ 6-го типа и ВЭБ (выявляются с одинаковой частотой), в то время как ВЗВ встречается достоверно реже.
- ЮСА характеризуется высокой частотой выявления ГВИ — 53%. Преимущественно за счет ВПГ 1-го типа и ВЗВ. Особенностью ЮСА является отсутствие маркеров ВГЧ 6-го типа.
- При ХРеА частота выявления ГВИ составляет 48%. В структуре ГВИ преобладает ВЭБ и ВГЧ 6-го типа — как в виде моно-, так и в форме микст-инфекции.
Литература
- Cassidy J. T., Petty R. E., Laxer R. M., Lindsley C. B. Textbook of pediatric rheumatology. 6 th ed. Philadelphia: Saunders Elsevier, 2010. 794 р.
- Cellucci T., Guzman J., Petty R. E., Batthish M., Benseler S. M., Ellsworth J. E., Houghton K. M., LeBLANC C. M., Huber A. M., Luca N., Schmeling H., Shiff N. J., Soon G. S., Tse S. M. Management of Juvenile Idiopathic Arthritis 2015: A Position Statement from the Pediatric Committee of the Canadian Rheumatology Association // J Rheumatol. 2016; 43 (10): 1773–1776.
- Жолобова Е. С., Шахбазян И. Е., Улыбина О. В. Афонина Е. Ю. Ювенильный ревматоидный (идиопатический) артрит. В кн.: Геппе Н. А., Подчерняева Н. С., Лыскина Г. А. (ред.). Ювенильный ревматоидный артрит. Рук-во по детской ревматологии. М.: ГЭОТАР-Медиа, 2011. С. 162–245.
- Баранов А. А., Алексеева Е. И., Бзарова Т. М. Протокол ведения пациентов с ювенильным артритом // Вопросы современной педиатрии. 2013; 12 (1): 37–56.
- Ravelli A. Handbook of Juvenile Idiopathic Arthritis. Switzerland, Adis (Springer International Publishing). 2016; 115–124.
- Donn R., De Leonibus., Meyer S., Stevens A. Network analysis and juvenile idiopathic arthritis (JIA): a new horizon for understanding of disease pathogenesis and therapeutic target identification // Pediatr Rheumatol Online J. 2016; 14 (1): 40. DOI: 10.1186/s12969–016–0078–4.
- Кравченко Н. П., Олейник Е. К. Механизмы нарушения иммунологической толерантности // Труды карельского научного центра РАН, 2015; (12): 3–22. DOI: 10. 17076/eb230.
- Соболева Н. Г. Ювенильный ревматоидный артрит у детей Краснодарского края (особенности этиопатогенеза, оптимизация лечебной тактики). Автореф. дис. … д.м.н. Краснодар, 2009.
- Ball R. J., Avenell A., Aucott L., Hanlon P., Vickers M. A. Systematic review and meta-analysis of the sero-epidemiological association between Epstein-Barr virus and rheumatoid arthritis // Arthritis Research & Therapy. 2015; 17: 274. DOI: 10.1186/s13075–015–0755–6.
- Halenius A., Hengel H. Human cytomegalovirus and autoimmune disease // Biomed Res Int. 2014; 2014: 472978. DOI: 10.1155/2014/472978. Epub 2014 Apr 29.
- Draborg A. H., Duus K., Houen G. Epstein-Barr virus in systemic autoimmune diseases // Clin Dev Immunol. 2013; 2013: 535738. DOI: 10.1155/2013/535738. Epub 2013 Aug 24.
- Бочанцев С. В., Потрохова Е. А., Соботюк Н. В., Устян Л. А., Пертельс Т. Г. Диагностика вирусной инфекции Эпштейна–Барр при системной красной волчанке и ревматоидном артрите // Российский педиатрический журнал. 2014; 17 (5): 42–48.
- Исаков В. А., Архипова В. И., Исаков Д. В. Герпесвирусные инфекции человека. СПб: СпецЛит, 2013. С. 51–198.
- Боковой А. Г. Герпесвирусные инфекции у детей: диагностика, клиника и лечение. Роль в формировании контингента часто болеющих детей. Учебное пособие. М.: МАКС Пресс, 2008. 144 с.
- James S. H., Kimberlin D. W. Neonatal Herpes Simplex Virus Infection // Infect Dis Clin North Am. 2015; 29 (3): 391–400. DOI: 10.1016/j.idc.2015.05.001. Epub 2015 Jul 4.
- Davies H. D., Byington C. L., Maldonado Y. A., Barnett E. D., Edwards K. M., Lynfield R., Munoz-Rivas F. M., Nolt D. L., Nyquist A. C., Rathore M. H., Sawyer M. H., Steinbach W. J., Tan T. Q., Zaoutis T. E. Infectious Complications With the Use of Biologic Response Modifiers in Infants and Children // Pediatrics. 2016; 138 (2): e20161209. DOI: 10.1542/peds.2016–1209. Epub 2016 Jul 18.
- Nicolai R., Cortis E., Ravà L., Bracaglia C., Pardeo M., Insalaco A., Buonuomo P. S., Tozzi A. E., De Benedetti F. Herpes Virus Infections During Treatment With Etanercept in Juvenile Idiopathic Arthritis // J Pediatric Infect Dis Soc. 2016; 5 (1): 76–79. DOI: 10.1093/jpids/piu078. Epub 2014 Jul 31.
- Comar M., Delbue S., Lepore L., Martelossi S., Radillo O., Ronfani L., D’Agaro P., Ferrante P. Latent viral infections in young patients with inflammatory diseases treated with biological agents: prevalence of JC virus genotype 2 // J Med Virol. 2013; 85 (4): 716–722. DOI: 10.1002/jmv.23525. Epub 2013 Jan 30.
- Kawada J., Iwata N., Kitagawa Y., Kimura H., Ito Y. Prospective monitoring of Epstein-Barr virus and other herpesviruses in patients with juvenile idiopathic arthritis treated with methotrexate and tocilizumab // Mod Rheumatol. 2012; 22 (4): 565–70. DOI: 10.1007/s10165–011–0552–2. Epub 2011 Nov 5.
- Zhang N., Wilkinson S., Riaz M., Ostor A. J., Nisar M. K. Does methotrexate increase the risk of varicella or herpes zoster infection in patients patients with juvenile rheumatoid arthritis? A systematic literature review // Clin Exp Rheumatol. 2012; 30 (6): 962–71. Epub 2012 Dec 17.
- Che H., Lukas C., Combe B. Risk of herpes/herpes zoster during antitumor necrosis factor therapy in patients with rheumatoid arthritis. Systematic rewiew and meta-analysis // Joint Bone Spine. 2014; 81 (3): 215–221. DOI: 10.1016/j.jbspin.2013.07.009. Epub 2013 Aug 7.
Е. Ю. Солдатова* , 1
Е. С. Жолобова**, доктор медицинских наук, профессор
Е. В. Мелёхина*, кандидат медицинских наук
А. В. Горелов**, доктор медицинских наук, профессор, член-корреспондент РАН
* ФГУН ЦНИИЭ Роспотребнадзора, Москва
** ФГБОУ ВО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Читайте также:

