Можно ли делать прививку ребенку если у него глисты
Обновлено: 19.04.2024
В чем заключаются трудности диагностики гельминтозов? Какова терапия гельминтозов? На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов
В чем заключаются трудности диагностики гельминтозов?
Какова терапия гельминтозов?
На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов (болезни адаптации), постоянного стресса, повышения уровня образованности и культуры населения многие давно известные заболевания человека изменили свою клиническую картину. Некоторые симптомы практически перестали встречаться, другие, наоборот, стали выходить на первый план. Это относится и к заболеваниям, вызываемым гельминтами, в частности, круглыми паразитическими червями (нематодами). В умеренном поясе наиболее широко распространенные нематоды — аскарида и острицы.
Гельминты могут вызывать нарушения функции желудочно-кишечного тракта (ЖКТ), быть причиной аллергических (или псевдоаллергических) реакций или усугублять их, вызывать интоксикацию, а также быть фактором, ослабляющим иммунитет [2]. В настоящее время редко встречаются случаи массивной инвазии, когда диагностика не вызывает затруднений, а клубки гельминтов вызывают обтурации кишечника, — значительно чаще гельминты стали являться причиной развития аллергических проблем. При этом гельминтозы относятся к тем заболеваниям, которые трудно диагностировать в связи с объективными и субъективными трудностями (длительные периоды отсутствия яйцекладки, возможность отсутствия среди паразитирующих особей самок, вероятность технических ошибок). Поэтому важно знать клиническую картину данных заболеваний, чтобы иметь возможность назначать углубленное обследование или эффективную терапию по совокупности косвенных признаков, даже не имея прямых доказательств наличия гельминтоза.
С целью оценить клиническую картину при нематодозах проанализированы жалобы, анамнез и результаты осмотра 150 детей, у которых были обнаружены аскариды (116 детей), острицы (27 детей), аскариды и острицы (7 детей). Гельминты выявлены стандартными методами: обнаружение яиц аскарид в фекалиях методом мазка или яиц остриц в соскобе на энтеробиоз, а также визуальное обнаружение аскарид или остриц в фекалиях, рвотных массах или при оперативном или эндоскопическом вмешательстве в брюшной полости или в области прямой кишки [3].
Среди детей было 67 мальчиков, 83 девочки. Распределение по возрасту представлено в табл. 1. Преобладали дети младшего дошкольного возраста (от одного до трех лет), их количество составило 63%. Именно в этом возрасте — наибольшие эпидемиологические предпосылки появления нематодозов.
У 150 детей с доказанными инвазиями аскаридами и/или острицами отмечались следующие клинические проявления.
У 107 детей (71,3%) были аллергические проблемы: кожные высыпания, диатез, атопический дерматит, нейродермит — у 99 (66%), из них у 18 эти проблемы носили периодический характер, у двух детей, кроме кожных высыпаний, отмечались конъюнктивиты; у десяти (6,7%) отмечалась доказанная пищевая аллергия на какие-то продукты с высоким уровнем специфических IgE в сыворотке крови; у шести детей (4%) отмечался астматический компонент или был установлен диагноз бронхиальная астма.
Бруксизм (скрежетание зубами) — симптом, который часто связывается с глистными инвазиями, но фактически является неспецифическим признаком интоксикации центральной нервной системы и может сопровождать любые хронические интоксикации — отмечался у 25 детей (16,7%).
Нарушения ночного сна отмечались у 81 ребенка (54%): беспокойство к вечеру, затруднения засыпания — у 15 детей (10%); беспокойный ночной сон (вскрикивания, постанывания, метания во сне, пробуждения, плач, бессонница, кошмарные сновидения) — у 76 (50,7%). Некоторые родители старших детей затруднялись охарактеризовать ночной сон ребенка, т. к. ребенок спит в другой комнате. Проблемы с засыпанием и ночным сном — важный симптом глистных инвазий, т. к. известно, что кишечные нематоды (в том числе аскариды и острицы) часто активизируются именно ночью.
У 54 детей (36%) отмечались зуд и/или покраснения в области заднего прохода (анальная эскориация) — у 43 детей (28,7%); зуд — у 38 (25,3%); оба симптома — у 27 (18%). Анальная эскориация и зуд считаются симптомами энтеробиоза (острицы), но при этом из 54 детей, у которых отмечались данные симптомы, энтеробиоз был доказан у 17 детей (31,5% от числа детей с этими симптомами). У других 37 детей (68,5% от числа детей с данными симптомами) было доказано наличие аскаридоза, но ни визуально, ни в анализах не были обнаружены острицы. Это может свидетельствовать либо о том, что в данных случаях присутствовали острицы, которые не были диагностированы, т. е. гельминтоз был смешанным, либо о том, что анальная эскориация и зуд — симптомы, характерные не только для энтеробиоза, но и аскаридоза.
У 29 детей (19,3%) отмечались признаки общего ослабления иммунитета: часто или длительно болеющие дети (по общепринятой классификации Monto J. et al., 87) — 18 детей (12%); рецидивирующие стоматиты, гингивиты отмечались у 13 детей (8,7%); кариес зубов — у шести (4%); рецидивирующие гнойные заболевания кожи или слизистых — у трех (2%).
У 15 детей (10%) имелись результаты исследования иммунного статуса по крови: у 13 детей было снижено количество Т-клеток; у всех 15 детей было снижено количество Т-хелперов, причем у шести из них — существенно; у 12 детей было снижено хелперно-супрессорное соотношение; у семи детей отмечалось снижение уровня IgA (секреторный иммуноглобулин), в том числе у трех — существенное, у остальных же восьми детей уровень IgA в сыворотке крови был либо нормальным, либо повышенным; у шести детей отмечалось снижение количества лимфоцитов, в том числе у одного ребенка была выраженная лимфо- и нейтропения. Эти результаты подтверждают известные данные о том, что аскариды и острицы угнетающе влияют на функции иммунитета, а также что у людей с ослабленным иммунитетом большая вероятность появления гельминтоза [1].
У большинства детей отмечалось более одного симптома. Обобщенные данные по клинической картине представлены в табл. 2.
Терапия во всех случаях состояла из двух этапов: сначала — антигельминтная терапия, причем назначались два разных препарата (декарис и вермокс) с интервалом три — пять дней между ними, чтобы максимально охватить различные стадии жизни гельминтов; через некоторое время после антигельминтной терапии — препараты для микробиологической и функциональной коррекции. Соответственно оценивались результаты противоглистной терапии, результаты всего лечения, а также катамнез в течение шести месяцев после терапии. В большинстве случаев улучшение наступало быстро в процессе лечения. У 36 детей только после антигельминтной терапии существенно уменьшились или полностью исчезли аллергические проявления, у 39 детей после первого этапа терапии нормализовалась работа ЖКТ, у 41 ребенка сразу прекратились боли в животе, по остальным симптомам также наступало улучшение после противоглистных препаратов. Это подтверждает то, что симптомы были вызваны наличием гельминтов.
У 92 детей после всего лечения не было никаких жалоб; о 37 нет данных об изменениях состояния в процессе и после лечения; у 16 детей эффект был неполным, т. е. какие-то симптомы сохранялись и после окончания лечения; у четырех детей эффект от терапии оказался нестойким, поскольку возникли рецидивы после окончания лечения; у трех детей эффекта от терапии не было.
Рассмотрены факторы риска паразитозов у детей, действие паразитов на организм ребенка, подходы к диагностике паразитарной инвазии и принципы комплексного лечения паразитозов с тем чтобы предотвратить дальнейшее развитие функциональных нарушений с формиров
Risk factors of parasitosis in children was considered, as well as the influence of parasites on a child's body, approaches to the diagnostics of parasitic invasions and principles of integrated treatment of parasitic diseases in order to prevent the further development of functional disorders of the formation of organic pathology.
.jpg)
Паразитарное заболевание — развитие болезненных симптомов в результате жизнедеятельности гельминта или простейших в организме человека [1]. Основной фактор выживания и распространения паразитов — их необычайно высокая репродуктивная способность, а также постоянно совершенствующиеся механизмы приспособления к обитанию в теле человека. К сожалению, настороженность медицинских работников в отношении паразитарных заболеваний у населения в настоящее время чрезвычайно низка, а профилактика гельминтозов сведена к лечению выявленных инвазированных пациентов [12, 13]. Вместе с тем многие исследователи отмечают связь широкой распространенности паразитозов у детского населения с развитием функциональной патологии органов пищеварения на фоне нарушений регуляции и высокий риск формирования хронических заболеваний даже при условии естественной санации ребенка с течением времени.
Самые распространенные и изученные заболевания — аскаридоз, энтеробиоз (рис. 1) и лямблиоз — регистрируются повсеместно. В России ежегодно выявляется более 2 млн больных нематодозами. При оценке территориального распределения лямблиоза по России установлено, что самый высокий средний уровень показателей заболеваемости в течение многих лет отмечен в Санкт-Петербурге, причем пораженность детей, посещающих детские учреждения, составляет 35% [2].
Каждый человек в течение жизни неоднократно переносит различные паразитарные заболевания [9]. В детском возрасте паразитозы встречаются чаще. У детей раннего возраста (до 5 лет) этому способствует широкая распространенность репродуктивного материала паразитов (цисты, яйца, личинки (рис. 2)) в окружающей среде и недостаточное развитие гигиенических навыков.
.jpg)
Значимость определенных факторов риска меняется в соответствии с возрастом ребенка. Доказано, что для детей младшего возраста более значимы санитарно-гигиенические условия проживания, а для подростков при сборе анамнеза необходимо уделить внимание социально-экономическим и географическим факторам (пребывание в лагере, туристическая поездка, наличие младшего брата или сестры) (рис. 3).
.jpg)
Транзиторное снижение противоинфекционного иммунитета как фактор риска возникновения паразитоза у детей регистрируется также в период реконвалесценции после вирусных заболеваний, вызываемых вирусами герпетической группы (цитомегаловирус, вирус простого герпеса I и II, вирус Эпштейна–Барр), может возникать в результате ятрогении (применение иммуносупрессивной терапии при аллергических и аутоиммунных заболеваниях). В настоящее время значимая доля детей находится в состоянии дезадаптации, которое также сопровождается снижением иммунной защиты.
Иммунную защиту желудочно-кишечного тракта (ЖКТ) ребенка можно условно разделить на специфическую и неспецифическую. К неспецифической защите относят комплекс условий нормального пищеварения: зрелость ферментативных систем, обеспечение кислотно-щелочного градиента в различных отделах ЖКТ, деятельность нормальной микрофлоры, адекватную моторику.
Отдельно необходимо отметить, что для такого заболевания, как лямблиоз, предрасполагающим фактором инвазии является нерегулярное и недостаточное отделение желчи в кишечник при аномалиях развития желчного пузыря (перетяжки, перегибы). Лямблиоз, выявленный у пациентов педиатрического отделения МОНИКИ, в 100% случаев сопровождался дисфункцией билиарного тракта.
.jpg)
У детей в восстановительном периоде после острых кишечных инфекций, после массивной антибиотикотерапии, а также у пациентов с хронической патологией органов пищеварения сопутствующие нарушения ферментного обеспечения, нормофлоры и моторики кишечника также делают ЖКТ более уязвимым для паразитов (рис. 4).
Специфическая защита слизистой оболочки органов пищеварения зависит от возраста ребенка и его зрелости. Механизм специфической иммунной защиты является одной из наиболее древних систем организма, так как гельминтозы сопровождают человечество в течение многих тысячелетий. Этот механизм представлен прежде всего эозинофилами крови и иммуноглобулином Е.
Классический развернутый антипаразитарный ответ может быть сформирован у ребенка не ранее достижения им 4 лет и тесно связан с качеством и количеством IgE, созревающего к этому возрасту. При контакте организма с паразитом в первую очередь выделяются медиаторы воспаления: интерлейкин, лейкотриен С4, D4, простагландины, тромбоксаны. Увеличивается количество лимфоцитов, продуцирующих IgM и IgG. В клиническом анализе крови отмечается рост уровня эозинофилов и базофилов, связанный с увеличением содержания этих клеток в тканях инвазированного органа. Встречаясь с личинками паразита, тканевые базофилы выделяют гепарин и гистамин, которые в сочетании с лейкотриенами и другими медиаторами воспаления вызывают общие проявления: зуд, реактивный отек, гиперемию, а также могут спровоцировать общие проявления: бронхоспазм, проявления крапивницы или диарею. Аллергическое воспаление при паразитозах развивается по классическому пути и призвано создать условия, приводящие к гибели и/или элиминации паразита [5].
Вместе с тем эозинофилы обладают выраженным цитотоксическим потенциалом, превышающим возможности других клеток крови, что объясняет первостепенное значение эозинофилов в антипаразитарных реакциях и их повреждающую роль при аллергии. Основное действие эозинофилы оказывают в барьерных тканях. В очаге инвазии они дегранулируют, оказывая гельминтотоксическое и цитотоксическое действие. Белки эозинофильных гранул (большой основной протеин, эозинофильная пероксидаза, эозинофильный катионный протеин, эозинофил-производный нейротоксин) токсичны не только для паразита, но и для клеток организма ребенка. Еще одной из важных причин системных и органных поражений, сопутствующих паразитозам, является образование иммунных комплексов [9, 10].
Действие паразитов на организм ребенка осуществляется с вовлечением многих систем. Практически все их виды могут вызывать сдвиг соотношения Th1/Th2 клеток в направлении, благоприятном для их выживания. Описаны случаи, когда продукты выделения паразита оказывали гормоноподобное действие на организм хозяина [5].
Местное влияние паразиты осуществляют, вызывая контактное воспаление слизистой оболочки и стимулируя вегетативные реакции. При этом нарушаются процессы кишечного всасывания, адекватная моторика ЖКТ и его микробиоценоз.
Системное влияние оказывается за счет использования паразитом энергетического и пластического потенциала пищи в ущерб организму ребенка, индукции аллергии и аутоиммунных процессов, целенаправленной иммуносупрессии и эндогенной интоксикации. Проведенными исследованиями показано, что аллергический синдром сопутствует аскаридозу и энтеробиозу в 71,3% случаев. Среди детей с атопическим дерматитом паразитозы выявляются у 69,1%, при этом лямблиоз из числа всех инвазий составляет 78,5% [4].
Особенно узнаваемую клиническую картину формирует токсокароз (рис. 5). Клиническими маркерами этой инвазии являются лейкемоидная реакция эозинофилов (от 20% и выше эозинофилов в формуле крови), сопровождающая ярко и упорно протекающий аллергический синдром в виде атопического дерматита с выраженным зудом и резистентностью к традиционной терапии или тяжелую бронхиальную астму с частыми приступами.
В 75,3% случаев паразитозы сопровождаются разнообразными функциональными нарушениями со стороны ЖКТ. Рядом работ доказано, что паразитарная инвазия способна вызывать нарушения углеводного обмена, а также дисахаридазную недостаточность за счет снижения уровня лактазы [7, 9].
У большинства детей нарушения адаптации являются одним из важных звеньев патогенетического процесса при паразитозе. Следует отметить, что состояние дезадаптации затрагивает в первую очередь лимфоцитарное звено иммуногенеза, что не может не сказываться на созревании и дифференцировке специфического иммунитета.
Диагностика паразитозов
До настоящего времени ведется поиск простого, доступного и надежного метода диагностики паразитозов. Разработанные методики прямого визуального обнаружения требуют минимальной экспозиции диагностического материала, многократных повторных исследований. Известные способы диагностики глистных инвазий и протозоозов, такие как метод толстого мазка фекалий по Като, метод формалин-эфирного осаждения, перианальный соскоб, микроскопия пузырной и печеночной желчи, имеют ряд недостатков, связанных как с особенностями развития паразита, так и с состоянием макроорганизма и его реактивностью.
Непрямые методы исследования (определение специфических антител) обладают недостаточной специфичностью и достоверностью. Известно, например, что, проходя сложный цикл развития от яйца до взрослого состояния, гельминты меняют свой антигенный состав. Антитела в организме хозяина вырабатываются в основном в ответ на поступление экскретов и секретов гельминта, тогда как в иммунодиагностических реакциях используются соматические антитела. Возникающая неспецифическая сенсибилизация организма, общность некоторых антигенов трематод, простейших и человека создают высокий удельный вес ложноположительных серологических реакций в титрах ниже достоверно диагностических. Таким образом, исследование методом иммуноферментного анализа (ИФА) на гельминты является высокочувствительным, но низкоспецифичным методом. Определение паразитов методом полимеразной цепной реакции (ПЦР) является высокоспецифичным и высокочувствительным методом, но из-за дороговизны и сложности не может быть скрининговым, когда, например, нужно обследовать группу детей из детского учреждения.
Не теряет своей актуальности клинический осмотр ребенка и внимательный учет косвенных признаков паразитоза. Важно отметить возможность течения паразитоза при аллергическом и астеническом синдроме, полилимфаденопатии неясного генеза, при нарушениях кишечного всасывания, углеводного обмена, при затяжном и хроническом течении болезней пищеварительного тракта, гепатоспленомегалии неясного генеза. Течение паразитарной инвазии имеет клинические особенности: обычно признаки поражения минимизированы, заболевание носит стертый характер, обострения полиморфны и неярки. Особенностью обострений заболеваний данной группы является их цикличность с периодом в 11–15 дней.
Косвенными лабораторными признаками паразитоза могут быть анемия, базофилия, эозинофилия, увеличение уровня аспартатаминотранферазы (АСТ).
Кроме того, признаки возможной паразитарной инвазии следует учитывать при оценке результатов инструментального исследования. При ультразвуковом исследовании органов брюшной полости у ребенка старше 3 лет косвенными признаками паразитоза являются гепатоспленомегалия, неравномерность паренхимы печени и селезенки за счет мелких гиперэхогенных сигналов, увеличенные лимфатические узлы в воротах селезенки.
Лечение гельминтозов
Лечение гельминтозов должно начинаться с применения специфических антигельминтных препаратов. Современный арсенал лекарственных средств, используемых для лечения кишечных паразитозов, включает значительное количество препаратов различных химических классов [11]. Они применяются как в клинической практике для лечения выявленных больных, так и с целью массовой профилактики.
Определяя препарат для специфической противопаразитарной терапии, следует понимать, что спектр действия этих препаратов не особенно широк. Практически все препараты этой группы применяются многие десятки лет и целесообразно предположить, что паразиты выработали системы приспособления и заболевание может быть резистентным к проводимой терапии. По данным Г. В. Кадочниковой (2004), эффективность такого традиционного препарата, как Декарис, в современных условиях не достигает 57%. Кроме того, эта группа противопаразитарных средств, к сожалению, имеет ряд побочных эффектов: тошноту, рвоту, абдоминальный синдром.
Таким образом, в современных условиях следует отдавать предпочтение более современным препаратам, которые, во-первых, являются универсальными для лечения как нематодозов, так и смешанных глистных инвазий и активны в отношении такого распространенного паразита, как лямблия. Во-вторых, использование одного противопаразитарного препарата, а не их комбинации, ощутимо снижает риск неприятных побочных эффектов. На сегодняшний день единственный представитель этой группы в нашей стране — альбендазол (Немозол).
Для лечения аскаридоза у детей старшего возраста или при рецидивировании заболевания в настоящее время под наблюдением врача может быть применен комбинированный прием антигельминтных средств (например, альбендазол в течение трех дней, затем — Вермокс в течение трех дней). Непременным условием успешной дегельминтизации больных энтеробиозом являются одновременное лечение всех членов семьи (коллектива) и строгое соблюдение гигиенического режима для исключения реинвазии. Следует отметить, что важное значение имеет ежедневная влажная уборка, так как были описаны казуистические случаи распространения репродуктивного материала остриц на частичках пыли на высоту до 1,5 метра.
В педиатрической клинике МОНИКИ разработаны принципы терапии паразитозов, учитывающие особенности патогенеза инвазии и позволяющие качественно и надежно вылечить данную группу заболеваний. Благодаря применению разработанной схемы терапии удается эффективно предотвратить реинвазию и развитие функциональных нарушений органов пищеварения у детей.
Принципы терапии больных паразитозами
1. Прием антипаразитарных препаратов проводится с учетом вида возбудителя инвазии.
Препараты, применяемые в лечениии аскаридоза:
- Вермокс (мебендазол) (для детей с 2 лет) — по 100 мг 2 раза в сутки в течение 3 дней;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении энтеробиоза:
- Вермокс (мебендазол) (для детей с 2 лет) — 100 мг однократно;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении лямблиоза:
- орнидазол 25–30 мг/кг (если масса тела больше 35 кг — 1000 мг) в два приема в течение 5 дней, 1 день — 1/2 дозы, повторный курс через 7 дней;
- Макмирор (нифурател) — по 15 мг/кг 2 раза в сутки в течение 7 дней;
- Немозол (альбендазол) — по 15 мг/кг однократно в течение 5–7 дней.
2. Лечение паразитоза предусматривает измененные в результате жизнедеятельности паразитов свойства пищеварительного тракта ребенка (функциональные нарушения органов пищеварения, ферментопатия, изменение микробиоценоза) и их коррекцию курсами ферментных препаратов и синбиотиков (табл. 1).
3. Обязательное применение энтеросорбентов и комплекса поливитаминов с микроэлементами (табл. 2 и 3).
Таким образом, разработанные в клинике педиатрии МОНИКИ принципы комплексной терапии паразитозов у детей предусматривают поэтапное восстановление функционального состояния ЖКТ, нарушенного в результате местного и системного влияния паразитов. Применение комплексной терапии позволяет предотвратить дальнейшее развитие функциональных нарушений с формированием органической патологии, а также избежать реинвазии.
Литература
Л. И. Васечкина 1 , кандидат медицинских наук
Т. К. Тюрина, кандидат медицинских наук
Л. П. Пелепец, кандидат биологических наук
А. В. Акинфиев, кандидат медицинских наук
Вакцинация – это введение специальных препаратов, благодаря которым организм начинает вырабатывать антитела, с помощью которых он борется с инфекциями. Большинство прививок человек получает в детстве, но некоторые из них нужно делать повторно во взрослом возрасте, так как со временем они утрачивают свою эффективность. Также сегодня появилась возможность защитить организм от инфекций перед поездкой в экзотические страны или при планировании беременности. И, конечно же, одна из актуальных и злободневных тем сегодня – вакцинация против коронавируса COVID-19.
Многие взрослые негативно относятся к вакцинации и без всяких оснований отказываются от прививок. Но при некоторых патологиях они действительно могут нанести организму существенный вред. Попробуем разобраться, когда прививаться все же необходимо. А при каких заболеваниях делать прививки взрослым нельзя.
Прививки взрослым – какие нужны
Никто не может заставить человека вакцинироваться без его добровольного согласия. Но учитывая важность прививок для общества в целом, проявить сознательность, наверное, все же стоит. Тем более, что особых причин для беспокойства нет: современные вакцины от хорошо изученных инфекций крайне редко вызывают тяжелые осложнения.
- столбняка и дифтерии – от этих заболеваний прививают в детстве, но в 26 лет нужно получить повторную прививку, которую затем необходимо повторять каждые 10 лет;
- гепатита В – вакцинация показана всем непривитым до 55 лет. Особенно она важна для медработников, контактирующих с кровью;
- кори – прививают взрослых до 35 лет, не болевших ранее. Людей из группы риска (медиков, работников образовательных учреждений), прививают до 55 лет;
- краснухи – вакцинируют только девушек до 25 лет, не болевших краснухой;
- пневмококковой инфекции – особенно такая прививка важна для пожилых людей и пациентов с хроническими заболеваниями;
- гепатита А – рекомендована проживающим в неблагополучных по заболеваемости гепатитом А районах, а также путешественникам, военным, беженцам.
При вспышках эпидемии взрослым делают прививки против ветряной оспы, холеры, брюшного тифа и других опасных инфекций.
Нет времени читать длинные статьи? Подписывайтесь на нас в соцсетях: слушайте фоном видео и читайте короткие заметки о красоте и здоровье.
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
Противопоказания к вакцинации от коронавируса у детей и взрослых
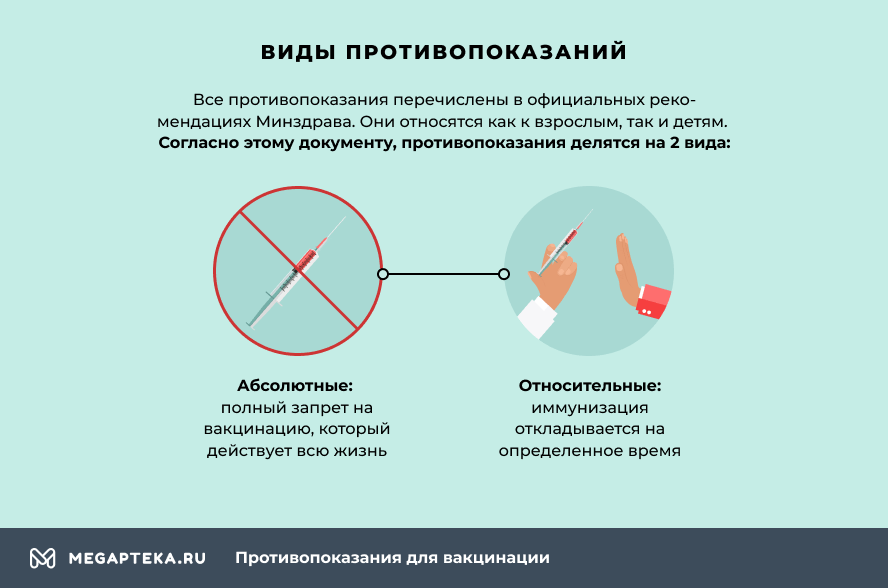
Все противопоказания перечислены в официальных рекомендациях Минздрава. Они относятся как к взрослым, так и детям.
- Абсолютные – полный запрет на вакцинацию, который действует всю жизнь, так как у организма имеются особенности, которые не исчезают с возрастом.
- Относительные – иммунизация откладывается по ряду причин, но при их исчезновении запрет на прививку снимается.
Относятся к небольшой группе людей. Не делают никакие прививки, если после предыдущей вакцинации наблюдалась выраженная реакция – температура выше 400, заметный отек и сильное покраснение в месте инъекции. Также прививки запрещены при анафилактических и аллергических реакциях на вакцины, вводившиеся ранее.
Также в некоторых случаях запрещается иммунизация конкретной вакциной, но запрет не распространяется на все остальные.
Например, коревую вакцину нельзя применять для людей с тяжелыми проявлениями аллергии на антибиотики-аминогликозиды (Гентамицин, Тобрамицин). А противопоказанием к прививке против гепатита В служит аллергия на дрожжи.
Решение о том, откладывать вакцинацию или нет, принимает врач. Основанием для временной отмены служит:
- близость к очагу эпидемии, контакт с зараженным человеком;
- острая фаза любой болезни;
- обострение хронических патологий;
- недавно перенесенные хирургические вмешательства;
- переливание крови.
При острой форме болезни вернуться к вопросу вакцинации можно через 2-4 недели после полного выздоровления. Пациентам с хроническими патологиями прививку делают только в стадии ремиссии. В течение 3-4 недель не следует без крайней необходимости проводить иммунизацию пациентам, перенесшим хирургическое вмешательство. Если операция плановая, лучше привиться заранее, за месяц и более до вмешательства.
При наличии одного из перечисленных противопоказаний, перед вакцинацией рекомендуется пройти обследование. Это даст возможность убедиться в отсутствии риска осложнений после введения вакцины.
Можно ли делать прививки онкологическим больным
Злокачественные опухоли значительно ослабляют иммунные силы и повышают восприимчивость организма к атакам вирусов и бактерий. В таких случаях очень важно максимально снизить вероятность заражения любой инфекцией. Поэтому наличие онкологического заболевания не служит поводом для полного отказа от вакцинации.
Согласно рекомендациям Минздрава, пациентов с онкологией нельзя прививать живыми вакцинами. Таким больным иммунизацию проводят инактивированными или рекомбинантными вакцинами. Эти препараты не содержат живых микроорганизмов и являются самыми безопасными.
Вакцинацию проводят не менее, чем за 2 недели до начала химиотерапии или через 3 и более месяцев после лечения. Также минимум на полгода откладывают прививки пациентам, получающим терапию анти-В-клеточными телами. Во время проведения лечебных мероприятий в случае крайней необходимости допускается введение противогриппозной инактивированной вакцины.
Благодаря совершенствованию технологий производства, современные вакцины вызывают все меньше побочных реакций. Соответственно, уменьшается и список противопоказаний для их введения.
Решение об иммунизации каждый человек принимает самостоятельно. Но при этом следует помнить, что многие инфекции без прививок наносят существенный вред здоровью и приводят к массовым эпидемиям. Сейчас, в период пандемии COVID-19, вакцинироваться необходимо, чтобы не допустить дальнейшего распространения и мутаций коронавируса, а также снизить риск развития заболевания в тяжелых формах.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.

Каждая клетка практически всех живых организмов содержит холестерин (ХС) – жироподобную субстанцию, передающуюся по системе кровообращения. Без этого вещества невозможно нормальное функционирование нервной, иммунной, пищеварительной систем. Но при повышенных показателях ХС начинает откладываться на сосудистых стенках. Это приводит к образованию бляшек, сужающих сосуды и нарушающих их эластичность. Почему же растет уровень холестерина и как с ним бороться?
Когда холестерин становится опасен
При увеличении показателей ЛПНП переработка и выведение избытков ХС нарушается. Постепенно откладывающиеся на сосудистых стенках излишки вызывают атеросклероз, от которого страдают сосуды, снабжающие кровью почки, кишечник, нижние конечности. Повреждения сосудов, питающих мозг, вызывают такие симптомы, как головокружения, обмороки, а затем развивается инсульт. Опасен атеросклероз и для сердечно-сосудистой системы. Ухудшение проходимости сосудов приводит к ИБС (ишемическая болезнь сердца), а в будущем – к инфаркту миокарда.
Высокая концентрация ХС до момента развития серьезных патологий никак не отражается на самочувствии. Поэтому даже молодым людям рекомендуется периодически сдавать анализ на общий холестерин. И при отклонениях от нормы срочно принимать меры.
Если повышен холестерин в крови: что делать
Решать проблему нужно комплексно. Для выбора оптимальных методов борьбы с повышенным ХС обязательно проконсультируйтесь с кардиологом. На начальных стадиях снижения показателей нередко удается добиться без применения медикаментов. В зависимости от степени риска, врач может посоветовать:
- Отказаться от плохих привычек – курение и алкоголь в больших количествах негативно влияют на сосуды, поэтому не стоит создавать для них дополнительную нагрузку.
- Повысить физическую активность – самый простой способ поддерживать хорошее состояние сосудов. Полезна ежедневная кардионагрузка продолжительностью не менее 30 минут: ходьба, бег трусцой, велосипед. Выработать привычку больше двигаться помогут фитнес-часы.
- Снизить вес – высокий ХС – частый спутник повышенной массы тела. Ожирение увеличивает риск диабета, гипертонии, болезней сердца. Чтобы защитить себя от этих болезней, нужно постараться сбросить лишние килограммы.
- Пересмотреть рацион – отказаться от продуктов, в состав которых входят трансжиры (фастфуд, продукты вторичной переработки), употреблять побольше клетчатки, ввести в меню морскую рыбу, заменить черный чай зеленым. Также лучше отказаться от продуктов с высоким содержанием животных жиров: сливочное масло, жирное мороженое, сосиски и колбасы.
- Скорректировать режим. В исследовании, опубликованном SleepTrusted Source, исследователи обнаружили, что слишком большое или малое количество сна негативно влияет на уровень холестерина. Они обследовали группу из 1666 мужчин и 2329 женщин старше 20 лет. Сон менее пяти часов повышал уровень триглицеридов и снижал ЛПВП у женщин. Сон более восьми часов дал аналогичный результат. Мужчины оказались не так чувствительны к чрезмерному сну, как женщины.
В зависимости от состояния и результатов обследования, пациенту также может быть предложено медикаментозное лечение.
Нет времени читать длинные статьи? Подписывайтесь на нас в соцсетях: слушайте фоном видео и читайте короткие заметки о красоте и здоровье.
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
Как снизить холестерин в крови
При каком холестерине надо начинать пить статины? Ответить на этот вопрос может только специалист после всестороннего обследования пациента. Идеальный уровень общего ХС не должен превышать 5,2 ммоль/л, а ЛПНП – 130 мг/дл. Но даже при повышенных показателях статины назначаются не всегда. При отсутствии высокой вероятности инфаркта или инсульта препараты не применяются. Если же в анамнезе присутствует сердечный приступ, они могут быть назначены даже при нормальном ЛПНП.
Американская кардиологическая ассоциация выделяет 4 группы пациентов, которым показано назначение этих лекарств. К ним относятся пациенты:
- С диабетом и гипертонией с большим стажем курения, у которых высокий уровень ХС сохраняется на протяжении последних 10 лет.
- Страдающих от атеросклероза. Также в эту группу входят больные с заболеваниями сердечно-сосудистой системы (ССС), перенесшие коронарное стентирование.
- С ЛПНП выше 190 мг/дл.
- Диабетики с постоянно повышенным уровнем ЛПНП.
Если пациент относится к одной или нескольким из этих групп, ему нужно принимать статины, начиная с низкой или средней дозировки. Возможно, изменив свой образ жизни и пересмотрев рацион, вам удастся снизить ХС без препаратов. Но, если статины были назначены, отказываться от их приема без консультации с кардиологом нельзя.

Относитесь к своему здоровью с максимальной ответственностью. Помните, что осложнения, вызываемые атеросклерозом, необратимы, полностью вылечить их невозможно. Лекарства не избавляют от уже имеющихся проблем, а лишь предотвращают развитие новых.
Читайте также:

