Можно ли вич инфицированным принимать иммуномодуляторы
Обновлено: 23.04.2024
Комбинированная антиретровирусная терапия разработана несколько лет назад в США и уже более года используется в России. Использование сочетаний ингибиторов обратной транскриптазы (АЗТ, фосфазид и т. д.) и ингибиторов протеаз (индинавир, невирапин и т.
Комбинированная антиретровирусная терапия разработана несколько лет назад в США и уже более года используется в России.
Использование сочетаний ингибиторов обратной транскриптазы (АЗТ, фосфазид и т. д.) и ингибиторов протеаз (индинавир, невирапин и т. д.) в ряде случаев позволяет при нормальном уровне СД4 добиться снижения вирусной нагрузки до уровня менее 200 копий в 1 мл плазмы.
Проводимый при лечении ингибиторами мониторинг СД4 и ВН (вирусной нагрузки) позволяет заключить, что комбинации препаратов необходимо достаточно часто менять из-за быстрой выработки резистентных штаммов. У данной комплексной терапии есть и ряд других отрицательных сторон: токсичность препаратов, высокая стоимость терапии — от 1000 долл. и выше. В настоящее время речь уже не идет о монотерапии, а только о ди-, а чаще тритерапии. Кроме того, сроки лечения ингибиторами удлинились до 5 и более лет.
Рост числа ВИЧ-инфицированных во всем мире, и в России в том числе, отсутствие достоверных сведений о возможности излечения с помощью существующих ныне методов, неизбежный летальный исход делают проблему терапии и разработку новых методов лечения ВИЧ-инфекции крайне актуальной. Среди возможных подходов к лечению ВИЧ-инфекции — усиление защитных сил макроорганизма. Одним из наиболее широко используемых с этой целью средств являются интерфероны (ИНФ). В последнее время все глубже изучаются механизмы противовирусной активности интерферонов, в том числе и при ВИЧ-инфекции [4, 5, 6, 7, 8].
Среди ИНФ-индуцируемых белков, обладающих противовирусной активностью, лучше всего изучены 2', 5'-олигоаденилатсинтетаза (ОАС), двухцепочная (дц) РНК-зависимая протеинкиназа и белок Мх. Протеинкиназа и ОАС обладают ферментативной активностью, однако до момента инфицирования клеток вирусами остаются в неактивном состоянии.
Протеинкиназа активируется дцРНК-зависимым автофосфорилированием. При этом протеинкиназа имеет две киназные активности: первая из них важна для автофосфорилирования, вторая — для субстратного фосфорилирования.
Белки Мх составляют семейство IFN-стимулируемых, антигенно родственных белков, детерминирующих селективную устойчивость клеток к ряду РНК-содержащих вирусов. Механизмы противовирусного действия белков Мх специфичны для разных систем вирус — хозяин. Доказано, что противовирусная активность и специфичность действия определенного белка Мх зависят от внутриклеточной локализации белка и стратегии размножения вирусов. Характерной особенностью белков Мх является то, что одни белки функционируют в ядре, а другие — в цитоплазме. В связи с этим чувствительны к действию определенного белка Мх вирусы, места внутриклеточного размножения которых совпадают с локализацией белка Мх.
В основе ингибирующего влияния белков Мх на вирусы лежит общий механизм, обусловленный взаимодействием белков Мх с компонентами РНК-полимеразного комплекса. Этот механизм для разных вирусов может, вероятно, действовать на разные этапы их внутриклеточного онтогенеза, вызывая либо ингибирование инициации транскрипции, либо преждевременную терминацию элонгации, либо нарушение транспорта вирусных белков из цитоплазмы в ядро.
Доказано, что в то время как другие вирусы производят нормальный интерферон, защищающий клетки от вирусной инфекции, ВИЧ способствует появлению ненормального интерферона, который помогает вирусу выжить.
В ходе лабораторных исследований острого и хронического ВИЧ-заболевания выявлено значительное антивирусное воздействие интерферонов a и b. К тому же интерферон a обладает значительным терапевтическим воздействием на ряд СПИД-индикаторных инфекций, в том числе cаркому Капоши. Натуральный ИФН a более эффективно подавляет воспроизводство ВИЧ 1, чем рекомбинантный a-интерферон [6].
Необходимо отметить, что, так как интерфероны включены в некоторые патогенетические аспекты ВИЧ-инфекции и СПИДа, они могут служить важными средствами в ограничении распространения вируса и прогрессирования заболевания; то есть борьба с одним из звеньев цепи репликации вируса может косвенно уничтожить ВИЧ и помочь в восстановлении иммунной системы [7].
Обычно длительное использование интерферонов, как природных, так и рекомбинантных, представляется проблематичным, так как они обладают антигенностью; необходимо их многократное введение в течение суток для поддержания достаточной концентрации в организме. Кроме того, ИФН дают большое количество побочных эффектов.
В этом плане хорошо себя зарекомендовали индукторы интерферона, обладающие не только иммунокорригирующим, но и антивирусным действием.
Использование их позволяет уменьшить лекарственную нагрузку и ее токсический эффект, а также преодолеть развитие резистентности.
Более чем пятилетний опыт работы с циклофероном на базе Санкт-Петербургского городского центра по профилактике и борьбе со СПИДом показал высокую эффективность препарата в поддержании иммунного статуса и профилактике СПИД-индикаторных инфекций при отсутствии побочного действия [2].
В 1998 году на базе Российского научно-методического центра по профилактике и борьбе со СПИДом была изучена динамика суррогатных маркеров ВИЧ-инфекции (уровень СД4 лимфоцитов) и вирусная нагрузка у ВИЧ-инфицированных лиц при лечении 12,5%-ным циклофероном. Полученные результаты свидетельствуют о достоверном росте уровня СД4 и снижении вирусной нагрузки на 0,5-1,5 log10, причем в ряде случаев (25%) до неопределяемых величин(
Вышеуказанное стало предпосылкой для проведения настоящего исследования, позволяющего изучить эффективность таблетированной формы циклоферона при длительном (6 месяцев) непрерывном использовании у ВИЧ-инфицированных лиц на разных стадиях заболевания с целью перспективной разработки моно- и комбинированной терапии, снижающей токсичность и резистентность традиционных методов лечения ВИЧ-инфекций [4].
Диагноз ВИЧ-инфекции ставился на основании клинико-эпидемиологических данных и подтверждается серологическими методами иммуноферментного анализа и иммунного блотинга. Стадия заболевания определялась согласно Российской классификации ВИЧ-инфекции (В. И. Покровский, 1989). Исходно в опытную и контрольную группы входили по 35 человек в каждую. Однако уже к моменту обследования больных во второй стандартной точке контрольная группа состояла из 31 человека. Состав опытной группы, до завершения исследования, не менялся.
Таблица 1. Группы исследуемых больных
| Стадия ВИЧ-инфекции | Исследуемая группа (чел.) | |
| Контрольная | Опытная | |
| 2Б + 2В | 14 | 17 |
| 3А + 3Б | 17 | 18 |
В связи с тем что стадии инфицирования 2Б и 3Б оказались представлены незначительным числом обследуемых, для дальнейшего анализа больные были объединены в подгруппы (табл. 1).
Исследование проводили двойным слепым методом с использованием плацебо.
Оценка эффективности проводимой терапии осуществлялась по клиническим и лабораторным критериям оценки прогрессирования ВИЧ-инфекции.
Клинико-лабораторное обследование больных проводили в трех стандартных точках:
1. Перед началом лечения.
2. Через три месяца после начала лечения.
3. Через шесть месяцев после начала лечения.
Количественное определение РНК ВИЧ в ПЦР проводили в первой и третьей стандартных точках. Включение в исследование разрешалось только после получения от больного письменного информированного согласия.
За шесть месяцев не отмечено ни одного случая перехода больных в следующую стадию как в опытной, так и в контрольной группе. Однако в опытной группе в 34% случаев отмечено уменьшение размеров лимфатических узлов, что может косвенно свидетельствовать об обратном развитии процесса. В контрольной группе такие явления отмечались в 9,6% случаев. Как в опытной, так и в контрольной группе отмечалось в 30% случаев уменьшение размеров печени и в 10% случаев — размеров селезенки. Исследование проводилось в осенне-зимний период (вспышка гриппа), что позволило отследить тяжесть перенесенных простудных заболеваний в опытной и контрольной группах. Существенной количественной разницы между заболевшими ОРВИ не отмечалось, однако длительность заболевания в опытной группе была на 25% меньше, а тяжесть токсических проявлений — значительно ниже.
В опытной группе за весь период исследования не отмечено появления новых СПИД-индикаторных инфекций, в то время как в контрольной группе в 16% случаев добавился диагноз оральный кандидоз и в 9,6% — Herpes simplex.
Показатели периферической крови не выявили достоверных различий между опытной и контрольной группами, однако в опытной группе наметилась тенденция к снижению абсолютности содержания нейтрофильных гранулоцитов.
Биохимические показатели периферической крови и анализ вирусспецифических белков и маркеров гепатита В и С также не выявили различий в опытной и контрольной группах. Динамика изменений иммунологических показателей в процессе лечения в опытной и контрольной группах достаточно показательна.
Таблица 2. Динамика средних значений количества СД4-Т-лимфоцитов для больных с исходным иммунодефицитом (количество СД4-Т-лимфоцитов до начала лечения менее 500 кл/мл)
| Периоды наблюдения | Количество CД4-Т-лимфоцитов (M±m) | |
| ОГ | КГ | |
| До начала лечения | 370,0±39,1 | 376,2±23,4 |
| Через 3 месяца | 505,0±130,3 | 366,3±50,9 |
| Через 6 месяцев | 609,0±58,7 | 368,3±53,8 |
Исследование функциональной активности лимфоцитов показало, что под влиянием циклоферона происходит достоверное повышение контрольных значений лимфакинпродуцирующей способности клеток (РТМЛ). Имеющий место в начале исследования компенсаторный энергетический дисбаланс (активностьЛДГ>СДГ) исчезает, и восстанавливается физиологическое соотношение циклов Кребса и трикарбоновых кислот.
Особенно показательной была динамика средних значений СД4-Т-лимфоцитов у больных с исходным иммунодефицитом (500 кл/мл) (см. табл. 2).
Характерными и прогнозируемыми с учетом анализа результатов использования ампульной формы циклоферона оказались показатели вирусной нагрузки при лечении ВИЧ-инфекции таблетированной формой циклоферона (табл. 3, 4).
Таблица 3. Параметры улучшения и увеличения ВН за 6 месяцев
| Параметры изменений ВН | Количество больных | p | 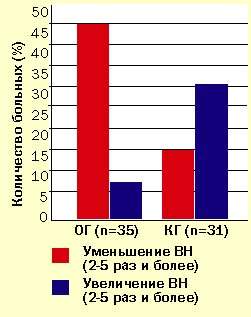 | |||
| ОГ (n=35) | КГ (n=31) | |||||
| абс. % | абс. % | |||||
| Уменьшени | ||||||
| до 2-х раз | 8 | 7 | p | |||
| в 2-5 раз | 7 | > 45.7 | 5 | > 16.1 | ||
| более 5 раз | 9 | - | ||||
| Увеличение | ||||||
| до 2-х раз | 4 | 8 | p | |||
| в 2-5 раз | 2 | > 8.6 | 7 | > 32.3 | ||
| более 5 раз | 1 | 3 | ||||
| Уменьшение до следовых значений ( | 5 | 0 | ||||
Таблица 4. Сопоставление показателей ВН до начала лечения и через 6 месяцев
| Показатели ВН (коий/мл) | Количество больных | |||||||
| ОГ (n=35) | КГ (n=31) | |||||||
| До лечения | Через 6 месяцев | До лечения | Через 6 месяцев | |||||
| абс. | % | абс. | % | абс. | % | абс. | % | |
| до 10000 | 10 | 28.6 | 18 | 51.4 | 15 | 48.4 | 14 | 45.2 |
| 10000 — 30000 | 13 | 37.1 | 9 | 25.7 | 5 | 16.1 | 5 | 16.1 |
| 30000 — 100000 | 5 | 14.3 | 5 | 14.3 | 5 | 19.4 | 3 | 9.7 |
| Более 100000 | 7 | 20.0 | 3 | 8.6 | 6 | 16.1 | 9 | 29.0 |
| Примечание: р | ||||||||
Отмечено значительное (более 70%) снижение концентрации РНК ВИЧ в опытной группе в стадии 2Б + 2В. Одновременно с этим нарастает и доля больных с низким, вплоть до неопределяемого уровня РНК. Аналогичная тенденция наблюдается в данной группе и на стадии инфицирования 3А + 3Б. Однако в данном случае снижение вирусной нагрузки составляет всего лишь 31,1%.
Литература
1. Романцов М. Г., Ершов Ф. И., Коваленко А. Л., Голубев С. Ю. Иммунодефицитные состояния: коррекция циклофероном. 1988. 80 с.
2. Ершов Ф. И., Коваленко А. Л., Аспель Ю. В., Романцов М. Г. Циклоферон в терапии вирусных гепатитов и ВИЧ-инфекций. 1999. 40 с.
3. Ершов Ф. И., Романцов М. Г., Коваленко А. Л., Исаков В. А., Аспель Ю. В. Циклоферон 12,5%-ный для инъекций: итоги и перспективы клинического применения. 1999, 80 с.
4. Отчет о клинико-иммунологической эффективности циклоферона (таблетированная форма) в терапии ВИЧ-инфекции СПб, гор. центр СПИД, ВМА им. С. М. Кирова, ин-т им. Пастера. 1999. 60 с.
5. Бажан С. И., Белова О. Е. Молекулярно-генетические аспекты индукции и противовирусного действия интерферона. 1998. 10 с.
6. Ямомото Дж. К., Крузель М. Л., Луи Х., Георгий Адис Дж. А. Ингибиция вируса иммунодефицита человека 1-го типа интерферонами человека альфа, бета и гамма. США, 1993.
7. Поли Г., Бисвас П., Фоки А. С. Интерфероны в патогенезе и лечении вируса иммунодефицита человека (обзор литературы). Италия, 1994.
8. Амбрус Дж. Л., Амбрус-мл. Дж. Л., Чадха С., Новик С., Рубинштейн М., Гопалакришнан Б., Бернштейн З., Приоре Р. Л., Чадха К. С. Механизмы ингибиторного действия интерферона в крови больных СПИДом и у больных красной волчанкой с васкулитом. США, 1997.
Лекарственные препараты, воздействующие на различные звенья иммунной системы, давно получили широкое распространение в современной клинической практике. Но если о пользе иммуномодуляторов при лечении ОРВИ и гриппа известно многим, то о применении этих препаратов в комплексной терапии ВИЧ, дерматологических и онкологических заболеваний слышали далеко не все.
Иммуномодуляторы – это лекарственные препараты с содержанием природных или синтетических веществ, которые при применении их в терапевтических дозах восстанавливают функции иммунной системы. Поэтому их применение показано при различных иммунодефицитных состояниях.
Применение иммуномодуляторов
Одна из главных мишеней иммуномодуляторов – вторичные иммунодефициты, или болезни иммунной системы, которые характеризуются развитием повторных, затяжных инфекционно-воспалительных заболеваний всех локализаций и любой этиологии. Патологические процессы при этом могут охватить кожу, подкожную клетчатку, верхние дыхательные пути, легкие, мочеполовую систему, пищеварительный тракт и другие органы. Причиной развития вторичных иммунодефицитов могут стать хронические вирусные инфекционные заболевания, включая такое серьезное заболевание, как ВИЧ-инфекция. Чтобы выявить наличие вируса иммунодефицита в крови, проводится тестирование на антитела.

Пока что наука не может предложить метод, который победил бы ВИЧ и полностью удалил его из организма человека. Но уже сейчас успешно применяется самая современная и эффективная на сегодняшний день высокоактивная антиретровирусная терапия (ВААРТ), которая направлена на замедление прогрессирования заболевания и остановку его перехода в СПИД (AIDS) – термальную стадию развития ВИЧ-инфекции, которая формируется в среднем через 9-10 лет после инфицирования человека вирусом иммунодефицита. Однако, при соответствующей терапии жизнь инфицированного человека может продолжаться до 70-80 лет. И помочь в этом могут в том числе и иммуномодуляторы.
Применение иммуномодуляторов при ВИЧ
Как известно, вирус иммунодефицита человека достаточно быстро видоизменяется. На один ген приходится до 1000 мутаций. При отсутствии лечения ВИЧ воспроизводит себя достаточно быстро: в организме инфицированного человека образуется от 10 до 100 миллиардов новых вирусов в день. Для сравнения: вирус гриппа мутирует примерно в 30 раз реже. Это одна из главных причин, препятствующих изобретению вакцины против ВИЧ.
Основное коварство ВИЧ состоит в том, что он постепенно разрушает клетки иммунной системы и делает человека беззащитным перед другими заболеваниями, которые обычно и приводят к изменению качества жизни больных. Для проведения терапии сопутствующих ВИЧ-инфекции других инфекционных заболеваний необходимо очень тщательно подходить к выбору лекарственных средств, а также не забывать о комплексном лечении, которое было бы направлено на несколько возбудителей одновременно. В список препаратов могут попасть антибиотики, противогрибковые и противовирусные препараты, а также иммуномодуляторы.
Список типов препаратов-иммуномодуляторов при ВИЧ-инфекции
При ВИЧ иммуномодуляторы применяют с обязательным учетом особенностей и механизмов их воздействия, возможных побочных эффектов и клинико-иммунологического состояния пациентов. Среди препаратов, которые врачи могут рекомендовать при вирусе иммунодефицита человека – препараты на основе:
- интерферонов,
- интерлейкинов
- лекарства с содержанием тимопоэтина,
- альфа-глутамил-триптофан натрия
- комплекса дезоксирибонуклеата натрия с железом и других составляющих.
Иммуномодуляторы при онкологических заболеваниях (раке)
Среди основных методов борьбы с онкологическими заболеваниями, которые применяются во всем мире, – лучевое и химиотерапевтическое лечение. Эффективность подобной терапии давно подтверждена, она ежегодно помогает спасать жизни десяткам тысяч людей. Однако, нельзя не принимать во внимание тот факт, что с целью повышения процента ремиссий заболевания ученые постоянно разрабатывают и внедряют в практику все более агрессивные схемы лечения, что приводит к развитию выраженных функциональных и количественных нарушений в иммунной системе. Это может стать причиной развития различных аутоиммунных, аллергических и инфекционных осложнений, что может дополнительно усугубить течение онкологического заболевания. Подобные осложнения могут препятствовать проведению лечения основного заболевания, снижать его эффективность и тем самым способствовать росту опухоли и ухудшению качества жизни пациентов.
По этой причине врачи-онкологи в процессе комплексного лечения особое внимание уделяют иммунокорригирующей терапии. Применение препаратов, положительно влияющих на иммунитет, способствует уменьшению токсичности химиопрепаратов, сокращению сроков восстановления лейкоцитов, снижению заболеваемости от вирусных инфекций, а в ряде случаев – увеличению продолжительности ремиссии. При онкологическом заболевании можно принимать только лекарственные средства с хорошо изученным механизмом действия, которые преимущественно могут влиять на то или иное звено иммунной системы. Очень важно понимать, что самостоятельно выбирать такие препараты не рекомендуется. Перед началом приема иммуномодуляторов при раке необходима оценка параметров иммунной системы врачом с последующим подбором соответствующего лекарства.
Корригировать показатели иммунитета может быть необходимо как после лучевой и химиотерапии, так и после оперативных вмешательств. Также подобное лечение проводится для коррекции иммунологических нарушений, которые возникают вследствие иммунодепрессивного воздействия на иммунную систему самой злокачественной опухоли. Среди иммуномодуляторов, которые применяют при лечении онкологических заболеваний, – препараты микробного происхождения, пептидные препараты, цитокины и препараты на их основе (интерфероны, интерлейкины), препараты на основе природных факторов (препараты иммуноглобулинов, экстракты растений).
Иммуномодуляторы при ВПЧ (вирусе папилломы человека)
Вирус папилломы человека (ВПЧ) – это совокупность микроорганизмов вирусной природы, которые передаются от одного живого организма другому. ВПЧ населяет исключительно базальный слой эпидермиса, а его размножение происходит в верхних слоях кожи. Проникая в организм своего хозяина, вирус внедряется в ДНК клеток. Инфицированная вирусом клетка интенсивно растет и делится, а через некоторое время на пораженном участке появляются характерные разрастания – папилломы, остроконечные кондиломы и бородавки. ВПЧ может быть с низким, средним и высоким риском онкологического перерождения.

Список препаратов-иммуномодуляторов при ВПЧ
С проявлениями ВПЧ борются препараты с содержанием:
- интерферона
- комплекса инозина и соли 4-ацетамидобензойной кислоты
- глюкозаминилмурамилдипептида
- веществ растительного происхождения.
Одним из препаратов интерферона, который используется для лечения папилломавирусной инфекции, является ВИФЕРОН – иммуномодулирующий препарат с противовирусным действием. Препарат выпускается в трех лекарственных формах: Свечи (суппозитории ректальные), Мазь и Гель.
Схема лечения препаратом ВИФЕРОН Свечи при ВПЧ
Рекомендуемая доза для взрослых для лечения папилломавирусной инфекции – ВИФЕРОН 500 000 ME по 1 суппозиторию 2 раза/сут через 12 ч ежедневно в течение 5-10 суток и более при рецидивирующей инфекции. По клиническим показаниям терапия может быть продолжена.
Так как элиминация любого инфекционного возбудителя является результатом синергического взаимодействия между защитными силами макроорганизма и антимикробными агентами, то лечение антибиотиками, противовирусными и противогрибковыми средствами будет малоэфф
Так как элиминация любого инфекционного возбудителя является результатом синергического взаимодействия между защитными силами макроорганизма и антимикробными агентами, то лечение антибиотиками, противовирусными и противогрибковыми средствами будет малоэффективным у лиц с исходно пониженной функциональной активностью иммунной системы. Поэтому оправдан поиск препаратов, стимулирующих иммунологическую реактивность и тем самым повышающих эффективность антимикробной терапии. Речь идет об иммуномодуляторах — лекарственных препаратах с иммунотропным действием, усиливающих эффективную иммунную защиту [9, 10, 13].
При вялотекущих, рецидивирующих, плохо поддающихся химиотерапии, имеющих тенденцию к хронизации заболеваниях целесообразно включение в комплексную терапию иммуномодулятора. Отечественный препарат последнего поколения — полиоксидоний — является иммуномодулятором первого выбора.
В условиях целостного организма полиоксидоний оказывает сложное и многогранное действие на иммунную систему. Так как развитие любого иммунного ответа начинается с клеток моноцитарно-макрофагальной системы, а цитокины, продуцируемые моноцитами/макрофагами, обладают плейотропным эффектом, то усиление под влиянием полиоксидония их функциональной активности ведет к активации и клеточного, и гуморального иммунитета. Так, в частности, при введении полиоксидония совместно с низкими дозами антигена происходит усиление синтеза антител к этому антигену в 5-10 раз по сравнению с контролем. Важно отметить, что такое усиление можно наблюдать у животных с генетически детерминированной слабой отвечаемостью на данный антиген [6]. Таким образом, полиоксидоний обладает способностью приводить в движение все факторы, защищающие организм от инфекционных агентов, причем защищающие естественным путем, так, как это происходит при развитии иммунного ответа в организме. А интенсивность иммунного ответа в большей степени зависит от исходного функционального состояния иммунной системы человека [6].
Рассмотрим, какова же клиническая и иммунологическая эффективность полиоксидония при трех основных формах иммунодефицитов.
Первичные иммунодефициты — это врожденные нарушения иммунной системы, связанные с наличием дефектов на генном уровне. Применение иммуномодуляторов при этих заболеваниях на первый взгляд кажется бесперспективным. Естественно, вылечить с помощью любого, даже самого хорошего иммуномодулятора первичный иммунодефицит невозможно, но применение этих препаратов в комплексном лечении таких состояний является обоснованным. Это связано с тем, что, согласно концепции иммунологических мобилей [4], иммунная система работает по типу весов. Наличие груза, даже очень небольшого, на одной из чашечек весов приводит в движение всю систему. Концепция иммунологических мобилей обосновывает применение иммуномодуляторов при первичных иммунодефицитах. Мы полагали, что активация, например, фагоцитарной системы у больных с дефектами в биосинтезе антител может в какой-то степени компенсировать этот недостаток и привести хотя бы к временному улучшению клинического состояния больного.
В отделении иммунопатологии нашего института полиоксидоний применялся в комплексном лечении первичного иммунодефицита — общей вариабельной иммунологической недостаточности (ОВИН) у взрослых. Это заболевание характеризуется снижением всех классов иммуноглобулинов — IgG, IgA, IgM и клинически чаще всего проявляется в виде хронических рецидивирующих заболеваний бронхолегочного аппарата. Как правило, при длительном течении ОВИН и выраженных очагах инфекции у этой категории больных формируется комбинированный клеточно-гуморальный дефект иммунитета; у многих пациентов отмечается тенденция к лейкопении, нейтропении и лимфопении.
У больных с ОВИН лечение полиоксидонием проводили по индивидуальной схеме: начинали с 12 мг, в/в, № 3 через день, а потом переводили на поддерживающую терапию по 6 мг в/м до 10 инъекций. В некоторых случаях полиоксидоний применяли в течение трех месяцев. У больных ОВИН в результате терапии полиоксидонием формула крови нормализовывалась, сокращались сроки лечения обострений, удлинялась ремиссия и в целом существенно улучшалось качество жизни.
К приобретенным иммунодефицитам относится ВИЧ-инфекция. Длительное время клинические иммунологи подвергали сомнению целесообразность применения иммуномодуляторов у больных с этой инфекцией, так как опасались активации под их влиянием Т-клеточного иммунитета и усиления размножения вируса. Однако в настоящее время накапливается положительный опыт применения иммуномодуляторов при ВИЧ-инфекции, и в частности полиоксидония. В НИИ клинической иммунологии Ростова-на-Дону применяли полиоксидоний совместно с антибиотиками (без противовирусной терапии) у больных в стадии пре-СПИДа с двусторонней очаговой пневмонией. У всех пациентов получен хороший клинический эффект, подтвержденный данными иммунологического и биохимического исследований. При применении антибиотиков и полиоксидония, по данным рентгенологического исследования, удалось на пять дней раньше ликвидировать очаги пневмонии в легких и вывести больных в состояние стойкой ремиссии по сравнению с теми, кто получал только антибиотики. У пациентов повысился уровень CD4+ T-клеток и вырос до единицы иммунорегуляторный индекс. Кроме того, улучшилась функциональная активность печени: снизился уровень билирубина и трансаминаз. Удивительным представляется факт существенного снижения вирусной нагрузки: с lg10 7 до lg10 6 . Мы полагаем, что снижение уровня ВИЧ связано со способностью полиоксидония повышать функциональную активность макрофагов и NK-клеток, осуществляющих элиминацию из организма инфицированных клеток. Мы также считаем, что включение полиоксидония в комплексную терапию больных СПИД, страдающих оппортунистическими инфекциями, является оправданным и целесообразным, так как резервные возможности организма человека очень велики и их повышение с помощью иммуномодулятора в ряде случаев может дать хороший клинический результат, пусть даже и кратковременный.
Вторичные иммунодефициты (ВИД) — это нарушения иммунной системы, развивающиеся в позднем постнатальном периоде или у взрослых и не являющиеся результатом генетических дефектов. Условно мы выделяем две формы ВИД: индуцированную и спонтанную [11]. Индуцированная форма возникает в результате конкретных причин, вызвавших ее появление: рентгеновское излучение, цитостатическая терапия, применение кортикостероидов, травмы и хирургические вмешательства. В этот перечень также входят нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию (диабет, заболевание печени, почек, злокачественные новообразования). Спонтанная форма вторичного иммунодефицита характеризуется отсутствием явной причины (хотя, без сомнения, она имеется), вызвавшей нарушение иммунной реактивности. Клинически она проявляется в виде хронических, часто рецидивирующих инфекционно-воспалительных процессов бронхолегочного аппарата, придаточных пазух носа, урогенитального и желудочно-кишечного тракта, глаз, кожи, мягких тканей, вызванных оппортунистическими (условно-патогенными) микроорганизмами. Поэтому хронические, часто рецидивирующие, вялотекущие, трудно поддающиеся лечению традиционными средствами воспалительные процессы любой локализации у взрослых рассматриваются как клинические проявления ВИД.
Наиболее ярким примером индуцированных ВИД являются хирургические инфекции. Доказана высокая клиническая эффективность полиоксидония, применяющегося как для их профилактики, так и при лечении [2]. В первом случае применение препарата перед операцией может существенно снизить развитие гнойно-септических осложнений, особенно при операциях на толстом кишечнике, когда велик риск их развития. При предоперационном применении полиоксидония почти в три раза удалось снизить частоту ампутации стопы вследствие язвенно-некротических поражений у больных сахарным диабетом [1]. Включение полиоксидония в комплексную терапию развившихся хирургических инфекций способствует более быстрому очищению раны от гнойно-некротических масс, ускоряет ее эпителизацию и заживление. Все это ведет к существенному снижению количества потребляемых антибиотиков и сокращению числа койко-дней. В силу наличия детоксицирующих и антиоксидантных свойств полиоксидоний особенно эффективен при токсико-септических состояниях; в этих случаях его целесообразно назначать капельно, внутривенно ежедневно в течение первых двух-трех дней и далее через сутки.
Как отмечалось выше, хроническое, рецидивирующее течение инфекционно-воспалительного процесса любой локализации может считаться проявлением ВИД. В этих случаях при назначении антимикробных препаратов целесообразным представляется также назначение иммуномодулятора. В нашем институте имеется положительный опыт применения полиоксидония в комплексном лечении хронического рецидивирующего фурункулеза [3] и хронического рецидивирующего герпеса.
У больных в стадии обострения фурункулеза в результате приема полиоксидония наблюдалось уменьшение признаков интоксикации, уменьшение инфильтрации фурункулов, более быстрая их регрессия. Наблюдение в течение двух лет выявило стойкую ремиссию заболевания у 44,6 % больных. Исходно у больных с хроническим рецидивирующим фурункулезом наблюдалось снижение функциональной активности фагоцитарных клеток, в частности снижение бактерицидных свойств нейтрофилов. Как правило, после применения полиоксидония у таких больных происходило восстановление их функциональной активности. Также имело место восстановление иммунорегуляторного индекса при его исходном нарушении.
При применении полиоксидония совместно с противовирусными препаратами у больных с рецидивирующим герпесом в стадии обострения острая фаза местного воспаления купировалась уже на вторые сутки, тогда как в контрольной группе везикулезные элементы сохранялись до пятого дня от начала лечения. Значительно быстрее достигалась и полная реэпитализация очагов поражения. У 95% больных, получавших полиоксидоний, длительность ремиссии составила в среднем три года. У этих больных наблюдалось повышение функциональной активности естественных киллеров и усиливался синтез α-интерферона, то есть полиоксидоний стимулировал развитие противовирусной защиты.
Литература
1. Гришина Т. Ю., Станулис А. И., Жданов А. В., Хаев А. В. Лечение гнойно-септических осложнений у больных диабетом // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 47-48.
2. Карсонова М. И., Пинегин Б. В., Хаитов Р. М. Иммунопрофилактика и иммунотерапия хирургических инфекций // Практикующий врач. 1998. № 12. С. 9-12.
3. Латышева Т. В., Сетдикова Н. Х. Эффективность полиоксидония при некоторых формах первичных иммунодефицитов (ОВИН) и вторичных иммунодефицитных состояниях // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 41-43.
4. Лусс Л. В. Полиоксидоний в общеклинической практике // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 21-41.
5. Петров Р. В. Я или не Я. Иммунологические мобили. М.: Молодая гвардия, 1987.
6. Петров Р. В., Хаитов Р. М., Некрасов А. В. и др. Полиоксидоний - иммуномодулятор последнего поколения: итоги трехлетнего клинического применения // Аллергия, астма и клиническая иммунология. 1999. № 3. С. 3-6.
7. Пинегин Б. В. Полиоксидоний — новое поколение иммуномодуляторов с известной структурой и механизмом действия // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 27-28.
8. Полосин А. В. Иммуномодулятор полиоксидоний — перспектива в лечении хронических урогенитальных инфекций//Аллергия, астма и клиническая иммунология. 2000. № 1. С. 45-46.
9. Хаитов Р. М., Пинегин Б. В. Иммуномодуляторы и некоторые аспекты их клинического применения // Клиническая медицина. 1996. № 8. С. 7-12.
10. Хаитов Р. М., Пинегин Б. В., Андронова Т. М. Отечественные иммунотропные лекарственные средства последнего поколения и стратегия их применения // Лечащий Врач. 1998. № 4. С. 46-51.
11. Хаитов Р. М., Пинегин Б. В. Вторичные иммунодефициты: клиника, диагностика, лечение // Иммунология. 1999. № 1. С. 14-17.
12. Хаитов Р. М., Пинегин Б. В. Современные представления о защите организма от инфекции // Иммунология. 2000. № 1. С. 61-64.
13. Хаитов Р. М., Пинегин Б. В. Основные принципы иммуномодулирующей терапии // Аллергия, астма и клиническая иммунология. 2000. № 1. С. 9-16.
14. Хоменко А. Г. Туберкулез вчера, сегодня, завтра//Проблемы туберкулеза. 1997. № 5. 9-11.
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препара
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препарата. Препарат относится к ингибиторам обратной траскриптазы.
Препаратами второго поколения являются дидеоксииназин (ДДИ), дидеоксицитидин (ДДС). В настоящее время спектр препаратов этой группы значительно расширился (ставудин-ДДТ, хивид, фосфозид и другие).
Эта группа лекарственных средств (ЛС) имеет ряд существенных недостатков. Указанные ЛС не подавляют полностью репликацию вируса, который может быть выделен у большинства больных во время терапии.
Как показали исследования, к ЗДВ достаточно быстро развивается устойчивость, в особенности на поздних стадиях болезни с усиленной репликацией ВИЧ, когда, по-видимому, возникает резистентность и к другим аналогам нуклеозидов.
Обычный фактор, существенно ограничивающий применение ЛС этой группы, — их токсичность. Для ЗДВ характерно главным образом токсическое действие на костный мозг, тогда как ДДИ и ДДС обладают нейротоксическим действием. Кроме того, ДДИ может вызывать тяжелый острый геморрагический панкреатит.
Установлена тесная связь между клинической неэффективностью ЗДВ и резистентностью к нему in vitro.
Вторая группа препаратов, открытая сравнительно недавно и уже широко используемая, — это ингибиторы протеаз: индиновир (криксиван), инвираза (саквиновир), вирасепт (нельфиновир) и другие.
В настоящее время речь не идет уже о монотерапии антиретровирусными средствами, а только о ди-, три- и даже тетратерапии. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем (< 200 копий/1 мл).
Предпочтительность комбинированной терапии обосновывается следующими положениями (В. В. Покровский).
- Использование многих этиотропных агентов более эффективно подавляет жизнедеятельность вируса, воздействуя на различные болевые точки или синергически воздействуя на одну из них.
- Это позволяет снизить дозы препаратов, что уменьшает частоту и выраженность побочных эффектов.
- Различные лекарства имеют различную способность проникать в ткани (головной мозг и т. д.).
- Комбинация лекарств затрудняет формирование устойчивости, или она появляется позднее.
Все описанные выше подходы к терапии ВИЧ-инфекции предполагали непосредственное воздействие на репликацию вируса. Другая возможная методика лечения ВИЧ-инфекции состоит в усилении защитных сил макроорганизма. Некоторые варианты такого подхода в большинстве случаев неспецифические, изредка специфические и могут воздействовать на защитные свойства клетки-хозяина.
Интерфероны, как природные, так и рекомбинантные, имеют ряд недостатков: антигенность, необходимость многократного введения для поддержания достаточной концентрации в организме, большое количество побочных эффектов и т. д.
Этих недостатков лишены многие индукторы эндогенного интерферона, некоторые из них способны включаться в синтез ИФН в некоторых популяциях клеток, что в ряде случаев имеет определенное преимущество перед поликлональной стимуляцией иммуноцитов интерфероном.
Специфическая активность циклоферона при ВИЧ-инфекции изучена в 1997 году в Институте гриппа РАМН
- Выявлена выраженная ингибирующая активность циклоферона на репродукцию ВИЧ в культуре клеток моноцитов.
- По показателям ингибирующей активности циклоферон значительно превосходит азидотимидин.
- Представленные экспериментальные данные обосновывают клиническое использование циклоферона для лечения больных ВИЧ-инфекцией.
Пятилетний опыт применения циклоферона у ВИЧ-инфицированных позволяет оценить результаты этой работы.
В период 1992 – 1997 годы в Санкт-петербургском городском центре по профилактике и борьбе со СПИД циклоферон получили 40 пациентов с разными стадиями ВИЧ-инфекции. Следует отметить, что 11 больных прошли два курса терапии циклофероном, в связи с чем общее число лиц, получивших один курс лечения циклофероном, составило 29 человек. В основном это были молодые люди в возрасте до 40 лет (20 человек), в том числе трое детей до 14 лет.
Все больные отмечали хорошую переносимость циклоферона, отсутствие пирогенных реакций после его введения.
Пациенты также констатировали улучшение общего состояния, сна и аппетита, повышение жизненного тонуса, работоспособности. 30% из числа получавших препарат и перенесших в осенне-зимний период грипп или ОРВИ отметили, что заболевание протекало непривычно легко и выздоровление наступило быстрее обычного.
Из клинической практики
После курса циклоферона отмечалось существенное снижение вирусной нагрузки (в 3,6 раза). Число CD4+ возросло на 62%. Монотерапия циклофероном оказала положительное стабильное влияние на изученные показатели у пациентов.
Определенный интерес представляют результаты многолетнего наблюдения больных ВИЧ-инфекцией, которые получали длительно циклоферон в своеобразном профилактическом режиме с целью стабилизации процесса и профилактики прогрессирования заболеваний.
В 1998 году на базе Российского научно-методического Центра по профилактике и борьбе со СПИД (руководитель член-корр. АМН В. В. Покровский) была изучена динамика суррогатных маркеров ВИЧ-инфекций (уровень CD4+) и вирусная нагрузка у больных ВИЧ-инфекцией при лечении циклофероном.
Оценка достоверности полученных результатов проводилась с помощью непараметрических критериев (критерий знаков, максимум-критерий, критерий Вилкоксона для сопряженных совокупностей).
В испытуемую группу вошли 10 взрослых больных ВИЧ-инфекцией в стадии первичных проявлений по Российской классификации ВИЧ-инфекции (В. И. Покровский, 1989 г.). Результаты исследования уровня CD4-лимфоцитов представлены в таблице и на рисунке, из которых видно, что после первых четырех недель исследования наметилась тенденция к повышению среднего уровня CD4-лимфоцитов, которое к 12-й неделе стало статистически достоверным. Это повышение сохранилось до конца исследования, несмотря на
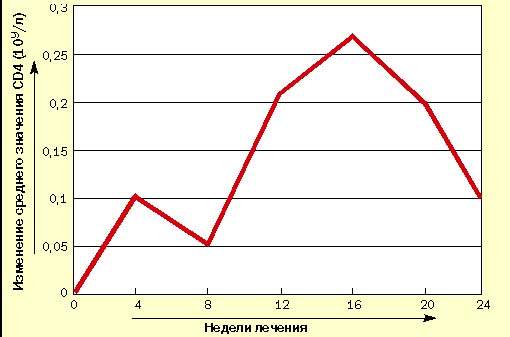 |
| Рисунок 1. Изменение уровня CD4-лимфоцитов у больных ВИЧ-инфекцией при лечении циклофероном (в сравнении с исходным уровнем) |
 |
| Рисунок 2. Средние значения изменения концентрации РНК ВИЧ (log10/мл) |
Таким образом, применение циклоферона в терапии ВИЧ-инфекций сопровождается стабилизацией клинических проявлений заболевания, улучшением состояния, а также гематологических и иммунологических показателей больных.
Циклоферон как монопрепарат оказывает иммуномодулирующее и противовирусное действие при лечении ВИЧ-инфицированных (стадии А1 3Б) в тех случаях, когда нет значительного снижения числа CD4+ клеток (<200). Хорошо зарекомендовало себя назначение циклоферона по следующей схеме.
- По 4 мл препарата в 1, 2, 4, 6, 8, 10, 13, 16, 19 и 22-й дни лечения (у детей по 2 мл). Первые две инъекции могут вводиться внутривенно, остальные внутримышечно. Повторные курсы циклоферона рекомендуется проводить через 6 месяцев под иммунологическим контролем.
- Циклоферон хорошо сочетается со всеми основными лекарственными средствами, его рекомендуется использовать в случае, когда имеются признаки активной репликации ВИЧ (высокие показатели вирусной нагрузки), у больных с обострениями различных оппортунистических заболеваний.
Исчезновение у некоторых больных иммунологических и вирусологических показаний для проведения противоретровирусной терапии может иметь важное значение для разработки новых подходов к проведению лечения больных ВИЧ-инфекцией, для снижения стоимости терапии и отсрочки развития резистентности к ней или преодолению последней.
Циклоферон может оказаться перспективным профилактическим средством при сомнительных контактах и контактах с заведомо ВИЧ-инфицированными партнерами.

— Ученые до сих пор спорят об определениях. Я считаю, что в общем и целом это защитная система, у которой нет конкретной локализации: ее элементы разбросаны по всему организму.
Но существуют органы, в которых созревают новые иммунные клетки. В тимусе (или зобной железе) происходит созревание Т-лимфоцитов, в костном мозге образуются В-лимфоциты, нейтрофилы и т. д. Затем, к примеру, лимфоциты переходят в лимфатические узлы (периферический орган иммунной системы), где приступают к защите организма. Иммунные клетки уничтожают не только микробы, но и наши собственные отмершие клетки (если их не удалять из организма своевременно, могут развиваться болезни).
— Поэтому пересадка костного мозга так эффективна в лечении ВИЧ?
— Да. При пересадке костного мозга возможно полностью избавиться от неправильных клеток — обновить состав лимфоцитов в организме, вытеснив старые. Но пересадка — очень сложная задача, потому что далеко не каждый костный мозг приживется в организме человека (даже если он вроде бы похож на оригинальный). Постепенно число удачных трансплантаций увеличивается — ученым удается подавить иммунные реакции, которые возникают при пересадке органов (организм плохо воспринимает новое чужеродное тело и стремится его отторгнуть).
— Почему у людей развиваются аутоиммунные заболевания — ревматоидный артрит, аллергии и т. д.?
— Людей обычно волнует, как укрепить или повысить иммунитет. А врачей — наоборот, как бы его снизить. Большинство проблем возникает, когда иммунитет становится гиперактивным. Это приводит к поддержанию воспалительных процессов, которые могут переходить в хроническую форму. Особенно опасны острые иммунные реакции вроде анафилактического шока, которые могут привести даже к смерти.
Не нужно пить специальные йогурты, покупать гомеопатию, есть пачками витамин С. Эффективность последнего так и не была доказана — наше представление о пользе витамина С зиждется на авторитете нобелевского лауреата Лайнуса Полинга, который пропагандировал его как средство для облегчения симптомов простуды.
— А как же весенний авитаминоз? Он вообще бывает?
— Авитаминоз — довольно редкая штука, и уж точно не бывает повальным. В МКБ-10 и МКБ-11 даже не всегда указывают как заболевание недостаток какого-нибудь конкретного витамина. Дефицит витаминов характерен для развивающихся стран, где люди могут банально плохо питаться. Если они станут есть нормально, организм сам придет в норму.
— То есть мультивитаминные комплексы не надо пить?
— Всемирная организации здравоохранения (ВОЗ) и американская Food and Drug Administration рекомендуют употреблять витамины с пищей, а не в виде таблеток. Многие говорят, что их концентрация в пище падает, но никакого дефицита не наблюдается. Также в еде содержатся вещества, которые помогают организму усваивать витамины. Например, витамины A, D, E и K обязательно нужно употреблять с жирами.
Кроме этого, некоторые исследования показывают, что большие дозы витаминов способствуют развитию опухолей.
— В каких случаях стоит посетить иммунолога?
— Обычно к иммунологу приходят с аллергиями, но также можно проверить свой уровень антител к разным возбудителям инфекций. Нам со школы не проводят ревакцинацию, а у иммунолога можно выяснить, нужно ли вам обновить прививку от гепатита B, кори, энцефалита и т. д.
Также к иммунологу стоит сходить перед поездкой в экзотические страны или регионы, где случилась вспышка инфекционного заболевания.
— Большинство из нас состояние иммунитета волнует в связи с простудами. Почему нельзя сделать прививку от простуды раз и навсегда?
— Патогены, которые вызывают у нас инфекции, довольно часто изменяют свою структуру, мутируют — поэтому каждый сезон создают новую вакцину от гриппа. К тому же разработка новых прививок — это дорого и долго, нужно проходить всякие лицензирования и сертифицирования. Проще самому переболеть.
— А иммуномодуляторы помогают от простуды?
— В России под иммуномодуляторами часто подразумевают гомеопатию, тогда как на самом деле это довольно серьезные лекарства. Например, печально известный препарат талидомид, который употребляли женщины, чтобы снять симптомы токсикоза во время беременности, приводил к рождению детей с разными отклонениями. С иммуномодуляторами надо быть поосторожнее.
Сейчас в качестве иммуномодуляторов используют цитокины (сигнальные молекулы иммунитета человека) — их модифицируют с помощью генной инженерии, благодаря чему они могут запускать иммунный ответ (уничтожение вредоносных клеток). Такие иммуномодуляторы используют в лечении онкологических заболеваний, гепатита B и С, ревматоидного артрита и т. д.
Среди иммуномодуляторов есть и те, что подавляют иммунный ответ, — супрессанты. Их используют во время пересадки органов, для лечения аллергических реакций и, к примеру, язвенного колита: цитокины подают сигнал остановить воспаление в кишечнике.
— О каких последних исследованиях в сфере иммунитета стоит знать?
— Иммунотерапия — лечение опухолевых заболеваний с помощью ресурсов иммунной системы — делает большие успехи. Исследователи научились модифицировать Т-лимфоциты, чтобы те боролись с опухолями: сначала они отбирают в организме Т-лимфоциты, которые способны убивать раковые клетки, искусственно их размножают и вводят обратно, чтобы те боролись с болезнью.
Читайте также:

