Можно смазывать папилломы витамином
Обновлено: 26.04.2024
Недавно в инстаграме и ВК опубликовал интересные назначения от коллеги по поводу диагноза себорейный кератоз. Тема вызвала живой интерес, и в результате я решил написать статью об этом явлении. В ней мы подробно разберем причины появления себорейного кератоза (и, конечно же, мифы), его разновидности, возможные сложности для здоровья, методы лечения и профилактики.
Для облегчения понимания: себорейный кератоз и кератома в дальнейшем будут использоваться как синонимы.
Что такое себорейный кератоз
Одна из наиболее частых доброкачественных опухолей кожи человека. Она развивается обычно в пожилом возрасте вследствие разрастания эпидермиса с выраженным ороговением. [1]
Эпидермис – верхний слой кожи, который постоянно отшелушивается и полностью меняется примерно в течение двух недель. Его толщина составляет от 0,07 до 1,4 мм. Таким образом, становится понятно, что кератома – очень поверхностное образование. Несмотря на то, что очаги себорейного кератоза могут быть очень большими по площади, в глубину кожи они не проникают.
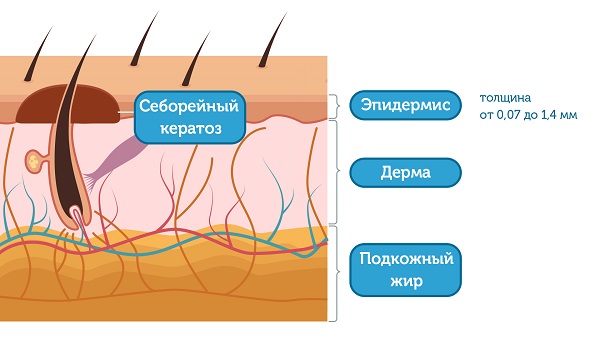
У кого чаще появляются кератомы
Из своей практики отмечу, что неоднократно видел эти образования и у людей более младшего, а иногда и детского возраста. По данным вот этого австралийского исследования [3], 12 % пациентов в возрасте от 15 до 25 лет имели в среднем 6 кератом на коже.
Где наиболее часто образуются кератомы
В порядке частоты убывания: туловище, шея, голова. Себорейный кератоз на коже конечностей встречается достаточно редко, но говорить о том, что его там не бывает, на мой взгляд, не стоит.
Факторы риска себорейного кератоза
- Солнечный свет. Как минимум одно исследование показывает связь между появлением кератом и воздействием ультрафиолета [3], хотя есть работы, подвергающие сомнению это утверждение. [2]
- Генетическая предрасположенность. Есть несколько описанных случаев семей с наследуемым большим количеством кератом, иногда в очень молодом возрасте [4].
- Вирус папилломы человека. Имеются указания, что на поверхности многих кератом методом ПЦР можно обнаружить ДНК вируса папилломы человека [4]. В то же время нельзя не отметить, что те же фрагменты ДНК ВПЧ обнаруживаются и на неизмененной коже. Роль ВПЧ в развитии кератом в настоящее время достаточно спорная.
- Нарушения иммунитета. Возникновение и прогрессирование очагов себорейного кератоза возможно у пациентов в состоянии иммуносупрессии [15]. К иммунодефициту может привести длительный прием глюкокортикостероидных гормонов.
Как выглядит кератома (себорейный кератоз)
Внешний вид кератомы во многом зависит от давности ее существования.
В начальной стадии это образование очень слабо выступает над уровнем кожи, незначительно отличается от нее по плотности и имеет цвет, очень близкий к телесному. Форма очагов круглая или овальная.
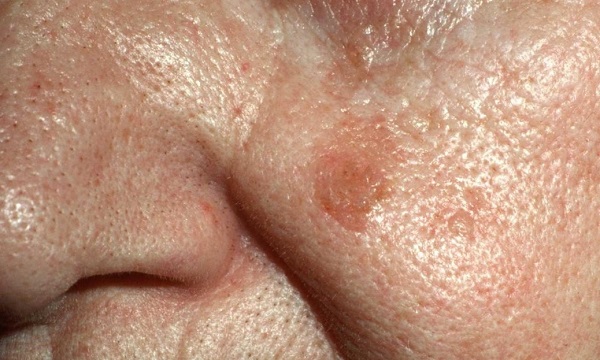
Затем, по мере увеличения количества клеток эпидермиса в образовании, кератома увеличивается в толщину и в высоту. Эти образования видны невооруженным глазом – милиаподобные кисты и комедоноподобные отверстия.


Одним из частых симптомов для кератомы, видимых невооруженным глазом, является поверхность, которая чем-то напоминает землю, потрескавшуюся после дождя. Такой рисунок образуют наслоения, состоящие из ороговевших клеток эпидермиса.
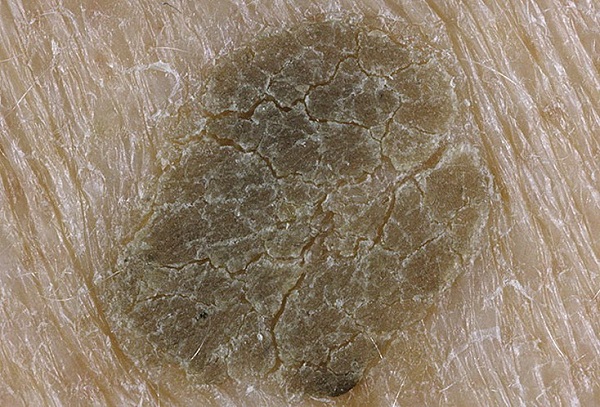
Кроме клинической формы – на широком основании – существует форма себорейного кератоза на ножке.

Вирус папилломы человека к этой форме кератом имеет очень отдаленное отношение. По моему опыту, только в единичных случаях при гистологическом исследовании таких образований были указания на признаки вирусного поражения.
Синдром Лезера-Трела
Об этом синдроме можно говорить, когда у человека внезапно появляется много кератом, особенно на туловище. В 35 % случаев это состояние ассоциировано с черным акантозом. Около 50 % пациентов отмечают выраженный зуд в области кератом. [4]
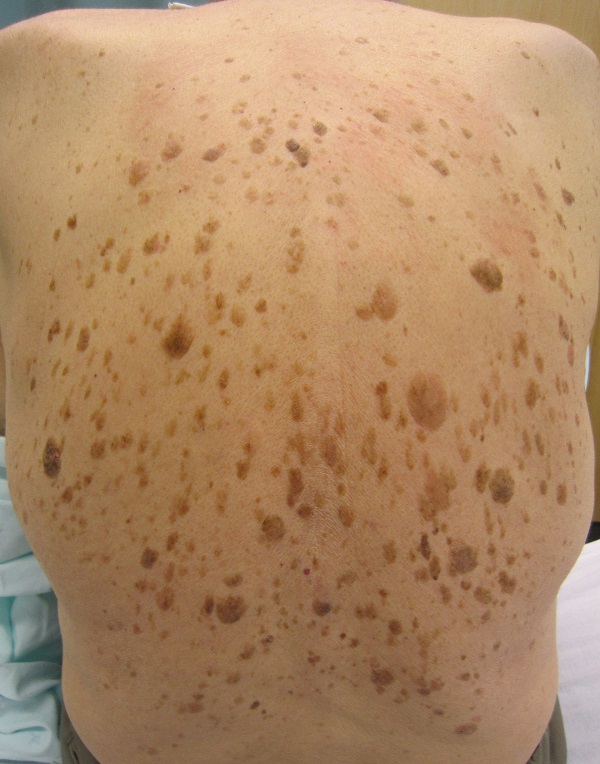
Это означает, что если множественные кератомы появлялись постепенно и присутствуют на туловище уже много лет – скорее всего, об этом синдроме речь не идет.
Некоторые исследователи подвергают сомнению существование синдрома. Это связано с тем, что указанные злокачественные опухоли чаще встречаются у пациентов старшего возраста, так же как и сам себорейный кератоз.
Лечение кератом
Подошли к самому интересному :)
Удаление
Принято считать, что лечить себорейный кератоз необязательно, т. к. природа этого заболевания доброкачественная. Тем не менее удаление очагов может быть показано для исключения озлокачествления в случаях, когда данные клинического осмотра неоднозначные. Регулярная травматизация, например одеждой, может привести к воспалению, кровоточивости и зуду и быть поводом для удаления.
Способы удаления кератом:
- лазер;
- радионож;
- электрокоагуляция;
- метод бритвенной эксцизии.
Я не буду подробно останавливаться на различных нюансах удаления. Скажу только, что, на мой взгляд, кератомы стоит удалять с гистологическим исследованием. Многие коллеги мне возразят, что в большинстве случаев диагностировать себорейный кератоз не сложно и гистологическое исследование – пустая трата денег.
В ответ приведу несколько исследований:
- В 1,4–4,4 % случаев на фоне себорейного кератоза обнаруживается плоскоклеточный рак in situ [5,6]. Аналогичный случай был в моей практике.
- Плоскоклеточный рак на фоне себорейного кератоза. [11]
- 43 случая базалиомы, 6 – плоскоклеточного рака, 2 меланомы на фоне себорейного кератоза. [9]
- 3 случая меланомы на фоне кератомы. [7,8,10]
Повторюсь, на мой взгляд, гистологическое исследование себорейного кератоза является обязательным.
Лекарственное лечение (осторожно, оно даже работает! Иногда)
Как НЕ нужно лечить кератомы:
Лучше уменьшите количество стрессов, увеличьте количество овощей и время сна (последнее не всегда работает, но точно не вредит).
Профилактика возникновения себорейного кератоза
С учетом факторов риска развития кератом, перечисленных в первой части статьи, можно смело рекомендовать избегать чрезмерного воздействия солнечного света. На эту тему есть подробная статья.
К сожалению, других методов профилактики мне придумать не удалось, т. к. на свой возраст воздействовать мы, увы, не можем. Аналогичная ситуация и с наследственностью. Роль ВПЧ в развитии кератом не настолько убедительно доказана, чтобы назначать профилактическое лечение.
Резюме
Если вам поставили диагноз кератома – в этом нет ничего страшного. Вы можете смело удалять их, если они доставляют неудобство, но я рекомендую делать это с гистологическим исследованием.
Если кератомы не удалять – это не приведет к негативным последствиям и не повлияет на их дальнейшее появление.
Помимо ярко выраженного антибактериального эффекта витамин D также оказывает противовирусное действие. Увеличивая экспрессию интерферона альфа, кателицидина, дефенсина и противовирусных микроРНК, витамин D активирует различные механизмы врожденного противовирусного иммунитета. Результаты фундаментальных и клинических исследований показывают необходимость компенсации дефицита витамина D для успешной терапии вирусных гепатитов, респираторной и папилломавирусной инфекций. Противовирусные эффекты витамина D также важны для повышения эффективности профилактики и терапии опухолевых заболеваний шейки матки.
- КЛЮЧЕВЫЕ СЛОВА: рак шейки матки, вирус папилломы человека, инфекции, заболевания кишечника, артрит, дерматит, Аквадетрим
Помимо ярко выраженного антибактериального эффекта витамин D также оказывает противовирусное действие. Увеличивая экспрессию интерферона альфа, кателицидина, дефенсина и противовирусных микроРНК, витамин D активирует различные механизмы врожденного противовирусного иммунитета. Результаты фундаментальных и клинических исследований показывают необходимость компенсации дефицита витамина D для успешной терапии вирусных гепатитов, респираторной и папилломавирусной инфекций. Противовирусные эффекты витамина D также важны для повышения эффективности профилактики и терапии опухолевых заболеваний шейки матки.
Рис. 1. Экспрессия вирусной РНК Con1-1b и J6/JFH-1 в культурах гепатоцитов под воздействием 1,25(OH)2D. Клетки обрабатывали 1,25(OH)2D в концентрациях от 0 до 0,4 мкМ в течение 48 часов, после чего их собирали и экстрагировали РНК. Уровни вирусной РНК изм
Рис. 3. Гистопатология поражений кожи, вызванных ДМБА, у мышей с делецией VDR(-/-). Участки опухолей кожи, окрашенные гематоксилином/эозином, получены от мышей с делецией VDR(-/-) через шесть месяцев после воздействия ДМБА:
Рис. 4. Результат воздействия канцерогена ДМБА на пролиферативный маркер BrdU у мышей с делецией VDR(-/-).
Рис. 5. Количественная оценка толщины эпидермиса (А) и клеток с маркером BrdU (Б) у мышей VDR(+/+) и VDR(-/-), обработанных ДМБА
Витамин D – комплексный регулятор врожденного и приобретенного иммунитета, поэтому недостаточность этого витамина снижает антибактериальный и противовирусный иммунитет, стимулирует развитие патологий, ассоциированных с хроническим системным воспалением (атопического дерматита, ревматоидного артрита, воспалительных заболеваний кишечника, аутоиммунных заболеваний щитовидной железы и сепсиса). Результаты фундаментальных и клинических исследований показали, что возникающие на фоне недостаточности витамина D хроническое воспаление и нарушения врожденного иммунитета значительно снижают резистентность организма к туберкулезу, хроническому бронхиту, вирусным заболеваниям (вирусному гепатиту, острому респираторному заболеванию, папилломавирусной инфекции) [1, 2]. Таким образом, обеспеченность витамином D может существенно влиять на иммунитет, в том числе на противовирусную защиту организма.
В настоящей статье последовательно рассмотрены молекулярные основы противовирусного действия витамина D, результаты фундаментальных и клинических исследований, указывающие на действие витамина D против вирусов гепатита, Эпштейна – Барр, папилломы человека (ВПЧ), респираторно-синцитиального вируса и др. Показана целесообразность применения витамина D в профилактике и терапии опухолевых заболеваний шейки матки.
О молекулярных механизмах противовирусного действия витамина D
Витамин-D-индуцированные механизмы, связанные с противовирусной активностью, включают корректировку врожденного иммунного ответа (интерфероны), повышение уровней кателицидина (LL-37) и дефенсина, а также активацию специфических противовирусных микроРНК. Витамин D усиливает эффект интерферона, уменьшая синтез вирусных белков в зараженных вирусами клетках. Например, при инфицировании гепатоцитов в культуре вирусом гепатита С воздействие витамина D в форме 1,25(OH)2D активирует гены, связанные с аутофагией вирусных частиц (рецептор 37 G-белков (GPR37), фактор, индуцируемый гипоксией 1-альфа (HIF-1-альфа), хемокиновый лиганд 20 (CCL20)), и подавляет интенсивность репликации вируса (рис. 1) [5].
Одна из основ противовирусного действия витамина D – повышение экспрессии антимикробных пептидов кателицидина и бета-дефенсина 2 [6], которые проявляют не только микробицидную, но и противогрибковую и противовирусную активность [7].
Антимикробный пептид кателицидин – неотъемлемый компонент витамин-D-зависимого врожденного антимикробного иммунитета. Антимикробные пептиды встраиваются в цитоплазматическую мембрану бактерий и белковые оболочки вирусов и, приводя к образованию пор, нарушают целостность бактерий и вирусов. Кроме того, проникая внутрь бактерий и вирусов, положительно заряженные антимикробные пептиды связываются с отрицательно заряженными ДНК и РНК, что также стимулирует гибель бактерий и вирусов.
Обработка моноцитов в культуре посредством биологически активной формы витамина D (1,25(OH)2D) дозозависимо повышала экспрессию мРНК антимикробного пептида кателицидина в 48–140 раз, причем увеличение экспрессии гена кателицидина коррелировало с повышенной экспрессией белка кателицидина [8]. В клиническом исследовании установлена корреляция между уровнями 25(OH)D и кателицидина в плазме крови (фактор корреляции 0,45, р = 0,05) [9]. Более высокая концентрация кателицидина в плазме существенно (в 3,7 раза) снижала риск смерти от инфекции у пациентов с диализом [10].
Витамин D повышает экспрессию определенных микроРНК, которые проявляют противовирусные и онкопротективные свойства. Напомним, что микроРНК представляют собой короткие специфические фрагменты РНК, которые ассоциируются с матричной РНК для синтеза того или иного белка и осуществляют тонкую настройку экспрессии этого белка. Иначе говоря, посредством микроРНК синтезируется столько молекул белка, сколько нужно для потребностей клетки. Как недостаточный, так и избыточный синтез белков может приводить к развитию опухолей.
Витамин D и активированные им микроРНК (в частности, miR-155 и miR-146) тормозят экспрессию целевых специфических белков, ассоциированных с формированием избыточного воспаления: толл-подобных рецепторов 2 и 4, фактора некроза опухоли альфа, интерлейкинов 1-бета и 6, транскрипционного фактора NF-kB, киназного комплекса IkB (IKK), супрессора сигналинга цитокинов 1 (SOCS1) [11]. Активная форма витамина 1,25(OH)2D потенцирует ингибирующее действие miR-130а при репликации вируса гепатита C [5], повышающего риск опухолевых процессов в печени в десятки раз. Фундаментальные исследования показали, что воздействие витамина D на иммунитет также осуществляется посредством регуляции деления Т-хелперных лимфоцитов, дифференцирования В-клеток, секреции интерферона и других цитокинов, что способствует снижению избыточного воспаления [1].
Витамин D против вирусного гепатита
25(OH)D подавляет продукцию вируса гепатита С. Клетки HuH-7 в культуре были инфицированы вирусом гепатита С в присутствии или в отсутствие витамина D. 25(OH)D дозозависимо уменьшал вне- и внутриклеточный уровни основного антигена вируса гепатита С. Ингибирующее действие 25(OH)D осуществлялось на стадии сборки инфицирующего вирусного комплекса [12].
25(OH)D подавляет репликацию вируса гепатита С и способствует более быстрому вирусологическому ответу организма. Выживаемость клеток и нагрузка вирусом наблюдались в линиях клеток Con1-1b и J6/JFH-2a в культуре, обработанных различными дозами 25(OH)D. Вирусная нагрузка клеток Con1-1b дозозависимо снижалась на 69, 80 и 86% после обработки 1, 5 и 10 мкМ 25(OH)D соответственно (р 3+ - и CD 4+ -T-лимфоцитов и отношение CD 4+ /CD 8+ значительно увеличивались (p 30 нг/мл (ОР 1,57, 95% ДИ 1,12–2,2), особенно у пациентов, получавших витамин D (ОР 4,59, 95% ДИ 1,67–12,63). Важно отметить, что противовирусный эффект витамина D не зависел от генотипа вируса гепатита С [16].
Витамин D против других вирусов
Респираторно-синцитиальная вирусная инфекция ослабляет противовирусную и противоопухолевую защиту организма путем негативного воздействия на метаболизм витамина D. При заражении клеток респираторно-синцитиальные вирусы уменьшают экспрессию рецептора витамина D (Vitamin D Receptor – VDR) и увеличивают экспрессию фермента 1-бета-гидроксилазы, которая инактивирует витамин D [19].
Витамин D способствует усилению противовирусной защиты бронхиальных эпителиальных клеток при участии противовирусного и антибактериального пептида кателицидина и активации сигнальных путей интерферона [20]. Поддерживая противовирусный иммунитет, витамин D также снижает вызываемую респираторно-синцитиальным вирусом активацию провоспалительного фактора NF-kB и соответствующих цитокинов в эпителии дыхательных путей. Витамин D индуцирует белок IkBa, ингибитор фактора NF-kB, и снижает вызываемую респираторно-синцитиальным вирусом активацию провоспалительных генов, управляемых NF-kB (интерферон бета, CXCL10 и др.). Ингибирование NF-kB посредством аденовирусных частиц, содержащих IkBa, имитировало эффекты витамина D. Таким образом, витамин D уменьшал воспалительную реакцию в ответ на вирусные инфекции, не снижая при этом противовирусного действия [21].
Метаанализ 25 рандомизированных исследований (n = 10 933), проведенный с использованием данных об индивидуальных пациентах, показал, что дотации витамина D способствовали снижению риска инфицирования острым респираторным заболеванием в среднем на 12% (ОР 0,88, 95% ДИ 0,81–0,96, p 30 нг/мл) [28]. В среднем риск инфицирования ВПЧ увеличивался на 14% при снижении уровня в сыворотке 25(ОН)D на каждые 10 нг/мл (ОР 1,14, 95% ДИ 1,02–1,27) (рис. 2).
Был опубликован клинический случай, который продемонстрировал эффективность местного применения витамина D у пациентки с папилломой на правом указательном пальце [29]. Так, пациентка А., 41 год, с врожденным заболеванием почек перенесла трансплантацию почки от умершего донора и находилась на терапии иммунодепрессантами (такролимус, микофенолата мофетил). Через 19 месяцев после трансплантации у пациентки образовалась папиллома на правом указательном пальце, которая вырастала вновь и вновь, несмотря на многократную криотерапию и электрокоагуляцию. Местное лечение папилломы с использованием раствора 1,25(OH)2D (0,5 мкг/сут) привело к полному излечению через три месяца.
Витамин D как нутриентная основа профилактики и терапии опухолевых заболеваний шейки матки
1,25(OH)2D ингибирует пролиферацию опухолевых клеток шейки матки путем подавления экспрессии онкогена рака шейки матки (HCCR-1) и увеличения экспрессии проапоптотического белка р21. Опухолевые клетки шейки матки (линия HeLaS3) культивировали в средах с различными концентрациями 1,25(OH)2D, которые индуцировали остановку клеточного цикла на фазе G1. 1,25(OH)2D дозозависимо уменьшал экспрессию белка HCCR-1 посредством транскрипционной регуляции экспрессии гена HCCR-1 и повышенной экспрессии белка p21 и промоторной активности [30].
1,25(OH)2D увеличивает экспрессию онкопротективных микроРНК в клетках рака шейки матки (линия SiHa). МикроРНК влияют на экспрессию многочисленных белков деления клетки, поэтому поддержание функции микроРНК играет важную роль в торможении возникновения и развития опухолей. Показано, что 1,25(OH)2D регулирует экспрессию онкозащитных микроРНК miR-22, miR-296-3p и miR-498 [31].
Иммуногистохимический анализ показал, что уровни экспрессии VDR при цервикальной карциноме повышены по сравнению с нормальной тканью шейки матки. Окрашивание на VDR было однородным, без визуальных различий между отдельными опухолевыми клетками. Умеренно-сильное окрашивание на VDR было обнаружено в 16 из 21 биопсии рака шейки матки независимо от того, экспрессировали эти опухоли цитокератин 10 или трансглутаминазу К. Повышенная экспрессия VDR – один из аспектов иммунного ответа организма на ВПЧ [32].
Делеция рецептора витамина D в эксперименте сенсибилизирует эпителий к химически индуцированному опухолегенезу. Данный эффект вполне понятен, так как 1,25(OH)2D – мощный регулятор клеточной пролиферации, дифференцировки и апоптоза в различных типах клеток, включая кератиноциты. У мышей, гомозиготных по делеции рецептора витамина D (VDR(-/-)), пероральное введение канцерогена 7,12-диметилбензатрацена (ДМБА) вызывало развитие папиллом на всех участках тела со средней опухолевой нагрузкой в 5,3 папиллом/мышь. Никаких папиллом или каких-либо других поражений кожи не наблюдалось у мышей соответствующего возраста и пола без делеции рецептора витамина D (VDR (+/+)) [33].
У мышей линии VDR(-/-) начиная с семинедельного возраста отмечалась гиперпролиферация клеток кожи, которая резко усиливалась после воздействия ДМБА. Без воздействия канцерогена у мышей VDR(-/-) образования опухолей не наблюдалось, но имел место прогрессирующий фенотип кожи, характеризующийся утолщенной морщинистой кожей, дермоидными кистами и длинными вьющимися когтями. Усиленная чувствительность мышей VDR(-/-) к химически индуцированному канцерогенезу кожи убедительно доказывает, что нарушение сигнализации VDR предрасполагает к неоплазиям, вызываемым ВПЧ [33].
Согласно гистопатологическому анализу поражений кожи, у мышей VDR(-/-) обнаружены 94 опухоли на коже, которые были классифицированы по гистологическим подтипам (рис. 3). Большинство всех опухолей (40%) были сальными папилломами (рис. 3А) – доброкачественными поражениями, которые связаны с волосяными фолликулами, сальными железами и межфолликулярной дермой. Кроме того, встречались плоскоклеточные папилломы (25% поражений, рис. 3Б) и фолликулярные папилломы (15% поражений, рис. 3В). Такие виды поражений, как базально-клеточная карцинома (рис. 3Г) и гемангиома (рис. 3Д), выявлялись гораздо реже. Пигментированные поражения, классифицированные как меланотические очаги, которые обычно отсутствуют в мышиной коже, наблюдались у мышей с делецией VDR(-/-) (11% поражений). Меланотические очаги (рис. 3Е) состояли из агрегатов сильно пигментированных клеток с плохо выраженными цитоплазматическими признаками [33].
Витамин D оказывает антипролиферативное и продифференцирующее действие на кератиноциты, поэтому были исследованы биопсии кожи мышей VDR(-/-) посредством количественного определения пролиферативного маркера BrdU. Во всех опухолях мышей VDR(-/-) уровни BrdU были выше, чем рядом в здоровой коже (рис. 4 и 5). В большинстве опухолей пролиферация клеток ограничивалась одним слоем. В других случаях (особенно при плоских папилломах) BrdU-положительные клетки были сгруппированы в несколько слоев. Данные показывают, что расширение опухоли связано с дальнейшим усилением пролиферации эпидермальных клеток у мышей с делецией гена рецептора витамина D [33].
В клинико-эпидемиологическом исследовании более высокое потребление кальция и витамина D ассоциировалось с уменьшением риска развития неоплазии шейки матки (n = 2430, в том числе 405 случаев цервикальной неоплазии). По сравнению с самым низким квартилем потребления кальция риск заболевания дозозависимо понижался в двух верхних квартилях на 14% (ОШ 0,86, 95% ДИ 0,63–1,17) и 50% (ОШ 0,50, 95% ДИ 0,34–0,73) соответственно (p = 0,004). Более высокое потребление витамина D независимо снижало риск заболевания на 20% в третьем (ОР 0,80, 95% ДИ 0,56–1,15) и 36% в четвертом квартиле (ОР 0,64, 95% ДИ 0,43–0,94, p = 0,013) [34].
Таким образом, противовирусное и противоопухолевое действие витамина D позволяет предположить, что повышение обеспеченности этим витамином улучшит результаты терапии опухолевых заболеваний шейки матки. Действительно, в рандомизированном плацебоконтролируемом исследовании долгосрочное применение витамина D индуцировало регрессию цервикальной интраэпителиальной неоплазии [35].
Однажды ко мне на приём пришла взволнованная молодая девушка. Показав папиллому на шее (размерами 3х3мм), она спросила: "ЭТО выросло за месяц. Доктор, у меня РАК. "
Заказ погребальных венков пришлось отменить, после чего я рассказал ей то, что знал об этих образованиях.
Опасность для здоровья: не представляют.
Что это такое?
Папилломы представляют собой разрастания поверхностного слоя кожи, похожие на сосочки.

Записывайтесь на вебинар "Канцерогены в косметике: правда, ложь и. маркетинг"
Как выглядят?
Характерная особенность - наличие у папилломы "ножки". Это означает, что верхняя часть шире, чем основание. Они имеют мягкую консистенцию, безболезненны и легко смещаются. Чаще всего их можно заметить на коже лица, шеи, подмышечных областей, промежности и под молочными железами.
Почему появляются?
Как и бородавки, папилломы не опасны. Их появление связывают с вирусом папилломы человека (ВПЧ), который передаётся при контакте с носителем. Также возможна передача ВПЧ с поражённого участка кожи на здоровый у одного человека. Увеличивают восприимчивость к вирусным частицам высокая влажность и микротрещины кожи. В связи с этим всегда следует использовать индивидуальные предметы гигиены при посещении бассейнов, саун и душевых.
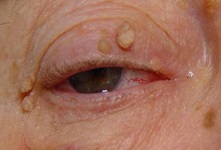
Важно: большое количество папиллом может говорить о проблемах с иммунитетом. Для женщин в таких случаях необходимо взятие мазка на ВПЧ, так как некоторые его виды могут вызывать рак шейки матки
Как лучше лечить?
Большое количество папиллом, безусловно, доставляет неудобство и выглядит не эстетично. Однако это не повод использовать для удаления нитку, плоскогубцы или паяльную лампу дедовские методы.
Для единичных небольших (1х1 мм) образований подходит сок чистотела - испытанное народное средство. Когда папиллом много или они крупные этот способ не подходит, так как может растянуться на месяцы и привести к выраженному воспалению.
Значительно более удобно и эффективно удаление методом радиоволновой хирургии. Операция не требует специальной подготовки, практически безболезненна, после неё можно управлять автомобилем.
Однажды мне довелось удалить сразу около 70 папиллом у одного пациента. Сложно передать всю радость избавившегося от них человека, которого они мучили несколько лет.
Гистологическое исследование при удалении
Результаты лечения
На фото ниже приведены результаты удаления папиллом шеи методом радиоволновой хирургии
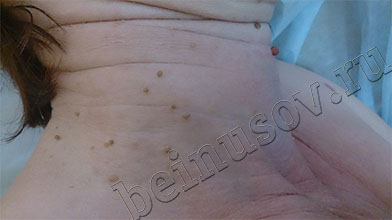
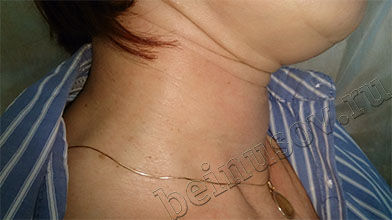
Редко возникают снова. Повторное появление папиллом возможно при высокой активности вируса в организме. В этой ситуации может потребоваться дополнительное лечение иммуномодуляторами или консультация иммунолога.
Другие статьи:
Полезная статья? Сделайте репост в Вашей социальной сети!
Оставьте комментарий или задайте вопрос
Здравствуйте.
Почему небольшие папилломы на теле есть (3 шт.), а анализ на ВПЧ онкогенных типов отрицательный. Везде пишут, что если есть папилломы, значит есть и вирус.
Пост специально для Вас.
Вам стоит более критично подходить к чтению информации в интернете. Источники, у которых не указан автор НЕ заслуживают доверия. Совсем. На них не нужно тратить время.

Записывайтесь на вебинар "Канцерогены в косметике: правда, ложь и. маркетинг"
Ученым и врачам еще не все известно о Сovid-19. Но многочисленные исследования уже свидетельствуют о высокой вероятности развития долгосрочных негативных симптомов у переболевших. Установлено, что даже легкие формы способны вызывать хронические патологии центральной нервной системы и внутренних органов. Поэтому доктора единодушно сходятся во мнении, что реабилитация после коронавируса необходима всем пациентам.
Почему требуется реабилитация после ковида?
Сегодня уже достоверно известно, что коронавирусная инфекция поражает в первую очередь дыхательную и сердечно-сосудистую системы. Но также вирус способен негативно воздействовать на почки, органы желудочно-кишечного тракта, печень, клетки мозга.
Слабость, усталость, сонливость – эти симптомы появляются одними из первых. Причиной их возникновения является не только интоксикация. Даже умеренное поражение легких на фоне Сovid-19 вызывает развитие гипоксии. А нехватка кислорода провоцирует нарушения процессов обмена, синтеза ферментов, ухудшение кровообращения.
В результате гипертермии происходит потеря жидкости и нарушение электролитного баланса. Также имеет значение и ухудшение аппетита, из-за чего в организм поступает недостаточное количество питательных веществ.
Поэтому упадок сил и недостаток энергии – вполне объяснимые явления после таких тяжелых нарушений. Несмотря на отсутствие точных данных, специалисты предполагают, что снижение работоспособности и нарушения функции легких могут сохраняться в течение года у каждого пятого пациента.
Параллельно с астенией, даже у психически здоровых пациентов, нередко наблюдаются и психоэмоциональные расстройства. Они проявляются:
- депрессивными признаками;
- тревожностью;
- поведенческими расстройствами;
- нарушениями сна.
Как восстановить нервную систему после коронавируса?

Для чего нужна диагностика
Обследование помогает определить вероятность развития осложнений или выявить уже имеющиеся нарушения после ковидной пневмонии.
- УЗИ внутренних органов;
- электрокардиограмму;
- КТ легких;
- анализы крови.
Полученные данные помогут подобрать наиболее действенные реабилитационные методы выявленных нарушений.

Немедикаментозные методы восстановления после коронавируса
По рекомендации Минздрава практически во всех санаториях России действуют программы реабилитации пациентов, перенесших ковид. Также восстановительные программы предлагаются во многих российских клиниках.
- восстановление дыхательной функции;
- улучшение общего физического состояния;
- борьба со стрессом, беспокойством, тревогой;
- устранение слабости в мышцах;
- повышение работоспособности.
Реабилитация после ковида в санаториях дополнительно включает плавание, терренкур, лечение микроклиматом соляных пещер.
Препараты для реабилитации
Большинство врачей считает, что при восстановлении должно использоваться минимальное количество медикаментозных средств. Для лечения инфекции (особенно тяжелых форм) используется немало сильнодействующих и достаточно токсичных препаратов. Поэтому, чтобы снизить нагрузку на печень и почки, оставляют только необходимый минимум лекарств.
- препараты для предупреждения образования тромбов;
- средства для нормализации обменных процессов;
- легкие седативные средства;
- антидепрессанты, транквилизаторы.
Вирус негативно действует на организм. Но правильно подобранные методы реабилитации позволяют избавиться от нарушений практически полностью. Главное условие – пройти полный курс сразу после завершения лечения, независимо от степени тяжести болезни. Это поможет значительно снизить риск серьезных последствий и восстановить в короткие сроки силы и энергию.
Читайте также:

